Quiz: TOP 100 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (Nâng cao - phần 1)
Câu hỏi trắc nghiệm
Có nAl = 0,24 mol
4Al + 3O2 → 2Al2O3
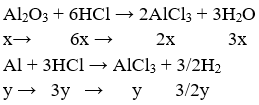
⇒ 2x + y = 0,24
Có m(dd HCl) = 3(2x + y).36,5 : 7,3% = 1500.(2x + y) = 360 g
m(dd Y) = 133,5.(2x + y) : 8,683% = 1537,487.(2x + y) ≈ 369 g
BTKL: 102x + 27y + 360 = 369 + 3y
Giải hệ: x = 0,06; y = 0,12
Suy ra mol H2 là 0,18 mol
→ Đáp án D
Gọi số mol của Cl2 và O2 lần lượt là x, y
Bảo toàn e
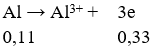
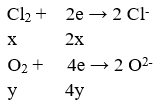
Có hpt: x + y = 0,12 và 2x + 4y = 0,33 ⇒ x = 0,075 và y = 0,045 ⇒ m = 9,735 gam
→ Đáp án C
Số mol của Hiđro bằng: nH2 = 6,72/22,4 = 0,3 (mol)
Lại có: nCl- (trong muối) = 2nH2 = 2.0,3 = 0,6 (mol)
Khối lượng muối tạo thành bằng: 12,45 + 0,6. 35,5 = 33,75 (gam).
→ Đáp án B
Số mol của Hiđro bằng: nH2 = 1/2 = 0,5 (mol)
Lại có: nCl- (trong muối) = 2nH2 = 2.0,5 = 1 (mol)
Khối lượng muối tạo thành bằng: 16 + 1. 35,5 = 51,5 (gam).
→ Đáp án D
Số mol của Hiđro bằng: nH2 = 8,736/22,4 = 0,39 (mol)
Lại có: nHCl = (500/1000). 1 = 0,5 (mol); nH2SO4 = (500/1000). 0,28 = 0,14 (mol)
Khối lượng muối tạo thành bằng: 7,74 + 0,5.36,5 + 0,14.98 – 0,39.2 = 38,93 (gam).
→ Đáp án A
Số mol của Hiđro bằng: nH2 = 2,912/22,4 = 0,13 (mol).
Đặt hoá trị của M là n, khối lượng mol là M. Số mol của M: nM = (2/n). 0,13 = 0,26/n.
Ta có: 7,28 = (0,26/n). M nên M = 28n.
Chỉ có n = 2; M = 56 thoả mãn. M là kim loại sắt.
→ Đáp án C
nH2 = 2,24/22,4 = 0,1 mol → nH2SO4 = nH2 = 0,1 mol
→ mH2SO4 = 0,1. 98 = 9,8 gam → mdd H2SO4 = (9,8.100)/10 = 98 gam
Khối lượng dung dịch sau phản ứng là:
mdd sau = mdd bd + mKL - mH2 = 98 + 3,68 - 0,1.2 = 101,48 gam
→ Đáp án C
Gọi kim loại cần tìm là M.
2M + nH2SO4 → M2(SO4)n + nH2 (1)
Theo bài ta có:
mmuối = mKL + mSO42- ⇔ mSO42- = 6,84 – 2,52 = 4,32 gam
→ nSO42- = 4,32/96 = 0,045 mol → nH2SO4 = 0,045 mol
Theo phương trình (1) ta có:
![]()
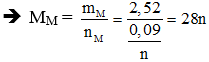
| n | 1 | 2 | 3 |
| MM | 28 | 56 | 84 |
| Loại | Fe (TM) | Loại |
→ Đáp án B
- Quá trình:
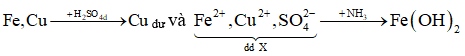
Lưu ý: Các hiđroxit hay muối của các kim loại Cu, Ag, Zn, Ni tạo phức tan trong dung dịch NH3 dư.
→ Đáp án A
- Khi cho m gam kim loại M tác dụng với 0,68 mol NaOH thì:
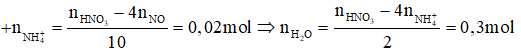
-BTKL→ mM + 63nHNO3 = mX + 30nNO + 18nH2O ⇒ m = 16,9 g
- Ta có ne trao đổi = 3nNO + 8nNH4+ = 0,52 mol
- Mà 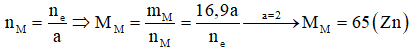 (với a là số e trao đổi của M)
(với a là số e trao đổi của M)
→ Đáp án D
nNO2 = 2nCu = (3,2/64).2 = 0,1 mol
→ Đáp án C
Hỗn hợp phản ứng với H2SO4 loãng dư chỉ có Fe phản ứng (vì Cu đứng sau H)
Hỗn hợp phản ứng với H2SO4 đặc nguội dư thì chỉ có Cu phản ứng (Fe bị thụ động)
![]()
→ Đáp án D
Do thu được khí không màu và MZ = 37 ⇒ có 2 trường hợp.
TH1: Z gồm N2 và N2O. Đặt nN2 = x; nN2O = y
⇒ nZ = x + y = 0,2 mol; mZ = 28x + 44y = 7,4(g).
⇒ giải hệ có: x = 0,0875 mol; y = 0,1125 mol. Đặt nNH4NO3 = a.
∑nNO3-/KL = ne = 10nN2 + 8nN2O + 8nNH4NO3 = (8a + 1,775) mol.
→ mmuối khan = 25,3 + 62.(8a + 1,775) + 80a = 122,3(g) ⇒ a = – 0,02 ⇒ loại.
TH2: Z gồm NO và N2O. Đặt nNO = x; nN2O = y
⇒ nZ = x + y = 0,2 mol; mZ = 30x + 44y = 7,4(g).
⇒ giải hệ có: x = y = 0,1 mol. Đặt nNH4NO3 = a.
∑nNO3-/KL = ne = 3nNO + 8nN2O + 8nNH4NO3 = (8a + 1,1) mol.
→ mmuối khan = 25,3 + 62.(8a + 1,1) + 80a = 122,3(g) ⇒ a = 0,05 mol.
⇒ nHNO3 = 4nNO + 10nN2O + 10nNH4NO3 = 1,9 mol
→ Đáp án C
4HNO3 + 3e → NO + 3NO3- + 2H2O ⇒ nHNO3 = 4nNO = 1,2 mol
→ Đáp án C
Mg + 2H2SO4(đ) -to→ MgSO4 + SO2 ↑ +2H2O
2Fe + 6H2SO4(đ) -to→ Fe2(SO4)3 + 3SO2 ↑ + 6H2O
Sau phản ứng Fe dư:
Fe dư + Fe2(SO4)3 → 3FeSO4
→ Chất tan có trong dung dịch Y gồm MgSO4 và FeSO4
→ Đáp án A
MY = 18,8 → Y chứa NO (3y) và H2 (2y) → X chứa H+ và NO3- dư.
nNO = 0,26 mol
Bảo toàn khối lượng:
m + 1,8.36,5 + 0,3.63 = m + 60,24 + 0,26.30 + mH2O
→ nH2O = 0,92 mol
Bảo toàn nguyên tố H → nH+ dư = 0,26 mol
Đặt nNH4+ = x
Bảo toàn nguyên tố N → x + 3y + 0,26 = 0,3
nH+, dư = 10x + 4.3y + 2.2y = 0,26
→ x = y = 0,1 mol
Ban đầu: nH+, pư = 0,92.2 = 4nNO + 2.nO (A) → nO (A) = 0,4 mol4
Trong khi cho Mg vào X thu được m – 6,04 > m – 6,4 nên Mg dư.
→ mMg dư = 6,4 - 6,04 = 0,36 gam
Mg + X Dung dịch chứa Mg2+ (p mol), NH4+ (0,01 mol), Cl- (1,8 mol)
Bảo toàn điện tích → p = 0,895 mol
→ mMg bd = 24.0,895 + 0,36 = 21,84 gam
→ Đáp án C
2FeCO3 + 4H2SO4 → Fe2(SO4)3 + 2CO2 + SO2 + 4H2O
2Fe3O4 + 10H2SO4 → 3Fe2(SO4)3 + SO2 + 10H2O
2FeS + 10H2SO4 → Fe2(SO4)3 + 9SO2 + 10H2O
2FeS2 + 14H2SO4 → Fe2(SO4)3 + 15SO2 + 14H2O
→ Đáp án A
Sau thí nghiệm ta thu được dd X là muối Fe(NO3)3 và AgNO3 dư.
Fe + 2AgNO3 (dư) → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3(dư) → Fe(NO3)3 + Ag
→ Đáp án B
Ta có :
Fe (x) + CuSO4 (x) → FeSO4 (x) + Cu (x)
Suy ra: mtăng = -56.x + 64x = 1,2
8x = 1,2 ⇒ x = 0,15.
mCu = 0,15.64 = 9,6 g
→ Đáp án D
Ta có: nFe = 0,15 mol, nAgNO3 = 0,4mol.
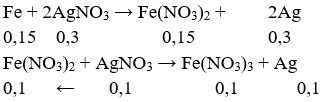
Suy ra: mAg = (0,1 + 0,3).108 = 43,2g.
→ Đáp án C
nFe = 5,6/56 = 0,1 mol; nAgNO3 = 0,5.0,5 = 0,25 mol
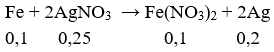
→ AgNO3 dư: 0,05 mol, Fe(NO3)2 tạo thành: 0,1 mol
![]()
→ Fe(NO3)2 dư : 0,05 mol , Fe(NO3)3 tạo thành 0,05 mol
→ Tổng số mol Ag ở hai phản ứng: 0,25 mol → mAg = 0,25.108 = 27 gam
Khối lượng muối: 0,05.180 + 0,05.242 = 21,1 gam
→ Đáp án A
Zn (a) + 2Fe(NO3)3 (2a) → Zn(NO3)2 + 2Fe(NO3)2 (1)
Zn + Fe(NO3)2 → Zn(NO3)2 + Fe (2)
Từ 2 phương trình trên ta thấy, để sau phản ứng không có kim loại thì Zn phải phản ứng hết ở phản ứng (1), khi đó 2a ≤ b hay b ≥ 2a.
→ Đáp án C
nAgNO3 = 1. 0,2 = 0,2 mol
M (0,1) + 2AgNO3 (0,2) → M(NO3)2 (0,1) + 2Ag
mmuối = 0,1(M + 62.2) = 18,8 → M = 64
Vậy M là Cu.
→ Đáp án B
![]()
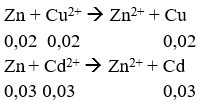
Δm = 0,02.64 + 0,03.112 – 0,05.65 = 1,39 gam
→ Tăng 1,39 gam.
→ Đáp án A
nZn = 19,5 : 65 = 0,3 mol 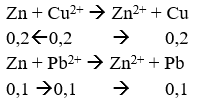
Vậy khối lượng rắn sau phản ứng là:
mrắn = mCu + mPb = 0,2.64 + 0,1.207 = 33,5 gam
→ Đáp án C
nAl = 6,48/27 = 0,24 mol; nFe2(SO4)3 = 0,1 mol; nZnSO4 = 0,8. 0,1 = 0,08 mol
→ nFe3+ = 0,1.2 = 0,2 mol
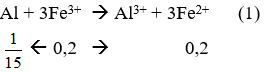
→ Phản ứng (1) kết thúc Fe3+ hết, Al dư: 0,24 - 1/15 = 13/75 mol
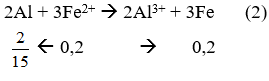
→ Phản ứng (2) kết thúc Fe2+ hết, Al dư: 13/75 - 2/15 = 0,04 mol
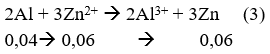
→ Phản ứng (3) kết thúc Al hết, Zn2+ còn dư.
Vậy sau khi các phản ứng kết thúc, ta thu được hỗn hợp các kim loại Fe (0,2 mol); Zn (0,06 mol)
→ m = mFe + mZn = 0,2.56 + 0,06.65 = 15,1 gam.
→ Đáp án C
nCu(NO3)2 = 0,2.1 = 0,2 mol; nAgNO3 = 0,12.1 = 0,12 mol.
Sau khi pư kết thúc thu đc dd A với màu xanh đã nhạt 1 phần → Fe đã phản ứng hết với AgNO3 và phản ứng với một phần Cu(NO3)2.
Gọi số mol Cu(NO3)2 phản ứng là x mol.
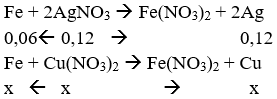
Vậy mtăng = 0,12.108 + x.64 – 0,06.56 – x.56 = 10,4 → x = 0,1 mol
Vậy khối lượng đinh sắt ban đầu là: mFe = 0,1.56 + 0,06.56 = 8,96 gam.
→ Đáp án D
nAl = 2,7 : 27 = 0,1 mol, nFe = 5,6 : 56 = 0,1 mol, nAgNO3 = 0,55.1 = 0,55 mol
Khi cho hỗn hợp kim loại gồm Al , Fe vào dung dịch AgNO3 thì Al sẽ phản ứng trước nếu Al hết sẽ đến Fe phản ứng , nếu AgNO3 dư sau phản ứng với Fe thì có phản ứng:
Ag+ + Fe2+ → Ag + Fe3+
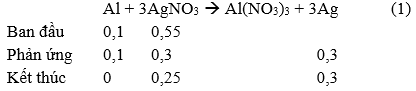
Al hết ⇒ Tính theo Al, nAgNO3 = 3.nAl ⇒ AgNO3 dư: 0,55 – 3.0,1 = 0,25 mol
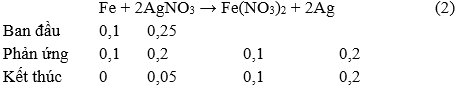
⇒ Sau phản ứng AgNO3 dư 0,05 mol tiếp tục có phản ứng
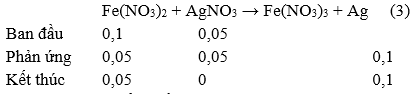
Từ (1), (2), (3) tổng số mol Ag = 0,3 + 0,2 + 0,05 = 0,55 ⇒ mAg = 0,55.108 = 59,4 gam
→ Đáp án A
Gọi số mol của Zn và Fe lần lượt là x và y mol
Phương trình hóa học:
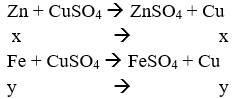
Theo bài ta có: mrắn bđ = mrắn sau → 65x + 56y = 64x + 64y ⇔ x = 8y.
Coi số mol của Fe là 1 mol thì số mol của Zn là 8 mol.
Thành phần phần trăm theo khối lượng của Zn trong hỗn hợp bột ban đầu là:
![]()
→ Đáp án B
Giả sử AgNO3 phản ứng hết khi đó Ag+ chuyển hết thành Ag
nAg = nAgNO3 = 0,4 mol → mAg = 0,4.108 = 43,2 gam > mA (=32,4 gam)
→ AgNO3 chưa phản ứng hết.
mA = mAg = 32,4 gam → nAg = 0,3 mol
Gọi số mol của Mg và Cu lần lượt là x và y mol
Theo bài ta có: 24x + 64y = 5,6 (1)
Ta có:
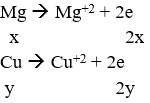
![]()
Bảo toàn e ta có: 2x + 2y = 0,3 (2)
Từ (1) và (2) ta có hệ phương trình:
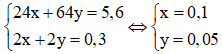
Khối lượng mỗi kim loại trong hỗn hợp đầu là:
mMg = 0,1.24 = 2,4 gam; mCu = 0,05.64 = 3,2 gam.
→ Đáp án D
Vì phản ứng giữa Al và AgNO3 xảy ra trước nên kim loại sau phản ứng phải có Ag, kế đến là CuSO4 có phản ứng tạo thành Cu. Theo giả thiết, có ba kim loại → kim loại thứ ba là Fe còn dư.
Ta có: nFe = 2,8/5,6 = 0,05 (mol)
nAl = 0,81/27 = 0,03 (mol)
và nH2 = 0,672/22,4 = 0,03 (mol)
Phản ứng: Fedư (0,03) + 2HCl → FeCl2 + H2 (0,03)
→ Số mol Fe phản ứng với muối: 0,05 – 0,03 = 0,02 (mol)
2Al + 3Cu2+ → 2Al3+ + 3Cu
Fe + 2Ag+ → Fe2+ + 2Ag
Fe + Cu2+ → Fe2+ + Cu
Ta có sự trao đổi electron như sau:
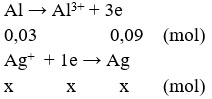
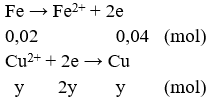
→ x + 2y = 0,09 + 0,04 = 0,13 (1); 108x + 64y + 56.0,03 = 8,12 (2)
Giải hệ phương trình (1) và (2), ta được x = 0,03; y = 0,05.
Vậy: CM AgNO3 = 0,03 : 0,2 = 0,15M
CM Cu(NO3)2 = 0,05 : 0,2 = 0,25M.
→ Đáp án A
Thay vì tính chất phản ứng giữa Mg, Zn với CuSO4 và AgNO3, ta tính số mol e mà hỗn hợp X có thể cung cấp và dung dịch Y có thể nhận:
nZn = 6,5/65 = 0,1 mol;
nMg = 4,8/24 = 0,2 mol
do: Zn → Zn2+ + 2e;
Mg → Mg2+ + 2e
Tổng ne (Mg, Zn): (0,1 + 0,2). 2 = 0,6 mol
nAg+ = nAgNO3 = 0,2.0,3 = 0,06 mol
nCu2+ = nCuSO4 = 0,2.0,5 = 0,1 mol
Ag+ + 1e → Ag
Cu2+ + 2e → 2Cu
Tổng ne (Ag+, Cu2+): 0,06 + 0,1.2 = 0,26 mol
Để khử hết Ag+ và Cu2+ chỉ cần 0,26 mol electron trong khi X có thể cung cấp 0,6 mol vậy Ag+, Cu2+ bị khử hết.
Ag và Cu kết tủa. Mg có tính khử mạnh hơn Zn nên Mg phản ứng trước: 0,2 mol Mg cung cấp 0,4 mol electron > 0,26 mol vậy chỉ có Mg phản ứng và
nMg phản ứng = 0,26 : 2 = 0,13 mol; còn dư: 0,2 – 0,13 = 0,07 mol
Do đó chất rắn A gồm 0,06 mol Ag và 0,1 mol Cu, 0,07 mol Mg và 0,1 mol Zn
mA = 0,06.108 + 0,1.64 + 0,07.24 + 0,1.65 = 21,6 gam
→ Đáp án C
Dựa vào đồ thị thấy tại thời điểm m-18 gam thì Mg phản ứng hết H+ và NO3- sinh ra Mg2+ và NO
Khi đó toàn bộ lượng NO3- chuyển hóa hết thành NO: 2a mol
Có nMg phản ứng = 18 : 24 = 0,75 mol
Bảo toàn electron → 0,75.2 = 2a. 3 → a = 0,25 mol
→ nH+ pư = 0,25. 8 = 2 mol → nH+ pư: b - 2 mol
Tại thời điểm m - 8 thì Mg phản ứng với Cu2+ sinh ra Cu
Tại thời điểm m - 14 thì Mg tiếp tục phản ứng với HCl dư sinh khí H2
Bảo toàn electron → nMg phản ứng = ![]() = 0,5b
= 0,5b
Khi đó 14 = 24. 0,5b - 0,25. 64 → b = 2,5
a : b = 0,25 : 2,5 = 1: 10.
→ Đáp án D
Số mol của Cu(NO3)2 và Pb(NO3)2 trong 2 dung dịch giảm như nhau → số mol M phản ứng ở 2 thí nghiệm là như nhau.
Coi khối lượng thanh M là 10 gam.
Gọi số mol M phản ứng là x mol.
Xét thí nghiệm ở thanh 1.
![]()
Δm = Mx – 64x = 0,998m = 0,02 (1)
Xét thí nghiệm ở thanh 2.
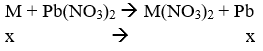
Δm = 207x – Mx = 2,84 (2)
Từ (1) và (2) ta có: Mx = 1,3; x = 0,02 → M = 65 → M là Zn
→ Đáp án A
Nhận xét: Kim loại + HCl → muối + H2
Ta có: mdung dịch tăng = mkim loại – mkhí thoát ra
⇒ mH2 = 7,8 - 7 = 0,8 (gam) ⇒ nH2 = 0,4 (mol)
Áp dụng bảo toàn nguyên tử H: nHCl = 2.nH2 = 0,8 (mol).
→ Đáp án A
n↓ BaSO4 = 27,96/233 = 0,12 mol
Gọi số mol của CuSO4 và FeSO4 lần lượt là x và y mol.
Bảo toàn nhóm SO42- ta có: x + y = 0,12 (1)
Cho m gam bột Zn dư tác dụng với dung dịch Y sau phản ứng thu được m gam chất rắn
Bảo toàn e ta có: nZn.2 = x.2 + y.2 → nZn = x + y
m rắn thu được sau thí nghiệm trên là Cu và Fe.
Theo bài ta có: mZn = mCu + mFe → (x + y).65 = 64x + 56y → x – 9y = 0 (2)
Từ (1) và (2) ta có: x = 0,108 mol; y = 0,012 mol.
→ p = 0,108.160 + 0,012.152 = 19,104 gam.
→ Đáp án D
nCu(NO3)2 = 0,1.1 = 0,1 mol; nFe(NO3)2 = 0,1.1 = 0,1 mol
Mg phản ứng trước với Cu(NO3)2 sau đó phản ứng với Fe(NO3)2.
Giả sử Mg phản ứng vừa đủ với Cu(NO3)2, khi đó:
mrắn = mCu = 0,1.64 = 6,4 gam < 9,2 gam
Giả sử Mg phản ứng vừa đủ với 2 dd trên, khi đó:
mrắn = mCu + mFe = 0,1.56 + 0,1.64 = 12 gam > 9,2 gam
→ Cu(NO3)2 phản ứng hết, Fe(NO3)2 phản ứng một phần.
mFe = 9,2 – 6,4 = 2,8 gam → nFe = nFe(NO3)2 pư = 2,8 : 56 = 0,05 mol.
→ Bảo toàn e: nMg.2 = 0,05.2 + 0,1.2 → nMg = 0,15 mol → mMg = 0,15.24 = 3,6 gam.
→ Đáp án C
Chất rắn sau phản ứng gồm 2 kim loại → 2 kim loại đó là Cu và Fe, Al đã phản ứng hết
→ CuSO4 không dư → nCu = 0,105 mol ⇒ m = 6,72 gam → còn 1,12 gam là của Fe .
Phản ứng: Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
nFe = 0,02 mol → nHNO3 = 0,08 mol.
nFe3+ = 0,02 mol
chú ý phản ứng: Cu + 2Fe3+ → Cu2+ + 2Fe2+
0,01 mol Cu + 0,02 mol Fe3+ → 0,01 mol Cu2+ và 0,02 mol Fe2+
Để HNO3 cần dùng là tối thiểu thì cần dùng 1 lượng hòa tan vừa đủ 0,105 – 0,01 = 0,095 mol Cu
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Từ đây tính được nHNO3 = 0,095.8/3 = 0,253 mol
→ tổng nHNO3 đã dùng là 0,253 + 0,08 = 0,333 mol
→ VHNO3 = 0,16667 lít = 166,67 ml
→ Đáp án C
nNO = 4,928 : 22,4 = 0,22 mol
Gọi số mol của Cu và Fe là x và y mol
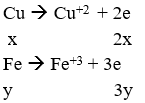
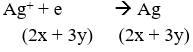
mrắn tăng = (2x + 3y).108 – x.64 – y.56 = 54,96 → 152x + 268y = 54,96 (1)
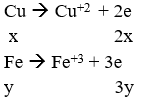
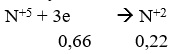
Bảo toàn e ta có: 2x + 3y = 0,66 (2)
Từ (1) và (2) ta được: x = 0,15 mol và y = 0,12 mol
→ m = 0,15. 64 + 0,12. 56 = 16,32 gam.
→ Đáp án B
- Các kim loại đứng trước cặp H+/H2 có thể tác dụng được với HCl.
- Các kim loại đứng trước cặp Ag+/Ag có thể tác dụng được với AgNO3.
Vậy các kim loại vừa tác dụng được với dung dịch HCl, vừa tác dụng được với dung dịch AgNO3 là Mg, Zn, Al, Fe, Ni và Sn.
→ Đáp án A