








Preview text:
ĐỀ TRƯỜNG SỞ 2025
ĐỀ SỐ 201: THPT Chuyên Lê Khiết – Quảng Ngãi – Lần 2
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
NAP 1: Cho sơ đồ các phản ứng hóa học sau: X1 + H2O X2 + X3 + H2 X2 + X4 BaCO3 + Na2CO3 + H2O X4 + X5
BaSO4 + K2SO4 + CO2 + H2O
(ghi chú: phương trình phản ứng chưa được cân bằng và chưa ghi điều kiện phản ứng)
Nhận định nào sau đây đúng? A. X1 là KCl.
B. X4 là NaHCO3. C. X5 là KHSO4. D. X2 là KOH.
NAP 2: Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:
Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,…để giúp nhận biết vật liệu
polymer cũng như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 5 được điều chế
bằng phản ứng trùng hợp monomer nào dưới đây? A. CH2=CH2. B. CH2=CH-Cl.
C. CH2=CH-C6H5. D. CH2=CH-CH3.
NAP 3: Vật liệu nào sau đây không phải là vật liệu cốt của vật liệu composite? A. Sợi carbon.
B. Nhựa polymer. C. Sợi vải. D. Bột nhôm.
NAP 4: Hình dưới đây mô tả tính chất vật lí nào của kim loại? (hình tròn to mô tả ion kim loại,
hình tròn nhỏ mô tả electron tự do) A. Tính dẻo.
B. Tính dẫn nhiệt. C. Tính dẫn điện. D. Tính cứng.
NAP 5: Hình ảnh dưới đây mô tả quá trình ăn mòn của gang và thép:
Phát biểu nào sau đây đúng?
A. Sắt bị oxi hóa thành ion Fe2+ sau đó Fe2+ tiếp xúc bị oxi hóa bởi O2 trong không khí tạo
ra gỉ sắt có thành phần chính là Fe3O4.nH2O.
B. Cực X (anode) là carbon và cực Y (cathode) là sắt.
C. Có thể bảo vệ gang, thép theo phương pháp điện hóa bằng cách tráng lên bề mặt một kim loại khác như Zn, Sn.
D. Lớp dung dịch chất điện li có thể là dung dịch acid, base, muối hoặc không khí ẩm.
Thay đổi tư duy – Bứt phá thành công | 1
NAP 6: Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong mẫu nước mưa được xác định có giá trị A. 1,0.10-5M.
B. lớn hơn 1,0.10-5M.
C. nhỏ hơn 1,0.10-5M. D. 1,0.10-4M.
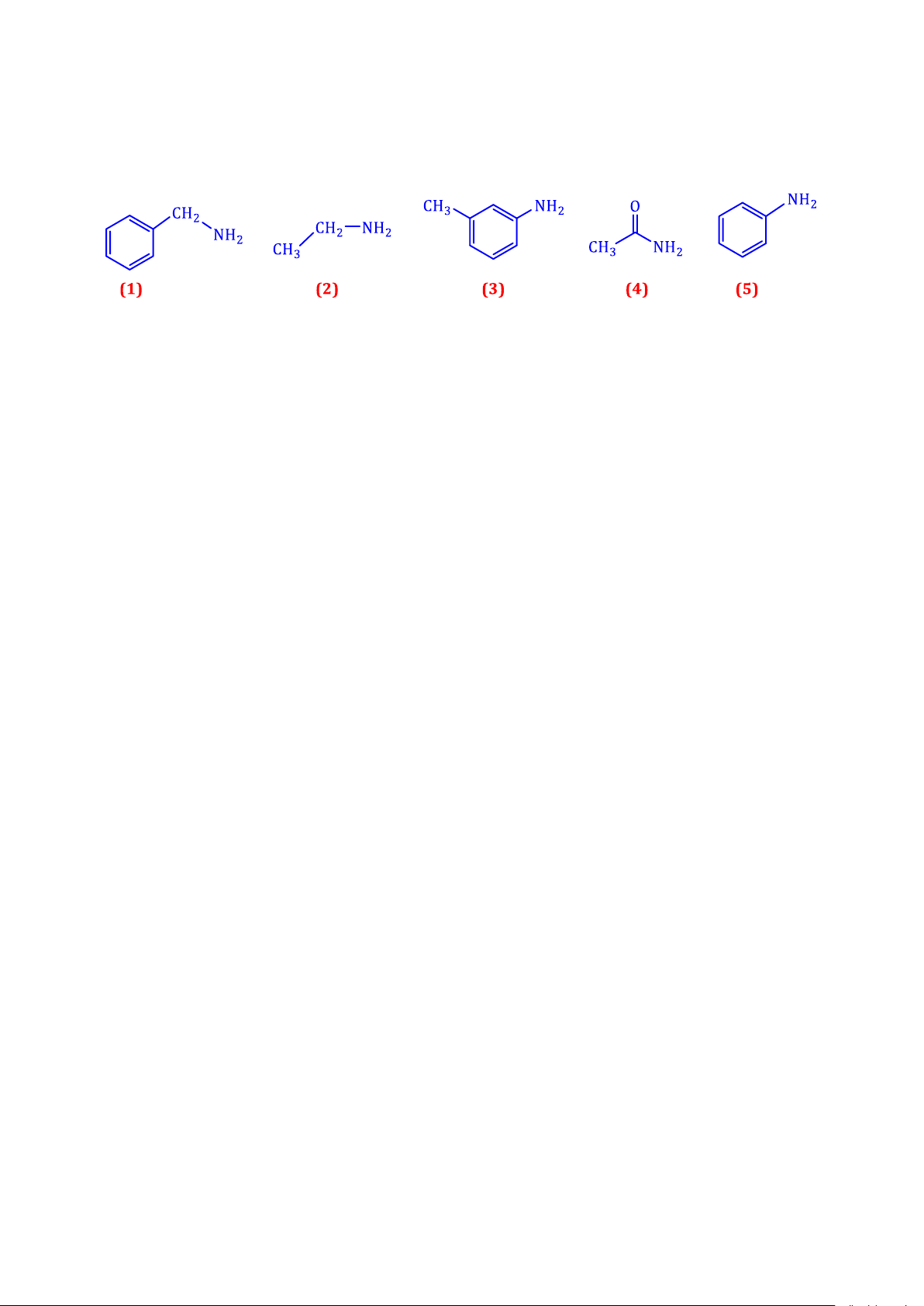
NAP 7: Cho các chất sau: Các chất arylamine là A. (1) và (5). B. (3) và (5). C. (1), (3), (5). D. (3) và (4).
NAP 8: Cho dãy các nguyên tố: Mg, K, Ba, Na, Al, Sr. Số nguyên tố thuộc nhóm IIA là A. 2. B. 4. C. 1. D. 3.
NAP 9: Phản ứng đốt cháy methane xảy ra như sau: CH4(g) + 2O2(g) o t
CO2(g) + 2H2O(l) (*) Biết nhiệt tạo thành o H của CH f 298
4(g) là -74,8 kJ/mol, của CO2(g) là -393,5 kJ/mol, của H2O(l) là
-285,8 kJ/mol. Giá trị biến thiên enthalpy chuẩn của phản ứng (*) là A. +809,3 kJ. B. +604,5 kJ. C. -604,5 kJ. D. -890,3 kJ.
NAP 10: Từ cấu hình electron của nguyên tử Cu ở trạng thái cơ bản là [Ar]3d104s1, cấu hình electron của ion Cu2+ là A. [Ar]3d9. B. [Ar]3d84s1. C. [Ar]3d8. D. [Ar]3d10.
NAP 11: Cho các phát biểu sau:
(1) Do có tính oxi hóa mạnh, nitric acid thường được sử dụng để phá mẫu quặng trong việc
nghiên cứu, xác định hàm lượng các kim loại trong quặng.
(2) Hiện tượng mưa acid là do không khí bị ô nhiễm bởi các khí SO2, CO, NO2.
(3) Hiện tượng phú dưỡng là do sự dư thừa các chất dinh dưỡng, bao gồm cả hợp chất chứa
nguyên tố nitrogen và sulfur.
(4) Mưa acid gây ra rất nhiều tác hại cho đời sống và sản xuất, nước mưa acid có pH nămg trong khoảng dưới 5,6. Số phát biểu đúng là A. 4. B. 3. C. 2. D. 1.
NAP 12: Tinh thể chất rắn X không màu, vị ngọt, dễ ran trong nước. X có nhiều trong cây mía,
củ cải đường và hoa thốt nốt. Trong công nghiệp, X được chuyển hóa thành chất Y dùng để
tráng gương, tráng ruột phích. Tên gọi của X và Y lần lượt là
A. glucose và fructose.
B. saccharose và glucose.
C. glucose và saccharose.
D. saccharose và tinh bột.
2 | Thay đổi tư duy – Bứt phá thành công
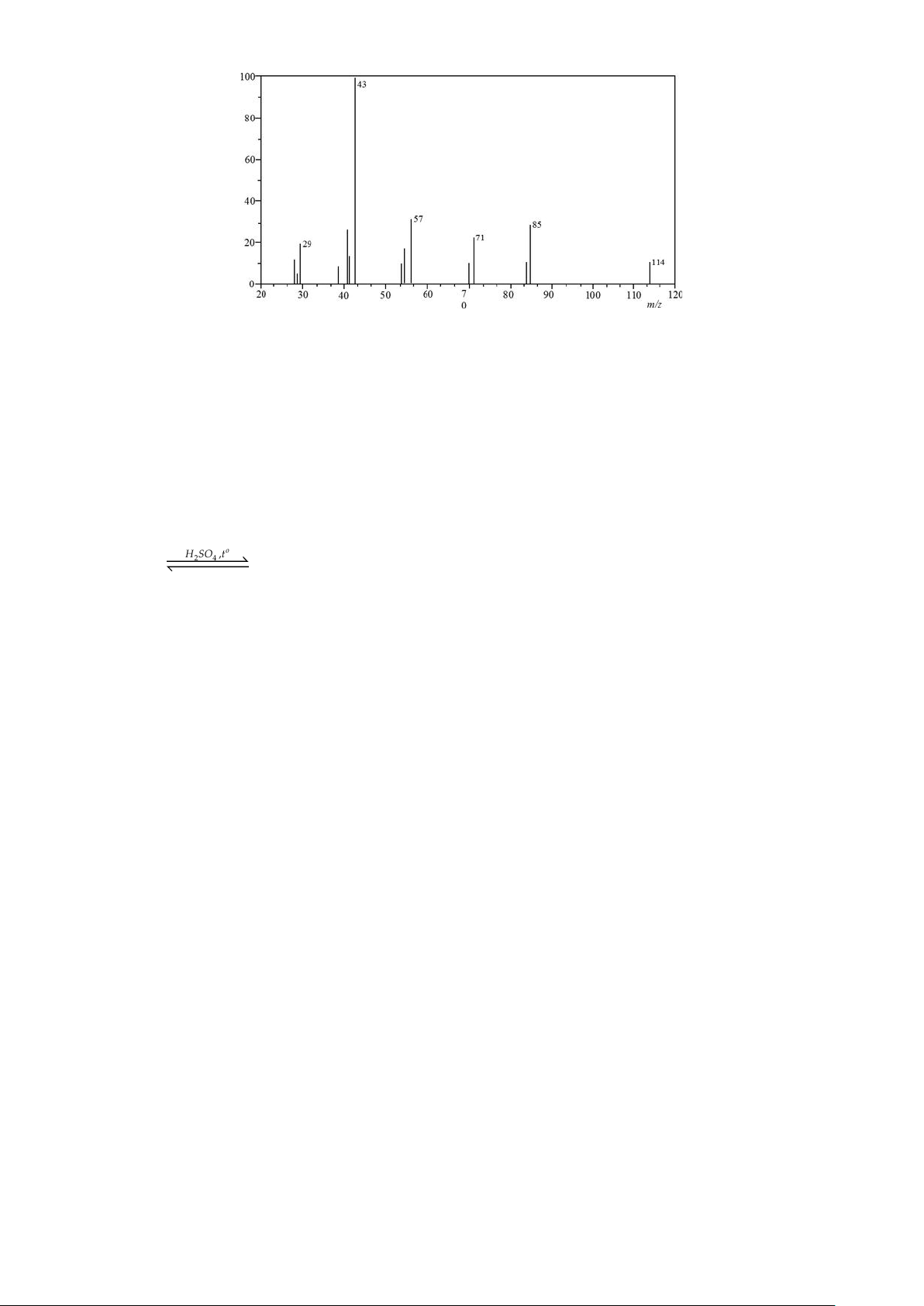
NAP 13: Hydrocacbon no X có kết quả phổ MS như hình dưới:
Phần trăm khối lượng carbon trong X là A. 30,77%. B. 84,21%. C. 50%. D. 15,79%.
NAP 14: Hợp chất CH2=CHCOOCH3 có tên là A. vinyl acetate.
B. methyl acetate. C. methyl acrylate. D. methyl propionate.
NAP 15: Ester no, đơn chức, mạch hở X là dung môi hữu cơ được sử dụng nhiều trong công
nghiệp hóa chất. Phổ MS cho biết khối lượng phân tử X là 88. Trong đời sống, hợp chất X2 được
điều chế từ quá trình lên men tinh bột và là một thành phần của xăng E5.
Cho các phương trình hóa học sau: (1) X + H2O 2 4 , o H SO t X1 + X2 (2) X2 + CuO o t X3 + Cu + H2O (3) X3 + 3I2 + 4NaOH X4 + CHI3 + 3NaI + 3H2O
Phát biểu nào sau đây là đúng?
A. Thứ tự nhiệt độ sôi được sắp xếp theo chiều X2 < X3 < X1.
B. X tan tốt trong nước hơn X1 và X2.
C. X4 có thể tham gia phản ứng tráng bạc với thuốc thử Tollens.
D. Có thể thực hiện phản ứng theo sơ đồ chuyển hóa X2 X3 X4.
NAP 16: Chất nào sau đây thuộc loại disaccharide? A. Glucose. B. Cellulose. C. Saccharose. D. Fructose.
NAP 17: Khi cho 100 kg một loại mỡ (giả sử có chứa 50% tristearin; 30% triolein và 20%
tripalmitin về khối lượng) tác dụng với potassium hydroxide vừa đủ thu được m kg muối (biết
hiệu suất phản ứng đạt 100%). Giá trị m là A. 108,7. B. 119,3. C. 87,6. D. 103,2.
NAP 18: Điện phân là
A. quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện 1 chiều với
hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
B. quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực ki có dòng điện 2 chiều với
hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
C. quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện 1 chiều đi
qua chất điện li nóng chảy hoặc dung dịch chất điện li.
D. quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện đi qua chất
điện li nóng chảy hoặc dung dịch chất điện li.
Thay đổi tư duy – Bứt phá thành công | 3
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
NAP 1: Hai ống nghiệm (1) và (2) đều chứa 1 mL dung dịch copper(II) sulfate 0,5% màu xanh
nhạt. Tiến hành hai thí nghiệm sau ở 20 oC:
Thí nghiệm 1: Thêm từ từ cho đến hết 2 mL dung dịch hydrochloric acid đặc không màu vào
ống nghiệm (1), vừa nhỏ vừa lắc đều thì sau đó thu được dung dịch có màu vàng chanh, do có quá trình: [Cu(OH2)6]2+(aq) + 4Cl-(aq) [CuCl4]2-(aq) + 6H2O(l) KC = 4,18.105
Thí nghiệm (2): Thêm từ từ cho đến hết 2 mL dung dịch sodium chloride không màu vào ống
nghiệm (2), vừa nhỏ vừa lắc đều thì sau đó thu được dung dịch có màu xanh nhạt hơn so với ban đầu.
a. Thí nghiệm 2, không có dấu hiệu của phản ứng hình thành phức chất.
b. Trong thí nghiệm 1 có sự thay đổi màu sắc dung dịch, chứng tỏ có phản ứng thay thế
phối tử H2O trong phức chất [Cu(OH2)6]2+ bởi các phối tử Cl-.
c. Liên kết trong phức [Cu(OH2)6]2+ là liên kết cho – nhận, trong đó mỗi phối tử H2O đã
cho 2 cặp electron chưa liên kết vào các orbital trống của ion trung tâm Cu2+ tạo nên phức có
dạng hình học bát diện.
d. Thí nghiệm 1 chứng minh phức [Cu(OH2)6]2+ bền hơn phức [CuCl4]2-.
NAP 2: Vị tanh của cá, đặc biệt là cá mè, là do các amine gây ra, trong đó có amine X. Phân tích
nguyên tố đối với X thu được kết quả: %C = 61,02%; %H= 15,25%; %N = 23,73% (về khối lượng).
Từ phổ khối lượng, xác định được phân tử khối của X bằng 59. Bằng các phương pháp khác,
thấy phân tử X có cấu trúc đối xứng cao.
a. pH của dung dịch X 0,1M ở 20 oC khoảng 11,4. (hằng số Kb ở nhiệt độ này là 6,5.10-5).
b. Để loại bỏ 5,9 gam X bằng dung dịch giấm ăn (acetic acdi) 5% thì cần tối thiểu 100 mL
giấm ăn biết Dgiấm ăn = 1002,5 g/L.
c. Danh pháp thay thế của X là trimethylamine.
d. Ở điều kiện thường, X là chất khí, tan tốt trong nước.
NAP 3: Cho biết giá trị thế điện cực của các cặp oxi hóa khử sau: Cặp oxi hóa – khử X+/X Y2+/Y Z2+/Z T2+/T
Thế điện cực chuẩn, V +0,799 -0,257 -0,44 +0,340
a. Pin Galvani Z-X có sức điện động lớn nhất trong các pin Galvani tạo từ 4 kim loại trên.
b. Kim loại Z có tính khử mạnh nhất nên có thể đẩy các kim loại còn lại ra khỏi dung dịch muối của chúng.
c. Pin Galvani được thiết lập bởi 2 cặp điện cực: Y2+/Y và T2+/T với anode là T2+/T và cathode là Y2+/Y.
d. Tính oxi hóa được xếp theo thứ tự: Z2+ > Y2+ > T2+ > X+.
4 | Thay đổi tư duy – Bứt phá thành công
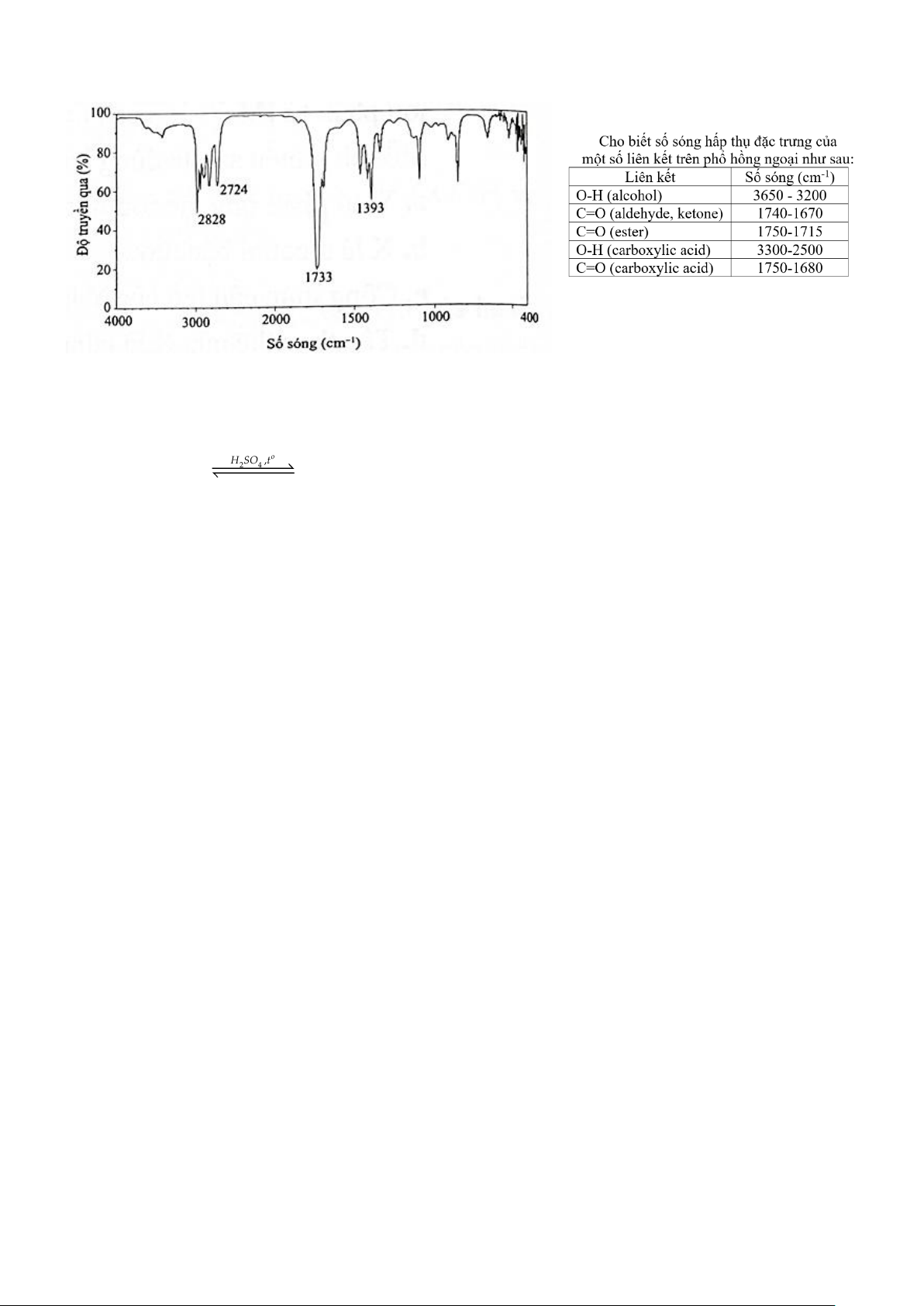
NAP 4: Hợp chất hữu cơ X no, mạch hở, công thức phân tử là C3H6O và phổ IR của chất X như sau:
Mối quan hệ các hợp chất X, Y, Z, T được biểu diễn bằng các phương trình: X + 2[H] LiA 4 lH alcohol Y (1) X + Br2 + H2O acid Z + 2HBr (2) Y + acid Z 2 4 , o H SO t ester T + H2O (3)
a. Dựa trên phổ IR có thể xác định X là acetone.
b. Ester T có danh pháp thay thế là propyl propionate.
c. Hợp chất X thể hiện tính oxi hóa ở phản ứng (1) và tính khử ở phản ứng (2).
d. Hợp chất X, Y, Z tan được trong nước vì đều có khả năng tạo liên kết hydrogen với nước.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
NAP 1: Nghành công nghiệp sản xuất nhiên liệu sinh học để phát triển bền vững cần áp dụng
các công nghệ mới theo hướng thân thiện môi trường, rơm rạ là một loại chế phẩm nông nghiệp
có thể dùng làm một nguồn nguyên liệu để sản xuất ethanol tạo xăng sinh học thay vì đốt gây ô nhiễm môi trường.
Để sản xuất 100,0 L xăng E5 (ethanol chiếm 5% về thể tích) thì cần m kg rơm rạ. Biết cellulose
chiếm 35% khối lượng khô của rơm rạ, việc tách cellulose ra khỏi rơm rạ thường đạt hiệu suất
40%. Trong khi đó, hiệu suất của quá trình chuyển hóa cellulose thành ethanol đạt 60%. Khối
lượng riêng của ethanol là 0,8 g/mL. Giá trị của m là bao nhiêu? (Kết quả làm tròn đến hàng phần mười)
Đáp số: ……………
NAP 2: Hợp chất hữu cơ X (C5H11NO2) tác dụng với dung dịch NaOH dư, đun nóng, thu được
muối sodium của -amino acid và alcohol. Hợp chất hữu cơ X có bao nhiêu công thức cấu tạo thỏa mãn?
Đáp số: ……………
NAP 3: Muối ăn khi khai thác từ nước biển, mỏ muối, hồ muối thường có lẫn nhiều tạp chất
như MgCl2, CaCl2, CaSO4 làm cho muối có vị đắng chát và dễ bị chảy nước gây ảnh hưởng xấu
tới chất lượng muối. Một trong những phương pháp loại bỏ tạp chất ở muối ăn là dùng hỗn
hợp A gồm Na2CO3, NaOH, BaCl2 tác dụng với dung dịch nước muối để loại tạp chất dưới
dạng các chất kết tủa CaCO3, Mg(OH)2, BaSO4.
Thay đổi tư duy – Bứt phá thành công | 5
Một mẫu muối thô thu được bằng phương pháp bay hơi nước biển có thành phần khối lượng
như sau: 96,25% NaCl, 0,190% MgCl2, 1,224% CaSO4, 0,010% CaCl2, 0,951% H2O, còn lại là tạp
chất trơ. Hỏi cần dùng bao nhiêu kilogam hỗn hợp A để loại bỏ hết tạp chất có trong 1 tấn muối
nói trên (kết quả làm tròn đến hàng đơn vị).
Đáp số: ……………
NAP 4: Cho sơ đồ chuyển hóa sau: CH H Ni Y(xtH SO ) 4 2 , o O t X 2 , Y , , o CO xt t Z 2 4 T
Biết X, Y, Z, T là các hợp chất hữu cơ. Phân tử khối của T có giá trị là bao nhiêu?
Đáp số: ……………
NAP 5: Điểm chớp cháy là nhiệt độ thấp nhất ở áp suất của khí quyển mà một chất lỏng hoặc
vật liệu dễ bay hơi tạo thành lượng hơi đủ để bốc cháy trong không khí khi tiếp xúc nguồn lửa.
Chất lỏng có thể điểm chớp cháy nhỏ hơn 37,8 oC gọi là chất lỏng dễ cháy. Cho bảng số liệu sau: Nhiên liệu Điểm chớp cháy (oC) Nhiên liệu Điểm chớp cháy (oC) Xăng -43 Biodiesel 130 Propane -105 Dầu hỏa 38-72 Pentane -57 Ethanol 13 Diethyl ether -45 Methanol 11 Acetone -20 Isopropyl alcohol 12 Benzene -11 Pyridine 20 Isooctane -12 Xylene 27-32 n-Hexane -22 Toluene 4
Số chất lỏng dễ cháy trong bảng trên là bao nhiêu?
Đáp số: ……………
NAP 6: Một nhà máy sản xuất túi nylon từ HDFE, túi có dạng hĩnh chữ nhật (kích thước 20cm x
30cm, bề dày của lớp nylon là 0,02cm). Biết hiệu suất phản ứng trùng hợp ethylene để điều chế
HDPE là 60%, quá trình chuyển nhựa thành túi có hiệu suất là 95% và khối lượng riêng của
nhựa HDPE là 0,95 g/cm3. Tính khối lượng (tấn) nguyên liệu ethylene cần dùng để sản xuất đơn hàng 10000 túi trên.
Đáp số: ……………
---------------- HẾT ----------------
6 | Thay đổi tư duy – Bứt phá thành công
ĐỀ TRƯỜNG SỞ 2025
ĐỀ SỐ 202: Cụm trường THPT TP Nam Định
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
NAP 1. Nhận xét nào sau đây không đúng?
A. Cao su Buna-S có chứa nguyên tố lưu huỳnh.
B. Trong phân tử cao su tự nhiên, các liên kết đôi C=C của mắt xích isoprene đều ở dạng cis.
C. Nylon-6,6 bị thủy phân trong dung dịch base, đun nóng.
D. Cao su chloroprene được điều chế bằng phản ứng trùng hợp chloroprene.
NAP 2. Thiết lập một pin Galvani từ hai cặp oxi hóa khử là Zn2+/Zn và Cu2+/Cu ở điều kiện
chuẩn. Khi pin hoạt động, ở anode xảy ra
A. sự khử Zn2+.
B. sự khử Cu2+.
C. sự oxi hóa Zn. D. sự oxi hóa Cu.
NAP 3. Số oxi hóa phổ biến của nguyên tố đồng (Cu) trong các hợp chất là A. +4. B. +2. C. +3. D. +1.
NAP 4. Polymer X được dùng để sản xuất thủy tinh hữu cơ. Công thức cấu tạo của polymer X
như hình bên. Tên gọi của polymer X là
A. poly(vinyl chloride). B. polystyrene.
C. poly(methyl methacrylate). D. polyethylene.
NAP 5. Tại điều kiện thường, hợp chất nào sau đây ở trạng thái lỏng? A. Alanine. B. Aniline. C. Methylamine. D. Trimethylamine.
NAP 6. Thạch cao có chứa muối của kim loại nào sau đây? A. Magnesium. B. Potassium. C. Calcium. D. Sodium.
NAP 7. Dung dịch nào sau đây có pH ≈ 7?
A. Dung dịch HCl 0,1M.
B. Dung dịch NaOH 0,5M.
C. Dung dịch NaCl 10%.
D. Dung dịch H2SO4 10%.
NAP 8. Cho các hợp chất có công thức cấu tạo sau đây:
Hợp chất thuộc loại chất béo no là A. X. B. Y. C. T. D. Z.
NAP 9. Methyl acetate dễ bay hơi và ít độc nên được sử dụng làm dung môi trong sản xuất keo
dán. Trong phân tử methyl acetate có chứa
A. 3 nguyên tử carbon.
B. 3 nguyên tử oxygen.
C. 1 nguyên tử nitrogen.
D. 4 nguyên tử hydrogen.
Thay đổi tư duy – Bứt phá thành công | 7
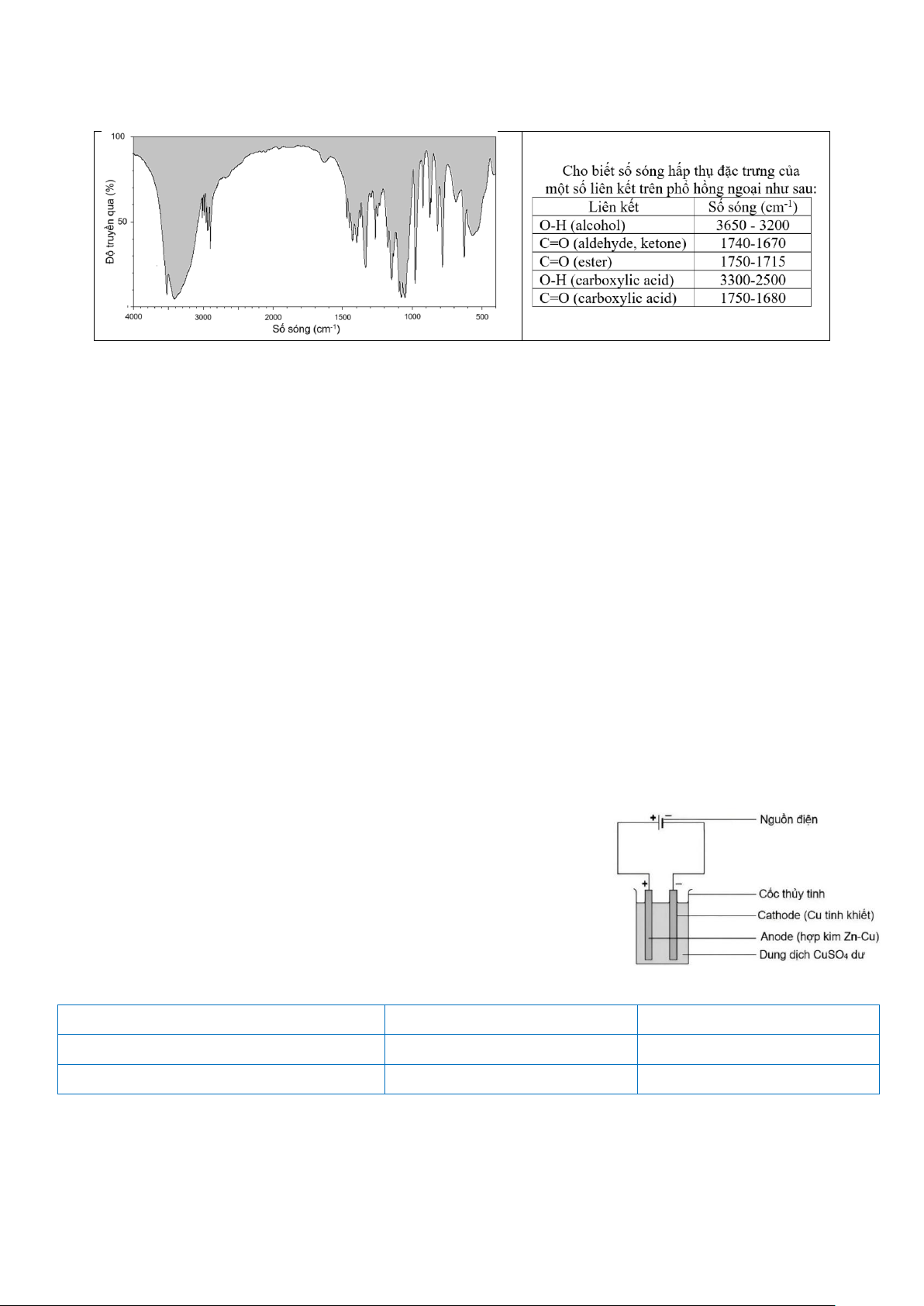
NAP 10. Chất lỏng X không màu là một trong số các chất lỏng hoặc dung dịch sau đây: acetone,
acetic acid, methyl acetate, dung dịch fructose. Khảo sát phổ IR của X thu được kết quả như sau: Chất lỏng X là A. fructose. B. acetic acid. C. acetone. D. methyl acetate.
NAP 11. Hợp kim gang được dùng để sản xuất nồi, khuôn đúc,… Nguyên tố kim loại chủ yếu có trong gang là A. kẽm. B. carbon. C. sắt. D. magnesium.
NAP 12. Ở 20oC, dung dịch nước vôi trong bão hòa có giá trị pH = 12,67. Khối lượng của
Ca(OH)2 có trong 1 L dung dịch nước vôi trong bão hòa ở nhiệt độ trên là (kết quả làm tròn đến hàng phần trăm): A. 2,55 gam. B. 1,26 gam. C. 1,73 gam. D. 3,48 gam.
NAP 13. Nhỏ từ từ dung dịch NH3 đến dư vào dung dịch AgNO3 thu được dung dịch trong
suốt có tên gọi là thuốc thử Tollens. Trong thuốc thử Tollens chứa phức [Ag(NH3)2]+. Khi tham
gia phản ứng oxi hóa – khử với glucose (thực hiện phản ứng tráng bạc), một ion phức [Ag(NH3)2]+
A. nhận 1 electron.
B. nhường 1 electron.
C. nhận 2 electron.
D. nhường 2 electron.
NAP 14. Để tách lấy kim loại Cu từ một thanh hợp kim Zn-
Cu (Cu chiếm khoảng 96% về khối lượng), tiến hành thí nghiệm như hình bên.
Trong quá trình điện phân, thể tích dung dịch không đổi.
Toàn bộ lượng kim loại tan ra ở anode tạo thành cation tan
trong dung dịch và lượng kim loại Cu sinh ra bám hết vào
cathode. Sau một thời gian, dừng điện phân, rửa sạch và sấy
khô rồi cân lại điện cực. Khối lượng của mỗi điện cực: Ban đầu Kết thúc điện phân
Thanh hợp kim Cu – Zn (anode) 33,6 gam 13,11 gam
Thanh Cu tinh khiết (cathode) 4,5 gam 24,98 gam
Cho các nhận xét sau đây:
(a) Khối lượng kim loại Cu tan ra ở anode là 19,84 gam.
(b) Ở anode, kim loại Zn dễ bị oxi hóa hơn Cu.
(c) Trong dung dịch sau khi kết thúc điện phân có chứa ion Zn2+ (aq).
8 | Thay đổi tư duy – Bứt phá thành công
(d) Nồng độ mol của ion Cu2+ (aq) trong dung dịch thu được sau khi kết thúc điện phân thấp
hơn so với dung dịch ban đầu.
(đ) Ở cathode, xảy ra sự oxi hóa ion Cu2+ (aq) thành Cu. Số nhận xét đúng là A. 4. B. 2. C. 3. D. 5.
NAP 15. Trong giấm ăn có chứa acetic acid với hàm lượng 2-5%. Công thức cấu tạo của acetic acid là A. CH3-CH=O. B. CH4. C. CH3-COOH. D. CH3-CH2-OH.
NAP 16. Hơi thủy ngân rất độc hại cho cơ thể người. Để loại bỏ thủy ngân rơi vãi khi nhiệt kế
thủy ngân bị vỡ, hạn chế tác động của thủy ngân đến sức khỏe, người ta có thể dùng hóa chất nào sau đây?
A. Dung dịch HCl. B. Dung dịch NaOH.
C. Bột than (có chứa carbon). D. Bột lưu huỳnh.
NAP 17. Hợp chất nào sau đây không tham gia phản ứng thủy phân? A. Saccharose. B. Glucose. C. Tinh bột. D. Cellulose.
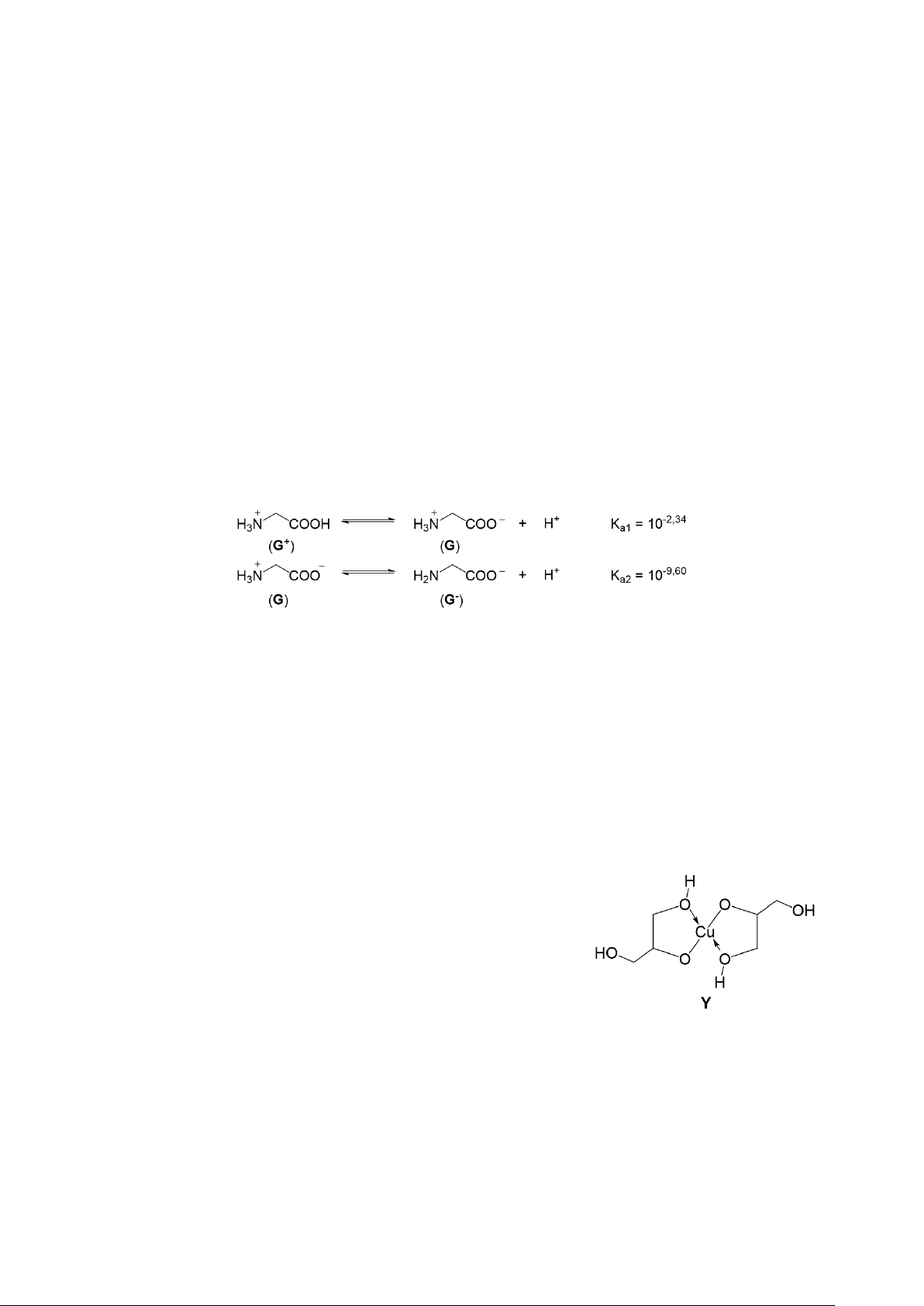
NAP 18. Trong dung dịch, glycine có cân bằng sau:
Trong dung dịch có pH = 1, nồng độ ion G+ chiếm x% so với tổng nồng độ các dạng G+, G và G-.
Giá trị của x% là (kết quả làm tròn đến hàng đơn vị): A. 96%. B. 90%. C. 82%. D. 88%.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí
sinh chọn đúng hoặc sai.
NAP 1. Dung lượng phối trí của phối tử là số liên kết giữa một phối tử đó với nguyên tử trung tâm. Để nghiên
cứu phản ứng của phức chất, một nhóm học sinh tiến hành thí nghiệm sau:
- Cho 1 mL dung dịch NaOH 20% vào ống nghiệm chứa sẵn 1
mL dung dịch CuSO4 5% thấy xuất hiện kết tủa X có công thức [Cu(OH)2(OH2)4].
- Thêm tiếp vào ống nghiệm ở trên 10 mL dung dịch glycerol
thấy kết tủa tan, thu được dung dịch màu xanh lam. Trong
dung dịch sản phẩm có chứa phức chất Y có công thức cấu tạo như hình bên.
a. Phức chất Y có dạng hình học là bát diện.
b. Phối tử trong phức chất Y có dung lượng phối trí là 2.
c. Trong thí nghiệm trên, nếu thay thế glycerol bằng ethylene glycol cũng thu được hiện tượng tương tự.
d. Phức chất X có 6 phối tử.
Thay đổi tư duy – Bứt phá thành công | 9
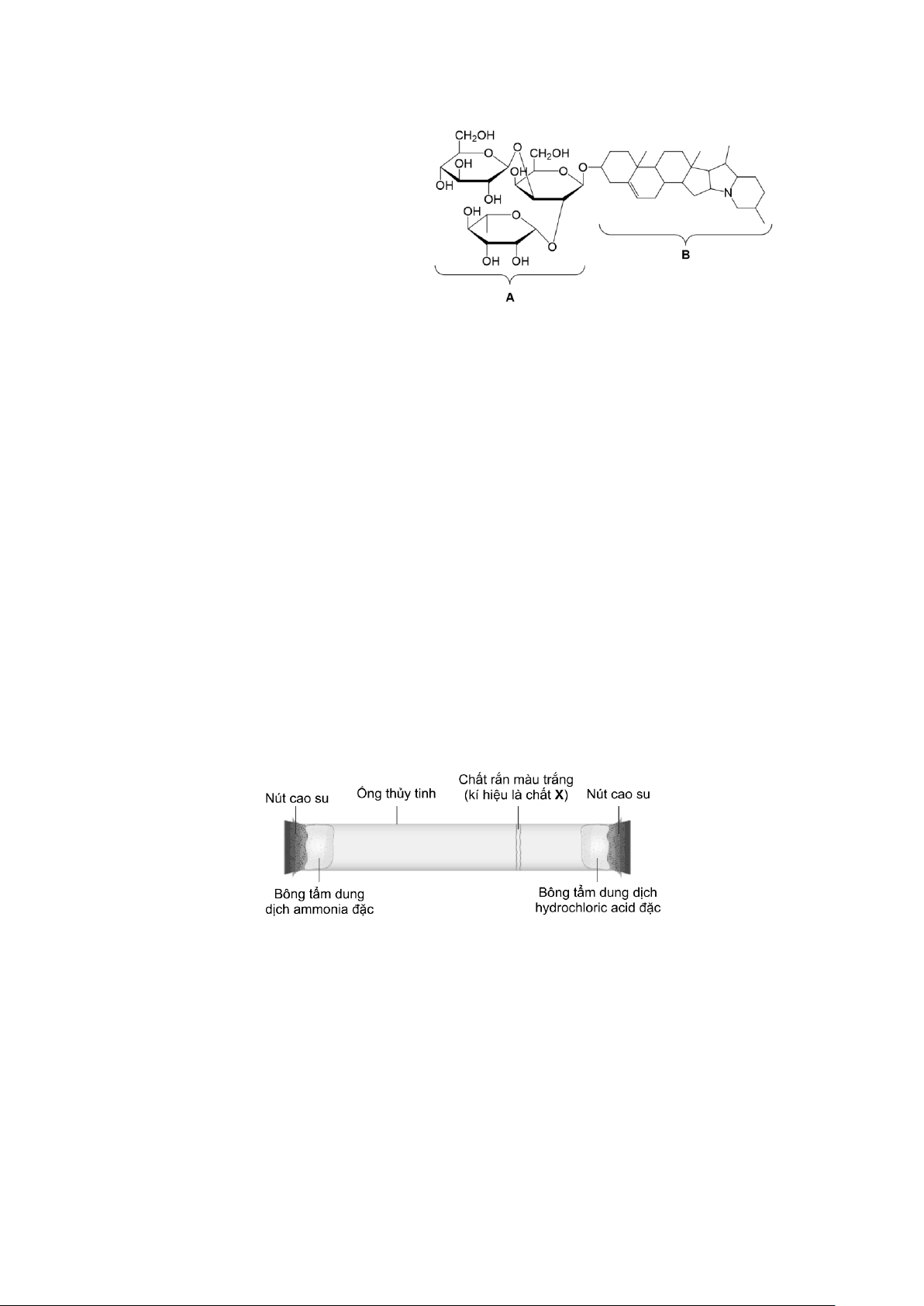
NAP 2. Một nhóm học sinh tạo ra nước giặt từ quả bồ hòn theo quy trình sau:
- Cho 10 quả bồ hòn và 1 lít nước vào nồi
rồi đun sôi với lửa nhỏ khoảng 60 phút.
- Ủ nóng nồi nước qua đêm.
- Vò nát quả bồ hòn, rồi lọc bỏ phần bã,
lấy phần nước sẽ thu được nước giặt.
Trong thành phần của nước giặt từ quả
bồ hòn có chất saponin, khi tiếp xúc với
nước tạo ra lớp bọt nhẹ nên có khả năng
giặt rửa. Công thức cấu tạo của saponin như hình bên.
a. Trong phân tử saponin có chứa một đơn vị β-glucose.
b. Quá trình tách chất hữu cơ từ quả bồ hòn ở trên được thực hiện theo phương pháp chiết lỏng – lỏng.
c. Trong phân tử saponin, A là phần kị nước, B là phần ưa nước.
d. Nước giặt từ quả bồ hòn ở trên bền vững, khó bị phân hủy khi thải ra ngoài môi trường.
NAP 3. Khuếch tán là sự dao động nhiệt của tất cả các phân tử. Sự khuếch tán dẫn đến sự dịch
chuyển các phân tử từ một khu vực có nồng độ cao hơn đến khu vực có nồng độ thấp hơn. Một
nhóm học sinh dự đoán “phân tử khối càng lớn, tốc độ khuếch tán càng cao”. Từ đó, học sinh
tiến hành thí nghiệm như sau:
Cho hai miếng bông tẩm dung dịch ammonia đặc và dung dịch hydrochloric acid đặc đặt ở hai
đầu ống thủy tinh. Đậy chặt miệng ống thủy tinh bằng nút cao su. Sau một thời gian thấy xuất
hiện chất rắn màu trắng dạng đám khói. Sơ đồ thiết bị thí nghiệm và kết quả thí nghiệm được
mô tả như hình vẽ dưới đây:
a. Phân tử khối của khí ammonia lớn hơn so với khí hydrogen chloride.
b. Thí nghiệm cho thấy tốc độ khuếch tán của khí ammonia chậm hơn so với khí hydrogen chloride.
c. Chất rắn X dễ tan trong nước.
d. Liên kết trong hợp chất X gồm liên kết cộng hóa trị và liên kết ion.
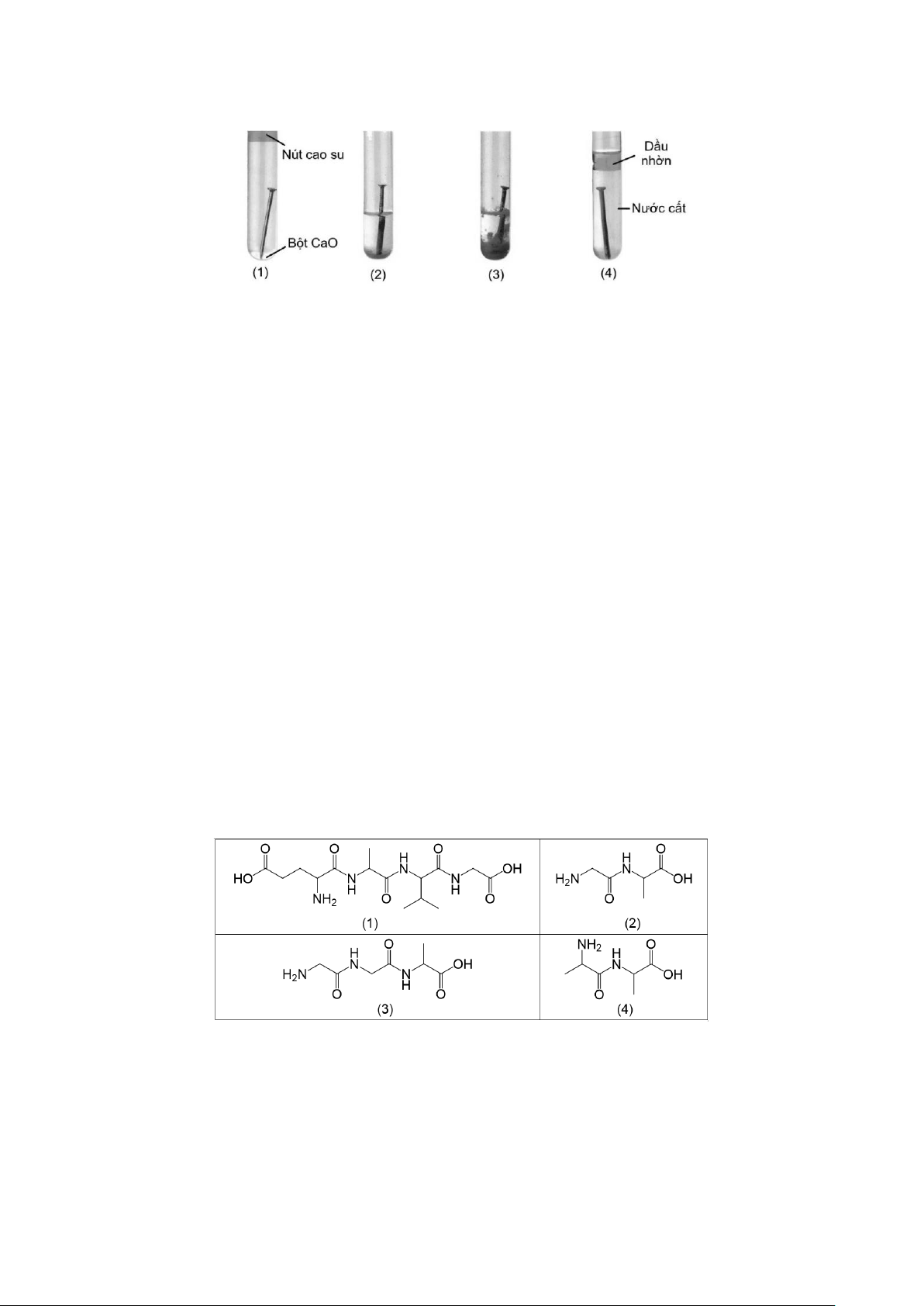
NAP 4. Một học sinh tiến hành thí nghiệm nghiên cứu ảnh hưởng của các chất môi trường đến
tốc độ ăn mòn điện hóa của chiếc đinh được làm từ thép (là hợp kim của sắt và carbon dạng than chì).
Ống nghiệm (1) được đậy kín bằng nút cao su, trong ống nghiệm, ngoài chiếc đinh thép còn có
một ít bột calcium oxide (CaO).
Ống nghiệm (2) có chứa chiếc đinh ngâm trong nước có hòa tan oxygen (trong không khí).
10 | Thay đổi tư duy – Bứt phá thành công
Ống nghiệm (3) có chứa chiếc đinh ngâm trong dung dịch muối ăn.
Ống nghiệm (4) có chứa chiếc đinh ngâm trong nước cất, phía trên có một lớp dầu nhờn.
Tiến hành đồng thời với 4 ống nghiệm. Sau vài ngày, kết quả thí nghiệm thu được như sau:
* Chú ý: ống nghiệm (1) và (4) đinh sắt không bị ăn mòn. Dầu nhờn là hỗn hợp các alkane ở trạng thái lỏng.
a. Ở ống nghiệm (1), bột CaO đã hấp thụ hết hơi nước, khí carbon dioxide nên không có
dung dịch điện ly khiến cho quá trình ăn mòn điện hóa học không xảy ra.
b. Ở ống nghiệm (3), khi đinh bị ăn mòn, tại anode xảy ra quá trình: O2 + 2H2O + 4e 4OH-.
c. Tốc độ ăn mòn của đinh ở các ống nghiệm (3) nhanh hơn so với ống nghiệm (2).
d. Ở ống nghiệm (4), dầu nhờn cản trở sự hòa tan khí oxygen và carbon dioxide trong
không khí vào nước cất khiến cho quá trình ăn mòn điện hóa không xảy ra.
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
NAP 1. Cho các dung dịch bão hòa sau đây (mỗi dung dịch chứa một chất tan): ammonia;
aniline; methylamine; lysine; glutamic acid; ethanol (cồn 70o). Trong các dung dịch trên, có bao
nhiêu dung dịch làm quỳ tím chuyển sang màu xanh?
Đáp số: ……………
NAP 2. Thế điện cực chuẩn của các cặp oxi hóa – khử: Al3+/Al và Ag+/Ag tương ứng là -1,68V;
+0,80V. Thiết lập một pin Galvani từ hai cặp oxi hóa khử là Al3+/Al và Ag+/Ag ở điều kiện
chuẩn. Pin có sức điện động chuẩn là bao nhiêu?
Đáp số: ……………
NAP 3. Cho các hợp chất sau:
Những chất nào trong ở trên tham gia phản ứng màu biuret cho màu tím đặc trưng? (kí hiệu các
chất được xếp dãy, theo thứ tự từ nhỏ đến lớn, viết liền. Ví dụ: 1234; 134;…)
Đáp số: ……………
NAP 4. Khi bảo quản trong phòng thí nghiệm, muối Mohr FeSO4.(NH4)2SO4.6H2O hút ẩm trong
không khí thành hỗn hợp rắn X. Để xác định phần trăm khối lượng muối Mohr trong X, tiến
hành thí nghiệm theo các bước sau:
Thay đổi tư duy – Bứt phá thành công | 11
Bước 1: Cân chính xác 12,81 gam X rồi hòa tan hoàn toàn trong nước để thu được 500,00 mL dung dịch Y.
Bước 2: Lấy 10,00 mL dung dịch Y cho vào bình tam giác, thêm 5 mL sulfuric acid nồng độ 1M.
Tiến hành chuẩn độ bằng dung dịch KMnO4 0,010M đến khi dung dịch chuyển từ không màu
sang màu hồng nhạt bền trong 20 giây thì kết thúc chuẩn độ. Lặp lại thí nghiệm chuẩn độ thêm
ba lần nữa. Kết quả thể tích dung dịch KMnO4 0,010M được ghi trong bảng sau: Thí nghiệm Lần 1 Lần 2 Lần 3 Lần 4 VKMnO4 (mL) 12,8 12,6 12,9 12,9
Phần trăm khối lượng của muối Mohr trong X là bao nhiêu? (Các phép tính chỉ làm tròn kết quả ở
bước cuối cùng. Kết quả làm tròn đến hàng đơn vị; ghi phần số, không ghi dấu %. Ví dụ: kết quả là 32,15% ghi thành 32;…)
Đáp số: ……………
NAP 5. Baking soda (NaHCO3) là phụ gia thực phẩm, được dùng làm tăng độ xốp của bánh do
dễ bị phân hủy tạo ra khí carbon dioxide và hơi nước, tạo nhiều lỗ xốp.
Khi làm bánh, một đầu bếp đã sử dụng 3,36 gam banking soda để tăng độ xốp. Bánh được
nướng ở nhiệt độ 160oC. Giả thiết có 10% lượng khí và hơi nước tạo ra ở lại bánh, tạo thành các
lỗ xốp. Biết ở điều kiện nhiệt độ, áp suất trên, 1,0 mol khí có thể tích 35,5 L. Tổng thể tích lỗ xốp
tạo ra từ 3,36 gam banking soda trong điều kiện trên là bao nhiêu mL?
Đáp số: ……………
NAP 6. Cho sơ đồ phản ứng sau:
Cho biết X1, X2 và X5 là các hợp chất hữu cơ chỉ chứa một loại nhóm chức. Trong chuyển hóa
(b), X phản ứng với khí hydrogen (xúc tác Ni, đun nóng) thu được hỗn hợp sản phẩm trong đó
có X3. Ở phản ứng (c), enzyme β-lipase chỉ xúc tác cho sự thủy phân nhóm ester liên kết với
nguyên tử carbon số 2 của gốc glycerol. Cho các nhận xét sau đây: (1) X1 là glycerol.
(2) Phân tử X2 có 17 nguyên tử carbon.
(3) Để tạo thành X3, 1 phân tử X cần phản ứng với 2 phân tử H2.
(4) X4 là hợp chất tạp chức.
(5) Thủy phân hoàn toàn 1 mol X4 bằng dung dịch NaOH dư thu được 2 mol X5.
Có những nhận xét nào đúng? (Các nhận xét đúng phải xếp theo thứ tự từ nhỏ đến lớn, viết liền. Ví dụ: 1234; 145;…)
Đáp số: ……………
---------------- HẾT ----------------
12 | Thay đổi tư duy – Bứt phá thành công
ĐỀ TRƯỜNG SỞ 2025
ĐỀ SỐ 203: THPT NGUYỄN KHUYẾN – LÊ THÁNH TÔNG
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
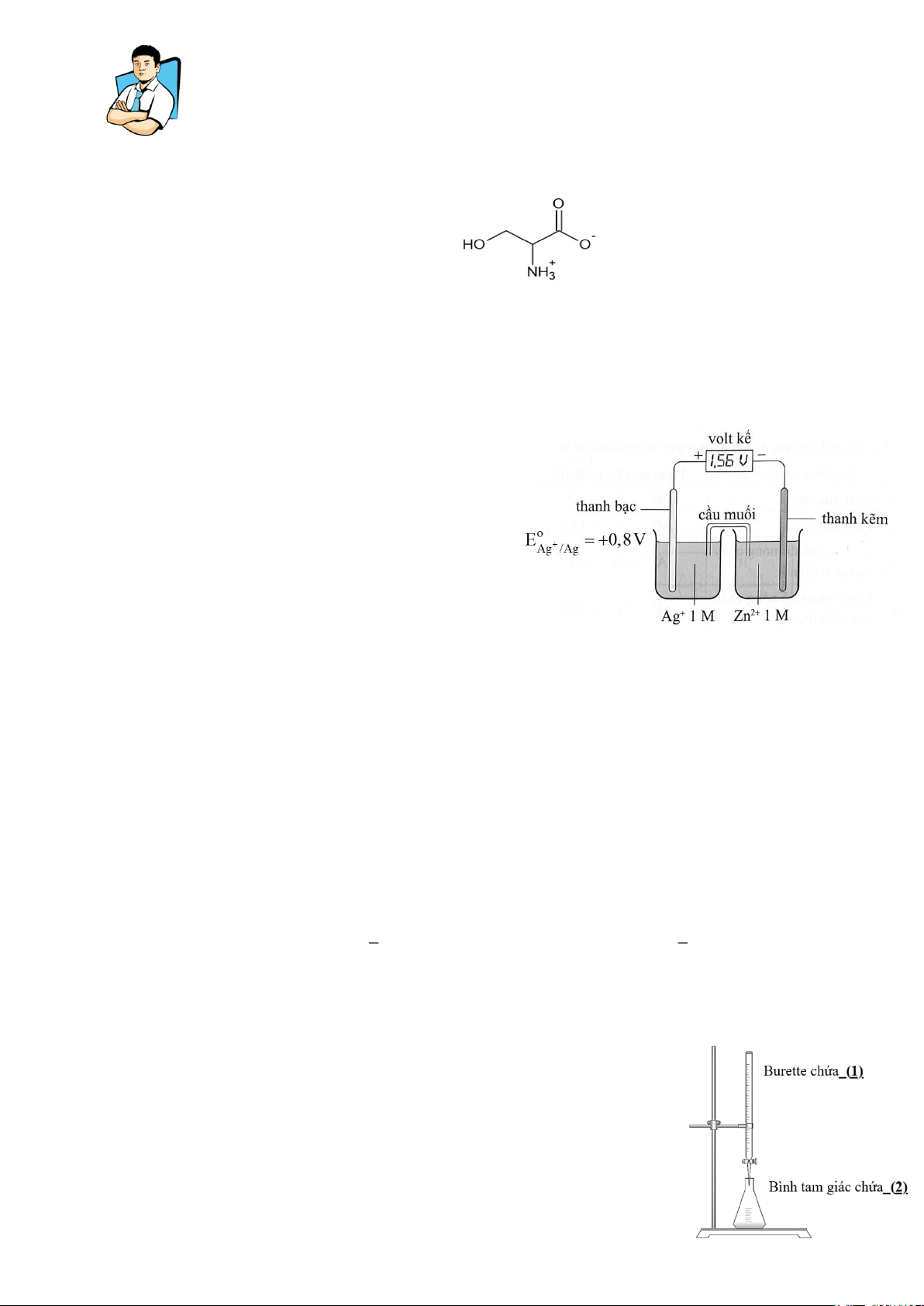
NAP 1. Serine là một α-aminoacid được sử dụng trong quá trình tổng hợp protein. Ở pH = 5,68
thì serine tồn tại chủ yếu ở dạng ion lưỡng cực.
Hiện tượng nào sau đây đúng khi đặt serine trong điện trường ở pH = 5,68.
A. Serine hầu như không di chuyển dưới tác dụng của điện trường.
B. Serine sẽ di chuyển về phía cực dương của điện trường.
C. Serine sẽ chuyển hoàn toàn về dạng cation.
D. Serine sẽ di chuyển về phía cực âm của điện trường.
NAP 2. Sử dụng một volt kế để đo sức điện động
của một pin điện hóa như sơ đồ bên.
Biết giá trị trên volt kế là suất điện động chuẩn của
pin. Nhận định nào sau đây đúng?
A. Thế điện cực chuẩn của Zn2+/Zn bằng 0,76 V.
B. Khi pin hoạt động thì nồng độ Ag+ tăng.
C. Khi pin hoạt động thì nồng độ Zn2+ tăng.
D. Thanh bạc là anode và thanh kẽm là cathode.
NAP 3. X là một ester đơn chức mạch hở có công thức phân tử C4H6O2. Phân tích phổ khối
lượng của X nhận thấy pic cơ bản ở m/z = 55. Tên gọi của X là A. Ally formate.
B. Ethyl acrylate. C. Vinyl acetate. D. Methyl acrylate.
NAP 4. Tơ nylon-6,6 có đặc tính dai, bền, bóng mượt, mềm mại nên được dùng dệt vải may
mặc, làm dây cáp, dây dù,…Cho phản ứng điều chế tơ nylon-6,6 như sau: o xt,t
nHOOC [CH2 4] COOH nH2N [CH2 6] NH2
( NH [CH2 6] NH CO [CH2 4] CO)n 2nH2O
Phản ứng trên thuộc loại phản ứng nào sau đây?
A. Phản ứng trùng ngưng.
B. Phản ứng tăng mạch polymer.
C. Phản ứng giảm mạch polymer.
D. Phản ứng trùng hợp.
NAP 5. Để xác định nồng độ của dung dịch FeSO4 bằng dung dịch
KMnO4 (dung dịch thuốc tím), người ta lắp bộ dụng cụ thí nghiệm như
hình bên. Nhận định nào sau đây đúng?
Thay đổi tư duy – Bứt phá thành công | 13
A. (1) dung dịch KMnO4; (2) dung dịch hỗn hợp FeSO4 và H2SO4 loãng.
B. (1) dung dịch KMnO4; (2) dung dịch hỗn hợp FeSO4 và quỳ tím.
C. (1) dung dịch hỗn hợp FeSO4 và H2SO4 loãng; (2) dung dịch KMnO4.
D. (1) dung dịch hỗn hợp FeSO4 và KMnO4; (2) dung dịch H2SO4 loãng.
NAP 6. Cho các chất sau: ethylamine, ethyl alcohol, methyl formate, ethane và các giá trị nhiệt
độ sôi không tương ứng 31,5 oC; 16,6 oC; -88,6 oC; 78,3 oC. Nhiệt độ sôi của ethylamine có giá trị là A. 16,6 oC. B. 31,5 oC. C. -88,6 oC. D. 78,3 oC.
NAP 7. Công nghiệp silicate là ngành công nghiệp sản xuất đồ gốm, xi măng, thủy tinh từ
nguồn nguyên liệu có trong tự nhiên, cơ bản là cát thạch anh (silicon dioxide), đất sét và các
phụ gia khác. Sản phẩm nào sau đây không thuộc sản phẩm của công nghiệp silicate?
A. Chậu hoa bằng gốm.
B. Kính ô tô bằng thủy tinh hữu cơ.
C. Ly pha lê thủy tinh.
D. Gạch, ngói xây dựng.
NAP 8. Khi để lâu ngày trong không khí ẩm gang, thép bị ăn mòn điện hóa. Khi đó Fe là anode
và carbon là cathode. Bán phản ứng xảy ra chủ yếu tại cathode là A. O
2(g) + H2O(l) + 4e 4OH (aq) .
B. 4OH (aq) O2(g) + H2O(l) + 4e. C. 2H(aq) + 2e H 2(g).
D. C(s) + 4H (aq) + 4e CH4(g).
NAP 9. Phức chất nào sau đây là phức chất aqua? A. [Cu(NH3)4(OH2)2]2+. B. [Fe(OH)3(OH2)3]. C. [Ti(OH2)6]3+. D. [Pt(NH3)2Cl2].
NAP 10. X là kim loại có tính dẫn điện tốt nên được sử dụng phổ biến làm ruột dây điện dân dụng…. Kim loại X là A. Fe. B. Cu. C. Al. D. Ag.
NAP 11. Vật liệu polymer nào sau đây có thành phần chính là polymer bán tổng hợp? A. Tơ nitron.
B. Thủy tinh hữu cơ. C. Tơ capron. D. Tơ visco.
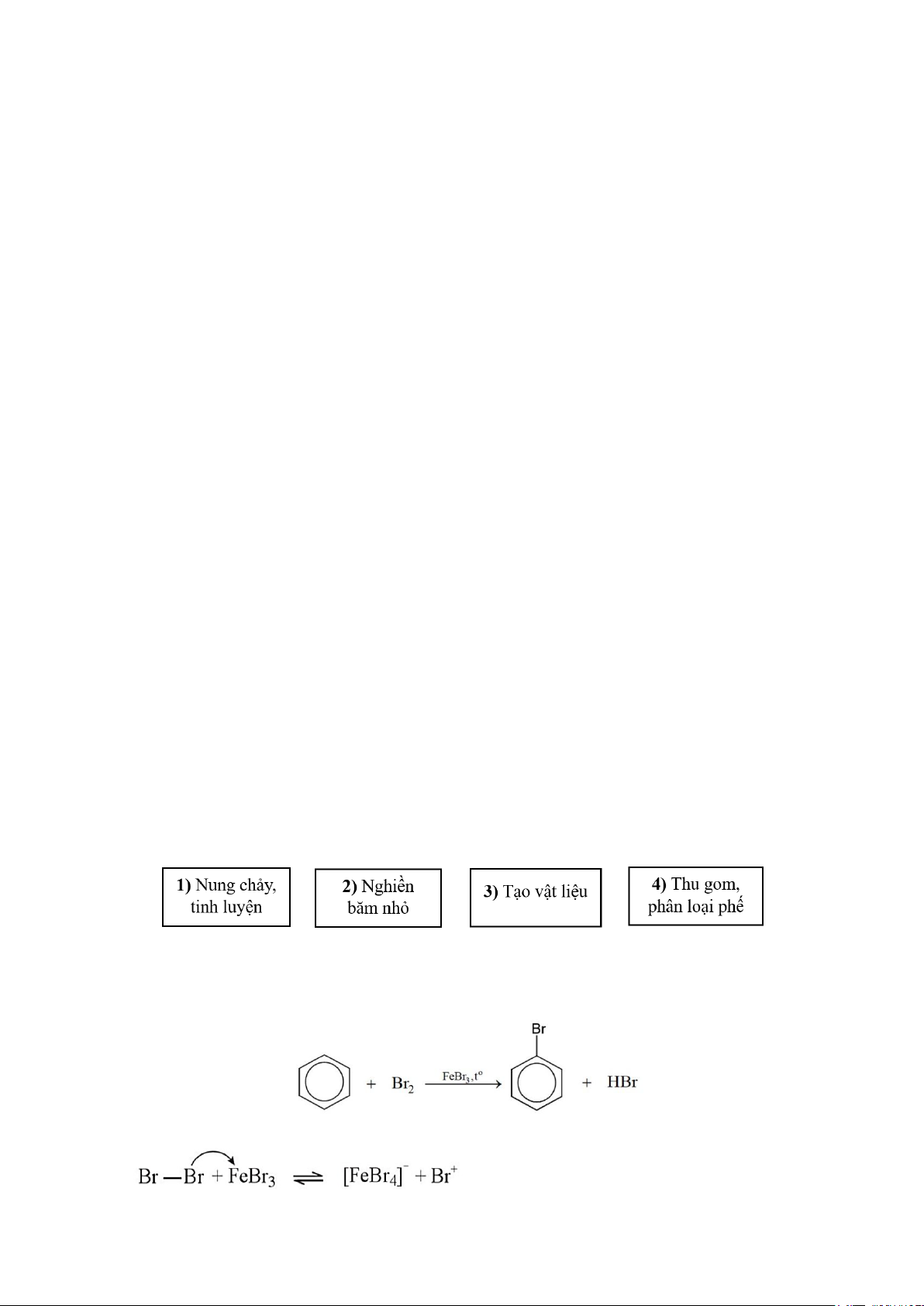
NAP 12. Việc tái chế các kim loại phổ biến (như sắt, thép, nhôm, đồng) thường được thực hiện
qua nhiều công đoạn. Cho các công đoạn sau:
Thứ tự sắp xếp hợp lí các công đoạn là A. 2-4-1-3. B. 4-3-2-1. C. 4-2-1-3. D. 4-2-3-1.
NAP 13. Khi có mặt xúc tác FeBr3, benzene tác dụng với bromine theo phản ứng:
Cơ chế của phản ứng trên như sau: Bước 1:
14 | Thay đổi tư duy – Bứt phá thành công Bước 2: Bước 3:
Nhận định nào sau đây không đúng?
A. Phản ứng giữa benzene với bromine thuộc loại phản ứng thế.
B. Bước 2 xảy ra quá trình tương tác giữa benzene với tác nhân nucleophile.
C. Bước 1 xảy ra sự phân cắt dị li phân tử Br2 (sự phân cắt mà cặp electron dùng chung
chỉ thuộc về 1 nguyên tử).
D. Bước 3 xảy ra quá trình tách proton (H+) để tạo ra sản phẩm.
NAP 14. Phát biểu nào sau đây đúng?
A. Maltose có nhiều trong quả chuối chín.
B. Đường mía chứa nhiều saccharose.
C. Glucose có nhiều nhất trong mật ong.
D. Cellulose có nhiều trong ngô, khoai.
NAP 15. X là amino acid có công thức cấu tạo H2NCH2COOH. Phát biểu nào sau đây không đúng về X?
A. X là một α-amino acid.
B. Tên thông thường của X là glycine.
C. X có nhiệt độ nóng chảy cao hơn acetic acid.
D. X ít tan trong nước.
NAP 16. Trong công nghiệp, dãy nào sau đây chỉ gồm những kim loại được sản xuất chủ yếu
bằng phương pháp điện phân nóng chảy? A. Al, Na, Mg. B. Cu, Au, Al. C. Na, Al, Au. D. Ag, Cu, Fe.
NAP 17. Ứng dụng nào sau đây không phải ứng dụng của sodium chloride (NaCl)?
A. Dùng để sản xuất nước muối sinh lí (dung dịch NaCl 0,9%).
B. Dùng để khử trùng nước sinh hoạt.
C. Làm nguyên liệu trong quá trình Solvay để sản xuất soda (Na2CO3).
D. Làm nguyên liệu trong công nghiệp chlorine – kiềm.
NAP 18. Nguyên tử cobalt (Co) có số hiệu nguyên tử bằng 27. Ở trạng thái cơ bản, cấu hình electron của ion Co3+ là A. [Ar]3d44s2. B. [Ar]3d7. C. [Ar]3d6. D. [Ar]3d74s2.
PHẦN II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí
sinh chọn đúng hoặc sai.
NAP 1. Có thể tinh chế đồng không tinh khiết có lẫn một lượng
nhỏ Ag, Zn, Ni bằng phương pháp điện phân như hình bên.
Trong quá trình điện phân phần lớn dòng điện được sử dụng
để hòa tan đồng ở anode và kết tủa đồng tinh khiết trên
cathode. Tuy nhiên, một phần nhỏ dòng điện bị hao phí cho
Thay đổi tư duy – Bứt phá thành công | 15
việc hòa tan các tạp chất ở anode. Khi cho dòng điện 20 A chạy qua bình điện phân tinh chế
đồng, sau 10 giờ ngắt dòng điện thì thấy có 225 g đồng tinh kiết bám trên cathode.
Cho biết: I t ne 96500; I là cường độ dòng điện (A), t là thời gian (s), ne là số mol electron trao đổi; o E 2 ; o 0, 34V E . 0,799V Cu /Cu Ag /Ag
a. Anode làm bằng khối đồng có độ tinh khiết cao.
b. Tỉ lệ phần trăm dòng điện bị hao phí là 5,76%. (kết quả làm tròn đến hàng phần trăm)
c. Do Ag có tính khử yếu hơn Cu, nên khi đồng trong cực dương tan ra thì bạc vẫn ở
dạng nguyên tử kim loại và lắng xuống đáy bình điện phân.
d. Muối X sử dụng trong quá trình điện phân luôn là CuCl2.
NAP 2. X là một amine mạch hở có công thức RNH2. Trong X nguyên tố nitrogen chiếm 31,11% về khối lượng.
a. Dung dịch của chất X hòa tan Cu(OH)2 tạo phức chất màu xanh lam.
b. X tan trong nước có cân bằng: RNH 2 H2O RNH2 3 H O .
c. X có tên thay thế là methanamine.
d. X tác dụng với hỗn hợp NaNO2 và HCl thì thu được alcohol có công thức CH3CH2CH2OH.
NAP 3. Enzyme pepsin có khả năng xúc tác
cho phản ứng thủy phân protein. Hoạt tính
xúc tác của enzyme càng cao thì phản ứng
thủy phân protein diễn ra càng nhanh. Hoạt
tính xúc tác của enzyme phụ thuộc vào các
yếu tố như nhiệt độ, pH,…Một nhóm học
sinh tiến hành thí nghiệm ở nhiệt độ không
đổi nhưng thay đổi pH của môi trường để
khảo sát thời gian thủy phân hết anbumin
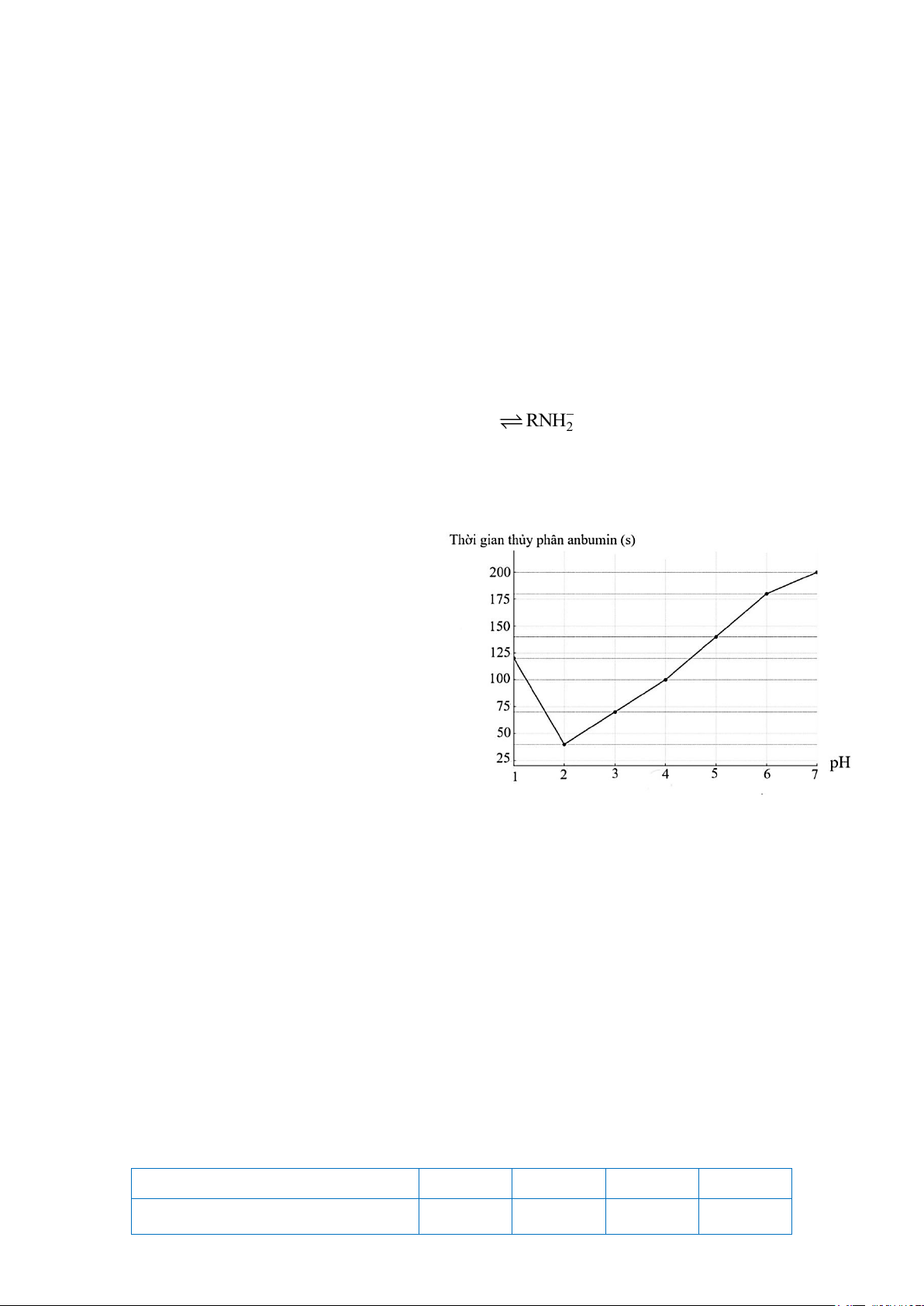
bằng enzyme pepsin. Khoảng pH nhóm học
sinh khảo sát là từ 1 đến 7. Nhóm học sinh vẽ được đồ thị như hình bên.
a. Ở các giá trị pH nghiên cứu, hoạt tính xúc tác của enzyme pepsin cao nhất tại pH = 2.
b. Từ kết quả thí nghiệm nhóm học sinh khác nhận định anbumin sẽ bị thủy phân hoàn
toàn bởi enzyme pepsin trong dung dịch NaHCO3.
c. Từ kết quả thí nghiệm, kết luận được hoạt tính xúc tác của enzyme pepsin giảm liên tục khi pH tăng.
d. Theo số liệu thu được, phản ứng thủy phân anbumin ở pH = 1 diễn ra nhanh hơn ở pH = 5.
NAP 4. Các muối carbonate của kim loại nhóm IIA khó tan trong nước và bị phân hủy theo phản ứng sau: MCO3(s) o t MO(s) + CO2(g) (*) Cho bảng thông tin sau: Muối MCO3 MgCO3 CaCO3 SrCO3 BaCO3 o
rH298 (kJ) của phản ứng (*) 100,7 179,2 234,6 271,5
16 | Thay đổi tư duy – Bứt phá thành công
Độ tan (g/100 g H2O) tại 20 oC
1,00.10-2 1,30.10-3 1,10.10-3 2,40.10-3
a. Để thu được cùng khối lượng các oxide kim loại thì phản ứng phân hủy BaCO3 cần
năng lượng nhiều nhất.
b. Tại 20 oC thì 1,5 lít H2O (d = 1 g/mL) hòa tan được tối đa 19,5 mg CaCO3.
c. Độ bền nhiệt của các muối có xu hướng tăng từ MgCO3 đến BaCO3.
d. Phản ứng (*) minh họa cho quá trình đun sôi để làm giảm tính cứng của nước cứng
tạm thời (với M = Ca2+, Mg2+).
PHẦN III. Thí sinh trả lời từ câu 1 đến câu 6.
NAP 1. Khi hàm lượng ion phosphate ( 3 4
PO ) trong nước tăng cao sẽ dẫn đến hiện tượng phú
dưỡng. Để tránh hiện tượng phú dưỡng có thể làm giảm hàm lượng ion phosphate bằng cách
thêm Fe3+ hoặc Al3+ để tạo thành các hợp chất phosphate không tan. Một nguồn nước thải có
hàm lượng ion phosphate là 16 mg L-1. Trong một hệ thống xử lý nguồn nước thải trên với lưu
lượng 25000 m3/ngày thì cần x kg FeCl3. Biết thực tế người ta sử dụng tỉ lệ mol Fe : P = 1,25 : 1.
(làm tròn kết quả đến hàng đơn vị)
Đáp số: ……………
NAP 2. Cho các thí nghiệm ở cột trái, khí và kết tủa ở cột phải như sau:
a. Cho Cu vào lượng dư dung dịch H2SO4 đặc, nóng.
1) khí SO2, kim loại Cu không
b. Cho hỗn hợp kim loại Cu và Fe vào lượng dư dung dịch tan. H2SO4 loãng. 2) khí CO2.
c. Cho lượng dư dung dịch NaHSO4 vào dung dịch
3) khí H2, kim loại Cu không Ba(HCO3)2. tan.
d. Cho sodium (Na) vào dung dịch CuSO4. 4) khí SO2.
5) khí H2, có Cu(OH)2 không tan. 6) khí CO2, có BaSO4 không tan.
Gán số thứ tự khí và kết tủa ở cột phải tương ứng với thí nghiệm ở cột trái và sắp xếp theo trình
tự dãy bốn số (ví dụ: 1234, 4321,…).
Đáp số: ……………
NAP 3. Methane hydrate hay còn được gọi là methane clathrate,
có công thức (CH4)x(H2O)46. Đây là hợp chất kết tinh, có khả năng
cung cấp khí đốt có giá trị. Biết trong methane clathrate nguyên
tố hydrogen chiếm 12,971% về khối lượng. Nếu phá hủy hoàn
toàn 1 tấn tinh thể methane clathrate rồi đốt cháy hết lượng CH4
thu được, khi đó năng lượng sinh ra tối đa tương đương bao
nhiêu kWh? (kết quả làm tròn đến hàng đơn vị)
Biết 1 kWh = 3600 kJ và phản ứng cháy của CH4 như sau: CH4(g) + 2O2 (g) CO2(g) + 2H2O(l) o 1
fH298(kJmol ) -74,6 0 -393,5 -285,8
Đáp số: ……………
Thay đổi tư duy – Bứt phá thành công | 17
NAP 4. Calcium hydroxyl-apatite [Ca10(PO4)6(OH)2] được ứng dụng làm thành phần chính
trong kem đánh răng với mục đích tái khoáng hóa men răng. Calcium hydroxyl-apatite có thể
được tổng hợp từ sơ đồ sau: 3 HNO (NH4)2HPO4NH3H2O Ca 3 CO Ca(N 3
O )2.4H2O 10 Ca (PO4)6(OH)2
Một nhà máy cần sản xuất 1 triệu tuýp kem đánh răng (loại 75g/1 tuýp) chứa 7% calcium
hydroxyl-apatite về khối lượng. Tính khối lượng (tấn) đá vôi (chứa 1% tạp chất trơ) cần để điều
chế đủ lượng [Ca10(PO4)6(OH)2] cho sản xuất 1 triệu tuýp kem đánh răng trên. Biết hiệu suất cả
quá trình đạt 88% và các sản phẩm khác sinh ra trong sơ đồ không chứa nguyên tố Ca. (làm tròn
kết quả đến hàng đơn vị).
Đáp số: ……………
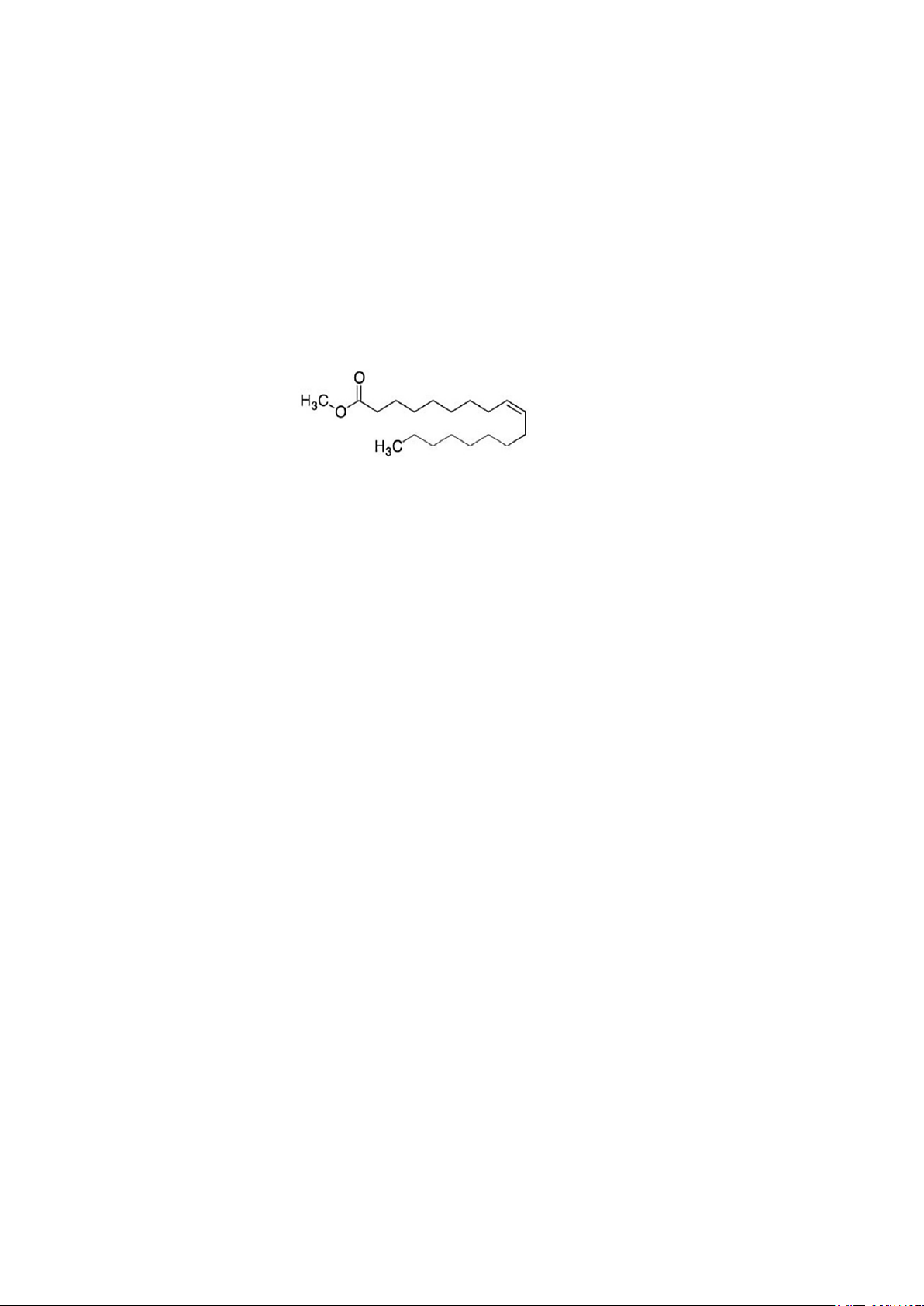
NAP 5. Methyl oleate được xem là một nhiên liêu biodiesel, đây là một loại nhiên liệu mới.
Methyl oleate có công thức:
, có bao nhiêu nguyên tử hydrogen
trong phân tử methyl oleate?
Đáp số: ……………
NAP 6. Copper(II) hydroxide tan trong dung dịch NH3 tạo phức chất bát diện X có công thức
[Cu(NH3)n(OH2)2]2+. Phân tử khối của X bằng bao nhiêu?
Đáp số: ……………
---------------- HẾT ----------------
18 | Thay đổi tư duy – Bứt phá thành công
ĐỀ TRƯỜNG SỞ 2025
ĐỀ SỐ 204: SỞ AN GIANG – MÃ 0301
PHẦN I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
NAP 1: Các hợp chất hữu cơ có các đặc điểm chung. Đặc điểm nào sau đây không phải đặc
điểm chung của hợp chất hữu cơ?
A. Các hợp chất hữu cơ dễ cháy, kém bền nhiệt nên dễ bị phân hủy.
B. Phản ứng của các hợp chất hữu cơ thường xảy ra chậm, theo nhiều hướng và tạo ra
hỗn hợp các sản phẩm.
C. Thành phần phân tử nhất thiết phải chứa nguyên tố carbon, thường có hydrogen,
oxygen, nitrogen, halogen, sulfur, phosphorus,...
D. Liên kết hóa học chủ yếu là liên kết ion.
NAP 2: Nhóm học sinh được giao nhiệm vụ thực hiện thí nghiệm kim loại kẽm (Zinc - Zn) phản
ứng với dung dịch copper (II) sulfate (CuSO4). Học sinh dự đoán “kim loại Zn khử được ion
Cu2+ và màu dung dịch có sự thay đổi”. Học sinh làm thí nghiệm theo các bước sau:
Bước 1: Lấy khoảng 3mL dung dịch copper (II) sulfate cho vào ống nghiệm.
Bước 2: Lấy viên kẽm đã được làm sạch cho vào ống nghiệm chứa dung dịch CuSO4. Sau thời
gian 5 phút xảy ra phản ứng học sinh rút ra nhận xét.
Nhận xét nào sau đây là không chính xác?
A. Sau 5 phút khối lượng của dung dịch tăng so với dung dịch ban đầu.
B. Kim loại Cu bám lên bề mặt viên kẽm có màu đỏ.
C. Sau 5 phút khối lượng viên kẽm tăng so với khối lượng ban đầu.
D. Màu của dung dịch CuSO4 nhạt dần.
NAP 3: Hợp chất R32 là chất làm lạnh đang được sử dụng phổ biến hiện nay. R32 có công thức
CH2F2. Tên gọi của CH2F2 là A. fluoromethane. B. fluoroethane. C. difluoroethane. D. difluoromethane.
NAP 4: Hợp chất X được dùng trong thực phẩm làm cho bột nở, giúp bánh xốp. Khi đốt cháy X
trên ngọn lửa vô sắc, ngọn lửa có màu vàng. Chất X là
A. NaNO3, khi đun nóng phân hủy thành khí O2 giúp cho bánh xốp.
B. NaCl, khi đun nóng phân hủy thành khí Cl2 giúp bánh xốp.
C. NaHCO3, khi đun nóng phân hủy thành khí CO2 giúp cho bánh xốp.
D. Na2CO3, khi đun nóng phân hủy thành khí CO2 giúp cho bánh xốp.
NAP 5: Trong dung dịch có môi trường pH = 6,0 alanine tồn tại như hình bên:
Đặt alanine trong điện trường dung dịch có pH = 2,0. Nhận định nào sau đây là đúng?
A. Alanine nhận proton, trở thành cation và di chuyển về cực âm.
B. Alanine trở thành dạng phân tử và không di chuyển.
C. Alanine chủ yếu ở dạng ion lưỡng cực và không di chuyển.
D. Alanine nhường proton trở thành anion và di chuyển về cực dương.
Thay đổi tư duy – Bứt phá thành công | 19


