










Preview text:
CHIẾN DỊCH TỔNG ÔN HÓA 12 TỪ A-Z
55 CÂU TỔNG ÔN PHỨC CHẤT
(Team TYHH chúc các em 2K7 đỗ nguyện vọng 1)
Câu 1: Cho phát biểu sau: “Phức chất đơn giản thường có một.(1). liên kết với các phối tử bao quanh. Liên kết
giữa nguyên tử trung tâm và phối từ trong phức chất là liên kết.(2).”. Cụm từ cần điền vào (1) và (2) lần lượt là
A. cation kim loại, ion.
B. nguyên tử kim loại, cho – nhận.
C. nguyên tử trung tâm, cho – nhận. D. phối tử, ion.
Câu 2: Công thức tổng quát của phức chất (với nguyên tử trung tâm M và phối tử L) có dạng tứ diện và bát
diện lần lượt là A. [ML2] và [ML4]. B. [ML4] và [ML6]. C. [ML6] và [ML2]. D. [ML6] và [ML4].
Câu 3: Phối tử trong phức chất [PtCl4]2– và [Fe(CO)5] lần lượt là A. Cl và. C. B. Pt và Fe.
C. Cl và CO. D. Cl và CO.
Câu 4: Điện tích của phức chất [PtCl4]2– và [Fe(CO)5] lần lượt là A. +2 và +5. B. +2 và 0. C. –1 và 0. D. –2 và 0.
Câu 5: Trong phân tử phức chất [Ag(NH3)2]OH, nhóm NH3 được gọi là A. phối tử. C. chất oxi hoá. B. acid.
D. nguyên tử trung tâm.
Câu 6: Số oxi hoá của nguyên tử trung tâm platinum trong phức chất [PtCl6]2– là A. +2. B. +3. C. +4. D. +6.
Câu 7: Điện tích của nguyên tử trung tâm trong phức chất [Co(NH3)6]3+ và [FeF6]3– lần lượt là A. +3 và +3. B. +3 và +2. C. +6 và –6. D. +3 và –3.
Câu 8: Dạng hình học có thể có của phức chất [FeF6]3– là A. tứ diện. B. bát diện. C. vuông phẳng.
D. tứ diện hoặc vuông phẳng.
Câu 9: Phức chất của Cr(0) có dạng hình học bát diện chỉ chứa phối tử CO có công thức hoá học là A. [Cr(CO)4]. B. [Cr(CO)6]. C. [Cr(CO)4]2+. D. [Cr(CO)6]2+.
Câu 10: Phức chất nào sau đây của Cu2+ có màu vàng? A. [Cu(H2O)6]2+. B. [CuCl4]2–.
C. [Cu(NH3)4(H2O)2]. D. [Cu(OH)2(H2O)4].
Câu 11: Phức chất [Cu(H2O)6]2+ có màu xanh; phức chất [Cu(NH3)4(H2O)2] có màu xanh lam và phức chất
[CuCl4]2– có màu vàng. Màu sắc của ba phức chất khác nhau là do chúng khác nhau về
A. nguyên tử trung tâm.
B. cả nguyên tử trung tâm và phối tử. C. phối tử.
D. số lượng phối tử.
Câu 12: Nhỏ vài giọt dung dịch HCl đặc vào dung dịch CuSO4 tạo thành phức chất [CuCl4]2–. Dấu hiệu nào sau
đây chứng tỏ phức chất [CuCl4]2– tạo thành? 1 | T Y H H
A. Hoà tan kết tủa.
B. Đổi màu dung dịch từ màu xanh sang màu vàng.
C. Xuất hiện kết tủa.
D. Đổi màu dung dịch từ màu vàng sang màu xanh.
Câu 13: Cho lượng dư dung dịch NH3 tác dụng với AgCl. Phát biểu nào sau đây đúng?
A. Kết tủa trắng tan dần, phức chất [Ag(NH3)2]+ không màu được tạo thành.
B. Không có hiện tượng gì xảy ra.
C. Kết tủa trắng tan dần, phức chất [Ag(NH3)2]+ màu xanh được tạo thành.
D. Kết tủa trắng tan dần, phức chất [Ag(NH3)4]+ không màu được tạo thành.
Câu 14: Nhỏ vài giọt dung dịch NaOH loãng vào dung dịch CuSO4 tạo thành phức chất [Cu(OH)2(H2O)4]. Dấu
hiệu nào sau đây chứng tỏ phức chất [Cu(OH)2(H2O)4] tạo thành?
A. Xuất hiện kết tủa màu xanh lam.
B. Hoà tan kết tủa.
C. Dung dịch chuyển từ màu xanh sang màu vàng.
D. Xuất hiện kết tủa màu xanh nhạt.
Câu 15: Các phối tử H2O trong phức chất [Ni(H2O)6]2+ có thể bị thế hết bởi sáu phối tử NH3 tạo thành phức chất là A. [Ni(NH3)6]2+.
B. [Ni(NH3)2(H2O)4]. C. [Ni(NH3)(H2O)5]2+. D. [Ni(NH3)5(H2O)]2+.
Câu 16: Phối tử H2O trong phức chất aqua [Cu(H2O)6]2+ có thể bị thế bởi 1 phối tử NH3 tạo thành phức chất là A. [Cu(NH3)6]2+.
B. [Cu(NH3)2(H2O)5]. C. [Cu(NH3)(H2O)5]2+. D. [Cu(NH3)(H2O)5]+.
Câu 17: Ion phức chất [Pt(NH3)4]2+ tham gia phản ứng thế hai phối tử NH3 bằng hai phối tử Cl–, tạo thành phức
chất có điện tích bằng A. 0. B. –2. C. –4. D. +2.
Câu 18: Trong dung dịch FeCl3, Fe3+ có thể tồn tại ở nhiều dạng phức chất khác nhau, một trong số đó là phức
chất bát diện có điện tích là +1 tạo bởi giữa ion Fe3+ với phối tử H2O và Cl–. Số phối tử H2O có trong phức chất là A. 4. B. 6. C. 5. D. 3.
Câu 19: Cho sơ đồ chuyển hoá sau: CuSO +H O + 4(s) 2 ⎯⎯⎯→ [Cu(OH ⎯⎯⎯⎯ → [Cu(OH) (1) 2)6]2+(aq) ddNaOH (2) 4(OH)2](s) [Cu(OH +ddNH 2)4(OH)2](s) 3 ⎯⎯⎯→ [Cu(NH (3) 3)4(OH2)]2+(aq)
Những phản ứng có sự tạo thành phức chất là A. (1) và (2). B. (1) và (3). C. (2) và (3). D. (1), (2) và (3).
Câu 20: Cho sơ đồ chuyển hoá sau: AgNO +H O +ddNH 3(s) 2 ⎯⎯⎯→ [Ag(OH ⎯⎯⎯→ Ag (1) 2)4]+(aq) 3 (2) 2O(s) Ag +ddNH + 2O(s) 3 ⎯⎯⎯→ [Ag(NH ⎯⎯⎯⎯ → [Ag(CN) (3) 3)2]+(aq) ddKCN (4) 2](aq) 2 | T Y H H
Những phản ứng có sự tạo thành phức chất là A. (1), (2), (3). B. (1), (3), (4). C. (2), (3), (4). D. (1), (2), (4).
Câu 21: Số electron độc thân của nguyên tử cobalt (Z = 27) là bao nhiêu?. 3
Câu 22: Cấu hình electron của Fe là 1s22s22p63s23p63d64s2. Xác định số electron độc thân trong ion Fe2+. 4
Câu 23: Cho dung dịch NH3 đặc vào dung dịch phức chất [PtCl4]2– thu được phức chất có điện tích +1 là do một
số phối tử Cl– trong phức [PtCl4]2– bị thay thế bởi phối tử NH3. Số lượng phối tử Cl– đã bị thay thế là bao nhiêu?. 3
Câu 24: Cho các phản ứng sau:
(1) [Co(OH2)6]2+(aq) + 6NH3(aq)
[Co(NH3)6]2+(aq) + 6H2O(l)
(2) 2[Co(NH3)6]2+(aq) + H2O2(aq)
2[Co(NH3)6]3+(aq) + 2OH–(aq) (3) Au(s) + NO –
3 (aq) + 4H+(aq) + 4Cl–(aq)
[AuCl4]–(aq) + NO(g) + 2H2O(l)
(4) [Ag(NH3)2]+(aq) + 2CN–(aq)
[Ag(CN)2]–(aq) + 2NH3(aq)
(5) [Fe(OH2)6]3+(aq) + 2Cl–(aq)
[Fe(OH2)4Cl2]+(aq) + 2H2O(l) 3
Số phản ứng xảy ra sự thay thế phối tử là bao nhiêu?.
Câu 25: Cho các phản ứng sau:
(1) 2[Au(CN)2]–(aq) + Zn(s) ⎯⎯
→ [Zn(CN)4]2–(aq) + 2Au(s)
(2) 2[Fe(CN)6]+(aq) + Cl2(g) ⎯⎯
→ 2[Fe(CN)6]3–(aq) + 2Cl–(aq) (3) [Ag(NH +
3)2]+(aq) + 2H+(aq) + Cl–(aq) ⎯⎯
→ AgCl(s) + 2NH4 (aq)
(4) [Fe(OH2)6]3+(aq) + 3F–(aq) ⎯⎯
→ [Fe(OH2)3F3](aq) + 3H2O(l)
(5) [Cr(OH2)6]3+(aq) + 6OH–(aq) ⎯⎯
→ [Cr(OH)6]3–(aq) + 6H2O(l)
Liệt phản ứng xảy ra sự thay thế phối tử theo số thứ tự tăng dần. 45
Câu 26: Sự gia tăng hàm lượng nitrate trong nước là một trong những nguyên nhân của hiện tượng phú dưỡng.
Một trong những quy trình xác định hàm lượng nitrate trong nước được thực hiện như sau:
- Thí nghiệm 1. Lấy 10,0 mL dung dịch muối Mohr [(NH4)2SO4.FeSO4.6H2O], thêm H2SO4 1 M vào
và chuẩn độ bằng dung dịch KMnO4.
- Thí nghiệm 2. Lấy 10,0 mL dung dịch muối Mohr cho vào 100 mL nước chứa ion nitrate, sau đó thêm
NaOH(s) vào để đạt khoảng 28%, khi đó muối Mohr khử nitrate thành ammonia theo các phản ứng: NO – –
3 (aq) + 2Fe(OH)2 + H2O ⎯⎯ → NO2 + 2Fe(OH)3; (1) NO –
2 (aq) + 6Fe(OH)2 + 5H2O ⎯⎯
→ NH3 + 6Fe(OH)3 + OH–; (2)
Sau khi các phản ứng (1) và (2) hoàn toàn, lọc bỏ kết tủa, acid hoá dung dịch bằng dung dịch H2SO4 1
M và chuẩn độ lượng Fe2+ dư bằng dung dịch KMnO4 (Các chất và ion khác trong dung dịch không
phản ứng với KMnO4). Hãy cho biết mỗi mmol KMnO4 chênh lệch giữa thí nghiệm 1 với thí nghiệm 2
sẽ tương ứng với bao nhiêu mg NO –
3 trong nước. (Làm tròn kết quả đến hàng phần mười). 38,8 0,625 nhân 62 3 | T Y H H
Câu 27: Siderite là một khoáng vật quan trọng trong ngành công nghiệp và khai thác quặng sắt, có thành chính
là FeCO3. Hàm lượng sắt trong quặng này có thể được xác định bằng phương pháp chuẩn độ. Người ta
tiến hành thí nghiệm như sau:
- Bước 1: Cân chính xác 1,095 gam mẫu quặng siderite đã nghiền mịn và chuyển toàn bộ sang cốc thủy tinh 100 mL.
- Bước 2: Thêm 50 mL dung dịch H2SO4 loãng vào cốc, đun nhẹ để hòa tan quặng và đuổi khí CO2. Sau
khi hòa tan hoàn toàn, lọc lấy dung dịch và loại bỏ phần không tan. Sau đó định mức thành 100 mL dung dịch. FeCO3 + H2SO4 ⎯⎯ → FeSO4 + CO2 + H2O
- Bước 3: Hút chính xác 10,00 mL dung dịch sau khi định mức cho vào bình tam giác, thêm 2 mL dung
dịch H2SO4 loãng và thêm tiếp 10 giọt dung dịch H3PO4 (để che màu vàng của ion Fe3+). Đun nóng bình
tam giác đến 60 °C, chuẩn độ bằng dung dịch KMnO4 nồng độ 0,015 M đến khi xuất hiện màu hồng
nhạt bền trong 10 giây thì dừng lại.
10FeSO4 + 2KMnO4 + 8H2SO4 ⎯⎯
→ 5Fe2(SO4)3 + 2MnSO4 + K2SO4 + 8H2O
Lặp lại bước 3 thêm hai lần nữa. Thể tích trung bình của dung dịch KMnO4 sau ba lần chuẩn độ là 10,06
mL. Phần trăm khối lượng sắt trong quặng siderite là bao nhiêu phần trăm? (Kết quả làm tròn đến hàng 38,6 phần mười).
Câu 28: Trong dung dịch, ion Fe2+ và ion Fe3+ đều tạo thành ion phức chất aqua có dạng hình học bát diện, kí
hiệu tương ứng là (I) và (II).
a. Phân tử khối của (I) bằng phân tử khối của (II). (fe(h20)6)2+
b. Điện tích của (I) là +3, điện tích của (II) là +2. (fe(h2o)6)3+
c. Số lượng phối tử của (I) bằng số lượng phối tử của (II).
d. Số liên kết cho – nhận trong (I) và (II) đều bằng 6.
Câu 29: Cho ion phức chất có điện tích +1 và có cấu trúc như hình dưới:
a. Nguyên tử trung tâm trong ion phức chất là Co2+. co +3
b. Số phối tử trong ion phức chất là 6.
c. Ion phức chất có dạng hình học bát diện.
d. Ion phức chất có chứa ba loại phối tử.
Câu 30: Phức chất [Ni(CO)4] và phức chất [Ni(NH3)6]2+ có cấu trúc như sau: 4 | T Y H H
Mỗi phát biểu sau là đúng hay sai?
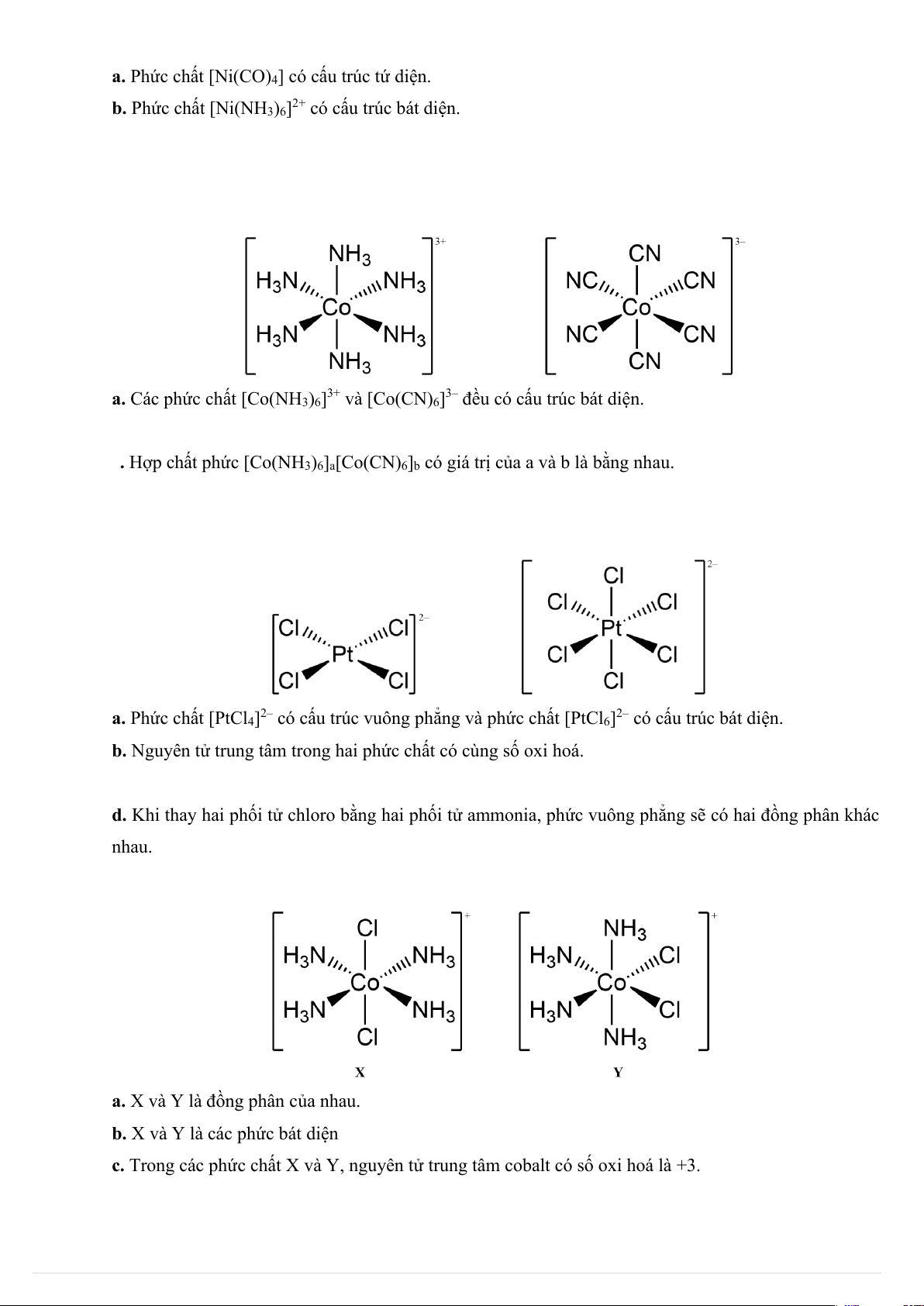
a. Phức chất [Ni(CO)4] có cấu trúc tứ diện.
b. Phức chất [Ni(NH3)6]2+ có cấu trúc bát diện.
c. Nguyên tử trung tâm nickel trong các phức chất trên có cùng số oxi hoá.
d. Phức chất [Ni(CO)4] tan tốt trong dung môi benzene do tạo liên kết hydrogen với benzene.
Câu 31: Các phức chất [Co(NH3)6]3+ và [Co(CN)6]3– có cấu trúc như sau:
a. Các phức chất [Co(NH3)6]3+ và [Co(CN)6]3– đều có cấu trúc bát diện.
b. Nguyên tử trung tâm cobalt trong các phức chất trên có cùng số oxi hoá.
c. Hợp chất phức [Co(NH3)6]a[Co(CN)6]b có giá trị của a và b là bằng nhau.
d. Các phức chất tạo từ cùng một nguyên tử trung tâm luôn có màu sắc giống nhau.
Câu 32: Các phức chất [PtCl4]2– và [PtCl6]2– có cấu trúc như sau:
a. Phức chất [PtCl4]2– có cấu trúc vuông phẳng và phức chất [PtCl6]2– có cấu trúc bát diện.
b. Nguyên tử trung tâm trong hai phức chất có cùng số oxi hoá.
c. Độ dài liên kết Pt–Cl trong các phức chất trên như nhau.
d. Khi thay hai phối tử chloro bằng hai phối tử ammonia, phức vuông phẳng sẽ có hai đồng phân khác nhau.
Câu 33: Cho hai phức chất đơn nhân X và Y có cấu trúc sau:
a. X và Y là đồng phân của nhau.
b. X và Y là các phức bát diện.
c. Trong các phức chất X và Y, nguyên tử trung tâm cobalt có số oxi hoá là +3.
d. Các phức chất X và Y có màu sắc giống nhau.
x là tran , y là cis nên ảnh hưởng đến màu 5 | T Y H H
Câu 34: Phức chất X có công thức cấu tạo như hình dưới:
a. Phức chất X thuộc loại phức bát diện.
b. Công thức của phức chất X là [Cr(O4C2)3]3–.
c. Số oxi hoá của nguyên tử trung tâm trong phức chất X là +3.
d. Trong phức chất X, nguyên tử trung tâm chromium liên kết với 3 phối tử oxalato (C 2– 2O4 ).
Câu 35: Metalloporphyrin có cấu trúc tương tự heme và được sử dụng việc kiểm soát chứng tăng bilirubin máu
ở trẻ sơ sinh (chứng này gây ra bệnh vàng da ở trẻ sơ sinh). Metalloporphyrin có công thức như sau: N 2+ N Fe N N
a. Ion trung tâm của phức Metalloporphyrin là Fe.
b. Số phối trí của phức là 4.
c. Metalloporphyrin là muối kép không phải là phức chất.
d. Liên kết trong phức Metalloporphyrin được tạo thành do nguyên tử N cho cặp electron chưa liên kết
vào orbital trống của nguyên tử Fe. cation fe2+
Câu 36: Để nhận biết sự có mặt của một số ion kim loại có thể tiến hành các thí nghiệm theo quy trình dưới đây:
- Ống nghiệm (1): Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm (1) chứa khoảng 1 mL dung dịch CuSO4.
- Ống nghiệm (2): Cho khoảng 4 – 6 giọt dung dịch NaOH vào ống nghiệm (2) chứa khoảng 1 mL dung dịch FeCl3.
a) Xuất hiện kết tủa màu xanh trong ống nghiệm (1), kết tủa nâu đỏ trong ống nghiệm (2).
b) Để kết tủa ống nghiệm (2) trong không khí một thời gian thì kết tủa chuyển sang màu vàng nâu.
c) Nếu thay dung dịch NaOH bằng dung dịch NH3 thì hiện tượng trong cả hai ống nghiệm vẫn xảy ra tương tự.
cu(oh)2 tạo phức với nh3 , phức tan
d) Dựa vào màu sắc của kết tủa có thể phân biệt được sự có mặt của ion Cu2+ và Fe3+ trong dung dịch.
Câu 37: Phèn sắt được sử dụng như là chất keo tụ trong quá trình xử lý nước (nước thải, nước giếng khoan,…)
do tạo chất kết tủa dạng keo kéo theo các chất bẩn lơ lửng trong nước lắng xuống. Phương trình thủy
phân ion Fe3+ được biểu diễn đơn giản như sau: 6 | T Y H H Fe3+ + 6H2O ⎯⎯ → phức chất X X phức chất Y + 3H+
a) Phức chất X là phức bát diện có công thức phân tử là [Fe(OH2)6]3+.
b) Để bảo quản dung dịch muối FeCl3 trong phòng thí nghiệm người ta thường nhỏ vài giọt dung dịch
acid vào trong lọ đựng dung dịch muối.
c) Dung dịch phèn sắt NH4Fe(SO4)3.12H2O có môi trường base. mtrg acid
d) Phức Y có công thức là [Fe(OH)2(H2O)3]. 3 oh
Câu 38: Thép thường hay thép carbon là hợp kim của Fe và C (≤ 2%), nguyên tố khác rất ít hoặc không có. Để xác
định hàm lượng Fe trong mẫu thép chứa Fe, C và Si người ta thực hiện các thí nghiệm sau:
- Cân 10,00 gam mẫu thép rồi cho vào 200 mL dung dịch H2SO4 1 M đến khi phản ứng xảy ra hoàn toàn
thu được 200 mL dung dịch X.
- Lấy 10,0 mL dung dịch X vào trong cốc thuỷ tinh, thêm tiếp dung dịch H2SO4 1 M (dư) rồi chuẩn độ
bằng dung dịch KMnO4 0,1 M. Kết quả chuẩn độ, thể tích (mL) dung dịch KMnO4 0,1 M sử dụng qua
3 lần chuẩn độ như sau: Lần chuẩn độ Lần 1 Lần 2 Lần 3 Thể tích dd KMnO4 0,1 M 17,6 17,4 17,5
a) Trong phản ứng chuẩn độ, chất khử là KMnO4.
b) Vai trò của C trong thép là bảo vệ Fe không bị ăn mòn điện hóa.
c) Điểm tương đương (kết thúc chuẩn độ) là khi dung dịch trong cốc bắt đầu chuyển màu tím. màu hồng
d) Hàm lượng Fe trong thép là 98,0%.
Câu 39: Để xác định hàm lượng Fe2+ trong một lọ muối Mohr (có công thức (NH4)2SO4.FeSO4.6H2O) người ta
tiến hành thí nghiệm như sau:
- Cân 5,00 gam muối rồi hoà tan vào nước, thêm tiếp 5 mL dung dịch H2SO4 20%, thêm nước cất vào
để định mức được 200 mL dung dịch (kí hiệu là dung dịch X).
- Lấy 10 mL dung dịch X đem chuẩn độ bằng dung dịch chuẩn KMnO4 0,02 M thì thấy hết 5 mL.
a) Phương trình phản ứng chuẩn độ:
6FeSO4 + 2KMnO4 + 4H2SO4 ⎯⎯
→ 3Fe2(SO4)3 + K2SO4 + 2MnO2 + 4H2O.
b) Thời điểm kết thúc chuẩn độ là lúc dung dịch xuất hiện màu hồng ổn định khoảng 20 giây.
c) Khi hòa tan muối Mohr trong nước sẽ cho môi trường acid. 11,2
d) Hàm lượng Fe trong mẫu muối Mohr đem phân tích ở trên là 1,12%.
Câu 40: Hoà tan 0,422 g mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả lượng sắt có
trong quặng đều chuyển thành Fe2+, thu được dung dịch A. Chuẩn độ Fe2+ trong dung dịch A bằng chất
chuẩn là dung dịch thuốc tím KMnO4 0,040 M. Khi đã sử dụng 23,50 mL thì phản ứng vừa qua điểm tương đương.
a) Nếu chỉ có Fe2+ trong dung dịch A tác dụng được với thuốc tím thì việc chuẩn độ dung dịch A sẽ giúp
xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được % (theo khối lượng) của
nguyên tố sắt có trong mẫu khoáng vật là 60,26%. 62,36 7 | T Y H H
b) Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch thuốc tím từ burette vào bình tam giác chứa dung dịch A.
c) Cần thêm chất chỉ thị phù hợp vào bình tam giác chứa dung dịch A để xác định được thời điểm kết
thúc quá trình chuẩn độ. knmo4 là thuốc tím, kết thúc cho màu hồng bền bững trong 20 giây
d) Cần lặp lại thí nghiệm chuẩn độ 2 lần để bảo đảm tính chính xác của kết quả. chuẩn độ ít nhất 4 lần
Câu 41: Hàm lượng sắt trong các mẫu quặng có thể biến đổi đa dạng, tùy vào vị trí tìm thấy. Một nhóm học sinh
tìm thấy một quặng sắt có thành phần chính là Fe2O3 và quan tâm đến việc có bao nhiêu sắt trong loại
quặng đó. Nhóm học sinh tiến hành các bước phân tích như sau:
- Bước 1: Cân 7,50 gam quặng, cho vào trong cốc rồi rót dung dịch nitric acid đậm đặc dư vào.
- Bước 2: Thêm một lượng phù hợp dung dịch sodium hydroxide vào dung dịch trên, thấy có kết tủa X
màu nâu đỏ xuất hiện.
- Bước 3: Thu lấy toàn bộ kết tủa bằng phễu lọc. Nung nóng kết tủa ở 900 °C cho đến khi khối lượng
không thay đổi thì thu được 3,19 gam chất rắn Y. Giả sử rằng các tạp chất trong mẫu quặng đã bị loại
bỏ hoàn toàn trước khi kết tủa.
a) Kết tủa X màu nâu đỏ là Fe(OH)3.
b) Dung dịch NaOH có tác dụng trung hòa acid dư và kết tủa ion Fe2+.
c) Có thể thay dung dịch NaOH bằng dung dịch KOH ở bước 2.
d) Hàm lượng sắt theo khối lượng trong mẫu quặng ban đầu là 35,0%. 29,867
Câu 42: Muối CoCl2 khan có màu xanh. Hòa tan một lượng muối này vào nước, thu được dung dịch màu hồng
(có chứa phức chất X). Nhúng mảnh giấy lọc vào dung dịch này, sấy khô, thu được mảnh giấy có màu
xanh (giấy Y). Giấy Y được sử dụng làm giấy chỉ thị để phát hiện nước.
a) CoCl2 là hợp chất của kim loại chuyển tiếp.
b) Phức chất X không chứa phối tử aqua (phối tử H2O).
c) Trong phức chất X, liên kết giữa nguyên tử trung tâm và phối tử là liên kết ion. liên kết phối trí
d) Khi nhỏ giọt nước lên giấy Y, giấy Y chuyển màu.
Câu 43: Muối FeCl3 khan là những tinh thể có màu vàng nâu. Hoà tan một lượng muối này vào nước, thu được
dung dịch có màu vàng nhạt (có chứa phức chất X). Lấy một ít dung dịch muối trên cho vào dung dịch
KSCN thì thấy xuất hiện màu đỏ đặc trưng, để giải thích hiện tượng trên là do xảy ra sự tạo phức như sau:
(1) Fe3+(aq) + 6H2O(l) ⎯⎯ → [Fe(OH2)6]3+(aq);
(2) [Fe(OH2)6]3+(aq) + SCN–(aq)
[Fe(OH2)5(SCN)]2+(aq) + H2O(l);
a) Phức chất X là phức chất của Fe3+ và phối tử H2O.
b) Dung dịch chứa phức X có môi trường base. mtrg acid
c) Trong môi trường base thì phức [Fe(OH2)5(SCN)]2+ khó hình thành hơn vì ion Fe3+ sẽ tạo kết tủa
Fe(OH)3 làm giảm nồng độ ion Fe3+.
d) Phản ứng trên dùng nhận biết ion Fe3+ cũng như nhận biết ion SCN–. 8 | T Y H H
Câu 44: Hemoglobin (Hb) là một loại protein chiếm khoảng 35% trọng lượng của hồng cầu. Hb có nhiệm vụ
nhận oxygen từ phổi và vận chuyển đi khắp cơ thể. Thành phần cấu tạo nên hemoglobin bao gồm nhân
heme và globin. Hình vẽ dưới đây mô tả cấu trúc của nhân heme:
- Nhân heme: Một heme sẽ bao gồm một ion Fe2+ ở chính giữa và một vòng porphyrin bao xung quanh.
Một phân tử Hb sẽ có chứa bốn nhân heme chiếm 5% trọng lượng hemoglobin.
- Hemoglobin: Được tạo từ các loại amino acid liên kết với nhau bằng các liên kết peptide để tạo thành chuỗi polypeptide.
Mỗi nguyên tử trung tâm trong nhân heme chỉ liên kết tối đa với 1 phân tử O2.
a) Dạng hình học của phức chất Fe(II) trong nhân heme là bát diện.
b) Mỗi phân tử hemoglobin có thể hấp thụ tối đa bốn phân tử oxygen.
c) Trong các nhân heme, nguyên tử trung tâm liên kết với phối tử qua các nguyên tử nitrogen.
d) Trong hemoglobin, iron chiếm 5% theo khối lượng.
Câu 45: Cho các quá trình tạo phức chất bát diện sau:
(1) Fe3+(aq) + 6H2O(l) ⎯⎯ → [Fe(OH2)6]3+(aq);
(2) [Fe(OH2)6]3+(aq) + SCN–(aq)
[Fe(OH2)5(SCN)]2+(aq) + H2O(l); KC = 1,4.102
(3) [Fe(OH2)6]3+(aq) + F–(aq)
[Fe(OH2)5F]2+(aq) + H2O(l); KC = 2,0.105
Biết dung dịch [Fe(OH2)6]3+ có màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch
[Fe(OH2)5F]2+ và các anion SCN–, F– đều không có màu.
a) Quá trình (1) xảy ra khi hoà tan iron(III) chloride trong nước. Kết thúc quá trình này thu được dung
dịch có chứa lượng lớn cation Fe3+ và phức chất aqua [Fe(OH
pư 1 chiều tạo ra phức aqua , ko còn 2)6]3+. fe 3+
b) So với anion F–, anion SCN– dễ thay thế phối tử H2O trong [Fe(OH)6]3+ hơn. dựa vào kc . kc lớn thay thế dễ
c) Khi cho từ từ dung dịch KSCN vào dung dịch ở quá trình (3) thì dung dịch này sẽ có màu.
d) Trong các quá trình (1), (2) và (3), mỗi phân tử H2O hoặc anion SCN– hay anion F– đều sử dụng số
cặp electron hoá trị riêng như nhau để cho vào orbital trống của cation Fe3+.
Câu 46: Cho dung dịch muối CoCl2 (có màu hồng) vào ống nghiệm, tồn tại cân bằng hoá học sau:
[Co(H2O)6]2+ (màu hồng) + 4Cl–
[CoCl4]2– (màu xanh) + 6H2O; o H 0 r 298
a) Dạng hình học của phức [Co(H2O)6]2+ là hình tứ diện.
b) Khi thêm từ từ HCl đặc vào ống nghiệm thì dung dịch chuyển dần thành màu xanh.
c) Ngâm ống nghiệm vào cốc nước nóng thì dung dịch chuyển thành màu hồng.
d) Phản ứng trên xảy ra sự thay thế phối tử của phức chất. 9 | T Y H H
Câu 47: Khi nhỏ dung dịch HCl đặc vào dung dịch CuSO4 0,5% thấy dung dịch CuSO4 chuyển từ màu xanh
sang màu vàng là do xảy ra quá trình: [Cu(H2O6)]2+ + 4Cl– [CuCl4]2– + 6H2O
a) Màu dung dịch phức của Cu2+ phụ thuộc vào phối tử.
b) Phức chất [Cu(H2O)6]2+ bền hơn phức chất [CuCl4]2–.
kém bền vì phức aqua chuyền đc thành phức cucl4...có màu vàng
c) Màu vàng là màu của ion Cl– trong dung dịch. màu của phức
d) Cấu trúc của phức [CuCl4]2– là bát diện.
Câu 48: Nhỏ muối thiocyanate (SCN–) vào dung dịch muối Fe3+ loãng, dung dịch từ màu vàng nhạt chuyển sang
màu đỏ máu là do 1 phối tử nước trong phức chất aqua có dạng hình học bát diện của Fe3+ bị thay thế bởi 1 phối tử SCN–.
a) Phức chất aqua có công thức hoá học là [Fe(H2O)6]3+.
b) Phức chất có màu đỏ máu là phức chất của Fe3+ có chứa 1 phối tử SCN– và 6 phối tử nước) 1scn- và 5 nước
c) Phức chất màu đỏ máu có công thức hoá học là [Fe(H2O)5(SCN)]2+.
d) Phức chất màu đỏ máu có điện tích +3. 2+
Câu 49: Cho CuSO4 khan không màu vào nước được dung dịch phức chất A màu xanh. Nhỏ từ từ dung dịch
NH3 đặc vào dung dịch A, lúc đầu thấy xuất hiện kết tủa phức chất B màu xanh nhạt, sau đó kết tủa tan
dần tạo thành dung dịch phức chất C màu xanh lam.
a) Phức chất A là [Cu(H2O)6]2+.
b) Phức chất B là [Cu(NH3)4(H2O)2]2+.
c) Phức chất C là [Cu(OH)2(H2O)4].
d) Dấu hiệu nhận biết sự tạo thành phức chất C là: hoà tan kết tủa và đổi màu dung dịch.
Câu 50: Xét phản ứng sau: [Cu(H2O)6]2+ + NH3 ⎯⎯ → [Cu(NH3)(H2O)5]2+
a) Phản ứng thuộc loại phản ứng oxi hoá – khử. phản ưng thay thế phối tử , bản chất là phản ứng trao đổi
b) 1 phối tử nước trong phức chất [Cu(H2O)6]2+ đã bị thế bởi 1 phối tử NH3.
c) Dấu hiệu của phức chất [Cu(NH3)(H2O)5]2+ tạo thành là tạo thành kết tủa. xuất hiện màu xanh lam
d) Phức chất tạo thành có tổng 6 phối tử.
Câu 51: Khi cho dung dịch ammonia dư vào dung dịch chứa phức chất [Ni(OH2)6]2+ và anion Cl– thì có phản
ứng sau: [Ni(OH2)6]2+(aq) + 6NH3(aq) ⎯⎯
→ [Ni(NH3)6]2+(aq) + 6H2O(l) (*)
a) Trong điều kiện của phản ứng (*), phức chất [Ni(NH3)6]2+(aq) kém bền hơn phức chất [Ni(OH2)6]2+ (aq).
b) Phản ứng (*) là phản ứng thế phối tử.
c) Dung dịch sau phản ứng có pH > 7.
d) Trong phản ứng không có sự thay đổi số oxi hoá của các nguyên tố.
Câu 52: Muối iron(III) chloride có màu nâu – đen. Khi hoà tan trong nước thu được dung dịch có màu vàng và
môi trường acid. Màu sắc và môi trường được giải thích do sự tạo thành phức chất và sự thuỷ phân của
phức chất trong nước. Một trong những lí giải được đưa ra là: 10 | T Y H H FeCl3 + 6H2O(l)
[Fe(OH2)6]3+(aq) + 3Cl–(aq); (1) [Fe(H2O)6]3+(aq)
[Fe(OH2)5(OH)]2+(aq) + H+(aq); (2)
a) Các phức chất [Fe(OH2)6]3+ và [Fe(OH2)5(OH)]2+ đều là các phức bát diện.
b) Liên kết O–H trong phức chất [Fe(OH2)6]3+ phân cực hơn liên kết O–H trong phân tử H2O.
c) Trạng thái oxi hoá của Fe trong phức [Fe(OH2)6]3+ và [Fe(OH2)5(OH)]2+ là khác nhau.
d) Khi thêm dung dịch HCl vào, cân bằng (2) chuyển dịch về phía nghịch.
Câu 53: Cho các quá trình tạo phức chất bát diện sau:
Fe3+(aq) + 6H2O(l) ⎯⎯
→ [Fe(OH2)6]3+(aq) (I)
[Fe(OH2)6]3+(aq) + SCN–(aq)
[Fe(OH2)5(SCN)]2+(aq) + H2O(l) KC = 1,4.102 (II)
[Fe(OH2)6]3+(aq) + F–(l)
[Fe(OH2)5F]2+(aq) + H2O(l) KC = 2,0.105 (III)
Biết dung dịch [Fe(OH2)6]3+ màu vàng nâu, dung dịch [Fe(OH2)5(SCN)]2+ có màu đỏ, dung dịch
[Fe(OH2)5F]2+ và các anion SCN–, F– đều không có màu. Mỗi phát biểu sau đây đúng hay sai?
a. Quá trình (I) xảy ra khi hoà tan iron(III) chloride trong nước. Kết thúc quá trình này thu được dung
dịch có chứa lượng lớn cation Fe3+ và phức chất aqua [Fe(OH2)6]3+.
b. So với anion F–, anion SCN– dễ thay thế phối tử H2O trong [Fe(OH)6]3+ hơn.
c. Khi cho từ từ dung dịch KSCN vào dung dịch ở quá trình (III) thì dung dịch này sẽ có màu.
d. Trong các quá trình (I), (II) và (III), mỗi phân tử H2O hoặc anion SCN– hay anion F– đều sử dụng số
cặp electron hoá trị riêng như nhau để cho vào orbital trống của cation Fe3+.
Câu 54: Cho hai quá trình sau:
[Cu(OH2)6]2+(aq) + 2NH3(aq)
[Cu(NH3)2(OH2)4]2+ (aq) + 2H2O(l); o 7,7 H = 4 − 6 kJ, K =10 r 298 C (I)
[Cu(OH2)6]2+(aq) + en(aq)
[Cu(en)(OH2)4]2+(aq) + 2H2O(l) o 10,6 H = 5 − 4 kJ, K =10 r 298 C (II)
Trong đó, en là ethylenediamine. Phân tử này đã dùng tất cả các cặp electron hoá trị riêng để tạo liên
kết cho – nhận với cation Cu2+.
a) Quá trình (II) thuận lợi hơn quá trình (I) về năng lượng.
b) Sự thế H2O trong phức chất [Cu(OH2)6]2+ bởi NH3 tạo ra phức chất bền hơn so với sự thế H2O trong
phức chất [Cu(OH2)6]2+ bởi en.
dựa vào kc , kc lớn phức tạo ra bền hơn
c) Xung quanh nguyên tử trung tâm trong phức chất [Cu(NH3)2(OH2)4]2+ và trong phức chất [Cu(en) (OH
liên kết phối trí hay liên kết cho nhận
2)4]2+ đều có 6 liên kết σ.
d) Phản ứng diễn ra ở quá trình (I) và (II) đều có sự tạo thành phức chất không tan và có sự biến đổi màu sắc.
dựa vào trạng thái phức thấy phức tan
Câu 55: Cho sơ đồ chuyển hoá sau: 11 | T Y H H
Biết rằng X, Y, Z đều là các phức chất vuông phẳng, đơn nhân.
a. Các phản ứng trên đều có sự thay thế phối tử trong phức chất.
b. Trong phức chất Y, có hai phối tử NH3 và hai phối tử iodo(I). 3 I , 1 Nh3
tồn tại ở dạng phức , còn càu ngoại k+ liên kết với
c. Trong nước, dung dịch phức chất X dẫn điện tốt.
cầu nội nên tạo nên kết ion
d. Các phản ứng trong chuỗi trên đều kèm theo sự thay đổi số oxi hoá của nguyên tử trung tâm.
Tự học – TỰ LẬP – Tự do!
⭐️⭐️⭐️ (Thầy Phạm Thắng | TYHH) ⭐️⭐️⭐️ 12 | T Y H H


