


















Preview text:
BÀI GI NG HÓA LÝ 1 CH NG 1 NGUYÊN LÝ I NHI T NG H C 1. M T S KHÁI NI M C B N 1.1. H
H là m t ph n vĩ mô có gi i h n xác đ nh đang đ c kh o sát v ph ơng di n trao đ i năng l
ng và v t ch t. Ph n th gi i xung quanh h là môi tr ng ngoài đ i v i h . Có ba lo i h :
H h (h m ): Là h có th trao đ i c năng l ng l n v t ch t v i môi tr ng ngoài.
H kín (h đóng): Là h ch trao đ i v i môi tr ng ngoài năng l ng nh ng không trao đ i v t ch t.
H cô l p: Là h không trao đ i c năng l ng l n v t ch t v i môi tr ng ngoài. 1.2. Tr ng thái
Tr ng thái là m t t nói lên đ c đi m c a h đang đư c kh o sát. M t h có
tr ng thái xác đ nh khi nh ng bi n s xác đ nh nh ng đ i lư ng c a h đư c bi t
m t cách chính xác như nhi t đ , th tích, áp su t, kh i lư ng riêng... các đ i lư ng
này đư c g i là bi n s tr ng thái c a h . Tr ng thái c a h s thay đ i n u ít nh t có
m t trong nh ng bi n s tr ng thái thay đ i.
1.3. Bi n i quá trình
M t h nhi t đ ng h c bi n đ i (hay th c hi n m t quá trình) khi tr ng thái
c a h thay đ i. Tr ng thái c a h thay đ i n u ít nh t có m t bi n s tr ng thái c a h thay đ i. Bi n đ i đ
c xác đ nh n u bi t rõ tr ng thái đ u và tr ng thái cu i. Ð ng bi n đ i ch đ c xác đ nh khi bi t đ
c tr ng thái đ u, tr ng thái cu i và t t
c nh ng tr ng thái trung gian mà h đã tr i qua. Ng
i ta chia ra các lo i bi n đ i: Page 1 BÀI GI NG HÓA LÝ 1
Bi n đ i h (m ): Là bi n đ i đem h t tr ng thái đ u đ n tr ng thái cu i khác nhau.
Bi n đ i kín (đóng): Là bi n đ i đem h t tr ng thái đ u đ n tr ng thái cu i gi ng nhau. Tr
ng h p này, h đã th c hi n m t chu trình bi n đ i kín(chu trình)
Bi n đ i thu n ngh ch: Là bi n đ i mà các tr ng thái trung gian c a h tr i qua đ
c xem nh do các quá trình cân b ng. M t cách đơn gi n đ xác đ nh tính ch t
thu n ngh ch c a m t bi n đ i là kh o sát xem bi n đ i ng c l i có th x y ra đ c
hay không khi ch thay đ i r t ít đi u ki n th c nghi m. N u bi n đ i ng c x y ra đ
c thì đó là bi n đ i thu n ngh ch, n u bi n đ i ng c không x y ra đ c thì đó là
bi n đ i b t thu n ngh ch (hay bi n đ i t nhiên).
Bi n đ i đ ng tích: Là bi n đ i đ
c th c hi n trong đi u ki n th tích c a h không thay đ i.
Bi n đ i đ ng áp: Là bi n đ i đ
c th c hi n trong đi u ki n áp su t không đ i.
Bi n đ i đ ng nhi t: Là bi n đ i đ
c th c hi n trong đi u ki n nhi t đ không đ i.
Bi n đ i đo n nhi t: Là bi n đ i đ
c th c hi n trong đi u ki n không có s trao đ i nhi t l ng gi a h v i môi tr ng ngoài.
1.4. Hàm tr ng thái ! " 1.5. Nhi t và công # !$ % $ & ' " ( ! )$ * )$ +" + $ ( ! * , + - . . Page 2 BÀI GI NG HÓA LÝ 1 - . . 2.
NGUYÊN LÝ TH NH T C A NHI T Đ NG H C
2.1. Nguyên lý th nh t nhi t đ ng h c và n i năng U , /0 1 % )$ ! ' 2 ! " 3 + 4 *
a. Qúa trình đ ng tích: V= h ng s , dV=0.
Do qúa trình là đ ng tích nên công t
h tích không th c hi n đư c. Do đó: QV = ΔU.
V y: Nhi t mà h nh n đư c trong quá trình đ ng tích b ng v i bi n thiên n i năng c a h .
b. Qúa trình đ ng áp: p = h ng s , dp=0.
Công th c hi n trong trư ng h p này là: Ap = p.(V2-V1).
Do đó nhi t c a quá trình: Qp = ΔH.
V y: Nhi t h nh n đư c trong quá trình đ ng áp b ng bi n thiên enthalpy c a h .
c. Qúa trình đ ng áp c a khí lý t ng: p = h ng s , dp=0.
Theo phương trình tr ng thái c a khí lý tư ng v i n mol khí như sau: pV=nRT.
Trong đó R là h ng s khí lý tư ng. Do đó công d n n đ ng áp có th tính theo phương trình sau: Ap = nRΔT. Page 3 BÀI GI NG HÓA LÝ 1 ΔUp = Qp – nRΔT.
d. Qúa trình dãn n đ ng nhi t c a khí lý t ng
Áp d ng tính ch t c a đ nh lu t Joule: n i năng c a khí lý tư ng ch ph thu c vào
nhi t đ , t đó có th suy ra: Bi n thiên n i năng đ ng nhi t c a quá trình là b ng không ΔUT = 0.
V y: QT = AT = nRTlnp2/p1=nRT.lnv2/v1. 3. Đ NH LU T HESS
3.1. N i dung đ nh lu t
Trong quá trình đ ng áp hay đ ng tích, nhi t ph n ng ch ph thu c vào tr ng thái
đ u và tr ng thái cu i mà không ph thu c vào tr ng thái trung gian c a quá trình. QV = ΔU và Qp = ΔH
Đ i v i các quá trình c a khí lý tư ng: ΔH=ΔU + RTΔn. 3.2. !
p d ng đ nh lu t Hess có th xác đ nh hi u ng nhi t c a các quá trình thông qua
hi u ng nhi t c a ác quá trình khác có liên quan ho c thông qua nhi t sinh, nhi t
cháy…c a các ch t trong quá trình.
- Nhi t ph n ng ngh ch b ng nhưng trái d u v i nhi t c a ph n ng thu n: ΔHngh ch = - ΔHthu n.
- Nhi t ph n ng t ng b ng nhi t sinh c a các ch t t o thành tr đi nhi t sinh c a các ch t tham gia quá trình: ΔH ph n ng =
- Nhi t ph n ng b ng t ng nhi t cháy c a các ch t tham gia quá trình tr đi t ng nhi t
cháy c a các ch t t o thành: ΔH ph n ng = Page 4 BÀI GI NG HÓA LÝ 1 4. NHI T DUNG 4.1. " nghóa # #
Nhi t dung riêng c a m t ch t b t kỳ là m t đ i lư ng v t lý có giá tr b ng nhi t
lư ng c n cung c p cho m t đơn v kh i lư ng ch t đó đ làm tăng nhi t đ thêm 1o.
Nhi t dung riêng phân t c a m t ch t b t kỳ là m t đ i lư ng v t lý có giá tr b ng
nhi t lư ng c n cung c p cho m t kmol ch t y đ làm tăng nhi u đ lên 1 đ .
Ký hi u nhi t dung riêng là c, Cal/g.K
Nhi t dung riêng phân t là C, Cal/mol.K
Ð i v i ch t khí ta c n phân bi t xem ta làm nóng ch t khí trong đi u ki n nào: đ ng
tích hay đ ng áp. Do đó ta có nhi t dung riêng đ ng tích và nhi t dung riêng đ ng áp. , 5 6/ (6 , 5 7 / ( (6 8 ( 3 9 5. : ; < ==/ Page 5 BÀI GI NG HÓA LÝ 1 CH NG II ! I. M T S KHÁI NI M C B N: >" + % ? $ ) ! ? $ " @" 0 ! 2 " A" + % ; ; "
II. NGUYÊN LÝ TH HAI C A NHI T Đ NG H C: 1 ENTROPY 1.1 # nh nghĩa entropy < ? 1 % ; B 5 % $ +C0 1 % ) ! B D 6 & ) ! 6 " , 7 B $ E 6$ )$ F" 3 +0,C0 G( C "< $ HC "1.2 C 7 6$" 0 J ĩ B % 6$ 7 / a, E 6$ J ư J ư 7 ! B ươ ư ă 6$ 7 " b, E 6$ ? K F 3 =GKI c, F ' 6$ ! ) 1 % ? B & ) ' " 1.3 L E 6$ ? & ! 6" 0 ! 6B 1 % ? $ $ + 3 .B $/ Page 6 BÀI GI NG HÓA LÝ 1 , F . 1 % ? $ , @F . $ F 3 . 1 % ! 2 " >"M" : ! E 6$ 1 % ; " 4 + % 5 6 5 7 / G 63 B N 3 I + % 5 / G03 I ( 1 % $ 6 / G 1 % ; 5 5 6I >"O" 0 ! & P ) & E 6$ $ " @QR 3 III. HÀM Đ C TR NG.
1. Đ nh nghĩa hàm đ c trưng.
Hàm đ c trưng là m t hàm tr ng thái mà thông qua đó các đ o hàm các c p c a nó
có th xác đ nh m"i thông s vĩ mô c a h . 2. Hàm entropy.
Mô t toán h"c như sau: dS = Qtn/T 3. Hàm n i năng U. Hàm Anthalpy H.
Còn g"i là hàm nhi t, mô t toán h"c như sau: H = U + PV. V i th nguyên là cal hay J.
4. Th nhi t đ ng đ ng nhi t, đ ng áp.
Còn g"i là hàm năng lư ng Gibbs, đư c mô t như sau: Page 7 BÀI GI NG HÓA LÝ 1
G = H – TS. V i th nguyên là cal ho c J.
5. Th đ ng nhi t, đ ng tích.
Còn g"i là th đ ng tích hay là hàm năng lư ng Helmholtz, đươck mô t b i bi u th c:
F = U – TS. V i th nguyên là cal ho c J.
* T m!i hàm đ c trưng và vi phân riêng ph n c a hàm theo các bi n s tương ng có th
xác đ nh đư c nh ng thu c tính nhi t đ ng c a h . IV. " # $% & ' ( ) & % * + ,
Các phương trình nhi t đ ng cơ b n là các mô t toán h"c c a n i dung nguyên lý 1
và nguyên lý 2 c a nhi t đ ng l c h"c.
1. K t h p hai nguyên lý 1 và 2. dU 0 F S P N S *T
2. T đ nh nghĩa c a hàm H.
H = U + PV, l y vi phân và thay hàm dU vào ta có: dH 0 F 8 N P 4 *T
3. T hàm th đ ng nhi t, đ ng áp.
G = H – TS, l y vi phân và thay hàm dH vào ta có: dG F 08 N P 4 *T
4. T hàm th đ ng nhi t, đ ng tích.
F = U – TS, l y vi phân và thay hàm dU vào ta có: U F 0 S P N 4 *T
* Các h th c trên là nh ng h th c nhi t đ ng cơ b n r t quan tr"ng trong nhi t đ ng
h"c, đư c dùng đ xét chi u và gi i h n c a quá trình trong các đi u ki n tương ng.
Trong các h th c trên thì d u b t đ ng th c tương ng v i quá trình b t thu n ngh ch, Page 8 BÀI GI NG HÓA LÝ 1
còn d u đ ng th c tương ng v i quá trình thu n ngh ch và l c này công A s# đ t giá tr c c đ i Amax.
V. DÙNG HÀM Đ C TR NG Đ XÉT CHI U CHO QUÁ TRÌNH.
Tiêu chu$n xét chi u trong h đ ng nhi t, đ ng áp.
Xu t phát t hàm nhi t đ ng cơ b n dG F 08 N P 4 *T
Trong đi u ki n đ ng nhi t, đ ng áp: dT = 0 và dP = 0 thay vào ta có: dG 4 *T
. Do công có ích là dương nên dG .
* N u quá trình x y ra trong h thu n ngh ch thì công c c đ i b ng đ gi m th đ ng áp G = - Amax
* N u quá trình x y ra trong h là b t thu n ngh ch thì th đ ng áp c a h gi m dG ."Và
khi quá trình đ t cân b ng thì th đ ng áp c a h s# đ t c c ti u Gmin nên dG = 0.
1. Tiêu chu$n xét chi u trong h đ ng nhi t, đ ng tích.
Xu t phát t hàm nhi t đ ng cơ b n: U F 0 S P N 4 *T"
Trong đi u ki n đ ng nhi t, đ ng tích: dT = 0 và dV = 0 thay vào ta có: U 4 *T
. Do công có ích là dương nên U .
* N u quá trình x y ra trong h thu n ngh ch thì công c c đ i b ng đ gi m th đ ng tích.
* N u quá trình x y ra trong h là b t thu n ngh ch thì th đ ng áp c a h gi m U
Và khi quá trình đ t cân b ng thì th đ ng áp c a h s# đ t c c ti u Fmin nên dF = 0. VI. TÍNH TH Đ NG ÁP.
Các th nhi t đ ng lag hàm s ph thu c vào nhi t đ nên n u bi t đư c các hàm này
ta có th ch đ ng thay đ i nhi t đ và ch"n các đi u ki n thích h p cho quá trình x y ra theo chi u mong mu n.
1. Phương trình Gibbs-Helmholtz. Page 9 BÀI GI NG HÓA LÝ 1
Ta có: dG = - SdT + VdP và ∆G = ∆H - T∆S. Thay vào thu đư c phương trình d ng tích phân như sau: G ∆ G ∆ T T 1 1 2 1 = − H ∆ .( − ). T T T T 2 1 2 1
% đây xét trong m t kho ng nhi t đ tương đ i h&p nên ∆H xem như là không thay đ i.
Hoàn toàn tương t như trên, áp d ng cho hàm F ta có k t qu : F ∆ F ∆ T T 1 1 2 1 = − U ∆ .( − ). T T T T 2 1 2 1
2. Phương trình Chomkin-Svartsman.
N u l y tích phân c a hàm Gibbs-Helmholtz theo c n nhi t đ t 298 đ n T, ta có: G G T T dT T 298 = - H + C dT , n u áp T 298 298 p 2 298 298 T d ng i ∆C = a ∆ T p i
, thu đư c phương trình sau: G ∆ = H T ∆ 298 −T S ∆ 298 −TΣ a ∆ M
i i , trong đó Mi ch ph thu c vào nhi t đ T và ch
s i nên luôn đư c tính s'n trong các b ng tra hoá lý. Như v y n u dùng phương trình
này đ tính toán s# nhanh hơn và có đ chính xác tương đ i.
3. Th đ ng áp rút g"n.
Đ tính toán bi n thiên th đ ng áp c a quá trình, trong m t s trư ng h p ngư i ta
còn s d ng hàm s th đ ng áp rút g"n, nó đư c đ nh nghĩa như sau: 0 0 G − H 0 0 T 0 G − H g 298 = − ho c T g = −
, trong đó g là m t hàm ít ph thu c vào nhi t T 298 T
đ nên thư ng tính s'n và có trong các b ng tra hoá lý. Bi u th c trên còn đư c chuy n v d ng d( s d ng hơn như sau: Page 10 BÀI GI NG HÓA LÝ 1 0 0 0 0 G − H T 298 G ∆ = H ∆ 298 −T T ∆ −
. Dùng s tay hoá lý có th tra ra các giá tr T 0 H
∆ 298 và giá tr hàm s g ho c g298 c a các ch t nh ng nhi t đ khác nhau, t đó tính đư c 0 G ∆ . T VII. Đ I L
NG MOL RIÊNG PH N VÀ TH HOÁ H C.
Trong các ph n trên, chúng ta đã xét nh ng h có kh i lư ng và thành ph n không
đ i, trong đó đã đưa ra các h th c mô t toán h"c nh hư ng c a nhi t đ , áp su t đ n các đ i l
ng khác c a h nh : V, S, U, H, G…Nh ng n u xét h m t cach st ng quát các
h có thành ph n thay đ i thì các đ i l
ng dung đ trên (ký hi u là X) c a h là hàm s
c a nhi t đ , áp su t và s mol ni c a các c u t có m t trong h .
X = X (T , P,n , n ...) 1 2 . nh h
ng c a s thay đ i s mol ch t đ n các hàm đ c tr ng s th hi n công có
ích dA trong các ph ơng trình nhi t đ ng cơ b n. M i lo i công đ u có th bi u di n d i d ng m t đ i l ng c
ng đ (ký hi u là I) và m t đ i l ng dung đ (ký hi u là
dY), v y công dA có th bi u di n: dA= I.dY 1. i l ng mol riêng ph n.
Xét h g m nhi u c u t có s mol t ơng ng là n1, n2, n3…thì m t i l ng
dung b t k X u có th bi u di n d i d ng hàm s nh sau:
X = X (T , P,n , n ...) 1 2 .
L y vi phân toàn ph n c a X ta có: X ∂ X ∂ X dX dT dP ∂ = + +
dn . Ta ký hi u X mol riêng ph n ∂ p,n ∂ T , i T T n n
∂ i p,T,nj
c a c u t I là X và đ
c đ nh nghĩa b!ng bi u th c: i Page 11 BÀI GI NG HÓA LÝ 1 X ∂ X = . i n
∂ i T,p,nj V y đ i l
ng mol riêng ph n là s đo nh h
ng c a s thay đ i s mol c a m t c u t
đ n dung đ chung c a h . N u thay đ i l
ng mol riêng ph n vào ph ơng trình vi
phân toàn ph n c a X, ta có: X ∂ X dX dT ∂ = +
dP + X dn . Nh v y ta còn th y đ i l ng mol riêng T ∂ , T p n ∂ T , i i n ph n còn là m t đ i l ng c ng đ . 2. Tính ch t c a i l ng mol riêng ph n. a. Tính ch t 1.
Nh"ng ph ơng trình vi t cho th #ng áp mol u có th vi t t ơng t cho hoá th . V i 1 mol khí lý t
ng, ta có ph ơng trình: P 0
G = G + RT ln P nên t ơng t ta có: 0
µ = µ (T ) + RT ln P . Áp su t P µ T i i i
i c a c u t i trong h$n h p khí lý t ng, 0( ) i
c g i là th hoá chu%n c a c u t i, nó b!ng th hoá c a c u t i khi Pi= 1 atm và là m t i l
ng ph& thu c vào nhi t . b. Tính ch t 2.
Trong i u ki n #ng nhi t, #ng áp, th #ng áp c a h b!ngth hoá c a các câú t t o thành h . G = ni i µ G
V i h 1 c u t thì: G = nµ hay µ =
, ngh'a là hoá th c a c u t trùng v i n
th #ng áp mol c a h 1 c u t . Nh v y tiêu chu%n xét chi u có th c vi t:
Trong h #ng nhi t, #ng áp Page 12 BÀI GI NG HÓA LÝ 1
Ph n ng theo chi u thu n N u (n µ ) dau > (m i i
jµ j )cuoi Ph n ng theo chi u ngh N u (n ch µ ) dau < (m i i
jµ j )cuoi Ph n ng t cân b N u (n !ng µ ) dau = (m i i
jµ j )cuoi
Bi u th c này càng làm rõ hơn ý ngh'a c a hoá th , ngh'a là: ch t s chuy n
t( tr ng thái có t ng th hoá cao sang tr ng thái có t ng hoá th th p hơn. Page 13 BÀI GI NG HÓA LÝ 1 -. / 0 ! , 1 & 2 3 4 * 1 & • - 5 B 5 6B 1 % ? $ V • < ! 2 G V 3 V IB 6 & 6 ! 2 ! 2 < @ (W 8 W@ 3 @ (W@ P@(W@ P2 P2 < CO CO P 3 2 <( 3 2 P2 P P2 P CO O2 cb CO O2 cb P / * 8 : 3 ( 8 L V0 3 "XL 8 ("X( 4 "X* 4 "X: Y ) X 3 X G0I 8 90 P ! / V0 3 V 0 8 90 )6 G6 % 5 N T - ==I V 0 3 "XL 8 ("X( 4 "X* 4 "X: d c P P ) D C P 3 a b P P A B cb < 6 ! 2 / V0 3 . V 0 3 490 )6 d c < P P D C P 3 G)P I 3 a b P P A B cb P % N T - ==/ Page 14 BÀI GI NG HÓA LÝ 1 V 0 3 490 <6 V0 3 490 <6 8 90 P P % N T - ==/ V0 3 90 P C
Z & 6 / V0 [ . P ; ? $ V0 \ . P ? $ V0 3 . P ! 2 ( 2 ! 2 ∆n P
ni cb (/ , & C ?/ 6 & ? 3 nini 3 8 4 4 P/ 6
<( / 6 <? / 6 6 < / 6 !B 6 B ) 7 ! 2 " , / 3 .
Page 15 BÀI GI NG HÓA LÝ 1 0$ 6 & 6 & & 6 P / -F(: ) 6 6 , / 0 5 6 7 • - ; $ X 3 X G0I 8 90 ? V0 3 V 0 8 90 ? V 0 3 490 <? < 3 < ∆ ? ( n ) n 3 <( N4 i cb ? 3 n n i B ( 3 i n V i 3 .
• - ) 7 $ X 3 X G0BPI 8 90 ? V0 3 V 0BP 8 90 V 0B6 3 490 <? , / 0 5 89 7 P ) 7 / X 3 X 8 90 P P ] X 3 X 8 90 ? , 6 6 ] ) ! ; % ) ! -F(: G 6 & 6 2 >I :, ; ; -. ; < / >" , / P % 5 N T - == V 0 3 490 <6 Page 16 BÀI GI NG HÓA LÝ 1 0 6 7 -B
Page 17 BÀI GI NG HÓA LÝ 1 CHÖÔNG IV
LÝ THUY T C B N C A QUÁ TRÌNH CÂN B NG PHA I. M T S KHÁI NI M C B N.
Trong nghiên c u v pha c n th ng nh t m t s khái ni m dùng trong vi c kh o sát cân b!ng pha nh sau: 1. Pha. f 2.H p ph n: r 2. S c u t . Ký hi u là k. V y k ≤ r .
Có th áp d&ng quy t*c sau: k= r – q.
Trong đó q là s các ph ơng trình quan h v n ng đ c a các c u t t i đi m cân b!ng. 3. Đ t do. Ký hi u là c.
H có c = 0 g i là h vô bi n.
H có c = 1 g i là h nh t bi n.
H có c = 2 g i là h nh bi n. II. ĐI U KI N CÂN B NG PHA.
1. Đi u ki n v nhi t đ .
+ cân b!ng, nhi t đ c a t t c các pha ph i b!ng nhau. T
2. Đi u ki n v cơ h c. Page 18 BÀI GI NG HÓA LÝ 1
Áp su t tác đ ng lên t t c các pha ph i b!ng nhau. P 3 P
3. Đi u ki n v hoá h c.
T i đi m cân b!ng, hoá th c a các c u t ph i b!ng nhau. III. QUI T C PHA GIBBS.
V i n thông s bên ngoài tác đ ng và h , thì: c = k –f + n.
N u c T và P là h!ng s thì c = k - f
Còn n u T là h!ng s ho c P là h!ng s thì c = k – f + 1.
Qui t*c pha Gibbs là m t trong nh"ng đ nh lu t t ng quát nh t áp d&ng cho m i cân
b!ng pha, nó cho phép đ nh tính m i quan h c a nh"ng thông s nhi t đ ng trong các
quan h cân b!ng d th và t( đó tìn ra các m i quan h đ nh l ng gi"a các thông s này.
IV. GI N Đ PHA VÀ CÁC QUI T C PHA.
Gi n đ pha còn g i là bi u đ tr ng thái là đ th mô t s ph& thu c gi"a các thông
s tr ng thái c a h n!m trong cân b!ng pha. V nguyên t*c mu n mô t đ y đ h thì
ph i dùng đ th có ( c+1) tr&c to đ . Trong th c t ng i ta s c đ nh m t thông s
ho c b, qua các thông s ít nh h
ng đ có th s d&ng đ th 2 chi u ho c 3 chi u.
M t gi n đ pha bao g m các đ
ng, các m t và các vùng. Các đ ng dùng mô t
s ph& thu c gi"a hai thông s , các m t trong không gian ba chi u mô t s ph& thu c
c a ba thông s nhi t đ ng và các vùng trên gi n đ pha mô t nh"ng h có s l ng và
d ng các pha xác đ nh n!m cân b!ng v i nhau.
Gi n đ pha là công c& đ*c l c đ nghiên c u đ nh tính cũng nh đ nh l ng các quá
trình chuy n pha, t( đó tính toán các thi t b trong dây chuy n c ng ngh hoá h c.
1. Cách bi u di n các thông s nhi t đ ng trên gi n đ pha. Page 19 BÀI GI NG HÓA LÝ 1
a. Đ i v i các thông s nhi t đ , th tích hay áp su t.
Đ i v i các thông s này ta dùng ph ơng pháp bi u di n thông th ng trên tr&c s . Trong m t s tr
ng h p, khi giá tr c a thông s thay đ i trong m t kho ng khá r ng thì có th bi u di n chúng d
i d ng ngh ch đ o hay logarit c a nó.
b. Bi u di n thành ph n c a h 2 c u t .
Thành ph n c a các c u t trên gi n đ pha th
ng dùng là ph n mol xi hay ph n trăm kh i l
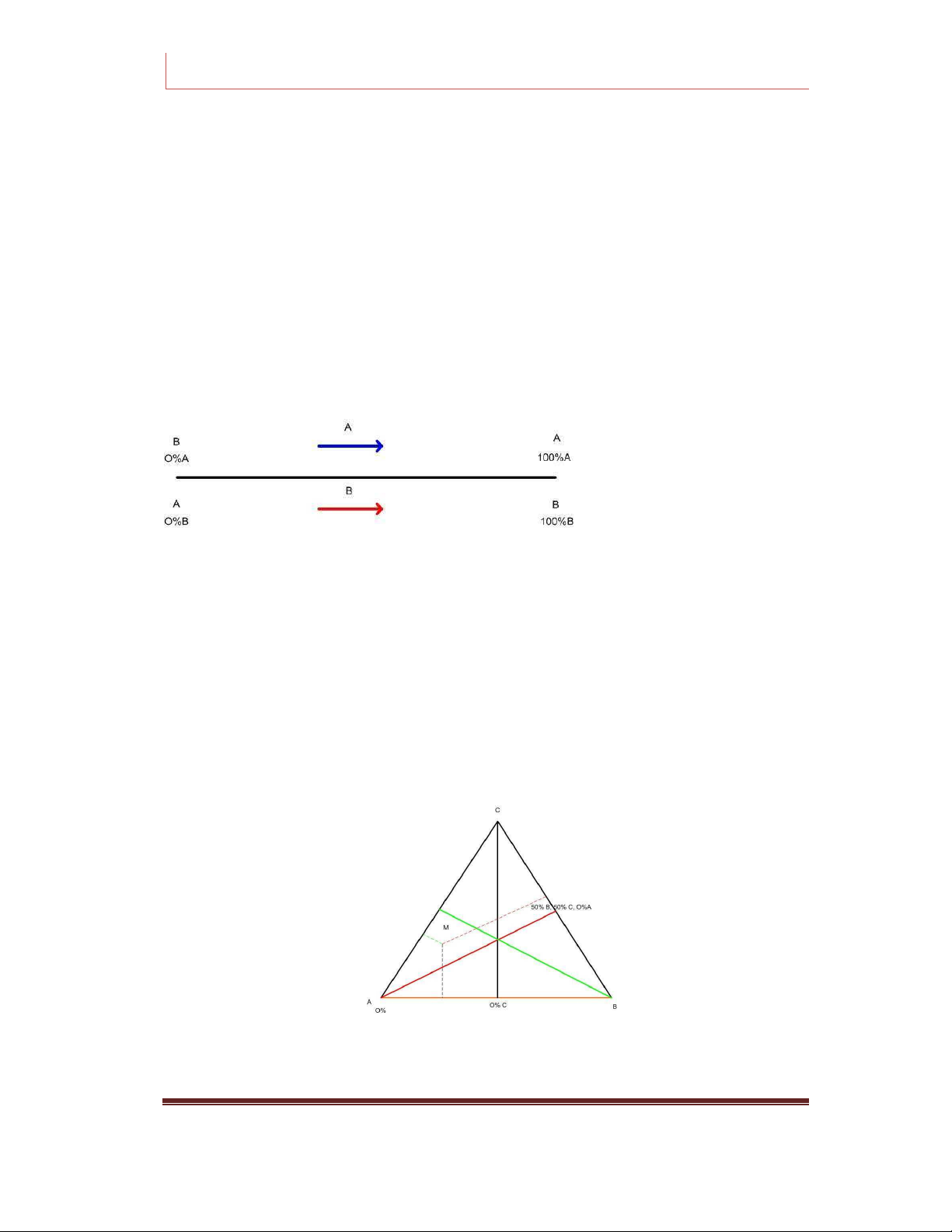
ng yi. Trong h hai c u t , dùng m t đo n th#ng đ c chia thành 100% nh sau:
Trên tr&c to đ ch- c n bi u di n cho m t c u t vì thành ph n c a c u t còn l i đ
c xác đ nh theo công th c: xA + xB = 1 hay y1 + y2 = 100%..
Khi đi m bi u di n c a h càng g n c u t nào thì hàm l ng c a c u t đó càng l n.
c. Bi u di n thành ph n c a h 3 c u t . Thành ph n c a h 3 c u t th ng đ
c bi u di n b!ng m t tam giác đ u nh sau:
V i cách bi u di n nh trên, ta có: Page 20



