






Preview text:
Trường Đại học Y Khoa Phạm Ngọc Thạch
Bộ môn Hóa – Sinh Hóa Đại Cương.
GVGD: ThS. Dương Thị Kim Yến. Mail: yendtk@pnt.edu.vn
MỤC TIÊU BÀI GIẢNG
Xác định được cấu tạo và danh pháp của ankane, ankene, alkyne, 1 arene.
2 Nêu được các tính chất vật lý của các hợp chất.
3 Liệt kê được các phản ứng đặc trưng của alkane, alkene, alkyne và aren
4 Trình bày được các phương pháp điều chế của các hydrocarbon. NỘI DUNG
ĐẶC ĐIỂM CHUNG CỦA HÓA HỮU CƠ. ALKANE. ALKENE ALKYNE ARENE
ĐẶC ĐIỂM CHUNG CỦA HOÁ HỮU CƠ
▪Thành phần chính gồm C và H, ngoài ra còn có O, N, S, P và nhóm halogen.
▪Liên kết trong hợp chất hữu cơ thường là liên kết công hóa trị, rất ít có liên kết ion.
▪Tính chất vật lý: các hợp chất dễ nóng chảy, dễ bay hơi; không hoặc ít tan trong nước,
nhưng tan nhiều trong dung môi hữu cơ.
▪Tính chất hóa học: phản ứng của các hợp chất hữu cơ xảy ra chậm, không hoàn toàn,
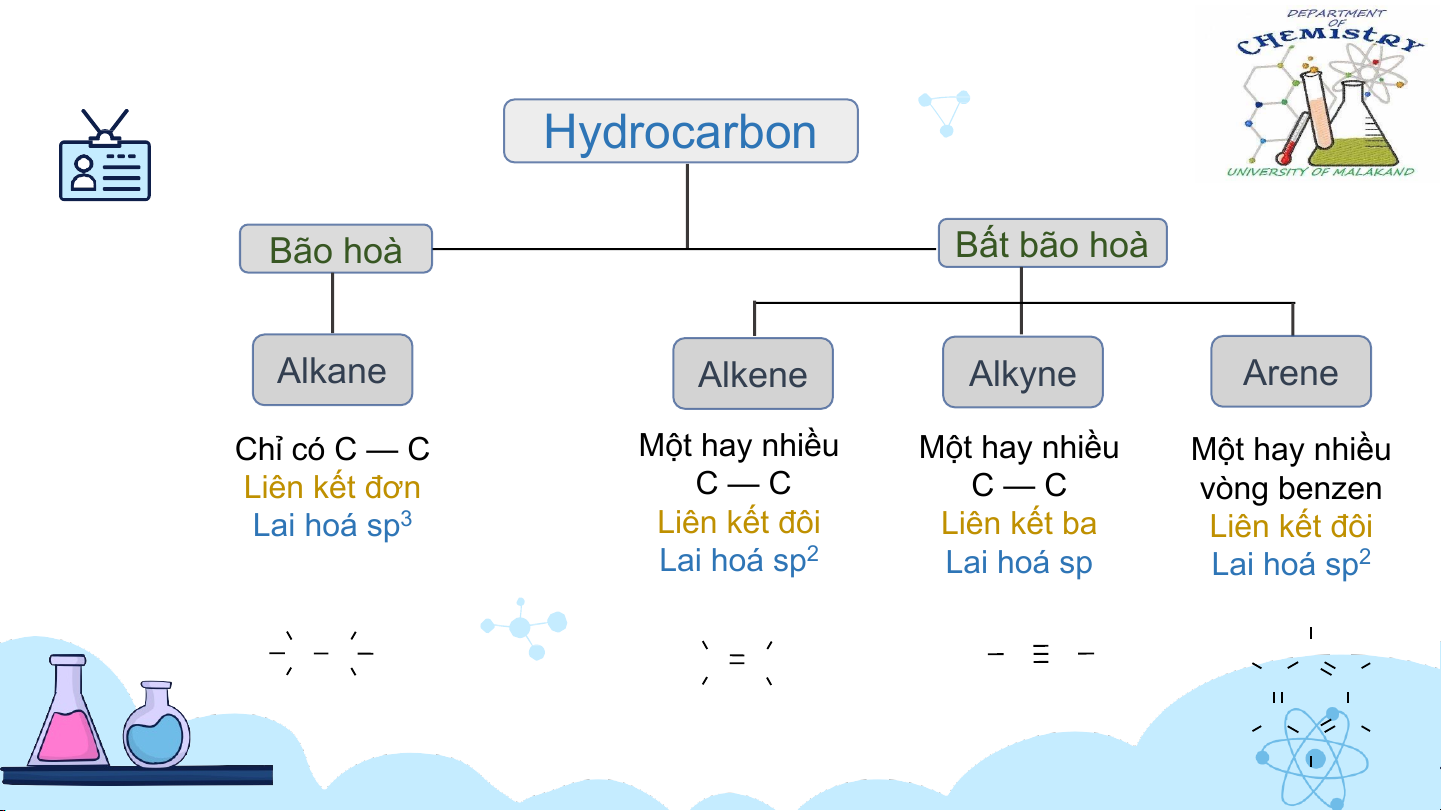
và không theo một hướng nhất định nên sinh ra nhiều sản phẩm phụ. PHÂN LOẠI Hydrocarbon Bão hoà Bất bão hoà Alkane Alkene Alkyne Arene Chỉ có C — C Một hay nhiều Một hay nhiều Một hay nhiều Liên kết đơn C — C C — C vòng benzen Lai hoá sp3 Liên kết đôi Liên kết ba Liên kết đôi Lai hoá sp2 Lai hoá sp Lai hoá sp2 H H H H H H C C H C C H C C H H C H H C C H H H C C H C H H 01 Alkane 1.1 Cấu tạo
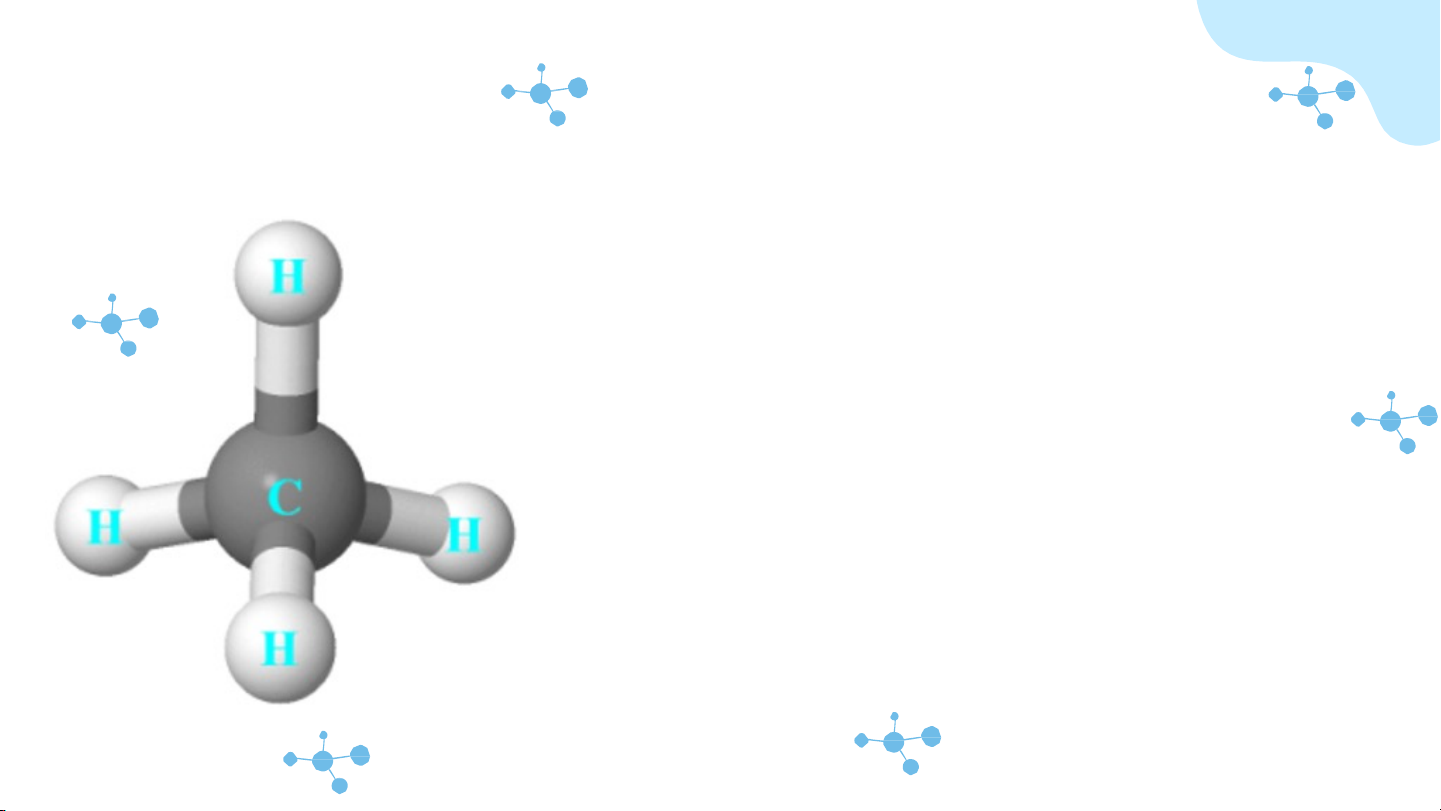
- Alkane là các hợp chất chỉ chứa 2 nguyên tố C và H.
- Công thức tổng quát C2nH(2n+1), n≥ 1
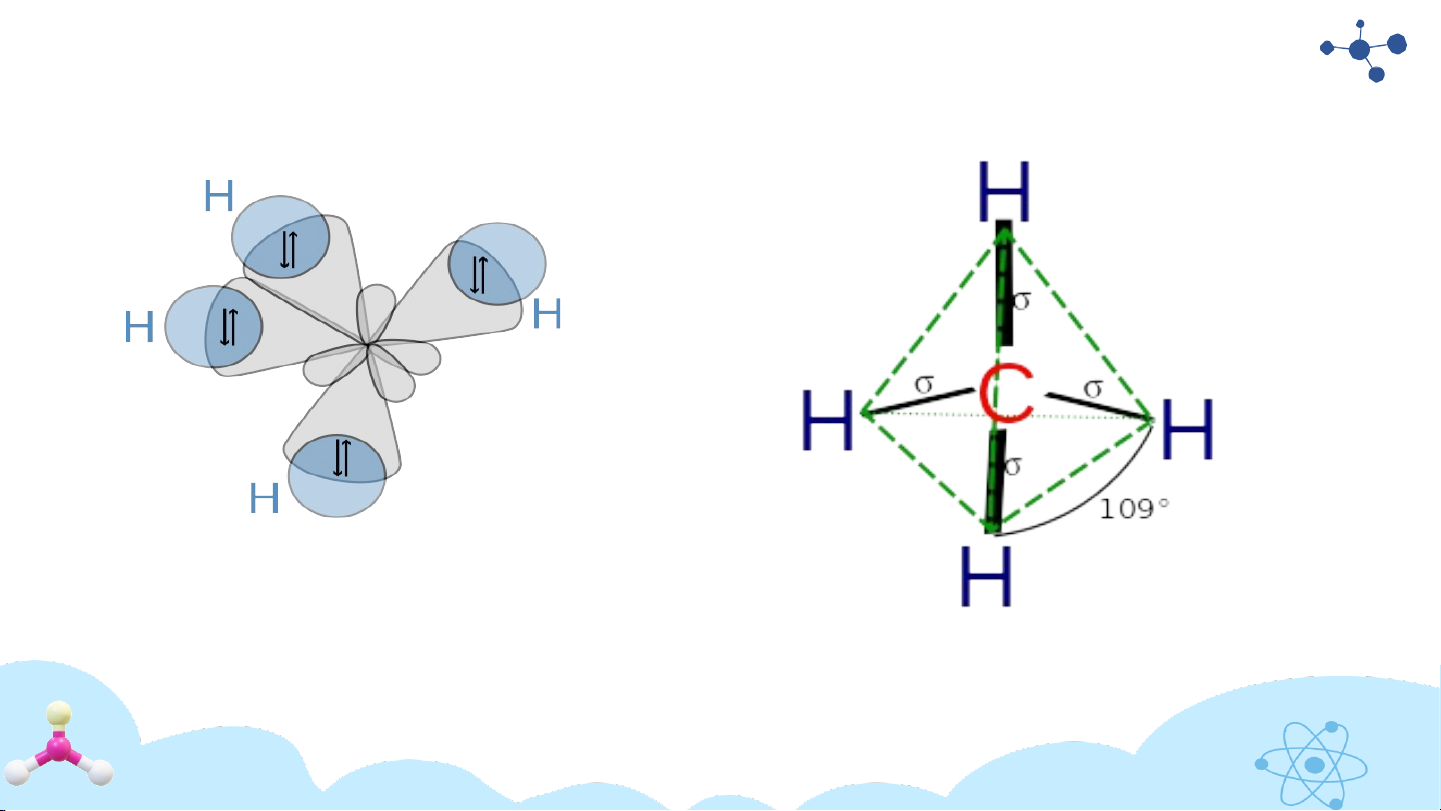
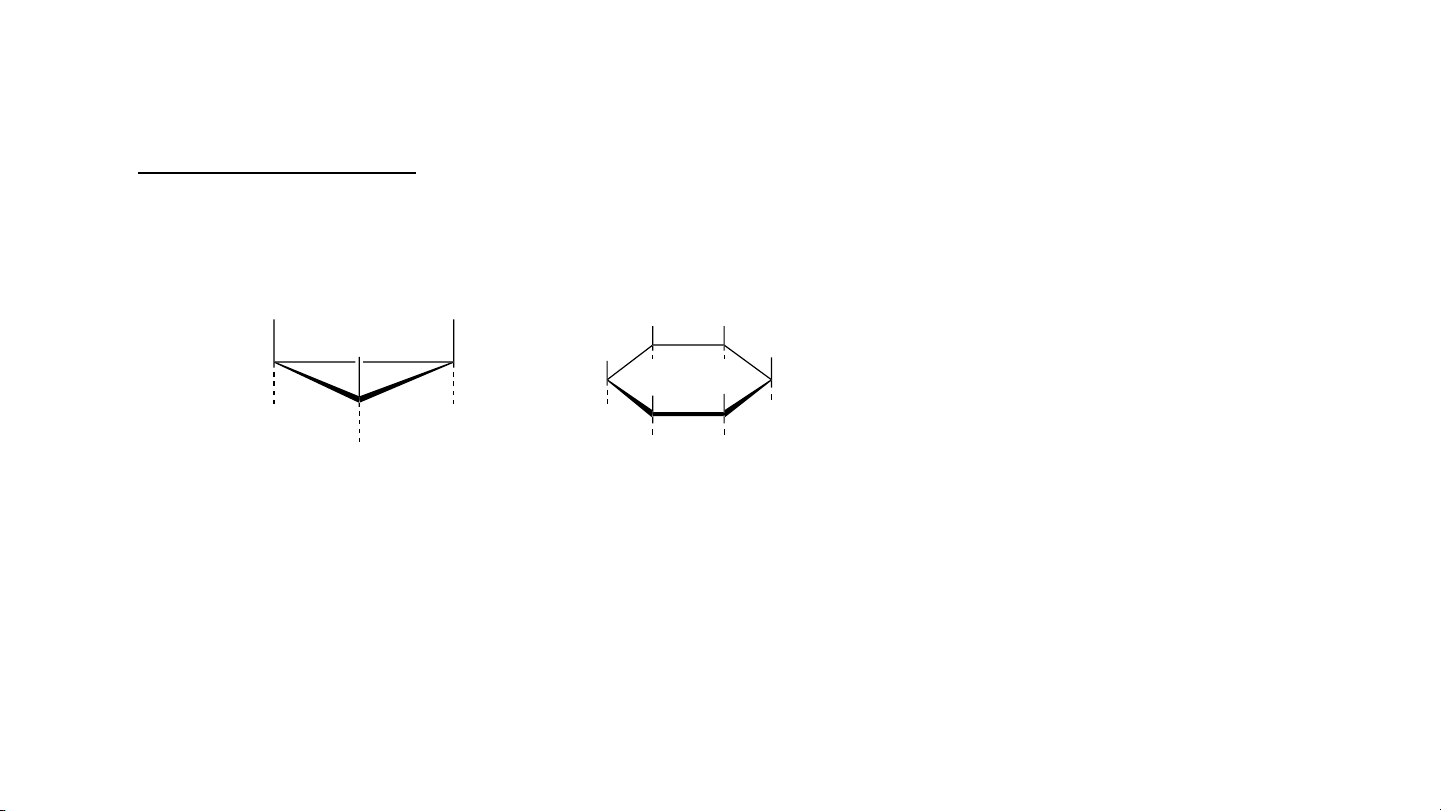
- Trong công thức phân tử chỉ có liên kết đơn giữa C - C - Trạng thái lai hoá sp3
• Các nguyên tử C trong alkan đều có lai hóa sp3 . Trạng thái lai hóa sp3 1.2 Danh pháp
Một số alkane cơ bản thường gặp. CH4 : Methane C11H24 : Udecane C21H44 : Henicosane C2H6 : Etane C12H26 : Dodecane C22H46 : Docosane C40H82 : Tetracontane C3H8 : Propane C13H28 : Tridecane C23H48 : Tricosane C50H102 : Pentacontane C4H10 : Butane C14H30 : Tetradecane C24H50 : Tetracosane C60H122 : Hexacontane C5H12 : Pentane C15H32 : Pendecane C25H52 : Pentacosane C70H142 : Heptacontane C6H14 : Hexane C16H34 : Hexdecane C26H54 : Hexacosane C80H162 : Octacontane C7H16 : Heptane C17H36 : Hepdecane C27H56 : Heptacosane C90H182 : Nonacontane C8H18 : Octane C18H38 : Octadecane C28H58 : Octacosane C100H202 : Hectane C9H20 : Nonane C19H40 : Nonadecane C29H60 : Nonacosane C200H402 : Dictane C10H22 : Decane C20H42 : Icosane C30H62 : Triacontane Cách gọi tên. ●
Alkane được chia làm 2 loại: công thức ở dạng mạch thẳng và mạch nhánh được gọi
tên theo danh pháp IUPAC (International Union of Pure and Applied Chemistry).
• Thêm tiếp đầu ngữ – n trước tên hydrocarbon tương ứng. v Mạch thẳng CH3CH2CH2CH3 : : n-butane
CH3CH2CH2CH2CH2CH2CH3: : n-heptane
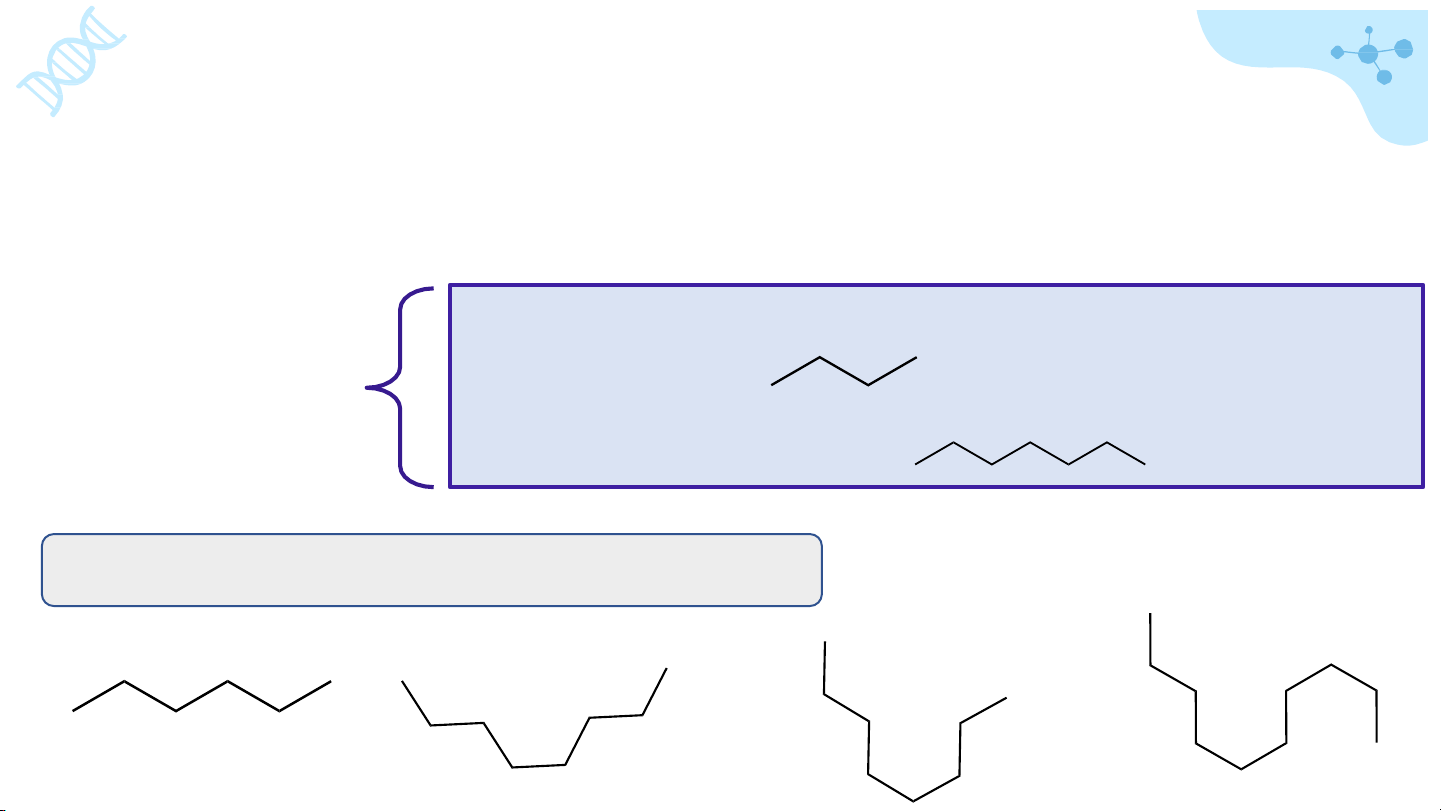
Hãy gọi tên các hợp chất alkane sau: 1 2 3 4
• Chọn mạch chính là mạch chứa nhiều C nhất.
• Đánh số ở mạch chính sao cho mạch C chứa nhóm thế có tổng
số định vị nhỏ nhất.
• Giữa các chữ số cách nhau bằng dấu phẩy (,); giữa chữ số và v Mạch nhánh
chữ viết cách nhau một dấu gạch ngang (-). Tên các mạch nhánh
được đặt theo thứ tự chữ cái.
• Nếu có nhiều nhánh giống nhau, sử dụng tiếp đầu ngữ: di-, tri-, tetra-……..
• Khi có nhiều nhánh, nhánh có chỉ số nhỏ được chọn theo mẫu tự
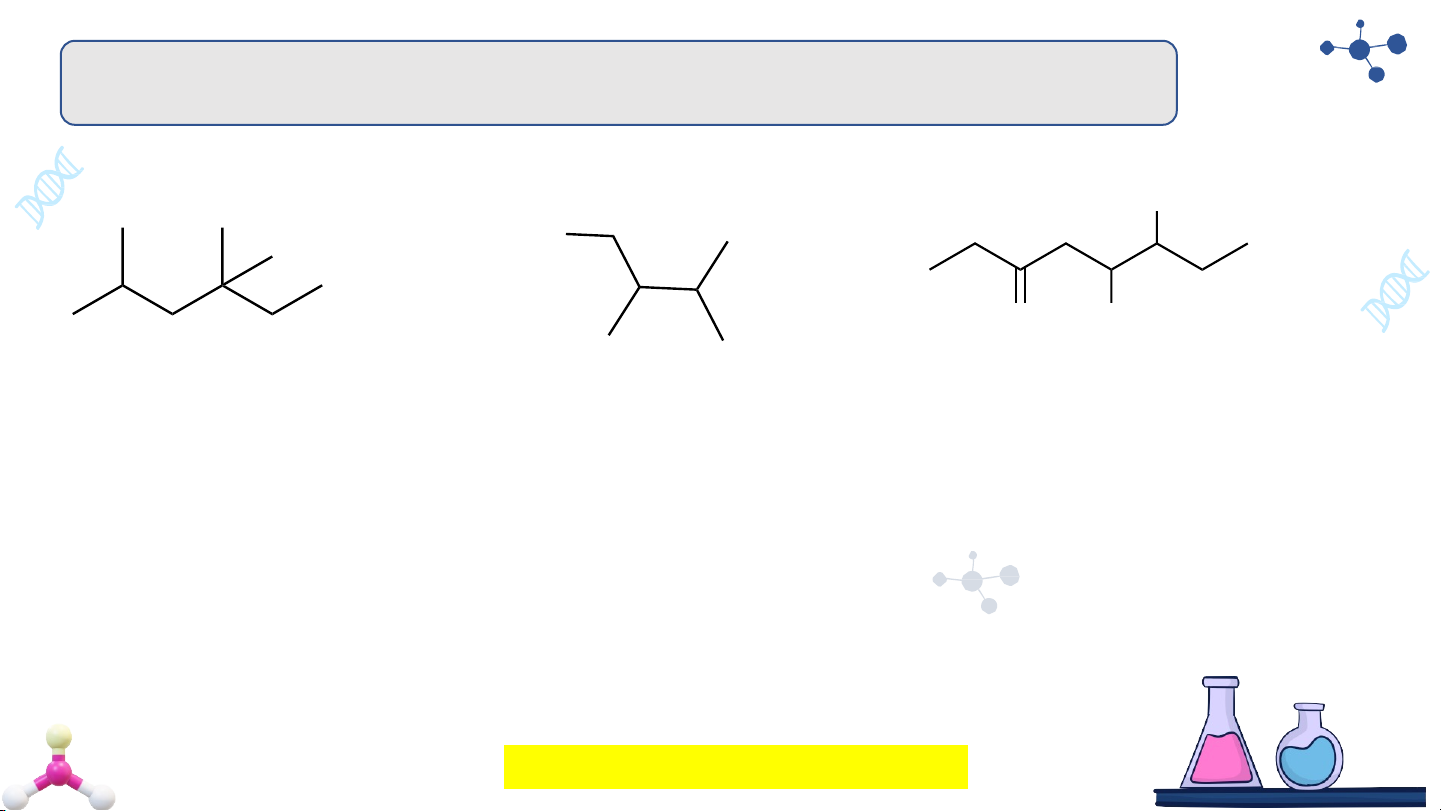
v Gọi tên các hợp chất hữu cơ sau theo danh pháp IUPAC. OH Br O CH3 1. 2. 3.
1. 2,4,4-trimethylhexane
2. 1-bromo-2,3-dimethylbutane
3. 3-hydroxy-4-methyl-6-oxooctane 6-hydroxy-5-methyloctan-3-one
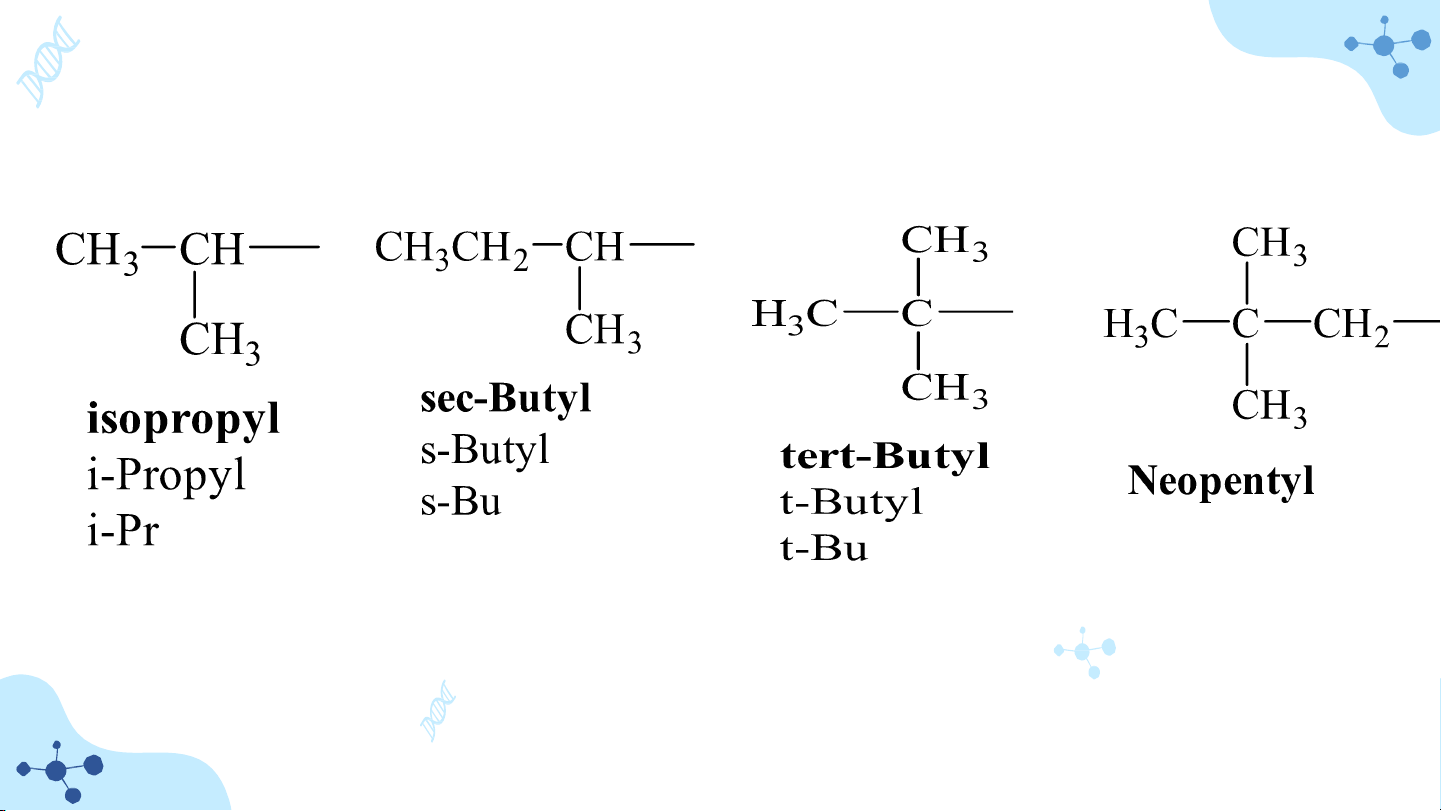
• Nếu gốc alkyl có nhánh: dùng các tiếp ngữ iso (i), neo, tert (t), sec (s)…. 1.3 Đồng phân a) Đồng phân phẳng
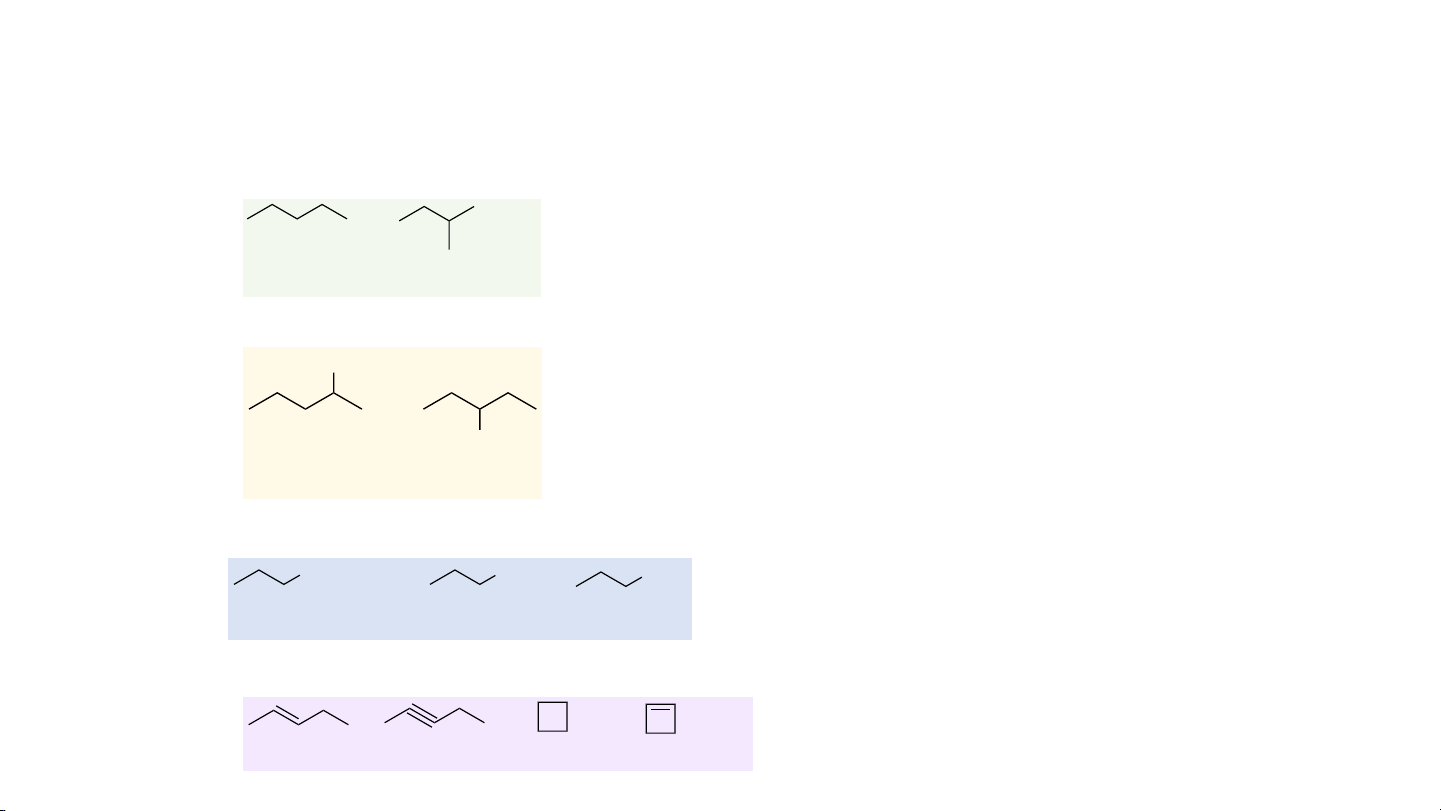
• Đồng phân mạch carbon: có mạch C sắp xếp khác nhau. Mạch thẳng hay mạch nhánh. n-butane 2-methylpropane
• Đồng phân vị trí nhóm định chức: nhóm định chức trên mạch C ở vị trí khác nhau. OH OH butane-2-ol butane-3-ol
• Đồng phân nhóm chức: có các nhóm chức khác nhau. COOH OH CHO Acid butanoic propanol butanal
• Đồng phân liên kết: cùng công thức phân tử nhưng trong mạch C có các liên kết khác nhau. but-2-ene but-2-yne cyclobutane cyclobutene
b) Đồng phân lập thể
• Đồng phân hình học là những hợp chất có cùng công thức phân tử nhưng có vị trí trong
không gian của các nguyên tử khác nhau đối với mặt phẳng 𝜋. Hay mặt phẳng vòng. Có
2 dạng : đồng phân cis và trans H H H H H H H H H H H H H H H H H H
Nếu 4 nhóm thế khác nhau thì ta có đồng phân E-Z
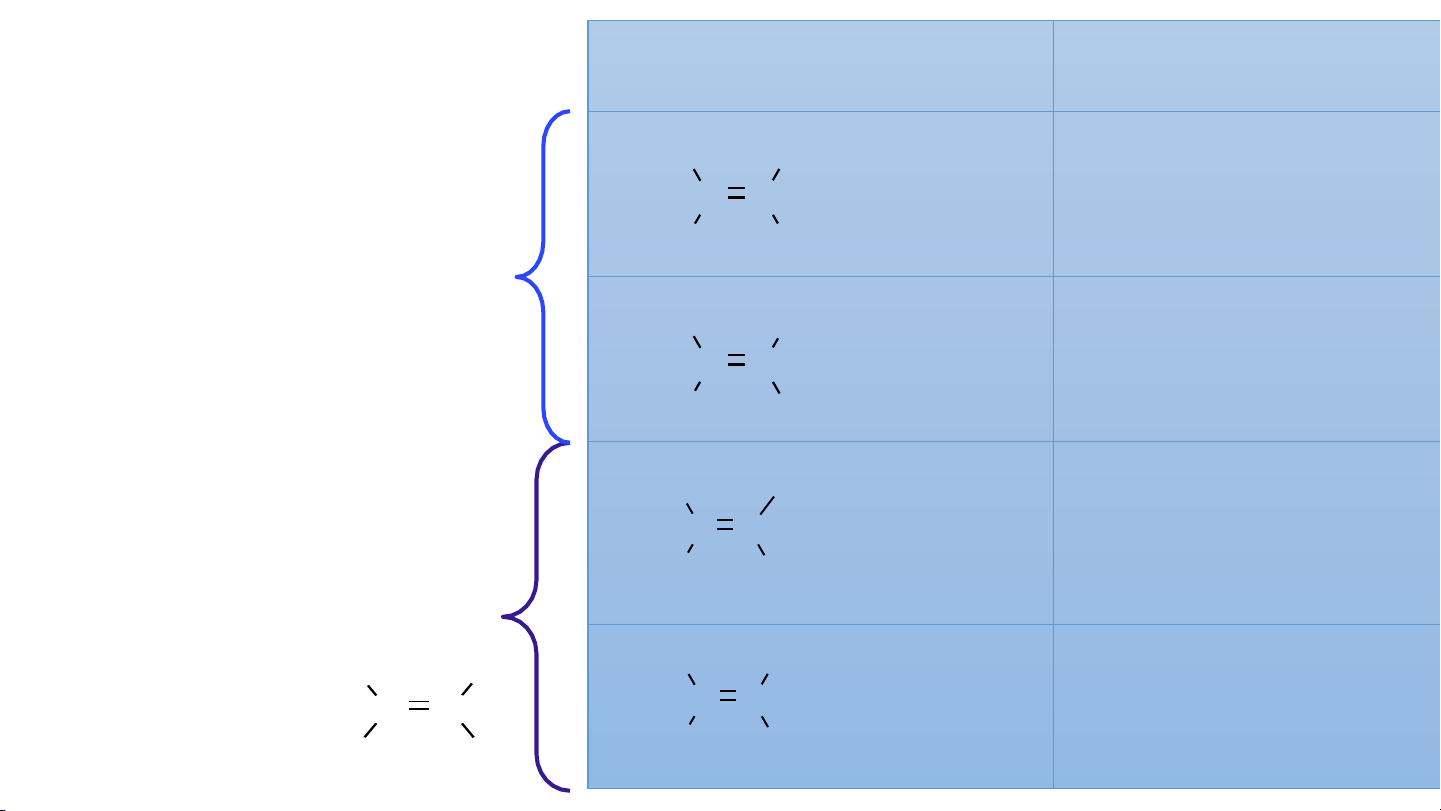
Đồng phân hình học Tên gọi §
Đồng phân trans bền hơn cis-2-butene H CH 3C 3
đồng phân cis vì dạng trans C C H H
có năng lượng thấp. Dạng trans-2-butene
cis, các nhóm thế cùng phía H H 3C C C đẩy nhau. H CH3 Z-3-ethylhex-2-ene §
Đồng phân E-Z. H C3H7 3C C C
E: eintgegen – khác phía H C2H5
Z: zusammen – cùng phía Khi các nhóm thế H C E-3-methylhex-2-ene a c 3C 2H5 C C a > b , c > d. C C b d H C3H7 E-Z
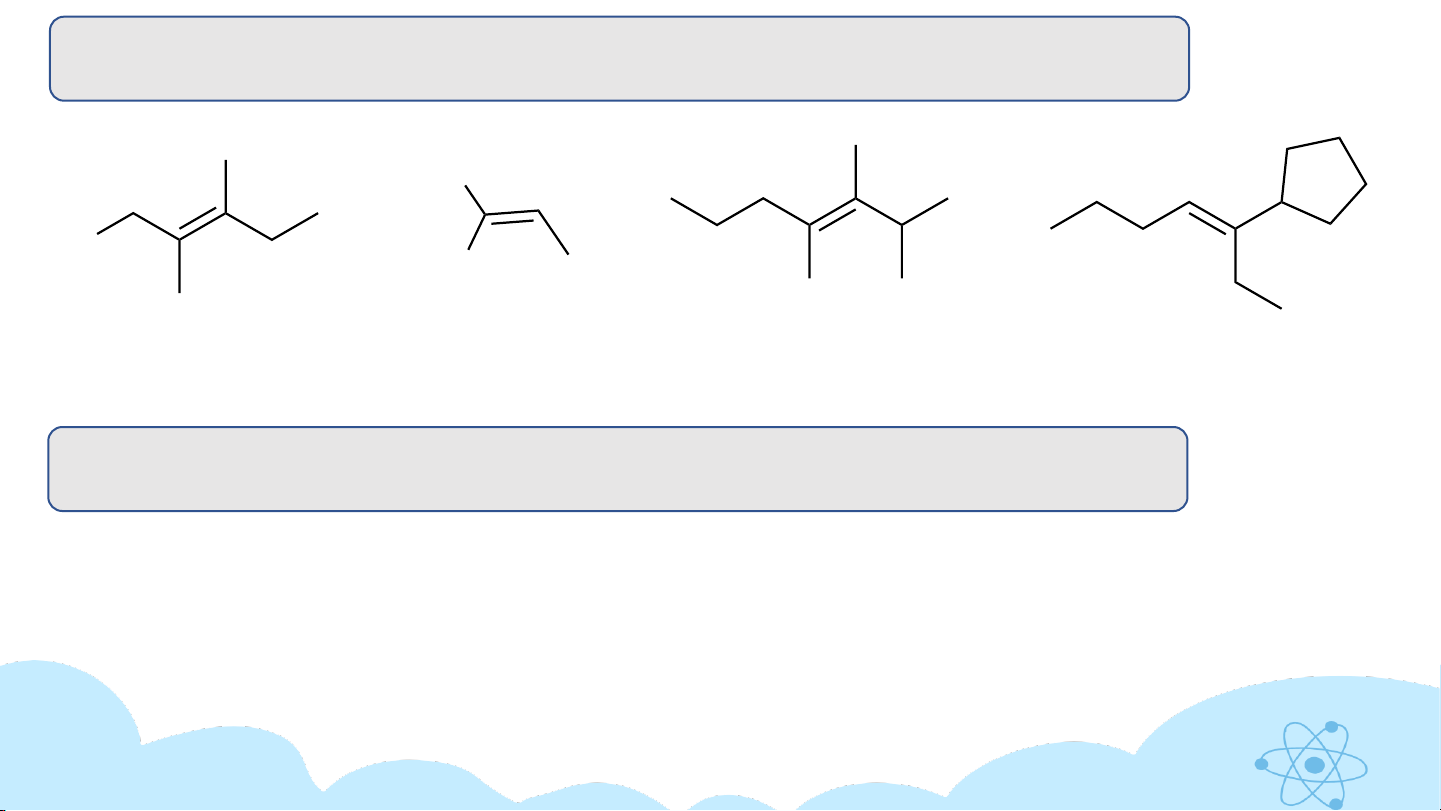
v Gọi tên các hợp chất hữu cơ và xác định cấu hình E-Z. H CH3 Cl H (a) C C (b) C C H CH(CH 3C 3)2 H C 3C 2H5
(a) Z-3,4-dimethylpent-2-ene (b) E-2-cloropent-2-ene
BT1: Gọi tên các hợp chất hữu cơ và xác định cấu hình E-Z. Cl Cl Br (2) (3) (4) (1)
BT2: Hãy viết cấu hình E-Z của các hợp chất có tên gọi sau. (a) E-2,4-hexadiene
(b) Z-1-cloro-2-methyl-3-ethylhexa-2-ene
(c) Z-1-hydroxy-2,3-dimethylpent-2-ene
• Đồng phân quang học là những hợp chất có tác dụng quay mặt phẳng
ánh sáng phân cực. Chất có tác dụng với ánh sáng phân cực là chất quang hoạt.
• Cách xác định hợp chất có tính quang hoạt dựa vào carbon bất đối (carbon thủ tính)
Các đồng phân đối quang ( enantiomer, theo từ gốc enantio: ngược chiều)
có cùng các tính chất nhưng khác nhau về sự tương tác ánh sáng phân cực.
Hợp chất có 1 carbon bất đối xứng có 2 đồng phân quang học.
Hợp chất có nhiều carbon bất đối xứng có 2n đồng phân quang học.
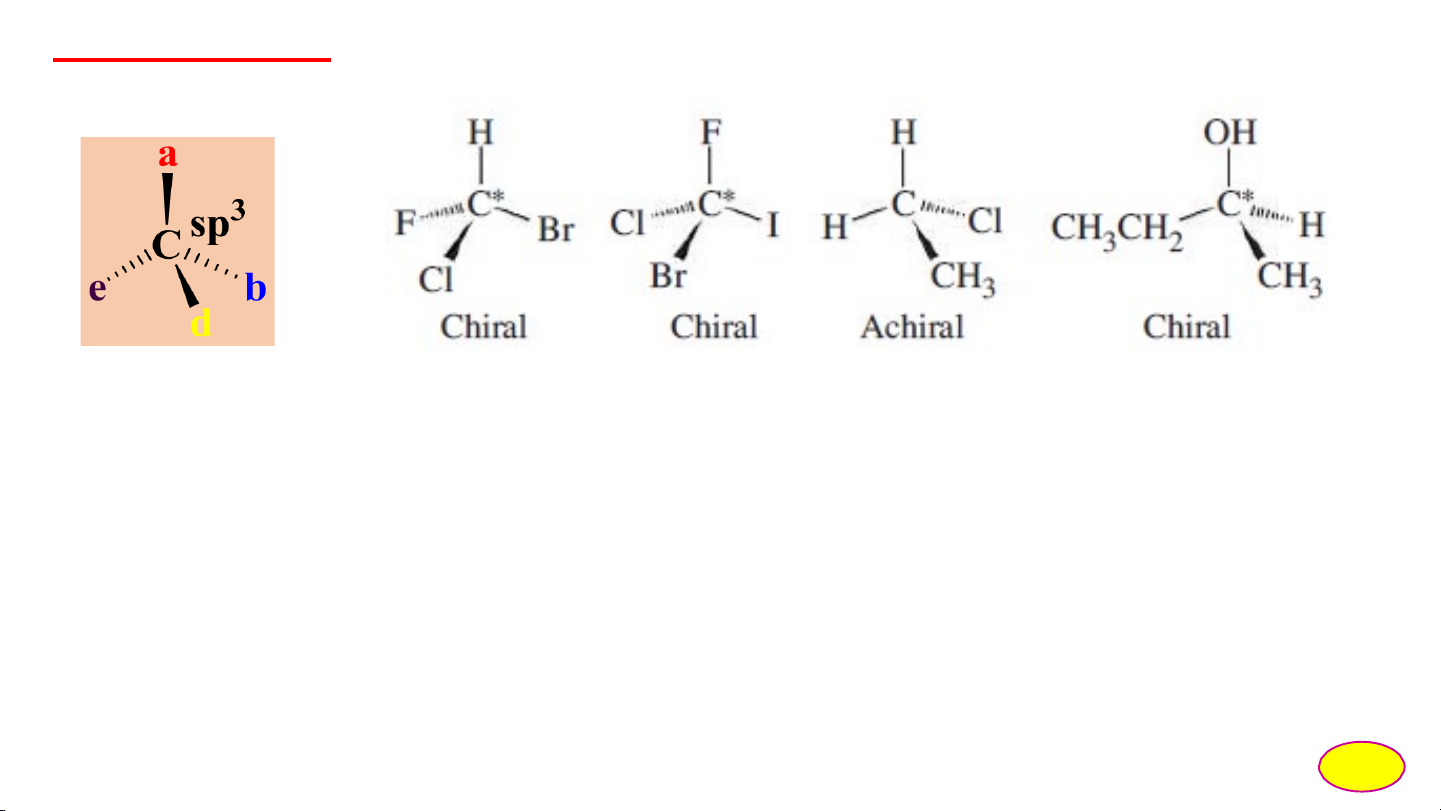
ØCARBON THỦ TÍNH - Carbon phi đối xứng, carbon mang 4 nhóm thế khác nhau: Ký hiệu : C* C*: chiral carbon -Carbon thủ tính
-Phi đối xứng, bất đối xứng (asymmetric).
-Tâm lập thể (stereocenter) C: achiral carbon - Carbon phi thủ tính 20



