
Preview text:
KHẢO SÁT HSG – CỤM 3 BẮC NINH
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 30. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
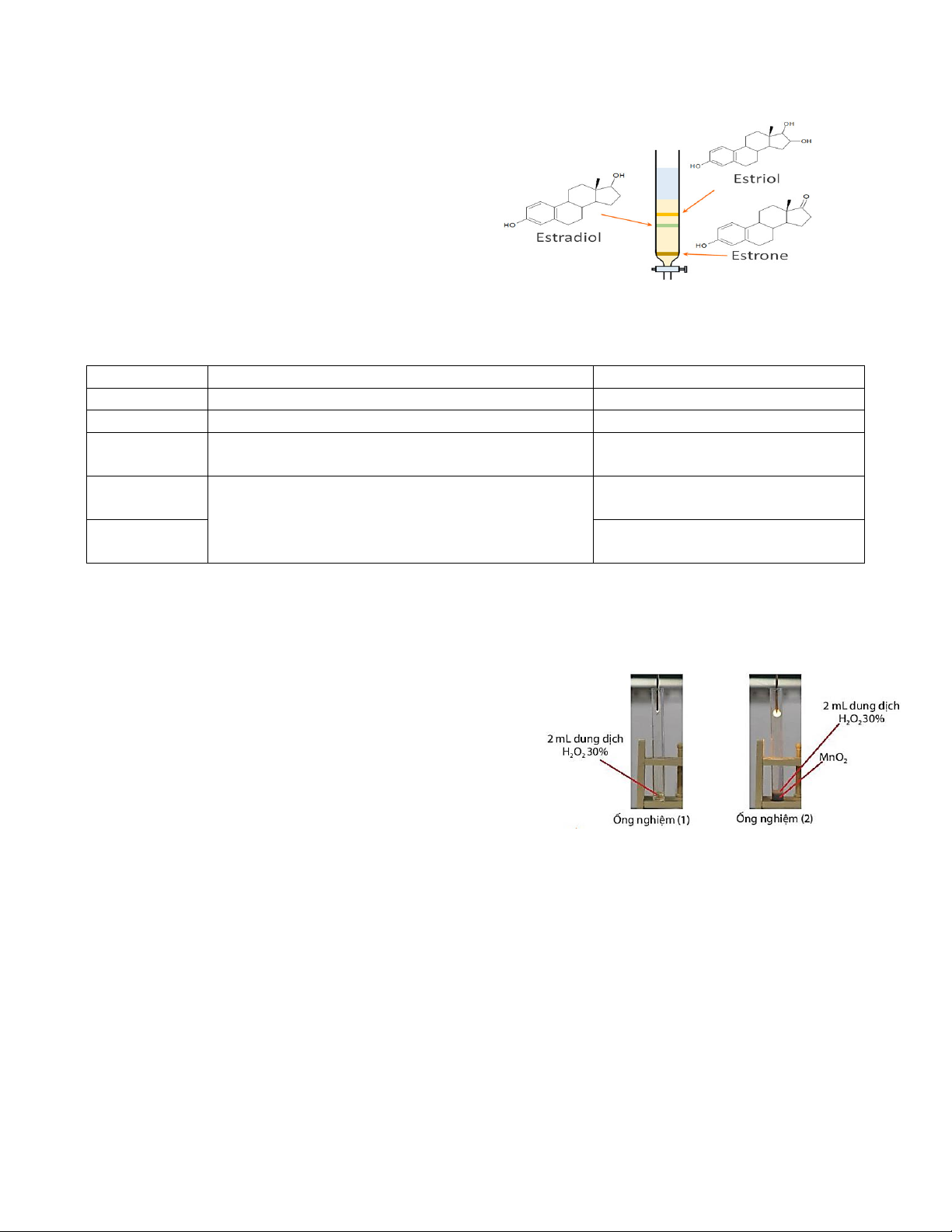
Câu 1. Phương pháp sắc kĩ cột có thể được dùng để tách các
hợp chất estriol, estradiol và estrone. Sau một thời gian có sự
tách các chất như trong sơ đồ sau:
Thứ tự giảm dần khả năng hấp phụ bởi pha tĩnh là
A. Estriol > Estradiol > Estrone.
B. Estrone > Estradiol > Estriol
C. Estriol > Estrone > Estradiol.
D. Estradiol > Estriol > Estrone.
Câu 2. Cho các dung dịch hoặc các chất lỏng riêng biệt: đường saccharose, acetic acid, ethyl alcohol, đường glucose,
dầu thực vật đựng trong các ống nghiệm được ký hiệu là X, Y, Z, P, Q không theo thứ tự. Thực hiện lần lượt các thí
nghiệm của các chất trên với một số thuốc thử, kết quả thí nghiệm được ghi ở bảng dưới đây: Ống nghiệm Thuốc thử Hiện tượng X NaHCO3 Có sủi bọt khí Y AgNO3 trong NH3 Có kết tủa Ag Đun với H Z
2SO4 loãng, trung hòa môi trường, sau Có kết tủa Ag
đó cho dung dịch AgNO3 trong NH3 vào
Tạo hai lớp chất lỏng không trộn P lẫn Nước cất
Tạo dung dịch đồng nhất không X,Y,Z,Q màu
Các chất X, Y, Z, P, Q lần lượt là các chất:
A. saccharose; dầu thực vật; acetic acid; glucose; ethyl alcohol.
B. acetic acid; glucose; saccharose; dầu thực vật; ethyl alcohol.
C. glucose; saccharose; dầu thực vật; ethyl alcohol; acetic acid.
D. acetic acid; glucose; dầu thực vật; ethyl alcohol; saccharose.
Câu 3. Nghiên cứu ảnh hưởng của chất xúc tác đến tốc độ phản ứng:
2H2O2(aq) → 2H2O(l) + O2(g)
- Hóa chất: dung dịch hydrogen peroxide (H2O2) 30%, bột MnO2.
- Dụng cụ: Ống nghiệm, tàn đóm đỏ. - Tiến hành:
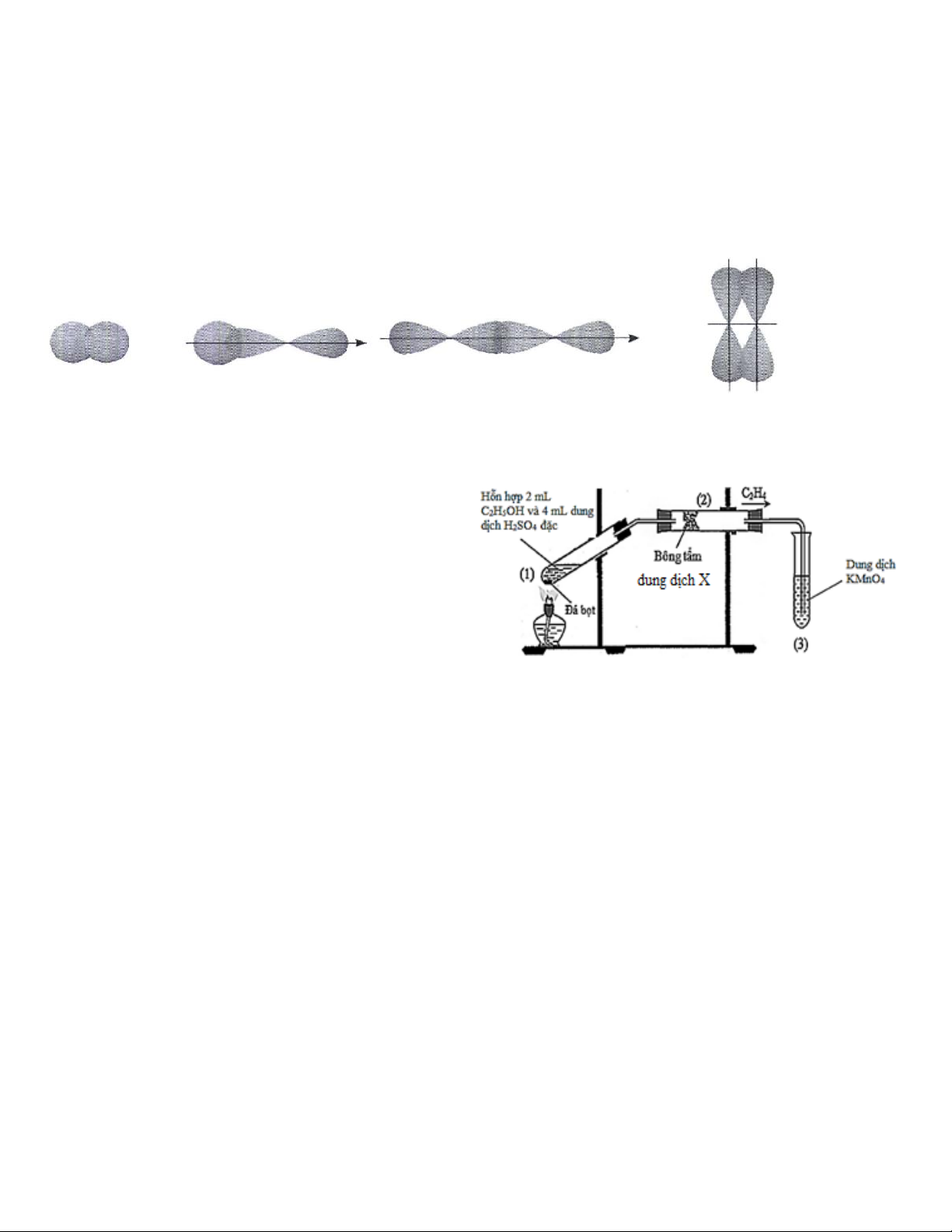
Bước 1: Rót khoảng 2 mL dung dịch H2O2 vào hai ống nghiệm (1), (2).
Bước 2: Thêm một ít bột MnO2 vào ống nghiệm (2) và đưa nhanh tàn
đóm đỏ vào miệng 2 ống nghiệm. Cho các phát biểu sau:
(1) Tàn đóm ở ống nghiệm (1) chỉ cháy nhẹ.
(2) Tàn đóm ở ống nghiệm (2) bùng cháy mãnh liệt hơn bên ống nghiệm (1).
(3) Sau khi phản ứng kết thúc, chất xúc tác MnO2 cũng bị tiêu hao hết.
(4) Khi có xúc tác, phản ứng sẽ xảy ra qua nhiều giai đoạn, mỗi giai đoạn đều có năng lượng hoạt hoá thấp hơn so với
phản ứng không xúc tác, do đó số hạt có đủ năng lượng hoạt hoá sẽ nhiều hơn, dẫn đến tốc độ phản ứng tăng.
Số phát biểu đúng là
A. (1), (2), (4). B. (1), (2). C. (1), (2), (3), (4). D. (1), (2), (3).
Câu 4. Trong phép chuẩn độ HNO3 bằng KOH, ý nào sau đây thể hiện đúng nhất các ion có mặt tại điểm cuối chuẩn độ? A. B. C. D
Câu 5. Khi iron (sắt) phản ứng với nitric acid với nồng độ
khác nhau, hàm lượng sản phẩm khử với nồng độ nitric
acid được thể hiện trong hình sau:
Phát biểu nào sau đây là sai?
A. Nồng độ nitric acid càng cao, thì trạng thái oxi hoá của N
trong sản phẩm khử càng cao.
B. Khi nồng độ nitric acid là 9,75 thì sản phẩm khử chỉ là NO.
C. Ở nồng độ nitric acid thấp, hàm lượng sản phẩm khử + NH 4 là cao.
D. Khi nồng động nitric acid là 12,2 mol/L, sản phẩm khử là NO và NO2 có tỉ lệ mol 1:1.
Câu 6. Thuốc chữa ghẻ DEP được điều chế từ nguồn
nguyên liệu đầu là naphthalene theo sơ đồ các quá trình
chuyển hoá và hiệu suất sau:
Tổng khối lượng naphthalene và ethanol cần thiết để điều chế 2 tấn DEP là
A. 2077,373 kg. B.975,093kg. C. 1102,28 kg. D. 1002,56 kg.
Câu 7. R là nguyên tố mà nguyên tử có phân lớp electron ngoài cùng là 3p5. Cho các phát biểu sau về R:
(1) Tổng số hạt mang điện trong nguyên tử R là 18.
(2) Số electron độc thân trong nguyên tử R là 3.
(3) Oxide cao nhất của R là R2O7.
(4) Dung dịch muối NaR tác dụng với dung dịch AgNO3 sinh ra kết tủa.
(5) Đơn chất R2 có nhiều trong tự nhiên.
Số nhận xét đúng là A. 2. B. 4. C. 1. D. 3.
Câu 8. Trong công nghiệp, một lượng lớn sodium hydrogencarbonate (baking soda) và sodium carbonate
(soda) được sản xuất bằng
phương pháp Solvay theo sơ đồ sau: Cho các phát biểu sau:
(a) NaHCO3 tách ra khỏi tháp carbonate hóa khi làm lạnh để thu được NaHCO3(s).
(b) Dựa vào tính chất lưỡng tính của NaHCO3 mà người ta dùng nó để sản xuất ra Na2CO3.
(c) Quá trình Solvay, góp phần giảm thiểu tác động đến môi trường và tiết kiệm chi phí sản xuất do tái sử dụng NH3 và CO2.
(d) Trong chế biến thực phẩm, NaHCO3 được ứng dụng làm bột nở.
(e) Soda là hóa chất được sử dụng trong làm mềm nước cứng.
Số phát biểu đúng là A. 5. B. 2. C. 4. D. 3.
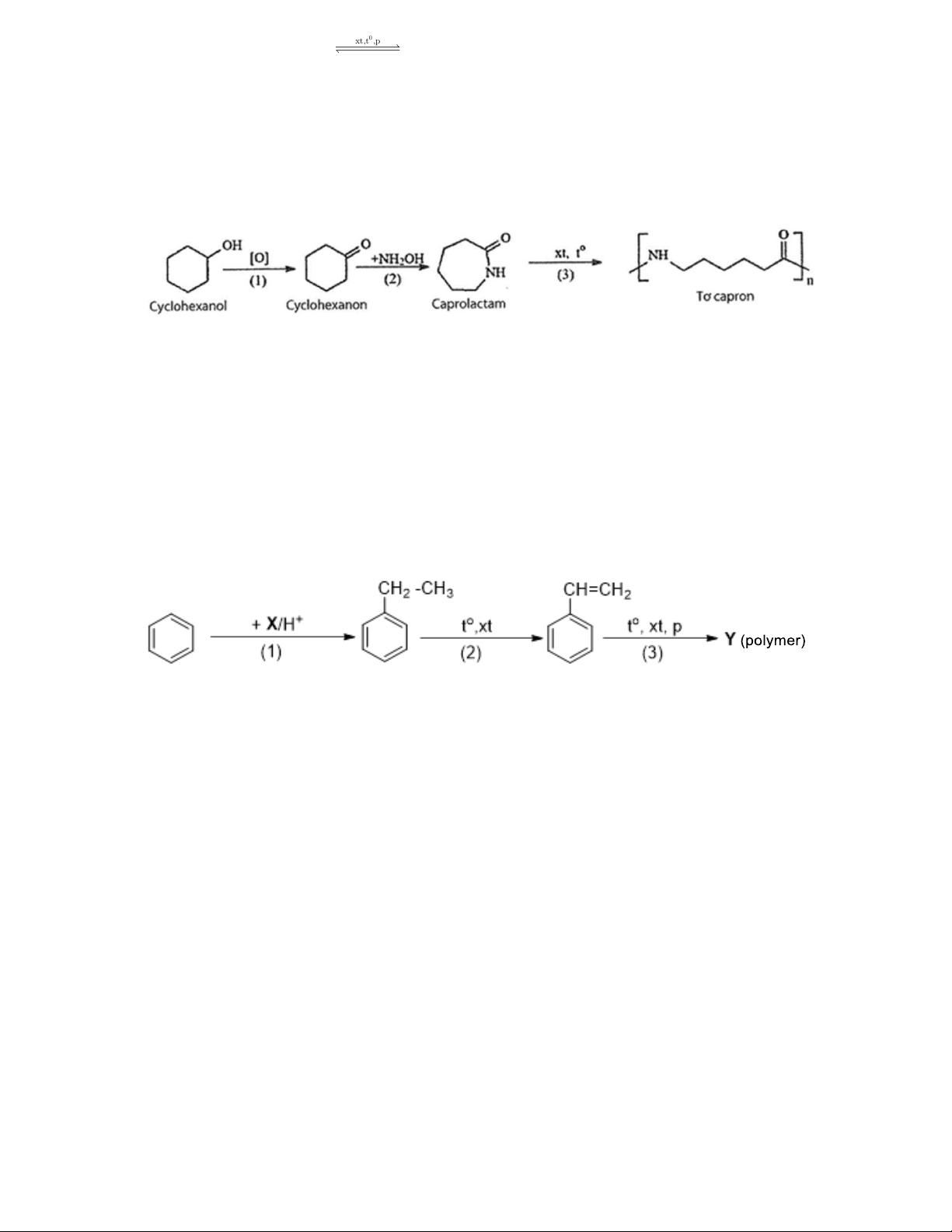
Câu 9. Cho các hình biểu diễn sự xen phủ orbital nguyên tử để tạo liên kết hóa học sau: (a) Xen phủ trục s-s (b) Xen phủ trục s-p (c) Xen phủ trục p-p (d) Xen phủ bên p-p
Biết số hiệu các nguyên tử của H, F và S lần lượt là 1, 9 và 16. Sự tạo liên kết trong các phân tử H2S và F2 theo kiểu xen phủ tương ứng là
A. (b) và (c). B. (b) và (d). C. (a) và (c). D. (c) và (d).
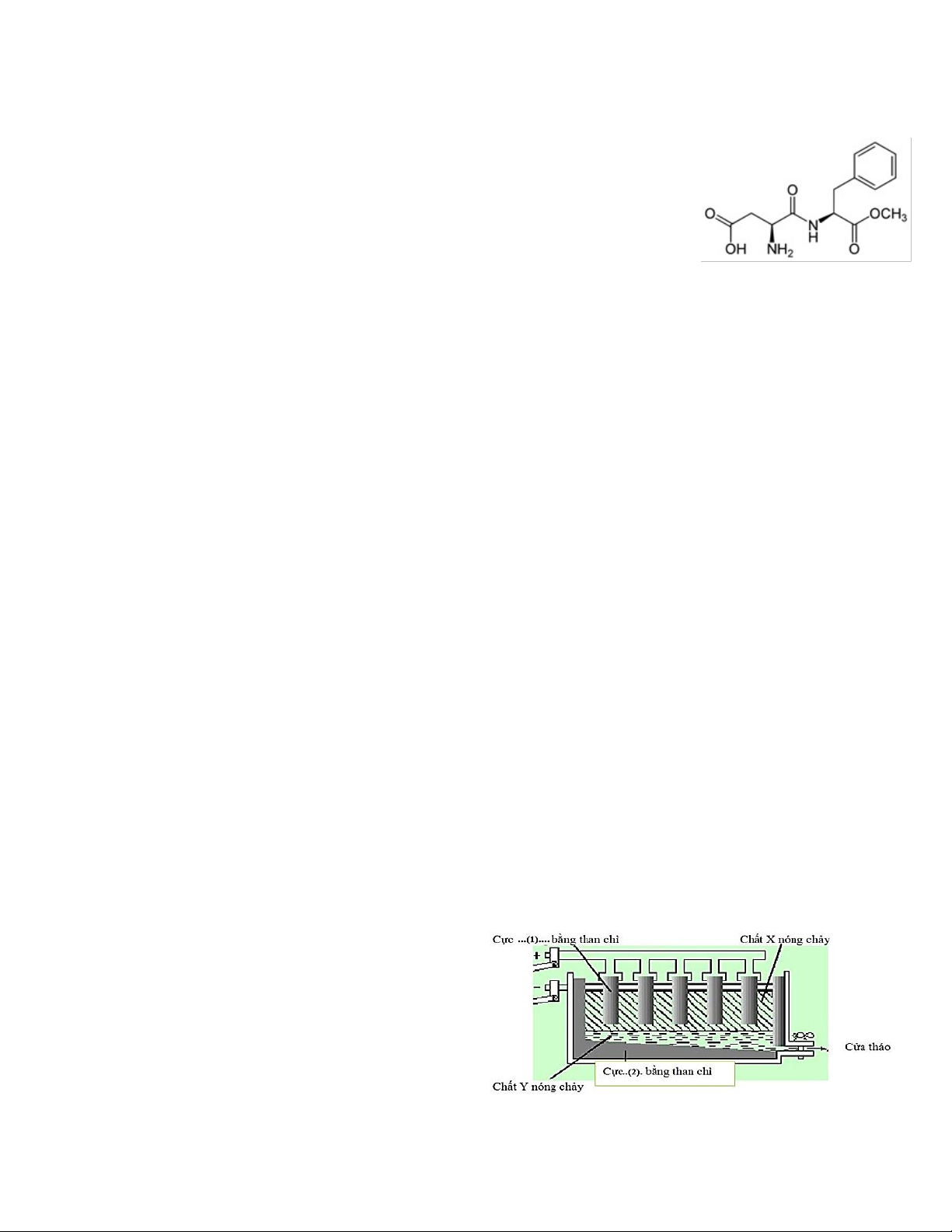
Câu 10. Thí nghiệm điều chế và thử tính chất của ethylene
được tiến hành như hình dưới đây: Cho các phát biểu sau:
(a) Đá bọt có vai trò làm cho chất lỏng sôi nhanh và mạnh hơn khi đun nóng.
(b) Dung dich X trong sơ đồ thí nghiệm trên có thể là NaOH
hoặc NaCl đặc và dung dịch X có tác dụng loại bỏ tạp chất khí trong thí nghiệm này.
(c) Trong quá trình phản ứng, mầu của ống nghiệm (3 ) nhạt
dần. Có thể thử tính chất của khí ethylene bằng cách thay dung
dịch KMnO4 bằng dung dịch Br2.
(d) Khi kết thúc thí nghiệm, tắt đèn cồn trước sau đó để nguội rồi rút ống dẫn khí.
Số phát biểu đúng là A. 4. B. 1. C. 2. D. 3.
Câu 11. Cho các phát biểu về pin Galvani Zn – Cu như sau:
(1) Trên bề mặt thanh kim loại Zn xảy ra quá trình khử và trên bề mặt thanh kim loại Cu xảy ra quá trình oxi hóa.
(2) Sự trao đổi electron trong quá trình oxi hoá và quá trình khử tại các điện cực phát sinh ra dòng điện.
(3) Cầu muối giúp cân bằng điện tích trong các dung dịch ở các điện cực.
(4) Giá trị sức điện động của Pin giảm dần theo thời gian.
(5) Khi pin hoạt động, khối lượng thanh kim loại Zn sẽ bị giảm dần và nồng độ ion Cu2+ cũng giảm dần.
Có bao nhiêu phát biểu đúng? A. 4. B. 5. C. 2. D. 3.
Câu 12. Cho phản ứng hóa học sau: C2H5OH + K2Cr2O7 + H2SO4 → CH3CHO + Cr2(SO4)3 + K2SO4 + H2O
Tổng hệ số cân bằng của các chất trong phản ứng hóa học trên là A. 20. B. 17. C. 19. D. 15.
Câu 13. Thực hiện các thí nghiệm sau:
(1) Ngâm lá đồng trong dung dịch AgNO3.
(2) Ngâm lá kẽm trong dung dịch HCl loãng.
(3) Ngâm lá sắt được cuộn dây đồng trong dung dịch HCI.
(4) Đặt một vật làm bằng gang ngoài không khí ẩm trong nhiều ngày.
(5) Ngâm một miếng đồng vào dung dịch Fe2(SO4)3.
Số thí nghiệm xảy ra ăn mòn điện hoá là A. 3. B. 4. C. 2. D. 1.
Câu 14. Cho cân bằng: 2SO2(g) + O2(g) 0 xt,t ,p
2SO3(g). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm
đi. Phát biểu đúng khi nói về cân bằng này là
A. phản ứng nghịch toả nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
B. phản ứng nghịch thu nhiệt, cân bằng dịch chuyển theo chiều thuận khi tăng nhiệt độ.
C. phản ứng thuận thu nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
D. phản ứng thuận toả nhiệt, cân bằng dịch chuyển theo chiều nghịch khi tăng nhiệt độ.
Câu 15. Tơ capron là polymer có tính dai, bền, mềm óng mượt, ít thấm nước, mau khô. Bên cạnh ứng dụng trong ngành
may mặc, tơ capron còn được sử dụng làm dây cáp, dù, đan lưới, chế tạo các chi tiết máy. Một quy trình sản xuất tơ
capron từ cyclohexanol được thực hiện theo sơ đồ sau: Cho các phát biểu sau:
(a) Tơ capron thuộc loại polypeptide.
(b) Phản ứng (3) là phản ứng trùng hợp.
(c) Phần trăm khối lượng của carbon trong tơ capron là 63,72% (kết quả làm tròn đến hàng phần trăm).
(d) Nếu hiệu suất chuyển hoá từ cyclohexanol đến tơ capron là 80%, thì cứ 1 tấn cyclohexanol thu được 1,13 tấn tơ capron.
(e) Oxi hóa cyclohexanon bởi LiAlH4 thu được cyclohexanol.
(f) Tơ capron không bền trong môi trường acid.
Số phát biểu đúng là A. 5. B. 4. C. 3. D. 2.
Câu 16. Polymer Y được dùng làm hộp đựng thực phẩm, đồ chơi trẻ em, vỏ đĩa CD, DVD, ... Trong công nghiệp sản
xuất chất dẻo, polymer Y được điều chế theo sơ đồ sau: Cho các phát biểu sau:
(a) Trong sơ đồ trên, X là ethane; Y có ký hiệu là PE.
(b) Phản ứng (3) trong sơ đồ thuộc loại phản trùng hợp.
(c) Đồ hộp làm từ chất Y có thể dùng đựng thực phẩm nóng hoặc sử dụng trong lò vi sóng để làm nóng thức ăn.
(d) Polymer Y có tính đàn hồi cao, dùng để sản xuất cao su, vật liệu chống thấm, lốp xe,…
(e) Từ 100 kg benzene và 32 m3 khí X (ở 25oC, 1 bar), với hiệu suất mỗi quá trình (1), (2), (3) lần lượt là 60%, 55%
và 60%, thu được 26,4 kg polymer Y.
Số phát biểu đúng là A. 3. B. 2. C. 5. D. 4.
Câu 17. Sử dụng vôi sữa là phương pháp phổ biến để xử lí khí thải SO2. 90% lượng SO2 trong khí thải được hấp thụ
theo phương trình hóa học: Ca(OH)2 + SO2 → CaSO3 + H2. Sau đó CaSO3 bị oxi hóa hoàn toàn thành CaSO4 dưới tác
dụng của oxygen. CaSO4 được lọc tách, làm sạch, nung khô và thu hồi dưới dạng thạch cao thương phẩm (2CaSO4.H2O)
với hiệu suất 80%. Một nhà máy trong một ngày thải ra 2500 m³ khí thải (ở đkc) chứa 1% SO2 về thể tích. Khối lượng
2CaSO4.H2O thu được trong 30 ngày theo phương pháp trên đạt là A. 3158,5 kg. B. 3262,5 kg. C. 3509,4 kg. D. 3948,1 kg.
Câu 18. Formic acid có trong nọc một loài kiến lửa và một số loại con côn trùng khác như: ong, rết... Trung bình mỗi
lần kiến cắn sẽ “tiêm” vào da 5,0.10-3 cm3 dung dịch chứa 50% thể tích formic acid. Cho các phát biểu sau:
(a) Công thức phân tử của formic acid là HCOOH.
(b) Biết mỗi lần cắn làm tiêu hao 80% formic acid có trong cơ thể kiến, thể tích formic acid tinh khiết trung bình có
trong một con kiến là 3,125.10-3 cm3.
(c) Khi bị ong đốt, để giảm sưng và đau người ta có thể dùng những giấm ăn hoặc chanh bôi lên vết đốt.
(d) Để làm giảm lượng formic acid trong vết cắn, bác sĩ thường dùng thuốc có chứa thành phần là sodium hydrogencarbonate
(NaHCO3). Khối lượng NaHCO3 cần dùng để trung hoà hoàn toàn lượng formic acid từ vết cắn của một con kiến (biết khối
lượng riêng của formic acid là 1,22 g/cm3) là 5,57 gam.
Số phát biểu không đúng là A. 4. B. 3. C. 1. D. 2.
Câu 19. Aspartame (APM) là một chất làm ngọt nhân tạo, còn được gọi là đường hóa học không
chứa đường saccharide, có độ ngọt gấp 200 lần đường ăn thông thường. Công thức cấu tạo của
APM cho như hình dưới đây: Cho các phát biểu sau:
(a) Công thức phân tử của APM là C14H18N2O5.
(b) Trong phân tử APM có 1 liên kết amide.
(c) APM bền trong môi trường axit nhưng kém bền trong môi trường kiềm.
(d) Cho 29,4 gam APM tác dụng hết với 200 mL dung dịch NaOH 2M thu được dung dịch X, cô cạn X thu được chất rắn có khối lượng 43,6 gam.
Số phát biểu đúng là A. 4. B. 3. C. 2. D. 5.
Câu 20. Cho các phát biểu sau:
(a) Chất béo là triester của glycerol với acid béo.
(b) Thành phần chính của cồn 70° thường dùng trong y tế để sát trùng là methanol.
(c) Glucose bị oxygen hóa bởi thuốc thử Tollens.
(d) Trong dung dịch, glucose tồn tại chủ yếu ở dạng mạch vòng và một phần nhỏ ở dạng mạch hở.
(e) Khi đun nóng fructose với Cu(OH)2/NaOH thu được kết tủa copper (I) oxide.
(f) Amylopectin và cellulose đều có mạch carbon phân nhánh.
(g)Trong công nghiệp dược phẩm, saccharose được dùng để pha chế thuốc.
Số phát biểu đúng là A. 2. B. 6. C. 5. D. 4.
Câu 21. Thành phần dầu tẩy trang hoa hồng Cocoon có C15-19 Alkane, tức là các alkane có từ 15 đến 19C. Hãy cho
biết vì sao người ta dùng alkane vào thành phần dầu tẩy trang?
A. Do alkane dễ hoa tan trong nước.
B. Do các alkane này có khả năng làm mềm da, trơ về mặt hóa học, vô hại với sức khỏe con người, không phân cực,
dễ hòa tan các chất không phân cực trong phấn, kem, bụi bẩn kéo theo và bị rửa trôi đi.
C. Do các alkane có khả năng chống nắng tốt.
D. Do alkane dễ tác dụng với các chất trong kem, phấn bôi da thành chất tan dễ bị rửa trôi.
Câu 22. Năm 1872, trong cuốn sách Không khí và Mưa, Robert Angus Smith (Rô-bớt An-gớt Smit) (nhà hoá học người
Scotland) đã trình bày chi tiết về hiện tượng mưa acid. Cho các phát biểu sau về mưa acid:
(a) Khi nước mưa có pH nhỏ hơn 6,5 thì gọi là hiện tượng mưa acid.
(b) Khi các khí như SO2 và các khí oxide của nitrogen (NOx) bị khử với xúc tác của các ion kim loại trong khói,
bụi,… Các khí này hòa tan trong nước tạo thành dung dịch H2SO4 và dung dịch HNO3.
(c) Mưa acid góp phần làm ra tăng hiện tượng phú dưỡng.
(d) Tác động của mưa acid đối với kim loại sắt có trong thép như sau: 6H+ + 2Fe ⟶ 2Fe3+ + 3H2.
Số phát biểu đúng là A. 4. B. 1. C. 2. D. 3.
Câu 23. Trong công nghiệp, người ta điều chế Al bằng phương
pháp điện phân nóng chảy Al2O3 theo sơ đồ sau: Cho các phát biểu sau:
(1) X là Al nóng chảy, Y là hỗn hợp Al2O3 và Na3AlF6 nóng chảy.
(2) Cực (1) và (2) lần lượt là cực âm (anode) và cực dương (cathode).
(3) Trong quá trình điện phân, xảy ra hiện tượng “dương cực
tan”, các thanh điện cực (1) sẽ sẽ bị mòn dần trong quá trình
sản xuất Al do bị oxi hóa thành oxide của carbon.
(4) Trung bình để sản xuất được 1,08 tấn Al thì lượng điện cực than chì bị tiêu hao 0,89 tấn do bị oxi hoá bởi O2 sinh ra
trong quá trình điện phân. (Giả thiết thành phần khí bay ra ở cực dương gồm 42% CO, 44% CO2 và 14% O2 về thể tích).
Số phát biểu đúng là A. 1. B. 2. C. 4. D. 3.
Câu 24. Một trong các phương pháp dùng để loại bỏ sắt (iron) trong nguồn nước nhiễm sắt là sử dụng lượng vôi tôi
(Ca(OH)2) vừa đủ để tăng pH của nước nhằm kết tủa ion sắt khi có mặt oxygen theo sơ đồ phản ứng: (1) Fe3+ +3OH- → Fe(OH)3
(2) 4Fe2+ + 8OH- + O2 + 2H2O → 4Fe(OH)3
Theo QCVN 01-1:2018/BYT, hàm lượng sắt cho phép trong nước là 0,30 mg/L. Một mẫu nước có hàm lượng sắt cao
gấp 28 lần so với ngưỡng cho phép trên. Biết sắt trong mẫu nước trên chỉ tồn tại ở hai dạng là Fe3+ và Fe2+ với tỉ lệ mol
Fe3+ : Fe2+ = 1 : 4. Cần tối thiểu m gam Ca(OH)2 để kết tủa hoàn toàn lượng sắt trong 30 m³ mẫu nước trên. Giá trị của m là A. 666,0. B. 333,0. C. 732,6. D. 366,3.
Câu 25. Tiến hành các thí nghiệm sau:
(1) Cho Zn vào dung dịch AgNO3. (2) Cho Fe vào dung dịch Fe2(SO4)3.
(3) Cho Na vào dung dịch CuSO4. (4) Dẫn khí CO (dư) qua ống nghiệm có bột CuO, nung nóng.
Các thí nghiệm tạo thành đơn chất kim loại sau phản ứng là A. (1) và (2). B. (2) và (3). C. (3) và (4). D. (1) và (4).
Câu 26. Hoà tan hoàn toàn một lượng barium vào dung dịch chứa a mol hydrochloric acid thu được dung dịch X và a
mol khí hydrogen. Trong các chất sau: sodium sulfate, sodium carbonate, aluminium, aluminium oxide, aluminium
chloride, magnesium oxide, sodium hydroxide, ammonium chloride và sodium bicarbonate. Số chất tác dụng được với dung dịch X là A. 4. B. 6. C. 5. D. 7.
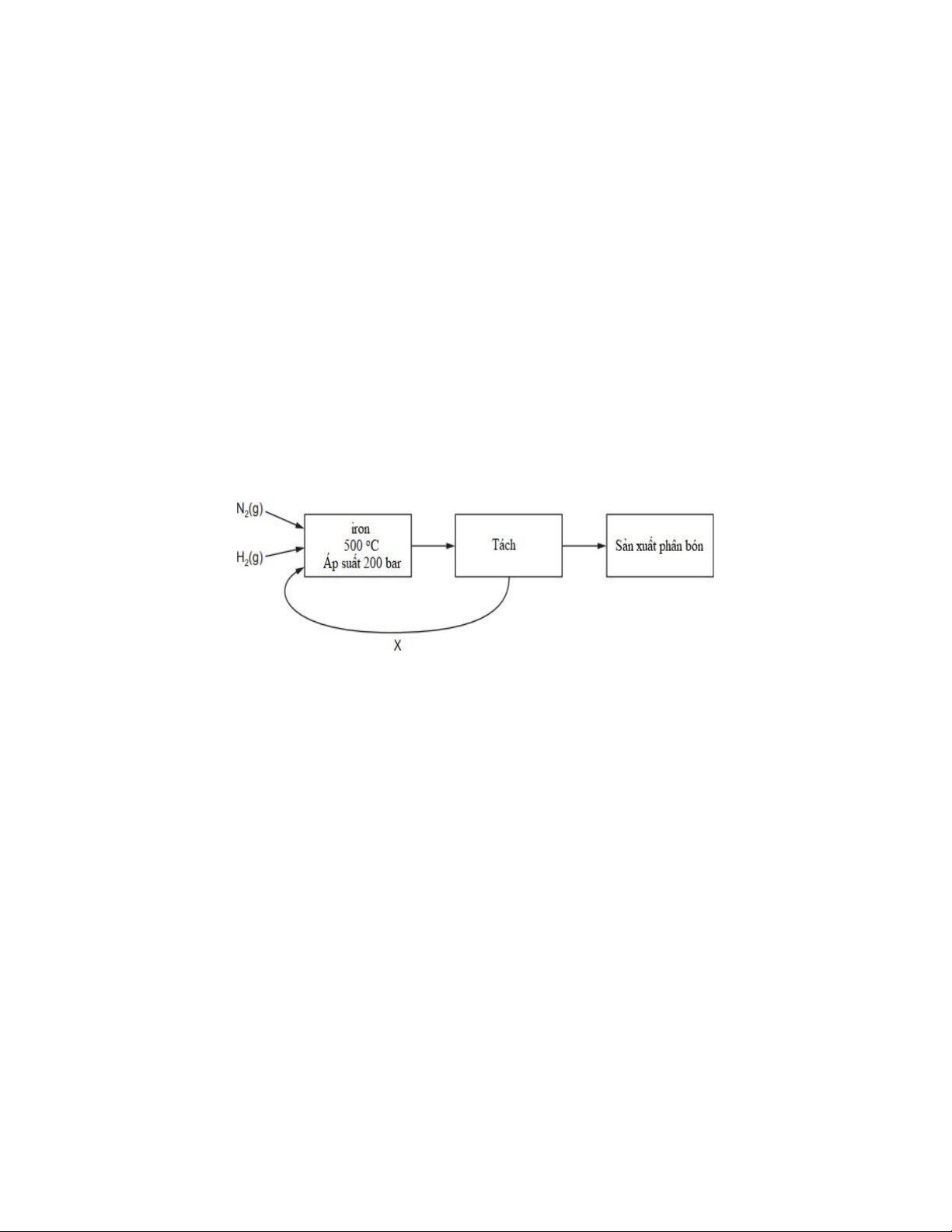
Câu 27. Quy trình sản xuất phân bón từ ammonia được thực hiện theo sơ đồ dưới đây:
Điều gì đang xảy ra trong quy trình có nhãn X?
A. Hydrogen và nitrogen chưa phản ứng được tái chế (tái sử dụng).
B. Ammonia được đưa trở lại đầu quá trình để chuyển dịch cân bằng về phía sản phẩm.
C. Chỉ hydrogen chưa phản ứng được tái chế.
D. Các khí được làm lạnh để làm cho ammonia tạo thành chất lỏng.
Câu 28. Cho các phát biểu sau:
(a) Các tính chất vật lý chung của kim loại là do electron tự do trong kim loại gây nên.
(b) Các kim loại nhóm IA, nhóm IIA và Al đều được gọi là kim loại nhẹ.
(c) Tính chất hoá học đặc trưng của kim loại là tính dễ bị khử.
(d) Kim loại có thế điện cực chuẩn càng lớn thì có tính khử càng mạnh.
(e) Trong công nghiệp, phương pháp nhiệt luyện và phương pháp điện phân đều được sử dụng để tách kim loại zinc (kẽm).
Số phát biểu đúng là A. 3. B. 4. C. 5. D. 6.
Câu 29. Để tìm hiểu tính chất của sulfuric acid, người ta tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho 1 mL dung dịch sulfuric acid đậm đặc vào ống nghiệm đựng 5 mL dung dịch barium chloride 0,1M
thấy có kết tủa trắng xuất hiện.
Thí nghiệm 2: Cho một mẩu kim loại đồng vào ống nghiệm chứa 2 mL dung dịch sulfuric acid đậm đặc, đun nóng thì
thấy dung dịch chuyển sang màu xanh, có khí T mùi hắc thoát ra.
Thí nghiệm 3: Cho một ít tinh thể hợp chất Y vào cốc thuỷ tinh, sau đó nhỏ từ từ 1 đến 2 mL dung dịch sulfuric acid
đậm đặc vào cốc thì thấy màu trắng của Y chuyển sang màu vàng, sau đó chuyển sang màu nâu và cuối cùng thành khối
xốp màu đen bị bọt khí đẩy lên miệng cốc. Cho các phát biểu sau:
(a) Nếu thay dung dịch sulfuric acid đậm đặc bằng dung dịch sulfuric acid loãng thì hiện tượng các thí nghiệm trên không thay đổi.
(b) Nếu toàn bộ lượng khí T thoát ra trong thí nghiệm 2 đem hấp thụ hoàn toàn vào dung dịch nước vôi trong dư, sau
phản ứng thu được 1,2 gam kết tủa thì lượng đồng cần dùng tối thiểu là 0,64 gam.
(c) Kết tủa trắng trong thí nghiệm 1, không tan trong nước và không tan trong dung dịch acid thông thường. Khí (T)
thoát ra trong thí nghiệm 2 có thể làm mất màu dung dịch bromine.
(d) Thí nghiệm 3 dùng để chứng minh sulfuric acid đậm đặc có tính háo nước và hiện tương trên được gọi là hiện tượng than hóa.
Số phát biểu đúng là A. 6. B. 4. C. 3. D. 5.
Câu 30. Phân tích nguyên tố hợp chất hữu cơ E cho kết quả phần trăm khối lượng carbon, hydrogen và oxygen lần lượt
là 54,55%; 9,09% và 36,36%. Dựa vào phương pháp phân tích phổ khối (MS) xác định được phân tử khối của E là 88.
Mặt khác, phổ hồng ngoại (IR) cho thấy phân tử E không chứa nhóm có số sóng từ 3600 – 3300 cm-1 nhưng lại chứa
nhóm có số sóng 1740 – 1670 cm-1. Thủy phân hoàn toàn E trong dung dịch NaOH, thu được muối của carboxylic acid
X và chất Y. Chất Y có nhiệt độ sôi (64,7 oC) nhỏ hơn nhiệt độ sôi của ethanol (78,3o C). Cho các phát biểu sau:
(a) Nhiệt độ sôi của E, X và Y được xếp theo chiều giảm dần: X > E > Y.
(b) Chất E có thể được điều chế trực tiếp từ phản ứng ester hóa giữa chất Y với propanoic acid.
(c) Trong công nghiệp, chất Y được trộn với xăng RON 92 để tạo ra xăng sinh học.
(d) Dung dịch muối tạo bởi giữa carboxylic acid X và NaOH có pH = 7.
Các phát biểu đúng là A. b, c. B. a, b. C. a, c, d. D. b, c, d.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 8. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
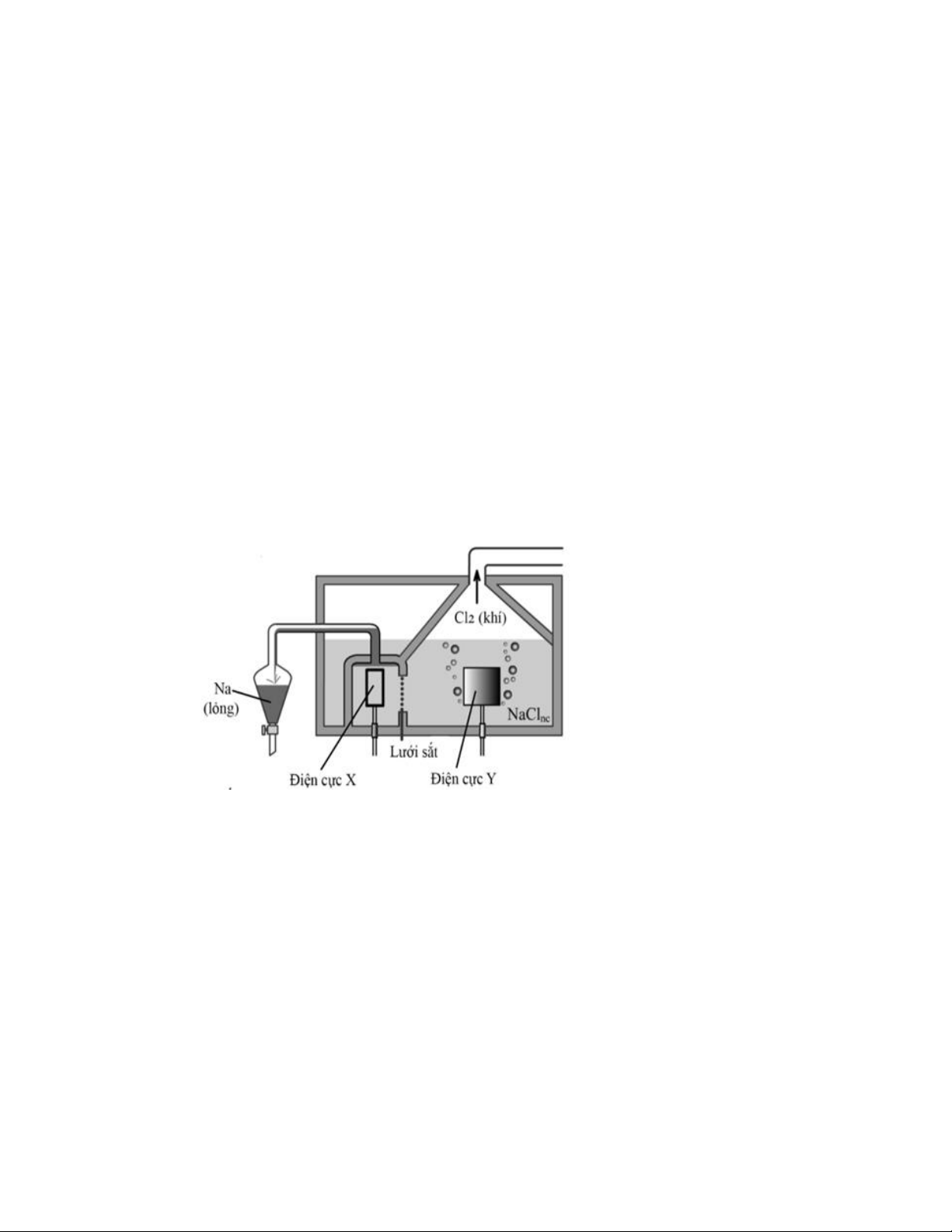
Câu 1. Sodium được sản xuất trong công nghiệp bằng cách điện phân muối ăn ở trạng thái nóng chảy. Sơ đồ bình điện
phân được cho ở hình vẽ:
a) Điện cực X là điện cực cathode; Y là điện cực anode.
b) Biết rằng trong hai điện cực sử dụng chế tạo bình điện phân, một điện cực làm từ sắt (iron), một điện cực làm từ
grafite (than chì). Do đó, điện cực X sẽ phải được làm bằng sắt (iron); điện cực Y sẽ phải được làm bằng grafite (than chì).
c) Với một quy mô sản xuất ở mức trung bình, người ta dùng cường độ dòng điện là 9000 A thì sau 8,0 giờ sản xuất
được 49,42 kg sodium, biết hiệu suất của cả quá trình đạt 80%. (Kết quả được làm tròn đến hàng phần trăm).
d) Hệ thống ống dẫn sodium và bình thu sodium nóng chảy luôn cần được đặt trong môi trường khí trơ, vì sodium có tính oxi hóa mạnh.
Câu 2. Hiện nay, pin lithium ion được sử dụng phổ biến trong nhiều thiết bị như điện thoại, laptop, xe điện,... do có ưu
điểm gọn nhẹ và có mật độ năng lượng cao. Xét một pin lithium ion có cathode làm từ LiMn2O4 và anode làm từ graphite.
Giữa các lớp của graphite có các nguyên tử xâm nhập tạo thành hợp chất ion có công thức dạng LixC6. Phản ứng tổng
cộng xảy ra trong pin khi phóng điện và khi nạp điện như sau: Li phãng ®iÖn
1 - xMn2O4 + LixC6 ⎯⎯⎯⎯ →
⎯⎯⎯⎯ Li1Mn2O4 + C6. n¹p ®iÖn
a) Khi pin phóng điện, ở anode xảy ra quá trình oxi hoá LixC6 thành xLi+ và C6.
b) Số oxi hoá của Mn trong Li1 - xMn2O4 thấp hơn trong Li1Mn2O4.
c) Nếu x = 0,24 thì khi phóng điện, 1 mol LixC6 cung cấp 0,04 mol electron.
d) Khi pin nạp điện, ở anode xảy ra quá trình khử LiMn2O4 thành Li1 - xMn2O4 và x Li+. Câu 3.
EpiGalloCatechin Gallate (EGCG) nổi bật với khả năng OH
chống oxi hóa, có vai trò quan trọng trong việc phòng ngừa OH
và hỗ trợ điều trị nhiều bệnh lý nghiêm trọng (một số loại
ung thư, tim mạch, loãng xương, …). Nhờ các đặc tính sinh O H O
học quý giá này, EGCG được ứng dụng rộng rãi trong sản OH
xuất thực phẩm chức năng và dược phẩm. EGCG có công thức như hình vẽ bên. O
a) EGCG có nhiều trong trà xanh, việc pha trà bằng nước OH
nóng là một ứng dụng của kỹ thuật chiết lỏng - rắn. OH
b) Phân tử EGCG có 4 loại nhóm chức. O
c) EGCG tác dụng tối đa với NaOH trong dung dịch theo tỉ
lệ mol tương ứng là 1 : 8. OH
d) Cho EGCG tác dụng với dung dịch NaOH dư, thu được OH
dung dịch X trong đó có ba chất tan.
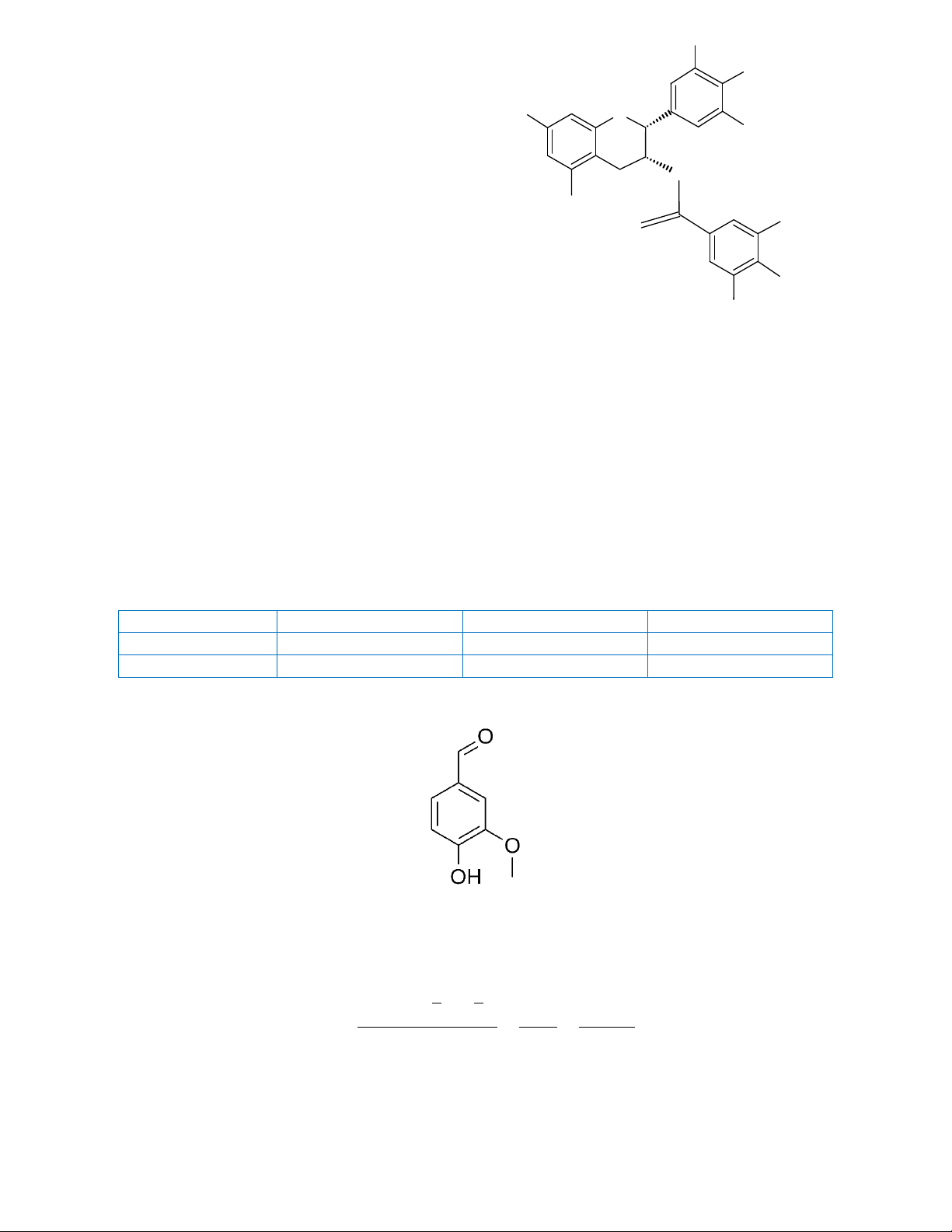
Câu 4. Vaniline là một dẫn xuất họ phenol – một trong những thành phần dùng để tạo hương vani trong thực phẩm. Một
nhóm học sinh được giao nhiệm vụ xác định độ tinh khiết của một loại vaniline thương mại bằng phương pháp chuẩn
độ acid – base. Nhóm học sinh tiến hành nghiên cứu và thấy rằng: khi chuẩn độ dung dịch chứa đồng thời NaOH và
muối của vaniline bằng chỉ thị thymolphthalein và methyl da cam thì khi dung dịch chuyển từ màu xanh sang màu vàng
thì coi như NaOH đã hết và khi dung dịch chuyển từ màu vàng sang màu đỏ thì muối của vaniline phản ứng vừa hết.
Nhóm học sinh đã tiến hành thí nghiệm như sau:
Bước 1: Cân 5,050 gam vaniline thương mại (dạng rắn) cho vào bình định mức 500 mL, hòa tan chất rắn bằng dung
dịch NaOH 0,100 M và định mức bằng dung dịch NaOH đến vạch định mức được dung dịch X.
Bước 2: Lấy dung dịch HCl 0,200 M cho vào burette và 20 mL dung dịch X cho vào cốc. Thêm hỗn hợp chỉ thị methyl
da cam và tiến hành chuẩn độ ở nhiệt độ 50 oC.
Bước 3: Nhỏ từ từ dung dịch HCl vào cốc đựng dung dịch X cho đến khi dung dịch chuyển từ màu xanh sang màu vàng
(ghi lại thể tích là V1) và khi dung dịch chuyển từ màu vàng sang màu đỏ (ghi lại thể tích là V2). Lặp lại thí nghiệm thêm
2 lần nữa. Kết quả của 3 lần chuẩn độ như sau: Thí nghiệm Lần 1 Lần 2 Lần 3 V1 (mL) 3,45 3,35 3,40 V2 (mL) 10,1 9,9 10,0
Trước khi tiến hành thí nghiệm, nhóm học sinh đưa ra giả thuyết rằng: “Dựa vào sự chênh lệch thể tích V2 với V1 có thể
xác định được hàm lượng vaniline trong mẫu”.
Cho công thức cấu tạo của Vaniline là:
a) Hàm lượng vaniline xác định được dựa vào phép chuẩn độ là khoảng 99,33%
b) Tại thời điểm dung dịch chuyển sang đỏ, thành phần chất tan chủ yếu của dung dịch là NaCl và muối sodium của vaniline.
c) Giả thuyết của nhóm học sinh là chính xác.
d) Biểu thức tính toán với hàm lượng vaniline trong thí nghiệm trên là 0, 200 (V − %m = V ) 500 152 2 1 100% vaniline 20 1000 5,0500
Câu 5. Để tiến hành mạ một tấm huy chương hình trụ, đáy tròn với bán kính 2,5 cm; chiều cao hình trụ 0,3 cm; với
lớp mạ bằng copper dày 0,1 cm. Người ta có thể tiến hành điện phân dung dịch CuSO4 0,5M, dư với cường độ dòng
điện không đổi 2A, khi kết thúc điện phân (quá trình mạ hoàn thành) thì hết thời gian là t giây. Biết khối lượng riêng
của copper là 8,95 g/cm³ và hiệu suất điện phân là 100%, giả thiết lớp mạ huy chương dày như nhau, toàn bộ lượng
copper tạo ra đều bám hết vào tấm huy chương. Cho hằng số Faraday F = 96500, π = 3,14.
a) Thanh copper là cực dương, huy chương được mạ sẽ đóng vai trò cực âm.
b) Khi kết thúc điện phân bên điện cực anode thoát ra 8,193 lít (đkc).
c) Chiều dòng electron di chuyển từ huân chương được mạ qua dây dẫn đến thanh copper.
d) Thời gian điện phân 64800 giây.
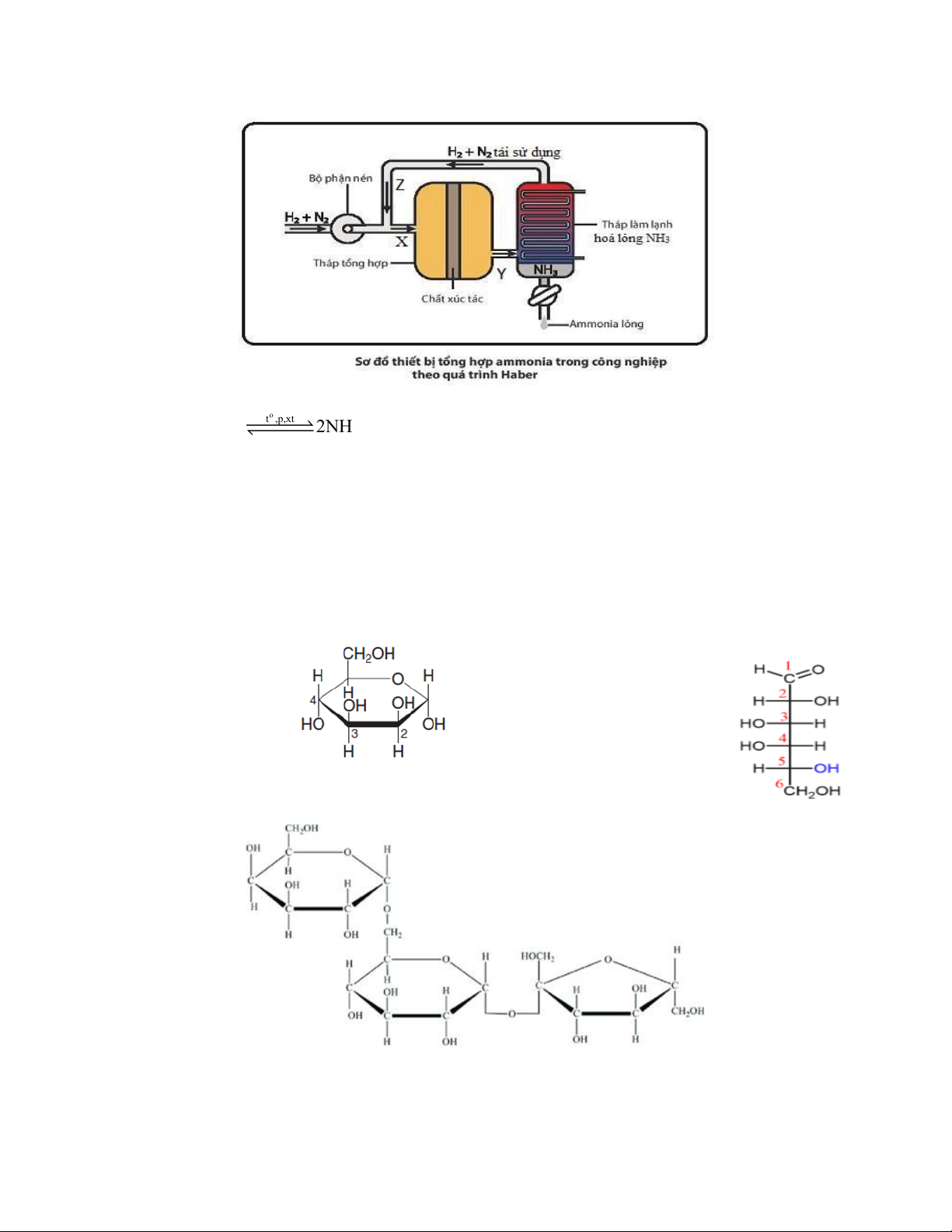
Câu 6. Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber theo dây chuyển sau:
Dòng khí chứa N2 và H2 tỉ lệ mol 1:3 được dẫn vào tháp tổng hợp với tốc độ khi đi qua điểm X là 800 mol/s tại đây xảy ra phản ứng: o t ,p,xt 0 N (g) + 3H (g) 2NH (g); Δ H = - 91,8 KJ (*) 2 2 3 r 298
a) Khi giảm áp suất của hệ phản ứng cân bằng (*) sẽ chuyển dịch theo chiều thuận.
b) Dòng khí đi qua điểm Y vào tháp làm lạnh sẽ có tốc độ nhỏ hơn 800 mol/s.
c) Nếu tốc độ dòng khí tái sử dụng khi đi qua điểm Z là 640 mol/s thì hiệu xuất của phản ứng (*) tại tháp tổng hợp là 40%.
d) Phản ứng (*) là phản ứng toả nhiệt.
Câu 7. Raffinose là trisaccharide xuất hiện trong nhiều loại thực vật, đặc biệt trong củ cải đường. Nó được cấu thành từ
ba đơn vị monosaccharide theo đúng thứ tự là α -galactose (vòng 6 cạnh); α -glucose (vòng 6 cạnh) và β -fructose (vòng
5 cạnh) bởi các liên kết −1,6 -glycoside và −1, 2 -glycoside.
a) Dạng vòng α - Galactose có công thức là
Cho biết cấu tạo mạch hở của galactose như sau
b) Raffinose có công thức cấu tạo là
c) Raffinose có không có tính khử như glucose.
d) Có thể dùng thuốc thử Tollens hoặc dung dịch Br2 để phân biệt dung dịch raffinose với dung dịch maltose.
Câu 8. Thủy phân hoàn toàn một hexapeptide M thu được Ala, Arg, Glu, Ile, Phe và Tyr. Các peptide E (chứa Tyr, Arg)
và G (chứa Arg, Glu, Tyr) được tạo thành trong số các sản phẩm thủy phân không hoàn toàn M. Dùng 2,4-
dinitrofluorobenzene xác định được amino acid đầu N là Ala. Thủy phân M nhờ tripsin thu được tripeptide A (chứa Phe,
Ala, Arg) và một chất B. Biết tripsin là enzyme đặc hiệu xúc tác cho phản ứng thủy phân liên kết peptide bằng cách tác
động lên đầu các nhóm carboxyl của các amino acid cơ bản như Lys và Arg.
a) Peptide G có cấu tạo là: Arg-Glu-Tyr.
b) Cấu tạo của M là: Ala-Phe-Arg-Tyr-Glu-Ile.
c) Khi cho M thủy phân hoàn toàn trong dung dịch môi trường acid (như HCl) hay môi trường base (như NaOH) thì sản
phẩm thu được đều là các α – amino acid.
d) Ở môi trường pH rất nhỏ, thì tất cả các α – amino acid ở trên đều tồn tại ở dạng cation.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Muối Mohr có công thức (NH4)2Fe(SO4)2.6H2O. Để xác định độ tinh khiết của một loại muối Mohr (cho rằng
trong muối Mohr chỉ có muối kép ngậm nước nêu trên và tạp chất trơ), một học sinh tiến hành các thí nghiệm sau: Cân
chính xác 7,237 gam muối Mohr, pha thành 100 mL dung dịch X. Lấy chính xác 10 mL dung dịch X, thêm 10 mL dung
dịch H2SO4 10%, được dung dịch Y. Chuẩn độ dung dịch Y bằng dung dịch chuẩn KMnO4 0,023M. Thực hiện chuẩn
độ 3 lần thu được kết quả như sau: Lần chuẩn độ 1 2 3
Thể tích dung dịch KMnO4 (mL) 16 16,1 16
Độ tinh khiết (% khối lượng (NH4)2Fe(SO4)2.6H2O) của muối Mohr có giá trị bằng bao nhiêu? (kết quả làm tròn đến hàng phần mười).
Câu 2. Sản xuất xà phòng từ mỡ lợn có tỉ lệ số mol là:
(C17H35COO)3C3H5:(C15H31COO)3C3H5: (C17H33COO)3C3H5) = 2 : 3: 5.
Dưới đây là bảng giá nguyên liệu và các chi phí: STT Nội dung Đơn giá 1 Mỡ lợn 32000/1kg 2 Dung dịch NaOH 40% 18000/1kg 3 Phụ gia + Chất độn 100000/1kg 4
Nhân công, máy móc, chi phí khác 3000/100 gam thành phẩm
Giả sử hiệu suất phản ứng đạt 80% (đối với cả 3 loại triester) và khối lượng muối của acid béo trong xà phòng thành
phẩm chiếm 70% về khối lượng, còn lại là chất phụ gia và chất độn. Giá tiền (làm tròn đến hàng đơn vị) của 1 bánh xà
phòng có khối lượng 90 gam mà nhà máy trên sản xuất là bao nhiêu (đồng)?
Câu 3. Cây xanh nhả khí oxygen sau khi hoàn tất quá trình quang hợp, con người và nhiều loài động vật khác cần khí
oxygen để duy trì sự sống. Phản ứng quang hợp được mô tả theo phương trình sau: ánh sáng nCO + mH O ⎯⎯⎯⎯ →C (H O) + nO 2 2 chlorophill n 2 m 2
Giả sử một cây xanh trưởng thành tiêu thụ lượng CO2 trung bình khoảng 22 kg/năm để thực hiện quá trình quang hợp
và trung bình một năm mỗi người cần tối thiểu 1,2 tấn oxygen để duy trì sự sống. Để cung cấp đủ lượng oxygen cho 8
tỉ người trên Trái đất trong một năm thì cần bao nhiêu tỉ cây xanh như trên?
Câu 4. Để mạ đồng một vật dụng kim loại có tổng diện tích bề mặt là 10 cm² (sau khi mạ), người ta tiến hành điện phân
dung dịch CuSO4 với cực âm là vật dụng cần mạ và cực dương là lá đồng thô. Biết cường độ dòng điện không đổi là 2A,
hiệu suất điện phân là 90%, khối lượng riêng của tinh thể Cu là 8,94 g/cm³. Thời gian điện phân để lớp mạ có độ dày
đồng nhất 0,1 mm là bao nhiêu phút? (Làm tròn kết quả đến hàng đơn vị).
Câu 5. Glutamic acid là một trong những amino acid thiết yếu. Bột ngọt (muối monosodium của glutamic acid) là một
loại gia vị, được sản xuất từ dung dịch NaOH 40% và tinh thể glutamic acid (chứa 80% khối lượng glutamic acid) bằng
cách dùng dung dịch NaOH trung hòa dung dịch glutamic acid đến pH = 6,8. Sau đó đem lọc, cô đặc và kết tinh dung
dịch sản phẩm bằng phương pháp sấy chân không ở nhiệt độ thấp. Bột ngọt thu được có độ tinh khiết 99%. Giả thiết
hiệu suất của cả quá trình tính theo glutamic acid là 90%. Để sản xuất được 1500 gói bột ngọt, mỗi gói có trọng lượng
1 kg cần m kg tinh thể glutamic acid. Giá trị của m là bao nhiêu? (kết quả làm tròn đến hàng đơn vị).
Câu 6. Cho các phát biểu sau:
(1) Ở điều kiện thường, methylamine là chất khí mùi khai khó chịu, độc, dễ tan trong nước.
(2) Ở điều kiện thường, alanine là chất lỏng ít tan trong nước.
(3) Dung dịch aniline làm đổi màu phenolphtalein.
(4) Khi nấu canh cua, hiện tượng riêu cua nổi lên trên là do sự đông tụ protein.
(5) Tripeptide Ala-Val-Gly có phản ứng màu biure.
(6) Các alkylamine đều tác dụng với nitrous acid ở nhiệt độ thường tạo thành alcohol và giải phóng khí nitrogen.
(7) Các arylamine được điều chế từ ammonia và dẫn xuất halogen.
Liệt kê số phát biểu đúng theo thứ tự tăng dần?



