
Preview text:
BÀI TẬP CÁC DẠNG ĐIỆN PHÂN VÀ PIN ĐIỆN HÓA DẠNG 1:
1. Nếu thế cực chuẩn của cực âm là 0.80 V và cực dương là -0.76 V thì suất điện
động chuẩn của pin Galvani là bao nhiêu?
2. Lắp ráp pin Fe-Sn ở điều kiện chuẩn. Tính sức điện động chuẩn của pin, biết rắng
thế 𝐸°𝐹𝑒2+/𝐹𝑒 = −0.44 𝑉, 𝐸° = −0.137 𝑉 𝑆𝑛2+ 𝑆𝑛
3. Cho pin điện hóa được tạo bởi hai cặp oxid hóa- khử Pb2+/Pb và Zn2+/Zn với thế
điện cực chuẩn lần lượt là -0.126 V, -0.762 V.
a. Xác định anode, cathode của pin
b. Viết quá trình xảy ra ở từng cực và phương trình hóa học xảy ra khi pin hoat động
c. Tính sức điện động chuẩn của pin
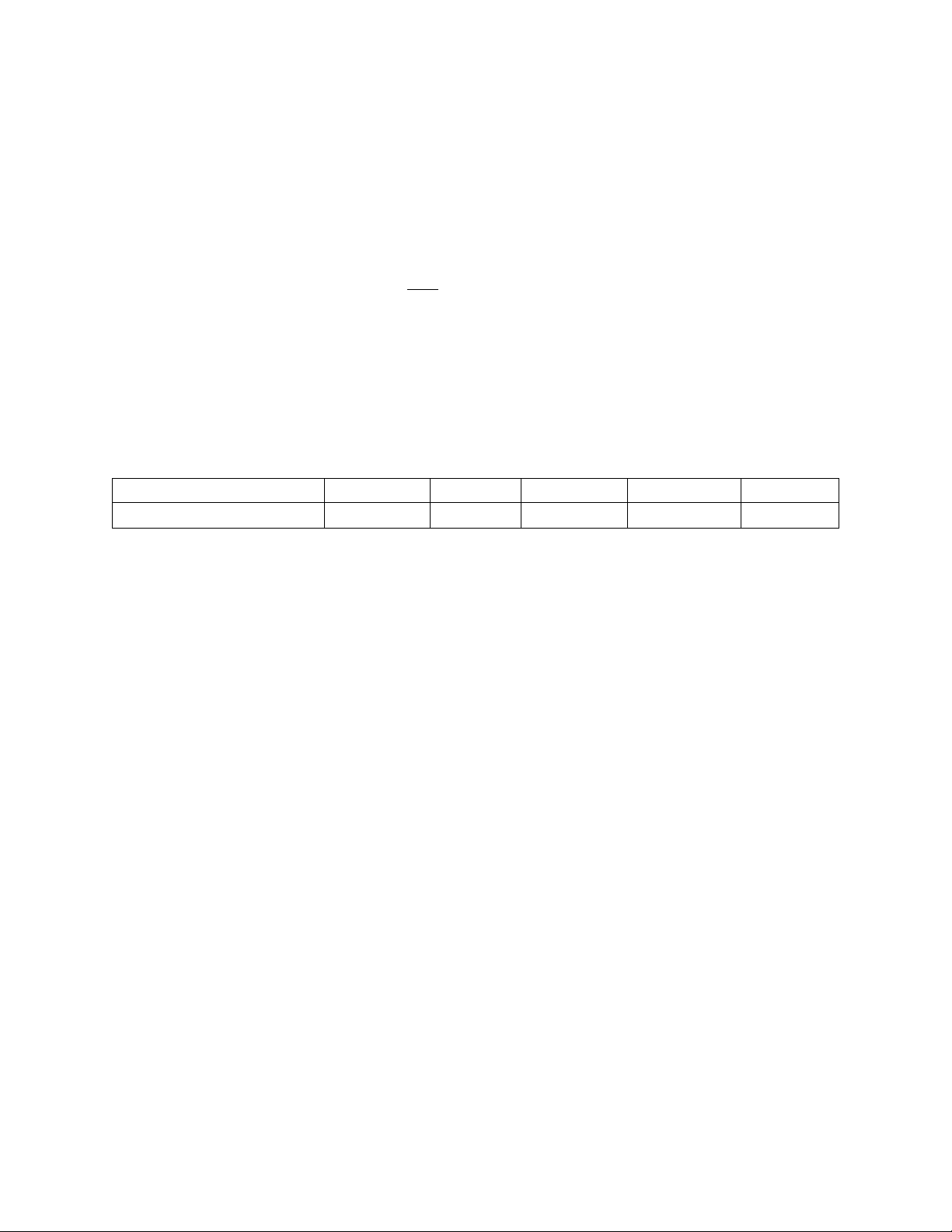
4. Một pin điện hóa được thiết lập bằng hai cặp oxid hóa- khử là M2+/M và Ag+/Ag. Cặp oxide hóa-khử Fe2+/Fe Ni2+/Ni Sn2+/Sn Cu2+/Cu Ag+/Ag E (V) -0.44 -0.257 -0.137 +0.340 +0.799
Nếu M là một trong dố các kim loại Fe, Ni, Sn, Cu thì sức điện động chuẩn lớn
nhất của Pin là bao nhiêu?
5. Cho Pin điện hóa Pb-Cu Epin= 0.47 (V), Pin Zn-Cu có Epin= 1.10 (V). thính Epin của Pin Zn-Pb. DẠNG 2:
1. Sức điện động chuẩn của một pin Galvani đước tạo bởi 2 cặp oxide hóa – khử là
2H+/H2 và Ag+/Ag.đo được bằng Volt kế có giá trị là 0.771 (V). Từ kết quẩ trên,
xác định thế điện cựa chuẩn của Ag+/Ag là bao nhiêu?
2. Biết Epin (Ni-Ag) =1.06 V, 𝐸°𝑁𝑖2+/𝑁𝑖 = −0.26 𝑉. Tính thế điện cực chuẩn của Ag+/Ag.
3. Cho Pin điện hóa Cu-Ag Epin= 0.46 (V), Pin Zn-Cu có Epin= 1.10 (V). Tính thế
điện cực chuẩn của Zn2+/Zn và Cu2+/Cu, biết rằng thế điện cực chuẩn của Ag+/Ag là +0.799 V DẠNG 3:
1. Cho 0.384 g kim loại M (hóa trị II) tác dụng với dung dịch AgNO3 dư, thu được
1.296 g Ag. Cho biết M là kim loại nào?
2. Cho m g bột Zn vào dung dịch CuSO4 dư, sau khi phản ứng hoàn toàn thu được 9.6 g Cu. Tìm giá trị m.
3. Cho 6 g Fe vào 100 ml dung dịch CuSO4 1M. Sau khi phản ứng hoàn toàn thu
được m g kim loại. Tìm giá trị m.
4. Nhúng một lá kim loại R (hóa trị II) có khối lượng 50 g vào 200 ml dung dịch
AgNO3 1M cho đến khi phản ứng xảy ra hoàn toàn. Lọc dung dịch thu được 18.8 g muối khan. Tẻn R là gì?
5. Cho 1.68 g bột Fe và 0.36 g bột Mg vào 375 ml dung dịch CuSO4, khuấy nhẹ đến
khi dung dịch mất màu xanh. Sau phản ứng thu được 2.82 g hỗn hợp kim loại. Xác
định nồng độ mol của dung dịch CuSO4 trước khi phản ứng.
6. Cho 0.42 g hỗn hớp Fe và Al vào 250 ml dụng dịch AgNO3 0.12 M. Sau phản ứng
thu được dung dịch X và 3.333 g chất rắn. Tìm khối lượng Fe trong hỗn hợp ban đầu.
7. Cho 2.24 g Fe vào 200 ml dung chứa AgNO3 0.1 M và Cu(NO3)2 0.5 M. Sau khi
phản ứng thu được m g chất rắn. Tìm giá trị m.
8. Cho 14 g Fe vào dung dịch X gồm AgNO3 0.5 M và Cu(NO3)2 x M. Sau khi phản
ứng kết thúc, thu được 30.4 g chất rắn Y. Tìm x DẠNG 4:
1. Điện phân dung dịch AgNO3 trong 10 phút với cường độ dòng điện là 5 A.
Khối lượng Ag thu được ở cathode là bao nhiêu?
2. Điện phân nóng chảy hoàn toàn 5.96 g MCln. thu được 0.04 mol Cl2. Kim loại M là?
3. Điện phân dung dịch chứa 0.1 mol CuSO4 với điện cực trơ. Khi anode có khí
thoát ra thì tại anode thu được x mol khí. Tìm x,
4. Điện phân V lít CuCl2 0.5 M với điện cực trơ. Khi dừng điện phân thu được
dung dịch X và 1.86 lít khí Cl2 duy nhất ở anode. Toàn bộ dung dịch X tác
dụng với 12.6 g Fe. Gía trị V là bao nhiêu?


