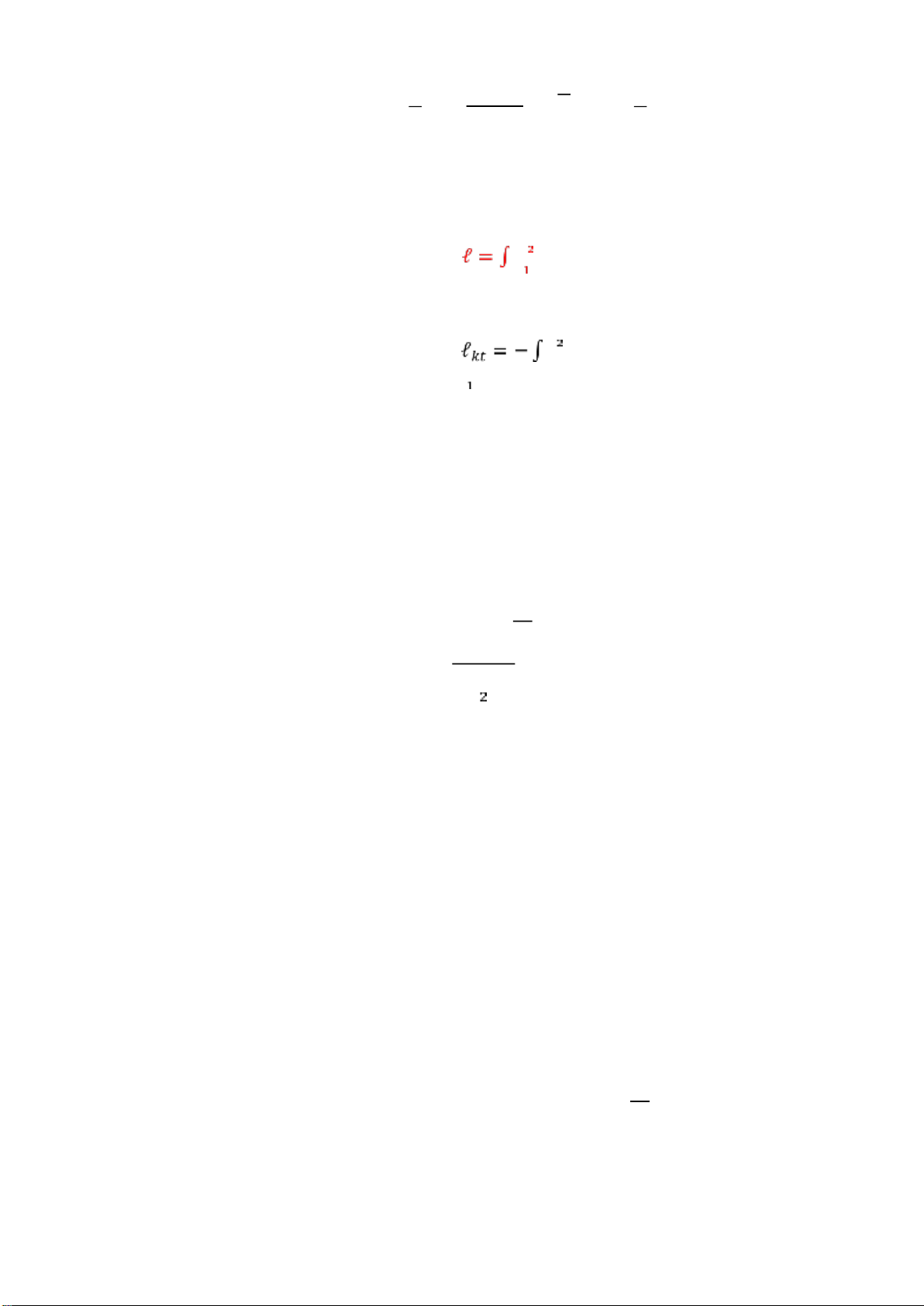



















Preview text:
lOMoARcPSD| 38841209
PHẦN I – NHIỆT ĐỘNG LỰC KỸ THUẬT
CHƯƠNG I – NHỮNG KHÁI NIỆM MỞ ĐẦU
1. Các thông số trạng thái a. Thể tích riêng 𝑉 3⁄𝑘𝑔) 𝜌 = (𝑚 𝐺 - Khối lượng riêng: 𝜌 = 𝐺 (𝑘𝑔3) 𝑉 𝑚 G: Khối lượng (kg) V: Thể tích (m3) b. Áp suất 𝑝 = 𝐹 𝑆
- Đơn vị Pascal, kí hiệu: Pa; 1𝑁 𝑚⁄ 2 = 1Pa 1𝑎𝑡 = 736 𝑚𝑚𝐻𝑔 = 9,81. 104 𝑁2 (1 at – mốt - phe) 𝑚 1𝑎𝑡𝑚 = 1,013. 10 5 𝑚𝑁2 𝑁 1𝑏𝑎𝑟 = 105
𝑚2 = 750 𝑚𝑚𝐻𝑔 c. Nhiệt ộ
𝑇(𝐾) = 273 + 𝑡( 0𝐶) t(0C)= (t0F - 32) d. Nội năng
- Ký hiệu U(J) hoặc u (J/kg).
- Độ biến thiên nội năng của khí lý tưởng:
𝑑𝑢 = 𝐶𝑉𝑑𝑇
∆𝑈 = 𝐺∆𝑢 = 𝐺𝐶𝑉(𝑇2 − 𝑇1)
𝐶𝑉: Nhiệt dung riêng ẳng tích. e. Entanpy
- Ký hiệu: I (J) hoặc i (J/kg). 𝑖 = 𝑢 + 𝑝𝑣 lOMoARcPSD| 38841209
- Độ biến thiên entapy của khí lý tưởng: 𝑑𝑖 = 𝐶𝑝dT;
∆𝐼 = 𝐺𝐶𝑃(𝑇2 − 𝑇1)
𝐶𝑝: Nhiệt dung riêng ẳng áp. f. Entropy
- Ký hiệu: S (𝐽 𝐾⁄ ) hoặc s (𝐽⁄𝐾𝑔. 𝐾) 𝑑𝑠 = 𝑑𝑞 (J/kgK) 𝑇
𝑑𝑆 = 𝐺𝑑𝑠 = 𝑑𝑄 (J/kg) 𝑇
- Độ biến thiên entropy: ∆𝑠 = 𝑠 𝑇𝑇 𝑑𝑞𝑇 2 ∆𝑆 = 𝑆 𝑇𝑇 𝑑𝑄𝑇 g. Execgy và anergie
- Ký hiệu: E (J) hoặc e (J/kg).
- Là phần năng lượng có thể biến ổi thành công của nhiệt trong quá trình thuận
nghịch và phần còn lại là Anergie (a). q= 𝑒 + 𝑎 e:
Execgy (J/kg). a: Anergie (J/kg).
e phụ thuộc vào nhiệt ộ của môi trường xung quanh, khi nhiệt ộ càng lớn thì e càng lớn. 𝑒 = (1 − 𝑇0)q 𝑇1
𝑒 = (𝑖 − 𝑖0) − 𝑇0(𝑠 − 𝑠0)
𝑖0, 𝑠0, 𝑇0: entapy, entropy, nhiệt ộ tuyệt ối của môi chất ở trạng thái cân bằng với môi trường.
i, s: entapy và entropy ở trạng thái ang xét.
2. Phương trình trạng thái của chất khí 𝑝𝑣 = 𝑅𝑇 𝑝𝑉 = 𝐺𝑅𝑇 𝑉 𝑉𝜇 𝑚3 𝑁
𝑣 = = : Thể tích riêng( ) p: Áp suất ( 2)
𝐺 𝜇 𝑘𝑔 𝑚 𝑅𝜇 𝐽 3) 𝑅 =
: Hằng số chất khí () V: Thể tích (𝑚 𝜇 𝐾𝑔𝐾
G: khối lượng chất khí (kg). lOMoARcPSD| 38841209
3. Hỗn hợp của khí lí tưởng
a. Các thành phần của hỗn hợp
- Thành phần khối lượng 𝑔𝑖 = 𝐺 𝐺𝑖
𝑔𝑖: Thành phần khối lượng của chất khí thứ i.
𝐺𝑖, G: Khối lượng của khí thành phần và của hỗn hợp (kg). - Thành phần thể tích 𝑟𝑖 = 𝑉𝑉𝑖
𝑟𝑖: Thành phần thể tích của chất khí thứ i.
𝑉𝑖, V: Thể tích của chất khí thứ I và của hỗn hợp (𝑚3). - Thành phần mol 𝑟𝑖 = 𝑚𝑚𝑖
𝑚𝑖, m: Số mol của chất khí thứ i và của hỗn hợp (𝑚3).
Thành phần mol bằng thành phần thể tích.
b. Xác ịnh các ại lượng của hỗn hợp khí - Số
mol 𝜇: 𝜇 = 𝑛𝑖=1 𝑟𝑖𝜇𝑖
𝜇 = 𝑔𝑖 𝜇𝑖 𝑅 ∑ =
- Hằng số chất khí của hỗn hợp: 𝜇 𝑖 𝑟𝑖𝜇𝑖
𝑅 = 𝑛𝑖 𝑔𝑖𝑅𝑖
𝑅𝑖: Hằng số chất khí của khí thành phần.
c. Xác ịnh áp suất của khí thành phần 𝑝𝑖
𝑝𝑖 = 𝑟𝑖𝑝 𝑝 = 𝑝𝑖
- p: Áp suất của hỗn hợp khí xác ịnh theo ịnh luật Danton: 𝑖
d. Quan hệ giữa các thành phần 𝑔𝑖 và 𝑟𝑖 𝑔𝑖
𝑟 𝜇 𝑟𝑖𝜇𝜇𝑖 𝑔𝑖 𝑟𝑖 = 𝑔𝑖 ∑ 𝜇𝑖 𝑖 𝜇𝑖 lOMoARcPSD| 38841209 BÀI TẬP
Bài 1.1: Thành phần thể tích của một hỗn hợp khí gồm 18% 𝑂2, 75% 𝑁2, 7% 𝐶𝑂2 ở áp
suất 0,5 MPa và nhiệt ộ 1070C. Với 5 kg khối lượng hỗn hợp hãy tính thành phần khối
lượng và phân áp suất của mỗi khí trong hỗn hợp khí.
Đáp số: 𝑟𝑂2 = = 0,18 𝑟𝑁2 = = 0,75 𝑟𝐶𝑂2 = = 0,07
𝑝𝑂2 = 0,18.0,5 = 0,09𝑀𝑝𝑎 𝑝𝑁2 = 0,75.0,5 = 0,375𝑀𝑝𝑎
𝑝𝑂2 = 0,07.0,5 = 0,35𝑀𝑝𝑎
Bài 1.2: Một hỗn hợp khí gồm 18 kg 𝐻2, 10 kg 𝑁2, 2 kg 𝐶𝑂2 chứa trong bình kín ở iều
kiện áp suất khí quyển. Tính thể tích và áp suất trong bình nếu nhiệt ộ trong bình ược
tăng lên 2 lần so với nhiệt ộ ầu, nhiệt ộ môi trường 270C. Đáp số: 𝑉 = 231,58 𝑚3 𝑝2 = 202,65 kPa
Bài 1.3: Một kg không khí khô có thành phần khối lượng 𝑔𝑁2 = 76,8%, 𝑔𝑂2 = 23,2%.
a. Xác ịnh thành phần thể tích 𝑟𝑂2, 𝑟𝑁2, hằng số khí R, phân tử lượng 𝜇 của hỗn hợp.
b. Tính phân áp suất của các chất khí biết áp suất hỗn hợp 𝑝 = 760 𝑚𝑚𝐻𝑔.
c. Tính thế tích riêng phần nếu biết nhiệt ộ hỗn hợp 𝑡 = 270𝐶. Đáp số: 𝑟𝑂2 = 21%; 𝑟𝑁2 = 79%;
𝜇 = 29 (𝑘𝑔⁄𝑘𝑚𝑜𝑙)
𝑝𝑁2 = 600 𝑚𝑚𝐻𝑔;
𝑝𝑂2 = 160 𝑚𝑚𝐻𝑔 𝑉𝑁2 = 0,674𝑚3; 𝑉𝑂2 = 0,179𝑚3;
Bài 1.4: Thành phần thể tích của sản phẩm cháy 𝑟𝐶𝑂2 = 12,3%, 𝑟𝑂2 = 7,2%, 𝑟𝑁2 =
80,5%. Xác ịnh khối lượng một kmol, hằng số chất khí, thể tích riêng và khối lượng
riêng của hỗn hợp ở áp suất 1 bar và nhiệt ộ 8000C. Đáp số:
𝜇 =30,3 (𝑘𝑔⁄𝑘𝑚𝑜𝑙); 𝑅 = 274 (𝐽⁄𝑘𝑔. 𝐾)
𝑣 = 2,94 (𝑚3⁄𝑘𝑔);
𝜌 = 0,34 (𝑘𝑔⁄𝑚3)
Bài 1.5: Một bình kín chứa 0,5 𝑚3không khí ở 𝑝1 = 2 𝑏𝑎𝑟, 𝑡1 = 200𝐶. Sau khi lấy một
ít, trong bình có ộ chân không 𝑝𝑐𝑘 = 420 𝑚𝑚𝐻𝑔 mà nhiệt ộ không ổi, biết áp suất khí
quyển 768 mmHg. Xác ịnh khối lượng trong bình trước và sau khi lấy ra, lượng khí ã
lấy. Biết không khí có 𝜇 = 29 𝑘𝑔⁄𝑘𝑚𝑜𝑙. Đáp số: 𝐺1 = 1,19 𝑘𝑔
𝐺2 = 0,28 𝑘𝑔 ∆𝐺 = 0,91 𝑘𝑔
Bài 1.6: Một bình có thể tích 0,625 m3 chứa O2 với p = 23 bar, nhiệt ộ 2800C. Hãy xác ịnh:
a. Khối lượng O2 trong bình. lOMoARcPSD| 38841209
b. Thể tích riêng, khối lượng riêng của O2 ở trạng thái ó và trạng thái tiêu chuẩn (p = 760 mmHg, t = 00C).
c. Tính thể tích O2 chứa trong bình quy ra iều kiện tiêu chuẩn. Đáp số:
𝐺 = 10 𝑘𝑔; 𝑣 = 0,0625 𝑚3⁄𝑘𝑔; 𝜌 = 16 𝑘𝑔⁄𝑚3
𝑣0 = 0,7 𝑚3⁄𝑘𝑔; 𝜌0 = 1,43 𝑘𝑔⁄𝑚3; 𝑉0 = 7 𝑚3𝑡𝑐
Bài 1.7: Xác ịnh thể tích riêng, khối lượng riêng của khí N2, ở iều kiện tiêu chuẩn và iều
kiện áp suất dư 0,2 at, nhiệt ộ 1270C. Biết áp suất khí quyển 760 mmHg. Đáp số: 𝑣0 = 0,8 𝑚3⁄𝑘𝑔 𝜌0 = 1,25 𝑘𝑔⁄𝑚3 𝑣 = 0,98 𝑚3⁄𝑘𝑔 𝜌 = 1,02 𝑘𝑔⁄𝑚3
Bài 1.8: Một bình có thể tích 200 ℓ, chứa 0,2 kg khí N2, áp suất khí quyển là 1 bar:
a. Nếu nhiệt ộ trong bình là 70C, xác ịnh chỉ số áp kế gắn trên nắp bình.
b. Nếu nhiệt ộ trong bình là 1270C, xác ịnh chỉ số áp kế gắn trên nắp bình. Đáp số:
a. 𝑝𝑐𝑘 = 0,1686 𝑏𝑎𝑟
b. 𝑝𝑐𝑘 = 1,1877 𝑏𝑎𝑟
Bài 1.9: Một bình kín chứa không khí có thể tích không ổi 2 m3 áp suất ban ầu p1 = 30
bar, nhiệt ộ t1 = 270C. Sau khi lấy một ít ra khỏi bình ể sử dụng, áp suất trong bình còn
12 bar, nhiệt ộ không ổi. Cho biết không khí 𝜇 = 29 𝑘𝑔⁄𝑘𝑚𝑜𝑙. Hãy xác ịnh khối lượng
không khí ã lấy ra, thể tích riêng không khí trong bình trước và sau khi lấy ra sử dụng. Đáp số: 𝐺1 = 70𝑘𝑔 𝐺2 = 28 𝑘𝑔 Δ𝐺 = 42 𝑘𝑔
𝑣1 = 0,0298 𝑚3⁄𝑘𝑔
𝑣2 = 0,0714 𝑚3⁄𝑘𝑔
Bài 1.10: Một bình chứa hỗn hợp khí có thể tích 𝑉 = 1,23 𝑚3, 𝑝1 = 5 𝑏𝑎𝑟, 𝑡1 = 180𝐶.
Thành phần thể tích của các chất khí như sau: H2 là 46%, CH4 là 32 %, của CO là 15%
và N2 là 7%. Sau khi sử dụng áp suất trong bình còn p2 = 3,2 bar, nhiệt ộ t2 = 120C. Hỏi
khối lượng của 1 kmol hỗn hợp 𝜇, hằng số chất khí R, khối lượng hỗn hợp ban ầu, còn
lại và lượng ã ẩy ra.
Đáp số: 𝜇 = 12,2 𝑘𝑔⁄𝑘𝑚𝑜𝑙
𝑅 = 681 𝐽⁄𝑘𝑔. 𝐾)
𝐺1 = 3,10𝑘𝑔 𝐺2 = 2,03 𝑘𝑔 Δ𝐺 = 1,07 𝑘𝑔 lOMoARcPSD| 38841209
CHƯƠNG II – NĂNG LƯỢNG VÀ CÁC ĐỊNH LUẬT NHIỆT ĐỘNG
TÓM TẮT LÝ THUYẾT 1. Nhiệt và công
- Ký hiệu: Nhiệt: Q (J) hoặc q (J/kg). Công: L (J) hoặc ℓ = 𝐿 ( 𝐽 ). 𝐺 𝑘𝑔
- Nhiệt lượng và công không phải là hàm của trạng thái mà là hàm của quá trình. - Quy ước:
Q > 0, L > 0: môi chất nhận nhiệt, nhận công
Q < 0, L < 0: môi chất nhả nhiệt, sinh công
2. Nhiệt dung riêng của chất khí -
Nhiệt dung riêng khối lượng: C ( 𝐽 ) 𝐾𝑔𝐾
- Nhiệt dung riêng thể tích tiêu chuẩn: 𝐶′ ( 𝐽 3 ) 𝑚 𝑡𝑐𝐾 -
Nhiệt dung riêng mol 𝐶𝜇 ((
𝑘𝑚𝑜𝑙𝐾𝐽 ) Quan hệ
giữa các loại nhiệt dung:
𝐶 = 𝑣𝑡𝑐𝐶′ = 𝜇 1 . 𝐶𝜇
- Nhiệt dung riêng ẳng áp (Cp, Cp′, Cμp).
- Nhiệt dung riêng ẳng tích (CV, CV′, CμV).
- Quá trình thay ổi trạng thái của chất môi giới là quá trình a biến thì có nhiệt dung a biến Cn, Cn′, Cμn.
- Quan hệ giữa 𝐶𝑝 , 𝐶𝑉 và nhiệt dung a biến 𝐶𝑛 𝐶𝑝 − 𝐶𝑉 = 𝑅
k = 𝐶𝑝: Chỉ số oạn nhiệt (số mũ oạn nhiệt) 𝐶𝑉
𝐶𝑉 = 𝑘−1𝑅 và 𝐶𝑉 = 𝑘−1 𝑘.𝑅
𝐶𝑛 = 𝐶𝑝 𝑘(𝑛−1)𝑛−𝑘 và 𝐶𝑛 = 𝐶𝑣 𝑛−𝑘𝑛−1
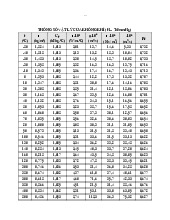
- Với khí thực, nhiệt dung riêng phụ thuộc vào nhiệt ộ nên ta có khái niệm nhiệt
dung riêng trung bình. Nhiệt dung riêng trung bình từ 00C ến t0C ược ký hiệu 𝑡
𝐶|0 và cho trong các bảng ở phần phụ lục. Nhiệt dung riêng trung bình từ t1 ến
𝑡2 t2 ký hiệu 𝐶|𝑡1 hay 𝐶𝑡𝑏, ược xác ịnh bằng công thức: lOMoARcPSD| 38841209 𝑡2 1 𝑡2 𝑡1 𝐶|𝑡1 =
[𝑡2. 𝐶|0 − 𝑡1𝐶|0 ] 𝑡2 − 𝑡1 3. Các loại công
- Công thay ổi thể tích (công giãn nở): 𝑑ℓ = 𝑝𝑑v; 𝑉𝑉
𝑝𝑑𝑣 - Công kỹ thuật:
𝑑ℓ𝑘𝑡 = −𝑣𝑑𝑝; 𝑉𝑉 𝑣𝑑𝑝 - Công lưu ộng:
𝑑ℓ𝑙đ = 𝑑(𝑝𝑣) 𝑝𝑑𝑣 = 𝑑ℓ𝑙đ + 𝑑ℓ𝑘𝑡
- Công ngoài: 𝑑ℓ𝑛 = 𝑑ℓ − 𝑑 (𝜔22) − 𝑔𝑑ℎ − 𝑑ℓ𝑙𝑑 Đối với hệ kín:
𝑑ℓ𝑛 = 𝑑ℓ = 𝑝𝑑𝑣 Đối với hệ hở:
𝑑ℓ𝑛 = −𝑣𝑑𝑝 − 𝑑 (𝜔22) − 𝑔𝑑ℎ 2 − 𝜔 1
ℓ𝑛 = ℓ𝑘𝑡 − 𝜔 2 2 − 𝑔(ℎ2 − ℎ1)
4. Định luật I nhiệt ộng - Dạng tổng quát:
𝑄 = ∆𝑊 + 𝐿𝑛 Q:
Nhiệt lượng cung cấp cho hệ.
∆𝑊: Độ biến thiên năng lượng của hệ.
𝐿𝑛: Công hệ sinh ra môi trường. - Đối với 1 kg môi chất: 𝑞 = ∆𝑤 + ℓ𝑛
- Phương trình ịnh luật nhiệt ộng I viết cho hệ kín:
𝑑𝑞 = 𝑑𝑢 + 𝑝𝑑𝑣
𝑑𝑞 = 𝑑𝑖 + 𝑑ℓ𝑘𝑡 𝑞 = ∆𝑢 + ℓ 𝑞 = ∆𝑖 + ℓ𝑘𝑡
- Phương trình ịnh luật nhiệt ộng I viết cho hệ hở: d𝑞 = 𝑑𝑖 + 𝑑ℓ
𝑑𝑞 = 𝑑𝑖 + 𝑑( 𝜔2) (lưu ộng) 2 𝑞 = ∆𝑖 + ℓ𝑘𝑡 lOMoARcPSD| 38841209
5. Các quá trình nhiệt ộng cơ bản của khí lý tưởng - Độ biến thiên nội năng:
𝑑𝑢 = 𝐶𝑣𝑑𝑇; ∆𝑢 = 𝐶𝑣(𝑇2 − 𝑇1); ∆𝑈 = 𝐺𝐶𝑣(𝑇2 − 𝑇1) - Độ biến thiên entanpy:
𝑑𝑖 = 𝐶𝑝𝑑𝑇; ∆𝑖 = 𝐶𝑝(𝑇2 − 𝑇1); ∆𝐼 = 𝐺𝐶𝑝(𝑇2 − 𝑇1) -
Phương trình ịnh luật nhiệt ộng I viết cho hệ kín:
𝑑𝑞 = 𝑑𝑢 + 𝑝𝑑𝑣 𝑑𝑞 = 𝑑𝑖 + 𝑑ℓ𝑘𝑡 𝑞 = ∆𝑢 + ℓ 𝑞 = ∆𝑖 + ℓ𝑘𝑡 - Quá trình ẳng tích:
𝑣2 = 𝑣1; 𝑝𝑝12 = 𝑇𝑇12; ℓ = 0 ; ℓ𝑘𝑡 = 𝑣(𝑝1 − 𝑝2);
𝑞 = 𝐶𝑣(𝑇2 − 𝑇1);
∆𝑠 = 𝐶𝑣𝑙𝑛 𝑇𝑇21 𝛼 = 1 - Quá trình ẳng áp:
𝑝2 = 𝑝1; 𝑣𝑣21 = 𝑇𝑇21 ℓ = 𝑝(𝑣2 − 𝑣1); ℓ𝑘𝑡 = 0
𝑞 = 𝐶𝑝(𝑇2 − 𝑇1);
∆𝑠 = 𝐶𝑝𝑙𝑛 𝑇𝑇21 𝛼 = 1 𝑘 - Quá trình ẳng nhiệt: 𝑇2 = 𝑇1; 𝑝𝑝21 = 𝑣𝑣12
ℓ = 𝑅𝑇𝑙𝑛 𝑣𝑣21 = ℓ𝑘𝑡
𝑞 = 𝑙 = 𝑙𝑘𝑡 = 𝑅𝑇𝑙𝑛 𝑣𝑣21
∆𝑠 = 𝑅𝑙𝑛 𝑣𝑣21 𝛼 = 0
- Quá trình oạn nhiệt: 𝑝𝑣𝑘 = 𝑐𝑜𝑛𝑠𝑡 𝑇1 = (𝑣2)𝑘−1 = (𝑝1)𝑘−1 𝑘 𝑇2 𝑣1 𝑝2
ℓ = −∆𝑢 = 𝐶𝑣(𝑇1 − 𝑇2)
ℓ𝑘𝑡 = −∆𝑖 = 𝐶𝑝(𝑇1 − 𝑇2) = 𝑘. 𝑙 𝑞 = 0 ∆𝑠 = 0 lOMoARcPSD| 38841209 - Quá trình a biến:
Chỉ số a biến: 𝑛 = 𝐶 𝑛−𝐶𝑝
𝑛 = 𝑞 (1 − 𝑘) + 𝑘 𝐶𝑛−𝐶𝑣 ℓ
𝑝𝑣𝑛 = 𝑐𝑜𝑛𝑠𝑡
𝑇1 = (𝑣2)𝑛−1 = (𝑝1) 𝑛−1𝑛 𝑇2 𝑣1 𝑝2 1 − 𝑘 𝑅 ℓ = 𝐶𝑣 (𝑇2 − 𝑇1) = (𝑇1 − 𝑇2) 𝑛 − 1 𝑛 − 1 ℓ𝑘𝑡 = 𝑛. 𝑙
𝑞 = 𝐶𝑛(𝑇2 − 𝑇1)
∆𝑠 = 𝐶𝑛𝑙𝑛 𝑇𝑇21 𝛼 = 𝑛−1 𝑛−𝑘
6. Hiệu suất của chu trình thuận chiều
𝜂𝑡 = 𝑞 ℓ1 = 1 − |𝑞𝑞12|
𝑞1: Nhiệt môi chất nhận từ nguồn nóng.
𝑞2: Nhiệt môi chất nhả cho nguồn lạnh.
ℓ: Công do môi chất thực hiện trong chu trình.
7. Hiệu suất của chu trình Carno thuận chiều 𝜂𝐶 = 1 − 𝑇𝑇21
𝑇1: Nhiệt ộ nguồn nóng. 𝑇2: Nhiệt ộ nguồn nóng.
8. Hệ số của chu trình ngược chiều 𝑞2 𝑞2 𝜀 = =
|ℓ| |𝑞1| − 𝑞2 𝑞2:
Nhiệt lượng môi chất nhận từ nguồn lạnh.
𝑞1: Nhiệt lượng môi chất nhận từ nguồn nóng. 9. Hệ số
của chu trình Carno ngược chiều 𝑇2 𝜀 = 𝑇1 − 𝑇2
10. Định luật nhiệt ộng II 𝑑𝑞 𝑑𝑆 ≥ lOMoARcPSD| 38841209 𝑇
11. Nguyên lý tăng entropy của hệ cô lập ∆𝑆 ≥ 0 BÀI TẬP
Bài 2.1: Xác ịnh nhiệt dung riêng ẳng áp và ẳng tích trung bình của nitơ trong khoảng
nhiệt ộ 2000C ến 8000C. Biết nhiệt dung riêng trung bình tử 00C ến t của nitơ như sau:
𝐶𝑝𝑡𝑏 = 1,024 + 0,00008855t 𝑘𝐽 𝑘𝑔. 𝐾⁄
𝐶𝑣𝑡𝑏 = 0,7272 + 0,00008855t 𝑘𝐽 𝑘𝑔. 𝐾⁄
Đáp số: 𝐶𝑝𝑡𝑏|20080000𝐶𝐶 == 1,113 𝑘𝐽 𝑘𝑔. 𝐾⁄; 𝐶𝑣𝑡𝑏|20080000𝐶𝐶 = 0,8158 𝑘𝐽 𝑘𝑔. 𝐾⁄
Bài 2.2: Xác ịnh nhiệt dung a biến của khí 𝐻2 khi thực hiện quá trình a biến n = 1,5.
Đáp số: 𝐶𝑛 = 0,5 𝑘𝑐𝑎𝑙 𝑘𝑚𝑜𝑙. 𝐾⁄ ,
Bài 2.3: Dòng không khí lưu lượng 𝐺 = 1,5 𝑘𝑔⁄𝑠 chuyển ộng qua một oạn ống (lưu
ộng). Cung cấp nhiệt lượng 𝑄 = 152 𝑘𝑊. Xác ịnh biến thiên entapi ∆𝐼 và tốc ộ ầu ra
của dòng môi chất khi bỏ qua tốc ộ ầu vào, biết ộ chênh lệch nhiệt ộ của môi chất ∆𝑇 =
100𝐾. Biết 𝜇 = 29 𝑘𝑔, 𝑘 = 1,4. Đáp số:
∆𝐼 = 150675 (J); 𝜔2 = 42 (𝑚 𝑠⁄ )
Bài 2.4: Một bình kín thể tích 0,12 m3 chứa O2 áp suất p1 = 10 bar, nhiệt ộ t1 = 500C.
Gia nhiệt ể nhiệt ộ tăng lên t2 = 1500C.
a. Xác ịnh khối lượng O2 trong bình, áp suất p2.
b. Tính ∆𝑈, ∆𝐼, ∆𝑆, 𝑄, 𝐿, 𝐿𝑘𝑡.
Đáp số: a. 𝐺1 = 1,43 (𝑘𝑔)
b. ∆𝑈 = 92875 (𝐽); ∆𝐼 = 130036 (𝐽); 𝐿 = 0
𝐿𝑘𝑡 = −37180 (𝐽); ∆𝑆 = 251 (𝐽/𝐾)
Bài 2.5: 10 kg không khí ở nhiệt ộ 270C ược ốt nóng ở áp suất không ổi ến 1270C. Xác
ịnh nhiệt lượng, ộ biến thiên entanpi, ộ biến thiên nội năng, công thay ổi thể tích của quá
trình ốt nóng. Cho biết không khí 𝜇 = 29 𝑘𝑔⁄𝑘𝑚𝑜𝑙.
Đáp số: 𝑄 = 1010 (𝑘𝐽) ∆𝐼 = 1010 (𝑘𝐽) ∆𝑈 = 720 (𝑘𝐽)
L = 290 (𝑘𝐽)
Bài 2.6: Người ta ốt nóng 1 kg không khí trong iều kiện áp suất không ổi p =2 bar từ
nhiệt ộ 200C ến nhiệt ộ 1100C. Tính thể tích cuối, nhiệt lượng, công thay ổi thể tích, ộ
biến thiên nội năng và ộ biến thiên entropy. lOMoARcPSD| 38841209
Đáp số: 𝑣2 = 0,549 (𝑚3⁄𝑘𝑔); 𝑞 = 20,9 (𝑘𝐽 𝑘𝑔⁄ ); ℓ = 25,8 (𝑘𝐽 𝑘𝑔⁄)
∆𝑢 = 64,8 (𝑘𝐽); ∆𝑠 = 0,27 (𝑘𝐽 𝑘𝑔. 𝐾⁄ )
Bài 2.7: Xy lanh có ường kính d = 400 mm chứa không khí có thể tích 0,08 m3, áp suất
3,06 at, nhiệt ộ 150C. Nếu không khí nhận nhiệt lượng trong iều kiện pittông chưa kịp
dịch chuyển và nhiệt ộ không khí tăng ến 1270C. Xác ịnh lực tác dụng lên pittông, khối
lượng không khí có trong xi lanh, nhiệt lượng cung cấp, ộ biến thiên entropy.
Đáp số: 𝐹 = 8,877. 105(𝑁) 𝐺1 = 29 𝑘𝑔 𝑄 = 79,97 (𝑘𝐽)
∆𝑆 = 0,177 (𝑘𝐽/𝐾)
Bài 2.8: Có 12 kg không khí ở nhiệt ộ 𝑇1 = 270C, áp suất tuyệt ối 𝑝1 = 6 𝑏𝑎𝑟 giãn nở
ẳng nhiệt ể thể tích tăng 4 lần. Cho biết không khí 𝜇 = 29 𝑘𝑔⁄𝑘𝑚𝑜𝑙.
a. Biểu diễn quá trình trên giản ồ p – v và T – S.
b. Xác ịnh các thông số trạng thái cuối.
c. Xác ịnh Q, ∆𝐼, ∆𝑈, 𝐿𝑘𝑡, ∆𝑆.
Đáp số: 𝑎. 𝑣2 = 0,574 (𝑚3⁄𝑘𝑔); 𝑇2 = 300𝐾; 𝑝2 = 1,5 𝑏𝑎𝑟
b. 𝑄 = 𝐿 = 𝐿𝑘𝑡 = 1432319 (𝐽)
∆𝐼 = ∆𝑈 = 0; ∆𝑆 = 4774 𝐽 𝐾⁄
Bài 2.9: Khi nén ẳng nhiệt 4 kg chất khí (coi là khí lý tưởng) có hằng số chất khí
𝑅 = 189 (𝐽⁄𝑘𝑔. 𝐾) từ áp suất 2 at ến 5,4 at, cần thải nhiệt lượng 378 kJ. Xác ịnh nhiệt
ộ của quá trình, thể tích ầu và cuối của chất khí ó.
Đáp số: 𝑇 = 500 (𝐾); 𝑉1 = 1,93 (𝑚3); 𝑉2 = 0,72 (𝑚3)
Bài 2.10: Không khí có thể tích 2,48 m3, nhiệt ộ 150C, áp suất p = 1 bar, khi bị nén oạn
nhiệt, không khí nhận công thay ổi thể tích là 471 kJ. Xác ịnh nhiệt ộ cuối, ộ biến thiên
nội năng và ộ biến thiên entanpy.
Đáp số: 𝑇2 = 2330𝐶; ∆𝑈 = −𝐿12 = 471 (𝑘𝐽); ∆𝐼 = 661(𝑘𝐽
Bài 2.11: Xác ịnh ộ biến thiên entanpy và ộ biến thiên entropy của quá trình giãn nở oạn
nhiệt của không khí từ 𝑝1 = 3 𝑀𝑝𝑎; 𝑉1 = 0,05 𝑚3 ến 𝑉2 = 0,3 𝑚3.
Đáp số: ∆𝑆 = 0; ∆𝐼 = 268,8 𝑘𝐽
Bài 2.12: 2 kg khí O2 thực hiện quá trình a biến với số mũ a biến n = 1,2 từ nhiệt ộ 270C
ến 5370C. Xác ịnh ộ biến thiên nội năng, ộ biến thiên entropy, nhiệt lượng, công thay ổi
thể tích và công kỹ thuật của quá trình.
Đáp số: ∆𝑆 = −1,3 (𝑘𝐽/𝐾)
𝑄 = −663 (𝑘𝐽); ∆𝑈 = 663 (𝑘𝐽)
𝐿 = −1326 (𝑘𝐽); 𝐿𝑘𝑡 = −1591 (𝑘𝐽) lOMoARcPSD| 38841209
Bài 2.13: 3 kg không khí áp suất 1,5 bar, nhiệt ộ 770C ở trạng thái 1 ược nén a biến ến
trạng thái 2 áp suất 7,5 bar, hệ số a biến n = 1,2. Sau ó nén ẳng áp ến trạng thái 3 rồi giãn
ẳng nhiệt về trạng thái 1. Vẽ chu trình trên giản ồ p – v. Xác ịnh công và nhiệt của chu
trình ó. 𝜇 = 29 𝑘𝑔⁄𝑘𝑚𝑜𝑙
Đáp số: 𝐿 = −71,31 𝑘𝐽; 𝑄 = 71,31 𝑘𝐽
Bài 2.14: Chu trình Carnot thuận chiều dùng 1 kg không khí ược tiến hành trong phạm
vi 𝑇𝑚𝑎𝑥 = 900 𝐾 và 𝑇𝑚𝑖𝑛 = 300 𝐾, 𝑝𝑚𝑎𝑥 = 60 𝑏𝑎𝑟, 𝑝𝑚𝑖𝑛 = 1 𝑏𝑎𝑟.
a. Biểu thị quá trình trên ồ thị p – v và T – s.
b. Xác ịnh các thông số cơ bản tại các iểm nút.
c. Xác ịnh: 𝑞1 và 𝑞2.
d. Xác ịnh công chu trình và hiệu suất.
Đáp số: b. Điểm a: 𝑝𝑎 = 60 𝑏𝑎𝑟, 𝑇𝑎 = 900 𝐾; 𝑣𝑎 = 0,043 (𝑚3⁄𝑘𝑔)
Điểm b: 𝑝𝑏 = 46,8 𝑏𝑎𝑟, 𝑇𝑏 = 900 𝐾; 𝑣𝑏 = 0,055 (𝑚3⁄𝑘𝑔)
Điểm c: 𝑝𝑐 = 1 𝑏𝑎𝑟, 𝑇𝑐 = 300 𝐾; 𝑣𝑐 = 0,861 (𝑚3⁄𝑘𝑔)
Điểm d: 𝑝𝑑 = 1,283 𝑏𝑎𝑟, 𝑇𝑑 = 300 𝐾; 𝑣𝑑 = 0,67 (𝑚3⁄𝑘𝑔)
c. 𝑞1 = 63502 (𝐽) 𝑞2 = −21560 (𝐽)
d. 𝜂 = 66,7% → |ℓ| = 42356 𝐽 Bài 2.15: Cho nhiệt dung riêng thực của một chất khí
𝐶 = 1,02344 + 0,00000548. 𝑡 𝑘𝐽 𝑘𝑔. 𝐾⁄ . Xác ịnh nhiệt dung riêng trung bình chất khí
ó trong khoảng từ 400 ÷ 16000𝐶. Đáp số:
𝐶𝑡𝑏|1600400= 1,078 𝑘𝐽 𝑘𝑔. 𝐾⁄
Bài 2.16: Đốt nóng 2 kg khí O2 trong iều kiện áp suất không ổi 𝑝 = 5 𝑏𝑎𝑟 từ nhiệt ộ t1 = 270C ến t2 = 1270C.
a. Biểu diễn quá trình trên giản ồ p – v và T – S.
b. Xác ịnh thể tích của O2 ở trạng thái ầu và cuối.
c. Xác ịnh Q, ∆𝐼, ∆𝑈, 𝐿𝑘𝑡, 𝐿. Đáp số:
𝑉1 = 0,312 𝑚3; 𝑉2 = 0,416 𝑚3
Q = ∆𝐼 = 182000 𝐽; ∆𝑈 = 130000 𝐽;
𝐿𝑘𝑡 = 0, 𝐿 = 52000 𝐽
Bài 2.17: 10 kg khí O2 ở nhiệt ộ 5270C ược làm lạnh ẳng áp ến 270C. Tính ộ biến thiên
entropy và nhiệt lượng tỏa ra. Đáp số:
∆𝑆 = −9,095 𝑘𝐽 𝑘𝑔. 𝐾⁄ 𝑄 = 4578 𝑘𝐽 lOMoARcPSD| 38841209
Bài 2.18: Xác inh công kỹ thuật quá trình ẳng nhiệt của 2,9 kg không khí ở nhiệt ộ
1270C, áp suất từ 1 bar ến 2,7 bar. Đáp số:
ℓ𝑘𝑡 = −332,6. 103 (𝐽)
Bài 2.19: Khảo sát 0,6 kg hỗn hợp 2 khí lý tưởng N2 và CO2 chứa trong một hệ thống
pittông xylanh. Ở trạng thái ban ầu hỗn hợp có 𝑝1 = 2 𝑏𝑎𝑟, 𝑉1 = 0,3 𝑚3. Sau ó người ta
nén oạn nhiệt hỗn hợp này ến trạng thái 2 có 𝑝2 = 5 𝑏𝑎𝑟; V2 = 0,15364 m3. Hãy xác ịnh:
a. Số mũ oạn nhiệt của quá trình.
b. Công trao ổi của quá trình. Nhận xét.
c. Khối lượng của từng khí chứa trong hỗn hợp.
d. Nhiệt ộ của hỗn hợp ở trạng thái 1 và 2.
Đáp số: a. 𝑘 = 1,4 b. 𝐿12 = −45,5 𝑘𝐽
c. 𝐺𝑁2 = 0,43 𝑘𝑔 𝐺𝐶𝑂2 = 0,17 𝑘𝑔 d. 𝑇1 = 1030C, T2 = 2080C
Bài 2.20: Nén a biến 1 kg không khí n = 1,2 từ t1 = 200C, p1 = 0,981 bar ến p2 = 7,845 bar.
a. Biểu diễn quá trình trên ồ thị p – v và T – S.
b. Xác ịnh các thông số trạng thái ở trạng thái cuối.
c. Xác ịnh Q, ∆𝐼, ∆𝑈, 𝐿𝑘𝑡, 𝐿.
Đáp số: 𝑣2 = 0,15 (𝑚3⁄𝑘𝑔); 𝑇2 = 4140𝐶; 𝑄 = 0;
∆𝑆 = 0; 𝐿 = −∆𝑈 411845 𝐽;
𝐿𝑘𝑡 = −∆𝐼 = 576583 𝐽
Bài 2.21: 1kg không khí thực hiện chu trình ngược chiều trong phạm vi nhiệt ộ tmax =
2500C, tmin = 300C và pmax = 10 bar, pmin = 1,2 bar.
a. Biểu diễn chu trình trên giản ồ p – v.
b. Xác ịnh nhiệt lượng q1, q2 và công ℓ.
c. Xác ịnh hệ số làm lạnh 𝜀 và hệ số nhiệt 𝜑 của chu trình.
Đáp số: 𝑞1 = −32,3 𝑘𝐽 𝑘𝑔⁄ ; 𝑞2 = 18,6 𝑘𝐽 𝑘𝑔⁄
ℓ = −13,7 𝑘𝐽 𝑘𝑔⁄ ; 𝜀 = 1,36; 𝜑 = 2,36
Bài 2.22: Xác ịnh hiệu suất của chu trình Carnot thuận chiều khi biết nhiệt ộ nguồn nóng
𝑡1 = 9270𝐶, nhiệt ộ nguồn lạnh 270𝐶. Xác ịnh hệ số làm lạnh của chu trình Carnot ngược
chiều biết nhiệt ộ nguồn nóng t1 =370C và nguồn lạnh là t2 = -30C. Đáp số: 𝜂𝐶 = 0,75 𝜀𝐶 = 6,75 lOMoARcPSD| 38841209
CHƯƠNG III – MÔI CHẤT VÀ CÁC QUÁ TRÌNH NHIỆT ĐỘNG
1. Các quá trình nhiệt ộng cơ bản của khí thực - Độ biến thiên nội năng:
∆𝑢 = 𝑢2 − 𝑢1 = (𝑖2 − 𝑝2𝑣2) − (𝑖1 − 𝑝1𝑣1) - Độ biến thiên entanpy: ∆𝑖 = 𝑖2 − 𝑖1
- Độ biến thiên entropy:
∆𝑠 = 𝑠2 − 𝑠1 - Độ khô: 𝑥 = 𝐺ℎ 𝐺𝑛+𝐺ℎ
- Thông số trạng thái của hơi bão hòa ẩm thông qua ộ khô: Nội năng:
𝑢𝑥 = 𝑢′ + 𝑥(𝑢′′ − 𝑢′) Entanpy:
𝑖𝑥 = 𝑖′ + 𝑥(𝑖′′ − 𝑖′) = 𝑖′ + 𝑥. 𝑟 Entropy:
𝑠𝑥 = 𝑠′ + 𝑥(𝑠′′ − 𝑠′) = 𝑠′ + 𝑟.𝑥 𝑇𝑠
Thể tích riêng: 𝑣𝑥 = 𝑣′ + 𝑥(𝑣′′ − 𝑣′)
- Các thông số ở các trạng thái nước sôi, hơi bão hòa khô ược xác ịnh trong bảng
phụ lục 3 và 4; còn nước chưa sôi và hơi quá nhiệt ược xác ịnh trong bảng bảng phụ
lục 5 hoặc theo ồ thị i-s, T-s. 2. Các quá trình nhiệt ộng cơ bản của khí thực - Quá trình ẳng tích:
ℓ = 0, ℓ𝑘𝑡 = 𝑣(𝑝1 − 𝑝2)
𝑞 = Δ𝑢 = 𝑢2 − 𝑢1 = (𝑖2 − 𝑖1) − 𝑣(𝑝2 − 𝑝1) - Quá trình ẳng áp:
ℓ = 𝑝(𝑣2 − 𝑣1), ℓ𝑘𝑡 = 0
𝑞 = Δ𝑖 = 𝑖2 − 𝑖1 - Quá trình ẳng nhiệt: 𝑞 = 𝑇(𝑠2 − 𝑠1)
ℓ = 𝑞 − Δ𝑢 = 𝑞 − (𝑢2 − 𝑢1)
ℓ𝑘𝑡 = 𝑞 − ∆𝑖 = 𝑞 − (𝑖2 − 𝑖1) - Quá trình oạn nhiệt:
𝑠2 = 𝑠1 = 𝑐𝑜𝑛𝑠𝑡 𝑞 = 0
ℓ = −∆𝑢 = 𝑢1 − 𝑢2 lOMoARcPSD| 38841209
ℓ𝑘𝑡 = −Δ𝑖 = 𝑖1 − 𝑖2
3. Quá trình lưu ộng của khí và hơi - Phương trình liên tục: 𝐺
= 𝜔. 𝜌. 𝑓 = 𝑐𝑜𝑛𝑠𝑡 hay 𝑓𝜔 = 𝑐𝑜𝑛𝑠𝑡 𝑣
G: Lưu lượng khối lượng (𝑘𝑔⁄𝑠) ω:
Vận tốc của dòng (𝑚 𝑠⁄ )
𝑓: Diện tích tiết diện ngang của dòng tại nơi khảo sát (m2)
𝜌: Khối lượng riêng của môi chất (𝑘𝑔⁄𝑚3) - Tốc ộ âm thanh: 𝑎 = √ 𝑘 𝑘 𝑝𝑣 𝑅𝑇 = S √ ố Mach: 𝑀 = 𝜔 𝑎⁄
- Các công thức cơ bản về lưu ộng
- Quan hệ giữa tốc ộ dòng khí và áp suất
𝜔𝑑𝜔 = −𝑣𝑑𝑝
Từ ó khái niệm: ống tăng tốc trong ó tốc ộ tăng, áp suất giảm, ống tăng áp trong o áp
suất tăng, tốc ộ giảm.
- Quan hệ giữa tốc ộ và hình dáng ống 𝑑𝑓 2 − 1). 𝑑𝜔 = (𝑀 𝑓 𝜔 -
Ống tăng tốc nhỏ dần: M <1 - Ống tăng tốc lớn dần: M >1, -
Ống tăng tốc hỗn hợp Laval:
+ Ống tăng áp hỗn hợp (khi vào ống M >1, khi ra M <1).
+ Ống tăng tốc hỗn hợp (khi vào dòng khí có M < 1, khi ra M >1). -
Các thông số của ống tăng tốc nhỏ dần - Vận tốc ầu ra của ống: 2 𝑘 𝑘−1 o Với khí lý tưởng: 2 𝜔 = [1 √ − (𝛽 𝑅𝑇 ) 𝑘 ] 𝑝2 𝑘−1 1 𝛽 = : Tỷ số áp suất 𝑝1 o Với hơi nước: -
Khi vận tốc ạt tới hạn: 𝜔𝑐 = 𝑎𝑐 lOMoARcPSD| 38841209 𝑘−1 √ 2 𝑘 2 𝑝 𝑘 ) = √ 𝑅𝑇
Với khí lý tưởng: 𝜔 1 𝑣 1 (1− 𝛽 𝑐 1 = √ 𝑐 = 𝑘−1 𝑘+1 𝑘𝑝𝑐𝑣𝑐 Với hơi nước: -
Tỷ số áp suất tới hạn: 2 𝑘 = ( 𝛽𝑐 𝑘+1)𝑘−1
Khí ơn nguyên tử:: 𝛽𝑐 = 0,484
Khí 2 nguyên tử: 𝛽𝑐 = 0,528
Khí 3 nguyên tử: 𝛽𝑐 = 0,546 Hơi
nước quá nhiệt: 𝛽𝑐 = 0,55 - Áp suất tới hạn: pc = βp1 -
Lưu lượng dòng khí G = f2ω2 (kg/s) v2 - Lưu lượng cực ại:
Với ống tăng tốc nhỏ dần: 𝑘+1 f c 2 G = 𝑣𝑐 = fc. p (𝑘+1 ) (kg/s) -
Các thông số của ống tăng tốc hỗn hợp Laval - Diện tích tiết diện nhỏ nhất của ống:
Đối với dòng hơi nước: 𝑓𝑚𝑖𝑛 𝐺.𝑣 Đối với khí lí tưởng: 𝑓𝑚𝑖𝑛 𝐺𝑣 𝐺 -
Diện tích tiết diện cửa ra:
Đối với hơi nước: 𝑓 𝐺.𝑣
Đối với khí lí tưởng: 𝑓 = 2 = 𝐺𝑣 𝐺 (𝑚2) 𝜔 2 2 𝑘+1 √ 2 𝑘 ( 𝛽 𝑘 𝑘 −𝛽 ) 𝑘−1 . 𝑝 1 𝑣 1 lOMoARcPSD| 38841209
Hoặc 𝑓 = 𝑓𝑚𝑖𝑛. 𝜔𝜔
𝑣𝑣𝑐 - Chiều dài của phần ống có tiết diện lớn dần:
ℓ = 𝑑2−𝑑𝑚𝑖𝑛𝛼 2𝑡𝑎𝑛 2
𝛼: góc loe của ống lớn dần, 𝛼 = 8 ÷ 12.
4. Quá trình tiết lưu của khí và hơi
a. Tính chất của quá trình tiết lưu - Quá trình oạn nhiệt
- Entropi tang: s2 > s1
- Tốc ộ dòng khí không ổi
- Áp suất giảm: 𝑝2 < 𝑝1
- Entanpy trước và sau tiết lưu không ổi: 𝑖2 = 𝑖1
- Nhiệt ộ khí lý tưởng không ổi: 𝑇2 = 𝑇1
- Nhiệt ộ khí thực giảm (𝑇1 < 𝑇𝑐𝑏: Nhiệt độ chuyển biến)
- Nhiệt ộ chuyển biến: 𝑇𝑐𝑏 = 6,75 𝑇𝑘 b. Ứng dụng lOMoARcPSD| 38841209 -
Quá trình tiết lưu ược ứng dụng trong máy lạnh như van tiết lưu nhiệt (giảm áp
suất và có iều chỉnh năng suất lạnh), ống mao dẫn (chỉ áp suất giảm) và trong
tuốc bin ể iều chỉnh công suất của tuốc bin.
5. Quá trình nén khí
a. Máy nén pittông 1 cấp lý tưởng và thực
- Công tiêu thụ của máy nén một cấp lý tưởng hoặc thực khi:
o Quá trình nén là ẳng nhiệt: 𝑝1
𝑙𝑘𝑡 = 𝑅𝑇 ln 𝑝2.
o Quá trình nén là oạn nhiệt: 𝑘 𝑘 𝑘 𝑘 ℓ𝑘𝑡 = 𝑘−1
𝑝1𝑣1 (𝛽𝑘−1 − 1) =
𝑘−1 𝑅𝑇1(𝛽𝑘−1 − 1).
o Quá trình nén là a biến, với số mũ a biến n: 𝑛 𝑛 𝑛 𝑛 ℓ𝑘𝑡 = 𝑛−1
𝑝1𝑣1 (𝛽𝑛−1 − 1) = 𝑛−1
𝑅𝑇1(𝛽𝑛−1 − 1).
- Nhiệt môi chất nhận ược trong các quá trình nén a biến: 𝑛 − 𝑘 𝑛−1
𝑞 = 𝐶𝑛(𝑇2 − 𝑇1) =
𝐶𝑉. 𝑇1 [(𝛽) 𝑛 − 1] 𝑛 − 1
- Nhiệt môi chất xả ra trong quá trình làm mát: 𝑛−1 𝑞𝑙𝑚 = 𝐶𝑝(𝑇2 − 𝑇1) = 𝐶𝑝. 𝑇1 [(𝛽) 𝑛 − 1]
b. Máy nén pittông nhiều cấp
- Tổng công nén của các cấp; 𝑚 𝑛𝑛−1 ℓ𝑘𝑡 = 𝑅𝑇 [𝑚 − 𝜋𝑖
𝑛 − 1 Với: 𝜋 = 𝛽 =
𝑝𝑖+1: Tỷ số áp suất của cuối và ầu của quá trình nén. 𝑝𝑖
T; nhiệt ộ ầu các cấp nén. m: số cấp nén.
- Để công tiêu tốn cực tiểu thì tỉ số nén mỗi cấp là giống nhau: 𝑝𝑚𝑎𝑥
1 = 𝜋 2 = ⋯=𝜋 𝑚 = √ 𝜋 = 𝜋 𝑝𝑚𝑖𝑛 lOMoARcPSD| 38841209 - 𝑇 { 2𝑚
o Công tiêu tốn: 𝑙 = 𝑚. 𝑛 𝑅𝑇 𝑛−1 . 𝑛−1 6. Không khí ẩm
a. Tính chất của không khí ẩm
- Không khí ẩm là hỗn hợp của không khí khô và hơi nước.
- Vì phân áp của hơi nước trong không khí ẩm rất nhỏ nên hơi nước ở ây có thể coi là khí lý tưởng.
Áp suất của không khí ẩm: p (áp suất khí quyển) là tổng của phân áp suất không
khí khô 𝑝𝑘 và hơi nước 𝑝ℎ: 𝑝 = 𝑝 + 𝑝𝑘
- Nhiệt ộ của không khí ẩm t bằng nhiệt ộ của không khí khô 𝑡𝑘 và bằng nhiệt ộ của hơi nước 𝑡ℎ: 𝑡 = 𝑡ℎ = 𝑡𝑘
- Thể tích của không khí ẩm V bằng thể tích của không khí khô 𝑉𝑘 bằng thể tích của hơi nước 𝑉ℎ: 𝑉 = 𝑉ℎ = 𝑉𝑘
- Khối lượng của không khí ẩm là G bằng khối lượng của không khí khô 𝐺𝑘 và hơi nước 𝐺ℎ: 𝐺 = 𝐺ℎ + 𝐺𝑘 -
Phương trình trạng thái ối với không khí khô:
𝑝𝑘𝑉 = 𝐺𝑘𝑅𝑘𝑇 với 𝑅𝑘 = 287 𝐽⁄𝑘𝑔. 𝐾 -
Phương trình trạng thái ối với hơi nước:
𝑝ℎ𝑉 = 𝐺ℎ𝑅ℎ𝑇 với 𝑅ℎ = = 462 𝐽⁄𝑘𝑔. 𝐾
b. Các thông số vật lý của không khí ẩm - Độ ẩm tuyệt ối: 𝜌ℎ = 𝐺𝑉ℎ kg/m3
- Độ ẩm tương ối (𝜑 (%)) 𝜑 = 𝜌ℎ . 100% 𝜌𝑚𝑎𝑥 𝜑 = 𝑝ℎ . 100% 𝑝𝑚𝑎𝑥 lOMoARcPSD| 38841209 -
𝜌ℎ: Độ ẩm tuyệt ối của không khí ẩm chưa bão hòa.
𝜌𝑚𝑎𝑥: Độ ẩm tuyệt ối của không khí ẩm bão hòa.
𝑝ℎ: Phân áp suất của hơi nước trong không khí ẩm chưa bão hòa. 𝑝𝑚𝑎𝑥:
Phân áp suất của hơi nước trong không khí ẩm bão hòa.
- Dung ẩm ( ộ chứa hơi) (d): 𝑑 = 𝐺ℎ = 0,622.
𝑝ℎ , kg/kg không khí khô. 𝐺𝑘 𝑝−𝑝𝑘
o Độ chứa hơi trong không khí ẩm bão hòa là ộ chứa hơi lớn nhất: 𝑝ℎ𝑚𝑎𝑥 𝑑𝑚𝑎𝑥 = 0,622. 𝑝 − 𝑝ℎ𝑚𝑎𝑥
o Liên hệ giữa dung ẩm và ộ ẩm tương ối: 0,622.𝜑.𝑝 𝜑 = 𝑑.𝑝ℎ↔ 𝑑 = 𝑚𝑎𝑥. (0,622+𝑑)𝑝𝑚𝑎𝑥 𝑝−𝜑.𝑝𝑚𝑎𝑥
Entanpy của không khí ẩm:
𝑖 = 1,005. 𝑡 + 𝑑(2500,9 + 1,83. 𝑡)
- Nhiệt ộ bão hòa oạn nhiệt 𝜏: Khi không khí tiếp xúc với nước, nếu sự bay hơi của
nước vào không khí chỉ do nhiệt lượng của không khí truyền cho, thì nhiệt ộ của
không khí bão hòa gọi là nhiệt ộ bão hòa oạn nhiệt
ư (nhiệt ộ nhiệt kế ướt).
- Nhiệt ộ ọng sương 𝑡𝑠: Nhiệt ộ ọng sương 𝑡𝑠 hay là iểm sương là nhiệt ộ tại ó
không khí chưa bão hòa trở thành không khí ẩm bão hòa trong iều kiện phân áp
suất của hơi nước không ổi 𝑝ℎ = 𝑐𝑜𝑛𝑠𝑡
- Nhiệt ộ nhiệt kế ướt 𝑡ư là nhiệt ộ o bằng nhiệt kế ướt (nhiệt kế có bọc vải ướt bên ngoài).
Khi 𝜑 = 100%: 𝑡𝑠 = 𝑡ư
Khi 𝜑 < 100%: 𝑡𝑠< 𝑡ư
7. Đồ thị i – d của không khí ẩm
- Đường d = const là ường thẳng ứng.
- Đường i = const là ường thẳng nghiêng xuống với góc nghiêng 135°.
- Đường t = const là ường thẳng chếch lên phía trên, gần như song song với nhau. lOMoARcPSD| 38841209 -
- Đường φ = const trong cùng không khí ẩm chưa bão hòa ở nhiệt ộ t < 𝑡𝑠(p) là
ường cong lồi, trong vùng nhiệt ộ t > 𝑡𝑠(p) là ường thẳng i lên.
- Đường φ = 100% chia ồ thị thành hai vùng phía trên là không khí ẩm chưa bão
hòa, vùng phía dưới là không khí ẩm quá bão hòa.
- Đường phân áp suất hơi nước 𝑝ℎ = 𝑓(𝑑), 𝑑 = 0,622. 𝑝−𝑝
𝑝ℎℎlà ường thẳng xiên.
𝑝ℎ tra cứu trên trục // i và nằm bên phải i –d. 8. Quá trình sấy
- Quá sấy là quá trình làm khô vật muốn sấy. Môi chất dùng ể sấy là không khí.
Có thể chia quá trình sấy thành 2 giai oạn:
+ Giai oạn ốt nóng không khí 1-2: d = const, 𝜑 ↓, nhiệt ộ không khí tăng.
+ Giai oạn 2 – 3: I = const (quá trình oạn nhiệt).
- Lượng không khí ẩm cần ể làm bay hơi 1 kg nước trong vật sấy: 1 + 𝑑 𝐺 = 𝑑3 − 𝑑1
- Nhiệt lượng cần ể bay hơi 1 kg hơi nước trong vật sấy: 𝐼 𝐺 = 𝑑3 − 𝑑1 BÀI TẬP lOMoARcPSD| 38841209
Bài 3.1: Xác ịnh các thông số: entanpy, thể tích riêng, nội năng của 1 kg hơi nước và
300 kg/h hơi nước ở áp suất p = 10 bar, ộ khô x = 0,9.
Đáp số: 𝑖𝑥 = 2576,5 𝑘𝐽 𝑘𝑔⁄ , 𝑣𝑥 = 0,17525 𝑚3⁄𝑘𝑔, 𝑢𝑥 = 2400 𝑘𝐽 𝑘𝑔⁄ .
𝐼𝑥 = 215 kW, 𝑉𝑥 = 2400 𝑘𝐽 𝑘𝑔,⁄ 𝑈𝑥 = 200 𝑘𝑊.
Bài 3.2: 1kg hơi nước ở áp suất 20 bar, ộ khô x = 0,85 tiến hành quá trình ẳng áp ến nhiệt ộ 3000C.
a. Biểu diễn quá trình trên ồ thị p – v, T –s và i – s.
b. Bằng bảng và ồ thị xác ịnh các thông số v, i, s, u ở trạng thái ầu và cuối.
c. Xác ịnh ∆𝑢, ∆𝑖, ∆𝑠, q, ℓ, ℓ𝑘𝑡.
a. Biểu diễn quá trình trên ồ thị p – v, T –s và i – s.
Đáp số: b. 𝑖1 = 2515 𝑘𝐽 𝑘𝑔⁄ ; 𝑣1 = 0,085 𝑚3⁄𝑘𝑔; 𝑠1 = 5,576 𝑘𝐽 𝑘𝑔. 𝐾⁄
𝑢1 = 2345 𝑘𝐽 𝑘𝑔⁄ ; 𝑣2 = 0,1255 𝑚3⁄𝑘𝑔; 𝑠2 = 6,757 𝑘𝐽 𝑘𝑔. 𝐾⁄
𝑖2 = 3019 𝑘𝐽 𝑘𝑔⁄ ; 𝑢2 = 2768 𝑘𝐽 𝑘𝑔⁄
c. ∆𝑢 = 423 𝑘𝐽/𝑘𝑔; ∆𝑖 = 504 𝑘𝐽 𝑘𝑔⁄ = 𝑞; ∆𝑠 = 1,181 𝑘𝐽 𝑘𝑔. 𝐾⁄ ℓ = 81 𝑘𝐽/kg
Bài 3.3: 1 kg hơi bão hòa khô có áp suất tuyệt ối 0,15 bar tiến hành quá trình ẳng tích ến nhiệt ộ 1600C.
a. Biểu diễn quá trình trên ồ thị p – v, T – s, i – s.
b. Xác ịnh các thông số ầu và cuối.
c. Xác ịnh ∆𝑢, ∆𝑖, ∆𝑠, q, ℓ, ℓ𝑘𝑡.
a. Biểu diễn quá trình trên ồ thị p – v, T – s, i – s.
b. Xác ịnh các thông số ầu cuối.
Đáp số: b. 𝑣1 = 10,02 𝑚3⁄𝑘𝑔; 𝑠1 = 8,007 𝑘𝐽 𝑘𝑔. 𝐾⁄ ; 𝑖1 = 2599 𝑘𝐽 𝑘𝑔⁄ u1 = 2449 kJ kg⁄
; 𝑣1 = 𝑣2 = 10,02 𝑚3⁄𝑘𝑔 𝑝2 ≈ 0,2 𝑏𝑎𝑟
𝑠2 = 8,406𝑘𝐽 𝑘𝑔. 𝐾⁄ ; 𝑖2 = 2801 𝑘𝐽 𝑘𝑔⁄ ; u2 = 2601 kJ kg⁄
∆𝑢 = 152 𝑘𝐽/𝑘𝑔; ∆𝑖 = 202 𝑘𝐽 𝑘𝑔⁄ ; ∆𝑠 = 0,4 𝑘𝐽 𝑘𝑔. 𝐾⁄ ; ℓ = 0 𝑘𝐽/𝑘𝑔
ℓ𝑘𝑡 = −50 𝑘𝐽 𝑘𝑔⁄
Bài 3.4: Giãn nở ẳng nhiệt hơi nước từ áp suất 10 bar nhiệt ộ 3000C ến áp suất 1 bar.
a. Biểu diễn quá trình trên ồ thị p – v, T – s, i – s.
b. Xác ịnh các thông số ầu và cuối. lOMoARcPSD| 38841209
c. Xác ịnh ∆𝑢, ∆𝑖, ∆𝑠, q, ℓ, ℓ𝑘𝑡.
Đáp số: b. 𝑣1 = 0,2578. 𝑚3⁄𝑘𝑔, 𝑠1 = 7,116𝑘𝐽 𝑘𝑔. 𝐾⁄ ; 𝑖1 = 3058 𝑘𝐽 𝑘𝑔⁄ u1 = 2800 kJ kg⁄
; 𝑣2 = 2,638 𝑚3⁄𝑘𝑔, 𝑠2 = 8,211 𝑘𝐽 𝑘𝑔. 𝐾⁄ ; 𝑖2 = 3074 𝑘𝐽 𝑘𝑔⁄ u2 = 2810 kJ kg⁄ ;
c. ∆𝑢 = 10 𝑘𝐽; ∆𝑖 = 16 𝑘𝐽 𝑘𝑔⁄ ; ∆𝑠 = 1,095 𝑘𝐽 𝑘𝑔. 𝐾⁄ ; 𝑞 = 627,4 (𝐽); 𝑘𝑔
ℓ = 617,4 𝑘𝐽 𝑘𝑔⁄ ; ℓ𝑘𝑡 = 𝑞 − Δ𝑖 = 611,4 𝑘𝐽 𝑘𝑔⁄
Bài 3.5: Giãn nở oạn nhiệt 1 kg hơi nước từ áp suất 10 bar, nhiệt ộ 3000C ến áp suất 0,2 bar.
a. Biểu diễn quá trình trên ồ thị p – v, T – s, i – s.
b. Xác ịnh các thông số ầu và cuối.
c. Xác ịnh ∆𝑢, ∆𝑖, ∆𝑠, q, ℓ, ℓ𝑘𝑡.
Đáp số: b. 𝑣1 = 0,2578 𝑚3⁄𝑘𝑔, 𝑠1 = 7,116𝑘𝐽 𝑘𝑔. 𝐾⁄
; 𝑖1 = 3058 𝑘𝐽 𝑘𝑔⁄
u1 = 2800 kJ kg⁄ ; 𝑥 = 0,89
𝑖2 = 2350 𝑘𝐽 𝑘𝑔⁄ ;
𝑣2 = 6,806 𝑚3⁄𝑘𝑔; u2 = 2214 kJ kg⁄
c. ∆𝑢 = −586 𝑘𝐽/𝑘𝑔; ∆𝑖 = 708 𝑘𝐽 𝑘𝑔⁄ ; ∆𝑠 = 0
𝑞 = 0 ; ℓ = 𝑞586𝑘𝐽/𝑘𝑔; ℓ𝑘𝑡 = −708 𝑘𝐽 𝑘𝑔⁄
Bài 3.6: Khí O2 áp suất 60 bar, nhiệt ộ 1000C lưu ộng qua ống tăng tốc nhỏ dần vào môi
trường có áp suất 36 bar. Hãy xác ịnh tốc ộ và lưu lượng của dòng O2, cho biết diện tích
mặt cắt cửa ra của ống bằng 20 mm2. Đáp số:
𝜔2 = 304(𝑚 𝑠⁄ ); 𝐺 = 0,258 𝑘𝑔/𝑠
Bài 3.7: Hơi nước ở áp suất 22 bar, ộ khô 0,95 lưu ộng qua ống tăng tốc nhỏ dần vào
môi trường có áp suất 1 bar. Xác ịnh tốc ộ tại cửa ra của ống và lưu lượng hơi qua ống
nếu biết tiết diện cửa ra của ống là 0,001 m2. Đáp số:
𝜔2 = 𝜔𝑐 = 489 𝑚/𝑠;
𝐺𝑚𝑎𝑥 = 2,445 𝑘𝑔
Bài 3.8: Không khí từ bể chứa có áp suất 𝑝1 = 100 𝑏𝑎𝑟, nhiệt ộ 𝑡1 = 150𝐶 chảy ra
ngoài trời ống có ường kính bằng 10 mm. Xác ịnh tốc ộ và lưu lượng của không khí
nếu biết áp suất khí quyển bằng 1 bar.
Đáp số: 𝑣𝑐 = 0,0131 𝑚3/kg; Gmax = 1,86 kg/s
Bài 3.9: Hơi nước quá nhiệt ở áp suất và nhiệt ộ ban ầu 𝑝1 = 30 𝑏𝑎𝑟, 𝑡1 = 4500𝐶 giãn
nở oạn nhiệt trong ống tăng tốc nhỏ dần vào môi trường trong hai trường hợp có áp suất lOMoARcPSD| 38841209
khác nhau. Xác ịnh tốc ộ hơi tại cửa ra của ống và lưu lượng hơi trong hai trường hợp
nếu biết tiết diện tại cửa ống 𝑓2 = 30 𝑐𝑚2. a. 𝑝2 = 18 𝑏𝑎𝑟 b. 𝑝2 = 10 𝑏𝑎𝑟
Đáp số:a. 𝜔2 = 559 𝑚 𝑠⁄ ; 𝐺 = 10,48 𝑘𝑔⁄𝑠
b. 𝜔2 = 616 𝑚 𝑠⁄ ; 𝐺 = 10,87 𝑘𝑔⁄𝑠
Bài 3.10: Không khí có áp suất 𝑝1 = 10 𝑎𝑡, nhiệt ộ 𝑡1 = 3000𝐶 phun vào môi trường có
𝑝2 = 1 𝑏𝑎𝑟 qua ống tăng tốc Laval. Biết lưu lượng không khí 𝐺 = 4 𝑘𝑔⁄𝑠. Xác ịnh lưu
lượng và kích thước cơ bản của ống nếu chọn gốc ống loe là 100.
Đáp số: 𝑑𝑚𝑖𝑛 = 5,5 𝑐𝑚; 𝑑2 = 7,7 𝑐𝑚;
Khi chọn ống loe 𝛼 = 100 , ℓ = 12,6 𝑐𝑚
Bài 3.11: Hơi quá nhiệt ở áp suất và nhiệt ộ ban ầu 𝑝1 = 30 𝑏𝑎𝑟, 𝑡1 = 4500𝐶, lưu ộng
oạn nhiệt qua ống tăng tốc hỗn hợp vào môi trường có áp suất 𝑝 = 10 𝑏𝑎𝑟. Xác ịnh tốc
ộ tại cửa ra của ống và lưu lượng nếu biết ường kính tại cửa ra của ống 𝑑2 = 40 𝑚𝑚,
xác ịnh tốc ộ thực nếu biết hiệu suất của ống tăng tốc 𝜂 = 0,81.
Đáp số: 𝐺 = 3,87 𝑘𝑔/𝑠; 𝜔2𝑡 = 708 𝑚 𝑠⁄
Bài 3.12: Sau khi tiết lưu hơi nước có áp suất 1 bar, nhiệt ộ 1400C. Áp suất trước khi
tiết lưu là 10 bar. Xác ịnh ộ khô của hơi nước trước khi tiết lưu.
Đáp số:𝑥 = 0,989
Bài 3.13: Máy nén lý tưởng một cấp, không khí ược nén từ thông số ban ầu
𝑝1 = 1 𝑏𝑎𝑟, 𝑡1 = 200𝐶 ến trạng thái cuối 𝑝2 = 4,5 𝑏𝑎𝑟. Xác ịnh nhiệt ộ cuối của quá trình,
công tiêu hao của máy nén và nhiệt lượng thải ra trong 3 trường hợp: a. Nén ẳng nhiệt. b. Nén oạn nhiệt. c. Nén a biến với n = 3.
Đáp số: a. 𝑇2 = 𝑇1 = 300 𝐾;
ℓ𝑘𝑡 = −126,3 𝑘𝐽 𝑘𝑔⁄ ;
𝑞 = −126,3 𝑘𝐽/𝑘𝑔 b. 𝑇2 = 450 𝐾;
ℓ𝑘𝑡 = −157,8 𝑘𝐽 𝑘𝑔⁄ ; 𝑞 = 0 𝑐. 𝑇2 = 415 𝐾;
ℓ𝑘𝑡 = −151 𝑘𝐽 𝑘𝑔⁄ ; 𝑞 = −29,1 𝑘𝐽/𝑘𝑔
Bài 3.14: Không khí ẩm ở áp suất p1 = 1 at, nhiệt ộ t1 = 250C, ộ ẩm tương ối 𝜑 = 0,6.
Xác ịnh phân áp suất hơi nước ph, nhiệt ộ ọng sương ts, ộ chứa hơi d, entanpy I của không khí ẩm. lOMoARcPSD| 38841209
Đáp số: 𝑝ℎ = 0,19 𝑏𝑎𝑟; 𝑡𝑠 = 170𝐶; 𝑑 = 622.
𝑝−𝑝𝑝ℎℎ = 12 𝑔/𝑘𝑔𝑘ℎô 𝐼 = 55,6J/kg khô.
Bài 3.15: 10m3 không khí ở áp suất p = 1 bar có nhiệt ộ t = 200C, nhiệt ộ ọng sương 𝑡𝑠
= 100𝐶. Xác ịnh ộ ẩm tương ối, ộ chứa hơi d, entanpy I, khối lượng không khí ẩm G,
khối lượng riêng của không khí ẩm 𝜌.
Đáp số: 𝑑 = 0,53 ; 𝜑 = 00,00775 𝑘𝑔 𝑘𝑔 𝑘ℎô⁄; I = 39,67kgJ/kg khô.
𝐺 = 𝐺ℎ + 𝐺𝑘 = 11,84 𝑘𝑔; 𝜌 = 1,2 𝑘𝑔⁄𝑚3
Bài 3.16: Không khí ẩm có ộ ẩm 𝜑 = 0,6, áp suất hơi bão hòa 𝑝𝑏ℎ = 0,06 𝑏𝑎𝑟, áp suất
khí quyển 𝑝0 = 1 𝑏𝑎𝑟. Xác ịnh ộ chứa hơi d.
Đáp số: 𝑑 = 27,3 𝑔⁄𝑘𝑔
Bài 3.17: Không khí ẩm ở trạng thái ầu có nhiệt ộ t1 = 200C, ộ ẩm tương ối 𝜑1 = 40%
ược ốt nóng tới nhiệt ộ t2 = 800C rồi ưa vào buồng sấy. Sau khi sấy nhiệt ộ giảm xuống
t3 = 350C. Xác ịnh ộ chứa hơi d, ộ ẩm tương ối 𝜑 sau khi sấy, nhiệt và lượng không khí
cần ể bốc hơi 1 kg nước trong vật sấy.
Đáp số: 𝑄 = 3415 𝑘𝐽 𝑘𝑔⁄ ; 𝑑 = 0,012 𝑘𝑔 𝑘𝑔 𝑘ℎô⁄
Bài 3.18: Một bình chứa 50 kg nước bão hòa ở nhiệt ộ 900C. Xác ịnh áp suất và thể tích bình chứa. Đáp số:
𝑝𝑏ℎ = 0,7011 𝑏𝑎𝑟; 𝑉 = 0,0052 𝑚3
Bài 3.19: Nước bão hòa có khối lượng 200 g bay hơi hoàn toàn ở áp suất không ổi 100
kPa. Hãy xác ịnh thể tích thay ổi và nhiệt lượng truyền cho nước. Đáp số: ∆𝑉 = 0,33859 𝑚3 𝑄 = 451,51 𝑘𝐽
Bài 3.20: Một bình chứa 10 kg nước ở 900C. 8 kg nước ở trạng thái lỏng và 2 kg còn lại
ở trạng thái hơi. Hãy xác ịnh áp suất trong bình và thể tích của bình chứa. Đáp số: 𝑉 = 4,73 𝑚3
𝑝 = 𝑝𝑏ℎ = 0,7011 𝑏𝑎𝑟
Bài 3.21: 100 kg hơi nước ở trạng thái ầu 𝑝1 = 8 𝑏𝑎𝑟, 𝑡1 = 2400𝐶 giãn nở oạn nhiệt ến
áp suất 𝑝2 = 2 𝑏𝑎𝑟. Xác ịnh ộ khô của hơi sau khi giãn nở và công kỹ thuật. Đáp số: 𝑥 = 0,997 𝐿𝑘𝑡 = 7,5 𝑘𝐽
Bài 3.22: Không khí có áp suất 10 bar, nhiệt ộ 3000C lưu ộng vào ống tăng tốc nhỏ dần,
áp suất sau ống là 5 bar. Hãy xác ịnh tốc ộ không khí ra khỏi ống. Đáp số:
𝜔𝑘 = 437,78 𝑚 𝑠⁄ lOMoARcPSD| 38841209
Bài 3.23: Tiết lưu không khí với áp suất ban ầu 5 bar, sau tiết lưu thể tích tăng gấp ôi.
Xác ịnh ộ biến thiên nhiệt ộ, áp suất và entropy của không khí.
Bài 3.24: Tiết lưu hơi nước từ áp suất 16 bar, nhiệt ộ 3000C xuống áp suất 1,2 bar.
a. Biểu diễn quá trình trên ồ thị i – s.
b. Xác ịnh thông số trạng thái của hơi nước sau khi tiết lưu, ộ quá nhiệt của hơi.
Bài 3.25: Cho một máy nén lý tưởng một cấp làm việc như sau: không khí có áp suất 1
bar, nhiệt ộ 270C ược hút ầy vào xylanh có lượng là 100 m3/h, sau ó nén a biến có n =
1,2 ến áp suất 8 bar, rồi thải toàn bộ vào bình chứa.
a. Biểu diễn các quá trình làm việc trên ồ thị p – v và xác ịnh công suất lý tưởng của máy nén.
b. Tính lượng nước cần thiết ể làm mát không khí trong quá trình nén, cho biết nhiệt
dung riêng của không khí là hằng số, của nước bằng 4,18 kJ/Kg ộ và nhiệt ộ nước làm mát tăng lên 110C.
Bài 3.26: Có 100m3 không khí ẩm ở áp suất 1 bar, nhiệt ộ 350C và ộ ẩm tương ối 75%.
Hãy xác ịnh bằng công thức và ồ thị.
a. Độ chứa hơi của không khí.
b. Nhiệt ộ ọng sương của không khí.
c. Khối lượng của không khí khô và hơi nước.
d. Nếu không khí ó ược làm mát ến 50C trong iều kiện áp suất không ổi. Hãy xác
ịnh lượng nước ã ngưng tụ.