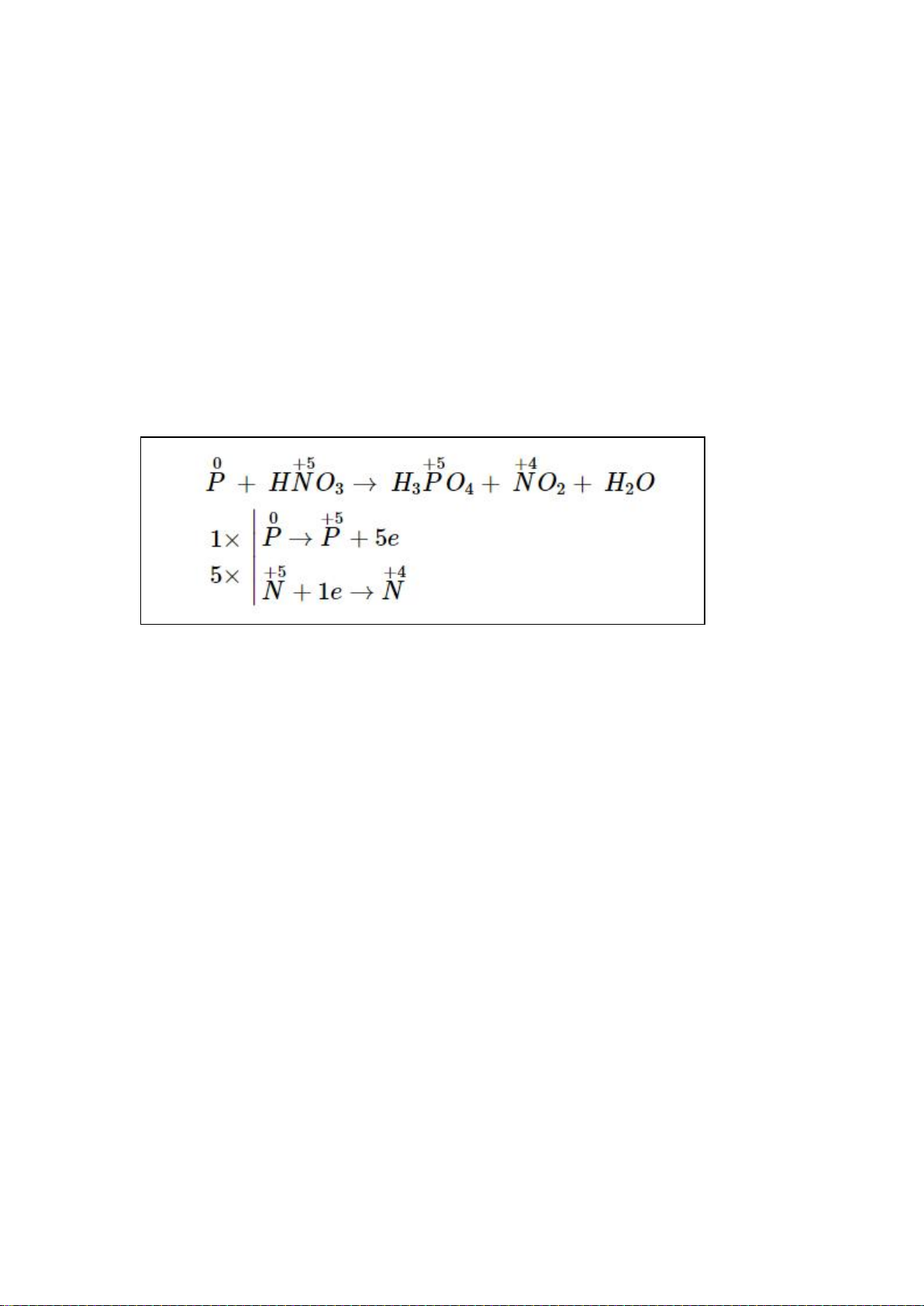






Preview text:
Cân bằng phương trình hóa học P + HNO3 → H3PO4 + NO2 + H2O
1. Phương trình phản ứng giữa P và HNO3
2. Điều kiện phản ứng giữa P và HNO3 ra NO2
- HNO3 đậm đặc, điều kiện thường.
3. Hiện tượng phản ứng
- Photpho tan dần, thoát ra khí màu nâu đỏ.
4. Cân bằng phản ứng P tác dụng với HNO3 đặc
Phản ứng hoá học được cân bằng:
P + 5HNO3 → H3PO4 + 5NO2 + H2O
5. Mở rộng tính chất hoá học của P
- Độ âm điện P < N nhưng P hoạt động hóa học hơn N2 vì liên kết N ≡ N bền vững.
- P trắng hoạt động hóa học mạnh hơn P đỏ.
- Các mức số oxi hóa của P là: -3, 0, +3, +5.
⇒ P thể hiện tính khử hoặc tính oxi hoá khi tham gia phản ứng hóa học.
Vị trí và cấu hình electron nguyên tử: Photpho ở ô thứ 15, nhóm VA, chu kì 3 trong bảng tuần hoàn.
Cấu hình electron nguyên tử của photpho: 1s22s22p63s23p3
Hóa trị của photpho có thể là 5. Ngoài ra, trong một số hợp chất, photpho còn có hóa trị 3.
Tính chất vật lí: Photpho có thể tồn tại ở một số dạng thù hình khác nhau,
nhưng quan trọng hơn cả là photpho trắng và photpho đỏ.
+/ Photpho trắng: - Là chất rắn trong suốt, màu trắng hoặc hơi vàng, trông
giống như sáp, có cấu trúc mạng tinh thể phân tử. Trong tinh thể, những phân
tử P4 nằm ở nút mạng và liên kết với nhau bằng lực tương tác yếu như hình vẽ:
- Mềm, dễ nóng chảy (tnc = 44,1oC).
- Không tan trong nước, tan trong một số dung môi hữu cơ như C6H6, CS2, ... ;
- Rất độc và gây bỏng nặng khi rơi vào da.
- Bốc cháy trong không khí ở nhiệt độ trên 40oC, nên được bảo quản bằng cách ngâm trong nước.
-Phát quang màu lục nhạt trong bóng tối ở nhiệt độ thường.
- Khi đun nóng đến nhiệt độ 250oC và không có không khí, photpho trắng
chuyển dần thành photpho đỏ là dạng bền hơn.
+/ Photpho đỏ: - Là chất bột màu đỏ, dễ hút ẩm và chảy rữa, bền trong không
khí ở nhiệt độ thường và không phát quang trong bóng tối.
- Không tan trong các dung môi thông thường.
- Bốc cháy ở nhiệt độ trên 250oC.
- Khi đun nóng không có không khí, photpho đỏ chuyển thành hơi, khi làm
lạnh thì hơi đó ngưng tụ lại thành photpho trắng.
- Có cấu trúc polime nên khó nóng chảy và khó bay hơi hơn photpho trắng.
Ứng dụng: - Photpho được dùng để sản xuất axit photphoric, trong sản xuất
diêm và sản xuất bom, đạn cháy, đạn khói, ...
Trạng thái tự nhiên: - Trong tự nhiên có hai khoáng vật chính của photpho là
photphorit Ca3(PO4)2 và apatit 3Ca3(PO4)2.CaF2. Nước ta có mỏ apatit ở
Lào Cai, một số mỏ photphorit ở Thái Nguyên, Thanh Hóa, ...
- Ngoài ra, photpho có trong protein thực vật; trong xương, răng, bắp thịt, tế
bào não, ... của người và động vật.
+/ Sản xuất: Photpho đỏ được sản xuất bằng cách nung hỗn hợp quặng
photphorit (hoặc apatit), cát và than cốc ở 1200 oC trong lò điện. Hơi photpho
thoát ra được ngưng tụ khi làm lạnh, sẽ thu được photpho trắng ở dạng rắn. 5.1. Tính oxi hoá
- Tác dụng với một số kim loại hoạt động, tạo ra photphua kim loại. Thí dụ: 5.2. Tính khử
- Tác dụng với các phi kim hoạt động như oxi, halogen, lưu huỳnh … cũng
như với các chất oxi hóa mạnh khác. + Tác dụng với oxi + Tác dụng với clo Thiếu clo: 2P + 3Cl2
+ Tác dụng với hợp chất: P dễ dàng tác dụng với các hợp chất có tính oxi
hóa mạnh như HNO3 đặc, KClO3, KNO3, K2Cr2O7, …
6. Bài tập vận dụng liên quan
Câu 1: Nguồn chứa nhiều photpho trong tự nhiên là A. quặng xiđerit. B. quặng pirit. C. protein thực vật.
D. cơ thể người và động vật. Hướng dẫn giải: Đáp án C
Photpho trong tự nhiên có nhiều trong protein thực vật.
Câu 2: Magie photphua có công thức là A. Mg2P2O7 B. Mg2P3 C. Mg3P2 D. Mg3(PO4)2 Hướng dẫn giải: Đáp án C
Công thức của magie photphua là Mg3P2.
Câu 3: Khi cho 0,25 mol P2O5 vào dung dịch chứa x mol KOH. Để thu được
2 muối K2HPO4 và KH2PO4 thì giá trị x phải thuộc khoảng A. 0 < x < 0,5 B. 0,5 < x < 1 C. 0,25 < x < 0,5 D. 1 < x < 1,5 Hướng dẫn giải: Đáp án B
Câu 4: Biết thành phần % khối lượng P trong tinh thể Na2HPO4.nH2O là
8,659%. Tinh thể muối ngậm nước đó có số phân tử H2O là A. 9 B. 10 C. 11 D. 12 Hướng dẫn giải: Đáp án D
Câu 5: Tìm phương trình hóa học viết sai? Hướng dẫn giải: Đáp án D
D sai vì P2O5 + 3H2O → 2H3PO4
Câu 6: Photpho (P) thể hiện tính oxi hoá trong phản ứng với chất nào dưới đây A. Cl2. B. O2. C. Ca. D. S. Hướng dẫn giải: Đáp án C
Câu 7: Photpho có mấy dạng thù hình quan trọng nhất:
A. 3 dạng: photpho đỏ, photpho trắng và photpho vàng
B. 2 dạng: photpho đỏ và photpho trắng C. 1 dạng photpho đỏ D. 1 dạng photpho trắng Hướng dẫn giải: Đáp án B
Photpho có thể tồn tại ở một số dạng thù hình khác nhau, nhưng quan trọng
hơn cả photpho trắng và photpho đỏ.
Câu 8: Cho hỗn hợp X gồm a mol photpho và b mol lưu huỳnh. Hòa tan hoàn
toàn X trong dung dịch HNO3 đặc lấy dư 20 so với lượng cần dùng thu được
dung dịch Y. Số mol NaOH cần dùng để trung hòa hết dung dịch Y là A. (3a + 2b) mol B. (3,2a + 1,6b) mol C. (1,2a + 3b) mol D. (4a + 3,2b) mol Hướng dẫn giải: Đáp án D
Câu 9: Để điều chế photpho (ở dạng P) người ta trộn một loại quặng có chứa
Ca3(PO4)2 với SiO2 và lượng cacbon vừa đủ rồi nung trong lò với nhiệt độ
cao (20000C). Nếu từ 1 tấn quặng chứa 62% là Ca3(PO4)2 thì sau phản ứng
sẽ thu được bao nhiêu kg photpho biết rằng hiệu suất phản ứng là 90%? A. 12,4 kg B. 137,78 kg C. 124 kg D. 111,6 kg Hướng dẫn giải: Đáp án D
Câu 10: Phát biểu nào sau đây sai?
A. NaHCO3 được dùng trong công nghiệp dược phẩm và công nghiệp thực phẩm.
B. Photpho trắng là chất rắn trong suốt, màu trắng hoặc hơi vàng.
C. Xenlulozơ là chất rắn, dạng sợi, màu xanh, dễ tan trong nước.
D. Photpho đỏ có cấu trúc bằng. Hướng dẫn giải: Đáp án C
C sai vì xenlulozơ là chất rắn, dạng sợi, màu trắng, không dễ tan trong nước.
Câu 11: Đốt cháy 15,5 gam photpho trong oxi dư rồi hòa tan sản phẩm vào
200 gam nước. C% của dung dịch axit thu được là A. 11,36% B. 20,8% C. 24,5% D. 22,7% Hướng dẫn giải: Đáp án B
Câu 12: Ứng dụng nào sau đây không phải của photpho? A. Sản xuất diêm. B. Sản xuất bom.
C. Sản xuất axit photphoric. D. Sản xuất axit nitric. Hướng dẫn giải: Đáp án D
Phần lớn photpho sản xuất ra được dùng để sản xuất axit photphoric, phần
còn lại chủ yếu được dùng để sản xuất diêm, ngoài ra còn được dùng với
mục đích quân sự: sản xuất bom, đạn cháy, đạn khói,…
Câu 13: Cho photpho tác dụng với các chất sau: Ca, O2, Cl2, KClO3, HNO3
và H2SO4 đặc, nóng. Photpho tác dụng được với bao nhiêu chất trong số các chất ở trên? A. 6. B. 5. C. 4. D. 3. Hướng dẫn giải: Đáp án A
P phản ứng được với cả 6 chất trên.
Câu 14: Nung 1000 gam loại quặng photphorit chứa Ca3(PO4)2 hàm lượng
77,5% với C và SiO2 đều lấy dư ở 1000oC. Biết hiệu suất phản ứng đạt 80%.
Khối lượng P thu được là A. 310 gam. B. 148 gam. C. 155 gam. D. 124 gam. Hướng dẫn giải: Đáp án D
Câu 15: Trong hợp chất, photpho có số oxi hóa là A. -3, +3, +5. B. -3, +3, +5, 0. C. +3, +5, 0, +1. D. -3, 0, +1, +3, +5. Hướng dẫn giải: Đáp án A
Trong hợp chất, photpho có số oxi hóa là -3, +3, +5.
Câu 16: Cho P tác dụng với Ca, sản phẩm thu được là A. CaP2. B. Ca2P3. C. CaP. D. Ca3P2. Hướng dẫn giải: Đáp án D
Câu 17: Hai khoáng vật chính của photpho là: A. Apatit và hematit B. Pirit và photphorit C. Apatit và photphorit D. Manhetit và apatit Hướng dẫn giải: Đáp án C
Hai khoáng vật chính chứa P là apatit (3Ca3(PO4)2.CaF2) và photphorit (3Ca3(PO4)2
Câu 18: Khi cho clo dư qua photpho nóng chảy, sẽ thu được sản phẩm nào sau đây: A. PCl3 B. PCl5 C. PCl2 D. PCl Hướng dẫn giải: Đáp án B
Câu 19: Nhận định nào sau đây đúng?
A. Số oxi hóa của photpho có thể tăng từ 0 đến +3 hoặc +5 nên photpho chỉ có tính khử.
B. Photpho có thể giảm số oxi hóa từ 0 xuống -3 nên photpho chỉ có tính oxi hóa.
C. Số oxi hóa của photpho có thể tăng từ 0 đến +3 hoặc +5, có thể giảm từ 0
đến -3 nên photpho thể hiện tính khử và tính oxi hóa.
D. Photpho rất trơ về mặt hóa học nên không thay đổi số oxi hóa trong phản các phản ứng hóa học. Hướng dẫn giải: Đáp án C
A và B sai vì photpho có các mức oxi hóa có thể có là: <![if !vml]><![endif]>, 0,
+3, +5 → P vừa có tính oxi hóa vừa có tính khử. C đúng.
D sai vì P trắng có cấu trúc kém bền nên hoạt động hóa học mạnh → Có sự
thay đổi số oxi hóa trong các phản ứng hóa học.
Câu 20: Trong các nhận định sau, nhận định nào đúng là:
A. Mặc dù độ âm điện của photpho nhỏ hơn nitơ nhưng photpho hoạt động
hóa học mạnh hơn nitơ là do liên kết trong phân tử photpho kém bền hơn trong phân tử nitơ.
B. Nitơ hoạt động hóa học yếu hơn photpho là do nitơ có độ âm điện kém hơn photpho
C. Ở nhiệt độ thường, cả nitơ và photpho đều trơ về mặt hóa học.
D. Nitơ có độ âm điện nhỏ hơn photpho nên hoạt động hóa học mạnh hơn. Hướng dẫn giải Đáp án A
Document Outline
- Cân bằng phương trình hóa học P + HNO3 → H3PO4 + N
- 1. Phương trình phản ứng giữa P và HNO3
- 2. Điều kiện phản ứng giữa P và HNO3 ra NO2
- 3. Hiện tượng phản ứng
- 4. Cân bằng phản ứng P tác dụng với HNO3 đặc
- 5. Mở rộng tính chất hoá học của P
- 5.1. Tính oxi hoá
- 5.2. Tính khử
- 6. Bài tập vận dụng liên quan




