
Preview text:
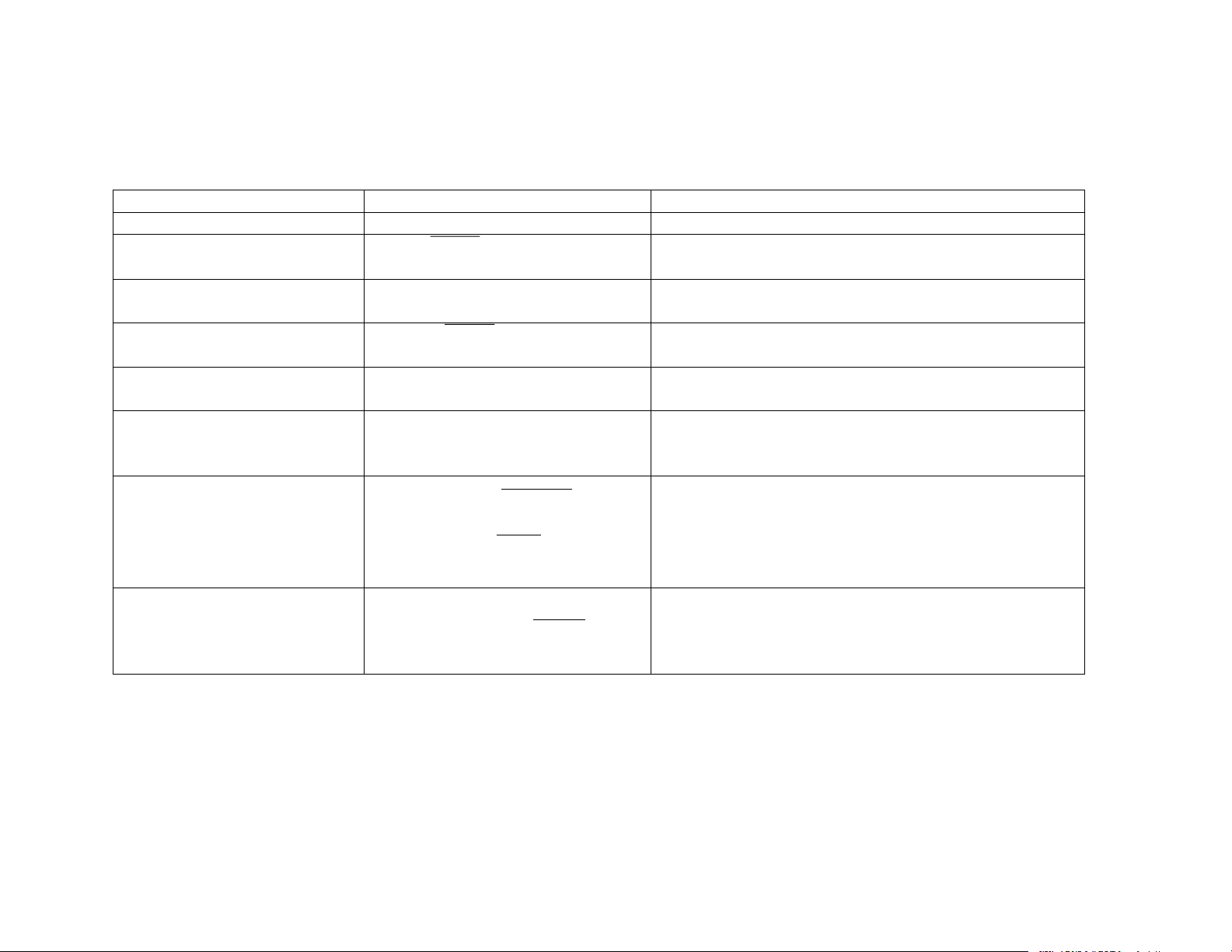
CÔNG THỨC TÍNH pH CỦA MỘT DUNG DỊCH Dung dịch Công thức tính Chú thích acid mạnh pH = - lg(Ca) với Ca là nồng độ acid acid yếu [H] = √ka. Ca
với Ca là nồng độ acid,
pH = - 1/2. lgKa -1/2.lgCa Ka là hằng số acid bazơ mạnh pOH = - lg(Cb)
với Cb là nồng độ của bazơ
pH = 14-pOH = 14 + lg(Cb) bazơ yếu [OH] = √kb. Cb
với Cb là nồng độ của base, Kb là hằng base
pH = 14 +1/2lgKb + 1/2.lgCb
dung dịch muối tạo thành từ
muối tạo thành có tính acid → pH được tính như pH acid mạnh với base yếu
pH = -1/2.lgKa - 1/2.lgCm
của một dung dịch acid yếu; với Cm: nồng độ của muối
dung dịch muối tạo thành từ
muối tạo thành có tính base → pH được tính như pH base mạnh với acid yếu
pH= 14 + 1/2.lgKb + 1/2.lgCm
của một dung dịch base yếu; với Cm: nồng độ của muối
Hổn hợp gồm muối của một (muối) pH = pKa + log
Hệ đệm –dung dịch đệm
dung dịch acid yếu và muối (acid yếu) TD: (CH3COONa và CH3COOH) liên hợp của acid đó
pH = pKa - log Ca
Ca : nồng độ của CH3COOH; Cmuối
Cm: nồng độ của CH3COONa
Hổn hợp gồm muối của một
Hệ đệm –dung dịch đệm
dung dịch base yếu và muối
pH = 14- (pKb - log Cb ) TD: (NH4Cl và NH4OH) liên hợp của base đó Cmuối Cb : nồng độ của NH4OH; Cm: nồng độ của NH4Cl Bài tập áp dụng
1. Tính pH của dung dịch HCl 0,05M, HNO3 0,15M, NaOH 10-2M, Ba(OH)2 10-3M
2. Tính pH của dung dịch CH3COOH 0,025M (ka= 10-4,75), dung dịch NH4OH 0,025M (kb= 10-4,75)
3. Trộn lẫn 10ml dung dịch CH3COOH 0,2M và 10ml dung dịch NaOH 0,2M. Dung dịch mới có pH bằng bao nhiêu? ? pKa = 4,8)
4. Trộn lẫn 10ml dung dịch HCl 0,2M và 10ml dung dịch NH4OH 0,2M. Dung dịch mới có pH bằng bao nhiêu? (pKb = 4,8).
5. Trộn lẫn 10ml dung dịch CH3COONa 0,2M và 20ml dung dịch CH3COOH 0,2M. Dung dịch mới có pH bằng bao nhiêu? (pKa = 4,8)
6. Trộn lẫn 10ml dung dịch NH4OH 0,4M và 40ml dung dịch NH4Cl 0,2M. Dung dịch mới có pH bằng bao nhiêu? (pKb = 4,8).
7. Trộn lẫn 10ml dung dịch HCl 0,2M và 20ml dung dịch NaOH 0,2M. Dung dịch mới có pH bằng bao nhiêu?
8. Trộn lẫn 10ml dung dịch NH4OH 0,2M và 90ml nước. Dung dịch mới có pH bằng bao nhiêu? (pKb = 4,8)
9. Trộn lẫn 10ml dung dịch HCl 0,1M và 40ml nước. Dung dịch mới có pH bằng bao nhiêu? (pKb = 4,8)
10. Dung dịch HCl có pH = 3, muốn được 1 dung dịch HCl mới có pH = 4,5 phải làm sao?


