

Preview text:
TRƯỜNG ĐẠI HỌC BÁCH KHOA KHOA: HOÁ
BỘ MÔN: CÔNG NGHỆ HOÁ HỌC-DẦU & KHÍ
---------------------------- ĐỀ THI CUỐI KỲ Tên học phần: HOÁ LÝ 1 Mã học phần: 1072642 Số tín chỉ: 2
Phương pháp đánh giá : Tự luận
Thời gian làm bài: 75 phút Đề số: 01
× Sinh viên không được sử dụng tài liệu khi làm bài.
Câu 1 (0,5 điểm): Viết biểu thức toán học và ý nghĩa của các đại lượng trong định luật Henry và phạm vi áp dụng của định luật.
Câu 2 (1,0 điểm): Các chất A và B tạo thành một dung dịch lý tưởng. Có một dung dịch gồm 1mol chất A và 2mol
chất B cân bằng với áp suất hơi của nó ở 500C dưới áp suất tổng cộng là 250 mmHg. Nếu người ta thêm 1mol chất A
vào dung dịch này thì áp suất tổng cộng tăng lên tới 300 mmHg. Hãy xác định áp suất hơi bão hoà của A và B nguyên chất ở 500C
Câu 3 (0,5 điểm): Một điện cực calomel bão hoà: Hg,Hg2Cl2 | KClbh
Điện cực trên thuộc loại nào; ứng dụng; viết phản ứng xảy ra trên điện cực
Câu 4 (1,0 điểm): Một chiếc pin có sơ đồ sau:
(-) Pt, H2 (PH2=1atm)| HCl || KClbh | Hg2Cl2, Hg (+)
1/ Viết phản ứng xảy ra trên các cực và trong pin
2/ Xác định pH của dung dịch axit HCl ở 25oC. Cho biết thế điện cực của calomel là φcal = 0,25 (V) và sức điện động
của pin đo được là Epin = 0,332 (V).
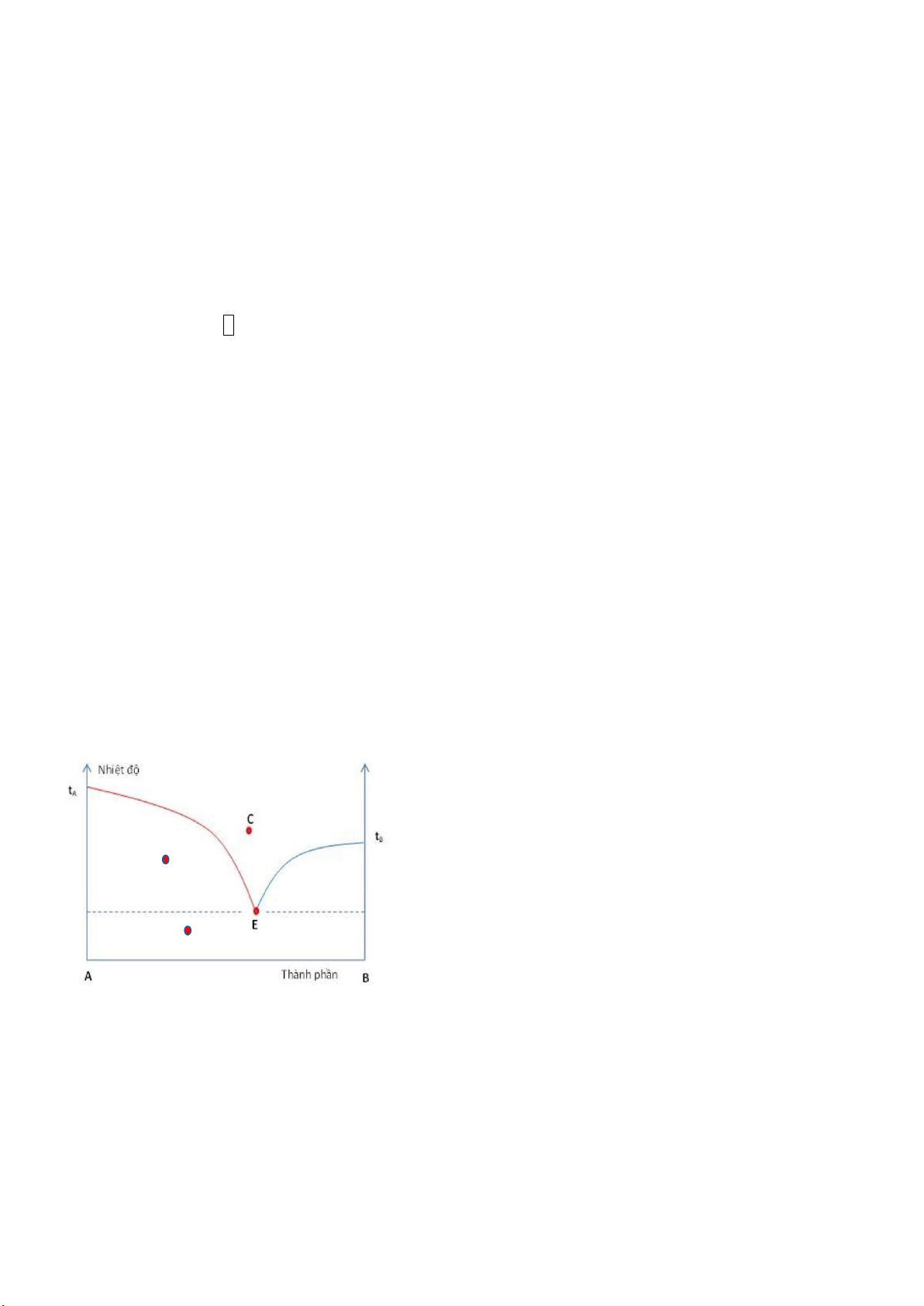
Câu 5 (0,5 điểm): Giản đồ trạng thái cân bằng lỏng-rắn hệ hai cấu tử không tạo thành hợp chất hóa học cho dưới đây.
Anh (chị) hãy cho biết tại các điểm E, A, B, C hệ tồn tại bao nhiêu pha và đó là pha nào? A B
Câu 6 (1,0 điểm): Nhúng một tấm kẽm vào dung dịch axit có pH = 2 đã đuổi hết khí hoà tan ở 25oC, thấy kẽm bị hoà
tan với tốc độ icorr,Zn=10(A/m2) đồng thời có khí hydro thoát ra (cho PH2=1atm). Tính điện thế ăn mòn của Zn (φcorr,Zn).
Biết φoZ n2 +/Z n = -0,76 (V); a Z n2 + = 10-6 (mol/l); i o ,Z n2 + = 10-2 (A/m2) và αZn 2+ = 0,5
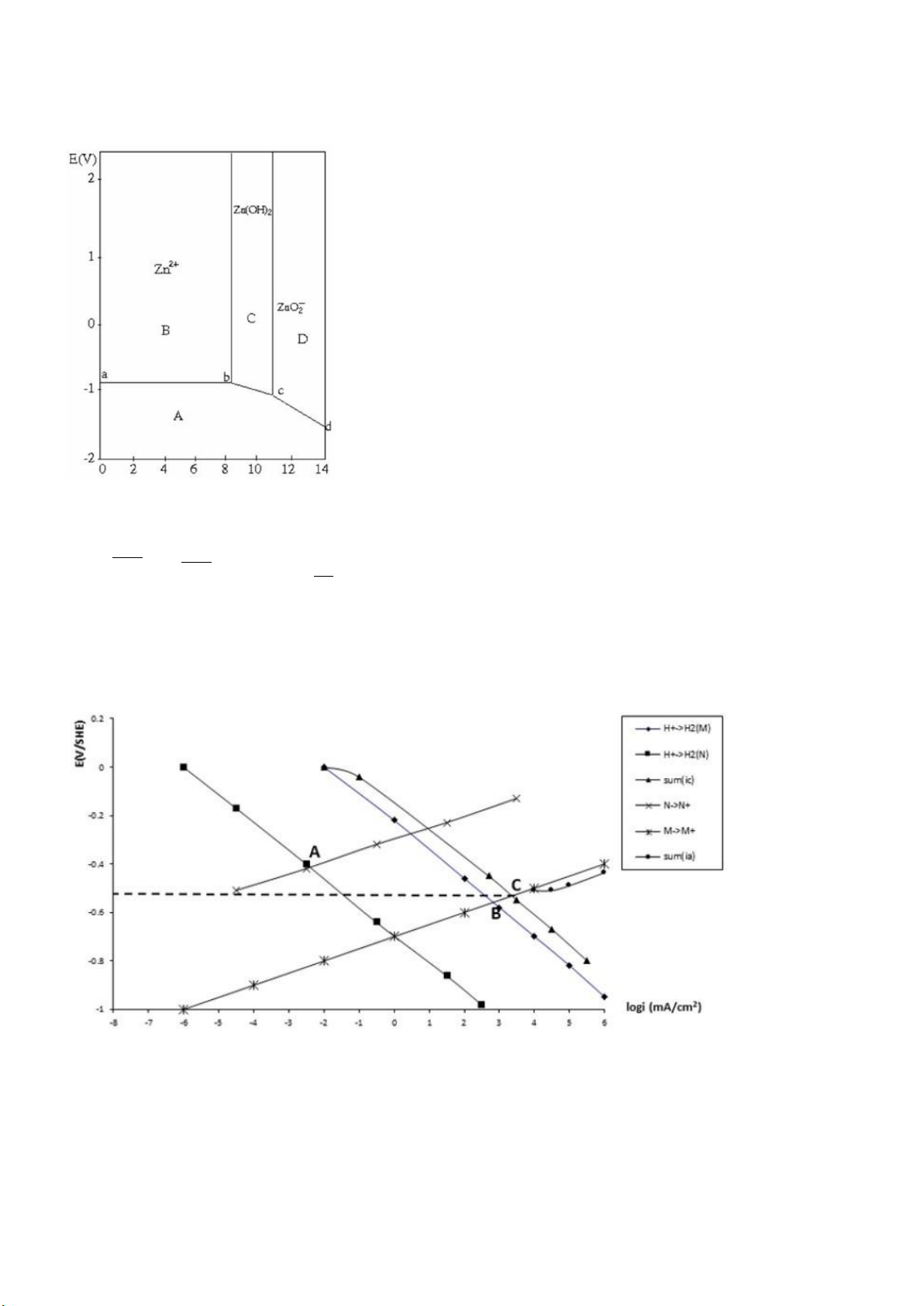
Câu 7 (0,5 điểm): Sử dụng đường cong phân cực φ-logi của phản ứng hòa tan kim loại: M → M2+ + 2e trong dung
dịch axit đã đuổi hết khí hòa tan: 2H+ + 2e → H2. Hãy xác định sự thay đổi của điện thế ăn mòn (φcorr,M) và tốc độ ăn
mòn (icorr,M) khi tăng nồng độ ion H+ trong dung dịch.
Câu 8 (0,5 điểm): Quá trình oxy nhôm và hợp kim nhôm bằng phương pháp điện hóa trong dung dich điện ly H 2SO4
để tạo ra màng oxyt γAl2O3, người ta thường sử dụng các biện pháp kỹ thuật nào để tăng tốc độ tạo màng lớn hơn tốc
độ hòa tan màng oxyt γAl2O3.
Câu 9 (1,5 điểm): Cho phản ứng: Zn+ 2AgCl = ZnCl2 + 2Ag
1/ Viết sơ đồ của pin tương ứng với phản ứng trên; viết phản ứng xảy ra trên các cực của pin
2/ Tính ΔH của phản ứng trên ở 0oC
Biết rằng sức điện động ở 0oC đối với pin có phản ứng xảy ra ở trên là Epin = 1,015 (V) ; hệ số nhiệt độ của sức điện
động là ( ∂E/∂T)p = - 0,000402 (V/K). Câu 10 (0,5 điểm):
Cho giản đồ điện thế E - pH của Zn ở 25oC phía bên. Anh
(chị) hãy cho biết các vùng A, B, C, D ghi trên giản đồ là các vùng gì? y
Câu 11 (0,5 điểm): Xét hệ gồm dung dịch lý tưởng gồm 2 cấu tử A (cấu tử dễ bay hơi) và B (cấu tử khó bay hơi) nằm
cân bằng với pha hơi của chúng. Theo định luật Konovalov ta có: y x P0 =α
trong đóα = A 1−x P 0 1− y B
Anh (chị) hãy cho biết nồng độ của x và y ở biểu thức trên và biểu thị cho cấu tử nào trong hai pha lỏng–hơi ở cân bằng. Câu 12 (1,5 điểm):
1/ Hãy cho biết ý nghĩa các điểm A, B, C trên đồ thị E-logi ở trên
2/ Dựa vào đồ thị trên hãy xác định gần đúng tốc độ ăn mòn của kim loại M khi chưa ghép đôi và khi có ghép đôi với thanh kim loại N
3/ Vai trò của thanh kim loại M khi ghép đôi với thanh kim loại N.
Tổng cộng có: 12 câu
Đà Nẵng, ngày ….. tháng …… năm 2022 TRƯỞNG BỘ MÔN
Document Outline
- KHOA: HOÁ
- ---------------------------- ĐỀ THI CUỐI KỲ
- Câu 10 (0,5 điểm):
- y
- y
- x
- trong đóα = A
- Câu 12 (1,5 điểm):




