








Preview text:
TRƯỜNG ĐẠI HỌC CÔNG NGHIỆP HÀ NỘI
KHOA CÔNG NGHỆ HÓA
BÀI TIỂU LUẬN HÓA LÝ
CHỦ ĐỀ: HẤP PHỤ VÀ HẤP THỤ
Giáo viên hướng dẫn: Phạm Thị Thắm
Sinh viên thực hiện: Nhóm 6 1. Trần Xuân Trường MSV: 2020608533 2. Tạ Đức Trung MSV: 2022604607 3. Phạm Minh Tú MSV: 2022606778 4. Trần Vũ Anh Tú MSV: 2022603065 5. Cao Thị Uyên MSV: 2022606297 6. Trương Quốc Văn MSV: 2022602945 7. Nguyễn Thị Vi MSV: 2022604191
8. Nguyễn Hoàng Anh Vượng MSV: 2022605950
Hà Nội, ngày 13 tháng 12 năm 2023 1 MỤC LỤC
PHẦN I: HẤP THỤ LÀ GÌ .................................................................................................................... 3 1.
Khái niệm .................................................................................................................................... 3 2.
Phân loại ...................................................................................................................................... 3 3.
Mục đích của hấp thụ ................................................................................................................. 3 4.
Lựa chọn dung môi hấp thụ ....................................................................................................... 3 5.
Các yếu tố ảnh hướng đến quá trình hấp thụ .......................................................................... 4 6.
Ứng dụng ..................................................................................................................................... 4 7.
Ví dụ minh hoạ thực tế ............................................................................................................... 5
PHẦN II: HẤP PHỤ LÀ GÌ .................................................................................................................. 5 1.
Khái niệm .................................................................................................................................... 5 2.
Phân loại hấp phụ ....................................................................................................................... 5 3.
Các yếu tố ảnh hưởng đến quá trình hấp phụ .......................................................................... 6
a) Sự phụ thuộc của nhiệt độ ...................................................................................................... 6
b) Năng lượng hoạt hóa hấp phụ ............................................................................................... 6 c)
Lượng chất bị hấp phụ ........................................................................................................... 6
d) Nhiệt hấp phụ .......................................................................................................................... 6 e)
Hoạt độ hấp phụ ..................................................................................................................... 6 f)
Tính thuận nghịch của hấp phụ ............................................................................................. 7
g) Tính chất của các mối nối hấp phụ ....................................................................................... 7
h) Sự chọn lọc hấp phụ ............................................................................................................... 7 i)
Trạng thái của chất bị hấp phụ ............................................................................................. 7 4.
Ứng dụng ..................................................................................................................................... 7 5.
Ví dụ minh họa thực tế ............................................................................................................... 8
PHẦN III: PHÂN BIỆT HẤP THỤ VÀ HẤP PHỤ ............................................................................. 9
BẢNG PHÂN CÔNG CÔNG VIỆC ................................................................................................... 10
*TÀI LIỆU THAM KHẢO .................................................................................................................. 11 2
PHẦN I: HẤP THỤ LÀ GÌ 1. Khái niệm
- Hấp thụ là quá trình hút khí (hơi) bằng chất lỏng, khí được hút gọi là chất bị hấp
thụ, chất lỏng dùng để hút gọi là dung môi, khí không bị hấp thụ gọi là khí trơ.
Quá trình ngược lại với quá trình hấp thụ là nhả hấp thụ
- Hấp thụ bên trong chất , không phải trên bề mặt (như trong trường hợp hấp phụ)
- Quá trình hấp thụ, các phân tử hoàn toàn hòa tan hoặc khuếch tán trong chất
hấp thụ để tạo thành dung dịch. Sau khi hòa tan, các phân tử không thể tách ra
dễ dàng khỏi chất hấp thụ. 2. Phân loại
Quá trình hấp thụ được chia thành hai loại :
• Hấp thụ vật lý: quá trình hấp thụ trong đó không có phản ứng giữa các phân tử
hấp thụ và chất hấp thụ và chỉ có liên kết yếu được gọi là hấp thụ vật lý.
Ví dụ, sự hấp thụ nước bằng một mảnh vải hoặc miếng bọt biển.
Tính chất: HTVL sử dụng sự khuếch tán và sự cân bằng áp suất để hòa tan các
chất ô nhiễm vào chất lỏng.
• Hấp thụ hóa học: quá trình hấp thụ trong đó có phản ứng giữa các phân tử hấp
thụ và chất hấp thụ và liên kết mạnh có mặt được gọi là hấp thụ hóa học.
Ví dụ, sự hấp thụ khí amoniac bằng nước và sự hấp thụ nước bằng canxi cacbonat.
Tính chất: sử dụng các phản ứng hóa học để tạo ra các kết tủa hoặc các muối tan trong chất lỏng.
3. Mục đích của hấp thụ
- Thu hồi các cấu tử có giá trị trong pha khí
- Tách hỗn hợp thành các cấu tử riêng biệt - Làm sạch pha khí
- Tạo thành một dung dịch sản phẩm
4. Lựa chọn dung môi hấp thụ
- Có tính hòa tan chọn lọc: Chỉ hòa tan với một cấu tử, các cấu tử khác không hòa tan hoặc hòa tan ít.
- Độ nhớt: Ít, để giảm trở lực và tăng hệ số truyền khối 3
- Nhiệt dung riêng: Bé, để tiết kiệm nhiệt năng khi hoàn nguyên dung môi
- Nhiệt độ sôi: Khác xa nhiệt độ sôi của cấu tử hòa tan, để dễ ràng phân riêng chúng khi tách
- Nhiệt độ đóng rắn: Thấp, để tránh hiện tượng tắc nghẽn thiết bị
- Tính ăn mòn: Thấp để không ăn mòn thiết bị
- Độ bay hơi: Ít bay hơi để tránh tổn thất
5. Các yếu tố ảnh hướng đến quá trình hấp thụ
- Ảnh hưởng bởi nhiệt độ: Khi các điều kiện khác không đổi mà nhiệt độ tháp
tăng thì hệ số Henry sẽ tăng. Kết quả là ảnh hưởng đường cân bằng dịch chuyển
về phía trục tung. Thậm chí sự hấp thụ không xảy ra được vì nhiệt độ tăng quá
cao . Nhưng nhiệt độ tăng cũng có lợi là làm cho độ nhớt cả hai pha khí và lỏng tăng.
- Ảnh hưởng bởi áp suất: Nếu các điều kiện khác giữ nguyên mà chỉ tăng áp suất
thì hệ số cân bằng sẽ tăng và cân bằng sẽ dịch chuyển về phía trục hoành. Tuy
nhiên, việc tăng áp suất thường kèm theo sự tăng nhiệt độ.
- Các yếu tố khác: như dung môi, độ pH,... 6. Ứng dụng
- Thu hồi các cấu tử quý
• Thu hồi SO2 trong khí thải của thiết bị oxy hóa SO2 thành SO3
• Thu hồi CO2 trong các nhà máy sản xuất bia
• Thu hồi NH3 trong thiết bị tổng hợp amoniac - Làm sạch khí
• Làm sạch khí thải trước khi thải ra môi trường
• Làm sạch khí nguyên liệu trước khi đưa vào sản xuất
- Tách hỗn hợp thành các cấu tử riêng biêt
• Tách SO2, CO, CO2 ra khỏi khí than
• Tách metan ra khỏi các hydrocacbon
- Tạo thành sản phẩm cuối cùng
• Hấp thụ khí HCL vào nước để sản xuất axit HCL
• Hấp thụ SO3 vào nước để sản xuất axit H2SO4
• Hấp thụ khí Cl2 vào dung dịch NaOH để sản xuất nước Javen 4
7. Ví dụ minh hoạ thực tế
Quá trình hấp thụ có thể được hiểu rõ ràng bằng một số ví dụ được sử dụng hàng
ngày được giải thích dưới đây:
• Sự hấp thụ nước của canxicacbonat
• Sự hấp thụ Oxy của nước với động vật thủy sinh
• Sự hấp thụ nước bằng miếng vải hoặc miếng bọt biển
• Việc loại bỏ hydro sunfua khỏi khí sinh học được thực hiện bằng quá trình hấp thụ
• Sự hấp thụ khí amoniac bằng nước
• Carbon dioxide được hòa tan trong không khí hoặc nước thông qua sự hấp thụ
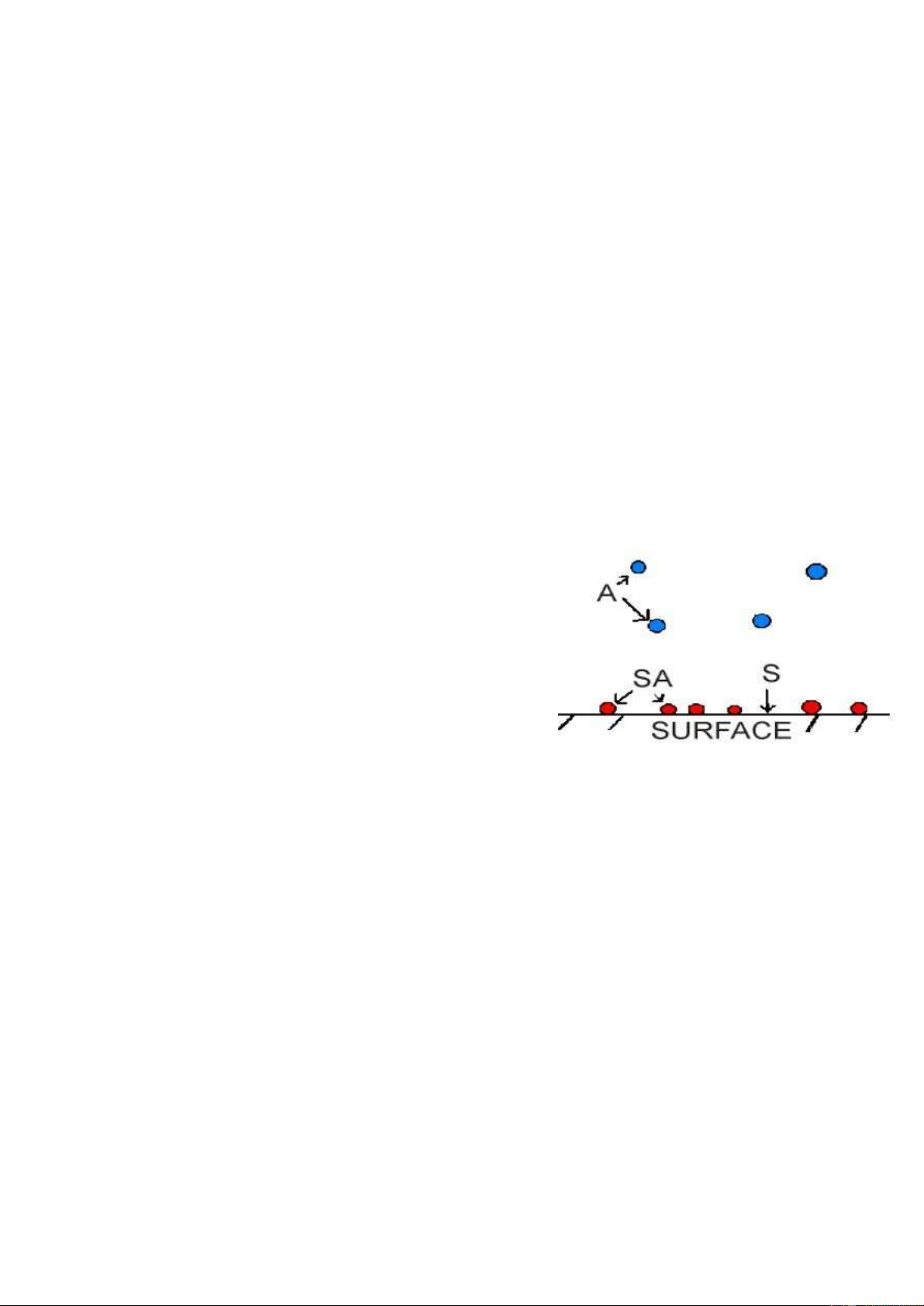
PHẦN II: HẤP PHỤ LÀ GÌ 1. Khái niệm
- Hấp phụ là quá trình tụ tập(chất chứa, thu
hút...) các phân tử khí, hơi hoặc các phân
tử, ion của chất tan lên bề mặt phân chia
pha. Bề mặt phân chia pha có thể là lòng –
rắn, khí – rắn. Chất mà trên bề mặt của nó
có sự hấp phụ xảy ra gọi là chất hấp phụ,
còn chất mà được tụ tập trên bề mặt phân chia pha được gọi là chất bị hấp phụ.
- Quá trình này xảy ra với các phân tử, ion hoặc nguyên tử bám vào bề mặt. Do
năng lượng được giải phóng khi chất bị hấp phụ bám vào chất bị hấp phụ nên
nó được coi là một quá trình tỏa nhiệt. -
2. Phân loại hấp phụ
- Hấp phụ hóa học: Là quá trình hấp phụ gây ra bởi lực có bản chất hoá học. Tại
đây, chất hấp phụ gắn với bề mặt thông qua các liên kết hóa học. Do đó, cơ chế
này liên quan đến phản ứng hóa học giữa chất bị hấp phụ và bề mặt chất hấp phụ. 5
- Hấp phụ vật lý: Là quá trình hấp phụ gây ra bởilực hấp phụ có bản chất vật lý
vàkhông hình thành liên kết hóa học,được thể hiện bởi các lực liên kết yếu như
liên kết Van der Waals hoặc lực tương tác tĩnh điện.
3. Các yếu tố ảnh hưởng đến quá trình hấp phụ
a) Sự phụ thuộc của nhiệt độ -
Hấp phụ vật lý thường xảy ra ở nhiệt độ thấp, khi nhiệt độ tăng thì lượng chất hấp phụ giảm -
Hấp phụ hóa học thường tiến hành ở nhiệt độ cao hơn hấp phụ vật lý, ở nhiệt độ
thấp thì lượng chất hấp phụ hóa học giảm và khi nhiệt độ lớn hơn nhiệt độ tối
ưu thì lượng chất hấp phụ hóa học cũng giảm.
b) Năng lượng hoạt hóa hấp phụ -
Hấp phụ hóa học tiến hành chậm và có năng lượng hoạt hóa khá lớn gần bằng
năng lượng hoạt hóa của phản ứng hóa học, phụ thuộc bởi khoảng cách giữa các
nguyên tử trong chất bị hấp phụ và các trung tâm trên bề mặt chất rắn. -
Hấp phụ vật lý tiến hành rất nhanh và năng lượng hoạt hóa gần bằng không
c) Lượng chất bị hấp phụ -
Hấp phụ vật lý có thể tạo thành nhiều lớp (đa lớp). -
Hấp phụ hóa học xảy ra rất ít, không hơn một lớp trên bề mặt xúc tác (đơn lớp).
d) Nhiệt hấp phụ -
Nhiệt hấp phụ vật lý thường không lớn, gần bằng nhiệt hóa lỏng hay bay hơi
của chất bị hấp phụ ở điều kiện hấp phụ và thường nhỏ hơn 20 kJ/mol. -
Nhiệt hấp phụ hóa học khá lớn, từ 40 - 800 kJ/mol, nhiều khi gần bằng nhiệt
của phản ứng hóa học => tạo thành mối nối hấp phụ khá bền và cần nhiệt độ
khá cao để đẩy chất bị hấp phụ khỏi bề mặt xúc tác rắn.
e) Hoạt độ hấp phụ -
Lượng chất bị hấp phụ tối đa bởi một đơn vị chất hấp phụ ở trạng thái cb được
gọi là độ tĩnh (g/g,kg/kg, mol/g) -
X=kl chất bị hấp phụ / kl chất hấp phụ. Khi đạt cân bằng hấp phụ - Phụ thuộc vào: 6 • Chất bị hấp phụ • Chất hấp phụ
• Nồng độ chất bị hấp phụ • Áp suất
• Nhiệt độ và thành phần các cấu tử bị hấp phụ khác
f) Tính thuận nghịch của hấp phụ -
Hấp phụ vật lý bao giờ cũng là thuận nghịch, nói cách khác quá trình ở trạng
thái cân bằng động: hấp phụ và nhả hấp phụ -
Hấp phụ hóa học không phải bao giờ cũng là quá trình thuận nghịch. Tuỳ theo
đặc tính mối nối liên kết hóa học mà tính chất thuận nghịch ở quá trình hấp phụ khác nhau.
g) Tính chất của các mối nối hấp phụ -
Hấp phụ vật lý không hình thành mối nối. Sự tương tác giữa phân tử bị hấp phụ
với các electron của chất rắn rất yếu (được coi như là 2 hệ thống, không phải 1 hợp chất thống nhất). -
Hấp phụ hóa học tạo thành mối nối bền vững và tính chất gần giống như mối
nối hóa học như: mối nối hóa trị, ion, .... Trong quá trình tạo mối nối có sự di
chuyển điện tử giữa chất bị HP và chất HP, tức là có tác dụng điện tử phần tử
HP và bề mặt chất rắn.
h) Sự chọn lọc hấp phụ -
Hấp phụ vật lý không có sự chọn lọc, tất cả các bề mặt chất rắn đều có tính chất hấp phụ vật lý. -
Hấp phụ hóa học có tính chất chọn lọc cao, phụ thuộc vào tính chất bề mặt chất
rắn và tính chất của chất bị hấp phụ.
i) Trạng thái của chất bị hấp phụ -
Trạng thái và tính chất hóa lý của chất bị hấp phụ không thay đổi. Lực giữa chất
hấp phụ và chất bị hấp phụ là lực Vander Waals. -
Trạng thái của chất bị hấp phụ thay đổi hoàn toàn -
Nhiệt hấp phụ : Qhp = nj - mD 4. Ứng dụng -
Xử lý nước: Hấp phụ các ion trong nước bằng vật liệu hấp phụ 7 -
Công nghệ nhuộm: Các chất hấp phụ được ngấm vào vải để hấp phụ hạt màu lên bề mặt -
Hút ẩm: Silica gel dùng hút ẩm -
Xử lý khí: Dùng than hoạt tính, hấp phụ các khí độc như CO2 và SO2 -
Sắc ký Hấp phụ: Lợi dụng sự hấp phụ chọn lọc để phân tích các chất -
Hấp phụ năng lượng mặt trời: Vật liệu Zeolit ứng dụng trong hấp phụ khí nóng từ môi trường -
Trong các ứng dụng của ngành dược phẩm, quá trình này được sử dụng như
một phương tiện để kéo dài thời gian tiếp xúc thần kinh với một số loại thuốc
và ứng dụng trong thiết bị y sinh và lớp phủ chống dính
5. Ví dụ minh họa thực tế -
Quá trình hấp phụ có thể được hiểu rõ ràng bằng một số ví dụ được sử dụng
hàng ngày được giải thích dưới đây:
• Bộ lọc xử lý nước cứng
• Chất ô nhiễm hấp phụ lên than hoạt tính
• Bạc dính vào kính và tạo ra một bề mặt gương
• Nước hấp phụ lên silica gel
• Lớp phủ chống dính trên nồi và chảo
• Hạt hấp phụ lên zeolit
• Virus hấp phụ lên bề mặt và tế bào
• Máy làm lạnh hấp phụ được sử dụng với chất làm lạnh • Mặt nạ phòng độc
• Tháp hấp phụ(Thiết bị thanh lọc hóa chất) 8
PHẦN III: PHÂN BIỆT HẤP THỤ VÀ HẤP PHỤ -
Hấp phụ một chất là quá trình chất đó bám dính lên bề mặt chất khác -
Hấp thụ một chất là quá trình chất đó đi sâu vào khe trống trong tinh thể hoặc phân tử Tiêu chuẩn Hấp thụ Hấp phụ
Đồng hóa hệ thống phân tử
Tích lũy các loại phân tử ở
Sự định nghĩa
trong toàn bộ phần lớn môi
đáy thay vì chất lỏng hoặc
trường rắn hoặc lỏng. chất rắn. Một Hiện
hiện tượng số lượng tượng Một lớn. hiện tượng bề mặt.
Trao đổi nhiệt Quá trình thu nhiệt Quá trình tỏa nhiệt
Bị ảnh hưởng bởi nhiệt độ Nhiệt độ
Nhiệt độ không có tác dụng. thấp
Tốc độ phản Tăng Xảy
đều và đạt trạng thái
ra với tốc độ đồng đều. ứng cân bằng.
Nồng độ ở dưới cùng của Sự
Nó không đổi trong suốt tập trung chất phương tiện.
hấp phụ khác với nồng độ ở dạng khối.
BẢNG PHÂN CÔNG CÔNG VIỆC
Tên thành viên Công việc
Thời gian hoàn thành Trần Xuân Trường Đúng hạn Power Point Tạ Đức Trung Thuyết Đúng hạn trình 9 Phạm Minh Tú Thuyết trình Đúng hạn Trần Vũ Anh Tú Đúng hạn Tìm nội dung Cao Thị Uyên Đúng hạn Power Point Trương Quốc Văn Đúng hạn Word Nguyễn Thị Vi Đúng hạn Tìm nội dung Nguyễn Hoàng Anh Đúng hạn Vượng Tìm nội dung
*TÀI LIỆU THAM KHẢO
[1] Nguyễn Vân Anh(Chủ biên), Cao Hồng Hà, Nguyễn Thu Hà, Giáo trình
Hấp phụ - Hóa keo, NXB Bách Khoa Hà Nội
[2] Giáo trình bài giảng quá trình hấp thụ
• Hóa kỹ môi trường – Chương 2: Quá trình hấp thụ
[3] Giáo trình bài giảng quá trình hấp phụ
• Hồ Sỹ Thắng, Giáo trình hóa keo và hấp phụ, NXB Giáo Dục Việt Nam
• Lê Thị Thái Hà, bài giảng Quá trình hấp phụ 10 11




