






Preview text:
UBND HUYỆN .............................
MA TRẬN ĐỀ KIỂM TRA GIỮA KÌ II
TRƯỜNG THCS TT .................. Năm học 2022- 2023 Môn : Hoá học Lớp : 9
Thời gian 45 phút ( Không kể thời gian giao đề )
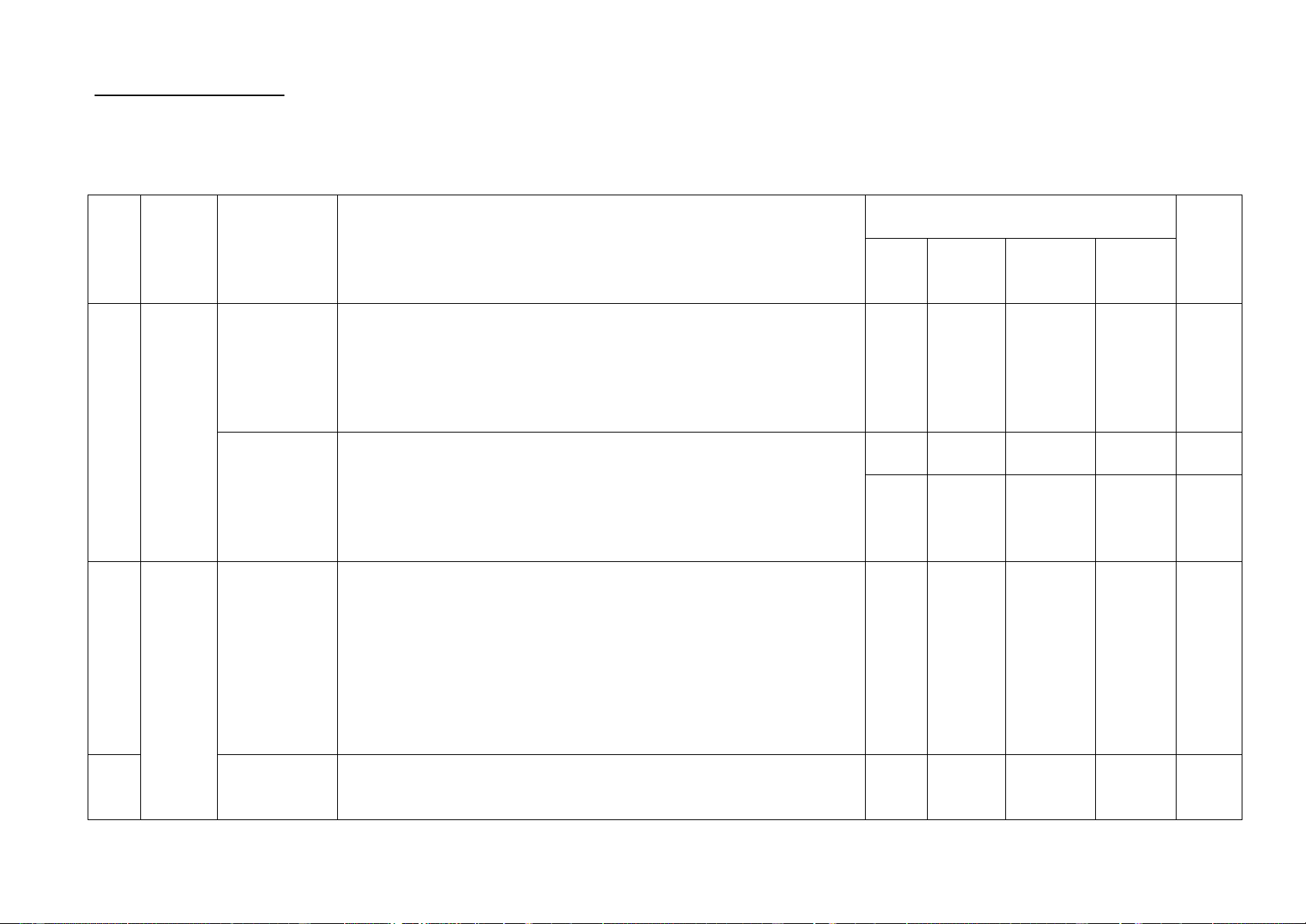
Mức độ nhận thức Tổng Nhận biết Thông hiểu Vận dụng Vận dụng cao % Nội dung TT
Đơn vị kiến thức Số CH Thời tổng kiến thức Thời Số Thời Số Thời Số Thời Số Thời gian điểm Số CH gian CH gian CH gian CH gian CH gian TN TL (phút (phút) TN (phút) TL (phút) (phút) (phút) ) Chương 3: 1 Phi kim-
Cacbon và hợp chất 2 2 0,5 4 2 0,5 6 10% Sơ lược của cacbon: (1t) 2 bảng tuần 3 hoàn các
Sơ lược về bảng nguyên tố
TH các NTHH (2t) 2 2 2 2 10% 4 hóa học
Khái niệm, CTPT hợp 5
chất hữu cơ và hóa học 4 4 4 4 20% hữu cơ. Chương 4: (1+1 = 2t) 6 Hiđrocac Metan (1t) 3 3 0,5 5 0,5 6 3 1 14 17,5% 7 Etilen 3 3 0,5 4 3 0,5 7 12,5% bon Axetilen 2 2 2 2 10%
Tổng hợp kiến thức. 8 1 10 1 10 20% (1+1 = 2t) Tổng 16 16 1,5 15 1 8 0,5 6 16 3 45 100 Tỉ lệ % 40% 30% 20% 10% Tỉ lệ chung 70% 30%
UBND HUYỆN ...................
BẢNG ĐẶC TẢ KĨ THUẬT ĐỀ KIỂM TRA GIỮA KÌ II
TRƯỜNG THCS .......................... Năm học 2022 - 2023 Môn : Hoá học Lớp : 9
Thời gian 45 phút ( Không kể thời gian giao đề )
Mức độ kiến thức, kĩ năng
Số câu hỏi theo các mức độ nhận Nội
cần kiểm tra, đánh giá thức dung Đơn vị kiến TT Vận Tổng kiến thức Nhận Thông Vận dụng thức biết hiểu dụng cao Nhận biết: 1 Cacbon và Phi hợp chất của
- Tính chất hoá học của muối cacbonat làm quỳ tím hóa đỏ [1]
kim- Sơ cacbon: Axit - Nhận biết muối trung hòa và muối axit. [10] C1 0,5 lược cacbonic và Thông hiểu: C10 C19 bảng muối
- Phân biệt được một số muối cacbonat cụ thể. tuần cacbonat Vận dụng: CO hoàn 2+ Ca(OH)2 [19] các Nhận biết: C3 nguyên Chương 3:
- Nêu được cấu tạo bảng tuần hoàn gồm: ô nguyên tố, chu kì, nhóm. tố hóa Phi kim – sơ
- Nhận biết về chu kì, nhóm. [3] C7 học. lược về bảng
- Nêu quy luật biến đổi tính KL, PK trong chu kì, nhóm. Lấy ví dụ tuần hoàn minh hoạ. [7]. Nhận biết: 2
- Khái niệm về hợp chất hữu cơ & hóa học hữu cơ. [14] Khái niệm, C2
- Cách phân loại hợp chất hữu cơ. [2]. [8] cấu tạo phân C4 tử hợp chất
- cấu tạo phân tử hợp chất hữu cơ và CTCT của chúng[4]. C8 Thông hiểu: hữu cơ và hóa C14 học hữu cơ.
- Đặc điểm cấu tạo phân tử hợp chất hữu cơ và CTCT của chúng. Vận dụng: C15 Hiđro
- Viết được CTCT mạch hở, mạch vòng của 1 số chất hữu cơ đơn
giản (tối đa 4 nguyên tử C) khi biết CTCT. [15]. Cacbon Nhận biết: C 5 0,5 3 Hdrocacbon
- Công thức phân tử, CTCT, đặc điểm cấu tạo của PT metan. [5]. C11 C17 no
- Tính chất hóa học: Tác dụng với clo (PƯ thế), với oxi (PƯ cháy). Thông hiểu:
- Viết phương trình hóa học (dạng CTPT và CTCT thu gọn) của
các phản ứng minh họa tính chất hóa học của metan. Metan
- Phản ứng đặc trưng của CH4 là phản ứng thế. [11]. Vận dụng:
- Tính thể tích khí trong phản ứng ở đktc. [17].
- Phân biệt khí metan với 1 vài khí khác. Nhận biết bằng phương pháp hóa học. [19]. Nhận biết: 4 0,5
- Công thức phân tử, CTCT, đặc điểm cấu tạo của PT etilen. [12]. C18 C6
Hidrocacbon [6]. [13]. [16]. C19 C12 không no
- Ứng dụng của etilen: Làm nguyên liệu điều chế nhựa PE, rượu C9 Etilen etylic, axit axetic… [9]. C13 Axetilen Thông hiểu: C16
- Phân biệt khí etilen với khí metan bằng phương pháp hóa học (cộng brom). [19]. Nhận biết: 5
- Biết được mối quan hệ mối quan hệ giữa cấu tạo và tính chất của hiđocacbon. [17]. Thông hiểu:
- Viết được các phương trình hoá học minh hoạ được mối quan hệ Tổng hợp
giữa metan, etilen, axetilen. [19]. 0,5 kiến thức
- Viết công thức cấu tạo đầy đủ và thu gọn của các hợp chất hữu cơ. C17 [18]. Vận dụng cao:
- Tính thể tích khí tham gia hoặc tạo thành trong phản ứng ở đktc. [17]. Tổng 16 1,5 1 0,5
Tỉ lệ % từng mức độ nhận 40% 30% 20% 10% thức Tỉ lệ chung 70% 30%
UBND HUYỆN ..........................
ĐỀ KIỂM TRA GIỮA KÌ II
TRƯỜNG THCS TT THẤT KHÊ Năm học 2022 - 2023 Môn : Hoá học Lớp : 9
Thời gian 45 phút ( Không kể thời gian giao đề )
(Đề gồm 1 trang 13 câu)
I.Trắc nghiệm ( 5 điểm) Hãy khoanh tròn vào một trong các chữ cái A, B, C hoặc D đứng
trước câu trả lời đúng nhất.
Câu 1: Cho khí CO tan vào nước cất có pha vài giọt quỳ tím. Dung dịch có màu nào? 2
A. Xanh B. Đỏ C. Tím D. Không màu
Câu 2: Chất nào sau đây là dẫn xuất của hiđrocacbon?
A. CH4 B. C2H6O C. C2H4 D. C2H2
Câu 3: Chu kì cho biết?
A. Số P B. Số electron C Số lớp electron D. Số electron lớp ngoài cùng
Câu 4:Trong các hợp chất hữu cơ, cacbon luôn có hoá trị là: A. I. B. II. C. III. D. IV.
Câu 5: Số liên kết đơn trong phân tử Metan? A.2 B. 4 C. 3 D. 5
Câu 6: Hãy cho biết chất nào sau đây trong phân tử có liên kết đôi?
A. C3H8. B. C3H6. C. C3H4 D. C4H10.
Câu 7: Hãy cho biết cách sắp xếp nào sau đây đúng theo chiều tính kim loại giảm dần:
A. Na, Mg, Al, K C. K, Na, Mg, Al
B. Al, K, Na, Mg D. Mg, K, Al, Na
Câu 8: Dãy các chất nào sau đây đều là Hiđrocacbon ? A. C2H6, C4H10, C2H4. C. CH4, C2H2, C3H7Cl. B. C2H4, CH4, C2H5Cl. D. C2H6O, C3H8, C2H2.
Câu 9: Trong quá trình chín trái cây đã thoát ra một lượng nhỏ khí nào sau đây? A. Etan
B. Metan. C. Etilen.. . D. Axetilen.
Câu 10:Dãy các chất nào sau đây là muối axit ? A. KHCO3, CaCO3, Na2CO3.
B. Ba(HCO3)2, NaHCO3, Ca(HCO3)2.
C. Ca(HCO3)2, Ba(HCO3)2, BaCO3.
D. Mg(HCO3)2, Ba(HCO3)2, CaCO3.
Câu 11: Phản ứng hóa học đặc trưng của metan là A. phản ứng cộng. B. phản ứng thế. C. phản ứng tách. D. phản ứng trùng hợp.
Câu 12: Trong phân tử etilen có A. 1 Liên kết đôi B.1 liên kết ba C. 1 Liên kết đơn D. 2 Liên kết đôi
Câu 13: Trong phân tử axetilen có chứa bao nhiêu nguyên tử cacbon A. 1 nguyên tử C B. 2 nguyên tử C C. 3 nguyên tử H D. 6 nguyên tử H
Câu 14: Trong thành phần hợp chất hữu cơ nhất thiết phải có nguyên tố: A. cacbon B. hidro C. oxi D. nito
Câu 15: Nguyên tử cacbon có thể liên kết trực tiếp với nhau tạo thành các dạng mạch cacbon là: A. mạch vòng.
B. mạch thẳng, mạch nhánh.
C. mạch vòng, mạch thẳng, mạch nhánh D. mạch nhánh.
Câu 16. Chất nào sau đây có chứa liên kết ba trong phân tử A. Metan. B. Êtilen. C. Axetilen. D. Propan
PHẦN TỰ LUẬN (6 điểm)
Câu 17 (2,0 điểm): Dẫn 6,72 lit khí CH4 đốt cháy trong không khí, sao cho phản ứng xảy ra
hoàn toàn. Sau thí nghiệm thấy có một chất khí làm đục nước vôi trong và hơi nước
a. Viết các phương trình hóa học xảy ra.
b.Tính thành thể tích của chất khí CO2 sinh ra sau phản ứng ở điều kiện tiêu chuẩn.
Câu 18 (2,0 điểm): Hãy viết 4 công thức cấu tạo dạng đầy đủ và thu gọn của C4H8
Câu 19 (2,0 điểm): Có 3 khí đựng trong 3 bình kín, CH4, C2H4, CO2 bằng phương pháp hóa
học em hãy nhận biết từng khí trên. Viết các PTHH nếu có.
Biết C = 12; O = 16; H = 1;
-------------HẾT -----------
UBND HUYỆN ..........................
HƯỚNG DẪN CHẤM ĐỀ THI GIỮA KÌ II
TRƯỜNG THCS TT THẤT KHÊ Năm học 2022 - 2023
Môn Hóa Học - Lớp: 9
I. Trắc nghiệm mỗi ý đúng được 0,5 điểm Câu 1 2 3 4 5 6 7 8 Đáp án B B C D B B C A Câu 9 10 11 12 13 14 15 16 Đáp án C B B A B A C C II. Tự luận Câu Nội dung Điểm 17 CH4 + 2O2 → CO2 + 2H2O 0.5 1mol 2mol 1mol 0.5 (2,0 0,3mol 0,3mol 0.5 điểm) Vc 0,5 O
= 22,4.0,3 = 6,72 lít. 2 18
- HS vẽ được CTCT dạng mạch thẳng, mạch nhánh và mạch vòng của C 2,0 2,0
4H8 mỗi công thức đúng được 0,5 điểm điểm 19
- Dẫn 3 khí lần lượt qua dung dịch brom, 1 khí làm dung dịch brom 0.5
mất màu là C2H2. Còn lại là CH4 và CO2. 2 điểm C2H2 + 2Br2 → C2H2Br4. 0.5
- Dẫn 2 khí lần lượt qua dung dịch nước vôi trong, khí nào nước vôi trong vẩn đục là CO 0.5 2. Còn lại là CH4 . PTHH: Ca(OH) 0.5 2 + CO2 → CaCO3 + H2O * Lưu ý
- Trong các bài tập chưa cho sẵn sơ đồ phản ứng, phương trình hoá học nào mà cân
bằng hệ số sai hoặc thiếu điều kiện thì trừ đi nửa số điểm của phương trình đó
- Có thể giải bài tập bằng nhiều phương pháp khác nhau nhưng nếu tính đúng, lập
luận và dẫn đến kết quả đúng vẫn được tính điểm tối đa. Trong khi tính toán, nếu nhầm
lẫn một phần nào đó dẫn đến kết quả sai thì trừ đi số điểm dành cho phần sai đó theo
hướng dẫn. Nếu tiếp tục dùng kết quả sai để giải các phần tiếp theo thì không tính điểm các phần sau đó.