

Preview text:
Bài 24: Acetic acid
Mở đầu trang 118 Bài 24 KHTN 9: Quan sát hình 24.1, mô tả và giải thích hiện
tượng xảy ra. Có hiện tượng trên là do trong giấm ăn có acetic acid. Vậy acetic acid
có cấu tạo như thế nào và có những tính chất gì? Trả lời:
- Giai đoạn đầu quả trứng lơ lửng trong cốc giấm ăn và xuất hiện các bọt nhỏ xung
quanh vỏ quả trứng. Do vỏ trứng được làm bằng calcium carbonate. Khi nhúng
trứng vào giấm, acid trong giấm sẽ phản ứng với calcium carbonate và tạo ra khí carbonic.
- Giai đoạn sau, thấy lớp vỏ tan ra chỉ lớp màng mỏng của trứng và chìm xuống đáy
cốc. Do màng có tính chất bán thấm nên giấm có thể đi qua màng. Từ đó, trứng hấp
thụ giấm làm trứng tăng kích thước và chìm trong giấm.
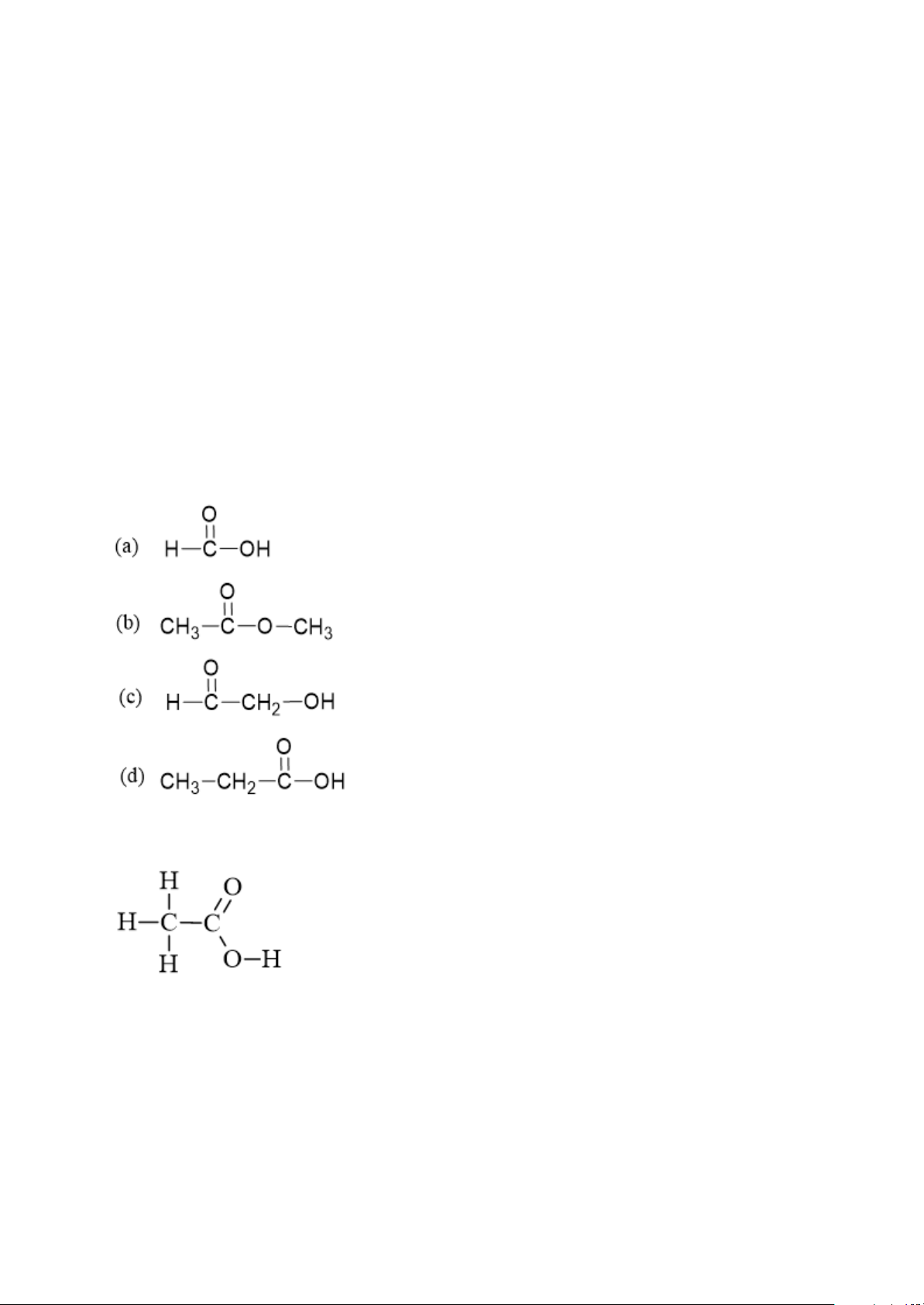
Câu hỏi 1 trang 118 KHTN 9: Chỉ ra những chất có đặc điểm cấu tạo tương tự cấu
tạo của acetic acid trong các chất sau: Trả lời:
Công thức cấu tạo của acetic acid là:
→ Những chất có đặc điểm cấu tạo tương tự cấu tạo của acetic acid là (a), (d). Vì
trong cấu tạo đều có nhóm chức – COOH.
Câu hỏi 2 trang 119 KHTN 9: Dùng ống hút nhỏ giọt lấy khoảng 2 mL acetic acid cho
vào ống nghiệm. Quan sát và nêu trạng thái, màu sắc của acetic acid. Trả lời:
Ở điều kiện thường, acetic acid là chất lỏng, không màu.
Thực hành trang 119 KHTN 9: Thí nghiệm 1 Chuẩn bị
Dụng cụ: mặt kính đồng hồ, ống hút nhỏ giọt, ống nghiệm, giá để ống nghiệm.
Hoá chất: dung dịch acetic acid 1 M, giấy quỳ tím, dung dịch NaOH 0,1 M, CuO, Zn,
đá vôi, dung dịch phenolphthalein.
Tiến hành thí nghiệm và thảo luận
Đặt mẩu giấy quỳ tím lên mặt kính đồng hồ, nhỏ vào đó một giọt dung dịch acetic acid và quan sát.
Đặt 4 ống nghiệm có đánh số thứ tự từ 1 đến 4 vào giá để ống nghiệm. Cho 1 mL
dung dịch NaOH 0,1M và một giọt phenolphthalein vào ống 1; một lượng nhỏ (bằng
hạt gạo) CuO vào ống 2; một viên kẽm vào ống 3; một mẫu đá vôi vào ống 4; sau đó
cho vào mỗi ống nghiệm 1 – 2 mL dung dịch acetic acid 1 M (riêng ống nghiệm số 2,
đun nóng nhẹ sau khi nhỏ dung dịch acetic acid).
Quan sát thí nghiệm, mô tả và giải thích hiện tượng xảy ra trong các ống nghiệm. Trả lời:
Bước tiến hành thí nghiệm
Hiện tượng, giải thích
Đặt mẩu giấy quỳ tím lên mặt kính Quỳ tím chuyển sang màu hồng. Vì acetic
đồng hồ, nhỏ vào đó một giọt dung acid có tính acid yếu.
dịch acetic acid và quan sát.
Cho dung dịch acetic acid vào ống - Ban đầu ống nghiệm chứa dung dịch
nghiệm 1 chứa 1 mL dung dịch NaOH, khi nhỏ 1 giọt phenolphthalein vào thì NaOH 0,1M và một
giọt dung dịch chuyển sang màu hồng vì dung phenolphthalein
dịch có môi trường base.
- Sau đó cho dung dịch acetic acid vào thì
màu hồng nhạt dần và dung dịch mất màu.
Do acetic acid có phản ứng trung hòa với NaOH.
CH3COOH + NaOH → CH3COONa + H2O
Cho dung dịch acetic acid vào ống - CuO tan dần, sau phản ứng dung dịch thu
nghiệm 2 chứa một lượng nhỏ được có màu xanh. CuO
2CH3COOH + CuO → (CH3COO)2Cu + H2O
Cho dung dịch acetic acid vào ống - Viên kẽm tan dần, có bọt khí thoát ra.
nghiệm 3 chứa 1 viên kẽm
2CH3COOH + Zn → (CH3COO)2Zn + H2
Cho dung dịch acetic acid vào ống - Mẩu đá vôi tan ra, có sủi bọt khí.
nghiệm 4 chứa một mẩu đá vôi
2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 + H2O
Câu hỏi 3 trang 119 KHTN 9: Trong thí nghiệm 1, sự thay đổi màu của giấy quỳ tím chứng tỏ điều gì? Trả lời:
Trong thí nghiệm 1 sự thay đổi màu của giấy quỳ tím chứng tỏ acetic acid có tính acid yếu.
Câu hỏi 4 trang 119 KHTN 9: Trong thí nghiệm 1, những dấu hiệu nào chứng tỏ
acetic acid đã phản ứng với NaOH? Chất khí nào thoát ra khi cho dung dịch acetic acid vào đá vôi? Trả lời:
- Trong thí nghiệm, dấu hiệu chứng tỏ acetic acid đã phản ứng với NaOH là màu
hồng ban đầu mất đi do có sự phản ứng giữa acetic acid với NaOH. Phương trình hóa học:
CH3COOH + NaOH → CH3COONa + H2O
- Khi cho dung dịch acetic acid vào đá vôi thì có khí CO2 thoát ra. Phương trình hóa học:
2CH3COOH + CaCO3 → (CH3COO)2Ca + CO2 + H2O
Luyện tập 1 trang 120 KHTN 9: Viết phương trình hóa học của phản ứng xảy ra khi
cho acetic acid tác dụng với: Cu(OH)2, MgO, Fe. Trả lời: Phương trình hóa học:
2CH3COOH + Cu(OH)2 → (CH3COO)2Cu + 2H2O
2CH3COOH + MgO → (CH3COO)2Mg + H2O
2CH3COOH + Fe → (CH3COO)2Fe + H2
Luyện tập 2 trang 120 KHTN 9: Chọn các chất thích hợp để điền vào dấu ? và hoàn
thành các phương trình hóa học sau:
a) ? + Na2CO3---> CH3COONa + ? + ?
b) CH3COOH + ? ---> (CH3COO)2Mg + H2 Trả lời:
a) 2CH3COOH+ Na2CO3→ 2CH3COONa + CO2 + H2O
b) 2CH3COOH + Mg→ (CH3COO)2Mg + H2
Vận dụng 1 trang 120 KHTN 9: Cặn trong ấm đun nước có thành phần chính là
CaCO3 (hình 24.3). Có thể làm sạch cặn bằng giấm ăn. Giải thích cách làm trên,
viết phương trình hóa học minh họa. Trả lời:
Cặn trong ấm đun nước là CaCO3 nên có thể sạch cặn bằng giấm ăn. Vì acetic acid
trong giấm ăn có thể hòa tan được CaCO3 theo phản ứng sau:
CaCO3 + 2CH3COOH → (CH3COO)2Ca + CO2 + H2O
Thực hành trang 120 KHTN 9: Thí nghiệm 2 Chuẩn bị
Dụng cụ: ống nghiệm, nút cao su có gắn ống thuỷ tinh gấp khúc, đèn cồn, giá kẹp
ống nghiệm, cốc thuỷ tinh, đá viên.
Hoá chất: C2H5OH, dung dịch CH3COOH đặc, dung dịch H2SO4đặc, nước cất.
Tiến hành thí nghiệm và thảo luận
Cho 2 mL C2H5OH, 2 mL dung dịch CH3COOH đặc vào ống nghiệm A, lắc nhẹ, sau
đó thêm tiếp khoảng 5 giọt dung dịch H2SO4đặc và lắp dụng cụ như hình 24.4.
Đun nóng cẩn thận ống nghiệm A khoảng 5-7 phút thì dừng lại. Thêm 2 mL nước cất
vào ống nghiệm B rồi lắc nhẹ, sau đó để yên và quan sát.
Nêu và giải thích hiện tượng xảy ra trong ống nghiệm B. Trả lời: Bước thí nghiệm
Hiện tượng, giải thích
Cho 2 mL C2H5OH, 2 mL dung Thu được được hỗn hợp đồng nhất. Vì các
dịch CH3COOH đặc vào ống chất tan được vào nhau.
nghiệm A, lắc nhẹ, sau đó thêm
tiếp khoảng 5 giọt dung dịch H2SO4 đặc
Đun nóng cẩn thận ống nghiệm A Ống nghiệm B ngưng tụ được chất lỏng có
khoảng 5-7 phút thì dừng lại. mùi giống mùi sơn móng tay. Khi thêm nước
Thêm 2 mL nước cất vào ống cất, lắc nhẹ, để yên thấy dung dịch phân làm
nghiệm B rồi lắc nhẹ, sau đó để 2 lớp, lớp bên trên có mùi là ester ethyl yên acetacte.
Giải thích: Khi đun nóng và có H2SO4 đặc làm
xúc tác, acetic acid tác dụng với ethylic
alcohol tạo ra ester ethyl acetate theo phương trình hóa học:
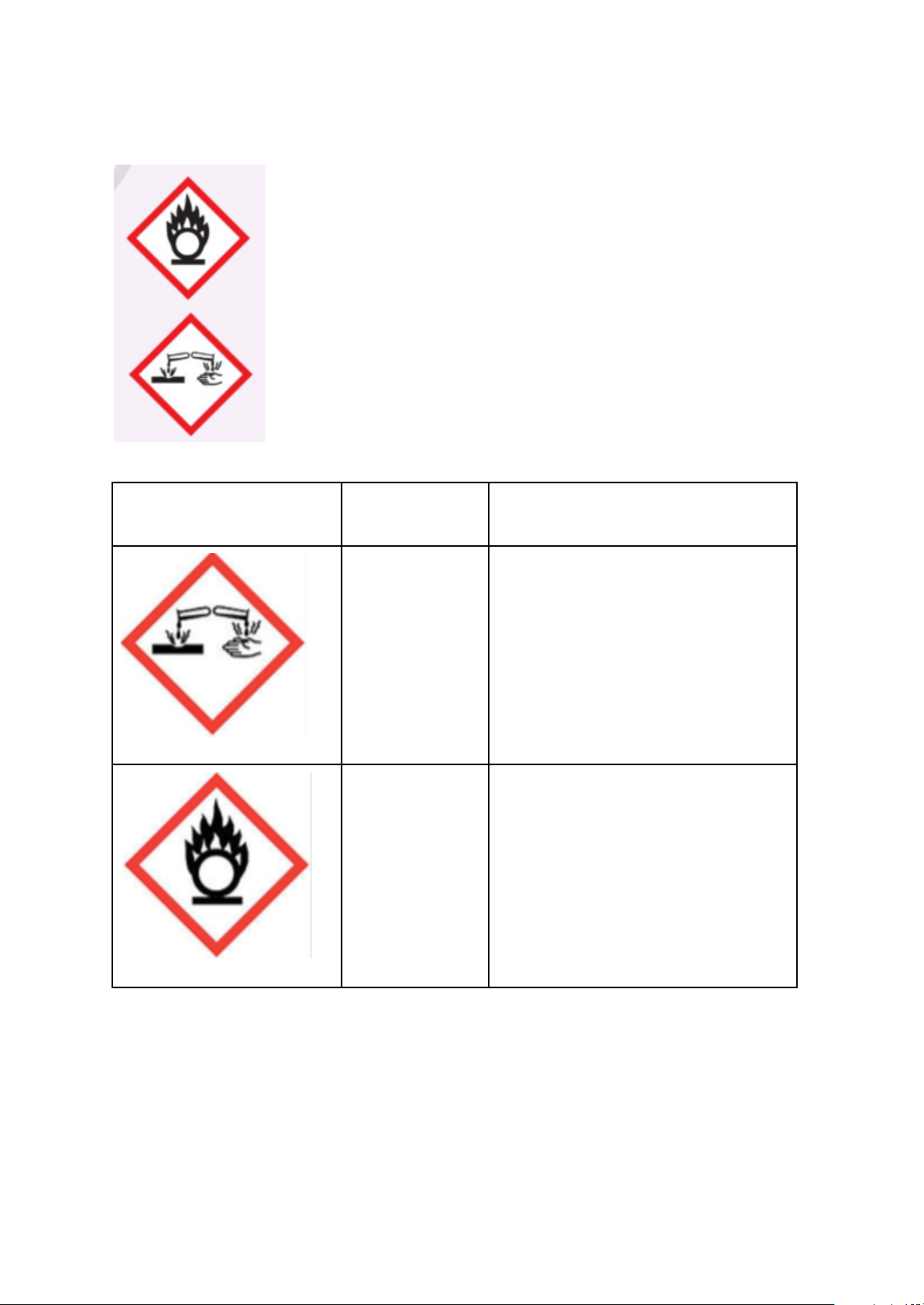
Vận dụng 2 trang 121 KHTN 9: Trên chai đựng acetic acid đặc có các kí hiệu:
Nêu ý nghĩa của các kí hiệu trên. Cần phải làm gì khi sử dụng và lưu trữ acetic acid đặc? Trả lời: Kí hiệu Ý nghĩa Cần làm - Ăn
mòn - Khi sử dụng cần cẩn thận. da/cháy da
- Cần trang bị thiết bị bảo hộ (khẩu
- Tổn thương trang, gang tay, kính mắt …) khi làm mắt
thí nghiệm với acetic acid đặc.
- Ăn mòn kim - Không bảo quản trong đồ kim loại. loại
- Hóa chất dễ - Bảo quản ở nhiệt độ thấp, tránh xa cháy
nguồn nhiệt và các chất dễ cháy.
- Khi sử dụng cẩn thận.
Vận dụng 3 trang 122 KHTN 9: Khi lên men dung dịch ethylic alcohol để sản xuất
acetic acid trong công nghiệp, người ta liên tục sục không khí vào dung dịch. Giải
thích ý nghĩa của việc làm trên. Trả lời:
Ý nghĩa: Cung cấp oxygen hòa tan trong nước cho vi khuẩn “Acetobacter” để lên
men dung dịch ethylic alcohol.
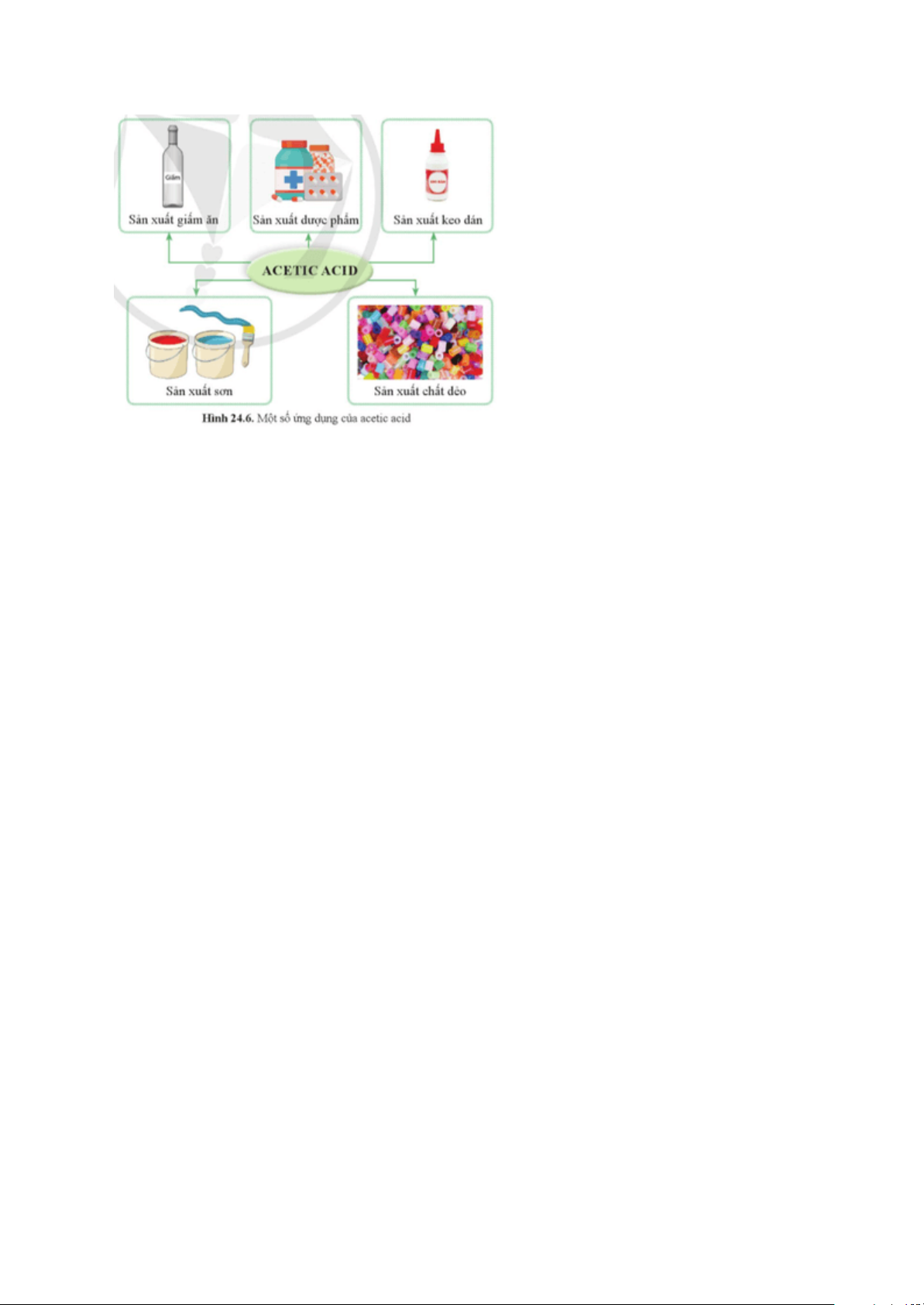
Câu hỏi 5 trang 122 KHTN 9: Dựa vào hình 24.6, nêu một số ứng dụng của acetic acid. Trả lời:
Một số ứng dụng của acetic acid như: - Sản xuất giấm ăn; - Sản xuất dược phẩm; - Sản xuất keo dán; - Sản xuất sơn; - Sản xuất chất dẻo…

