






Preview text:
Sự hấp thụ nhiệt Mục lục 01 02 03 Các khái
Đại lượng đặc trưng cho Quá trình chuyển pha niệm cơ bản hấp thụ nhiệt 04 Một số ví dụ 1 1. Các khái niệm cơ bản Nhiệt độ:
- Nhiệt độ là đại lượng vật lý đặc trưng cho mức độ "nóng – lạnh" của một vật thể.
- Nhiệt độ tỉ lệ với năng lượng chuyển động trung bình của các phân tử cấu thành vật. Nhiệt lượng:
- Nhiệt lượng là phần năng lượng mà vật nhận được hoặc mất đi trong quá trình truyền nhiệt. Trong đó: Q: nhiệt lượng (J) 𝑄 = 𝑚𝑐∆𝑇 m: khối lượng vật (kg)
c: nhiệt dung riêng (J/kg·K)
ΔT: độ tăng/giảm nhiệt độ (K hoặc°C) 2 1. Các khái niệm cơ bản Sự truyền nhiệt:
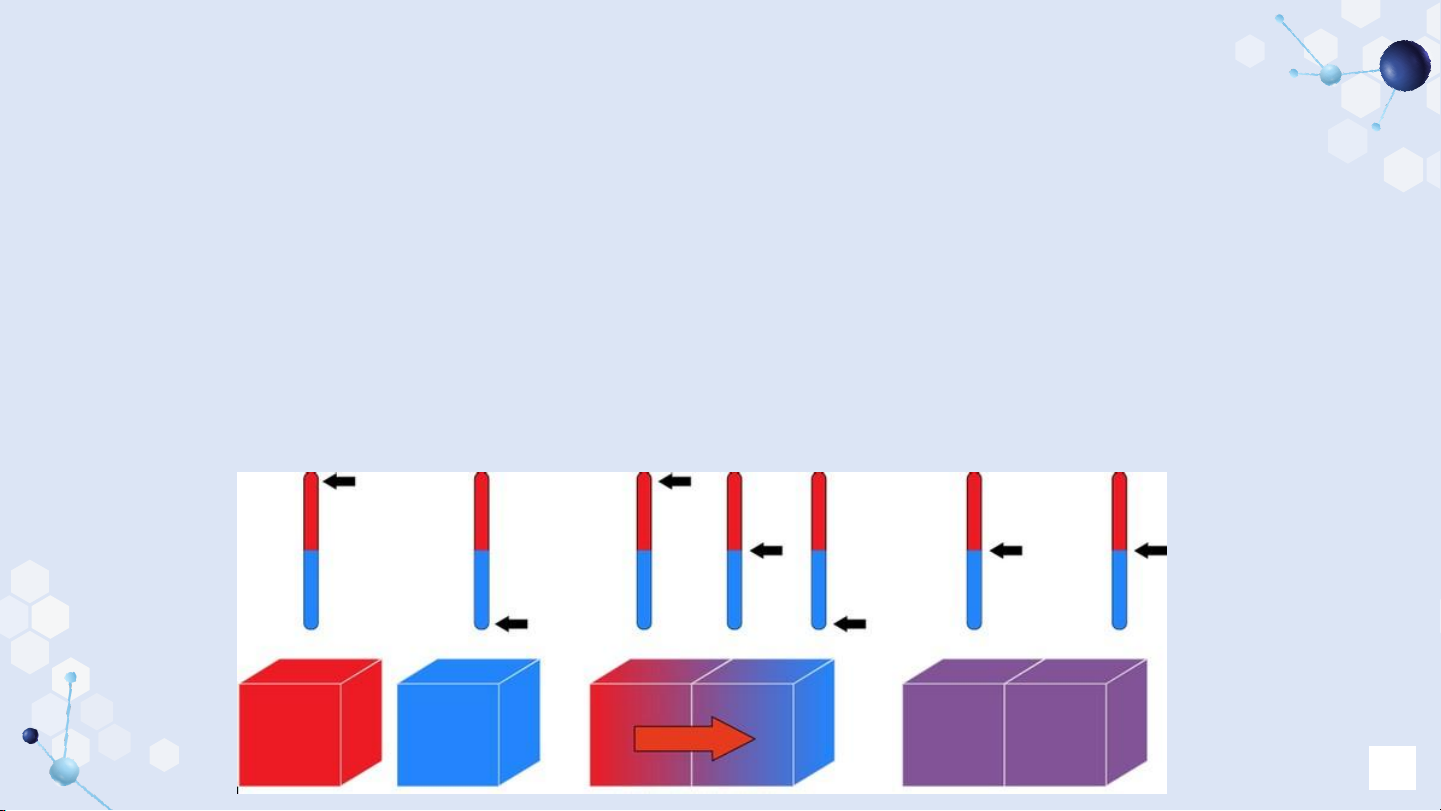
- Trạng thái khi các vật tiếp xúc không còn truyền nhiệt cho nhau nữa,
nghĩa là nhiệt độ của chúng bằng nhau.
- Trong một hệ cô lập, tổng nhiệt lượng thu = tổng nhiệt lượng tỏa:
𝑄𝑡ℎ𝑢 = 𝑄𝑡ỏ𝑎 3
2. Các đại lượng đặc trưng cho sự hấp thụ nhiệt Nhiệt dung:
- Nhiệt dung (C) là lượng nhiệt cần để làm tăng nhiệt độ của toàn bộ một vật thể lên 1 đơn vị nhiệt độ.
- Nhiệt dung thường có đơn vị J/K Nhiệt dung riêng:
- Nhiệt dung riêng (𝑐) là lượng nhiệt cần để làm tăng 1 kg của vật lên 1 K (hoặc 1°C).
- Nhiệt dung riêng thường có đơn vị J/Kg.K Nhiệt dung mol:
- Nhiệt dung mol (𝐶𝑚) là nhiệt lượng cần thiết để làm tăng nhiệt độ của 1 mol chất lên 1 độ K (hoặc 1°C).
- Nhiệt dung mol thường có đơn vị J/mol.K 4
2. Các đại lượng đặc trưng cho sự hấp thụ nhiệt
Công thức nhiệt lượng theo nhiệt dung khác nhau : Trong đó:
Theo nhiệt dung: 𝑄 = 𝐶∆𝑇 𝐽 • C là nhiệt dung.
• ∆𝑇 là độ thay đổi nhiệt độ. Trong đó:
Theo nhiệt dung riêng: • c là nhiệt dung riêng. 𝑄 = 𝑚𝑐∆𝑇 𝐽
• m là khối lượng của vật.
• ∆𝑇 là độ thay đổi nhiệt độ. Trong đó:
• 𝐶𝑚 là nhiệt dung, 𝑚 Theo nhiệt dung mol:
• n là số mol của vật, 𝑄 = 𝑛𝐶𝑚∆𝑇 = 𝐶 𝑀 𝑚∆𝑇 𝐽
• m là khối lượng của vật, • M là khối lượng mol, 5
• ∆𝑇 là độ thay đổi nhiệt độ. 3. Quá trình chuyển pha
- Chuyển pha là quá trình một chất thay đổi
trạng thái vật lý khi có sự thay đổi nhiệt độ hoặc áp suất.
- Quá trình này không làm thay đổi thành phần hóa học của chất.
- Trong quá trình chuyển pha, vật nhận (hoặc
tỏa) nhiệt nhưng nhiệt độ không thay đổi.
- Nhiệt lượng cung cấp không dùng để tăng nhiệt độ, mà để:
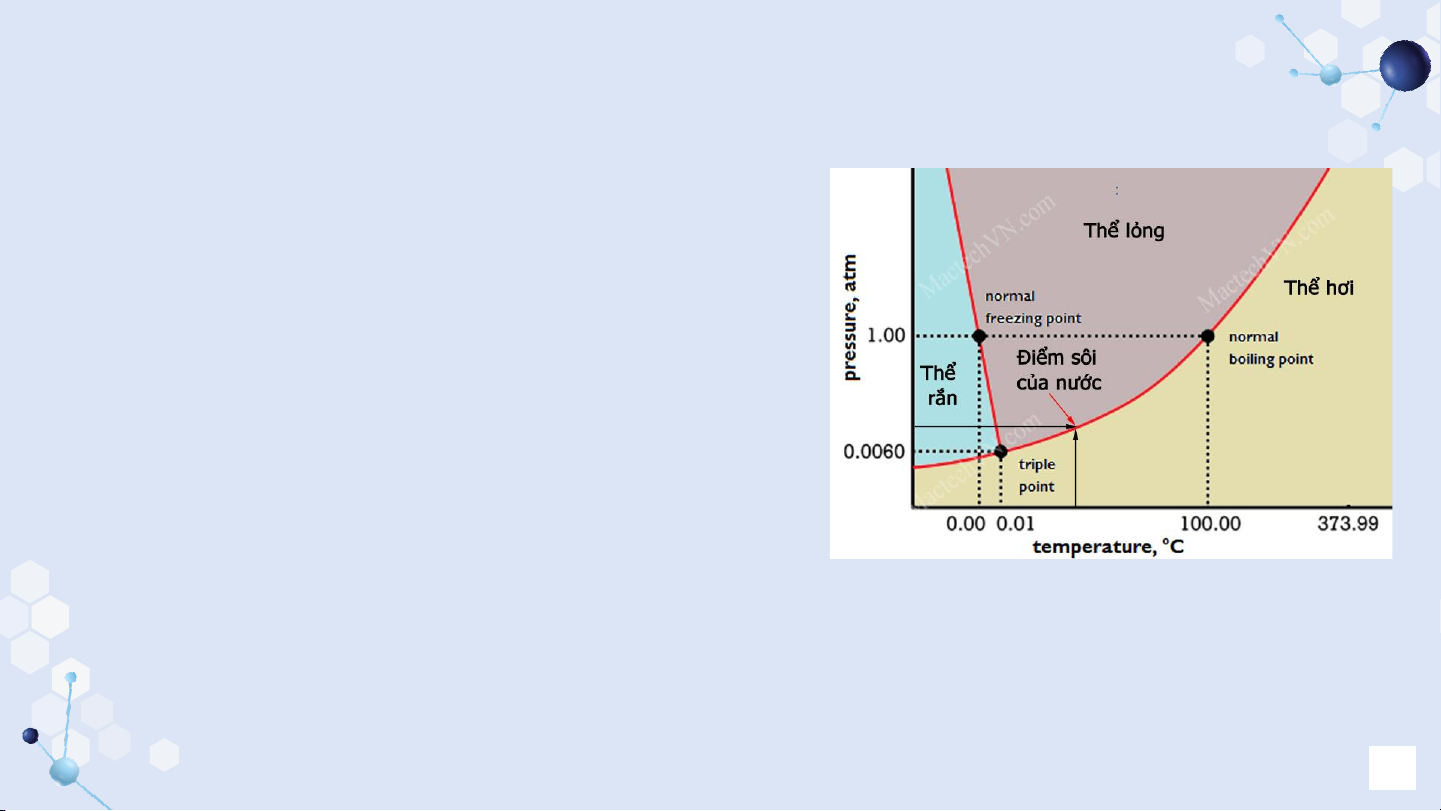
Làm đứt các liên kết giữa các phân tử (khi Giản đồ pha của nước nóng chảy, bay hơi…)
Hình thành liên kết mới (khi đông đặc, ngưng tụ…) 6 3. Quá trình chuyển pha Nhiệt hóa hơi:
Nhiệt hóa hơi là là lượng nhiệt cần thiết để chuyển 1 kg (hoặc 1 mol) chất từ trạng
thái lỏng → hơi tại nhiệt độ sôi, không thay đổi nhiệt độ. 𝑄 = 𝑚𝐿𝑣 Trong đó:
• m (kg) là khối lượng của vật,
• 𝐿𝑣 (J/kg) là nhiệt hóa hơi riêng Nhiệt nóng chảy:
Nhiệt nóng chảy là lượng nhiệt cần thiết để chuyển 1 kg (hoặc 1 mol) chất từ trạng
thái rắn → lỏng tại nhiệt độ nóng chảy, không làm thay đổi nhiệt độ: 𝑄 = 𝑚𝐿𝑓 Trong đó:
• m (kg) là khối lượng của vật, 7
• 𝐿𝑓 (J/kg) là nhiệt nóng chảy riêng 4. Một số ví dụ
Tính nhiệt lượng cần cung cấp cho một miếng nước đá có khối lượng
𝑚=720 𝑔 ở nhiệt độ −10℃ để nó biến thành lỏng ở 15 ℃.
Giả sử ta chỉ cung cấp cho miếng nước đá một nhiệt lượng 𝑄=210 𝑘𝐽.
Xác định trạng thái cuối cùng và nhiệt độ của miếng nước đá sau khi nhận nhiệt.
Cho nhiệt dung riêng của nước đá: 𝑐1=2,22 𝑘𝐽/𝑘𝑔⋅𝐾, nhiệt nóng chảy của nước đá: 𝜆=333 𝑘𝐽/𝑘𝑔, nhiệt dung riêng của nước
𝑐3=4,186 𝑘𝐽/𝑘𝑔⋅𝐾 8 4. Một số ví dụ
1. Làm nóng nước đá từ −10 °C đến 0 °C:
𝑄1 = 𝑚𝑐1∆𝑇 = 15,984 𝑘𝐽
2. Nung chảy nước đá ở 0 °C:
𝑄2 = 𝑚𝜆 = 239,76 𝑘𝐽
3. Làm nóng nước từ 0 °C đến 15 °C: 𝑄3 = 45,2028 𝑘𝐽
Tổng nhiệt lượng cần thiết để làm tan nước đá từ 0 °C đến 15 °C:
𝑄𝑡ổ𝑛𝑔 = 𝑄1 + 𝑄2 + 𝑄3 = 300, 9468 𝑘𝐽
Như vậy nếu cung cấp một nhiệt lượng 210 kJ chỉ đủ làm nước đá bị tan một phần.
Sau khi làm nóng từ −10°C đến 0°C thì còn lại 𝑄′ = 194,016 𝐽
Khối lượng đá tan do lượng nhiệt 𝑄′ 𝑸′ là 𝑚 = = 0.5826 𝑘𝑔 𝜆
Trạng thái cuối cùng bao gồm 137,4g nước đá chưa bị nung chảy và 582,6g nước đã bị nung chảy.
Nhiệt độ cuối cùng của miếng nước đá là 0 °C 9
Document Outline
- Slide 1: Sự hấp thụ nhiệt
- Slide 2: Mục lục
- Slide 3: 1. Các khái niệm cơ bản
- Slide 4: 1. Các khái niệm cơ bản
- Slide 5: 2. Các đại lượng đặc trưng cho sự hấp thụ nhiệt
- Slide 6: 2. Các đại lượng đặc trưng cho sự hấp thụ nhiệt
- Slide 7: 3. Quá trình chuyển pha
- Slide 8: 3. Quá trình chuyển pha
- Slide 9: 4. Một số ví dụ
- Slide 10: 4. Một số ví dụ



![[TailieuVNUcom] Giáo trình Kinh tế chính trị Mác - Lê Nin](https://docx.com.vn/storage/uploads/images/documents/banner/9c3d1c95e250a3c9ef70c03c83de7c08.jpg)