










Preview text:
lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
CHƯƠNG 1: ĐẠI CƯƠNG HÓA DƯỢC ........................................................................................................................................... 1
CHƯƠNG 2: KHÁNG SINH ............................................................................................................................................................... 6
ĐẠI CƯƠNG KHÁNG SINH ................................................................................................................................................................. 6
KHÁNG SINH NHÓM QUINOLON ........................................................................................................................................................ 9
SULFAMID ......................................................................................................................................................................................... 11
PHENICOL .......................................................................................................................................................................................... 14
KHÁNG SINH Β-LACTAM ................................................................................................................................................................... 16
KHÁNG SINH PHOSPHONIC ............................................................................................................................................................... 20
KHÁNG SINH LINCOSAMID................................................................................................................................................................ 22
KHÁNG SINH PEPTID ......................................................................................................................................................................... 23
THUỐC TRỊ VIRUS ............................................................................................................................................................................. 26
THUỐC KHÁNG NẤM........................................................................................................................................................................ 28
THUỐC KHÁNG LAO .......................................................................................................................................................................... 29
CHƯƠNG 5: THUỐC TRỊ UNG THƯ ............................................................................................................................................... 30
CHƯƠNG 8: THUỐC CẢN QUANG ................................................................................................................................................ 33
CHƯƠNG 1: ĐẠI CƯƠNG HÓA DƯỢC. 1.
Nhiệm vụ của Hóa Dược.
- Theo IUPAC, Hóa dược là một ngành khoa học dựa trên nền tảng hóa học để nghiên cứu các
vấn đề của các ngành khoa học sinh học, y học và dược học. 2.
Một số đặc điểm lịch sử quan trọng trong lịch sử hóa Dược (thế kỉ VII – XII, thế chiến
thứ I, thế chiến thứ II…).
- Thế kỉ VII – XII: các nhà luyện đan (Alchimist): tìm được một số muối vô cơ trị bệnh (Hg, As).
- Cuối thế kỷ XIX, đầu thế kỷ XX: ngành tổng hợp hữu cơ phát triển, phát minh phản ứng nitro
hoa benzen tạo nitrobenzen (Zinin, 1812-1880), khử hóá tạo anilin. Từ đó điều chế ra các
phẩm màu anilin, sulfamid, thuốc hạ nhiệt dẫn chất anilin (acetanilid, phenacetin, paracetamol).
- Thế chiến I: công nghiệp hóá dược phát triển rất nhanh ở Đức (do nhu cầu chiến tranh, thay
sản phẩm thiên nhiên bằng tổng hợp).
- Trong và sau thế chiến II: công nghiệp hoá dược phát triển mạnh ởMỹ (từ 1937- 1960 tăng 9 lần). 3.
Các nguồn nguyên liệu cho ngành Hóa Dược (nêu ví dụ).
- Khoáng sản: o Nước ót. o Rong biển: Iod, agar, alginate. o Cát. 1 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược o Quặng mỏ: barytin (BaSO4); Thạch cao
(CaSO4.2H2O); đất sét trắng (kaolin, phèn nhôm) … - Động vật: o Phủ tạng: pancreatin, insulin, thyroxin,
heparin, mật và acid mật… o Sinh
vật biển: prostaglandin, toxin… - Thực vật: o Các alkaloid: morphin, papaverin, cafein, scopolamine, atropine…. o Camphor, tinh dầu… o Terpen khác: artemisinin. - Hóa chất: o Than. o Gỗ. o Khí đốt.
o Cracking dầu mỏ. 4.
Các yếu tố ảnh hưởng đến hiệu quả trị liệu của thuốc. - 2 yếu tố ảnh hưởng đến hiệu quả trị liệu:
• Yếu tố dược học: kỹ thuật bào chế.
• Yếu tố sinh học: người dùng. 5.
Thành phần cấu tạo của 1 phân tử thuốc (nêu các ví dụ về sự thay đổi cấu trúc làm thay
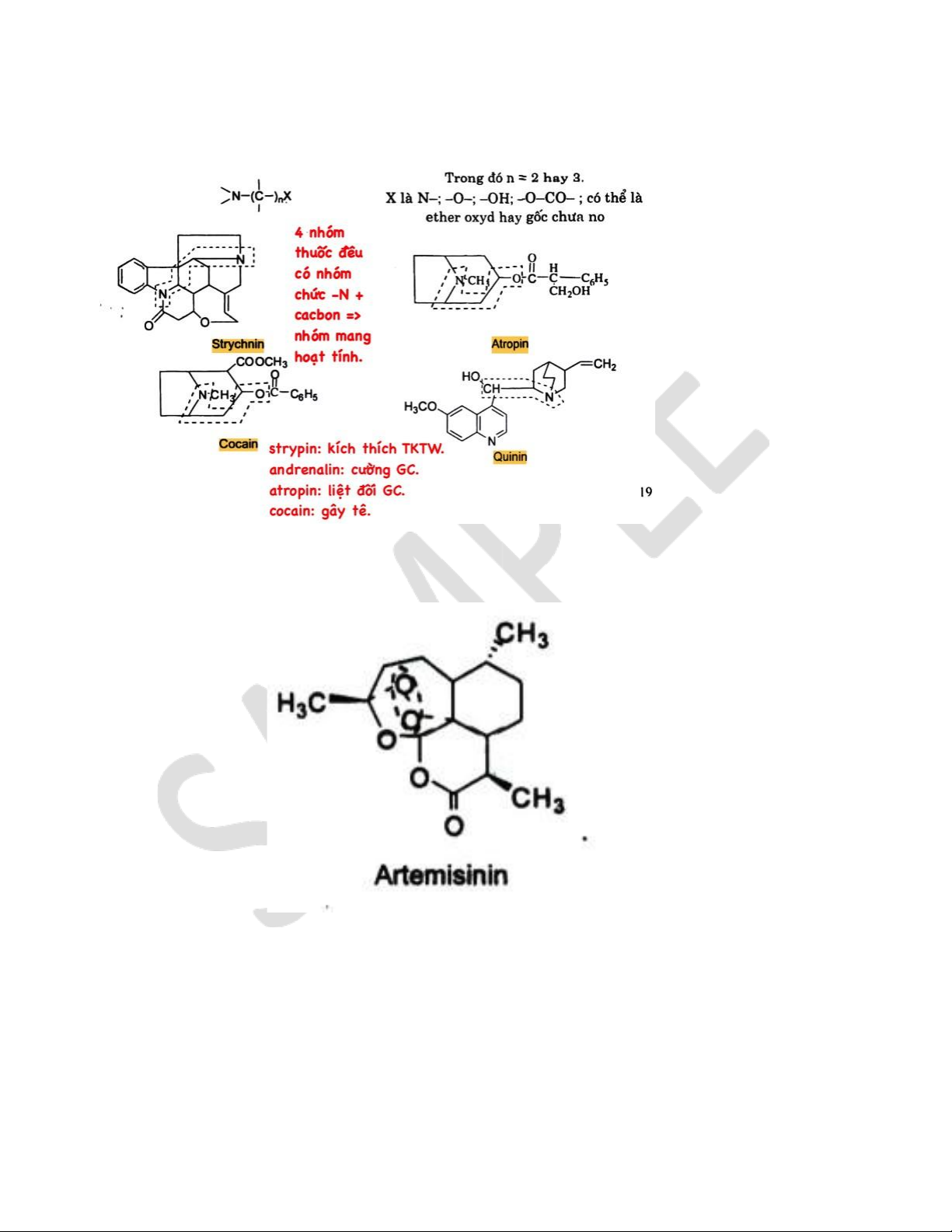
đổi tác dụng: Strychnin, atropine, quinin, acetylcholine, artemisinin, ascaridol, …..).
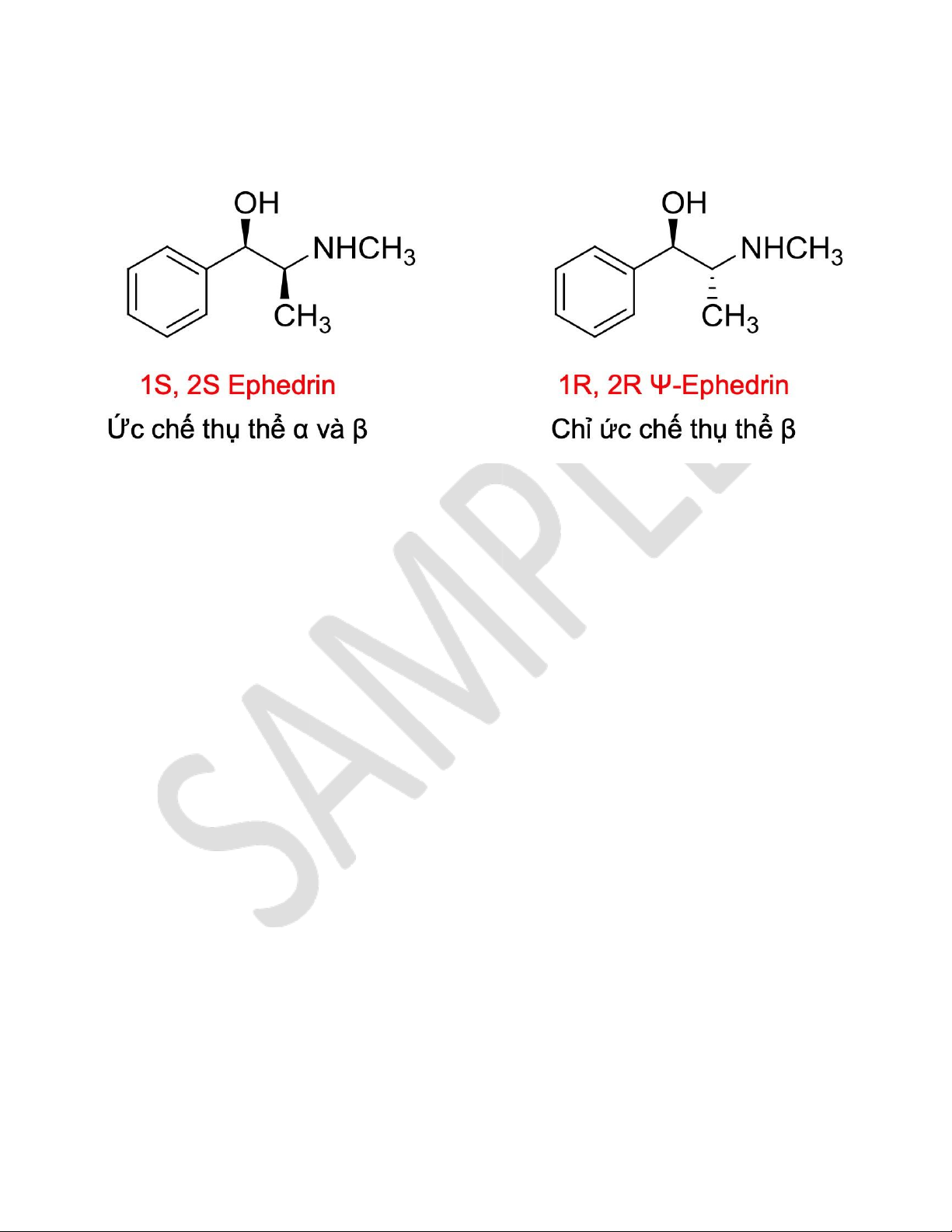
Nêu đặc điểm của các đồng phân quang học, các ví dụ của epinephrin, terpin.
- Thành phần cấu tạo của 1 phân tử thuốc: Khung phân tử và nhóm chức. o VD: Nhóm thuốc
chứa nhóm chất N-Cacbon = hoạt tính dược lực. 2 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
● Strypin: kích thích TKTW. ● Andrenalin: cường GC.
● Atropin: liệt đối GC. ● Cocain: gây tê. ▪
o VD: Artemisin chứa nhóm peroxyd nội (nhóm mang hoạt tính diệt KST) nhưng phải
gắn trong cấu trúc sesquiterpenlacton, tạo nên tác dụng của cả phân tử. 3 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
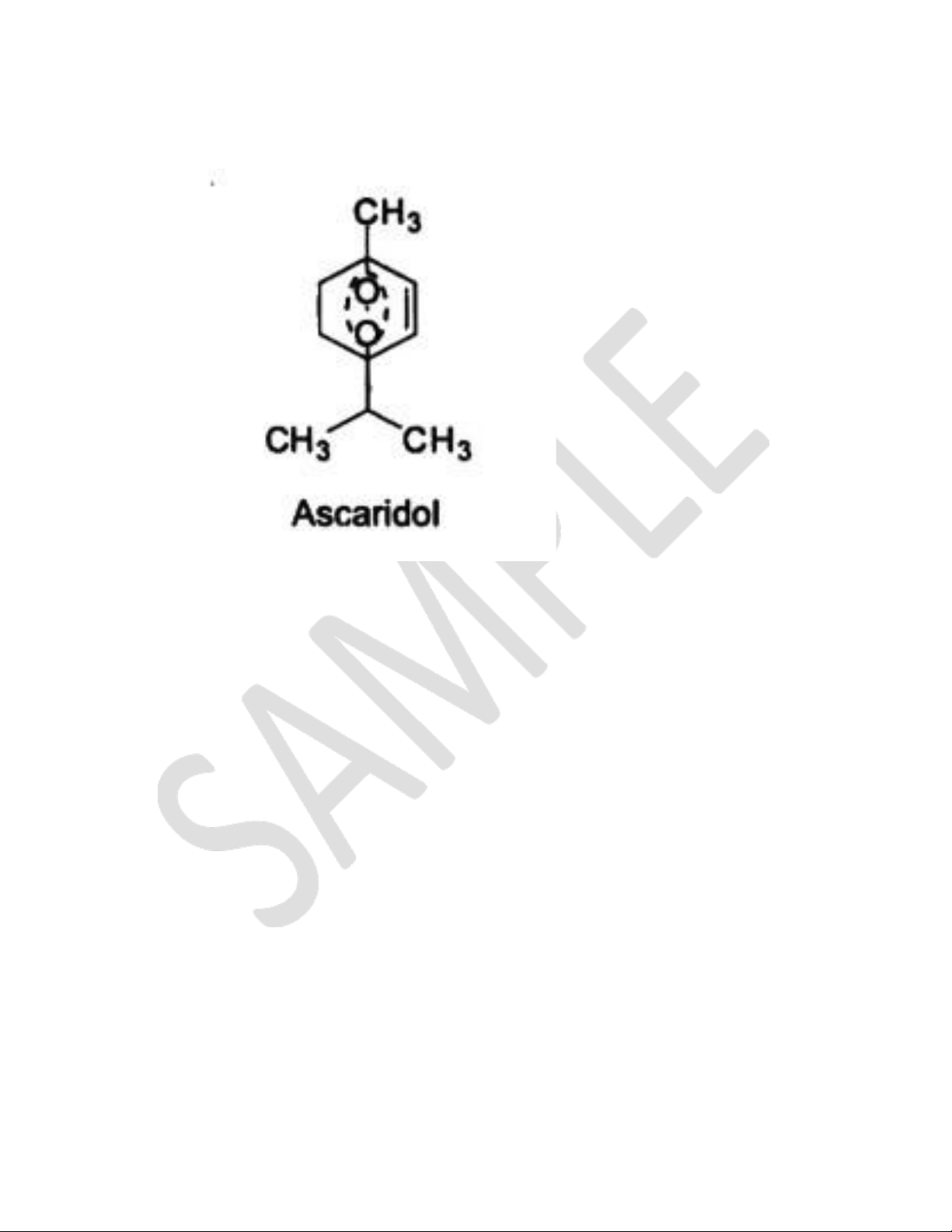
o VD: Ascaridol chứa nhóm peroxyd nội nằm trong cấu trúc monoterpen vòng đơn (trị giun).
- Đặc điểm của đồng phân quang học:
o Các chất đối quang (Enantiomers): Có Carbon bất đối C*.
● Có cùng tính chất lý hóa (To nc, To sôi, d, chỉ số khúc xạ…).
● Quay phải hay quay trái mặt phẳng ánh sáng phân cực.
→ Tác dụng sinh học khác nhau
o Các đồng phân (-) thường có hoạt tính cao hơn (+).
- Các chất không đối quang: (±).
o Có các đặc tính lý hóa như nhau.
o Cấu hình dạng S hay R → tốc độ phản ứng khác nhau. 4 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược 6.
Sự thay đổi các nhóm chức trong phân tử chất hữu cơ ảnh hưởng tới tác động (thay đổi
các hydrocarbon no và không no, nhóm -COOH, Nhóm -OH, Nhóm -SH…).
- Nhóm thiol SH: o Dễ liên kết và phản ứng hóa học (Red-Ox, liên hợp).
o Ứng dụng làm thuốc giải độc, kháng khối U.
- Oxygen: tùy thuộc nhóm chức năng chứa oxy. o OH alcol: làm tăng hoạt tính. Tác dụng gây
ngủ tăng từ alcol bậc nhất lên alcol bậc ba và giảm khi tăng các nhóm OH alcol (tăng vị ngọt).
o OH phenol: làm tăng hoạt tính cũng như độc tính. Phenol biểu hiện tính khử trùng mà
hoạt tính tăng lên theo số lượng nhóm OH.
- Các hợp chất hydrocarbon chưa no: Có hoạt tính mạnh hơn những hợp chất no, đồng thời khả
năng phản ứng của nó cũng cao hơn.
- Nhóm carboxyl có hai nguyên tử oxy làm giảm hoạt tính và độc tính, làm tăng tính hòa tan.
Quá trình acid hoá ảnh hưởng lớn đến hoạt tính và độc tính của các hợp chất hữu cơ. Nó có
thể làm thay đổi hoàn toàn dược lực tính và độc tính của cồn, amin, phenol ban đầu. 7.
Các giai đoạn chính trong nghiên cứu thuốc mới và đưa thuốc ra thị trường.
- Giai đoạn nghiên cứu tiền lâm sàng: Nghiên cứu hoá học + sàng lọc về dược lý (screening). o
Thử tính an toàn trước mắt và lâu dài của thuốc.
o Thử in vitro (vi trùng, ký sinh trùng, virus...), thử in vivo, in situ (trên súc vật thí
nghiệm) và thử trên người tình nguyện.
o Nghiên cứu dược động học (đường đi của thuốc trong cơ thể).
o Lập hồ sơ xin phép thử lâm sàng.
- Giai đoạn nghiên cứu lâm sàng (thử lâm sàng): o Giai đoạn 1: nghiên cứu trên người khoẻ
mạnh và tình nguyện (20-50 người). 5 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
o Giai đoạn 2: nghiên cứu tác dụng của thuốc trên bệnh nhân (số lượng 50-100 người).
o Giai đoạn 3: thử lâm sàng trên số đông bệnh nhân.
o Giai đoạn 4 (thử lâm sàng): theo dõi các tác dụng phụ bất ngờ (các phản ứng có hại
của thuốc khi thuốc đã được lưu hành).
- Nghiên cứu chuẩn bị đưa thuốc (dạng hóa chất dược dụng) ra thị trường. 8.
Các phương pháp điều chế thuốc. - Tổng hợp toàn phần:
o Các phân tử hữu cơ có hoạt tính sinh học. (Ví dụ: các dẫn chất barbituric) - Giống
hợp chất thiên nhiên. (Ví dụ: papaverin, cafein).
o Thay thế hợp chất thiên nhiên. (Ví dụ: pethidin). - Bán tổng hợp:
o Ví dụ: Racemic hoá (-) hyoscyamin→ atropine. o Camphor (không tan trong
nước) sulfon hoá → Na camphosulfonat (tan).
o Penicillinum → A.6AP → các penicilin bán tổng hợp (amoxycilin). - Sinh tổng hợp:
o Acid lactic; glucose → acid citric → vitamin C; glucose → dextran, calci gluconat...
Phương pháp ADN tái tổ hợp (DNA recombinated) sản xuất các hormon (hCG,
insulin), các thuốc interferon (roferon, intron, PEG-intron...).
- Chiết xuất và tinh chế:
o Chiết xuất: artemisinin từ Thanh cao hoa vàng.
o Tinh chế: NaC1 dược dụng từ muối ăn. 9.
Các khái niệm về định tính, định lượng, độ tinh khiết.
- Độ tinh khiết: xác định % tạp chất trong mẫu.
- Định tính: xác định sự hiện diện chất phân tích.
- Định lượng: xác định hàm lượng/nồng độ chất cần phân tích. 10.
Một số các thuốc thử để xác định giới hạn các tạp thường gặp.
- Các Dược điển thường quy định thử giới hạn một số tạp chất ion vô cơ. Dược điển Việt Nam
III quy định thử giới hạn các ion sau trong thuốc: amoni, arsenic, calci, chì trong đường,
clorid, kali, kim loại nặng, nhôm, nikel trong polyols, phosphat, sắt, sulfat, magnesi,
magnesi và kim loại kiềm thổ.
CHƯƠNG 2: KHÁNG SINH
ĐẠI CƯƠNG KHÁNG SINH
1. Định nghĩa kháng sinh. -
Kháng sinh là những chất ức chế sự phát triển và sống sót của vi sinh vật mà không gây độc
tính trầm trọng trên ký chủ. 6 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
2. Phân biệt kháng sinh kiềm khuẩn và kháng sinh diệt khuẩn. Cho biết những kháng sinh
thuộc họ nào diệt khuẩn và những kháng sinh thuộc họ nào kìm khuẩn? -
Sự kiềm khuẩn: ức chế sự nhân đôi/tổng hợp protein (trừ aminoside) của vi khuẩn tại liều điều trị. -
Sự diệt khuẩn: giết vi khuẩn tại liều điều trị.
3. Cách sử dụng kháng sinh hợp lý. -
Kháng sinh cần được sử dụng ngay khi có thể. -
Tuân thủ điều trị và không ngừng điều trị trong quá trình trị liệu.
4. Cách phối hợp kháng sinh đúng: Nên phối hợp 2 cái cùng loại: diệt khuẩn + diệt khuẩn or kiềm
khuẩn + kiềm khuẩn khác cơ chế tác động.
5. Tận cùng (tiếp vị ngữ) của các kháng sinh nhóm penicillin, flouroqinolon, các kháng sinh
được sản xuất từ Micromonospora, Streptomyces. -
Fluoroquinolon: tiếp vĩ ngữ -floxacin. -
Penicillin: tiếp vĩ ngữ -cillin. -
Streptomyces: tiếp vĩ ngữ -mycin. -
Micromonospora: tiếp vĩ ngữ -micin.
6. Định nghĩa kháng sinh, cơ chế tác dụng của kháng sinh. 7 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
7. Nguyên tắc sử dụng kháng sinh. -
Chỉ dùng kháng sinh khi có nhiễm khuẩn. - Chọn đúng kháng sinh. -
Chọn dạng dùng thích hợp. -
Sử dụng kháng sinh đúng liều lượng. -
Sử dụng kháng sinh đúng thời gian quy định. -
Sử dụng kháng sinh dự phòng hợp lý. -
Phối hợp kháng sinh khi cần thiết.
8. Phổ kháng khuẩn của kháng sinh, tác động hậu kháng sinh. -
Tác động hậu kháng sinh: vài kháng sinh thể hiện độc tính đáng kể trên một vài vi khuẩn
mà độc tính này vẫn kéo dài trong một thời gian sau khi ngừng kháng sinh. -
Mỗi KS chỉ tác dụng lên một số chủng vi khuẩn nhất định, gọi là phổ kháng khuẩn KS.
9. Kháng sinh tác động phụ thuộc thời gian, nồng độ. 8 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
KHÁNG SINH NHÓM QUINOLON 1.
Tên gọi khung cấu trúc chung của quinnolon: 1,4-dihydro-oxo-3-pyridinecarboxylic. 2.
Đặc điểm của các quinolone thế hệ đầu? thế hệ sau (về cấu trúc, về tác dụng, chỉ định, tác dụng phụ).
- Các quinolon thế hệ 1 không chứa F (trừ flumequin), hấp thu kém và chuyển hoá nhiều ở
gan thành sản phẩm không có tác dụng. Phổ kháng khuẩn của những chất này hẹp, chỉ có tác
dụng trên một số vi khuẩn đường ruột và đường tiết niệu: E. coli, Proteus, Salmonella,
Enterobacter, Gonorrhea. Nhóm này bị đề kháng nhanh do đó hiện nay ít được sử dụng.
- Các quinolon thế hệ lI: Gắn thêm floro vô vị trí số 6 => tác động trên ADN gyrase và enzym
topoisomerase => ức chế tổng hợp acid nucleic vi khuẩn => tác động kháng sinh x10, mở
rộng phổ sang gram +. 3.
Quinolone chuyển tiếp giữa thế hệ 1 và 2 có tên là gì? Flumequine. 4.
Cơ chế tác dụng của quinolone: Ức chế tổng hợp acid nucleic vi khuẩn. 5.
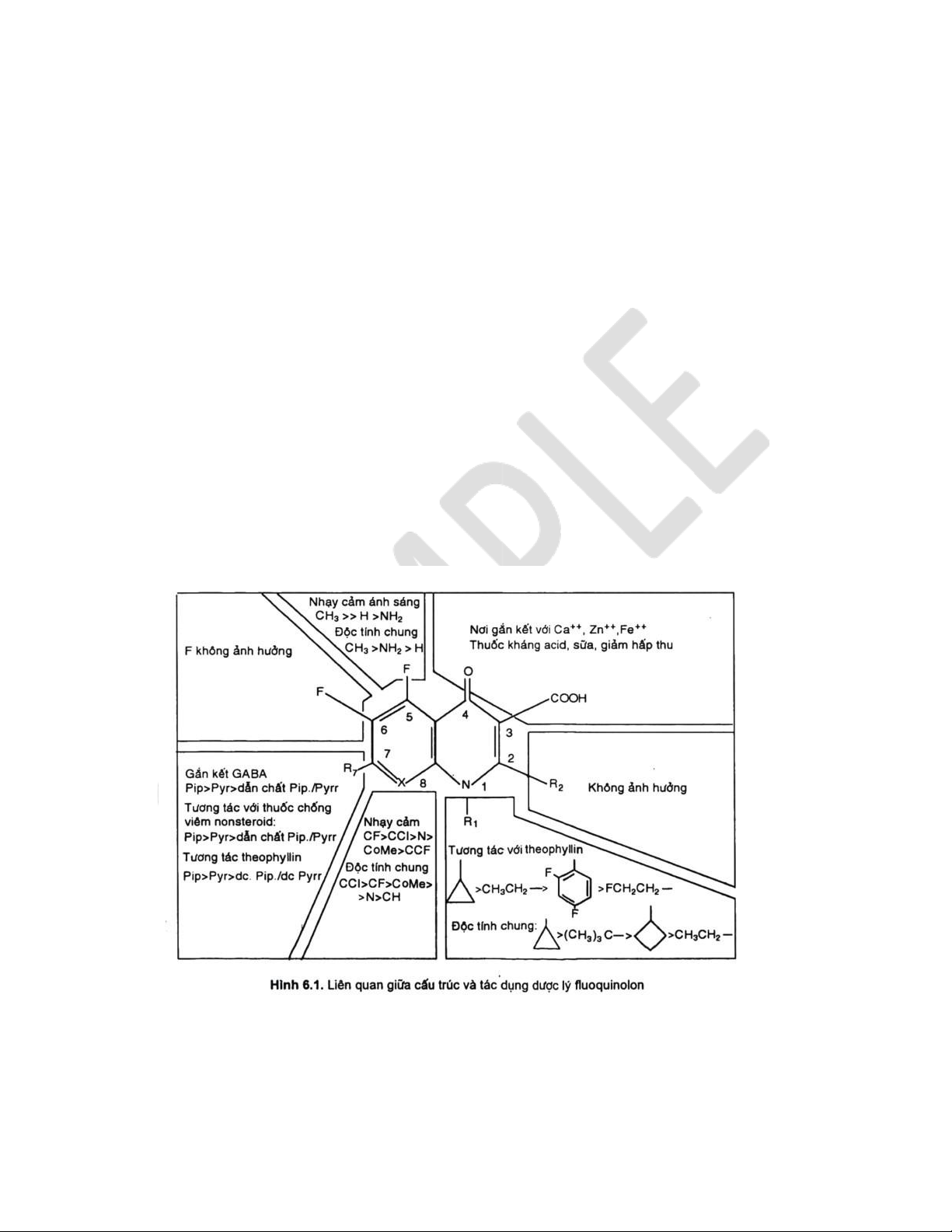
Liên quan cấu trúc và tác dụng của quinolon.
- Nhân quinolon = pyridin + phenyl.
- Vị trí số 3 là - cooh và số 4 -C=O (nhóm thế bắt buộc) => tác động dược lực + dễ tạo phức
chelat với Ca2+ máu = loãng xương/dễ đứt gân archilles và sụn.
- R5 gắn nhóm với methyl (tăng tác động trên G-) khiến da dễ bị nhạy cảm ánh sáng tăng nguy cơ kích ứng.
- Vị trí 6 gắn -F, gắn với nhóm thế khác giảm tác dụng. 9 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
- Vị trí số 7 thêm -N-CH3 thì tăng T1/2 (liên kết chặt với pro HT), gắn với nhóm PIPERZARIN:
gắn đc với trực khuẩn mũ xanh do qua được màng lipid tác dụng với trực khuẩn mũ xanh.
- Vị trí R1: gắn với nito bậc 3 (kiềm yếu)/nhóm akyl ngắn. 6.
Định tính quinolone:
- Dùng các phương pháp hóa lý: phổ tử ngoại, hồng ngoại, sắc ký lớp mỏng, sắc ký lỏng hiệu năng cao.
- Phản ứng tạo phức: các quinolon đều có thể tạo phức chelat với các ion hóá trị 2,3 như Ca*+, Mg, Al, Fe….
- Nhóm acid có thể cho phản ứng tạo ester.
- Nhóm C=0 cho phản ứng với natri nitroprussiat cho màu đặc trưng.
- Cấu trúc cứng nhắc, cồng kềnh, nối đôi liên hợp
phát huỳnh quang trong mt acid H2SO4. 7.
Kể tên các quionolon thế hệ 1: Acid oxolinic, Cinoxacin, Mibxacin, Acid piromidic, Acid pipemidic, Resoxacin. 8.
Kể tên các thuốc kháng sinh thuộc nhóm quinolone: ciprofloxacin, ofloxacin, sparfloxacin,
norfloxacin, lomefloxacin, moxifloxacin. 9.
Phương pháp định lượng ciprofloxacin: - Sắc ký lớp mỏng. - Phản ứng của ion F.
- Phổ hồng ngoại so sánh với phổ của chất chuẩn.
- Phản ứng của C=0: với natri nitroprussiat cho màu tím. 10.
Mô tả cấu trúc của ciprofloxacin.
- Có vòng nito 5 + R1 (amin bậc 3) gắn với 1 cyclonakan. 11.
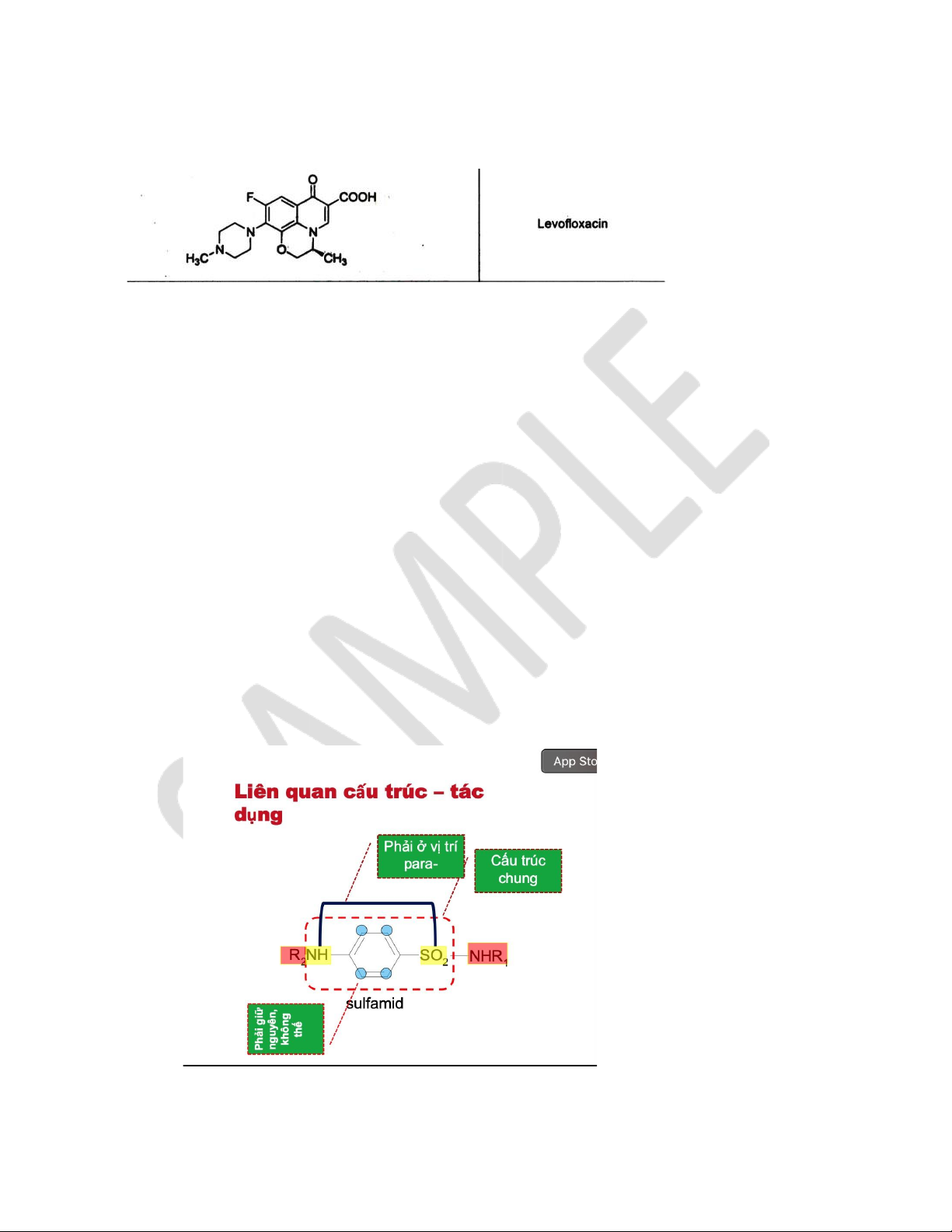
So sánh đặc điểm cấu trúc của ofloxacin và levofloxacin. 10 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
- Dị vòng nito của levo có gắn thêm nhóm -CH3.
- Vị trí cacbon số 8 gắn nhóm ete tăng độ phân cực. THUỐC KHÁNG LAO
1. Kể tên các thuốc kháng lao.
2. Tác dụng của các thuốc kháng lao.
3. INH: tên gọi, nguyên liệu tổng hợp, cơ chế tác dụng, tính chất hóa học, phương pháp định tính và định lượng.
4. Rifapicin: màu sắc, cơ chế tác dụng, phương pháp định lượng.
5. Ethambutol: cơ chế tác dụng, phương pháp định, định lượng.
6. Pyrazinamid: cơ chế tác dụng, Phương pháp định tính, định lượng. SULFAMID 1.
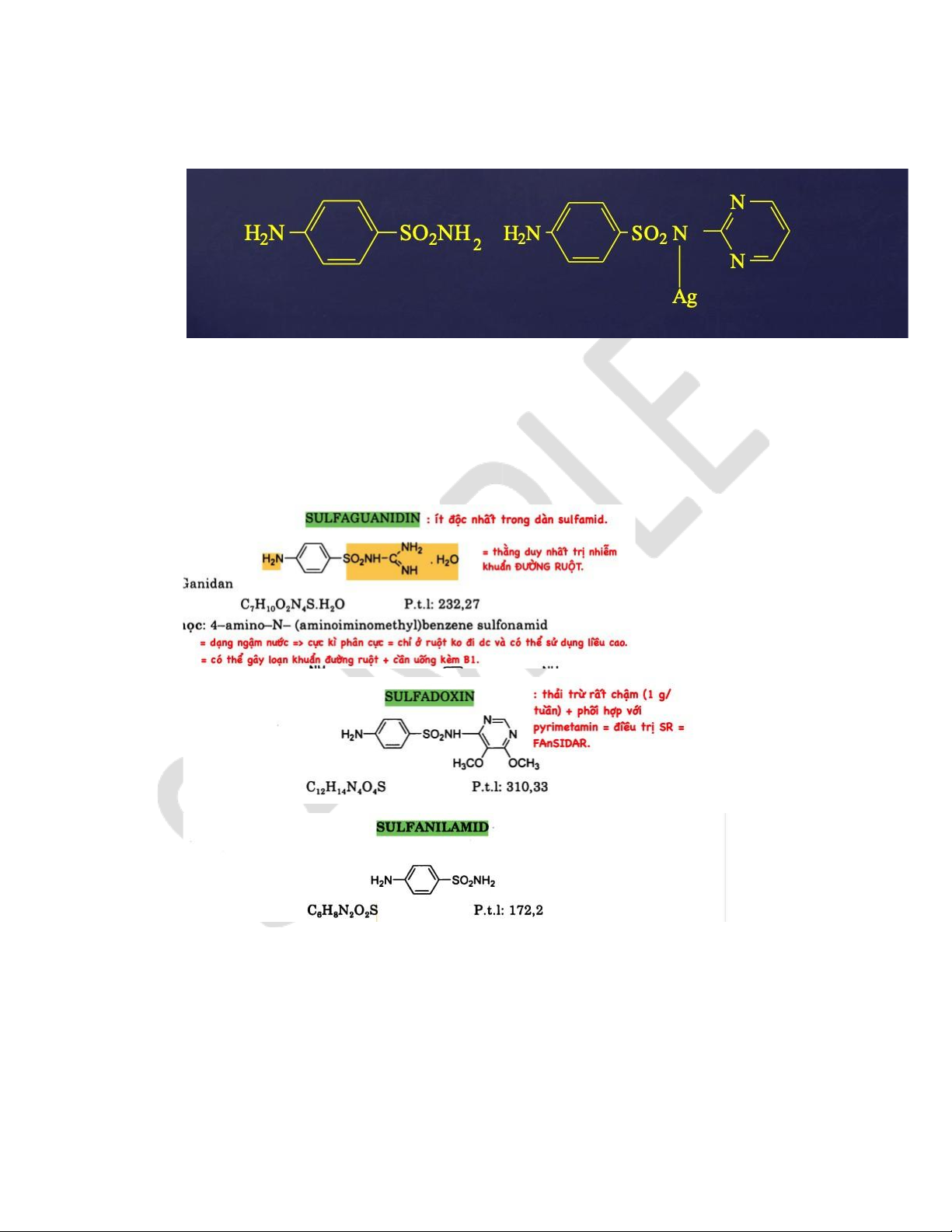
Kể tên các sulfamid đời đầu (TH1): sulfanilamid, sulfapyridin, sulfathiazol, sulfasalazin, sulfadiazin. 2.
Liên quan cấu trúc và tác dụng của sulfamid.
- Phải có vòng benzen như PABA.
- Phải có nhóm SO2 tại -para.
Khi thay nhóm sulfamid bằng các nhóm khác đều làm giảm hay làm mất tác dụng. 11 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
- Không thể gắn lên vị trí 1-2-3-4 C vì khác cấu trúc PABA.
- N4 phải gắn trực tiếp trên nhân thơm.
- Nhóm NH2 phải ở vị trí para với nhóm sulfamid mới có tác dụng.
Nhóm NH2 phải tự do, mọi sự thế trên NH2 đều làm mất tác dụng. 3.
Các giai đoạn trọng điều chế sulfamid từ anilin (tên gọi, phương trình phản ứng).
- Giai đoạn 1: Bảo vệ nhóm amin.
- Giai đoạn 2: sulfon hoá.
- Giai đoạn 3: Thuỷ phân giải phóng sulfamid. 12 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược 4.
Phản ứng tổng hợp sulfacetamide, sulfaguanidin từ sulfanilamid: câu trên. 5.
Tính chất hóa học của sulfamid: lưỡng tính.
- Tính acid: sulfamid tan trong kiềm loãng.
- Tính base: do có nhóm NH2 tự do nên các sulfamid cho muối với các acid. 6.
Các phương pháp định lượng sulfamid.
- Phương pháp chuẩn độ acid - base.
- PDAB: andehyd = phản ứng tạo imin.
- Tính base yếu thì môi trường khan: chỉ thị tím tinh thể > < mạnh thì môi trường nước.
- Tính acid yếu: định lượng trong môi trường khan. Dung môi thường dùng là
dimethylformamid, chất chuẩn độ là natri methylat, chỉ thị xanh thymol. - Tủa Ag. 7.
Cơ chế tác dụng kháng khuẩn của sulfamid: ức chế sự chuyển hoá acid folic do cạnh tranh PABA. 8.
Dược động học của sulfamid:
- Hấp thu qua đường ruột là ít tác dụng phụ nhất.
- Sulfamid dược phân phối khắp các tế bào của cơ thể. Sulfamid có thể nhanh chóng đi vào
màng phối, hoạt dịch mắt và các dịch tương tự.
- Sulfamid có thể đi vào màng não.
- Sulfamid kết hợp với protein huyết tương tốt: dùng với thuốc trị liệu hẹp tăng C tự
do thuốc tăng độc tính thuốc.
- Acetyl hoá: quá trình acetyl hoá sulfamid xảy ra ở gan.
- Sulfamid liên hợp: glucuronic nhiều thường được dùng làm thuốc kháng khuẩn đường tiết niệu. 9.
Đặc điểm của sulfamid tác dụng nhanh: hấp thụ nhanh/thải trừ nhanh = uống liên tục. 10.
Kể tên các sulfamid tác dụng nhanh: sulfanilamid, sulfapyridin, sulfathiazol, sulfasalazin, sulfadiazin. 11.
Kể tên các sulfamid tác dụng chậm: sulfadxon, sulfadimethoxin, sulfamethoxyprydiazin. 12.
Kể tên các sulfamid tác động trung gian: sulfamethoxazol. 13.
Độc tính trên thận của các sulfamid: gây kết tinh khiến tổn thương thận, viêm thận, sỏi
thận, đái ra máu ... 14.
Sulfacetamide: tác dụng, phân nhóm. 15.
Cấu trúc của sulfamid dùng ngoài, tác dụng nhanh, tác dụng chậm, tiết niệu,
sulfaguanidin, sulfanilamid, sulfadoxin. - Dùng ngoài: 13 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược - Tác dụng nhanh: o
Hấp thu, thải trừ nhanh nên phải uống nhiều lần. o
Ít liên hợp protein. o Liên hợp glucuronic nhiều. o
Thường là những sulfamid
thế hệ đầu. o Dễ gây kết tinh ở thận. o Đào
thải nhanh ít tích lũy nên tương đối ít độc. PHENICOL
1. Tính chất hóa học của chloramphenicol: - Nhóm nitro thơm:
o Khử hoá nhóm nitro trong cloramphenicol thành amin thơm bậc nhất, sau đó tạo muối
diazoni và tạo phẩm màu azoic với B-naphtol. 14 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
o Khử hóa từng phần nhóm nitro bởi Zn/CaCl, tạo N-arylhydroxylamin, chất này được
chuyển thành dẫn chất hydroxamic khi tác dụng với benzoyl clorid, sản phẩm thu được
tạo phức với Fe2+ cho màu đỏ tím.
o Đun nóng cloramphenicol với dung dịch NaOH, màu vàng xuất hiện, sau đó chuyển thành màu cam. - Nhóm dicloacetyl:
o Khi đun nóng cloramphenicol với KOH, thu được dung dịch chứa ion Cl- cho o
phản ứng trầm hiện với AgNO3/HNO3.
o Phản ứng Fujiwara-Ross đặc trưng cho nhóm gem-diclo: đun cách thủy cloramphenicol
với pyridin và NaOH, màu đỏ xuất hiện.
- Nhóm alcol bậc nhất:
o Phản ứng tạo ester với các acid tương ứng cho các tiền chất của cloramphenic bớt đắng.
2. Phương pháp định lượng chloramphenicol.
- Phương pháp vô cơ hoá, xác định hàm lượng Cl, từ đó suy ra hàm lượng cloramphenicol.
- Phương pháp quang phổ tử ngoại ở 278 nm.
- Phương pháp sắc ký lỏng.
- Phương pháp vi sinh
3. Cấu trúc của chloramphenicol, thiamphenicol.
- Cấu trúc của thiamphenicol tương tự cloramphenicol, nhưng nhóm thế nitro ởvị trí para được
thay bằng nhóm methyl-sulfonyl.
- Cấu trúc cloramphenicol gồm ba phần: nhân benzen nitro hoá ở vị trí para, chuỗi amino-2
propandiol-1,3 và nhóm dicloracetyl. Trong cấu trúc có 2 C* (carbon bất đối) nên có 4 đồng
phân quang học, nhưng chỉ có đồng phân D(-) là có hoạt tính.
4. Dạng đồng phân quang học có hoạt tính của chloramphenicol: đồng phân D(-) là có hoạt tính.
5. Liên quan cấu trúc và tác dụng của chloramphenicol. - NO2 ngay vị trí para.
- 2 C* (carbon bất đối) nên có 4 đồng phân quang học.
- Không đc thay thế 2 nhóm - OH.
- Thế -so2ch3 thì độc tính giảm, hoạt tính tăng.
6. Nguyên liệu tổng hợp chloramphenicol: para nitroacetophenon, acetophenon,
paranitrobenzaldehyd, styren, alçol cinamic.
7. Tính tan của chloramphenicol: ít tan trong nước (2,5mg/ml), dễ tan trong propylen glycol
(150,8 mg/ml), rất tan trong methanol, ethanol, ethyl acetat, aceton. 15 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
8. Đặc điểm tiền chất của chloramphenicol: ester palmitat, stearat không dắng (không tan trong
nước) dùng cho trẻ em hoặc ester succinat natri, glicinat tan được dùng làm thuốc tiêm. KHÁNG SINH Β-LACTAM
1. Cơ chế tác dụng, đề kháng, phổ kháng khuẩn (P.aureus, MRSA), phân bố (hàng rào máu não). - Cơ chế tác dụng:
o Ức chế hoạt động của các transpeptidase, còn được gọi là các PBP (Penicillin
Binding Proteins), enzym tham gia vào quá trình tổng hợp peptidoglycan (thành
phần chính của vách tế bào vi khuẩn).
o Hoạt hoá hệ thống thủy giải ở tế bào vi khuẩn, gây tổn thương và giết chết vi khuẩn. - Đề kháng:
o Đề kháng enzym: vi khuẩn tiết ra beta lactamase, thủy phân vòng beta lactam tạo
những dẫn chất không có hoạt tính.
o Đề kháng không enzym bằng cách thay đổi tính thẩm thấu của màng tế bào vi khuẩn:
biến mất hoặc biến đổi các transpeptidase. - Phổ kháng khuẩn: tuỳ thuộc từng loại b- lactam.
2. Liên quan cấu trúc – tác dụng.
- Hoạt tính kháng khuẩn của những kháng sinh họ B-lactam phụ thuộc vào:
o Sự nguyên vẹn của vòng B-lactam (Có 3 C bất đối, 2 phải ở đồng phân S,
số 5 và 6 đồng phân R).
o - COOH: có khả năng phân huỷ polypeptid - ngay vị trí C1 hoặc C5. o Nito số 1, cacbon số 5
giống transpeptid để gắn vào bất hoạt. o
Acyl ngoại vòng: tăng khả năng gắn kết với transpeptid. o Sự kết hợp
dị vòng B-lactam với một dị vòng khác.
3. Tác nhân ảnh hưởng đến cấu trúc vòng β-lactam.
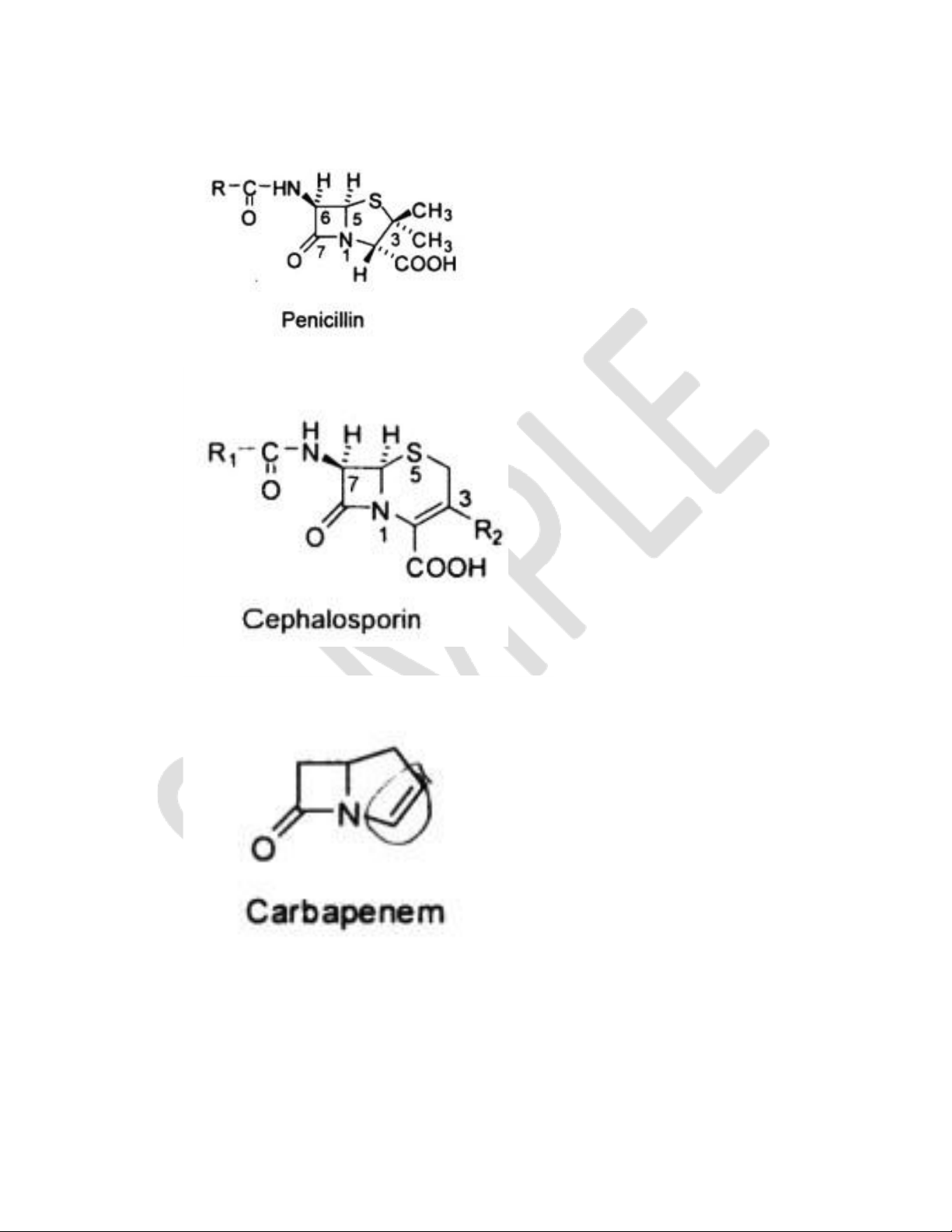
4. Cấu trúc chung của penicillin, cephalosporin, carbapenem.
- Penicilin: Azetidin-2- on +thiazolidin → cấu trúc penam. 16 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
- Cephalosporin: Azetidin-2-on +dihydrothiazin → cấu trúc cephem.
- Carbapenem: Sự thay thế S bằng CH2.
5. Cách điều chế penicillin, cephalosporin. - Penicilin:
o Phương pháp sinh học: Các penicillin thiên nhiên có được từ môi trường nuôi
cấy Penicillium notatum + tiền chất tương ứng.
o Phương pháp bán tổng hợp: Giai đoạn tạo 6-APA giai đoạn acyl hoá 6 - APA. - Cephalosporin: 17 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
o Bán tổng hợp từ cephalosporin C: Cephalosporin C từ sự lên men được thủy giải
thành acid 7- aminoce - phalosporinic (TACA), sau đó có thể biến đổi (hoặc
không) ở R3, tiếp tục được acyl hoá bằng acid clorid thích hợp.
o Bán tổng hợp từ penicillin: mở rộng vòng thiazolidinyl của penicillin bằng cách
gắn thêm một nhóm CH2 ở vị trí 2 sau đó biến vòng penam thành vòng cephem.
6. Định tính penicillin: IR, phản ứng định tính chung, phân biệt.
- Tác nhân mở vòng hydroxylamin: tạo ra kết tủa xanh ngọc dẫn xuất acid hydroxylamin
(phản ứng với đồng) phản ứng định tính chung.
- Phản ứng với thuốc thử acid sulfuric-formaldehyd: định tính phân biệt.
7. Định lượng penicillin.
- Phương pháp oxy hóa khử. o
Penicillin D-penicillamin + acid
penaldic - Phương pháp HPLC.
- Phương pháp vi sinh vật.
8. Phân biệt cấu trúc các thế hệ penicillin. Link word:
https://docs.google.com/document/d/1F7NZAc-LI3Euc7rie-prhH6YUiwZRqqV/edit?usp=
drive_link&ouid=105251606966754388486&rtpof=true&sd=true. 9. Chất
cần kiểm giới hạn trong kiểm tinh khiết Ampicillin và Amoxicillin: N,N-dimethylanilin.
10. Đặc điểm của cephalosporin, cấu trúc cần lưu ý khi sử dụng.
Đặc điểm của cephalosporin C:
- Khó ly trích và tinh chế do bởi nhánh bên rất phân cực. - Không độc. - Nguy cơ dị ứng thấp.
- Bền hơn penicillin G đối với sự thủy giải của acid. 18 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
- Bền hơn penicillin G đối với penicillinase (tương đương với oxacillin). - Hoạt tính trên cả vi
khuẩn Gram dương lẫn Gram âm.
11. Đặc điểm cấu trúc các thế hệ cephalosporin, đường sử dụng.
12. Phân loại các cephalosporin theo cấu trúc.
13. Liên quan cấu trúc – tác dụng của các thế hệ cephalosporin (tính kháng khuẩn, tác động trên gram dương). Link word:
https://docs.google.com/document/d/1F7NZAc-LI3Euc7rie-prhH6YUiwZRqqV/edit?usp=
drive_link&ouid=105251606966754388486&rtpof=true&sd=true.
14. Định tính cephalosporin (UV, IR).
- Phổ UV: cấu trúc cephem cho hai hấp thu cực đại ở 260 nm và 220 nm.
- Phổ IR: như trường hợp penicillin vùng 1600 - 1800 cm-1 là vùng đặc trưng nhất.
15. Cấu trúc có tác động bảo vệ vòng β-lactam của các thế hệ cephalosporin.
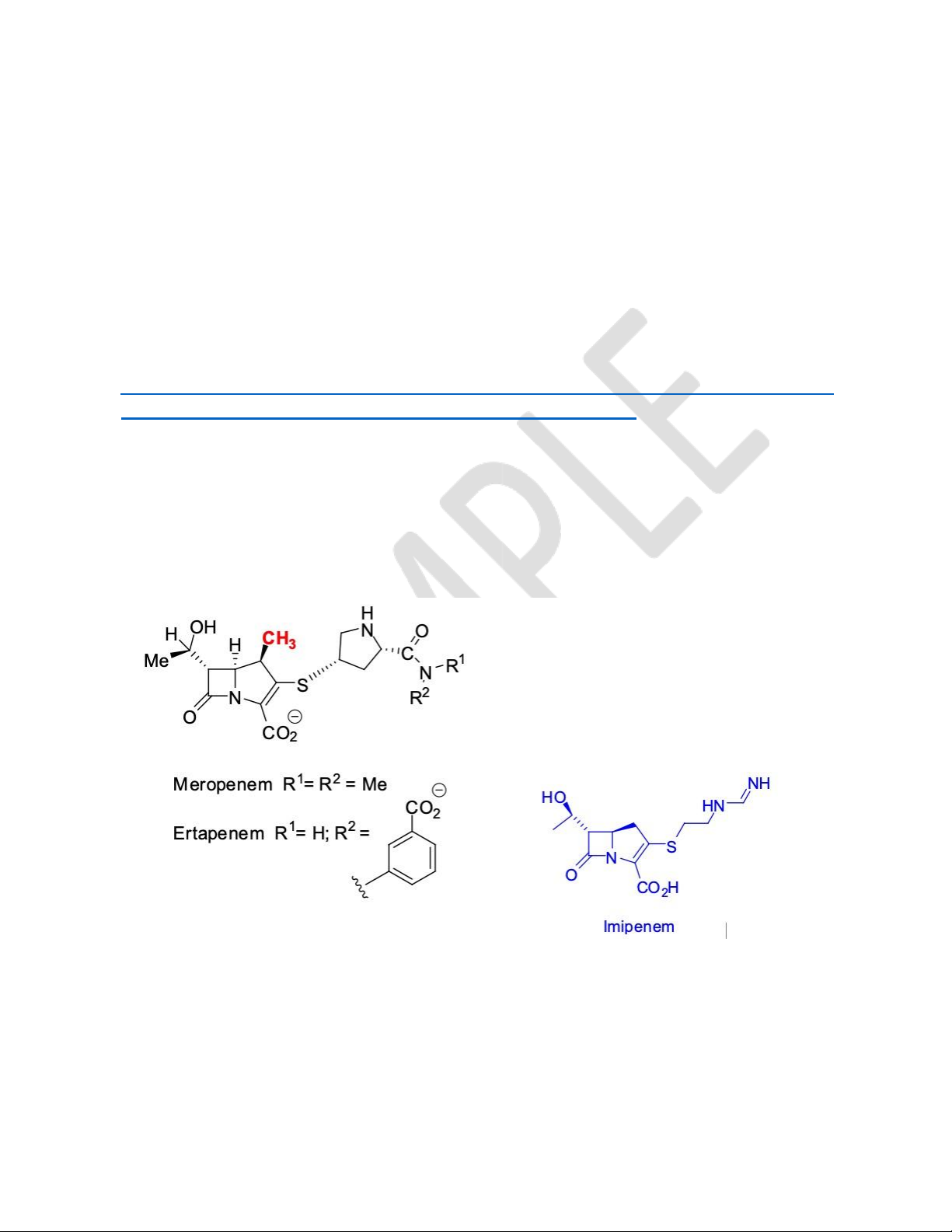
16. Cấu trúc Imipenem, Meropenem.
17. Lưu ý khi sử dụng Imipenem. - IV chậm.
- Dễ bị phân hủy bởi dehydropeptidase ở ống thận → khi sử dụng thường kết hợp với
cilastatin (chất ức chế enzyme dehydropeptidase) để giới hạn sự chuyển hóa này.
18. Đặc điểm cấu trúc của Imipenem gắn với hoạt tính trên Pseudomonas.
- Amino-2-thioethyl (cysteamin) ở vị trí 3 → hoạt tính trên Pseudomonas.
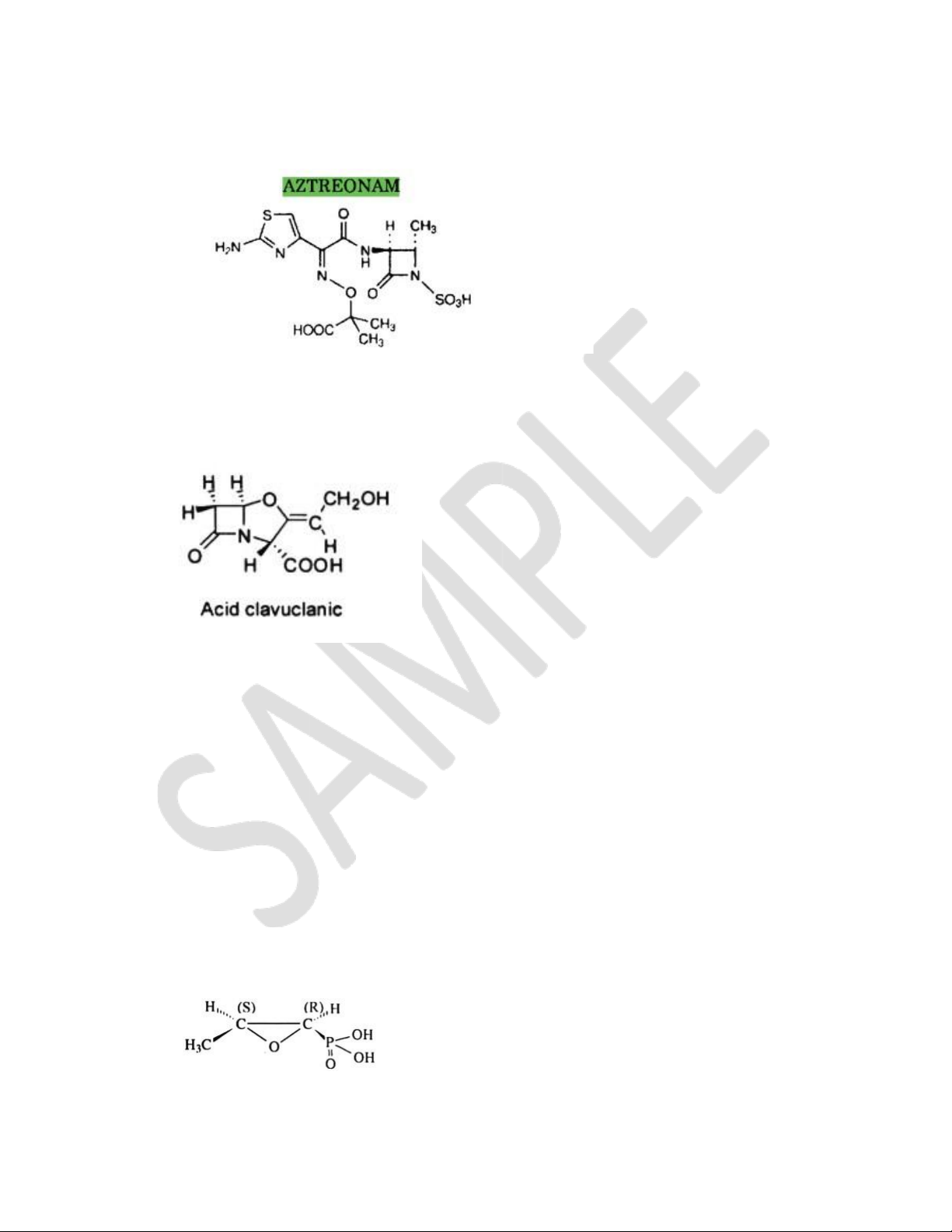
19. Đặc điểm của Aztreonam. 19 lOMoAR cPSD| 58448089
Khoa Dược Đề cương ôn tập Bộ môn Hóa Dược
- Không tác động trên G+, trị G- nặng. - Thuộc nhóm monobatam.
20. Đặc điểm của acid clavulanic.
- Dẫn chất của nhân clavam (oxapenam), khác với penam của penicillin bằng cách thế S bởi
O; không có nhóm thế ở C6.
21. Phối hợp kháng sinh β-lactam với chất ức chế β-lactamase.
- Ampicilin + sulbactam = mở rộng phổ kháng khuẩn.
- Amoxilin + acid cluvalinic = augmentin. Sulltamid +Trimetoprim = bactrim.
- Piperacilin + chất ức chế b-lactam (tazobactam)/aminosid = điều trị Pseudomonas aeruginosae.
- Carbenicillin, ticarcillin (dùng tiêm), carindacillin + đồng vận aminosid = trị trực khuẩn mũ xanh. KHÁNG SINH PHOSPHONIC
1. Đặc trưng cấu trúc của Fosfomycin. 20



