Preview text:
THẦY NGUYỄN VĂN THÁI ĐT :09.789.95.825 Mã đề: 301
KHẢO SÁT CHẤT LƯỢNG HỌC SINH LỚP 12 LẦN 1 – CỤM 09 TRƯỜNG MÔN: HÓA HỌC
Thời gian làm bài: 50 phút, không kể thời gian phát đề
Đề khảo sát có: 04 trang
Họ và tên thí sinh………………………………. Số báo danh……………….
PHẦN I (4,5 điểm). Câu hỏi trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu
18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1. Cho 4,5 gam C2H5NH2 tác dụng vừa đủ với dung dịch HCl, lượng muối thu được là A. 8,10 gam. B. 0,85 C. 8,15 gam. D. 7,65gam.
Câu 2. Cho phản ứng: C2H5OH + O2 enzyme
CH3COOH + H2O. Phản ứng đã cho là phản ứng
A. lên men giấm.
B. thủy phân.
C. lên men rượu. D. lên men lactic.
Câu 3. Để bảo quản thức ăn, người ta cất chúng trong tủ lạnh. Yếu tố được tác động để làm giảm tốc độ
của phản ứng phân hủy thức ăn là
A. nồng độ.
B. nhiệt độ.
C. chất xúc tác. D. áp suất.
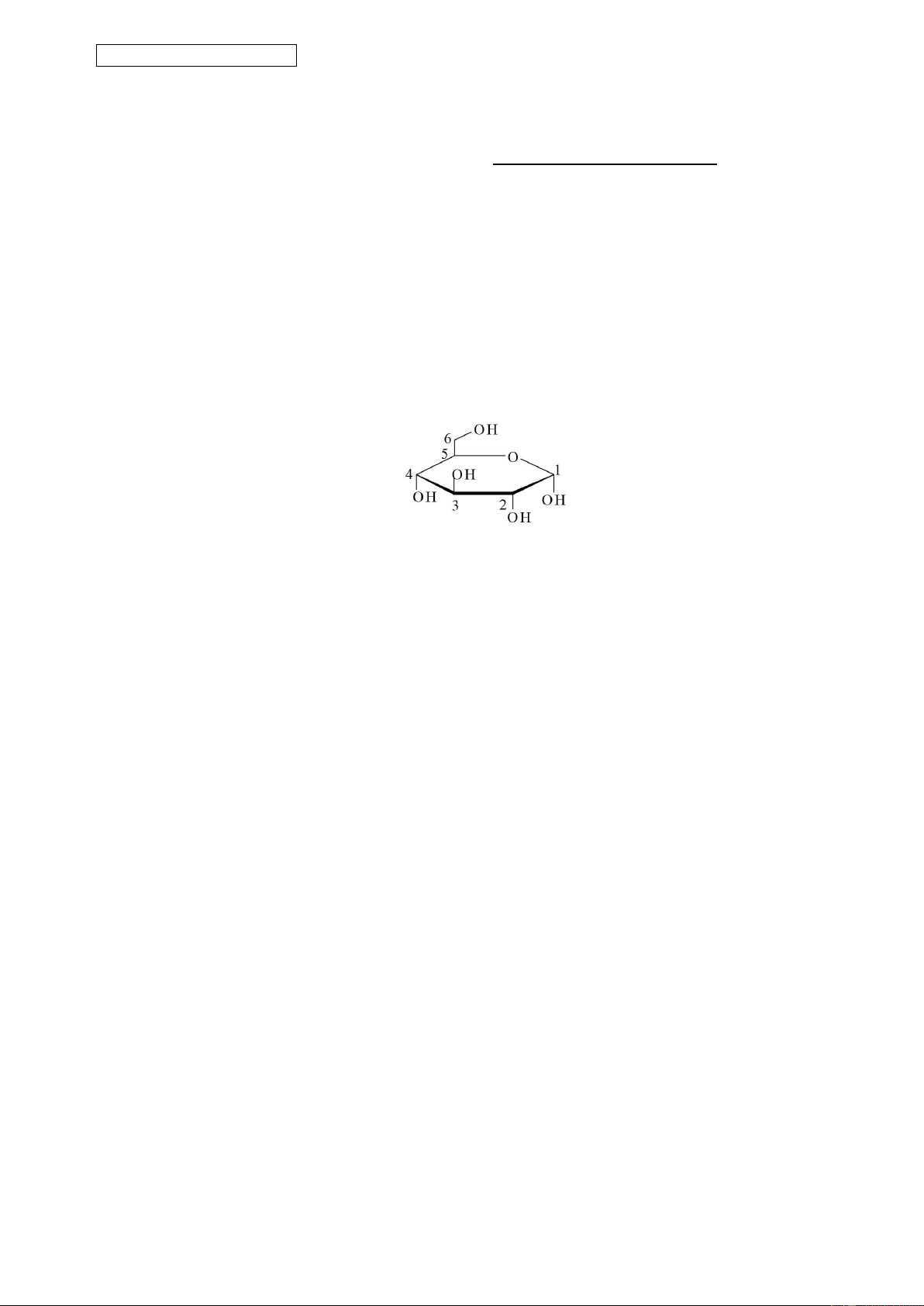
Câu 4. Cho công thức cấu tạo dạng mạch vòng α-glucose như sau:
Nhóm –OH hemiacetal trong α-glucose liên kết với nguyên tử carbon số mấy? A. 2. B. 1. C. 4. D. 3.
Câu 5. Cho dãy các chất: CH2=CHCl, CH2=CH2, CH2=CH-CH=CH2, H2NCH2COOH. Số chất trong dãy
có khả năng tham gia phản ứng trùng hợp là A. 4 B. 2 C. 3 D. 1
Câu 6. Cho các phát biểu sau:
(a) Phản ứng thủy phân ester trong môi trường base được gọi là phản ứng ester hóa.
(b) Các ester được dùng làm chất tạo hương trong công nghiệp thực phẩm.
(d) Dầu mỡ bị ôi do sự oxi hóa các gốc acid béo không no trong chất béo.
(d) Xà phòng có phần phân cực là nhóm carboxylate. Số phát biểu đúng là A. 2. B. 1. C. 4. D. 3.
Câu 7. Số electron lớp ngoài cùng của nguyên tử sodium (Z = 11) là A. 4. B. 2. C. 1. D. 3.
Câu 8. Aldehyde là hợp chất hữu cơ có nhóm ...(1)... liên kết với nguyên tử carbon (trong gốc hydrocarbon
hoặc CHO) hoặc nguyên tử hydrogen. Từ còn thiếu trong ô trống số (1) là A. >CO. B. –COOH. C. –CHO. D. –OH.
Câu 9. Chromium được sử dụng để cắt thuỷ tinh có thể được giải thích dựa vào tính chất vật lí nào?
A. Tính cứng.
B. Tính dẫn nhiệt. C. Tính dẻo.
D. Tính dẫn điện.
Câu 10. Cho các cặp oxi hóa - khử được sắp xếp theo thứ tự tăng dần tính oxi hóa của các ion kim loại:
Al3+/Al; Fe2+/Fe; Sn2+/Sn; Cu2+/Cu. Tiến hành các thí nghiệm sau:
(a) Cho sắt vào dung dịch đồng (II) sunfate.
(b) Cho đồng vào dung dịch nhôm sunfate.
(c) Cho thiếc vào dung dịch đồng (II) sunfate.
(d) Cho thiếc vào dung dịch sắt (II) sunfate.
Trong các thí nghiệm trên, những thí nghiệm có xảy ra phản ứng là: A. (b) và (d). B. (a) và (b). C. (b) và (c). D. (a) và (c).
Câu 11. Trong tự nhiên, phản ứng giữa nitrogen và oxygen xảy ra trong những cơn mưa dông sấm sét, khởi
đầu cho quá trình chuyển hóa từ nitrogen thành nitric acid. Nitric acid tan trong nước mưa và phân li ra ion nitrate (NO –
3 ) là một dạng phân đạm mà cây trong hấp thụ được để sinh trưởng và phát triển. Quá trình
chuyển hóa từ nitrogen thành nitric acid qua mấy giai đoạn? A. 2. B. 3. C. 4. D. 1.
Câu 12. Gang và thép là hai hợp kim quan trọng nhất của sắt. Chúng có rất nhiều ứng dụng trong đời sống
và sản xuất. Để sản xuất gang, người ta khử oxide của sắt (Fe2O3 hoặc Fe3O4) trong quặng sắt bằng khí CO
(được tạo ra do đốt cháy than cốc). Sắt được tạo ra trong quá trình sản xuất gang bằng phương pháp nào? A. Chiết.
B. Nhiệt luyện. C. Kết tinh. D. Thuỷ luyện.
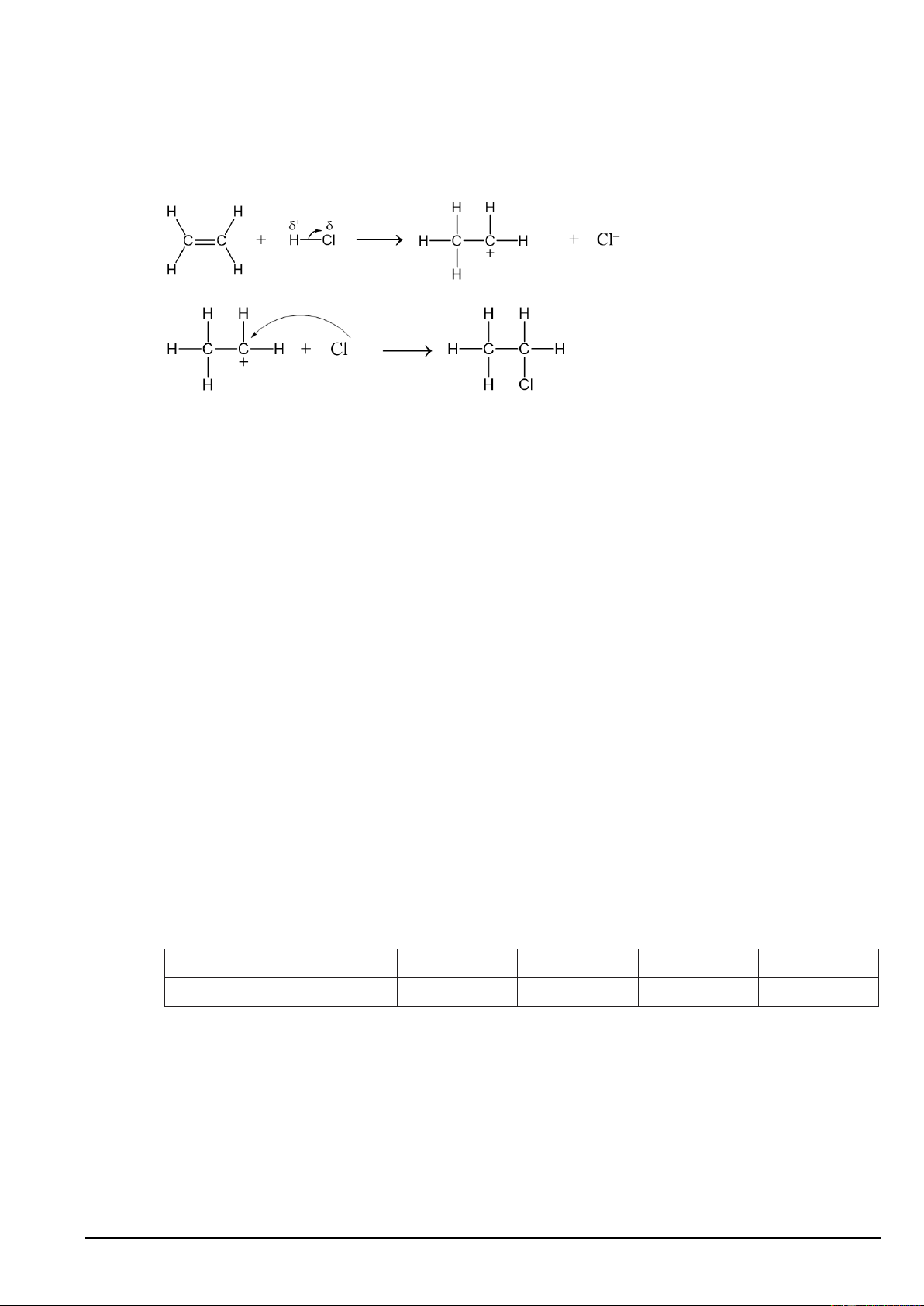
Câu 13. Phương trình hoá học của phản ứng ethylene với hydrochloric acid (HCl) xảy ra như sau: CH 2=CH2 + HCl CH3CH2Cl
Cơ chế phản ứng xảy ra theo hai giai đoạn sau: (1) (2)
Nhận định nào sau đây không đúng?
A. Trong giai đoạn (1) có sự phân cắt liên kết π.
B. Phản ứng trên là phản ứng cộng.
C. Phản ứng cộng HX vào alkene đối xứng chỉ thu được một sản phẩm cộng.
D. Thay CH2=CH2 bằng CH2=CHCH3 chỉ thu được sản phẩm CH3CH2CH2Cl.
Câu 14. Trong nước, thế điện cực chuẩn của kim loại M2+/M càng lớn thì dạng khử có tính khử..(1).. và
dạng oxi hoá có tính oxi hoá..(2).. Cụm từ cần điền vào (1) và (2) lần lượt là
A. càng mạnh và càng yếu.
B. càng yếu và càng mạnh.
C. càng mạnh và càng mạnh.
D. càng yếu và càng yếu.
Câu 15. Cho các phát biểu sau về tính chất của ethylamine:
(a) Ethylamine làm giấy quỳ tím ẩm hóa đỏ.
(b) Ethylamine phản ứng được với HCl trong dung dịch.
(c) Ethylamine không phản ứng được với dung dịch FeCl3 ở điều kiện thường.
(d) Dung dịch ethylamine phản ứng được với Cu(OH)2. Số phát biểu đúng là A. 2. B. 3. C. 4. D. 1.
Câu 16. Cách làm nào sau đây là đúng trong việc khử chua bằng vôi và bón phân đạm cho lúa?
A. Bón đạm và vôi cùng lúc.
B. Bón vôi khử chua trước rồi bón đạm ngay sau khi bón vôi.
C. Bón đạm trước rồi vài ngày sau mới bón vôi khử chua.
D. Bón vôi khử chua trước rồi vài ngày sau mới bón đạm.
Câu 17. Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là A. Na, Ba, K. B. Na, Cr, K. C. Mg, Na, Ca. D. Na, Fe, K.
Câu 18. Cho các cặp oxi hoá − khử của các kim loại và thế điện cực chuẩn tương ứng:
Cặp oxi hoá − khử Li+/Li Mg2+/Mg Zn2+/Zn Ag+/Ag
Thế điện cực chuẩn, V –3,040 –2,356 –0,762 +0,799
Trong số các kim loại trên, kim loại có tính khử mạnh nhất là A. Mg. B. Ag. C. Zn. D. Li.
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi
câu, thí sinh chọn đúng hoặc sai.
Câu 1. Quá trình đốt cháy nhiên liệu trong ô tô sinh ra nhiều khí như SO2, CO, NO. Từ năm 1975, người
ta thiết kế “bộ chuyển đổi xúc tác” trong hệ thống xả khí của ô tô (và cả trong máy phát điện) nhằm tạo
điều kiện thuận lợi cho phản ứng: 2CO(g) + 2NO(g) → 2CO2(g) + N2(g)
a) Trong phản ứng trên CO là chất oxi hóa, NO là chất khử.
b) Cho giá trị enthalpy tạo thành chuẩn của CO(g), NO(g), CO2(g) lần lượt là -110,5; 91,3; -393,5
(kJ.mol-1), biến thiên enthalpy chuẩn của phản ứng trên bằng 748,6 kJ. Mã đề 301 Trang 2/4
c) Bộ chuyển đổi xúc tác có ý nghĩa quan trọng trong việc giảm thiểu ô nhiễm môi trường.
d) Phản ứng trên chuyển từ khí ít độc hại thành khí độc hại hơn.
Câu 2. Tiến hành thí nghiệm theo các bước sau:
- Bước 1: Cho vào 3 ống nghiệm, mỗi ống 2 mL dung dịch H2SO4 0,5 M.
- Bước 2: Cho 3 lá kim loại có kích thước như nhau gồm lá nhôm (Al) đã làm sạch lớp bề mặt vào ống
nghiệm (1), lá sắt (iron, Fe) vào ống nghiệm (2) và lá đồng (Cu) vào ống nghiệm (3). Biết: o E o o 1, 676 V ; E 0, 44 V ; E 0,34 V . 3 Al /Al 2 Fe /Fe 2 Cu /Cu
a) Ở bước 2, ở cả ba ống nghiệm đều có khí thoát ra.
b) Tốc độ thoát khí ở ống (1) nhanh hơn ống (2).
c) Ở bước 2, nếu thêm tiếp 2 mL dung dịch H2SO4 0,5 M vào cả 3 ống thì tốc độ thoát khí ở cả ba ống sẽ tăng.
d) Nếu thay H2SO4 loãng bằng H2SO4 đặc thì hiện tượng ở bước 2 sẽ không đổi.
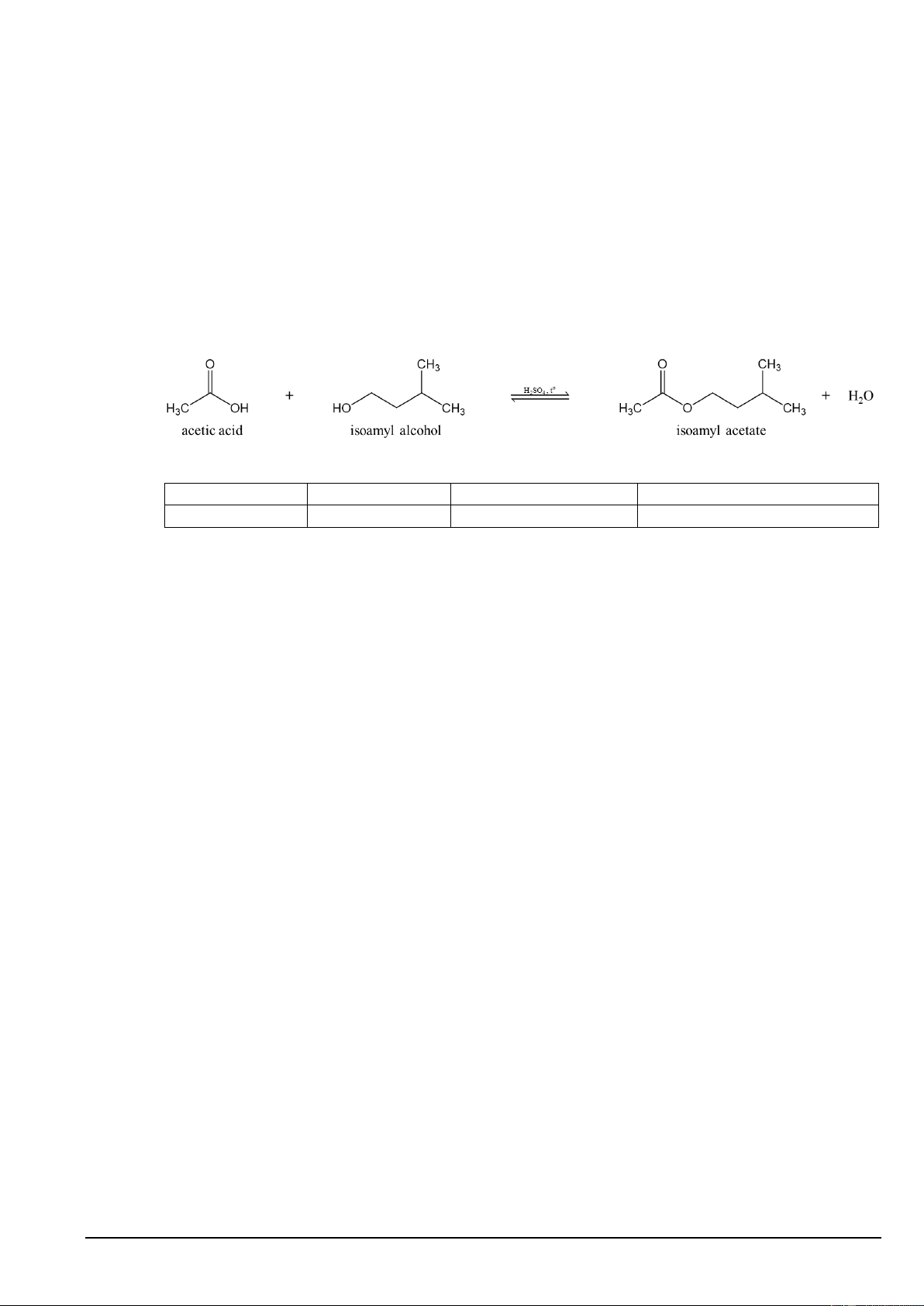
Câu 3. Một học sinh tiến hành tổng hợp isoamyl acetate (thành phần chính của dầu chuối) từ acetic acid và
isoamyl alcohol theo phương trình hóa học sau:
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, isoamyl alcohol và
isoamyl acetate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng như sau: Liên kết O–H (alcohol) O–H (carboxylic acid) C=O (ester, carboxylic acid) Số sóng (cm–1) 3 650 – 3 200 3 300 – 2 500 1 780 – 1 650
a) Phổ hồng ngoại có số sóng hấp thụ ở 3350 cm–1 là phổ của isoamyl alcohol.
b) Phản ứng tổng hợp trong thí nghiệm này là phản ứng thủy phân ester.
c) Dựa vào phổ hồng ngoại, phân biệt được acetic acid, isoamyl alcohol và isoamyl acetate.
d) Phổ hồng ngoại có số sóng hấp thụ ở 1750 cm–1 mà không có số sóng hấp thụ đặc trưng của liên kết
O–H là phổ của isoamyl acetate.
Câu 4. Isoamyl acetate (d = 0,876 g/mL) có mùi chuối nên được dùng làm hương liệu nhân tạo. Trong
ngành sơn, isoamyl acetate được dùng làm dung môi sơn mài. Isoamyl acetate được điều chế theo các bước sau:
- Bước 1: Cho vào bình cầu 15 mL isoamyl alcohol (d = 0,810 g/mL), 10 mL acetic acid (d = 1,049
g/mL) và 7,0 mL H2SO4 đậm đặc, cho thêm vào bình vài viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng
đứng vào miệng bình cầu. Sau đó đun nóng bình cầu trong khoảng 1 giờ.
- Bước 2: Sau khi đun, để nguội rồi rót sản phẩm vào phễu chiết, lắc đều rồi để yên khoảng 5 phút, chất
lỏng tách thành hai lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
- Bước 3: Cho từ từ dung dịch Na2CO3 10% vào phần chất lỏng thu lấy ở bước 2 và lắc đều cho đến khi
không còn khí thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hòa rồi để yên khi đó chất lỏng tách thành
hai lớp. Chiết lấy phần chất lỏng phía trên, làm khan, ta thu được isoamyl acetate.
a) Isoamyl acetate rất ít tan trong nước vì có khối lượng riêng nhỏ hơn khối lượng riêng của nước.
b) Ở bước 1, xảy ra phản ứng thế nhóm –OH của alcohol bằng gốc CH3COO–.
c) Nếu hiệu suất phản ứng este hóa là 54% và lượng isoamyl acetate bị hao hụt tối đa 6% thì thể tích
isoamyl acetate thu được là 10,4 mL. (Làm tròn kết quả đến hàng phần mười).
d) Ở bước 3, không thể thay dung dịch Na2CO3 bằng dung dịch NaOH dư.
PHẦN III: Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Cho các phản ứng sau:
(1) Nhiệt phân polystyrene thu được styrene.
(2) Đun nóng cao su thiên nhiên với sulfur.
(3) Thủy phân tinh bột với xúc tác enzyme.
(4) Đun nóng poly(vinyl acetate) với dung dịch NaOH.
(5) Đun nóng capron với dung dịch HCl.
Sắp xếp các phản ứng cắt mạch polymer theo thứ tự tăng dần (ví dụ 123, 134,…).
Câu 2. Trong công nghiệp, người ta sản xuất nitric acid (HNO3) từ ammonia theo sơ đồ chuyển hoá sau: 0 O ,t ,xt O O H O 2 2 2 2 NH NO NO HNO 3 2 3 Mã đề 301 Trang 3/4
Để sản xuất 1 tấn dung dịch HNO3 63%, cần dùng m kg ammonia, biết rằng hiệu suất của toàn bộ quá trình
là 75%. Giá trị của m là bao nhiêu (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối
cùng được làm tròn đến hàng đơn vị)?
Câu 3. Amine đơn chức X có chứa 23,73% nitrogen về khối lượng. Tổng số nguyên tử trong một phân tử X bằng bao nhiêu?
Câu 4. Một đồ vật được làm bằng kim loại Fe dạng hình trụ rỗng có bán kính trong là 1,00 cm, bán kính
ngoài là 2,50 cm và chiều cao là 0,50 cm như hình vẽ:
Người ta mạ kim loại Ni cho đồ vật trên bằng cách sử dụng kim loại Ni và đồ vật này làm hai điện cực rồi
nhúng vào trong dung dịch NiSO4 1 M để tiến hành điện phân. Để đạt yêu cầu về mặt kĩ thuật thì lớp kim
loại Ni phải có độ dày là 0,05 mm và phủ đều trên các bề mặt của đồ vật. Biết khối lượng riêng của kim
loại Ni là 8,90 g/cm³; lấy π = 3,1416, F = 96500 C/mol và Ni = 58,7. Tính thời gian (theo phút) của quá
trình mạ điện nếu sử dụng dòng điện có cường độ không đổi là 1,50A (Kết quả các phép tính trung gian
không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng đơn vị).
Câu 5. Có bao nhiêu alcohol có công thức phân tử C4H10O?
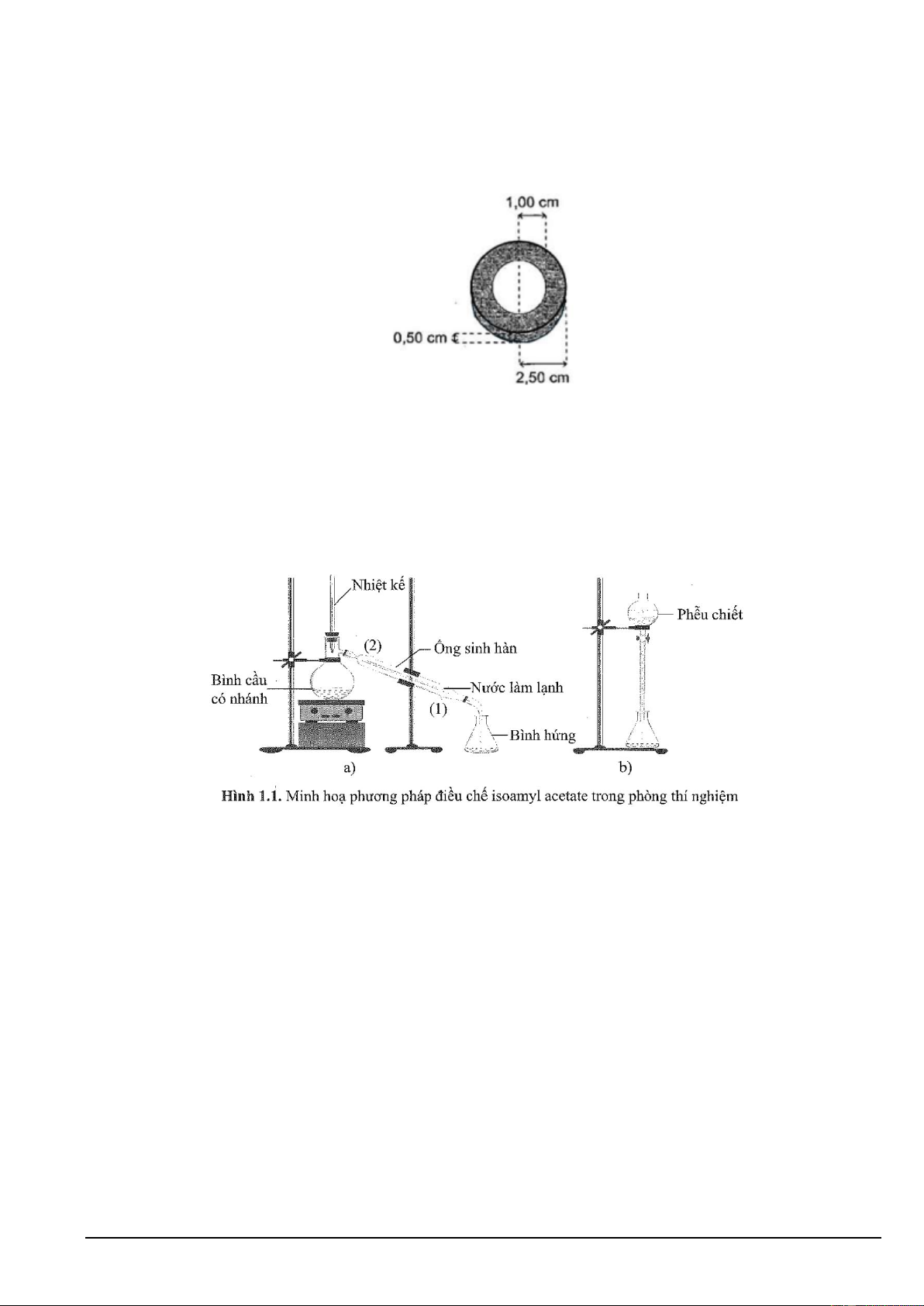
Câu 6. Quan sát hình sau:
Cho các phát biểu liên quan tới Hình 1.1 như sau:
(a) Hỗn hợp chất lỏng trước phản ứng trong bình cầu có nhánh gồm isoamyl alcohol, acetic acid và sulfuric acid đặc.
(b) Trong phễu chiết, lớp chất lỏng nặng hơn có thành phần chính là isoamyl acetate.
(c) Nhiệt kế dùng để kiểm soát nhiệt độ trong bình cầu có nhánh.
(d) Phễu chiết dùng để tách isoamyl acetate ra khỏi hỗn hợp sau phản ứng.
(e) Nước làm lạnh cho chảy vào ống sinh hàn ở vị trí số (1) và chảy ra ở vị trí số (2).
Số phát biểu đúng là bao nhiêu?
------ HẾT ------ Mã đề 301 Trang 4/4



