



Preview text:
KHÓA CHUYÊN ĐỀ LIVE T | TYHH
THI THỬ TỐT NGHIỆP 2026 | LẦN 3
(Tự Học – TỰ LẬP – Tự Do!)
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí
sinh chỉ chọn một phương án. Câu 1:
Từ phổ khối lượng, phân tử khối của ester X được xác định là 88. Công thức phù hợp với X là A. CH3COOC2H5. B. C5H11OH. C. C3H7COOH. D. HCOOC2H5. Câu 2:
Nguồn điện nào sau đây có thể tái sử dụng nhiều lần bằng cách sạc điện? A. Pin chanh. B. Acquy chì. C. Pin con thỏ. D. Pin mặt trời. Câu 3:
Carbohydrate nào có cấu trúc phân tử được biểu diễn dưới đây? A. Saccharose. B. Cellulose. C. Maltose. D. Amylose. Câu 4:
Hình dưới đây là ký hiệu của 6 polymer nhiệt dẻo phổ biến có thể tái chế:
Các ký hiệu này thường được in trên bao bì, vỏ hộp, đồ dùng,… để giúp nhận biết vật liệu polymer cũng
như thuận lợi cho việc thu gom, tái chế. Polymer có ký hiệu số 3 được điều chế bằng phản ứng trùng
hợp monomer nào dưới đây? A. CH2=CH2. B. CH2=CH–C6H5. C. CH2=CH–Cl. D. CH2=CH–CH3. Câu 5:
Ở dạng mạch vòng, glucose và fructose lần lượt còn nhóm.(I). và nhóm.(II). Đây là nguyên nhân dẫn
đến glucose và fructose.(III). Cụm từ cần điền vào (I), (II) và (III) lần lượt là
A. –OH hemiacetal, –OH hemiketal, có thể mở vòng.
B. –OH hemiketal, –OH hemiacetal, có thể mở vòng. 1 | T Y H H
C. –OH hemiacetal, –OH hemiketal, có thể tham gia phản ứng thuỷ phân.
D. –OH hemiketal, –OH hemiacetal, không thể tham gia phản ứng thuỷ phân. Câu 6:
Cho các pin điện hoá và sức điện động chuẩn tương ứng: Pin điện hóa Cu - X Y - Cu Z - Cu
Sức điện động chuẩn (V) 0,459 2,016 2,696 (X, Y, Z là ba kim loại)
Dãy các kim loại xếp theo chiều tăng dần tính khử từ trái sang phải là A. X, Cu, Z, Y. B. X, Cu, Y, Z. C. Z, Y, Cu, X. D. Y, Z, Cu, X. Câu 7:
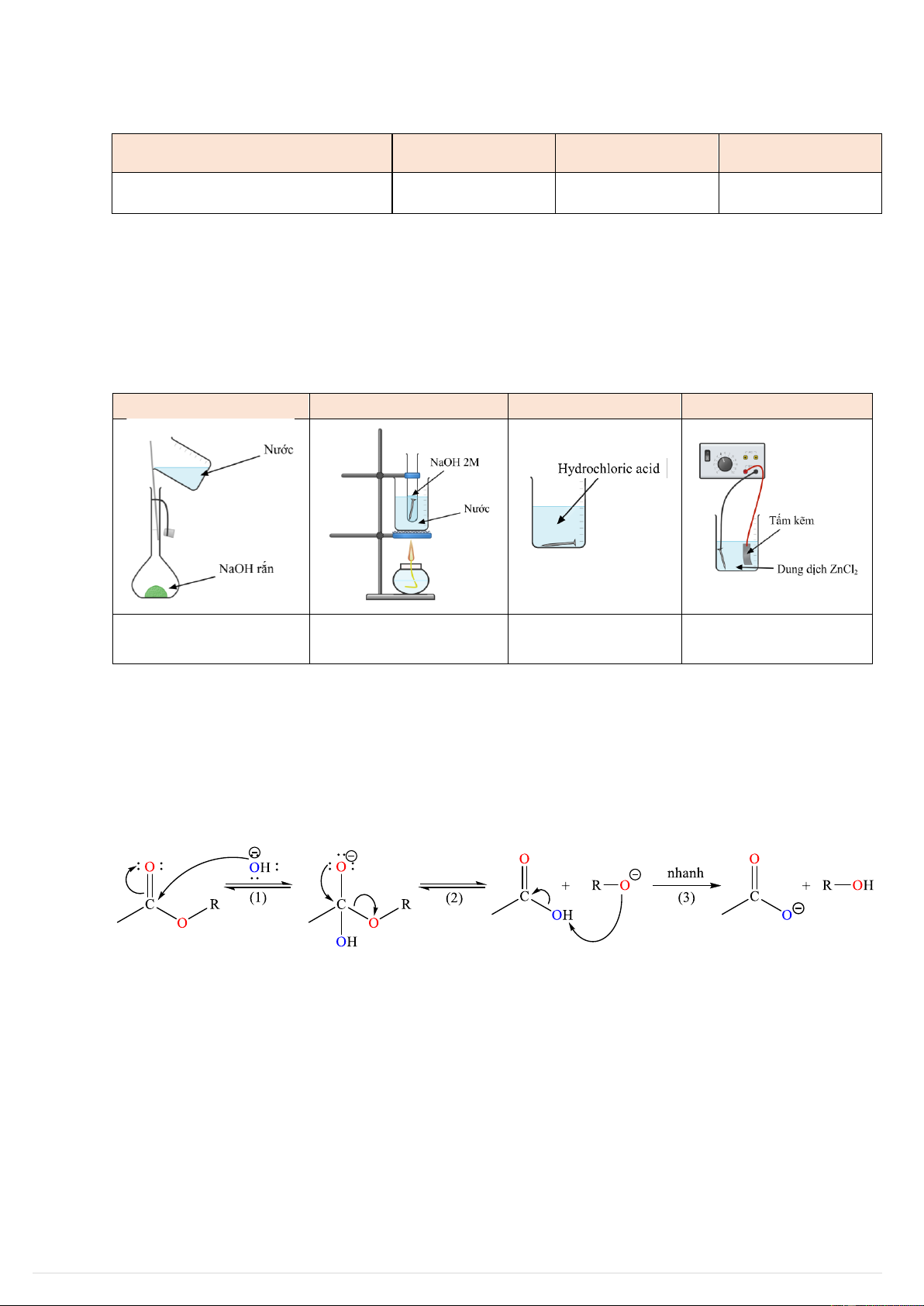
Trong phòng lab của TYHH, một học sinh LOVEVIP đang tiến hành thí nghiệm mạ kẽm lên một chiếc
đinh sắt (có dính dầu mỡ, đã bị gỉ sét) theo quy trình A, B, C, D trong bảng dưới đây. (A) (B) (C) (D) Chuẩn bị dung dịch
Loại bỏ dầu mỡ trên bề Loại bỏ gỉ sét trên
Mạ kẽm lên đinh sắt đã NaOH mặt đinh sắt bề mặt đinh sắt làm sạch
Hãy cho biết nguyên lý, thiết bị hay thao tác ở giai đoạn nào sau đây là sai? A. D. B. C. C. B. D. A. Câu 8:
Khi đun nóng ester của acetic acid trong dung dịch NaOH xảy ra phản ứng hoá học sau:
CH3COOR + NaOH → CH3COONa + ROH (*)
Cơ chế của phản ứng xảy ra như sau:
Nhận định nào sau đây không đúng?
A. Giai đoạn (3) là phản ứng acid-base theo bronsted - Lowry.
B. Giai đoạn (2) có sự thay thế nhóm -OH bằng nhóm -OR.
C. Giai đoạn (1) có sự phá vỡ liên kết π hình thành liên kết σ.
D. Phản ứng (*) là phản ứng thuỷ phân ester trong môi trường kiềm. Câu 9:
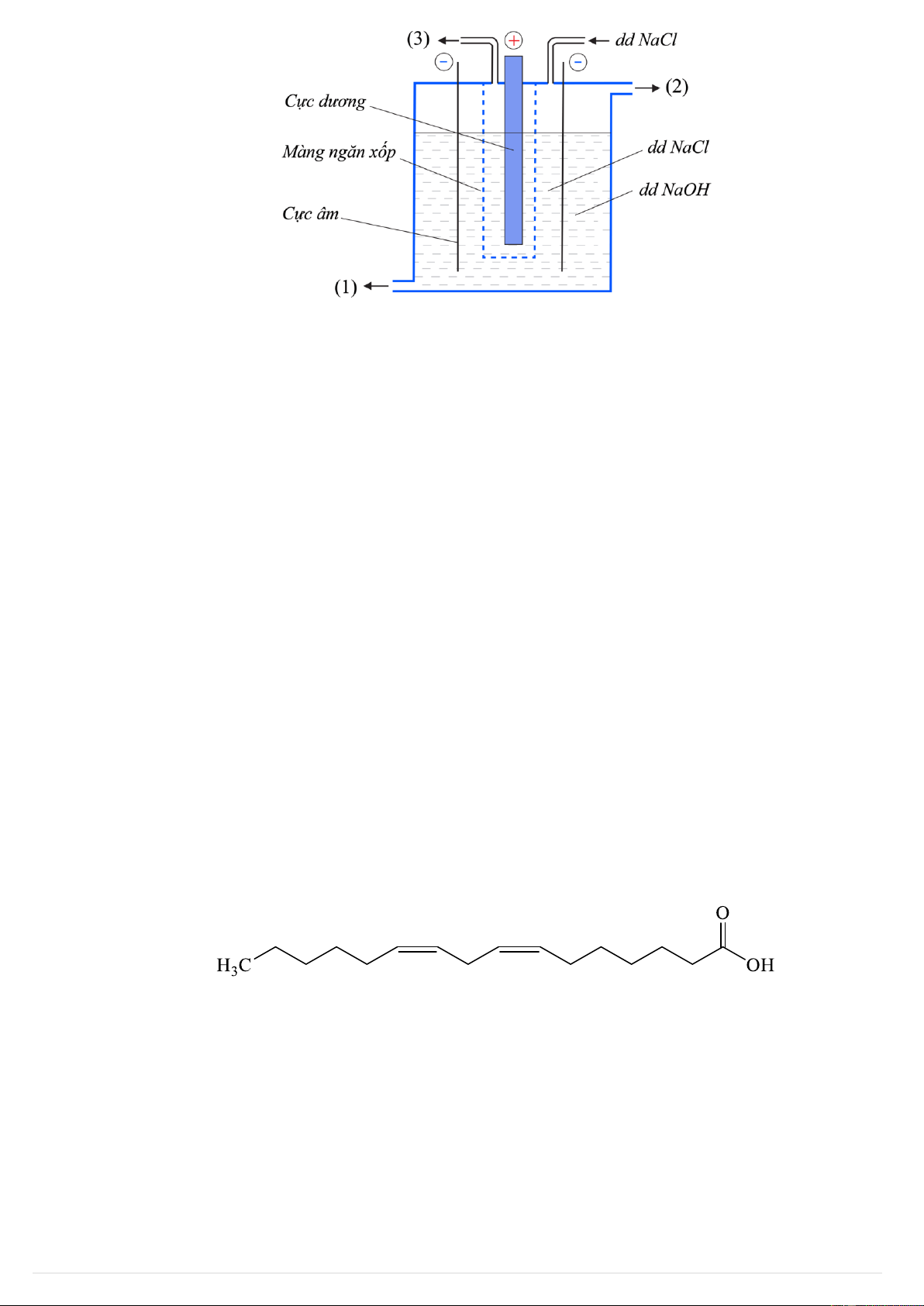
Trong công nghiệp, NaOH được điều chế bằng cách điện phân dung dịch NaCl bão hòa, thùng điện phân
có cực âm bằng sắt, cực dương bằng than chì, giữa hai điện cực có màng ngăn xốp (như sơ đồ bên dưới). 2 | T Y H H
Theo sơ đồ trên, khí Cl2 được thoát ra tại cửa ở vị trí số mấy? A. (1) và (2). B. (1). C. (3). D. (2).
Câu 10: Trong quá trình hoạt động của pin điện hoá Cu – Ag, nồng độ của các ion trong dung dịch biến đổi như thế nào?
A. Nồng độ của ion Ag+ tăng dần và nồng độ của ion Cu2+ giảm dần.
B. Nồng độ của ion Ag+ giảm dần và nồng độ của ion Cu2+ giảm dần.
C. Nồng độ của ion Ag+ tăng dần và nồng độ của ion Cu2+ tăng dần.
D. Nồng độ của ion Ag+ giảm dần và nồng độ của ion Cu2+ tăng dần.
Câu 11: Glucose được tìm thấy trong tự nhiên dưới dạng D-glucose hoặc L-glucose, trong đó D-glucose có nhiều
trong tự nhiên còn L-glucose ít gặp hơn. Dextrose là tên gọi khác của D-glucose. Phát biểu nào sau đây
không đúng về dextrose?
A. Do không thể mở vòng, dextrose không có cấu tạo dạng mạch hở.
B. Dextrose và glucose có cùng công thức phân tử.
C. Dextrose phản ứng được với thuốc thử Tollens.
D. Dextrose là một carbohydrate.
Câu 12: Linoleic acid (có cấu tạo như hình dưới) là một trong những acid béo có lợi cho sức khỏe tim mạch,
ngăn ngừa các bệnh về tim, động mạch vành.
Nhận xét nào sau đây đúng về linoleic acid?
A. Trong phân tử linoleic acid có 3 liên kết πC=C.
B. Tên thay thế của linoleic acid là trans,trans-9,12-octadecadienoic acid.
C. Linoleic acid thuộc loại omega - 6.
D. Linoleic acid có 17 nguyên tử carbon trong phân tử.
Câu 13: Qiana là tên thương mại của một loại tơ nylon được sử dụng để sản xuất vải lụa chống nhăn cao cấp.
Qiana có công thức cấu tạo sau đây: 3 | T Y H H
Nhận xét nào sau đây đúng?
A. Các monomer dùng để tổng hợp Qiana có cấu tạo như sau: O H N NH 2 2 O OH và OH
B. Tơ này kém bền trong môi trường acid hoặc base mạnh.
C. Tơ nylon làm từ tơ Qiana thuộc loại tơ nhân tạo.
D. Qiana thuộc loại loại polyamide được điều chế từ phản ứng trùng hợp các monomer đa chức tương ứng.
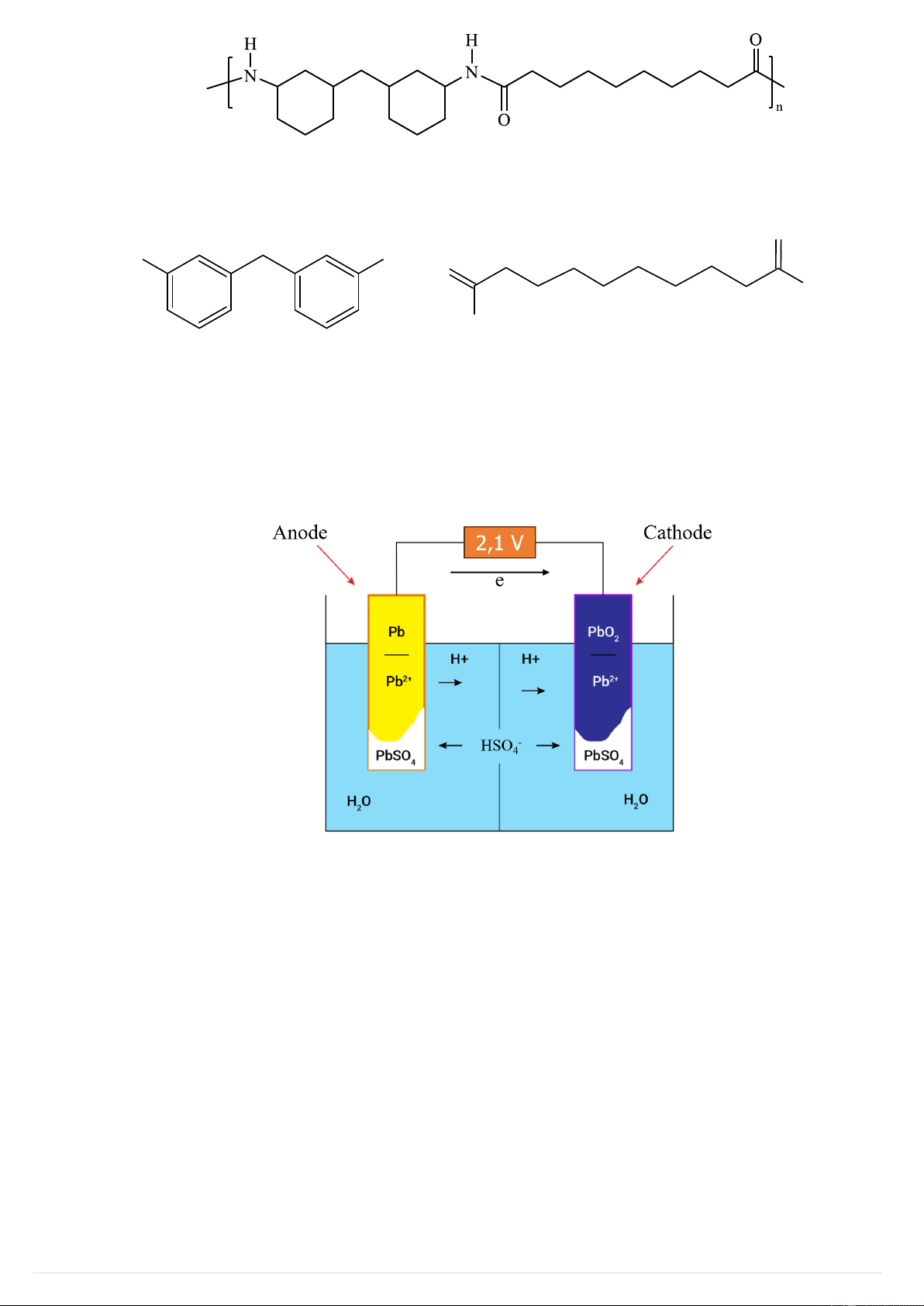
Câu 14: Ắc quy chì (Lead-acid Battery) là nguồn điện thông dụng, tạo ra dòng điện ổn định và đặc biệt có thể tái sử dụng.
Khi ắc quy phóng điện, quá trình xảy ra tại các điện cực như sau: Anode: Pb + HSO − 4 → PbSO4 + H+ + 2e Cathode: PbO −
2 + HSO4 + 3H+ + 2e → PbSO4 + 2H2O
Khác với pin Galvani, ắc quy có thể tái sử dụng bằng cách áp dòng điện bên ngoài để các phản ứng ở
điện cực xảy ra theo chiều ngược khi phóng điện (gọi là quá trình nạp điện hay tích điện).
Mệnh đề nào dưới đây không đúng?
A. Khi ắc quy phóng điện, tại anode xảy ra quá trình oxi hóa chì (lead).
B. Khi ắc quy phóng điện, tại cathode xảy ra quá trình khử lead dioxide (PbO2).
C. Khi ắc quy phóng điện cũng như nạp điện, nồng độ H2SO4 giảm dần.
D. Khi nạp điện, ắc quy đóng vai trò như bình điện phân. 4 | T Y H H
Câu 15: Cho sơ đồ chuyển hóa: Cellulose → X1 → X2 → X3 → PE. Người ta đã dùng một loại gỗ có chứa 40%
cellulose cần dùng để sản xuất 14 tấn nhựa PE với hiệu suất chung của cả quá trình là 60%. Phát biểu đúng là?
A. X1 và X2 đều có thể hòa tan Cu(OH)2/OH- ở điều kiện thường tạo thành dung dịch xanh lam.
B. X3 được ứng dụng trong việc bảo quản hoa quả.
C. Phản ứng số 1 và 3 đều là phản ứng thủy phân trong môi trường acid.
D. Để sản xuất ra lượng nhựa PE như trên, khối lượng gỗ đã sử dụng bằng 168,75 tấn.
Câu 16: Khí thải CO2 đang làm cho Trái Đất ngày càng nóng lên do hiệu ứng nhà kính. Dự đoán khí thải CO2
năm 2026 toàn cầu sẽ là 36,3 tỉ tấn. Nhờ quá trình quang hợp ( 6CO2 + 6H2O + 673 kcal ⟶ C6H12O6
+6O₂), hàng năm cây cối trên Trái Đất hấp thụ hàng chục tỉ tấn CO2, đồng thời giải phóng vào khí quyển
một lượng khí oxygen khổng lồ cần thiết cho sự sống trên Trái Đất. Cứ trong 1 giây, mỗi cm² lá xanh
nhận được 0,5 cal từ năng lượng mặt trời, nhưng chỉ có 10% được sử dụng vào quá trình quang hợp.
Thời gian để 1 cây có 1000 lá xanh, mỗi lá có diện tích 20 cm² hấp thụ hết 36,3 tấn CO2 là bao nhiêu
năm? (kết quả làm tròn đến hàng phần trăm) A. 2,93. B. 3,92. C. 9,32. D. 2,39.
Câu 17: Để mạ đồng (Cu) một vật dụng kim loại có tổng diện tích bề mặt là 10 cm², người ta tiến hành điện phân
dung dịch CuSO4 với cực âm là vật dụng cần mạ và cực dương là lá đồng thô. Biết cường độ dòng điện
không đổi là 2A, hiệu suất điện phân là 80%, khối lượng riêng của tinh thể Cu là 8,94 g/cm³ và lượng
đồng tạo ra được tính theo công thức Faraday là m = AIt/nF (với A là nguyên tử khối của Cu = 64; I là
cường độ dòng điện, F là hằng số Faraday = 96485 C/mol, n là số electron mà 1 ion Cu2+ nhận, t là thời
gian điện phân tính bằng giây). Thời gian điện phân để lớp mạ có độ dày đồng nhất 0,1 mm là bao nhiêu
phút? (Làm tròn kết quả đến hàng phần mười). A. 25. B. 26. C. 27. D. 28.
Câu 18: Pin nhiên liệu sử dụng ethanol (C2H5OH) được đặc biệt quan tâm do có nguồn nhiên liệu sinh học dồi
dào. Phản ứng xảy ra khi một pin ethanol - oxygen phóng điện ở 25°C trong dung dịch chất điện li là
potassium hydroxide như sau: C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l)
Một pin ethanol - oxygen được dùng để thắp sáng 5 bóng đèn LED, mỗi bóng có công suất 6 W (6 J/s)
liên tục trong t giờ, tiêu thụ hết 230 gam ethanol với hiệu suất quá trình oxi hoá ethanol ở anode là 60%.
Cho biết nhiệt tạo thành chuẩn của các chất: Chất C2H5OH(l) O2(g) CO2(g) H2O(l) Δ 0 fH298 (kJ/mol) −277,6 0,00 −393,5 −285,8
Giá trị của t bằng bao nhiêu? (Kết quả làm tròn đến hàng đơn vị). A. 35. B. 36. C. 38. D. 37. 5 | T Y H H
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu.
Thí sinh chọn đúng hoặc sai. Câu 1:
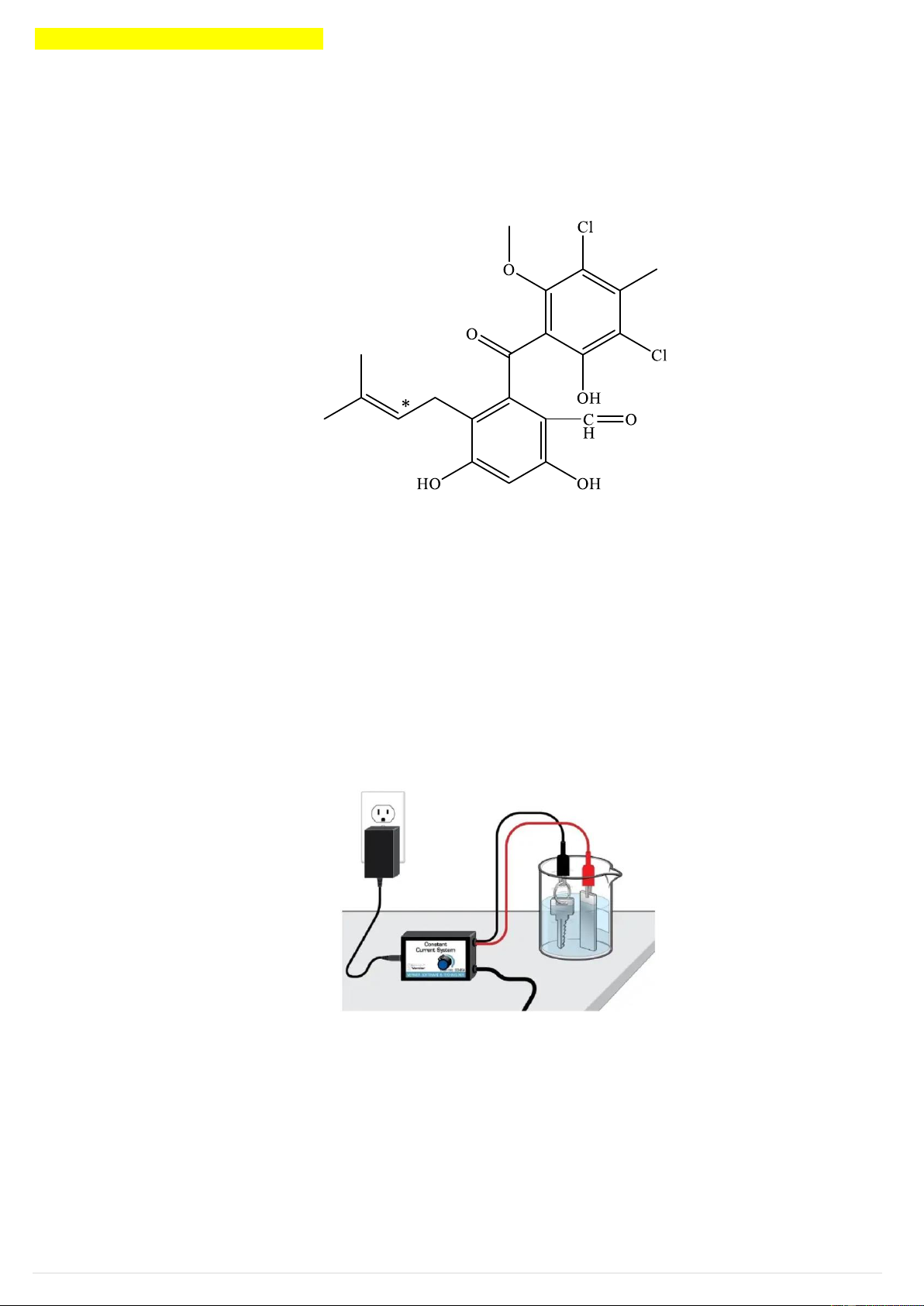
Hợp chất X là một sản phẩm tự nhiên được phân lập từ quá trình nuôi cấy cộng sinh giữa vi khuẩn và
nấm, thể hiện tính đặc trưng của các hợp chất sinh học thứ cấp do vi sinh vật tạo ra. X có công thức cấu
tạo đơn giản như hình vẽ:
Phát biểu dưới đây là đúng hay sai về X?
a) Có thể xảy ra phản ứng cộng và phản ứng thế với Br2.
b) Có khả năng phản ứng với tối đa 3 nguyên tử Na.
c) Chứa 4 loại nhóm chức có chứa oxygen.
d) X có đồng phân hình học ở vị trí nối đôi *. Câu 2:
Để mạ kẽm lên chiếc chìa khóa làm bằng sắt để chìa khóa không bị gỉ, học sinh A thực hiện thí nghiệm
điện phân như hình vẽ:
a) Để mạ 1,3 gam Zn lên chiếc chìa khóa bằng cách điện phân dung dịch muối Zn2+ với cường độ dòng
điện không đổi 1,5A cần thời gian là 43 phút. Giả sử hiệu suất điện phân là 100% và điện lượng: q = It
= ne.F; F = 96500 C/mol (làm tròn kết quả đến hàng đơn vị)
b) Cực anode gắn với vật cần mạ (chìa khóa).
c) Cực cathode là thanh Zn.
d) Nguồn điện qua máy biến áp một chiều (DC/DC converter) là một thiết bị chuyển đổi nguồn điện
xoay chiều thành nguồn điện một chiều để điện phân. 6 | T Y H H Câu 3:
Ascorbic acid (hay vitamin C) được biết đến như một hợp chất quan trọng đối với con người. Nó đóng
vai trò chất chống lão hoá, tăng sức đề kháng của cơ thể.
Một nhóm học sinh được giao nhiệm vụ xác định hàm lượng ascorbic acid trong một viên uống cung
cấp vitamin C. Nhóm học sinh đã biết được ngoài ascorbic acid (kí hiệu là H2As), các hoạt chất còn lại
coi như không có phản ứng với NaOH. Phản ứng giữa ascorbic acid với NaOH được biểu diễn bởi phương trình sau: H2As + NaOH → NaHAs + H2O
Điểm tương đương được xác định dựa vào chỉ thị phenol đỏ (màu tại điểm tương đương là màu da cam,
pH = 8,72). Nhóm học sinh tiến hành thí nghiệm theo các bước sau:
Bước 1: Lấy một viên vitamin C, đem cân được 800 mg.
Bước 2: Hoà tan phần đã nghiền vào nước, lọc bỏ phần không tan, thêm nước để được 100,0 mL (dung
dịch X). Lấy 10 mL dung dịch X cho vào cốc sạch và nhỏ 1 - 2 giọt phenol đỏ vào, dung dịch thu được có màu đỏ.
Bước 3: Lấy dung dịch NaOH 0,02M cho vào burette đến vạch số 0. Mở khoá burette cho dung dịch
NaOH từ từ vào cốc đựng dung dịch X (lắc nhẹ cốc trong quá trình thí nghiệm) cho đến khi dung dịch
trong cốc có màu da cam và dừng lại. Ghi lại thể tích dung dịch NaOH đã dùng là V1 (mL). Lặp lại bước
3 thêm 2 lần nữa, kết quả thu được như sau: Thí nghiệm Lần 1 Lần 2 Lần 3
Thể tích dung dịch NaOH (mL) 14,20 14,25 14,15
a) Giả thuyết khoa học phù hợp là "Sử dụng phản ứng chuẩn độ acid - base xác định được hàm lượng
của hoạt chất ascorbic acid có trong viên uống".
b) Trong quá trình chuẩn độ, lúc đầu có thể mở khóa burette cho NaOH chảy nhanh, sau đó chậm dần,
nhỏ từng giọt chậm rãi, lắc và quan sát. Để biết chuẩn độ nhanh tới khoảng bao nhiêu mL nên thử chuẩn
độ nháp trước 1 lần (lần nháp này bỏ, chỉ lấy kết quả để áng chừng cho 3 lần sau).
c) Trong quá trình chuẩn độ, việc lắc nhẹ cốc giúp cho tốc độ phản ứng giữa ascorbic acid với NaOH diễn ra nhanh hơn.
d) Kết quả thí nghiệm của nhóm học sinh xác định được hàm hoạt chất ascorbic acid có trong viên uống
là 65,2% (Kết quả được làm tròn đến hàng phần mười). 7 | T Y H H Câu 4:
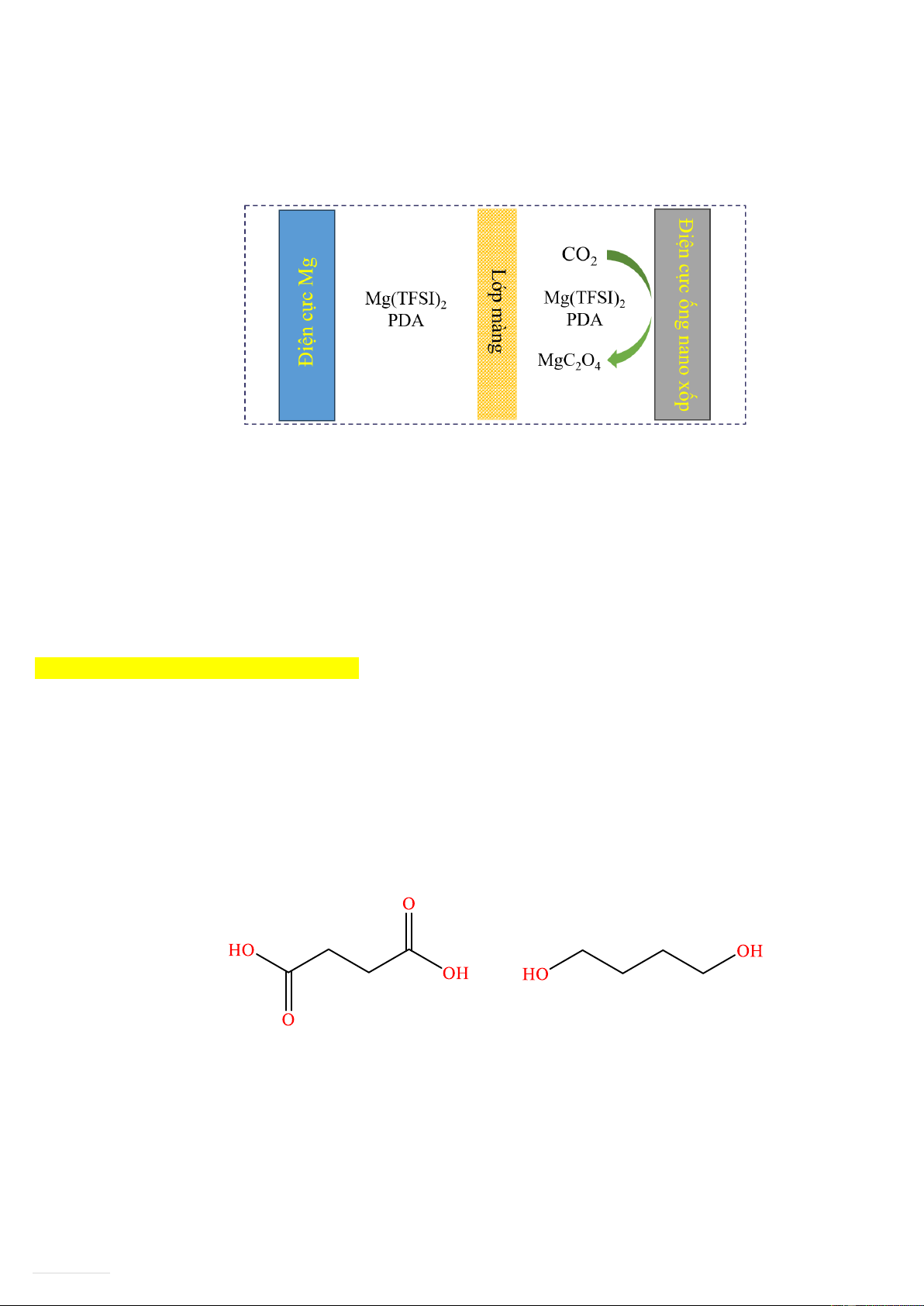
Các nhà khoa học công nghệ trên thế giới đã thiết kế một loại pin Mg-CO2 có thể sạc lại như hình. Pin sử
dụng Mg(TFSI)2 làm chất điện giải và thêm chất trung gian 1,3-PDA (1,3-propylenediamine) vào dung dịch
điện giải để hấp thu CO2. Trong quá trình phóng điện, CO2 được khử thành sản phẩm MgC2O4. Thiết kế này
đã khắc phục được những hạn chế về tính dẫn điện kém và khả năng phân hủy CO2 kém của MgCO3, đồng
thời cải thiện khả năng solvat hóa của Mg2+, nâng cao hiệu suất chu trình sạc-xả của pin.
Phát biểu dưới đây là đúng hay sai?
a) Khi phóng điện, phản ứng tổng quát của pin là: 2CO2 + Mg → MgC2O4
b) Khi sạc điện, điện cực ống nano carbon xốp được nối với cực dương của nguồn điện.
c) Khi sạc điện, electron di chuyển từ điện cực Mg về phía cực dương, còn Mg2+ di chuyển về phía cực âm.
d) Khi phóng điện, mỗi mol electron được trao đổi thì về lý thuyết có thể khử 1 mol CO2.
PHẦN III. Câu trắc nghiệm trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6. Câu 1:
PBS - Poly(butylene succinate), có tên thương mại Bionolle, là một polymer phân huỷ sinh học có tính
dẻo và bền nhiệt tương tự polyethylene (PE). Nhờ cấu trúc mạch chính chứa các nhóm ester dễ bị thủy
phân, PBS có khả năng phân rã trong môi trường tự nhiên. Với đặc tính này, PBS được ứng dụng rộng
rãi trong sản xuất bao bì và túi nylon thân thiện với môi trường, trở thành giải pháp tiềm năng thay thế
các loại nhựa truyền thống khó phân huỷ. PBS được tổng hợp bằng phản ứng trùng ngưng giữa hai monomer sau:
Tính khối lượng của một mắt xích polymer PBS theo đơn vị amu. Câu 2:
Một học sinh thực hiện các thí nghiệm để kiểm tra tính chất hóa học của một số hợp chất chứa nitrogen
và thu được các kết quả sau:
TN1: Dung dịch methylamine làm phenolphtalein đổi màu hồng.
TN2: Thêm vài giọt nước bromine vào dung dịch alanine, thấy có kết tủa trắng xuất hiện.
TN3: Nhỏ dung dịch ethylamine vào dung dịch FeCl3, thấy có kết tủa nâu đỏ xuất hiện.
TN4: Dung dịch methylamine tác dụng với HNO2 (ở nhiệt độ thường), thấy có khí thoát ra. 8 | T Y H H
Đã có một thí nghiệm trên bị sai kết quả, hỏi đó là thí nghiệm số mấy?. Câu 3:
Khi thủy phân không hoàn toàn x mol pentapeptide T có công thức A-B-C-B-C thì dung dịch thu được
có tối đa bao nhiêu peptide có thể tham gia phản ứng màu biuret? Biết A, B, C là các amino acid thiên
nhiên. Hiệu suất quá trình thủy phân đạt 90%. Câu 4:
Poly (vinyl acetate) (viết tắt là PVAc) được làm keo dán gỗ, keo dán giấy,. PVAc được tổng hợp từ ethylene theo sơ đồ sau: o o o o + 2 O ,xt ,t + 2 O , xt, t + 2 O + CH2 =CH2, xt, t xt, t
CH =CH ⎯⎯⎯⎯→ CH CHO ⎯⎯⎯⎯⎯
→ CH COOH ⎯⎯⎯⎯⎯⎯⎯⎯→ X ⎯⎯⎯ → PVAc 2 2 (1) 3 (2) 3 (3) (4)
Trong các phản ứng (1), (2), (3), (4) lần lượt có 90%, 95%, 80% và 90% lượng chất hữu cơ chuyển hoá
thành sản phẩm theo sơ đồ phản ứng, lượng chất hữu cơ còn lại chuyển hoá thành các sản phẩm khác
hoặc không tái sử dụng được. Riêng phản ứng (3), tỉ lệ mol các chất hữu cơ được lấy theo đúng hệ số
trong phương trình phản ứng. Khối lượng PVAc (theo kg) thu được từ 10 m³ ethylene (đo ở 25°C, 1 bar)
là bao nhiêu? Biết: hằng số R = 0,08314 bar.L.mol-1.K-1; (Không làm tròn các phép tính trung gian, chỉ
làm tròn kết quả cuối cùng đến hàng đơn vị). Câu 5:
Biodiesel (diesel sinh học) là một loại nhiên liệu lỏng, thân thiện hơn với môi trường so với diesel truyền
thống. Biodiesel được sản xuất thông qua phản ứng giữa chất béo với các alcohol mạch ngắn (thường là
methanol), với xúc tác là kiềm, thu được biodiesel (ester của acid béo) và glycerol. Một nhà máy tái chế
dầu ăn đã qua sử dụng để sản xuất biodiesel theo phương trình phản ứng tổng quát sau:
(RCOO)3C3H5 + 3CH3OH (NaOH) → 3RCOOCH3 + C3H5(OH)3
Từ 500 kg một loại dầu ăn đã qua sử dụng có chứa 85% chất béo (phân tử khối trung bình của chất béo là
860), còn lại là tạp chất không có khả năng chuyển hóa thành biodiesel, có thể sản xuất được tối đa m kg
biodiesel dạng methyl ester với hiệu suất 90%. Tính giá trị của m (làm tròn kết quả đến hàng đơn vị). Câu 6:
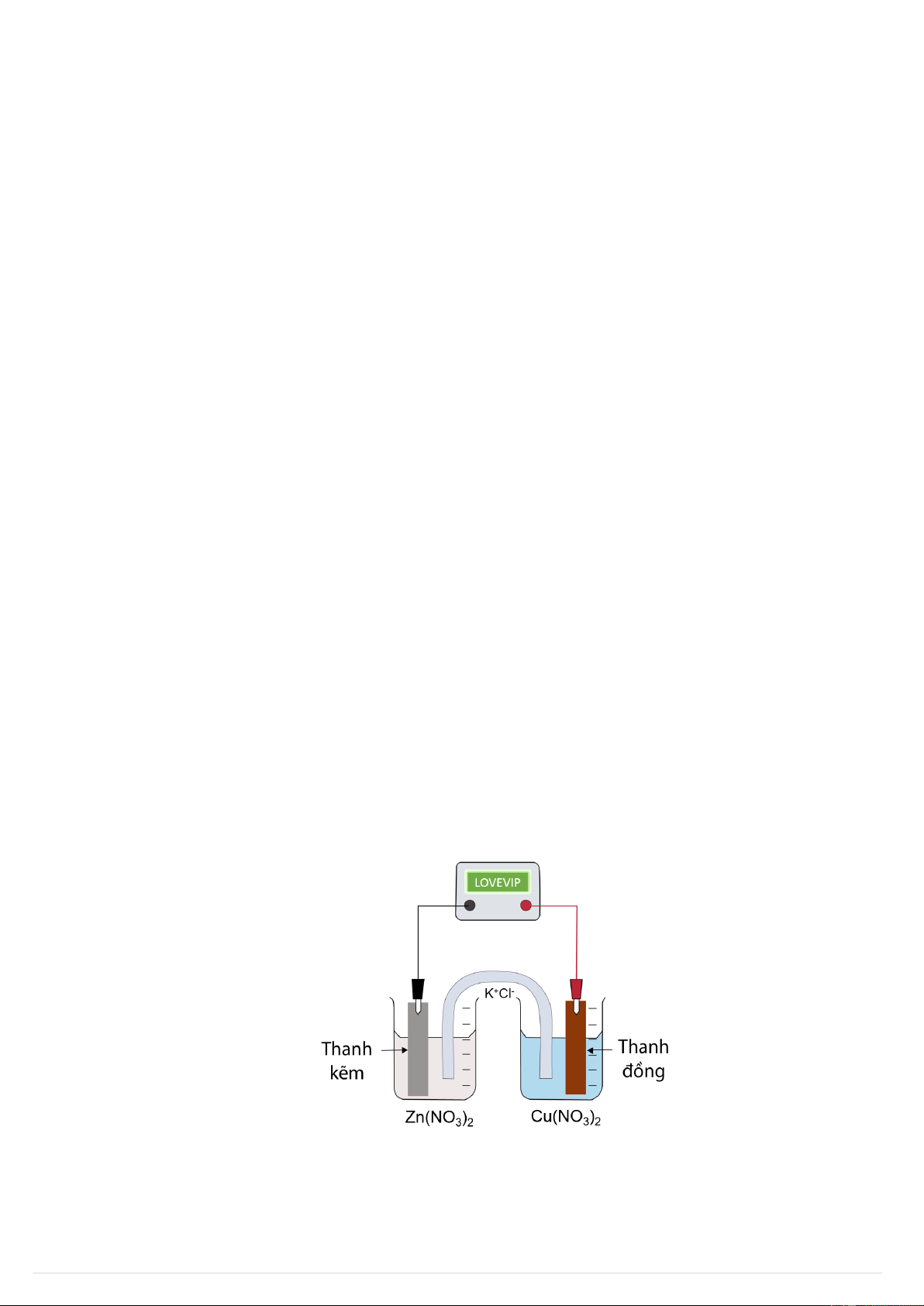
Một học sinh LOVEVIP thiết lập một pin Galvani gồm:
Nửa pin 1: Thanh Zn có khối lượng 200 gam nhúng vào 1,00 L dung dịch Zn(NO3)2 1M
Nửa pin 2: Thanh Cu có khối lượng 100 gam nhúng và 1,00 L dung dịch Cu(NO3)2 1M.
Hai thanh kim loại được nối với vật tiêu thụ điện và hai dung dịch nối với nhau bằng cầu muối (chứa
KCl nhão). Pin trên sản sinh dòng điện có cường độ ổn định là I = 0,5A. Xác định thời gian (theo ngày)
pin đó hoạt động. Biết rằng pin chỉ dừng hoạt động khi một trong các chất tham gia phản ứng hết. (Không
làm tròn các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần trăm). Điện lượng (q) 9 | T Y H H
của pin điện liên hệ với số mol electron trao đổi giữa hai điện cực (ne) hoặc thời gian (t, giây) pin hoạt
động theo biểu thức sau: q = ne.F = I.t
Với F là hằng số Faraday, F = 96500 C/mol; I là cường độ dòng điện của pin.
Tự học – TỰ LẬP – Tự do!
⭐️⭐️⭐️ (Thầy Phạm Thắng | TYHH) ⭐️⭐️⭐️ 10 | T Y H H



