








Preview text:
MA TRẬN + BẢN ĐẶC TẢ + ĐỀ KIỂM TRA GIỮA HKI KHTN 7 A) MA TRẬN
- Thời điểm kiểm tra: Kiểm tra giữa học kì I, khi kết thúc nội dung: Bài 7.
- Thời gian làm bài: 90 phút.
- Hình thức kiểm tra: Kết hợp giữa trắc nghiệm và tự luận (tỉ lệ 30% trắc nghiệm, 70% tự luận). - Cấu trúc:
- Mức độ đề: 40% Nhận biết; 40% Thông hiểu; 20% Vận dụng; 0% Vận dụng cao.
- Phần trắc nghiệm: 3,0 điểm, gồm 12 câu hỏi (ở mức độ nhận biết: 12 câu)
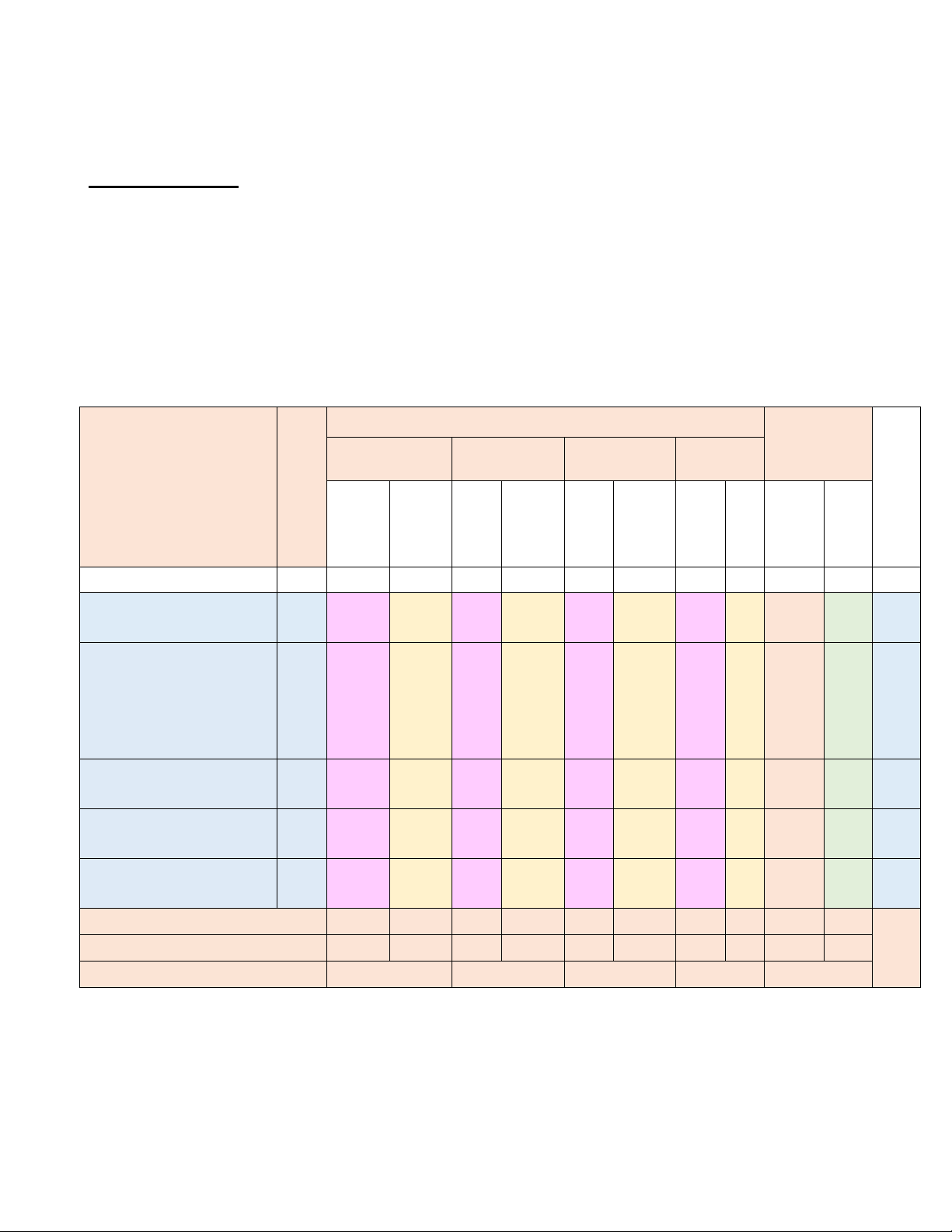
- Phần tự luận: 7,0 điểm (Nhận biết: 1 điểm, Thông hiểu:4 điểm; Vận dụng: 2 điểm; Vận dụng cao: 0 điểm) MỨC ĐỘ Tổng số Vận câu/ý Nhận biết dụng cao Điể Số Thông hiểu Vận dụng CHỦ ĐỀ tiết m Trắ Trắ Trắ số Trắc c c c Tự Trắc Tự nghiệ Tự ngh Tự ngh Tự ngh lu nghiệ luậ m luận iệm luận iệm luận iệm ận m n (1) 36 (2) (3) (4) (5) (6) (7) (8) (9) (10) (11) (12) 1.Mở đầu 4 4 (1đ) 4 0 1 2.Nguyên tử. Nguyên tố hóa học
Sơ lược về bảng tuần 15
hoàn các nguyên tố 4 hoá học (1đ) 1(1đ) 2(2đ) 4 3 4
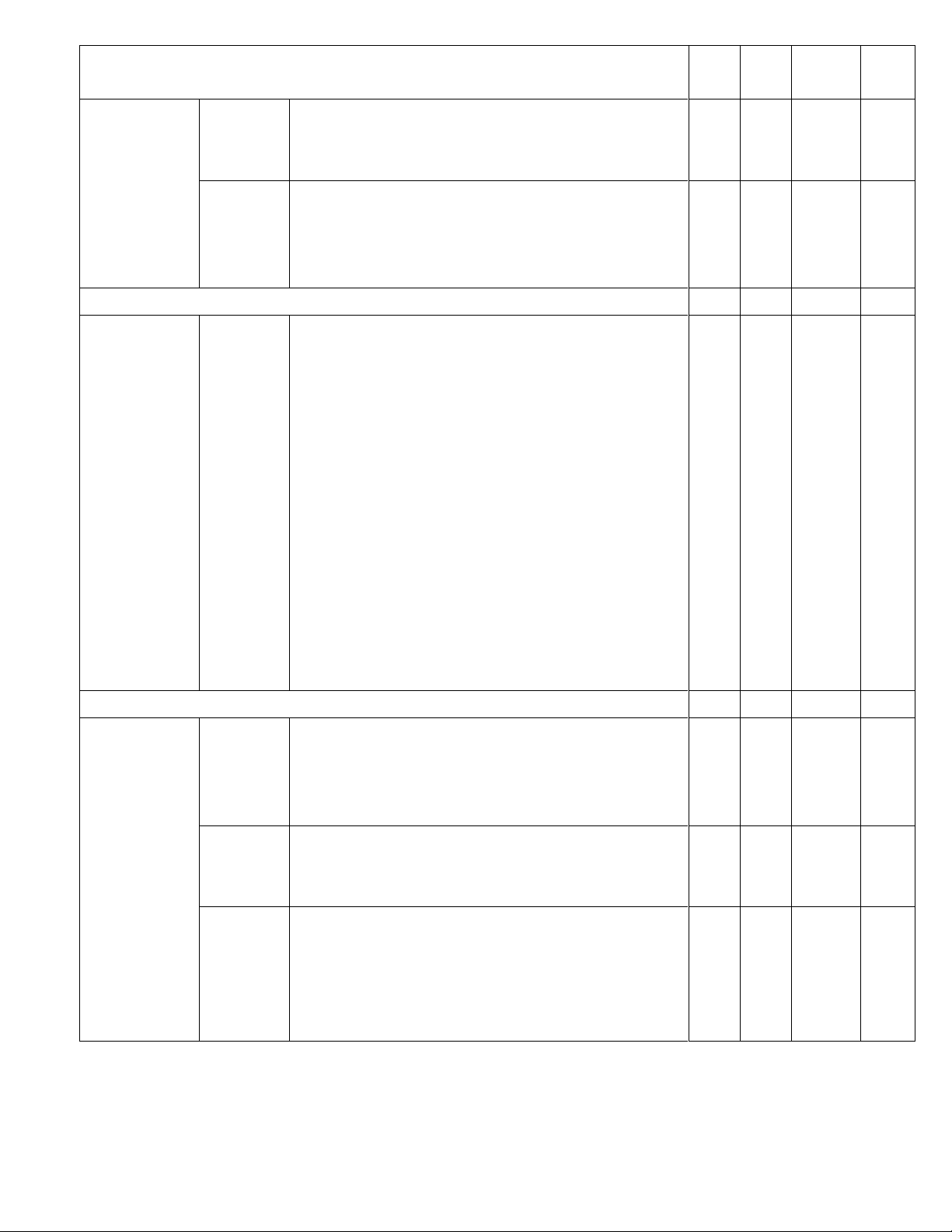
3..Phân tử-Đơn chất- 4 2 Hợp chất (0,5đ) 1(1đ) 2 1 1,5 4.Lk hóa học 6 1(1đ) 0 1 1 5.Hóa trị-CTHH 7 2 (0,5đ) 1(1đ) 1(1đ) 2 2 2,5 Số câu/Số ý 12 1 0 4 0 2 0 0 12 7 Điểm số 3 1 0 4 0 2 0 0 3 7 10 Tổng số điểm 4 4 2 0 10 B) BẢNG ĐẶC TẢ Số ý TL/số câu Câu hỏi hỏi TN Nội dung Mức độ
Yêu cầu cần đạt TL TN TN TL (Số (Số (câu ( ý số) ý) câu) số)
1/Mở đầu (4 tiết) 0 4 Nhận C9 biết
Trình bày được một số phương pháp và kĩ C10
năng trong học tập môn Khoa học tự nhiên C11 C12 Thông
- Thực hiện được các kĩ năng tiến trình: quan hiểu
sát, phân loại, liên kết, đo, dự báo. Mở đầu
- Sử dụng được một số dụng cụ đo (trong nội
dung môn Khoa học tự nhiên 7). Vận dụng
Làm được báo cáo, thuyết trình.
2/Nguyên tử. Nguyên tố hóa học Sơ lược về bảng tuần hoàn các 3 4
nguyên tố hoá học (15tiết) Nhận
– Trình bày được mô hình nguyên tử của biết
Rutherford – Bohr (mô hình sắp xếp electron
trong các lớp vỏ nguyên tử).
– Nêu được khối lượng của một nguyên tử
theo đơn vị quốc tế amu (đơn vị khối lượng nguyên tử).
– Nêu được các nguyên tắc xây dựng bảng C17
tuần hoàn các nguyên tố hoá học. C1
– Mô tả được cấu tạo bảng tuần hoàn gồm: ô, nhóm, chu kì. – C2,C3
Phát biểu được khái niệm về nguyên tố hoá
học và kí hiệu nguyên tố hoá học. C4 Thông
-Sử dụng được bảng tuần hoàn để chỉ ra các hiểu
nhóm nguyên tố/nguyên tố kim loại, các nhóm C13
nguyên tố/nguyên tố phi kim, nhóm nguyên tố C14
khí hiếm trong bảng tuần hoàn.
3/Phân tử; đơn chất; hợp chất(4 tiết) 1 2 Nhận
- Nêu được khái niệm phân tử, đơn chất, hợp biết C5,C6 chất. Thông
- Đưa ra được một số ví dụ về đơn chất và hợp hiểu chất. C18b
– Tính được khối lượng phân tử theo đơn vị amu.
4/ Giới thiệu về liên kết hoá học (ion, cộng hoá trị)(6 tiết) 0 1
– Nêu được mô hình sắp xếp electron trong vỏ
nguyên tử của một số nguyên tố khí hiếm; sự
hình thành liên kết cộng hoá trị theo nguyên
tắc dùng chung electron để tạo ra lớp vỏ
electron của nguyên tố khí hiếm (Áp dụng
được cho các phân tử đơn giản như H2, Cl2, NH3, H2O, CO2, N2,….). –
Nêu được sự hình thành liên kết ion theo C15
nguyên tắc cho và nhận electron để tạo ra ion
có lớp vỏ electron của nguyên tố khí hiếm (Áp
dụng cho phân tử đơn giản như NaCl, MgO,…).
– Chỉ ra được sự khác nhau về một số tính chất
của chất ion và chất cộng hoá trị.
5/Hoá trị; công thức hoá học(7 tiết) 2 2 Nhận
– Trình bày được khái niệm về hoá trị (cho chất C7 biết
cộng hoá trị). Cách viết công thức hoá học.
– Nêu được mối liên hệ giữa hoá trị của C8
nguyên tố với công thức hoá học. Thông
– Viết được công thức hoá học của một số chất hiểu
và hợp chất đơn giản thông dụng. C18a Vận
– Xác định được công thức hoá học của hợp dụng
chất dựa vào phần trăm (%) nguyên tố và khối lượng phân tử C16
– Tính được phần trăm (%) nguyên tố trong hợp
chất khi biết công thức hoá học của hợp chất C. ĐỀ:
I TRẮC NGHIỆM: (3 diểm)
Bảng tuần hoàn các nguyên tố hoá học được sắp xếp theo nguyên Câu 1 tắc:
A) nguyên tử khối tăng dần.
B) tính kim loại tăng dần.
C) điện tích hạt nhân tăng dần
D) tính phi kim tăng dần. Đáp án C
Câu 2 Số thứ tự chu kì trong bảng hệ thống tuần hoàn cho biết:
A) Số thứ tự của nguyên tố.
B) Số hiệu nguyên tử.
C) Số electron lớp ngoài cùng.
D) Số lớp electron. Đáp án D
Câu 3 Những nguyên tố hóa học nào sau đây thuộc cùng một nhóm? A) O, S, Se; B) N, O, F; C) Ne, Na, Mg.
D) C. Na, Mg, K. Đáp án A Câu 4
Nguyên tố hóa học là tập hợp các nguyên tử cùng loại có...
A) cùng số electron trong hạt nhân.
B) cùng số proton trong hạt nhân.
C) cùng số proton và neutron trong hạt nhân.
D) cùng số neutron trong hạt nhân. Đáp án B Cho các chất sau đây?
Câu 5 (a) Phosphoric acid (chứa H, P, O).
(b) Kim cương do nguyên tố carbon tạo nên.
(c) Khí ozone có công thức hóa học là O3.
(d) Kim loại silver tạo nên từ Ag. Số đơn chất là: A) 1. B) 2. C) 3. D) 4. Đáp án C
Câu 6 Trong số các chất dưới đây, thuộc loại hợp chất có:
A) khí hydrogen. B) phosphorus. C) aluminium. D) water. Đáp án D
Câu 7 Phát biểu nào sau đây đúng?
A) Công thức hóa học cho biết thành phần nguyên tố và số nguyên tử của chất.
B) Công thức hóa học dùng để biểu diễn chất và cho biết hóa trị của chất.
C) Công thức hóa học dùng để biểu diễn chất và cho biết khối lượng phân tử của chất.
D) Công thức hóa học dùng để biểu diễn các nguyên tố có trong chất. Đáp án A
Câu 8 Trong chất cộng hóa trị, phát biểu nào sau đây đúng?
A) Hóa trị của nguyên tố bằng số H liên kết với nguyên tử nguyên tố đó.
B) Hóa trị của nguyên tố là đại lượng biểu thị khả năng liên kết của
nguyên tử nguyên tố đó với nguyên tử khác có trong phân tử.
C) Hóa trị của nguyên tố bằng số nguyên tử H và nguyên tử O liên
kết với nguyên tố đó.
D) Hóa trị của nguyên tố bằng số nguyên tử O liên kết với nguyên tố đó nhân với 2. Đáp án B Câu 9 A) B) C) D) Đáp án Câu 10 A) B) C) D) Đáp án Câu 11 A) B) C) D) Đáp án Câu 12 A) B) C) D) Đáp án
9/Kết nối thông tin ở cột (A) với cột (B) để được câu hoàn chỉnh. Cột A Cột B Nối
9.Không khí là một hỗn hợp các A.phản xạ ánh sáng mặt trời. chất khí trong đó
10.Ánh sáng Mặt Trăng có
B.sẽ cung cấp đầy đủ chất dinh dưỡng được là do
cho cơ thể nhằm phát triển khỏe mạnh.
11.Kết hợp với các loại lương
C.bao gồm 78% khí nitrogen,21% khí
thực, thưc phẩm phù hợp với
oxygen và 1% các khí khác. lứa tuổi giới tính
Chọn đáp án đúng
12.Việc kết nối thông tin ở trên thể hiện kĩ năng gì trong các kĩ năng học tập môn Khoa học tự nhiên?
A.Kĩ năng quan sát. B. Kĩ năng phân loại. C. Kĩ năng liên kết. D. Kĩ năng đo.
9/Kết nối thông tin ở cột (A) với cột (B) để được câu hoàn chỉnh. Cột A Cột B Nối
9.Không khí là một hỗn hợp các A. sẽ cung cấp đầy đủ chất dinh dưỡng chất khí trong đó
cho cơ thể nhằm phát triển khỏe mạnh.
10.Ánh sáng Mặt Trăng có
B. bao gồm 78% khí nitrogen,21% khí được là do
oxygen và 1% các khí khác.
11.Kết hợp với các loại lương
C. phản xạ ánh sáng mặt trời.
thực, thưc phẩm phù hợp với lứa tuổi giới tính
Chọn đáp án đúng
12.Việc kết nối thông tin ở trên thể hiện kĩ năng gì trong các kĩ năng học tập môn Khoa học tự nhiên?
A.Kĩ năng quan sát. B. Kĩ năng liên kết. C. Kĩ năng phân loại. D. Kĩ năng đo.
II. TỰ LUẬN: (7 điểm) ĐỀ 1
13/(1đ) X là một nguyên tố ở ô số 15, thuộc chu kì 3, nhóm VA trong bảng tuần hoàn. Hãy xác định
điện tích hạt nhân, số electron, số lớp electron, số electron lớp ngoài cùng của X. Cho biết tên, kí
hiệu và vẽ sơ đồ cấu tạo nguyên tử của X.
14/(1đ) Cho các nguyên tố hóa học sau: H, B, Na,Ne, He, Al.
a) Những nguyên tố nào thuộc cùng một nhóm?
b) Những nguyên tố nào thuộc cùng một chu kì?
c) Những nguyên tố nào là kim loại? Phi kim? Khí hiếm?
15/(1đ) Hãy vẽ sơ đồ và mô tả quá trình tạo thành
a/Liên kết ion trong phân tử hợp chất sodium chloride (Na+Cl-).
b/Liên kết cộng hóa trị trong phân tử khí N
16/(1đ) Citric acid là hợp chất được sử dụng nhiều trong công nghiệp thực phẩm, dược phẩm. Trong
tự nhiên, citric acid có trong quả chanh và một số loại quả như bưởi, cam, … Citric acid có công
thức hóa học là C6H8O7. Hãy tính phần trăm khối lượng của nguyên tố C,O trong citric acid.
17/ Những phát biểu sau nói về đặc điểm của các hạt cấu tạo nên nguyên tử. Với mỗi phát biểu hãy
điền vào bảng tên hạt,từ phù hợp vào ô trống.( proton, neutron , electron,8amu,9amu,13amu) Phát biểu Loại hạt
(1) Hạt có trong lớp vỏ xung quanh hạt nhân ?
(2) Hạt có thể xuất hiện với số lượng khác nhau trong các nguyên tử của cùng một ? nguyên tố
(3) Hạt được tìm thấy cùng với proton trong hạt nhân ?
(4)Hạt mang điện tích dương ?
(5) Hạt không mang điện tích ?
(6) Hạt có khối lượng rất nhỏ, có thể bỏ qua khi tính khối lương nguyên tử ?
(7) Hạt mang điện tích âm ?
(8)Một nguyên tử có 4 proton, 5 neutron và 4electron. Khối lượng của nguyên tử đó …………. là:
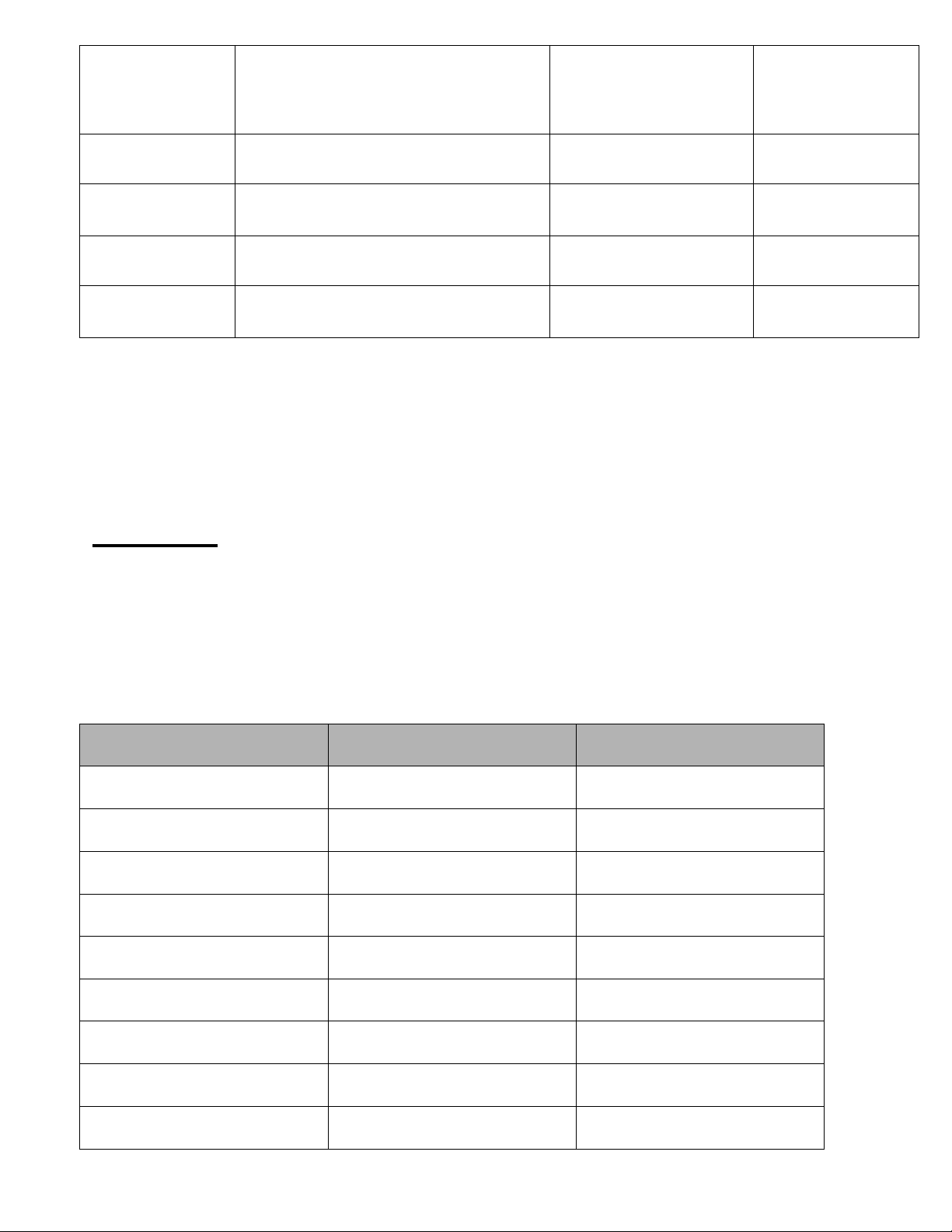
18/(2đ).Viết công thức hóa học và tính khối lượng phân tử (điền vào bảng )của các hợp chất có cấu
tạo phân tử như sau: Công thức hóa Khối lượng phân Hợp chất Cấu tạo phân tử học tử Melthane
1 nguyên tử C và 4 nguyên tử H Potassium oxide
2 nguyên tử K và 1 nguyên tử O Sodium chloride
1 nguyên tử Na và 1 nguyên tử Cl Water
2 nguyên tử H và 1 nguyên tử O ĐỀ 2
13/(1đ) X là một nguyên tố ở ô số 16, thuộc chu kì 3, nhóm VIA trong bảng tuần hoàn. Hãy xác định
điện tích hạt nhân, số electron, số lớp electron, số electron lớp ngoài cùng của X. Cho biết tên, kí
hiệu và vẽ sơ đồ cấu tạo nguyên tử của X.
14/(1đ) Cho các nguyên tố hóa học sau: O, S, Na, K, Ar,Ne.
a) Những nguyên tố nào thuộc cùng một nhóm?
b) Những nguyên tố nào thuộc cùng một chu kì?
c) Những nguyên tố nào là kim loại? Phi kim? Khí hiếm?
15/(1đ) Hãy vẽ sơ đồ và mô tả quá trình tạo thành:
a/Liên kết ion trong phân tử hợp chất magnesium oxide(Mg2+O2-)
b/Liên kết cộng hóa trị trong phân tử khí O2 .
16/(1đ) Calcium carbonate là thành phần chính của đá vôi, có công thức hóa học là CaCO3. Tính
phần trăm khối lượng của nguyên tố Ca,O trong hợp chất trên.
17/(1đ) Những phát biểu sau nói về đặc điểm của các hạt cấu tạo nên nguyên tử. Với mỗi phát biểu
hãy điền vào bảng tên hạt,từ phù hợp vào ô trống.( proton, neutron electron,10amu,11amu,16amu) Phát biểu Loại hạt
(1) Hạt mang điện tích dương ?
(2) Hạt được tìm thấy cùng với proton trong hạt nhân ?
(3) Hạt có thể xuất hiện với số lượng khác nhau trong các nguyên tử của cùng một nguyên tố ?
(4) Hạt có trong lớp vỏ xung quanh hạt nhân ?
(5) Hạt mang điện tích âm ?
(6) Hạt có khối lượng rất nhỏ, có thể bỏ qua khi tính khối lương nguyên tử ?
(7) Hạt không mang điện tích ?
(8)Một nguyên tử có 5 proton, 6 neutron và 5electron. Khối lượng của nguyên tử đó …………. là:
18/(2đ). Viết công thức hóa học và tính khối lượng phân tử (điền vào bảng) của các hợp chất có cấu
tạo phân tử như sau: Khối lượng phân Hợp chất Cấu tạo phân tử
Công thức hóa học tử Water
2 nguyên tử H và 1 nguyên tử O Sodium chloride
1 nguyên tử Na và 1 nguyên tử Cl Potassium oxide
2 nguyên tử K và 1 nguyên tử O Melthane
1 nguyên tử C và 4 nguyên tử H D) ĐÁP ÁN I/TRẮC NGHIỆM(3đ):
(Mỗi câu chọn đúng được 0,25 điểm) BANG DAP AN 08:27' Ngay 30/10/2022 Cau ĐỀ 1 ĐỀ 2 1 D B 2 B A 3 D B 4 C D 5 B C 6 A A 7 C D 8 A C 9 C B 10 A C 11 B A 12 C B II/TỰ LUẬN(7đ):
Câu 13. (1,0 điểm):
-Mỗi ý trả đúng 0,125đ -Vẽ sơ đồ dúng 0,25đ
✓ X ở ô số 15 ↔ Điện tích hạt nhân là +15 ✓ X có 15 electron
✓ X nằm ở chu kì 3 ↔ X có 3 lớp electron.
✓ X nằm ở nhóm VA ↔ X có 5 electron lớp ngoài cùng. ✓ X là Phosphorus ✓ Kí hiệu (P)
✓ Sơ đồ cấu tạo nguyên tử X: Câu 14. (1,0 điểm): a/(0,25đ điểm): b/(0,25đ điểm): c/(0,5đ điểm): Câu 15 (1 điểm):
-Vẽ đúng mỗi sơ đồ 0,5đ Câu 16 (1 điểm):
-Tính phần trăm đúng mỗi nguyên tố 0,5đ Câu 17. (1 điểm):
-Mỗi ý điền đúng 0,125đ Câu 18 (2 điểm):
-Mỗi CTHH đúng 0,25đ:CH4, K2O, NaCl, H2O
-Mỗi KLPT đúng 0,25đ:16amu,94amu,58,5amu,18amu ĐỀ 2
Câu 13. (1,0 điểm):
-Mỗi ý trả đúng 0,125đ -Vẽ sơ đồ dúng 0,25đ
✓ X ở ô số 16 ↔ Điện tích hạt nhân là +16 ✓ X có 16 electron
✓ X nằm ở chu kì 3 ↔ X có 3 lớp electron.
✓ X nằm ở nhóm VIA ↔ X có 6 electron lớp ngoài cùng. ✓ X là sulfur ✓ Kí hiệu (S)
✓ Sơ đồ cấu tạo nguyên tử X:
Câu 14. (1,0 điểm):
a/(0,25đ điểm): b/(0,25đ điểm): c/(0,5đ điểm): Câu 15 (1 điểm):
-Vẽ đúng mỗi sơ đồ 0,5đ Câu 16 (1 điểm):
-Tính phần trăm đúng mỗi nguyên tố 0,5đ Câu 17. (1 điểm):
-Mỗi ý điền đúng 0,125đ Câu 18 (2 điểm):
-Mỗi CTHH đúng 0,25đ:H2O,K2O,NaCl,CH4
-Mỗi KLPT đúng 0,25đ:18amu,94amu,58,5amu,16amu.




