

Preview text:
Cụm Bình Giang, Cẩm Giàng
ĐỀ THI THỬ TỐT NGHIỆP THPT NĂM 2025 Thanh Miện
MÔN THI: Hóa học 12 ĐỀ CHÍNH THỨC
Thời gian làm bài: 50 phút, không kể thời gian phát đề
(Đề thi gồm có 03 trang) Mã đề thi
Họ và tên thí sinh:.............................................................................. SBD:..................... 121
Cho biết nguyên tử khối của các nguyên tố: H=1; He=4; C =12; N=14; O=16; Na =23; Mg = 24; Al =27; S
=32; Cl = 35,5; K =39; Ca = 40; Cr =52; Mn = 55; Fe =56; Cu = 64; Zn =65; Br = 80; Ag = 108; Ba = 137.
PHẦN I. Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí
sinh chỉ chọn 1 phương án.
Câu 1. Khi điện phân dung dịch nào sau đây, tại anode xảy ra quá trình oxi hoá nước?
A. Dung dịch MgCl2.
B. Dung dịch ZnCl2.
C. Dung dịch CuCl2.
D. Dung dịch AgNO3.
Câu 2. Tiến hành các thí nghiệm sau:
(1)Cho Mg vào lượng dư dung dịch FeCl3.
(2)Cho Ba vào lượng dư dung dịch CuSO4.
(3)Cho Zn vào dung dịch CuSO4.
(4)Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
Thí nghiệm nào thu được kim loại ?
A. (2) và (3). B. (1) và (4). C. (1) và (2). D. (3) và (4).
Câu 3. Cho 0,02 mol Na vào 1 000 mL dung dịch chứa CuSO4 0,05 M và H2SO4 0,005 M. Hiện tượng của thí nghiệm trên là
A. chỉ có khí bay lên.
B. chỉ có kết tủa màu xạnh lam.
C. có khí bay lên và có kết tủa sau đó kết tủa tan.
D. có khí bay lên và có kết tủa màu xanh lam.
Câu 4. Liên kết trong mạng tinh thể kim loại là liên kết:
A. Cộng hoá trị B. Kim loại C. Cho nhận D. ion
Câu 5. Trong phân tử hydrocarbon X, hydrogen chiếm 25% về khối lượng. Công thức phân tử của X là A. C2H6. B. C2H4. C. C6H6. D. CH4.
Câu 6. Chất hay hỗn hợp chất nào sau đây không phải là hợp kim?
A. Đồng thiếc. B. Đồng. C. Thép. D. Đồng thau.
Câu 7. Cho biết số thứ tự của Al trong bảng tuần hoàn là 13. Số electron lớp ngoài cùng của Al là A. 3 B. 2 C. 4 D. 1
Câu 8. Kim loại nào sau đây khi tác dụng với HCl và tác dụng với Cl2 (được nung nóng) tạo thành cùng một sản phẩm muối chloride? A. Fe. B. Cu. C. Ag. D. Mg.
Câu 9. Cho các kim loại sau: K, Ba, Cu và Ag. Số kim loại điều chế được bằng phương pháp điện phân dung
dịch (điện cực trơ) là A. 1. B. 4. C. 2. D. 3.
Câu 10. Số nhóm amino (NH2) có trong một phân tử Lysine là A. 1 B. 4 C. 2 D. 3
Câu 11. Dung dịch X có pH =12, thì OH− của dung dịch là A. 0,12M B. 0,01M C. 0,20M D. 1,2M Trang 1/3 - Mã đề 121
Câu 12. Nguyên tử Fe có cấu hình 56Fe 26
. Cho các phát biểu sau về Fe:
(1) Nguyên tử của nguyên tố Fe có 8 electron ở lớp ngoài cùng.
(2) Nguyên tử của nguyên tố Fe có 30 neutron ở trong hạt nhân. (3) Fe là một phi kim. (4) Fe là nguyên tố d.
Trong các phát biểu trên, phát biểu nào là đúng
A. (2), (3) và (4).
B. (1), (2) và (4).
C. (1), (2), (3) và (4). D. (2) và (4).
Câu 13. Điện phân dung dịch gồm NaCl và HCl (điện cực trơ, có màng ngăn). Trong quá trình điện phân, giá
trị pH của dung dịch thu được so với dung dịch ban đầu là
A. không thay đổi.
B. tăng lên sau đó giảm xuống.
C. giảm xuống. D. tăng lên.
Câu 14. Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là A. Mg, Na, Ca. B. Na, Fe, K. C. Na, Cr, K. D. Na, Ba, K.
Câu 15. Cho các phát biểu sau:
(a) Glutamic acid có tính chất lưỡng tính.
(b) Amino acid là loại hợp chất hữu cơ tạp chức.
(c) Trong phân tử protein luôn chứa liên kết peptide.
(d) Thực hiện phản ứng trùng ngưng các amino acid đều thu được peptide.
(e) Thành phần nguyên tố của bột ngọt (mì chính) chỉ gồm C, H, Na và O.
Số phát biểu sai là A. 3 B. 4 C. 1 D. 2.
Câu 16. Ion kim loại nào sau đây bị điện phân trong dung dịch (với điện cực graphite)? A. Ca2+. B. Cu2+. C. K+. D. Na+.
Câu 17. Có thể thu được kim loại nào trong số các kim loại sau: Cu, Na, Ca, Al bằng cả ba phương pháp tách kim loại phổ biến? A. Al. B. Cu. C. Ca. D. Na.
Câu 18. Hợp chất nào dưới đây thuộc loại ester?
A. HOCH2CH2CHƠ.
B. CH3CH2CH2COOH. C. CH3CH2COOCH3. D. HOCH2COCH3.
PHẦN II. Câu hỏi trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d)
ở mỗi câu thí sinh chọn đúng hoặc sai.
Câu 1. Điện phân dung dịch chứa 0,1 mol CuSO4 và 0,2 mol NaCl (với điện cực trơ, màng ngăn xốp) đến
khi nước bắt đầu bị điện phân ở cả hai điện cực.
a) Dung dịch sau điện phân làm quỳ tím chuyển màu xanh.
b) Thứ tư điện phân ở cathode là Cu2+, H2O.
c) Thể tích khí (ở đkc) thoát ra ở cả 2 điện cực là 4,48 lit
d) Ở anode, số mol Cl2 tạo ra gấp bốn lần số mol O2.
Câu 2. Cho 3 thí nghiệm sau:
- Thí nghiệm 1: Cho mẩu sodium vào nước đã thêm vài giọt dung dịch phenolphtalein.
- Thí nghiệm 2: Cho một mẩu Aluminium (Al- nhôm) vào dung dịch hydrochloric acid loãng.
- Thí nghiệm 3: Cho một mẩu đồng(copper) vào dung dịch sulfuric acid đặc.
Mỗi phát biểu dưới đây là đúng hay sai?
a) Thí nghiệm 3 có sinh ra khí Z. Tỉ khối hơi của Z so với khí X thoát ra ở thí nghiệm 1 là 32.
b) Các kim loại bị oxi hoá trong cả ba thí nghiệm trên.
c) Tổng hệ số tối giản của các chất trong phương trình hoá học ở thí nghiệm 3 là 8.
d) Cả ba thí nghiệm trên đều thu được khí không màu, nhẹ hơn không khí. Trang 2/3 - Mã đề 121
Câu 3. Cho các phản ứng sau:
(1) CH3COOC2H5 + H2O (trong dung dịch H2SO4, đun nóng).
(2) HCOOCH3 + NaOH (dung dịch, đun nóng).
a) Sản phẩm thủy phân phản ứng (1) và (2) đều thu được CH3OH.
b) Vai trò NaOH trong phản ứng (2) là chất xúc tác.
c) Phản ứng (1) thuận nghịch, phản ứng (2) một chiều.
d) Phản ứng (1) và (2) đều là phản ứng thủy phân.
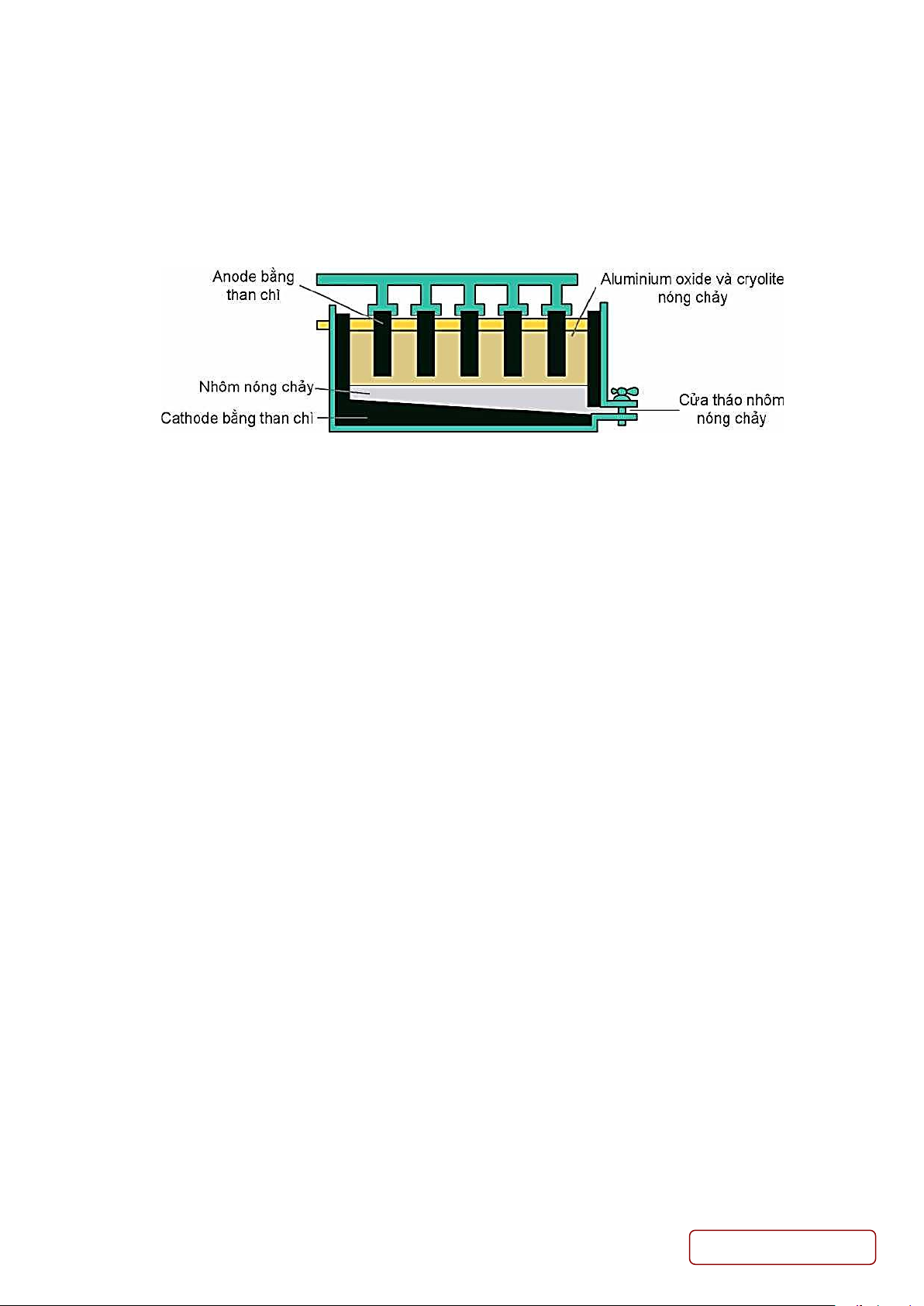
Câu 4. Quặng bauxite (thành phần chính Al2O3.2H2O) thường lẫn tạp chất. Sau khi loại bỏ tạp chất bằng
phương pháp hoá học thu được Al2O3. Do Al2O3 có nhiệt độ nóng chảy rất cao (2050 °C) nên Al2O3 được trộn
cùng với cryolite (Na3AlF6) để tạo thành hỗn hợp nóng chảy ở gần 1000 °C.
Sơ đồ thùng điện phân Al2O3
a) Phương pháp được sử dụng để tách Al từ Al2O3 (tinh chế từ quặng bauxite) là điện phân nóng chảy
b) Xúc tác cryolite tuy tiết kiệm nhiều năng lượng cũng như giảm giá thành chế tạo thùng điện phân., đồng
thời tạo ra chất lỏng vừa có tính dẫn điện tốt, vừa nổi lên trên Al lỏng để ngăn cách Al lỏng với không khí
c) Ở cực âm xảy ra sự oxi hoá ion O2–, cực dương xảy ra sự khử ion Al3+
d) Khí O2 tạo thành ở nhiệt độ cao, đốt cháy dần điện cực anode than chì thành CO và CO2. Do vậy, trong
quá trình điện phân phải hạ thấp dần các điện cực anode vào thùng điện phân.
PHẦN III. Câu trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1. Kim loại Fe có thể tan trong bao nhiêu dung dịch muối sau đây CuSO4, AgNO3, AlCl3, FeCl3, NaNO3?
Câu 2. Hỗn hợp khí X gồm ethylene và propyne. Cho a mol X tác dụng với dung dịch AgNO3 trong NH3, thu
được 17,64 gam kết tủa. Mặt khác a mol X phản ứng tối đa với 0,34 mol H2. Giá trị của a là ?
Câu 3. Điện phân dung dịch hỗn hợp gồm 7,45 gam KCl và 28,2 gam Cu(NO3)2 với các điện cực trơ, và màng
ngăn xốp, đến khí khối lượng dung dịch giảm đi 10,75 gam thì ngừng điện phân. Giả thiết lượng nước bay hơi
không đáng kể và hiệu suất điện phân là 100%. Xác định số lượng chất tan có trong dung dịch sau điện phân ?
Câu 4. Nếu thế khử chuẩn của điện cực dương là 0,80 V và thế khử chuẩn của điện cực âm là –0,76 V thì sức
điện động chuẩn của pin Galvani tạo từ hai điện cực trên là bao nhiêu?
Câu 5. Hỗn hợp X gồm FeO, Fe2O3 và Fe3O4. Cho khí CO qua m gam X nung nóng, sau một thời gian thu
được hỗn hợp chất rắn Y và hỗn hợp khí Z. Cho toàn bộ Z vào dung dịch Ca(OH)2 dư, đến phản ứng hoàn toàn,
thu được 4 gam kết tủa. Mặt khác, hòa tan hoàn toàn Y trong dung dịch H2SO4 đặc, nóng (dư), thu được
1,11555 lít khí SO2 (đkc, sản phẩm khử duy nhất) và dung dịch chứa 18 gam muối. Giá trị của m là bao nhiêu?
Câu 6. Cho các kim loại Al, Zn, Fe, Ag, Au. Có bao nhiêu kim loại nào tác dụng được với O2?
-------------- HẾT -------------- Trang 3/3 - Mã đề 121
Cụm Bình Giang, Cẩm Giàng
ĐỀ THI THỬ TỐT NGHIỆP THPT NĂM 2025 Thanh Miện
MÔN THI: Hóa học 12 ĐỀ CHÍNH THỨC
Thời gian làm bài: 50 phút, không kể thời gian phát đề
(Đề thi có 03 trang) BẢNG ĐÁP ÁN
ĐỀ THI THỬ TỐT NGHIỆP THPT NĂM 2025
PHẦN I: Trắc nghiệm nhiều lựa chọn
- Mỗi câu đúng được 0,25 điểm.
Mã đề 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 121
D D D B D B A D C C B D D D D B B C 122
B D B B B B A C B A C B C A B A D B 123
D A D A A A A C A A A D D C D A D D 124
B B B B D A D A D C A A D D A C B A 125
B D D C B A B A B D D A B C C B B C 126
D D A C A A C A B A D D D A A A A A 127
C C B A C B B A A A C B A C C B C D 128
D A D A D B D D D B A B B B B D C C
PHẦN II: Trắc nghiệm đúng sai
- Điểm tối đa mỗi câu là 1 điểm.
- Đúng 1 câu được 0,1 điểm; đúng 2 câu được 0,25 điểm; đúng 3 câu được 0,5 điểm; đúng 4 câu được 1 điểm. Mã đề Câu 1 Câu 2 Câu 3 Câu 4 121 a)S - b)Đ - c)S - d)S
a)Đ - b)Đ - c)S - d)S
a)S - b)S - c)Đ - d)Đ
a)Đ - b)Đ - c)S - d)Đ 122 a)S - b)S - c)S - d)Đ
a)Đ - b)Đ - c)S - d)Đ
a)Đ - b)S - c)S - d)Đ
a)S - b)Đ - c)S - d)Đ 123
a)Đ - b)S - c)Đ - d)Đ
a)Đ - b)Đ - c)S - d)S
a)Đ - b)S - c)S - d)Đ a)S - b)Đ - c)S - d)S 124 a)S - b)S - c)S - d)Đ
a)Đ - b)Đ - c)S - d)S
a)S - b)Đ - c)S - d)Đ
a)S - b)Đ - c)Đ - d)Đ 125 a)S - b)Đ - c)S - d)S
a)Đ - b)S - c)Đ - d)Đ
a)Đ - b)S - c)S - d)Đ
a)S - b)Đ - c)S - d)Đ 126 a)Đ - b)S - c)S - d)S
a)Đ - b)S - c)Đ - d)Đ
a)Đ - b)S - c)S - d)Đ
a)S - b)S - c)Đ - d)Đ 127 a)S - b)Đ - c)S - d)S
a)S - b)Đ - c)S - d)Đ
a)Đ - b)Đ - c)Đ - d)S
a)S - b)Đ - c)Đ - d)S 128
a)S - b)Đ - c)S - d)Đ
a)S - b)Đ - c)S - d)Đ a)Đ - b)S - c)S - d)S
a)Đ - b)Đ - c)Đ - d)S
PHẦN III: Trắc nghiệm trả lời ngắn - tự luận
- Mỗi câu đúng được 0,5 điểm. Mã đề Câu 1 Câu 2 Câu 3 Câu 4 Câu 5 Câu 6 121 3 0,22 3 1,56 7,12 3 122 0,22 3 1,56 3 7,12 3 123 7,12 3 1,56 0,22 3 3 124 3 7,12 3 3 0,22 1,56 125 7,12 3 1,56 3 3 0,22 126 3 3 1,56 0,22 3 7,12 127 1,56 3 7,12 0,22 3 3 128 3 7,12 3 1,56 0,22 3
Document Outline
- Made 121
- Câu 1. Khi điện phân dung dịch nào sau đây, tại anode xảy ra quá trình oxi hoá nước?
- Câu 14. Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là
- Dap an




