



Preview text:
Khoa học tự nhiên 8 Chân trời sáng tạo bài 7
Mở đầu trang 35 Khoa học tự nhiên 8: Có 2 cốc chứa cùng một thể tích nước muối
(dung dịch NaCl), một cốc mặn (đặc) và một cốc nhạt (loãng). Đại lượng nào dùng để
đánh giá độ đặc, loãng của dung dịch? Trả lời:
Đại lượng dùng để đánh giá độ đặc, loãng của dung dịch là nồng độ. 1. Dung dịch
Câu hỏi thảo luận 1 trang 35 Khoa học tự nhiên 8: Hãy xác định chất tan và dung môi
trong các dung dịch tạo thành ở Hình 7.1. Trả lời:
- Trong dung dịch muối: chất tan là muối ăn (NaCl); dung môi là nước.
- Trong dung dịch đường: chất tan là đường (C12H22O11); dung môi là nước.
Câu hỏi thảo luận 2 trang 35 Khoa học tự nhiên 8: Tại sao lại gọi nước đường, nước muối là các dung dịch? Trả lời:
Khi hòa tan đường hay muối (chất rắn) vào nước (chất lỏng) sẽ tạo thành nước đường hay
nước muối (hỗn hợp đồng nhất).
Do đó có thể gọi nước đường, nước muối là các dung dịch.
2. Độ tan của một chất trong nước
Câu hỏi thảo luận 3 trang 35 Khoa học tự nhiên 8: Độ tan của một chất trong nước
phụ thuộc vào những yếu tố nào? Trả lời:
Độ tan của một chất trong nước phụ thuộc vào nhiệt độ. Ngoài ra đối với chất khí, độ tan
phụ thuộc vào nhiệt độ và áp suất.
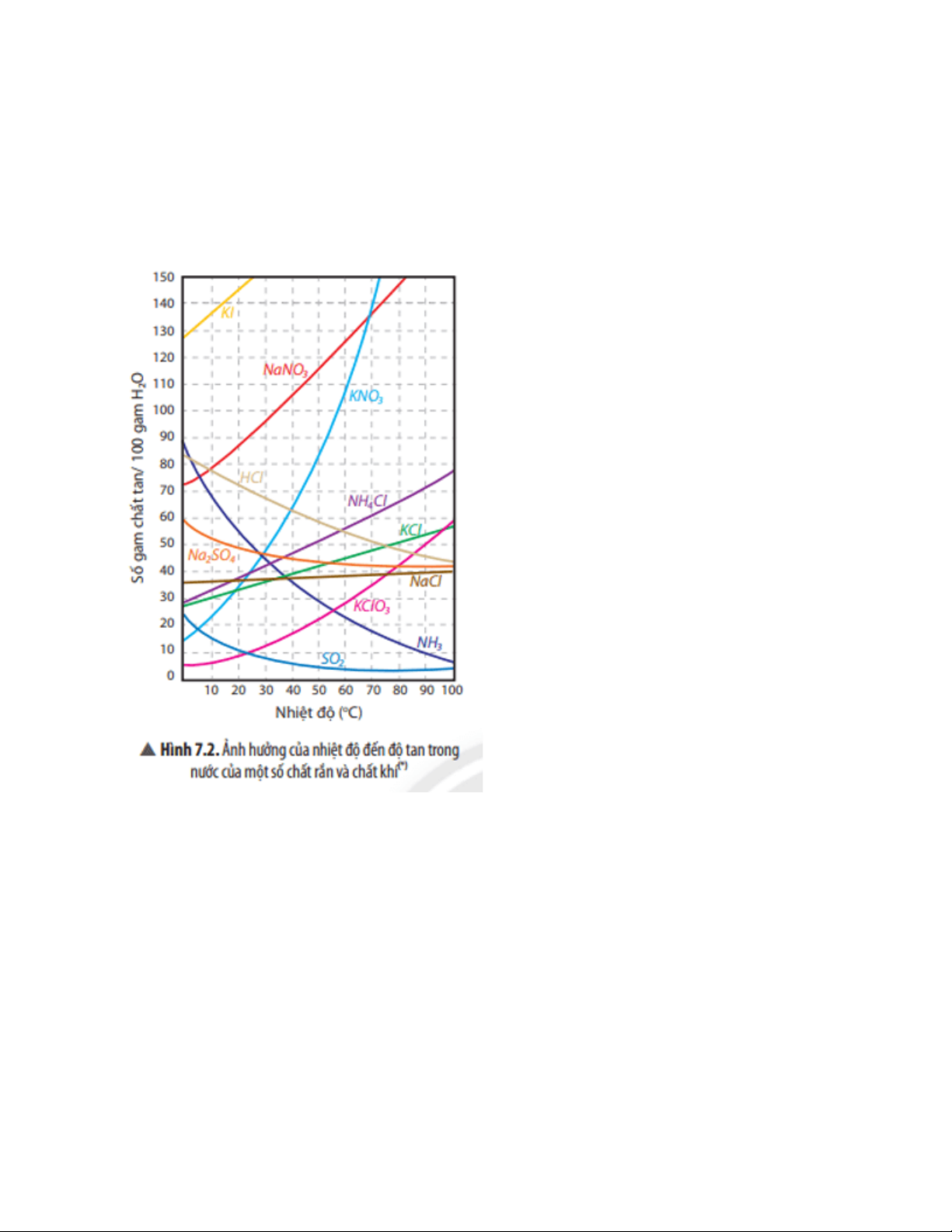
Câu hỏi thảo luận 4 trang 36 Khoa học tự nhiên 8: Quan sát đồ thị Hình 7.2, hãy nhận
xét độ tan của một số chất rắn và chất khí thay đổi như thế nào khi tăng nhiệt độ. Trả lời:
- Độ tan của chất rắn sẽ tăng khi tăng nhiệt độ (trừ số ít trường hợp như Na2SO4 …)
- Độ tan của chất khí sẽ tăng khi giảm nhiệt độ.
Luyện tập trang 36 Khoa học tự nhiên 8: Tính độ tan của muối Na2CO3 trong nước ở
25oC. Biết rằng ở nhiệt độ này khi hòa tan hết 76,75 gam Na2CO3 trong 250 gam nước thì
được dung dịch bão hoà. Trả lời: Áp dụng công thức:
Vận dụng trang 36 Khoa học tự nhiên 8: Hãy giải thích tại sao:
a) Khi pha nước chanh đá, người ta thường hòa tan đường hoặc muối ăn vào nước nóng,
sau đó mới cho đá lạnh vào.
b) Trong sản xuất nước ngọt có gas, người ta thường nén khí (carbon dioxide) ở áp suất cao. Trả lời:
a) Đường hoặc muối ăn tan tốt trong nước nóng, tan kém trong nước lạnh. Do đó khi pha
nước chanh đá, người ta thường hoà tan đường hoặc muối ăn vào nước nóng, sau đó mới cho đá lạnh vào.
b) Độ tan của khí carbon dioxide tăng khi ở áp suất cao. Do đó trong sản xuất nước ngọt
có gas, người ta thường nén khí (carbon dioxide) ở áp suất cao.
3. Nồng độ dung dịch
Câu hỏi thảo luận 5 trang 36 Khoa học tự nhiên 8: Quan sát Hình 7.3, hãy cho biết vì
sao 3 dung dịch của cùng một chất nhưng màu sắc của chúng lại khác nhau. Trả lời:
3 dung dịch của cùng một chất nhưng màu sắc của chúng lại khác nhau do nồng độ của chúng khác nhau.
Câu hỏi thảo luận 6 trang 36 Khoa học tự nhiên 8: Để tính nồng độ phần trăm của
dung dịch ta cần biết những thông tin gì? Trả lời:
Công thức tính nồng độ phần trăm của dung dịch:
Để tính nồng độ phần trăm của dung dịch ta cần biết những thông tin:
+ Khối lượng chất tan (mct);
+ Khối lượng dung dịch (mdd).
Luyện tập trang 37 Khoa học tự nhiên 8: Hoà tan 21 gam KNO3 vào 129 gam nước thu
được dung dịch KNO3. Tính nồng độ phần trăm của dung dịch KNO3 thu được. Trả lời:
Khối lượng dung dịch = khối lượng dung môi + khối lượng chất tan = 129 + 21 = 150 gam.
Nồng độ phần trăm của dung dịch KNO3 thu được là:
Câu hỏi thảo luận 7 trang 37 Khoa học tự nhiên 8: Làm thế nào để xác định được
nồng độ mol của dung dịch? Trả lời:
Công thức tính nồng độ mol của dung dịch:
Như vậy để tính nồng độ mol của dung dịch cần biết: số mol chất tan và thể tích dung dịch.
Luyện tập trang 37 Khoa học tự nhiên 8: Hoà tan 16 gam CuSO4 khan vào nước thu
được 200 ml dung dịch CuSO4. Tính nồng độ mol của dung dịch CuSO4. Trả lời: Số mol chất tan: Đổi 200 ml = 0,2 lít.
Nồng độ mol của dung dịch CuSO4 là:
4. Pha chế dung dịch
Luyện tập trang 38 Khoa học tự nhiên 8: Từ muối ăn NaCl, nước cất và các dụng cụ
cần thiết. Hãy tính toán và nêu cách pha chế 100 mL dung dịch NaCl có nồng độ 1 M. Trả lời:
Dụng cụ và hoá chất: 1 ống đong có dung tích 150 mL, đũa thuỷ tinh, cân đồng hồ hoặc
cân điện tử, muối ăn, nước cất. Tính toán:
Số mol chất tan: nNaCl= 0,1 × 1 = 0,1 (mol);
Khối lượng của 0,1 mol NaCl: mNaCl = 0,1 × 58,5 = 5,85 (gam).
Cách pha chế:
- Cân lấy 5,85 gam NaCl cho vào ống đong có dung tích 150 mL.
- Rót từ từ nước cất vào ống đong và khuấy nhẹ cho đủ 100 mL dung dịch, ta thu được 100 mL dung dịch NaCl.
Vận dụng trang 38 Khoa học tự nhiên 8: Gia đình bác nông dân muốn thực hiện dự án
nuôi cá trong một hồ nước lợ. Để có được một hồ chứa nước lợ (dung dịch 1% muối ăn)
thì bác nông dân đã cho vào hồ rỗng 1 000 kg nước biển (nước mặn chứa muối ăn với
nồng độ dung dịch 3,5%). Bác nông dân phải đổ thêm vào hồ một khối lượng nước ngọt
(có khối lượng muối ăn không đáng kể) là bao nhiêu để được một hồ chứa nước lợ có nồng độ 1% muối ăn? Trả lời:
Khối lượng muối có trong 1 000 kg nước biển là: mNaCl=1000×3,5100=35(kg)
Gọi x (kg) là khối lượng nước ngọt mà bác nông dân phải thêm vào hồ (x > 0).
Khi đó lượng nước trong hồ sau khi đổ nước ngọt là: 1 000 + x (kg).
Theo bài ra ta có phương trình: 351000+x×100=1⇔x=2500.
Vậy bác nông dân phải thêm vào hồ 2 500 kg nước ngọt.



