Preview text:
HÓA HỌC 10 BÀI 3 LUYỆN TẬP: THÀNH PHẦN NGUYÊN TỬ
A. Tóm tắt trọng tâm lý thuyết Hóa 10 bài 3
1. Nguyên tử được tạo nên bởi electron và hạt nhân. Hạt nhân được tạo nên
bởi proton và nơtron
qe = -1,602.10-19 C, quy ước bằng 1-; me ≈ 0,00055u
qp = 1,602.10-19C, quy ước bằng 1+; mp ≈1u qn = 0; mn ≈ 1u
2. Trong nguyên tử, số đơn vị điện tích hạt nhân Z = số proton = số electron
Số khối của hạt nhân (A) bằng tổng số proton (Z) và tổng số notron (N) Công thức: A = Z + N
- Nguyên tử khối coi như bằng tổng số các proton và các nowtron (gần đúng)
- Nguyên tử khối của một nguyên tố có nhiều đồng vị là nguyên tử khối trung
bình của các đồng vị đó.
- Nguyên tố hóa học là những nguyên tử có cùng số Z.
- Các đồng vị của một nguyên tố hóa học là các nguyên tử có cùng số Z, khác số N
3. Số hiệu nguyên tử Z và số khối A đặc trưng cho nguyên tử
Kí hiệu nguyên tử AX Z
- X là kí hiệu nguyên tố
- A là số khối (A = Z + N)
- Z là số hiệu nguyên tử 4. Đồng vị A .x + A .y + A .z + ....A .n Công thức 1 2 3 n A = 100
- Trong đó A1, A2, A3,… là số khối của các đồng vị.
- x,y,z,… là thành phần % của các đồng vị.
B. Bài tập mở rộng nâng cao
Bài 1. Cho biết 1u = 1,6605.10-27kg, nguyên tử khối của oxi bằng 15,999. Hãy tính
khối lượng của một nguyên tử oxi ra kg. Hướng dẫn giải
mO = 15,999.1,6605.10-27 = 2,667.10-26 kg
Bài 2. Cho biết khối lượng nguyên tử của C gấp 11,905 lần khối lượng nguyên tử
của hiđro. Hãy tính nguyên tử khối hiđro ra u và gam. Biết rằng nguyên tử khối của C bằng 12. Hướng dẫn giải
Vì khối lượng của C =12 nên khối lượng của nguyên tử H bằng:
+ Tính theo u: 12 u/11,905 = 1,008u + Tính theo gam:
1,008u.1,6605.10-24 = 1,674.1-24 gam
Bài 3. Kết quả phân tích cho thấy trong phân tử hơi H2O có 88,809% O và
11,191% H theo khối lượng. Biết nguyên tử khối của O là 15,999. Hãy xác định
nguyên tử khối của hiđro. Hướng dẫn giải CTPT của nước H2O
Ta có hơi nước có 88,809% khối lượng O nên ta có
MH2O = 16. (100/88,809%) = 18,0162 Mà MH2O = 2.MH + MO => 2MH + 15,999 = 18,0162 => MH = 1,0086
Bài 4. Trong 1,5 kg đồng có bao nhiêu gan electron? Cho biết 1 mol nguyên tử
đồng có khối lượng bằng 63,546 gam, một nguyên tử đồng có 29 electron. Hướng dẫn giải
1 nguyên tử Cu có khối lượng = 63,546 x 1,6605. 10-24 = 1,055.10-22g.
Ta có trong 1,5 kg Cu có 1,5. 1000 : (1,055.10 - 22) = 1,42.1025 nguyên tử Cu
=> KL electron trong 1,5 kg Cu là 29. 9,1095. 10-28 . 1,42. 1025 = 0,3755g
Bài 5. Nguyên tử kẽm có bán kính R = 1,35.10-10m, có khối lượng nguyên tử là 4
65u. Tính khối lượng riêng của nguyên tử kẽm. Biết Vhình cầu = . r3. 3 Hướng dẫn giải
a) rZn = 1,35.10-10m = 0,135.10-7 cm ( 1 nm = 10-9 m) 1 u = 1,6605.10-24 g
mZn = 65.1,6605.10-24 g = 1,079.10-22
V nguyên tử Zn = 4/3πr3 = 4/3.π(0,135.10-7 ) = 10,3.10-24 cm3
D nguyên tử Zn = m/V = 1,079.10-22/10,3.10-24 =10,48 g/cm3 0
Bài 6. Nguyên tử nhôm có bán kính 1,43 A và nguyên tử khối là 27u. Hãy xác
định khối lượng riêng khối lượng riêng của nhôm là bao nhiêu? Biết rằng trong
tinh thể nhôm các nguyên tử chỉ chiếm 74% thể tích còn lại là các khe trống? Hướng dẫn giải
Ta có V 1 mol nguyên tử Al = M/d.74% = 27/d.74%
V 1 mol nguyên tử Al = V 1 mol nguyên tử Al/ 6,023.1023 = 27/(d. 6,023.1023).74% Mặt khác ta có:
V1 mol nguyên tử Al = 4/3πr3 = 27/(d. 6,023.1023).74% => D = 2,7 g/cm3
Bài 7. Tính bán kính gần đúng của nguyên tử canxi, biết thể tích của 1 mol canxi
bằng 25,87cm3. Biết rằng trong tinh thể các nguyên tử canxi bằng 74% thể tích. Hướng dẫn giải 25,87 74 Ta có V − nguyên tử canxi = 23 3 . = 3,19.10 cm 23 6,10 100 V nguyên tử Ca = 4/3πr3 23 − 3 = 3,19.10 cm 1 3 23 3,19.10− 8 r =
=1,96.10− cm = 0,196nm 4 3
Bài 8. Nếu thực nghiệm nhận rằng nguyên tử Ca, Cu đều có dạng hình cầu, sắp
xếp đặt khít bên cạnh nhau thì thể tích chiếm bởi các nguyên tử kim loại chỉ bằng
74% so với toàn thể tích khối tinh thể. Khối lượng riêng ở điều kiện tiêu chuẩn
của chúng ở thể rắn tương ứng là 1,55g/cm3; 8,9g/cm3 và nguyên tử khối của
canxi là 40,08u, của đồng là 63,546u. Hãy tính bán kính nguyên tử Ca và nguyên tử Cu. Hướng dẫn giải Thể tích 1 mol Ca 40, 08 74 4 23 3 V = . = 6,02.10 . r 1, 55 100 3 4 Trong đó 3 V = r 3
Còn 6,02.1023 là số lượng nguyên tử của 1 mol Ca => r = 1,96.10-8
Bài 9. Nguyên tử của một nguyên tố X có tổng số hạt cơ bản (e, p, n) là 82, trong
đó số hạt mang điện nhiều hơn số hạt không mang điện là 22. Xác định số hiệu
nguyên tử, số khối và kí hiệu nguyên tố. Hướng dẫn giải
Ta có tổng số hạt là 82 => 2p + n = 82 (1)
Số hạt mang điện ( p + e = 2p) nhiều hơn số hạt không mang điện (n) là 22: 2p - n = 22 (2)
Giải hệ phương trình (1), (2) được: p = e = 26, n = 30
Số hiệu nguyên tử là 26
Số khối 56 . Kí hiệu hóa học là Fe 79
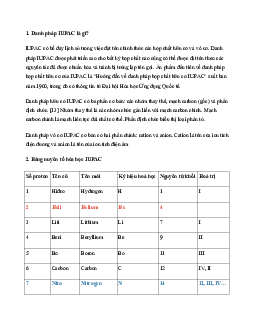
Câu 10. Trong tự nhiên nguyên tố Brom có 2 đồng vị, trong đó đồng vị Br 35
chiếm 54,5% về số lượng. Số khối của đồng vị còn lại bằng bao nhiêu Hướng dẫn giải
Đặt A2 là số khối của đồng vị thứ hai
Phần trăm số lượng của nó là: 100 - 54,5 = 45,5
x .A + x .A 54,5.79 + 45,5.A Ta có: 1 1 2 2 2 M = = = 79,91 = A = 81 2 100 100