











Preview text:
HỌ TÊN:---------------------------------------------
ĐỀ CƯƠNG ÔN TẬP CUỐI KÌ 1- HOÁ 11 (2025-2026)
Phần 1. TRẮC NGHIỆM NHIỀU LỰA CHỌN
A. THỜI GIAN: 45 PHÚT
B. CẤU TRÚC ĐỀ THI (04 PHẦN)
PHẦN 1: 16 Câu trắc nghiệm 4 lựa chọn – 4.0 điểm.
PHẦN 2: 02 câu trắc nghiệm (Đ/S)- 2.0 điểm.
PHẦN 3: 04 trắc nghiệm trả lời ngắn – 2.0 điểm
PHẦN 4: 03 câu tự luận - 2.0 điểm.
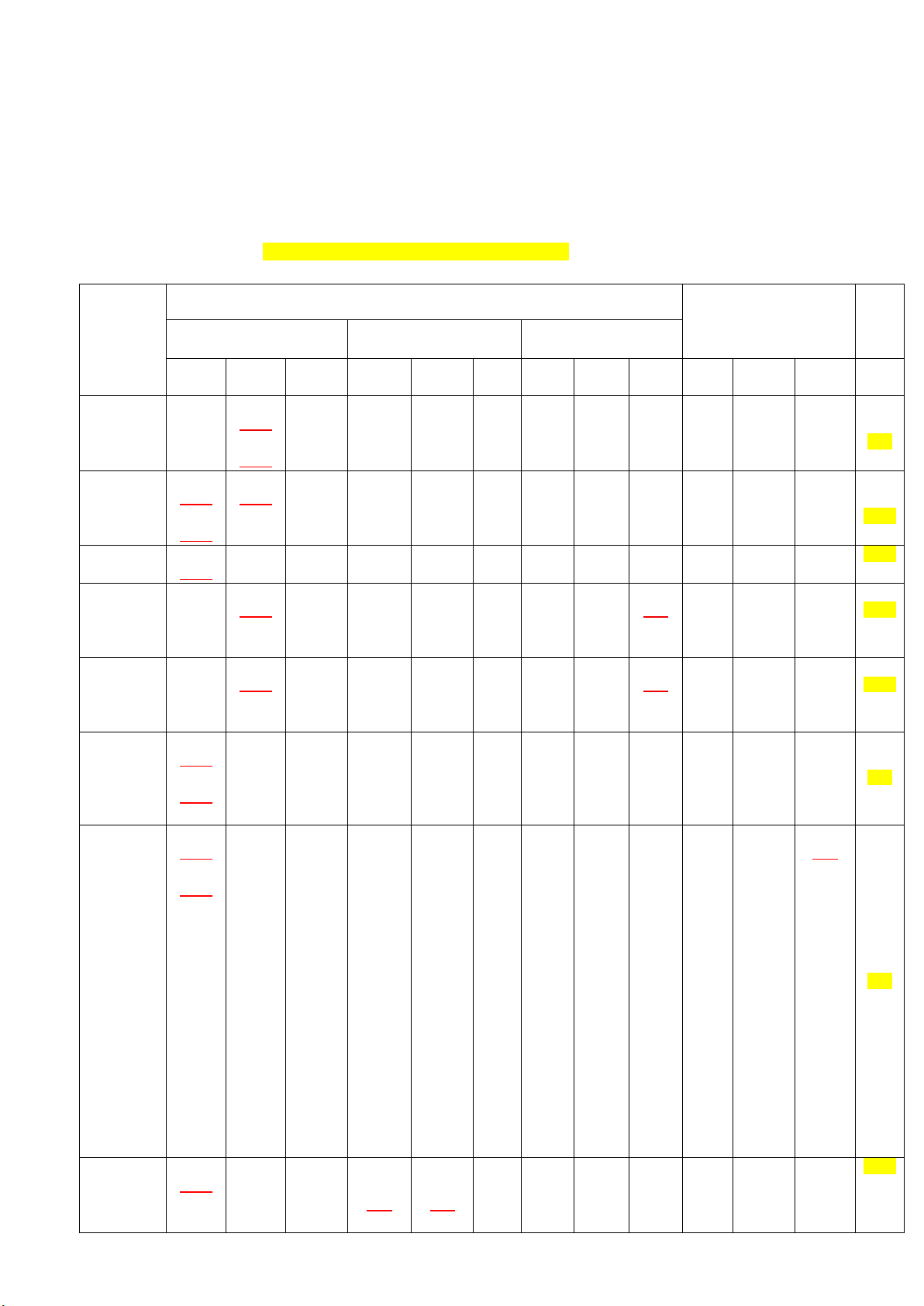
C. MỨC ĐỘ ĐÁNH GIÁ: 40% Nhận biết; 30% Thông hiểu; 30% Vận dụng D. MA TRẬN Đơn vị kiến Phần trắc nghiệm Phần tự luận Điểm thức Phần I (TNNLC) Phần II (TN Đ/S) Phần III (TN TLN) Nhận Thông Vận Nhận Thông Vận Nhận Thông Vận Nhận Thông Vận biết hiểu dụng biết hiểu dụng biết hiểu dụng biết hiểu dụng Khái niệm P1.C1 cân bằng hoá 0,25đ học P1.C2 0,5đ 0,25đ Cân bằng P1.C3 P1.C4 trong dung 0,25đ 0,25đ dịch nước P1.C5 0,75đ 0,25đ Đơn chất P1.C6 0,25đ nitrogen 0,25đ Ammonia P1.C7 P3.C1 và một số 0,25đ 0,5đ 0,75đ hợp chất ammnium Một số hợp P1.C8 P3.C2 chất với 0,25đ 0,5đ 0,75đ oxygen của nitrogen P1.C9 Sulfur và 0,25đ Sulfur P1.C10 0,5đ dioxide 0,25đ P1.C11 P4.C1 0,25đ 0,5đ P1.C12 (Bài 0,25đ toán thực tế liên quan đến Sulfuric sản 1,0đ acid và xuất muối sulfate H2SO4 Hoặc bài toán liên qua đên oleum) Hợp chất P1.C13 P2.C1a, P2.C1c, 1,25đ hữu cơ và 0,25đ C1b C1d hóa học hữu 0,5đ 0,5đ cơ 1 Phương P1.C14 P2.C2a, P2.C2c, P3.C3 pháp tách 0,25đ C2b C2d 0,5đ 1,75đ biệt và tinh 0,5đ 0,5đ chế hợp chất hữu cơ P1.C15 P3.C4 P4.C2 0,25đ 0,5đ 1,0đ (Lập CTPT HCHC 1,75đ dựa Công thức phân tử hợp vào chất hữu cơ %m các nguyên tố và phổ khối lượng) P1.C16 P4.C3 0,25đ 0,5đ (Cho CTCT của Cấu tạo hóa HCHC, học hợp xác định 0,75đ chất hữu cơ các nhóm chức có trong HCHC đã cho) 10 6 4 4 1 3 1 2 2,5đ 1,5đ 1,0đ 1,0đ 0,5đ 1,5đ 0,5đ 1,5đ Tổng 16 8 4 2 10,0đ 4,0đ 2đ 2,0đ 2,0đ
ĐỀ CƯƠNG ÔN TẬP
A. PHẦN TRẮC NGHIỆM
Phần 1. TRẮC NGHIỆM NHIỀU LỰA CHỌN
CHỦ ĐỀ 1. Khái niệm về cân bằng hoá học
Câu 1. Phản ứng thuận nghịch là phản ứng
A. phản ứng xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
B. có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
C. chỉ xảy ra theo một chiều nhất định.
D. xảy ra giữa hai chất khí.
Câu 2. Phản ứng nào sau đây là phản ứng thuận nghịch?
A. Mg + 2HCl → MgCl2 + H2.
B. 2SO2 + O2 ⇌ 2SO3. o o C. C t t 2H5OH + 3O2 2CO2 + 3H2O. D. 2KClO3 2KCl + 3O2
Câu 3. Phát biểu nào sau đây không đúng?
A. Cân bằng hóa học là một cân bằng tĩnh.
B. Ở trạng thái cân bằng, các chất không phản ứng với nhau.
C. Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
D. Ở trạng thái cân bằng, nồng độ các chất sản phẩm luôn lớn hơn nồng độ các chất đầu.
Câu 4. Trạng thái cân bằng của mọi phản ứng thuận nghịch luôn có tốc độ phản ứng thuận … (1) … tốc độ phản
ứng nghịch, các phản ứng thuận và nghịch luôn diễn ra. Như vậy, cân bằng hóa học là … (2) … Điền cụm từ thích
hợp vào (1), (2) lần lượt là
A. (1) lớn hơn, (2) cân bằng động.
B. (1) nhỏ hơn, (2) cân bằng tĩnh. 2
C. (1) bằng, (2) cân bằng động.
D. (1) bằng, (2) cân bằng tĩnh.
Câu 5. Hằng số cân bằng KC của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ.
B. Nhiệt độ. C. Áp suất. D. Chất xúc tác.
Câu 6. Sự phá vỡ cân bằng cũ để chuyển sang một cân bằng mới do các yếu tố bên ngoài tác động được gọi là
A. sự biến đổi chất.
B. sự dịch chuyển cân bằng.
C. sự chuyển đổi vận tốc phản ứng.
D. sự biến đổi hằng số cân bằng.
Câu 7. Cho các nhận xét sau:
(a) Ở trạng thái cân bằng, nồng độ chất trong hỗn hợp phản ứng không thay đổi.
(b) Phản ứng thuận nghịch là phản ứng chỉ xảy ra theo một chiều nhất định.
(c) Ở trạng thái cân bằng, các chất không phản ứng với nhau.
(d) Với một phản ứng hóa học, khi hằng số cân bằng rất lớn so với 1 thì ở trạng thái cân bằng, nồng độ các chất
sản phẩm lớn hơn nồng độ các chất phản ứng.
Số nhận xét đúng là A. 1. B. 2. C. 3. D. 4.
Câu 8. Cho cân bằng tổng quát sau: aA(g) + bB(g) ⇌ cC(g) + dD(g). Biểu thức tính hằng số cân bằng (KC) của cân bằng trên là [A].[B] a b [A] .[B] c d [C] .[D] [C].[D] A. K . B. K . C. K . D. K . C [C].[D] C c d [C] .[D] C a b [A] .[B] C [A].[B]
Câu 9. Phản ứng tổng hợp ammonia xảy ra như sau: N (g) 3H (g) 2NH (g) 2 2 3
Biểu thức biểu diễn hằng số cân bằng Kc của phản ứng là 3 NH NH H . N H . N 2 2 2 2 3 3 2 A. K = . B. K = . C. K . D. K = . C C C 2 C H 3 . N H . N NH NH3 3 2 2 2 2
Câu 10. Biểu thức nào sau đây là biểu thức hằng số cân bằng (KC) của phản ứng:
C(s) + 2H2(g) ⇌ CH4(g) [CH ] [CH ] [CH ] [CH ] A. 4 K . B. 4 K . C. 4 K . D. 4 K . C [H ] C 2 [C].[H ] C [C].[H ] C 2 [H ] 2 2 2 2
Câu 11. Cho cân bằng sau trong bình thủy tinh kín màu: 2NO
2 (g) (màu nâu đỏ) ⇌ N2O4 (g) (không màu); H r
Khi hơ nóng bình thì màu nâu đỏ đậm dần, điều này chứng tỏ phản ứng thuận có
A. H > 0, phản ứng tỏa nhiệt.
B. H < 0, phản ứng tỏa nhiệt. r r
C. H > 0, phản ứng thu nhiệt.
D. H < 0, phản ứng thu nhiệt. r r
Câu 12. Cân bằng nào dưới đây không có sự chuyển dịch khi tăng hay giảm áp suất của hệ?
A. 2SO (g) O (g) 2SO (g) . B. PCl (g) Cl (g) + PCl (g) . 2 2 3 5 2 3
C. H (g) I (g) 2HI(g) .
D. N (g) 3H (g) 2NH (g) . 2 2 2 2 3
Câu 13. Cho cân bằng hoá học sau: 4NH
3(g) + 5O2 ⇌ 4NO(g) + 6H2O(g) o H = –905 kJ. r 298
Yếu tố nào sau đây không làm cân bằng bị chuyển dịch?
A. Giảm nhiệt độ.
B. Tăng áp suất.
C. Giảm nồng độ của O2. D. Thêm xúc tác Pt.
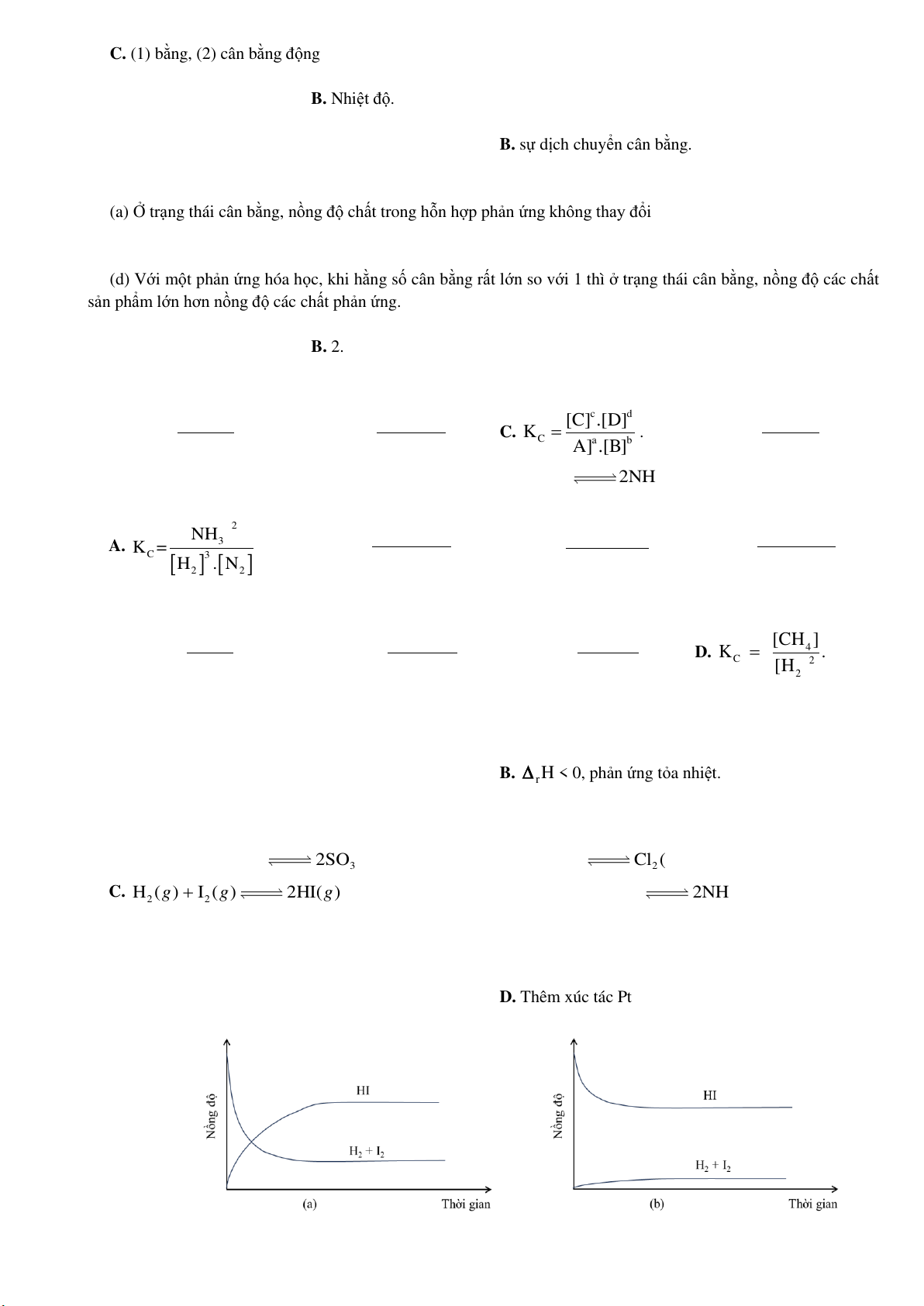
Câu 14. Quan sát hình dưới đây và chọn phát biểu đúng: 3
A. Cả hai đồ thị đều mô tả phản ứng đã đạt đến trạng thái cân bằng.
B. Cả hai đồ thị đều không mô tả phản ứng đã đạt đến trạng thái cân bằng.
C. Chỉ đồ thị (a) mô tả phản ứng đã đạt đến trạng thái cân bằng.
D. Chỉ đồ thị (b) mô tả phản ứng đã đạt đến trạng thái cân bằng.
Câu 15. Ester là hợp chất hữu cơ có mùi thơm nên một số ester được sử dụng làm bánh, thực phẩm. Phản ứng điều
chế ester ethyl acetate như sau: CH COOH(l) C H OH(l)
CH COOC H (l) + H O(l) . Cân bằng trên 3 2 5 3 2 5 2
dịch chuyển theo chiều nghịch nếu
A. tăng nồng độ của CH3COOH.
B. tăng nồng độ của C2H5OH.
C. tăng nồng độ của CH3COOC2H5.
D. thêm chất xúc tác H2SO4 đặc vào hệ.
Câu 16. Cho cân bằng hoá học sau: H g I g 2HI g 0 H 9 ,6KJ 2 2 r 298
Nhận xét nào sau đây không đúng?
A. Khi tăng nhiệt độ, cân bằng trên chuyển dịch theo chiều nghịch.
B. Ở nhiệt độ không đổi, khi tăng áp suất thì cân bằng không bị chuyển dịch.
C. Ở nhiệt độ không đổi, khi tăng nồng độ H2, hoặc I2 thì giá trị hằng số cân bằng tăng.
D. Ở trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
Câu 17. Cho các phản ứng sau: 1) H 2(g) + I2(g) ⇌ 2HI(g), H 0 r 298 2) 2NO(g) + O 2(g) ⇌2NO2, H 0 r 298 3) CO(g) + Cl 2(g) ⇌ COCl2(g), H 0 r 298 4) CaCO ( s) CaO(s) CO ( g) , H 0 3 2 r 298
Khi giảm nhiệt độ hoặc tăng áp suất những cân bằng nào trên đây đều chuyển dịch theo chiều thuận? A. 1, 2. B. 1, 3, 4. C. 2, 3. D. 1, 3.
Câu 18. Cho phản ứng: N 2 (g) + 3H2 (g) ⇌ 2NH3 (g); o H
= –92 kJ. Hai biện pháp đều làm cân bằng chuyển r 298
dịch theo chiều thuận là
A. giảm nhiệt độ và giảm áp suất.
B. tăng nhiệt độ và tăng áp suất.
C. giảm nhiệt độ và tăng áp suất.
D. tăng nhiệt độ và giảm áp suất.
Câu 19. Cho các cân bằng hoá học:
(1) CH4(g) + H2O(g) ⇌CO(g) + 3H2(g).
(3) 2SO2(g) + O2(g) ⇌2SO3(g) (2) H2(g) + I2(g) ⇌ 2HI(g) (4) 2NO2(g) ⇌ N2O4(g)
Khi thay đổi áp suất những cân bằng hóa học bị chuyển dịch là
A. (1), (2), (3). B. (2), (3), (4).
C. (1), (3), (4). D. (1), (2), (4).
Câu 20. Cho phản ứng: 2NOCl(g) ⇌ 2NO(g) + Cl2(g). Ở nhiệt độ không đổi, hằng số cân bằng của phản ứng trên 1
là KC = 2,4.10–7. Hằng số cân bằng KC’ của phản ứng: NO(g) +
Cl2(g) ⇌ NOCl(g) là bao nhiêu? 2
A. KC’ = 2,4.10–7.
B. KC’ = 1,2.10–7.
C. KC’ = –1,2.10–7. D. KC’ = 2041,2.
CHỦ ĐỀ 2. Cân bằng trong dung dịch nước
Câu 1. Phát biểu nào sau đây đúng khi nói về sự điện li?
A. Sự điện li là quá trình phân li một chất trong nước thành ion.
B. Sự điện li quá trình hoà tan một chất vào nước tạo thành dung dịch.
C. Sự điện li là quá trình phân li một chất dưới tác dụng của dòng điện.
D. Sự điện li thực chất là quá trình oxi hoá - khử.
Câu 2. Vì sao dung dịch của các muối, acid, base dẫn điện?
A. Do có sự di chuyển của electron tạo thành dòng elctron.
B. Do phân tử của chúng dẫn được điện.
C. Do các ion hợp phần có khả năng dẫn điện.
D. Do muối, acid, base có khả năng phân li ra ion trong dung dịch.
Câu 3. Dung dịch nào sau đây có khả năng dẫn điện?
A. Dung dịch đường.
B. Dung dịch rượu. 4
C. Dung dịch muối ăn. D. Nước cất.
Câu 4. Chất nào sau đây thuộc loại điện li yếu? A. HF. B. NaCl. C. HCl. D. KNO3.
Câu 5. Các chất trong dãy nào sau đây là những chất điện li mạnh?
A. HCl, NaOH, CH3COOH. B. KOH, NaCl, H3PO4.
C. HCl, NaOH, NaCl. D. NaNO3, NaNO2, NH3.
Câu 6. Cho các chất: NaOH, HCl, HNO3, NaNO3, saccharose (C12H22O11), ethanol (C2H5OH), glycerol
(C3H5(OH)3), KAl(SO4)2.12H2O. Trong các chất trên, có bao nhiêu chất tạo được dung dịch dẫn điện? A. 5. B. 3. C. 6. D. 2.
Câu 7. Phương trình điện li nào dưới đây viết đúng? A. H – 2SO4 → 2H+ + SO4
B. NaOH ⇌ Na+ + OH–.
C. HF ⇌ H+ + F–.
D. AlCl3 → Al3+ + Cl3–.
Câu 8. Cho phương trình: HCOOH + H2O ⇌ HCOO– + H3O+. Trong phản ứng nghịch, theo thuyết Bronsted – Lowry chất nào là acid? A. HCOOH. B. H2O.
C. HCOO–. D. H3O+.
Câu 9. Đặc điểm nào sau đây là không đúng khi mô tả về base yếu?
A. Trong dung dịch, không phân li hoàn toàn ra OH–.
B. Có khả năng nhận H+.
C. Dung dịch nước của chúng dẫn điện.
D. Có khả năng cho H+.
Câu 10. Dung dịch chất nào sau đây có môi trường base? A. HCl. B. NaCl. C. KOH. D. H2SO4.
Câu 11. Dung dịch của một base ở 25oC có A. [H+] = 1,0.10-7M.
B. [H+] < 1,0.10-7M.
C. [H+] > 1,0.10-7M.
D. [H+][OH-] > 1,0.10-14M.
Câu 12. Dung dịch chất nào sau đây có pH < 7? A. NaI. B. NaNO2. C. NaNO3. D. FeBr2.
Câu 13. Hòa tan một acid vào nước ở 250C, nhận xét nào sau đây là đúng?
A. [H ] [OH ]. B. [H ] [OH ]. C. [H ] [OH ]. D. 14 [H ].[OH ] 1, 0.10 .
Câu 14. Dung dịch chất nào sau đây làm quỳ tím chuyển thành màu xanh? A. HCl. B. Na2S. C. KNO3. D. C2H5OH.
Câu 15. Phương trình ion rút gọn của phản ứng cho biết
A. những ion nào tồn tại trong dung dịch.
B. nồng độ những ion nào trong dung dịch lớn nhất.
C. bản chất của phản ứng trong dung dịch các chất điện li.
D. không tồn tại phân tử trong dung dịch các chất điện li.
Câu 16. Dãy nào sau đây gồm các ion cùng tồn tại trong một dung dịch? A. Ba2+, Ag+, CO 2- 3 , Cl–. B. Na+, H+, F–, K+. C. NH + – 2– 4 , NO3 , Cl–, Na+.
D. Mg2+, CO3 , Cl–, Ca2+.
Câu 17. Trong số các dung dịch NaOH, HCl, Ba(OH)2, H2SO4 đều có cùng nồng độ 0,1 M, dung dịch chất nào có giá trị pH nhỏ nhất? A. NaOH. B. HCl. C. Ba(OH)2. D. H2SO4.
Câu 18. Cho các dung dịch có cùng nồng độ: NaOH (1), CH3COOH (2), HCl (3), KNO3 (4). Giá trị pH của các
dung dịch được sắp xếp theo chiều tăng từ trái sang phải là
A. (3), (2), (4), (1). B. (4), (1), (2), (3).
C. (1), (2), (3), (4). D. (2), (3), (4), (1).
Câu 19. Đối với dung dịch acid yếu CH3COOH 0,10M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng? A. [H+] = 0,10M.
B. [H+] < [CH3COO-].
C. [H+] > [CH3COO-]. D. pH > 1.
Câu 20. Giá trị pH của dung dịch NaOH 0,1 M là A. 1. B. 13. C. 11. D. 3. 5
Câu 21. Mục đích chính của chuẩn độ acid - base là
A. xác định xem phản ứng hóa học có xảy ra hay không.
B. xác định nồng độ của một chất bằng dung dịch chuẩn đã biết nồng độ.
C. kiểm tra lại nồng độ của dung dịch đã biết.
D. để kiểm tra chất lượng của chất phản ứng.
Câu 17. Để xác định nồng độ của một dung dịch NaOH, người ta đã tiến hành chuẩn độ bằng dung dịch HCl 0,1
M. Để chuẩn độ 10 mL dung dịch NaOH này cần 12 mL dung dịch HCl. Nồng độ của dung dịch NaOH trên là A. 0,1. B. 1,2. C. 0,12. D. 0,012.
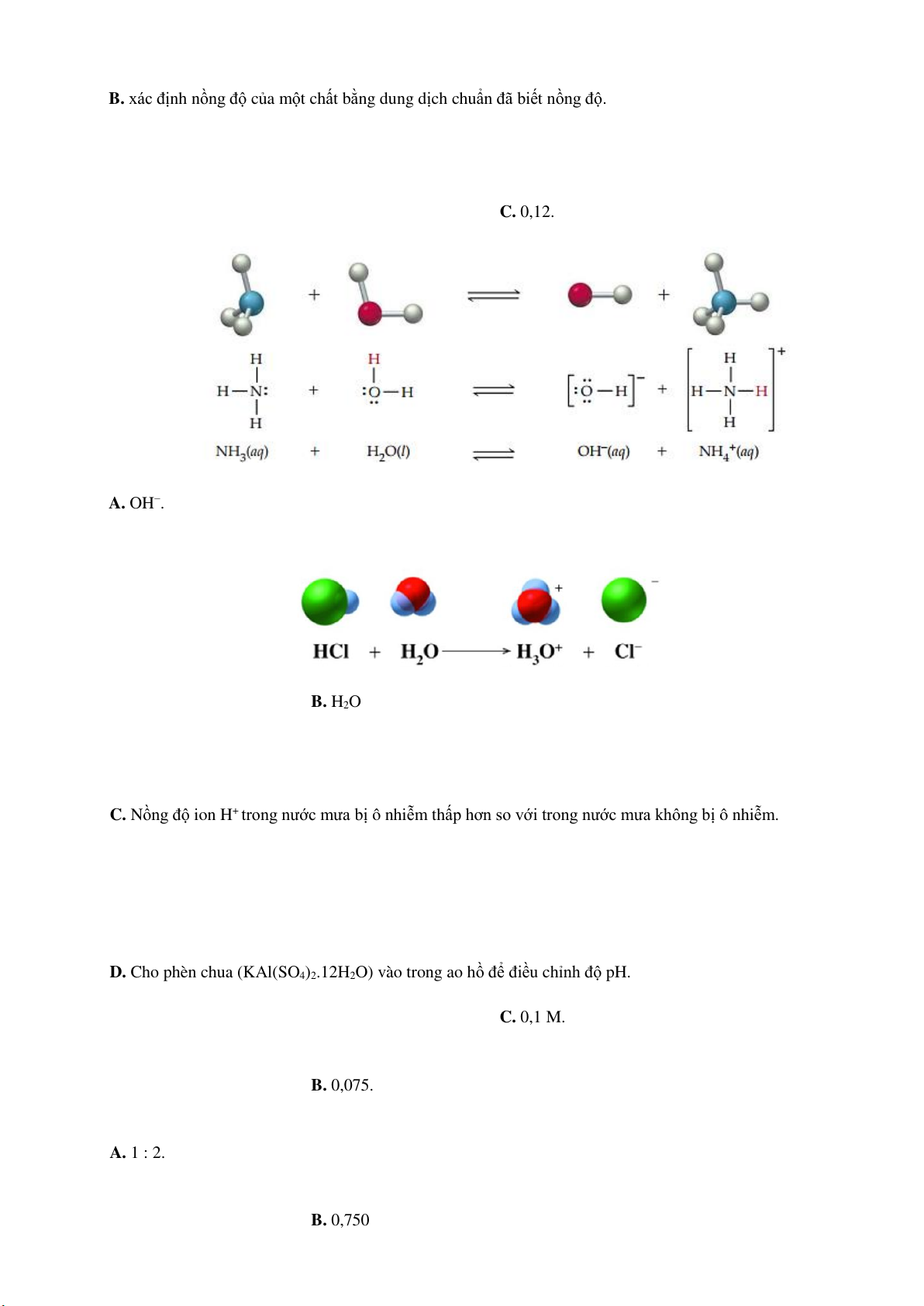
Câu 22. Hình dưới đây mô tả sự phân li của NH3 trong nước:
Trong phản ứng nghịch, chất đóng vai trò base là A. OH−. B. H2O. C. NH3. D. NH . 4
Câu 23. Hình dưới đây mô tả sự phân li của HCl trong nước:
Chất nhận H+ trong phương trình trên là A. HCl. B. H2O. C. H3O+. D. Cl–.
Câu 24. Tại khu vực bị ô nhiễm, pH của nước mưa đo được là 4,5 còn pH của nước mưa tại khu vực không bị ô
nhiễm là 5,7. Nhận xét nào sau đây không đúng?
A. Nồng độ ion H+ trong dung dịch nước mưa bị ô nhiễm là 10-4,5.
B. Nồng độ ion H+ trong dung dịch nước mưa không bị ô nhiễm là 10-5,7.
C. Nồng độ ion H+ trong nước mưa bị ô nhiễm thấp hơn so với trong nước mưa không bị ô nhiễm.
D. Nồng độ ion OH- trong nước mưa bị ô nhiễm thấp hơn so với trong nước mưa không bị ô nhiễm.
Câu 25. Khi mưa liên tục nhiều ngày có thể làm cho độ pH của nước trong ao hồ giảm xuống dưới 6,5. Biện pháp
nào sau đây xử lí nào sau đây là không phù hợp?
A. Tăng cường độ sục khí để tạo điều kiện khuếch tán CO2 ra ngoài không khí.
B. Rắc vôi bột (CaO) vào trong ao hồ để điều chỉnh độ pH.
C. Cho muối natri bicarbonate (NaHCO3) vào trong ao hồ để điều chỉnh độ pH.
D. Cho phèn chua (KAl(SO4)2.12H2O) vào trong ao hồ để điều chỉnh độ pH.
Câu 26. Nồng độ mol của cation trong dung dịch Al2(SO4)3 0,05 M là A. 0,25 M. B. 0,15 M. C. 0,1 M. D. 0,05 M.
Câu 27. Một dung dịch có chứa các ion: Mg2+ (0,05 mol), K+ (0,15 mol), NO - 2-
3 (0,1 mol), và SO4 (x mol). Giá trị của x là A. 0,05. B. 0,075. C. 0,1. D. 0,15.
Câu 28. Theo thuyết điện li, khi hòa tan muối Mohr ((NH4)2SO4.FeSO4.6H2O) vào nước, tỉ lệ nồng độ mol giữa ion Fe2+ và SO 2– 4 tương ứng là A. 1 : 2. B. 2 : 3. C. 1 : 1. D. 1 : 3.
Câu 29. Để trung hòa 30 mL dung dịch H2SO4 0,25 M cần 20 mL dung dịch NaOH nồng độ x mol/L. Giá trị của x là A. 0,100. B. 0,750. C. 0,500. D. 0,375. 6
Câu 30. Thêm nước vào 10 mL dung dịch NaOH 1,0 mol/L, thu được 1000 mL dung dịch A. Dung dịch A có pH
thay đổi như thế nào so với dung dịch ban đầu?
A. pH giảm đi 2 đơn vị.
B. pH giảm đi 1 đơn vị.
C. pH tăng 2 đơn vị.
D. pH tăng gấp đôi.
CHỦ ĐỀ 3. Đơn chất nitrogen
Câu 1. Phân tử nitrogen có cấu tạo là A. N = N. B. N N. C. N – N. D. N N.
Câu 2. Vị trí (chu kì, nhóm) của nguyên tố nitrogen trong bảng tuần hoàn là
A. Chu kì 2, nhóm VA.
B. chu kì 3, nhóm VA.
C. chu kì 2, nhóm VIA.
D. chu kì 3, nhóm IVA.
Câu 3. Nhận định nào sau đây về phân tử nitrogen là đúng?
A. Có ba liên kết đơn bền vững.
B. Chứa nguyên tử nitrogen có số oxi hóa là -3.
C. Có liên kết cộng hóa trị có cực.
D. Thể hiện cả tính oxi hóa và tính khử.
Câu 4. Trong nghiên cứu, khí nitrogen thường được dùng để tạo bầu khí quyển trơ dựa trên cơ sở nào?
A. Nitrogen có tính oxi hóa mạnh.
B. Nitrogen rất bền với nhiệt.
C. Nitrogen khó hóa lỏng.
D. Nitrogen không có cực.
Câu 5. Công thức hóa học của diêm tiêu Chile là A. Ca(NO3)2. B. NH4NO3. C. NH4Cl. D. NaNO3.
Câu 6. Trong những nhận xét dưới đây, nhận xét nào là đúng?
A. Nitrogen không duy trì sự cháy, sự hô hấp và là một khí độc.
B. Ở điều kiện thường, nitrogen trơ về mặt hóa học do phân tử có một liên kết ba bền vững.
C. Trong các phản ứng hóa học, nitrogen chỉ thể hiện tính khử.
D. Số oxi hóa của nitrogen trong các ion và hợp chất NH + -
4 , NO3 , N2O lần lượt là -3,+5,+4.
Câu 7. Xét phản ứng hóa học thường xảy ra cùng với quá trình đốt cháy nhiên liệu trong buồn đốt động cơ: N g O g 2NO g , H 180, 6 kJ 2 2 r
Nhận xét nào sau đây về phản ứng là không đúng?
A. Nitrogen là chất oxi hóa. B. Phản ứng thuận thu nhiệt.
C. Hiệu suất phản ứng rất thấp.
D. Nitrogen là chất khử.
CHỦ ĐỀ 4. Ammonia và một số hợp chất ammonium
Câu 1. Công thức phân tử của ammonia là A. HNO3. B. N2. C. NH3. D. N2H4.
Câu 2. Trong các phát biểu sau, phát biểu nào không đúng?
A. Ở điều kiện thường, NH3 là chất khí không màu.
B. Khí NH3 nặng hơn không khí.
C. Khí NH3 dễ hoá lỏng, tan nhiều trong nước.
D. Khí NH3 có mùi khai, xốc.
Câu 3. Khi tác dụng với nước và hydrochloric acid, ammonia đóng vai trò là A. acid. B. base.
C. chất oxi hóa. D. chất khử.
Câu 4. Tã lót trẻ em sau khi giặt vẫn giữ lại một lượng nhỏ ammonia. Để khử sạch ammonia nên dùng chất gì sau
đây cho vào nước xả cuối cùng để giặt? A. Phèn chua. B. Giấm ăn. C. Muối ăn. D. Gừng tươi.
Câu 5. Ammonia đóng vai trò chất khử khi tác dụng với chất nào sau đây? A. H2O. B. HCl. C. H3PO4. D. O2 (Pt, to).
Câu 6. Cho dung dịch NH3 vào dung dịch chất nào sau đây thu được kết tủa trắng? A. HCl. B. H2SO4. C. H3PO4. D. AlCl3.
Câu 7. Trong quá trình tổng hợp ammonia theo quy trình Haber (Haber – Bosch), sau khi đã hóa lỏng ammonia, hydrogen và nitrogen sẽ:
A. qua ống dẫn khí thải và được loại bỏ.
B. đưa trở lại buồng phản ứng để tái sử dụng.
C. tiếp tục qua lò phản ứng số 2 để tăng hiệu suất tổng hợp.
D. hydrogen được tái sử dụng, còn nitrogen loại bỏ dựa vào tỉ trọng. 7
Câu 8. Xét phản ứng tổng hợp ammonia theo phương trình hoá học: o N 2(g) + 3H2(g) ⇌2NH3(g) H = - 92 kJ r 298
Cho các yếu tố sau: (a) tăng nhiệt độ, (b) tách ammonia ra khỏi hỗn hợp phản ứng, (c) giảm thể tích của hệ phản
ứng, (d) thêm H2. Có bao nhiêu yếu tố làm tăng hiệu suất tổng hợp NH3? A. 1. B. 2. C. 3. D. 4.
Câu 9. Một nhà máy phân bón tổng hợp ammonia với công suất 34 tấn/giờ. Trong một giờ, khối lượng nitrogen và
hydrogen đã phản ứng lần lượt là
A. 28 tấn và 2 tấn.
B. 14 tấn và 2 tấn.
C. 28 tấn và 6 tấn.
D. 28 tấn và 4 tấn.
Câu 10. Ammonia (NH ) được điều chế bằng phản ứng: N (g) 3H (g)
2NH (g) . Ở t oC, nồng độ các 3 2 2 3
chất ở trạng thái cân bằng như sau: N = 0,9 M, H = 0,28 M, NH = 1,24 M . 2 2 3
Hằng số cân bằng K của phản ứng trên tại t oC là C A. 77,82. B. 31,35. C. 49,22. D. 18,90.
Câu 11. Phát biểu nào sau đây đúng?
A. Muối ammonium tan kém trong nước.
B. Muối ammonium là chất điện li yếu.
C. Muối ammonium kém bền với nhiệt.
D. Dung dịch muối ammonium có tính chất base.
Câu 12. Khi so sánh phân tử ammonia với ion ammonium, nhận định nào sau đây là đúng?
A. Đều chứa liên kết ion.
B. Đều có tính acid yếu trong nước.
C. Đều có tính base yếu trong nước.
D. Đều chứa nguyên tử N có số oxi hoá là -3.
Câu 13. Nhiệt phân hoàn toàn muối nào sau đây thu được sản phẩm chỉ gồm khí và hơi? A. NaCl. B. CaCO3. C. KClO3. D. NH4HCO3.
Câu 14. Có thể nhận biết muối ammonium bằng cách cho muối tác dụng với dung dịch kiềm thấy thoát ra một chất khí. Chất khí đó là A. NH3. B. H2. C. NO2. D. NO.
Câu 15. Cho dung dịch NaOH vào 100 ml dung dịch NH4NO3 1M, đun nóng thu được V lít khí ở đkc. Giá trị của V là A. 2,4790. B. 4,9580. C. 7,4370. D. 1,2395.
CHỦ ĐỀ 5. Một số hợp chất với oxygen của nitrogen
Câu 1. Oxide của nitrogen được tạo thành khi nguyên tố nitrogen trong nhiên liệu hoặc sinh khối kết hợp với
oxygen dư thừa trong không khí được gọi là
A. NOx tức thời. B. NOx nhiệt.
C. NOx nhiên liệu. D. NOx tự nhiên.
Câu 2. Oxide của nitrogen được tạo thành ở nhiệt độ cao, khi nitrogen có trong không khí bị oxi hóa được gọi là
A. NOx tức thời. B. NOx nhiệt.
C. NOx nhiên liệu. D. NOx tự nhiên.
Câu 3. Đặc điểm nào sau đây là đúng để giải thích tính kém bền nhiệt của HNO3?
A. Liên kết O – H phân cực mạnh về phía O.
B. Liên kết N O là liên kết cho nhận kém bền.
C. Nguyên tử N có số oxi hóa +5 là số oxi hóa cao nhất của N.
D. HNO3 có khả năng nhường proton cho nước.
Câu 4. Nitric acid dễ bị phân hủy bởi ánh sáng hoặc nhiệt độ tạo thành các sản phẩm là A. NO2, H2O.
B. NO2, O2, H2O. C. N2, O2, H2O. D. N2. H2O.
Câu 5. Kim loại nào sau đây không tác dụng với HNO3 đặc, nóng? A. Fe. B. Cu. C. Ag. D. Pt.
Câu 6. Phú dưỡng là hiện tượng xảy ra do sự gia tăng hàm lượng của hai nguyên tố nào trong nước? A. Fe, Mn. B. N, P. C. Ca, Mg. D. Cl, F.
Câu 7. Hoạt động nào sau đây góp phần gây nên hiện tượng phú dưỡng?
A. Sự quang hợp của cây xanh.
B. Nước thải sinh hoạt thải trực tiếp vào nguồn nước chưa qua xử lí.
C. Ao hồ thả quá nhiều tôm, cá.
D. Khử trùng ao hồ sau khi tát cạn bằng vôi sống (CaO).
Câu 8. Trong công nghiệp, quá trình sản xuất Ca(NO3)2 cùng làm phân bón được thực hiện bằng phản ứng giữa
dung dịch HNO3 với hợp chất phổ biến, giá rẻ nào sau đây? 8 A. CaO. B. Ca(OH)2. C. CaCO3. D. CaSO4.
CHỦ ĐỀ 6. Sulfur và sulfur dioxide
Câu 1. Nguyên tố sulfur có số hiệu nguyên tử là 16. Vị trí của sulfur trong bảng tuần hoàn các nguyên tố hóa học là
A. chu kì 3, nhóm VIA.
B. chu kì 5, nhóm VIA.
C. chu kì 3, nhóm IVA.
D. chu kì 5, nhóm IVA.
Câu 2. Tính chất nào sau đây không phải tính chất vật lí của sulfur?
A. Màu vàng ở điều kiện thường.
B. Thể rắn ở điều kiện thường.
C. Không tan trong benzene. D. Không tan trong nước.
Câu 3. Ở điều kiện thường, sulfur tồn tại ở dạng tinh thể, được tạo nên từ các phân tử sulfur. Số nguyên tử trong
mỗi phân tử sulfur là A. 2. B. 4. C. 6. D. 8.
Câu 4. Kim loại nào sau đây tác dụng với sulfur ở nhiệt độ thường? A. Al. B. Fe. C. Hg. D. Cu.
Câu 5. Cho các phản ứng sau: o (a) S + O t 2 SO2 (b) Hg + S HgS o (c) S + 6HNO t 3 H2SO4 + 6NO2 + 2H2O (d) Fe + S FeS
Có bao nhiêu phản ứng trong đó sulfur đóng vai trò là chất khử? A. 1. B. 2. C. 3. D. 4.
Câu 6. Sulfur được dân gian sử dụng để pha chế vào thuốc trị các bệnh ngoài da. Tên gọi dân gian của sulfur là A. diêm sinh. B. đá vôi. C. phèn chua. D. giấm ăn.
Câu 7. Trong công nghiệp, phần lớn sulfur đơn chất sau khi khai thác ở các mỏ được dùng làm nguyên liệu để
A. lưu hóa cao su tự nhiên.
B. sản xuất sulfuric acid.
C. điều chế thuốc bảo vệ thực vật.
D. bào chế thuốc đông y.
Câu 8. Sulfur dioxide và các oxide của nitrogen trong khí quyển hòa tan trong nước tạo thành mưa acid. Khẳng
định nào sau đây là đúng?
A. Nước mưa có pH > 5,6 được xem là mưa acid.
B. Thành phần chính của mưa acid là H2SO3 và HNO2.
C. Công thức hóa học của NOx trong khí thải ô tô luôn là NO2.
D. Thu hồi sulfur từ các khí thải như H2S, SO2….có thể làm giảm sự hình thành mưa acid.
Câu 9. Chất khí (X) tan trong nước tạo ra dung dịch làm quỳ tím hoá đỏ và khí (X) có thể được dùng làm chất tẩy màu. Khi (X) là A. NH3. B. CO2. C. SO2. D. O3.
Câu 10. Cho các ứng dụng sau:
(1) sản xuất sulfuric acid;
(2) tẩy trắng bột giấy;
(3) diệt nấm mốc, thuốc đông y;
(4) diệt trùng nước sinh hoạt.
Số ứng dụng của khí sulfur dioxide trong đời sống, sản suất là A. 1. B. 2. C. 3. D. 4.
Câu 11. Một nhà máy luyện kim, ở giai đoạn đầu của quá trình sản xuất Zn từ quặng blend thu được sản phẩm phụ
là SO2 theo sơ đồ phản ứng: ZnS + O2 ZnO + SO2
Đốt cháy 1 tấn quặng blend (chứa 77,6% khối lượng ZnS) bằng không khí, thu được tối đa V m3 khí SO2 (đkc). Giá trị của V là A. 99,2. B. 198,3. C. 297,5. D. 396,6. Đáp án: B. ZnS + O2 ZnO + SO2 776 3 m ZnS = 1000.77,6% n n 8 kmol V 8.24, 79 198,32m ZnS SO2 97 SO2
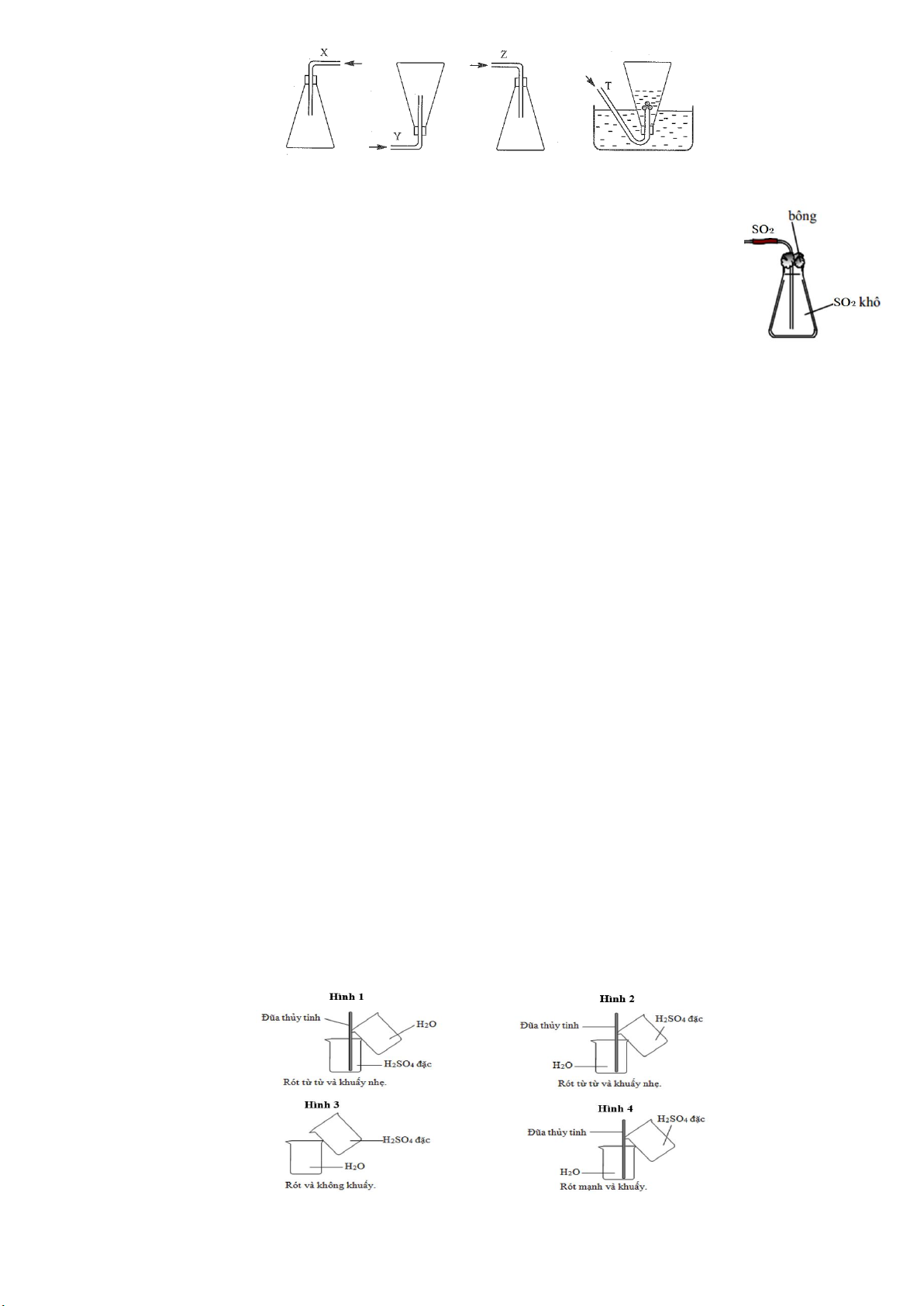
Câu 12. Các chất khí được thu vào bình theo đúng nguyên tắc bằng cách đẩy không khí (X, Y, Z) và đẩy nước (T) như sau: 9
Nhận xét nào sau đây không đúng?
A. X là sulfur dioxide. B. Y là ammonia.
C. Z là hydrogen. D. T là nitrogen.
Câu 9. Một bạn học sinh thu khí SO2 vào bình tam giác và đậy miệng bình bằng bông tẩm
dung dịch E (để giữ không cho khí SO2 bay ra) theo sơ đồ bên. Theo em, để hiệu quả nhất,
bạn học sinh cần sử dụng dung dịch E là dung dịch nào sau đây? A. Giấm ăn. B. Muối ăn.
C. Nước vôi. D. Nước máy.
Câu 10. Phản ứng hóa học nào sau đây đóng vai trò chính chuyển hóa sulfur dioxide
trong không khí ô nhiễm gây mưa acid? A. SO2 + NaOH NaHSO3. B. SO2 + 2H2S 3S + 2H2O.
C. SO2 + H2O + Br2 2HBr + H2SO4. D. SO2 + NO2 SO3 + NO.
CHỦ ĐỀ 7. Sulfuric acid và muối sulfate
Câu 1. Nhỏ dung dịch H2SO4 98% vào cốc đựng đường saccarose khiến đường hóa đen gọi là hiện tượng gì?
A. Hiện tượng bốc hơi.
B. Hiện tượng than hóa.
C. Hiện tượng đông tụ.
D. Hiện tượng vón cục.
Câu 2. Chất nào sau đây không bay hơi ở điều kiện thường do nhiệt độ sôi rất cao (337 oC)? A. H2O. B. HNO . C. NH H SO . 3 3. D. 2 4
Câu 3. Cho vài giọt dung dịch BaCl2 vào dung dịch nào sau đây sẽ tạo kết tủa trắng? A. NaCl. B. Na2SO4. C. NaNO3. D. NaOH.
Câu 4. Thuốc thử duy nhất để nhận biết 4 dung dịch đựng trong 4 lọ mất nhãn là KOH, NH4Cl K2SO4, (NH4)2SO4 là
A. dung dịch AgNO3
B. dung dịch BaCl2.
C. dung dịch NaOH.
D. dung dịch Ba(OH)2.
Câu 5. Thạch cao sống là một dạng tồn tại phổ biến của sulfur trong tự nhiên, được sử dụng làm nguyên liệu để sản
xuất xi măng, phấn viết bảng, … Công thức của thạch cao sống là A. BaSO4. B. CaSO4.2H2O. C. MgSO4. D. CuSO4.5H2O.
Câu 6. Cho các phát biểu sau:
(a) Sulfuric acid tan tốt trong nước, quá trình hòa tan tỏa nhiệt mạnh.
(b) Dung dịch sulfuric acid đặc hòa tan được tất cả các kim loại.
(c) Dung dịch sulfuric acid đặc có tính háo nước và tính oxi hóa mạnh.
(d) Nhiều muối sulfate tan tốt trong nước nhưng một số muối như CaSO4, BaSO4 rất ít tan trong nước.
(e) Khi bị bỏng sulfuric acid đặc, điều đầu tiên cần làm là xả nhanh chỗ bỏng với nước lạnh.
Số phát biểu đúng là A. 5. B. 2. C. 3. D. 4.
Câu 7. Các hình ảnh dưới đây mô tả cách pha loãng H2SO4 đặc:
Hình ảnh mô tả đúng cách pha loãng acid đảm bảo an toàn là A. Hình 1. B. Hình 2. C. Hình 3. D. Hình 4. 10
Câu 8. Một trong những nguồn nguyên liệu sản xuất sulfuric acid hiện nay là quặng pyrite. Thành phần chính có trong quặng pyrite là A. FeS2. B. CuFeS2. C. CaSO4.H2O D. HgS.
Câu 9. Muối X không tan trong nước và các dung môi hữu cơ. Trong y học, X thường được dùng làm chất cản
quang xét nghiệm X-quang đường tiêu hóa. Công thức của X là A. BaSO4. B. Na2SO4. C. K2SO4. D. MgSO4.
Câu 10. Cho các chất: Cu, CuO, NaCl, Mg, KOH, C, Na2CO3. Số chất vừa tác dụng với dung dịch H2SO4 loãng,
vừa tác dụng với dung dịch H2SO4 đặc, nóng là bao nhiêu ? A. 5. B. 6. C. 3. D. 4.
CHỦ ĐỀ 8. Hợp chất hữu cơ và hoá học hữu cơ
Câu 1. Hợp chất hữu cơ là các hợp chất của ……… (trừ các oxide của carbon, muối carbonate, cyanide, carbide,
……). Từ thích hợp điền vào chỗ trống trong định nghĩa trên là: A. carbon. B. hydrogen. C. oxygen. D. nitrogen.
Câu 2. Hóa học hữu cơ là ngành hóa học chuyên nghiên cứu về các …………………. Cụm từ thích hợp điền vào
chỗ trống trong định nghĩa trên là
A. hợp chất hữu cơ.
B. hợp chất vô cơ.
C. hợp chất thiên nhiên.
D. hợp chất phức.
Câu 3. Trong các hợp chất sau, chất nào không phải là hợp chất hữu cơ? A. (C6H10O5)n. B. C2H2. C. NH3. D. C12H22O11.
Câu 4. Trong các hợp chất sau, chất nào là hợp chất hữu cơ? A. CO2. B. C6H6. C. Na2CO3. D. Al4C3.
Câu 5. Trong các hợp chất sau, chất nào là dẫn xuất của hydrocarbon? A. CH4. B. CH3OH. C. C2H4. D. C3H8.
Câu 6. Liên kết hóa học trong phân tử hợp chất hữu cơ chủ yếu là
A. liên kết ion.
B. liên kết cộng hóa trị.
C. liên kết cho - nhận.
D. liên kết hydrogen.
Câu 7. Cho các đặc điểm chung của các phân tử hợp chất hữu cơ:
(1) Thành phần nguyên tố chủ yếu là C và H.
(2) Có thể chứa nguyên tố khác như Cl, O, N,...
(3) Liên kết hóa học chủ yếu là liên kết cộng hoá trị.
(4) Dễ bay hơi và khó cháy.
(5) Tan nhiều trong nước và dung môi hữu cơ không phân cực. Nhóm các ý đúng là A. (1), (3). B. (1), (2), (4). C. (2), (3), (5). D. (2), (3).
Câu 8. Phản ứng hóa học của các hợp chất hữu cơ có đặc điểm là
A. thường xảy ra rất nhanh và cho một sản phẩm duy nhất.
B. thường xảy ra chậm, không hoàn toàn, không theo một hướng nhất định.
C. thường xảy ra rất nhanh, không hoàn toàn, không theo một hướng nhất định.
D. thường xảy ra rất chậm, nhưng hoàn toàn, không theo một hướng xác định.
Câu 9. Trong các chất sau đây, chất nào dễ cháy nhất? A. CO2. B. C2H5OH. C. Na2CO3. D. N2.
Câu 10. Cho các hợp chất sau: CH4, NH3, C2H2, CCl4, C2H4, C6H6. Số hợp chất thuộc loại hydrocarbon là A. 1. B. 2. C. 3. D. 4.
Câu 11. Trường hợp nào dưới đây khoanh đúng nhóm chức carboxylic acid của ethanoic acid? A. B. C. D. 11
Câu 12. Phổ hồng ngoại của hợp chất hữu cơ nào sau đây không có hấp thụ ở vùng 1750 – 1600 cm-1? A. Alcohol. B. Ketone. C. Ester. D. Aldehyde.
Câu 13. Phổ hồng ngoại là phương pháp vật lí rất quan trọng và phổ biến để nghiên cứu về
A. thành phần nguyên tố chất hữu cơ.
B. thành phần phân tử hợp chất hữu cơ.
C. cấu tạo hợp chất hữu cơ. D. cấu trúc không gian hợp chất hữu cơ.
Câu 14. Phổ IR của chất X được cho như dưới đây:
X có thể là chất nào sau đây? A. CH3CH2-COOH. B. CH3CH2CH2-CHO. C. CH3CH2-NH-CH2CH3. D. CH3-CO-CH2CH3.
Câu 15. Cho các phát biểu sau:
(a) Hợp chất hữu cơ là hợp chất của carbon (trừ CO, CO2, các muối carbonate, cyanide, carbide, …)
(b) Phổ hồng ngoại cho phép xác định cả loại nhóm chức và số lượng nhóm chức đó có trong phân tử hợp chất hữu cơ.
(c) Phổ khối lượng (MS) cho biết tỉ lệ phần trăm khối lượng của các nguyên tố.
(d) Một hydrocarbon và một hợp chất ion có khối lượng phân tử gần bằng nhau thì hydrocarbon tan trong nước
ít hơn và có nhiệt độ sôi thấp hơn so với hợp chất ion.
Số phát biểu đúng là A. 2. B. 4. C. 1. D. 3.
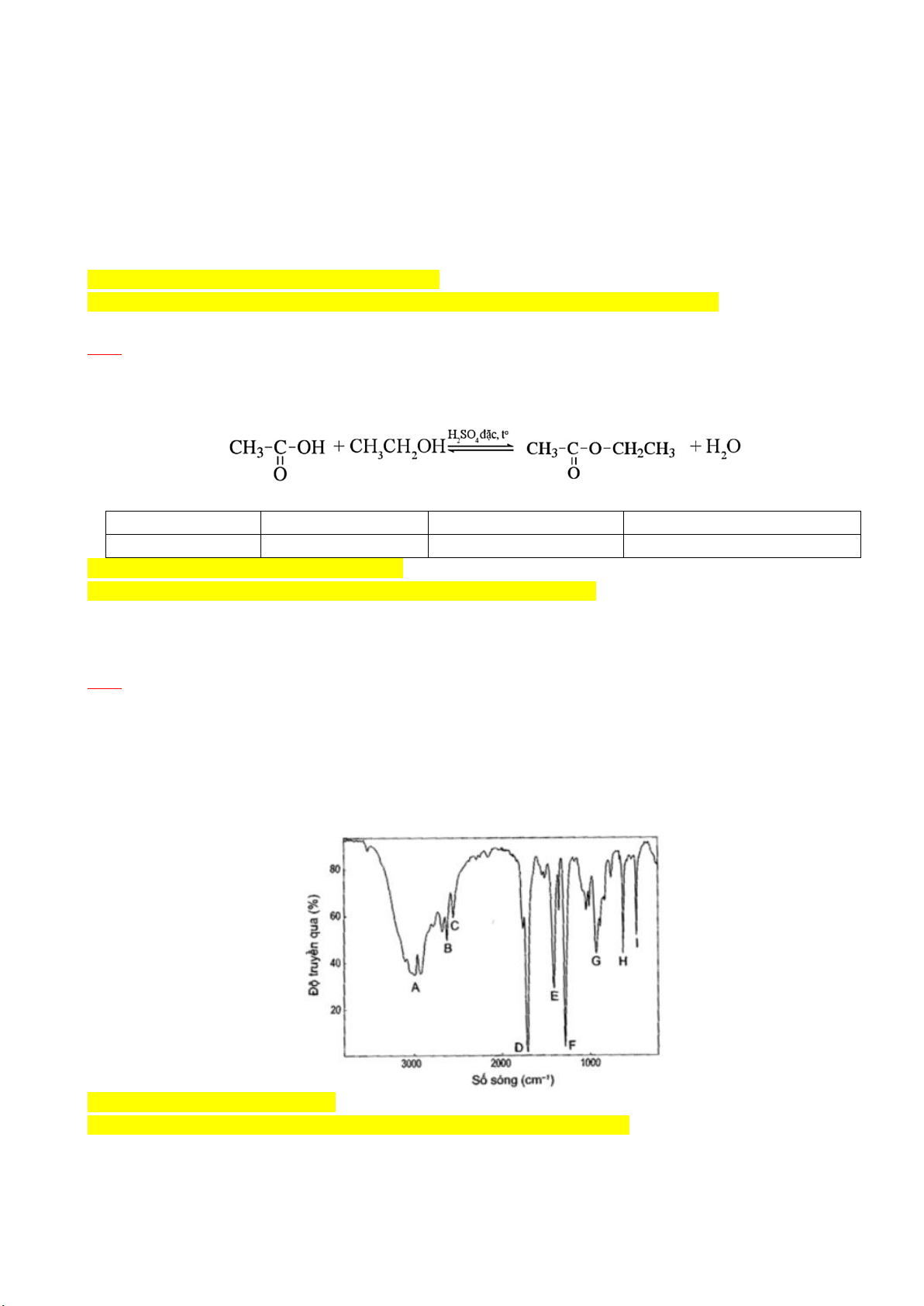
Câu 16. Glycerol là hợp chất dùng làm dược phẩm để giảm cân, cải thiện hoạt động tập thể dục, giúp cơ thể bù
lượng nước bị mất trong suốt thời gian bị tiêu chảy và nôn mửa cũng như làm giảm áp lực bên trong mắt ở những
người bị tăng nhãn áp. Dựa vào phổ IR dưới đây:
Cho biết peak nào có thể xác định được nhóm chức -OH có trong hợp chất (X)? A. Peak D. B. Peak E. C. Peak A. D. Peak B.
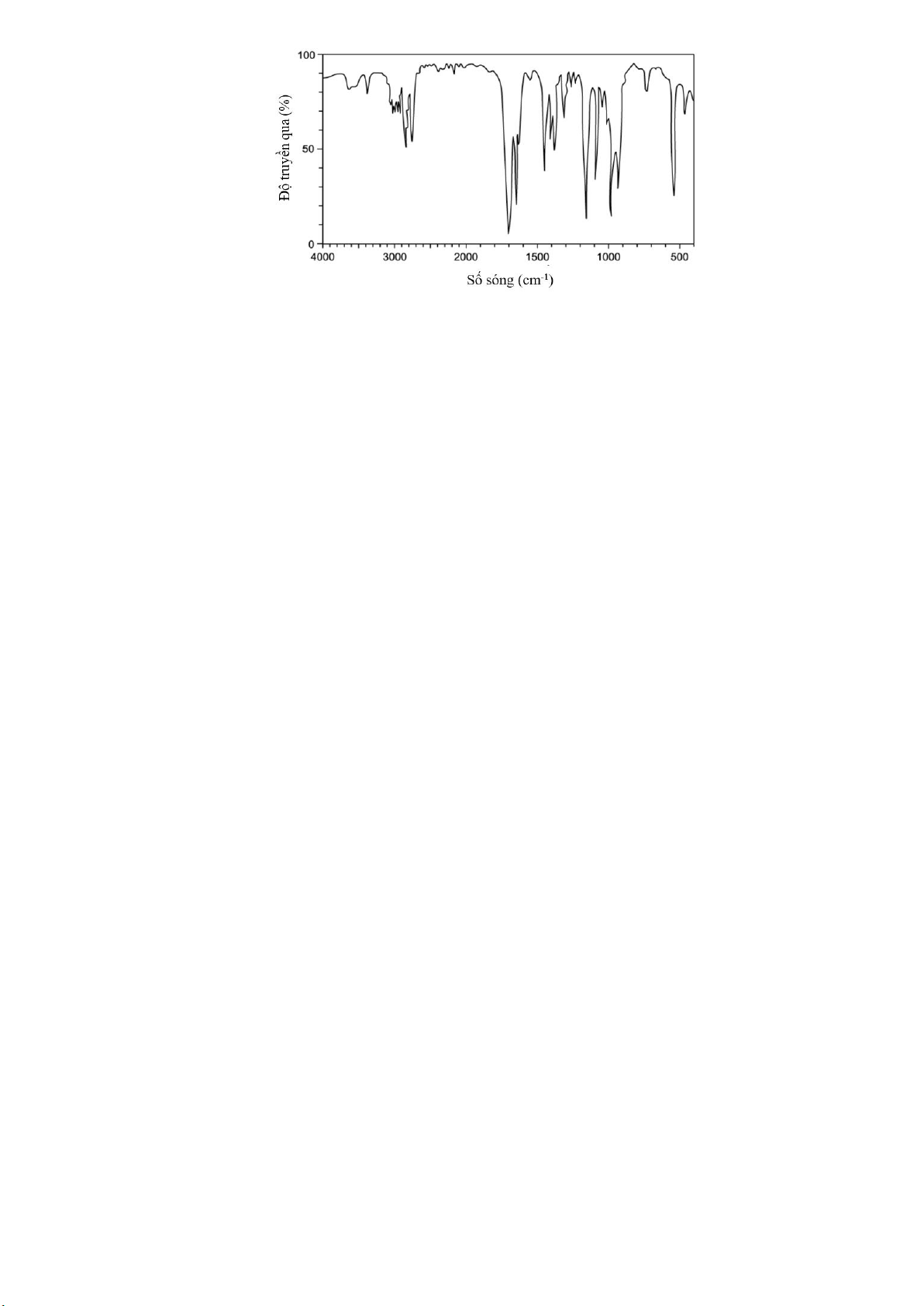
Câu 17: Cho phổ hồng ngoại của chất X như hình dưới đây: 12
Phân tử chất X có chứa nhóm chức nào sau đây? A. Aldehyde (-CHO).
B. Carboxylic acid (-COOH). C. Alcohol (-OH).
D. Amine (-NH-).
Câu 18. Vì sao có thể dựa vào nhóm chức để phân loại các hợp chất hữu cơ?
A. Vì biết được nhóm chức thì biết được thành phần các nguyên tố hóa học có trong phân tử hợp chất hữu cơ.
B. Vì nhóm chức không bị biến đổi khi phân tử hữu cơ tham gia phản ứng.
C. Vì nhóm chức tham gia vào các phản ứng trong cơ thể sống.
D. Vì nhóm chức gây ra các phản ứng hoá học đặc trưng cho phân tử hữu cơ.
CHỦ ĐỀ 9. Phương pháp tách và tinh chế hợp chất hữu cơ
Câu 1. Phương pháp chiết là sự tách chất dựa vào sự khác nhau
A. về kích thước phân tử.
B. ở mức độ nặng nhẹ về khối lượng.
C. về khả năng bay hơi.
D. về khả năng tan trong các dung môi khác nhau.
Câu 2. Để tách các chất lỏng ra khỏi hỗn hợp các chất có nhiệt độ sôi khác nhau, nhằm thu được chất lỏng tinh
khiết hơn là phương pháp nào sau đây?
A. Phương pháp chưng cất. B. Phương pháp chiết.
C. Phương pháp kết tinh. D. Sắc kí cột.
Câu 3. Chưng cất là phương pháp tách và tinh chế chất lỏng dựa trên sự khác nhau về nhiệt độ sôi của các chất
lỏng trong hỗn hợp ở áp suất nhất định. Quá trình chưng cất gồm 2 giai đoạn nào sau đây?
A. Hóa hơi và ngưng tụ.
B. Đông đặc và ngưng tụ.
C. Đông đặc và ngưng tụ.
D. Ngưng tụ và đông đặc.
Câu 4. Phương pháp dùng để tách các chất hữu cơ có hàm lượng nhỏ và khó tách ra khỏi nhau là phương pháp nào sau đây?
A. Phương pháp chưng cất. B. Phương pháp chiết
C. Phương pháp kết tinh.
D. Phương pháp sắc kí cột.
Câu 5. Trong phương pháp sắc kí, hỗn hợp lỏng hoặc khí của các chất cần tách là pha động. Pha động tiếp xúc liên
tực với pha tĩnh là một chất rắn có diện tích bề mặt rất lớn, có khả năng hấp phụ …(1)… với các chất trong hỗn
hợp cần tách, khiến cho các chất trong hỗn hợp di chuyển với tốc độ …(2)… và tách ra khỏi nhau. Cụm từ thích
hợp điền vào chỗ trống (1) và (2) lần lượt là
A. (1) giống nhau và (2) giống nhau.
B. (1) khác nhau và (2) khác nhau.
C. (1) khác nhau và (2) giống nhau.
D. (1) giống nhau và (2) khác nhau.
Câu 6. Phương pháp sắc kí cột có đặc điểm:
(a) Pha tĩnh là bột silicagel hoặc bột aluminium oxygende,…
(b) Pha động là dung môi thích hợp được đổ ở phía dưới pha tĩnh.
(c) Chất có độ chuyển dịch lớn hơn sẽ cùng với dung môi ra khỏi cột trước.
(d) Chất ra khỏi cột trước là chất có khả năng bị hấp phụ trên pha tĩnh tốt hơn.
(e) Pha động cho vào sắc kí ở trạng thái lỏng.
Số đặc điểm đúng là A. 1. B. 2. C. 3. D. 4. 13
Câu 7. Để phân tích thổ nhưỡng hoặc phân tích dư lượng thuốc bảo vệ thực vật trong nông sản người ta dùng
phương pháp nào sau đây?
A. Chiết lỏng – lỏng.
B. Chiết lỏng – rắn.
C. Phương pháp kết tinh. D. Sắc kí cột.
Câu 8. Ngâm củ nghệ với ethanol nóng, sau đó lọc bỏ bã, lấy dung dịch đem cô để làm bay hơi bớt dung môi. Phần
dung dịch còn lại sau khi cô được làm lạnh, để yên một thời gian rồi lọc lấy kết tủa curcumin màu vàng. Từ mô tả ở
trên, hãy cho biết, người ta đã sử dụng các kĩ thuật tinh chế nào để lấy được curcumin từ củ nghệ?
A. Chiết, chưng cất và kết tinh.
B. Chiết và kết tinh.
C. Chưng cất và kết tinh.
D. Chưng cất, kết tinh và sắc kí.
Câu 9. Cây neem (cây thường xanh Ấn Độ) hay còn gọi là cây nim, sầu đâu (tên khoa học Azadirachta indica)
được người Ấn độ dùng hơn 4000 năm nay để làm đẹp và chữa bệnh. Các chiết xuất từ là neem có thể ức chế sự
sao chép của virus Dengue, kháng virus nên có tác dụng điều trị bệnh sốt xuất huyết hiệu quả. Người ta hái một ít
lá neem tươi, rửa sạch, cho vào nồi đun kĩ, lọc lấy nước để sử dụng. Hãy cho biết cách làm trên thuộc loại phương
pháp tách và tinh chế nào?
A. Phương pháp chưng cất. B. Phương pháp chiết
C. Phương pháp kết tinh. D. Sắc kí cột.
Câu 10. Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36oC), heptane (sôi ở 98oC), octane (sôi
ở 126oC) và nonane (sôi ở 151oC). Có thể tách riêng các chất đó bằng cách nào sau đây? A. Chiết. B. Kết tinh. C. Bay hơi. D. Chưng cất.
CHỦ ĐỀ 10. Công thức phân tử hợp chất hữu cơ
Câu 1. Công thức phân tử cho biết thông tin nào sau đây về phân tử hợp chất hữu cơ?
A. Thành phần nguyên tố và số lượng nguyên tử của mỗi nguyên tố.
B. Thành phần nguyên tố và tỉ lệ số lượng nguyên tử của mỗi nguyên tố.
C. Số lượng nguyên tử mỗi nguyên tố và trật tự liên kết giữa các nguyên tử.
D. Tỉ lệ số lượng nguyên tử của mỗi nguyên tố và trật tự liên kết giữa các nguyên tử.
Câu 2. Glucose là hợp chất hữu cơ có nhiều trong các loại quả chín, đặc biệt là quả nho. Công thức phân tử của
glucose là C6H12O6. Công thức đơn giản nhất của glucose là A. C1,5H3O1,5. B. CH2O. C. C3H4O3. D. CHO2.
Câu 3. Để xác định phân tử khối của hợp chất hữu cơ, người ta sử dụng phổ khối lượng MS, trong đó phân tử khối
của chất là giá trị m/z của
A. peak [M+] lớn nhất.
B. peak [M+] nhỏ nhất.
C. peak xuất hiện nhiều nhất. D. nhóm peak xuất hiện nhiều nhất.
Câu 4. Sau khi biết công thức thực nghiệm, có thể xác định công thức phân tử của hợp chất hữu cơ dựa trên đặc điểm nào sau đây?
A. Phân tử khối của chất.
B. Thành phần phần trăm về khối lượng các nguyên tố có trong phân tử chất.
C. Khi lượng các sản phẩm thu được khi đốt cháy hoàn toàn một lượng chất xác định.
D. Các hấp thụ đặc trưng trên phổ IR của chất.
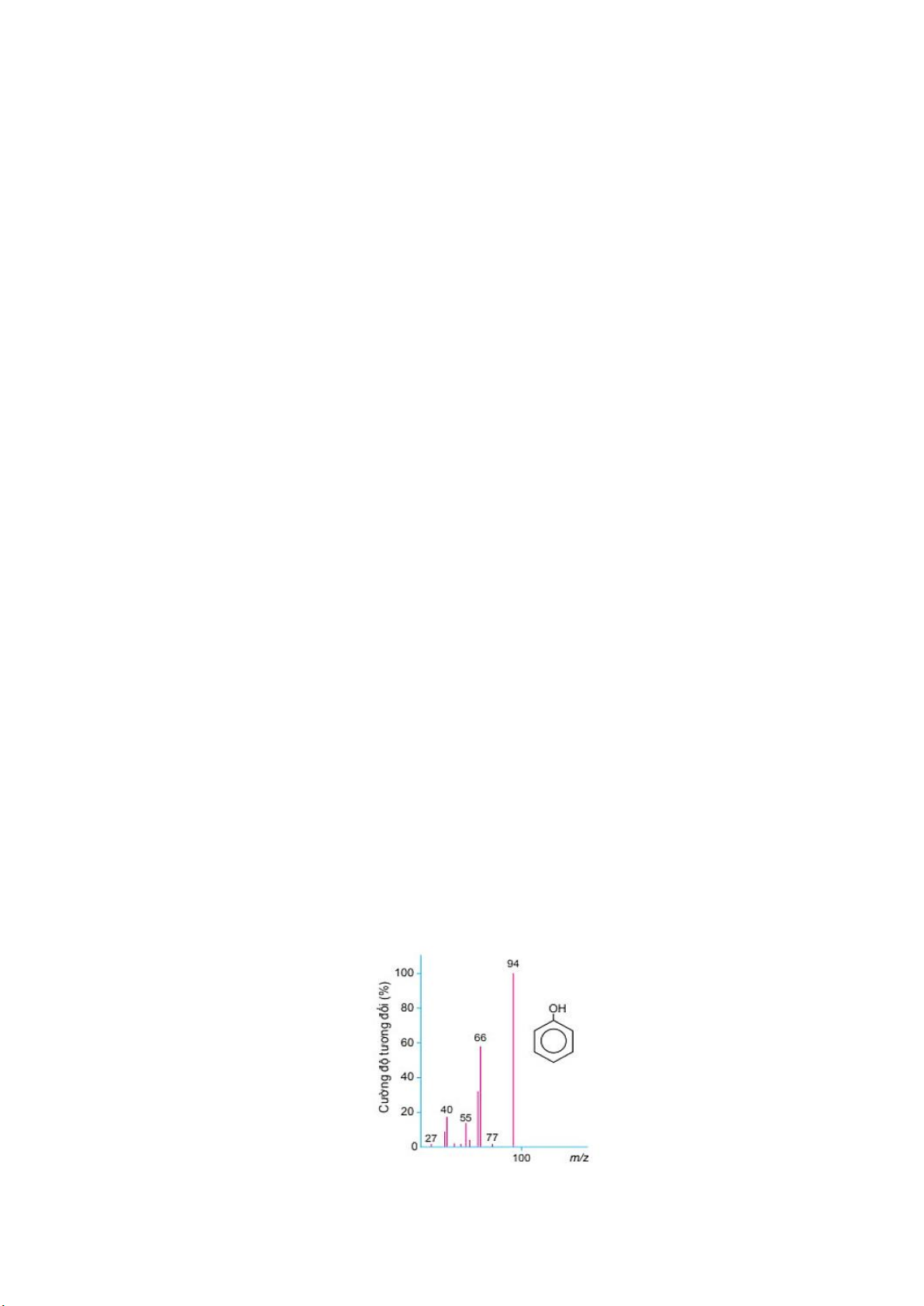
Câu 5. Cho phổ khối lượng của phenol như hình vẽ:
Biết phân tử khối tương ứng với peak có cường độ tương đối lớn nhất hiển thị trên phổ khối lượng. Phân tử khối của phenol là A. 66. B. 77. C. 66. D. 94. 14
Câu 6. Phổ MS của chất Y có thấy chất Y có phân tử khối bằng 60. Cthức phân tử nào dưới đây không phù hợp với Y? A. C3H8O. B. C2H4O2. C. C3H7F. D. C2H8N2.
Câu 7. Hợp chất X có chứa hai hoặc ba nguyên tố C, H, O. Peak ion phân tử trên phổ MS của nó có m/z = 30. X có
thể là chất nào sau đây? A. CH3OH hoặc C2H6. B. CH3CHO hoặc C2H4. C. C2H6 hoặc C2H5OH. D. HCHO hoặc C2H6.
Câu 8. Hợp chất hữu cơ X có 82,76% khối lượng là carbon, còn lại là hydrogen. Công thức thực nghiệm của X là A. CH5. B. C5H. C. C2H5. D. C5H2.
Câu 9. Acetic acid có công thức phân tử là C2H4O2. Kết luận nào dưới đây là đúng?
A. Acetic acid có công thức thực nghiệm là CH2O và có khối lượng riêng lớn gấp 30 lần so với hydrogen ở cùng
điều kiện (nhiệt độ, áp suất).
B. Acetic acid có cthức phân tử là CH2O và có tỉ khối hơi so với hydrogen ở cùng điều kiện (nhiệt độ, áp suất) là 30.
C. Acetic acid có công thức thực nghiệm là CH2O và có phân tử khối là 60.
D. Acetic acid có công thức thực nghiệm là (CH2O)2 và có phân tử khối là 60.
Câu 10. Cho hai chất hữu cơ: acetylene (C2H2) và benzene (C6H6). Phát biểu nào sau đây đúng?
A. Hai chất đó giống nhau về công thức phân tử.
B. Hai chất đó có cùng công thức đơn giản nhất.
C. Hai chất có giá trị m/z của peak [M+] giống nhau trên phổ MS.
D. Hai chất đó cho tín hiệu về số sóng như nhau trên phổ IR.
CHỦ ĐỀ 11. Cấu tạo hoá học hợp chất hữu cơ
Câu 1. Phát biểu nào sau đây không đúng khi nói về hợp chất hữu cơ?
A. Tính chất của các chất phụ thuộc vào thành phần phân tử và cấu tạo hóa học.
B. Các chất có cùng khối lượng phân tử là đồng phân của nhau.
C. Các chất là đồng phân của nhau thì có cùng công thức phân tử.
D. Trong hợp chất hữu cơ, carbon có hóa trị 4, nó có thể liên kết với nguyên tử nguyên tố khác và liên kết với
nhau để tạo thành mạch carbon gồm: nhánh, không nhánh và vòng.
Câu 2. Để viết được cấu tạo hóa học của một chất cần biết những yếu tố nào sau đây?
(a) Thành phần phân tử của chất.
(b) Hóa trị của các nguyên tố có trong phân tử chất.
(c) Trật tự liên kết của các nguyên tử có trong phân tử chất.
(d) Nhiệt độ sôi của chất. A. a, b, c. B. a, c, d. C. b, c, d. D. a, b, d.
Câu 3. Cấu tạo hoá học là ...(1)… giữa các nguyên tử trong phân tử. Cụm từ thích hợp điền vào (1) là
A. thứ tự liên kết.
B. phản ứng. C. liên kết.
D. tỉ lệ số lượng.
Câu 4. Những hợp chất hữu cơ khác nhau nhưng có cùng công thức phân tử được gọi là các chất
A. đồng phân của nhau.
B. đồng đẳng của nhau.
C. đồng vị của nhau.
D. đồng khối của nhau.
Câu 5. Nhận xét nào sau đây về 2 công thức cấu tạo bên là đúng?
A. Biểu diễn cấu tạo hóa học của 2 chất đồng phân mạch carbon.
B. Biểu diễn cấu tạo hóa học của 2 chất đồng phân vị trí nhóm chức.
C. Biểu diễn cấu tạo hóa học của 2 chất thuộc cùng dãy đồng đẳng.
D. Biểu diễn cấu tạo hóa học của cùng một chất.
Câu 6. Các chất hữu cơ có tính chất hoá học tương tự nhau và thành phần phân tử hơn kém nhau một hay nhiều
nhóm CH2 được gọi là các chất
A. đồng phân của nhau.
B. đồng đẳng của nhau.
C. đồng vị của nhau.
D. đồng khối của nhau. 15
Câu 7. Methanol, ethanol, propan-1-ol thuộc cùng một dãy đồng đẳng. Phát biểu nào sau đây về các hợp chất này là đúng?
A. Các hợp chất này có tính chất vật lí tương tự nhau và có tính chất hoá học biến đổi theo quy luật.
B. Các hợp chất này có tính chất hoá học tương tự nhau và có tính chất vật lí biến đổi theo quy luật.
C. Các hợp chất này có cùng công thức phân tử nhưng có các tính chất vật lí, tính chất hoá học khác nhau.
D. Các hợp chất này có các tính chất vật lí và tính chất hoá học tương tự nhau.
Câu 8. Cho công thức cấu tạo của một số chất hữu cơ như sau: (1) (2) (3) (4)
Chất có mạch carbon phân nhánh là A. (1). B. (2). C. (3). D. (4).
Câu 9. Trong các dãy chất sau đây: (1) C2H6, CH4, C4H10. (2) C2H5OH, CH3CH2CH2OH. (3) HCHO, CH3CHO, C2H5CHO. (4) CH3COOH, HCOOCH3.
Có mấy dãy gồm các chất là đồng đẳng của nhau? A. 1. B. 2. C. 3. D. 4.
Câu 10. Menthol (mùi bạc hà) có công thức là C10H18O, chỉ chứa một liên kết đôi. Phát biểu nào sau đây không đúng?
A. Menthol là dẫn xuất của hydrocarbon.
B. Menthol có cấu tạo mạch hở.
C. Menthol có cấu tạo mạch vòng.
D. Menthol có nhiệt độ sôi thấp hơn muối ăn (NaCl).
Câu 11. Cặp chất nào dưới đây là đồng phân vị trí nhóm chức?
A. CH OCH CH và CH CH CH OH . 3 2 3 3 2 2
B. CH COCH và CH CH CH O . 3 3 3 2
C. CH CCH CH và CH CH CH CH CH CH . 2 3 3 2 2 3
D. CH CH CH OH và CH CH OH CH . 3 3 2 2 3
Câu 12. Methadone là một loại thuốc dùng trong cai nghiện ma túy, nó thực chất cũng là một loại chất gây nghiện
nhưng “nhẹ” hơn các loại ma túy thông thường và dễ kiểm soát hơn. Công thức cấu tạo thu gọn như hình dưới.
Công thức phân tử của methadone là A. C17H27NO. B. C17H22NO. C. C21H29NO. D. C21H27NO.
Câu 13. Cho các cặp chất sau đây:
Số cặp chất là đồng đẳng của nhau là A. 2. B. 4. C. 1. D. 3.
Câu 14. Chất X có công thức cấu tạo dạng khung phân tử như sau:
Công thức phân tử của X là 16 A. C4H10. B. C4H8. C. C4H6. D. C3H6.
Câu 15. Trong các cặp chất sau đây, cặp chất nào là đồng phân của nhau? A. C2H5OH, CH3OCH3. B. CH3OCH3, CH3CHO.
C. CH3CH2CH2OH, C2H5OH. D. C4H10, C6H6.
Phần 2. TRẮC NGHIỆM ĐÚNG -SAI
CHỦ ĐỀ. Hợp chất hữu cơ và hoá học hữu cơ
Câu 1. Các hợp chất hữu cơ đóng vai trò quan trọng đối với sự sống như protein, nucleic acid, hormone, … Cho
các đặc điểm chung của các hợp chất hữu cơ như sau:
a. Thành phần phân tử hợp chất hữu cơ nhất thiết phải chứa nguyên tố carbon và hydrogen.
b. Liên kết hoá học chủ yếu là liên kết cộng hoá trị.
c. Các hợp chất hữu cơ thường không tan hoặc ít tan trong nước, tan trong dung môi hữu cơ.
d. Các hợp chất hữu cơ thường khó bay hơi, bền với nhiệt và khó cháy. Giải:
a. Sai. Hợp chất hữu cơ nhất thiết phải chứa C, thường có H, O, N, …
d. Sai. Các hợp chất hữu cơ thường dễ bay hơi, kém bền với nhiệt và dễ cháy.
Câu 2. Cho phản ứng sau:
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên trong phổ hồng ngoại như sau: Liên kết O–H (alcohol) O–H (carboxylic acid) C=O (ester, carboxylic acid) Số sóng (cm–1) 3650 – 3200 3300 – 2500 1780 – 1650
a. Có ba hợp chất hữu cơ trong phản ứng trên.
b. Phổ hồng ngoại có số sóng hấp thụ ở 3450 cm-1 là phổ của CH3CH2OH.
c. Phổ hồng ngoại có số sóng hấp thụ ở 1750 cm-1 mà không hấp thụ đặc trưng của liên kết O–H là phổ của CH3COOH.
d. Dựa vào phổ hồng ngoại, không thể phân biệt được các chất hữu cơ có trong phản ứng trên. Giải:
c. Sai. Đó là CH3COOCH2CH3.
d. Sai. Có thể phân biệt được dựa vào phổ IR.
Câu 3: Phổ hồng ngoại (IR) của hợp chất hữu cơ (Y)° có công thức phân tử là C2H4O2 như hình bên dưới. Chất (Y)
này được sử dụng trong nhiều ngành công nghiệp khác nhau như tạo ra polymer trong công nghiệp sản xuất sơn,
chất kết dính, là dung môi hoà tan các chất hoá học, sản xuất và bảo quản thực phầm, đặc biệt dùng để sản xuất giấm.
a) Chất Y có nhóm chức carboxylic.
b) Peak A ở khoảng 3300 – 3000 cm-1 chứng tỏ có sự hiện diện của nhóm -OH.
c) Peak D khoảng 1700 cm-1 chứng tỏ có nhóm O-H. d) Chất Y là hydrocarbon.
Câu 4. Hợp chất hữu cơ benzene (C6H6, có nhiệt độ sôi là 80 °C) và acetic acid (CH3- COOH, có nhiệt độ sôi là 118 °C). 17 a. Benzene là hydrocarbon.
b. Acetic acid là dẫn xuất của hydrocarbon.
c. Trong phân tử benzene và acetic acid chỉ chứa các liên kết đơn.
d. Để tách benzene và acetic acid ra khỏi nhau, ta có thể dùng phương pháp chưng cất.
Câu 5. Cho các hợp chất hữu cơ sau: (1) CH4; (2) CH3OH; (3) CH2=CH2; (4) CH2OH-CH2OH-CH2OH; (5) CH
CH; (6) CH3CH=O; (7) CH3COOH; (8) HOOC[CH2]4COOH; (9) C6H6 (benzen); (10) H2NCH2COOH; (11) CH2OH[CHOH]4CH=O.
a. Có hai hợp chất hữu cơ đa chức và hai hợp chất hữu cơ tạp chức.
b. Có hai hợp chất thuộc loại alcohol và ba hợp chất thuộc loại carboxylic acid.
c. Có bốn hợp chất thuộc loại hydrocarbon, trong đó có hai hydrocarbon không no.
d. Có bảy hợp chất thuộc loại dẫn xuất của hydrocarbon, trong đó ba hợp chất đơn chức.
CHỦ ĐỀ. Phương pháp tách và tinh chế hợp chất hữu cơ
Câu 1. Cho các phát biểu sau:
a. Phân tích dư lượng thuốc bảo vệ thực vật trong nông sản người ta dùng chiết lỏng – rắn.
b. Lấy rượu có lẫn cơm rượu sau khi lên men bằng phương pháp chưng cất.
c. Quá trình làm muối từ nước biển dùng phương pháp kết tinh.
d. Thu tinh dầu cam từ vỏ cam dùng phương pháp kết tinh.
Câu 2. Thực hiện thí nghiệm chưng cất ethanol từ dung dịch ethanol – nước:
- Cho 60 mL rượu được nấu thủ công vào bình cầu có nhánh (chú ý chất lỏng trong bình không vượt quá 2/3 thể
tích bình), thêm vài viên đá bọt.
- Lắp dụng cụ như hình dưới đây:
- Đun nóng từ từ đến khi hỗn hợp sôi, quan sát nhiệt độ trên nhiệt kế thấy tăng dần, khi nhiệt độ trên nhiệt kế ổn
định, đó chính là nhiệt độ sôi của hỗn hợp ethanol và nước. Khi nhiệt độ bắt đầu tăng trở lại thì tắt nguồn nhiệt, ngừng chưng cất.
a. Nhiệt độ sôi của ethanol cao hơn nhiệt độ sôi của hỗn hợp ethanol và nước.
b. Nhiệt độ sôi của hỗn hợp ethanol và nước cao hơn nhiệt độ sôi của nước.
c. Độ cồn của sản phẩm sẽ lớn hơn so với độ cồn ban đầu do sản phẩm thu được tinh khiết hơn lẫn ít nước hơn rượu ban đầu.
d. Ống sinh hàn có tác dụng làm lạnh để các chất (ở trạng thái lỏng trong điều kiện thường) đang hóa hơi, đi ngang qua ống sẽ ngưng tụ.
a. Sai. Nhiệt độ sôi của ethanol thấp hơn nhiệt độ sôi của hỗn hợp ethanol và nước.
b. Sai. Hỗn hợp ethanol và nước có nhiệt độ sôi thấp hơn nhiệt độ sôi của nước.
Câu 3. Thực hiện thí nghiệm tách β-carotene từ nước ép cà rốt như sau:
- Chuẩn bị: nước ép cà rốt, hexane; cốc thuỷ tinh 100 mL, bình tam giác 100 mL, phễu chiết 60 mL, giá thí nghiệm. - Tiến hành:
Bước 1: Cho khoảng 20 mL nước ép cà rốt vào phễu chiết. Thêm tiếp khoảng 20 mL hexane, lắc đều khoảng 2 phút.
Bước 2: Để yên phễu chiết trên giá thí nghiệm khoảng 5 phút để chất lỏng tách thành hai lớp.
Bước 3: Mở khoá phễu chiết cho phần nước ở dưới chảy xuống, còn lại phần dung dịch β-carotene hoà tan trong hexane. 18
a. Trước khi chiết lớp hexane trong phễu không có màu; sau khi chiết lớp hexane trong phễu có màu vàng cam.
b. Thí nghiệm tách β-carotene từ nước cà rốt dựa theo nguyên tắc chiết lỏng – lỏng.
c. Dùng dung môi là hexane có khả năng hoà tan β-carotene nhưng không tan trong nước và có nhiệt độ sôi thấp để chiết.
d. Phễu chiết tách thành hai lớp, lớp bên trên là nước, lớp dưới là β-carotene hoà tan trong hexane. Giải:
d. Sai. Lớp dưới là nước, lớp trên là β-carotene hòa tan trong hexane.
Câu 4. Mỗi phát biểu sau là đúng hay sai?
a. Có thể tách riêng được acetic acid (ts = 118 °C), ethanol (ts = 78,3 °C) và ethyl acetate (ts = 77,1 °C) ra khỏi hỗn
hợp ester hoá bằng phương pháp chưng cất.
b. Oxi hoá không hoàn toàn hỗn hợp gồm o-xylene và p-xylene bằng dung dịch acid HNO3 thu được hỗn hợp
benzene-1,2-dicarboxylic acid (độ tan 6 g L-1 nước ở 25 °C) và benzene-1,4-dicarboxylic acid (độ tan 0,065 g L-1
nước ở 25 °C). Tách 2 acid này khỏi nhau bằng phương pháp kết tinh.
c. Xăng, dầu là các phân đoạn chưng cất dầu mỏ gồm các hydrocarbon có nhiệt độ sôi gần nhau, được sử dụng làm nhiên liệu động cơ.
d. Để tách tinh dầu chanh, bưởi, hồi, quế từ các cây, quả tương ứng, người ta thường sử dụng phương pháp chưng
cất lôi cuốn hơi nước. Giải:
a. Sai. Vì ethanol và ethyl acetate có nhiệt độ sôi gần nhau nên không sử dụng phương pháp chưng cất.
Câu 5. Quan sát hình mô phỏng thí nghiệm sắc kí cột sau:
a) Chất a bị hấp phụ mạnh nhất.
b) Chất b bị hấp phụ kém nhất.
c) Chất b hoà tan tốt trong dung môi hơn chất c.
d) Chất c hoà tan tốt trong dung môi hơn chất a.
Phần 3. TRẮC NGHIỆM TRẢ LỜI NGẮN
CHỦ ĐỀ. Ammonia và một số hợp chất ammonium
Câu 1. Có bao nhiêu liên kết cộng hóa trị trong ion muối ammonium?
Câu 2: Phản ứng tổng hợp NH3 theo quá trình Haber thường thực hiện ở áp suất bao nhiêu bar?
Câu 3: Tiến hành thí nghiệm trộn từng cặp dung dịch sau: (a) NH3 và AlCl3; (b) (NH4)2SO4 và Ba(OH)2; (c) NH4Cl
và AgNO3; (d) NH3 và HCl. Sau khi phản ứng kết thúc, có bao nhiêu thí nghiệm thu được kết tủa?
Câu 4: Cho các phát biểu sau:
(1) Ammonia lỏng được dùng làm chất làm lạnh trong thiết bị lạnh.
(2) Để làm khô khí NH3 có lẫn hơi nước, có thể dẫn khí NH3 đi qua bình đựng dung dịch H2SO4 đặc.
(3) Khi cho quỳ tím ẩm vào lọ đựng khí NH3, quỳ tím chuyển thành màu đỏ.
(4) Nitrogen lỏng được dùng để bảo quản máu và các mẫu vật sinh học.
Có bao nhiêu phát biểu sai?
Câu 5: Ammonium sulfate, (NH4)2SO4 và ammonium nitrate, NH4NO3, được sử dụng làm phân bón. Các muối này
có phần trăm khối lượng nitrogen khác nhau. Chúng có ảnh hưởng giống nhau đối với độ pH của đất trung tính. Trong các phát biểu sau:
a. Hai loại phân này đều thuộc loại phân đạm.
b. Phần trăm khối lượng Nitrogen của ammonium nitrat lớn hơn của ammonium sulfate.
c. Ammonium sulfate làm giảm pH của đất. 19
d. Ammonium nitrat làm tăng pH của đất.
Có bao nhiêu phát biểu sai?
Câu 6. Cho các PTHH sau: o o (1). NH t t 4NO2 N2 + 2H2O (2). NH4HCO3 NH3 + H2O + CO2. o o (3). NH t t 4NO3 NH3 + HNO3. (4). NH4Cl NH3 + HCl.
Có bao nhiêu phương trình đúng ?
Câu 7: Cho dung dịch NaOH dư vào ống nghiệm chứa VmL dung dịch NH4Cl 4M , đun nóng, thu được 14,874 Lít khí (đkc). Tính giá trị V ?
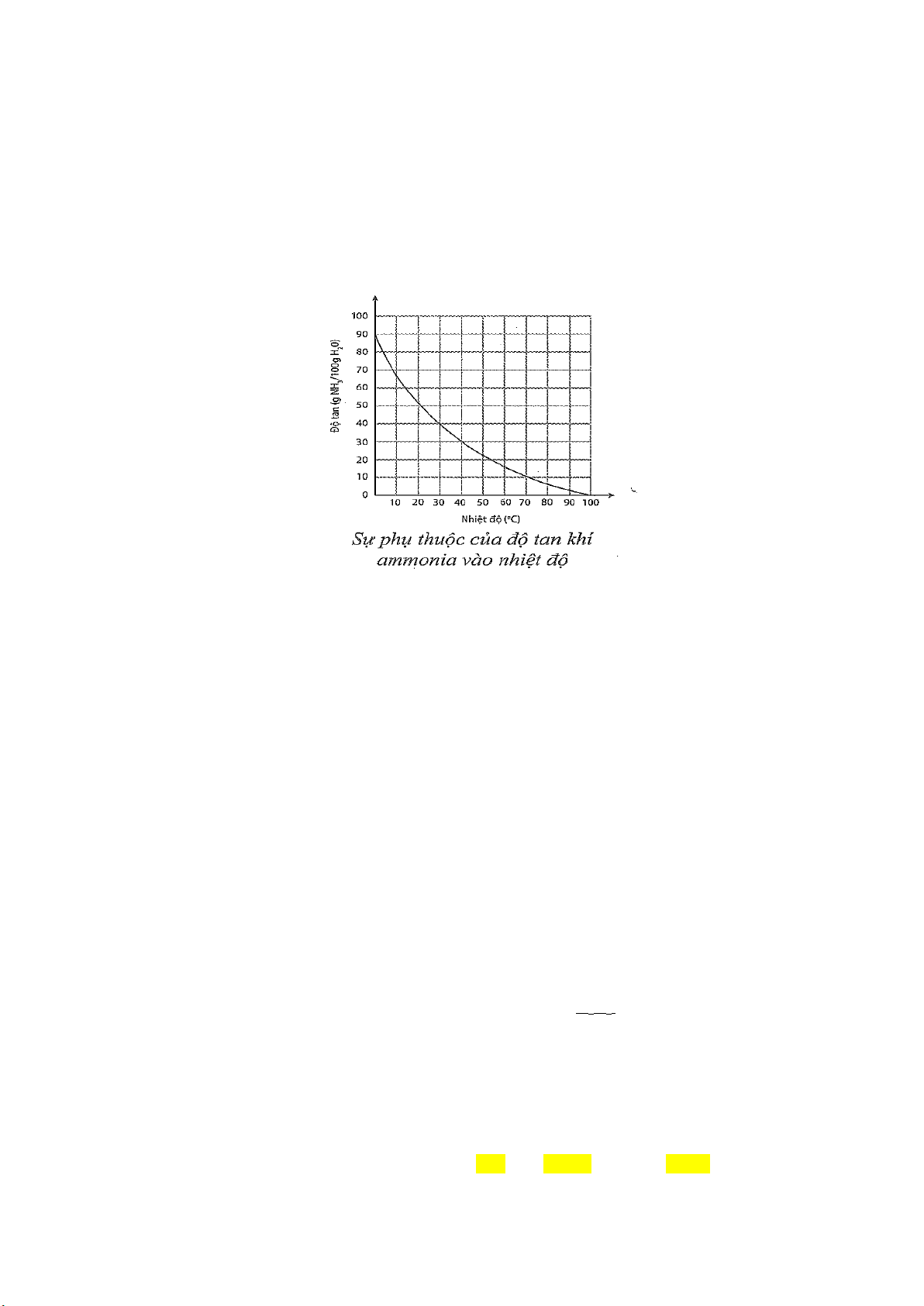
Câu 8. Sự phụ thuộc của độ tan khí ammonia trong nước vào nhiệt độ được mô tả ở hình dưới đây:
Nồng độ phần trăm (%) của dung dịch ammonia bão hòa ở 30oC là bao nhiêu? (Kết quả làm tròn đến hàng phần mười).
CHỦ ĐỀ. Một số hợp chất với oxygen của nitrogen
Câu 1: Xét các phát biểu sau về hiện tượng phú dưỡng:
(1) Hiện tượng phú dưỡng là khi sinh vật phù du, rong và tảo phát triển rất mạnh trong môi trường nước.
(2) Nguyên nhân gây phú dưỡng là do nước bị nhiễm kim loại nặng và thiếu ánh sáng.
(3) Khi hàm lượng nitrogen trong nước đạt 300 μg/L và phosphorus đạt 20 μg/L thì có thể gây ra hiện tượng phú dưỡng.
(4) Một trong các nguyên nhân gây phú dưỡng là nước thải sinh hoạt và thức ăn dư thừa trong nuôi trồng thủy sản.
(5) Hiện tượng phú dưỡng có thể gây thiếu oxygen trong nước, làm mất cân bằng sinh thái và gây ô nhiễm môi trường.
Các nhận định đúng là (Ghi thứ tự các nhận định đúng từ nhỏ đến lớn, VD: 123, 234, 125…)
Câu 2. Trong những cơ mưa dông kèm sấm sét, sự chuyển hoá của nitrogen đơn chất xảy ra theo sơ đồ sau: O 2 O2 O2 H2O N NO
NO HNO H + NO 2 (1) (2) 2 (3) 3 (4) 3
Trong sơ đồ trên, có bao nhiêu phản ứng xảy ra quá trình oxi hóa khử
Câu 3. Trong các phát biểu về một số hợp chất với oxygen của nitrogen:
(1). Trong phân tử nitric acid, nguyên tử N có hóa trị là IV và số oxi hóa là +5.
(2). Khí thải có chứa NO2 góp phần gây ra mưa acid và hiện tượng phú dưỡng.
(3). Khi cho kim loại tác dụng với HNO3 thì không thể tạo ra hợp chất N2O5.
(4). Nitric acid đặc nguội phản ứng với kim loại Fe thu được khí X có màu nâu đỏ, khí X là NO2.
Các phát biểu đúng là (Ghi thứ tự các phát biểu đúng từ nhỏ đến lớn, VD: 123, 234, 125…)
Câu 4: Cho các chất: Cu, Al, MgO, Fe3O4, Fe(OH)2, CaCO3, K2SO4 lần lượt tác dụng với dung dịch HNO3 loãng.
Có bao nhiêu trường hợp xảy ra phản ứng oxi hóa – khử?
Câu 5: Cho phản ứng: Fe3O4 + HNO3 → Fe(NO3)3 + NO ↑ + H2O. Hệ số tỉ lượng của HNO3 trong phương trình hoá học trên là
Câu 6. Cho dung dịch HNO3 tác dụng với các chất sau: NH3, Cu, CaCO3, Fe3O4 và NaOH. Có bao nhiêu phản ứng
trong đó HNO3 đóng vai trò acid theo Bronsted? 20



