
Preview text:
Lý thuyết Hóa 10 Bài 13
I. Phản ứng tỏa nhiệt, phản ứng thu nhiệt
- Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt
- Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt Ví dụ
- Phản ứng tỏa nhiệt: Đốt than, củi để không khí xung quanh ấm hơn
- Phản ứng thu nhiệt: Pha viên sủi vitamin C vào nước, thấy nước trong cốc mát hơn
II. Biến thiên enthalpy của phản ứng
- Khái niệm: Biến thiên enthalpy của phản ứng (nhiệt phản ứng) là nhiệt lượng tỏa ra hay thu
vào của phản ứng ở điều kiện áp suất không đổi. Kí hiệu: ∆rH
- Phương trình hóa học kèm theo trạng thái của các chất và giá trị ∆rH gọi là phương trình nhiệt hóa học
Giải Hóa 10 Bài 13 trang 86, 87 Bài 1
Phương trình nhiệt hóa học giữa nitrogen và oxygen như sau: N2(g) + O2(g) → 2NO(g)
Kết luận nào sau đây đúng?
A. Nitrogen và oxygen phản ứng mạnh hơn khi ở nhiệt độ thấp B. Phản ứng tỏa nhiệt
C. Phản ứng xảy ra thuận lợi ở điều kiện thường
D. Phản ứng hóa học xảy ra có sự hấp thụ nhiệt năng từ môi trường Gợi ý đáp án Đáp á D Bài 2
Biến thiên enthalpy của một phản ứng được ghi ở sơ đồ dưới. Kết luận nào sau đây là đúng? A. Phản ứng tỏa nhiệt
B. Năng lượng chất tham gia phản ứng nhỏ hơn năng lượng chất sản phẩm
C. Biến thiên enthalpy của phản ứng là a kJ/mol D. Phản ứng thu nhiệt Gợi ý đáp án Đáp án A Bài 3
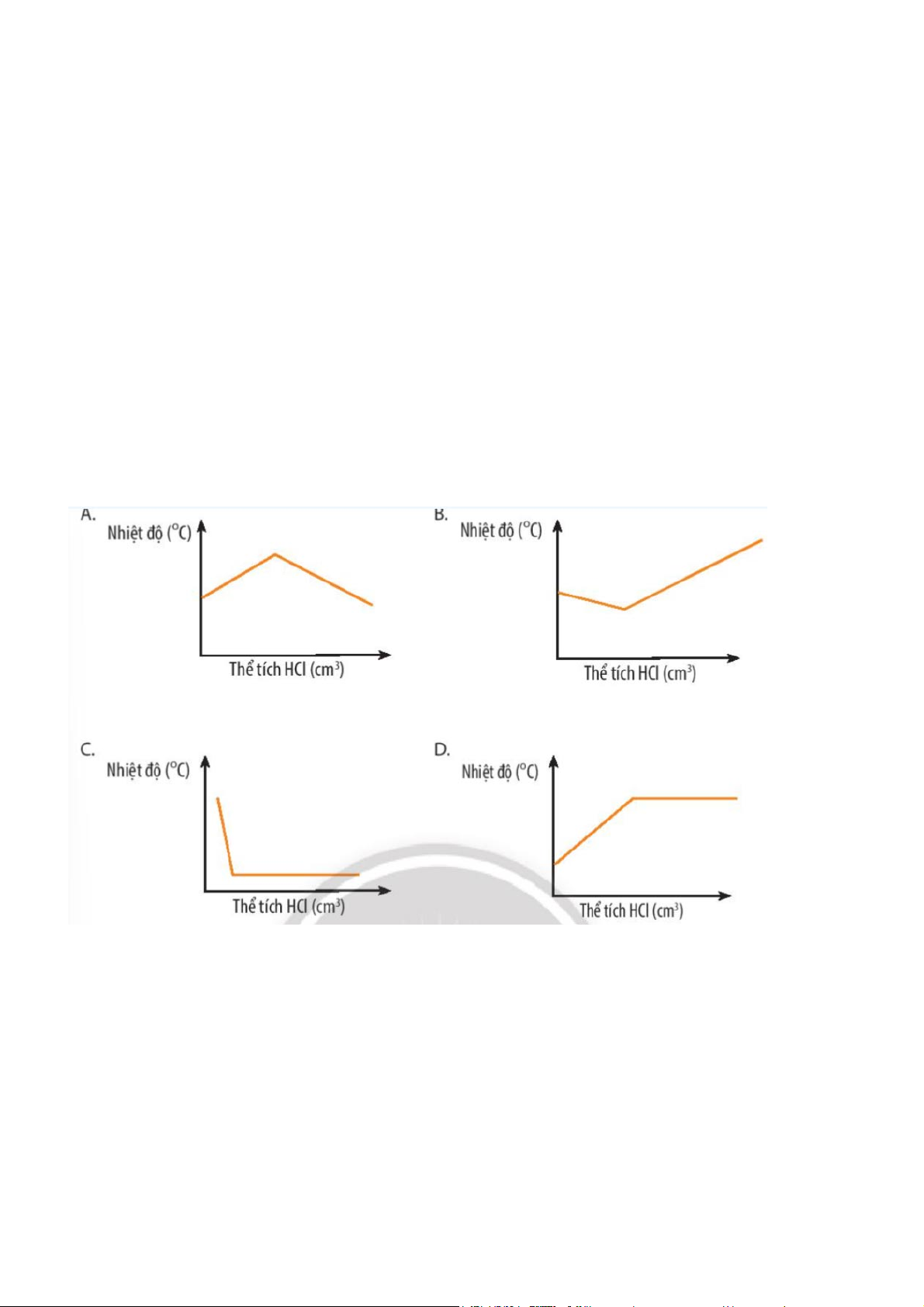
Đồ thị nào sau đây thể hiện đúng sự thay đổi nhiệt độ khi dung dịch hydrochloric acid được
cho vào dung dịch sodium hydroxide tới dư? Gợi ý đáp án
Phản ứng giữa dung dịch hydrochloric acid và dung dịch sodium hydroxide là phản ứng tỏa nhiệt
Khi phản ứng nhiệt độ tăng dần lên. Kết thúc phản ứng nhiệt độ giảm dần để cân bằng với
nhiệt độ của môi trường
