

Preview text:
Giải bài tập trang 58 SGK Hóa 10 Bài 1
Ion Mg2+ có cấu hình electron giống cấu hình electron của khí hiếm nào? A. Helium B. Neon C. Argon D. Krypton Gợi ý đáp án Đáp án B
Cấu hình electron của nguyên tử Mg (Z = 12): 1s22s22p63s2
Nguyên tử Mg nhường 2 electron tạo thành ion Mg2+ có cấu hình electron là:
1s22s22p6 giống với cấu hình electron của khí hiếm neon. Bài 2
Cho các ion sau: Ca2+, F-, Al3+ và N3-. Số ion có cấu hình electron của khí hiếm neon là A. 4 B. 2 C. 1 D. 3 Gợi ý đáp án Đáp án D
- Cấu hình electron của nguyên tử Ca (Z = 20): 1s22s22p63s23p64s2
Nguyên tử Ca nhường 2 electron tạo thành ion Ca2+ có cấu hình electron là:
1s22s22p6 3s23p6 giống với cấu hình electron của khí hiếm Ar.
- Cấu hình electron của nguyên tử F (Z = 9): 1s22s22p5
Nguyên tử F nhận 1 electron tạo thành ion F- có cấu hình electron là:
1s22s22p6 giống với cấu hình electron của khí hiếm neon.
Cấu hình electron của nguyên tử Al (Z = 13): 1s22s22p63s23p1
Nguyên tử Al nhường 3 electron tạo thành ion Al3+ có cấu hình electron là:
1s22s22p6 giống với cấu hình electron của khí hiếm neon.
- Cấu hình electron của nguyên tử N (Z = 7): 1s22s22p3
Nguyên tử N nhận 3 electron tạo thành ion N3- có cấu hình electron là:
1s22s22p6 giống với cấu hình electron của khí hiếm neon.
Vậy có 3 ion là F-, Al3+ và N3- có cấu hình electron giống với cấu hình electron của khí hiếm Ne. Bài 3
Potassium và magnesium là các nguyên tố thiết yếu đối với cơ thể sinh vật sống.
a) Viết cấu hình electron của các ion được tạo thành từ nguyên tử của các nguyên tố
này. Chúng có cấu hình electron của những nguyên tử khí hiếm nào?
b) Có hợp chất ion nào chỉ tạo bởi các ion trên với nhau không? Vì sao? Gợi ý đáp án a)
Potassium (K, Z = 19) có cấu hình electron là: 1s22s22p63s23p64s1
Nguyên tử K nhường 1 electron tạo thành ion K+ có cấu hình electron là:
1s22s22p63s23p6giống với cấu hình electron của khí hiếm Ar.
Cấu hình electron của nguyên tử Mg (Z = 12): 1s22s22p63s2
Nguyên tử Mg nhường 2 electron tạo thành ion Mg2+ có cấu hình electron là:
1s22s22p6 giống với cấu hình electron của khí hiếm neon.
b) Không có hợp chất ion nào chỉ tạo bởi các ion K+ và Mg2+ với nhau vì hai ion này
cùng mang điện tích dương. Hợp chất ion chỉ được tạo bởi lực hút tĩnh điện giữa các
ion mang điện tích trái dấu. Bài 4
Hoàn thành những thông tin còn thiếu trong bảng sau:
Công thức hợp chất ion Cation Anion CaF2 ? ? ? K+ O2- Gợi ý đáp án
Công thức hợp chất ion Cation Anion CaF2 Ca2+ F- K2O K+ O2- Bài 5
Sodium oxide (Na2O) có trong thành phần thủy tinh và các sản phẩm gốm sứ. Trình
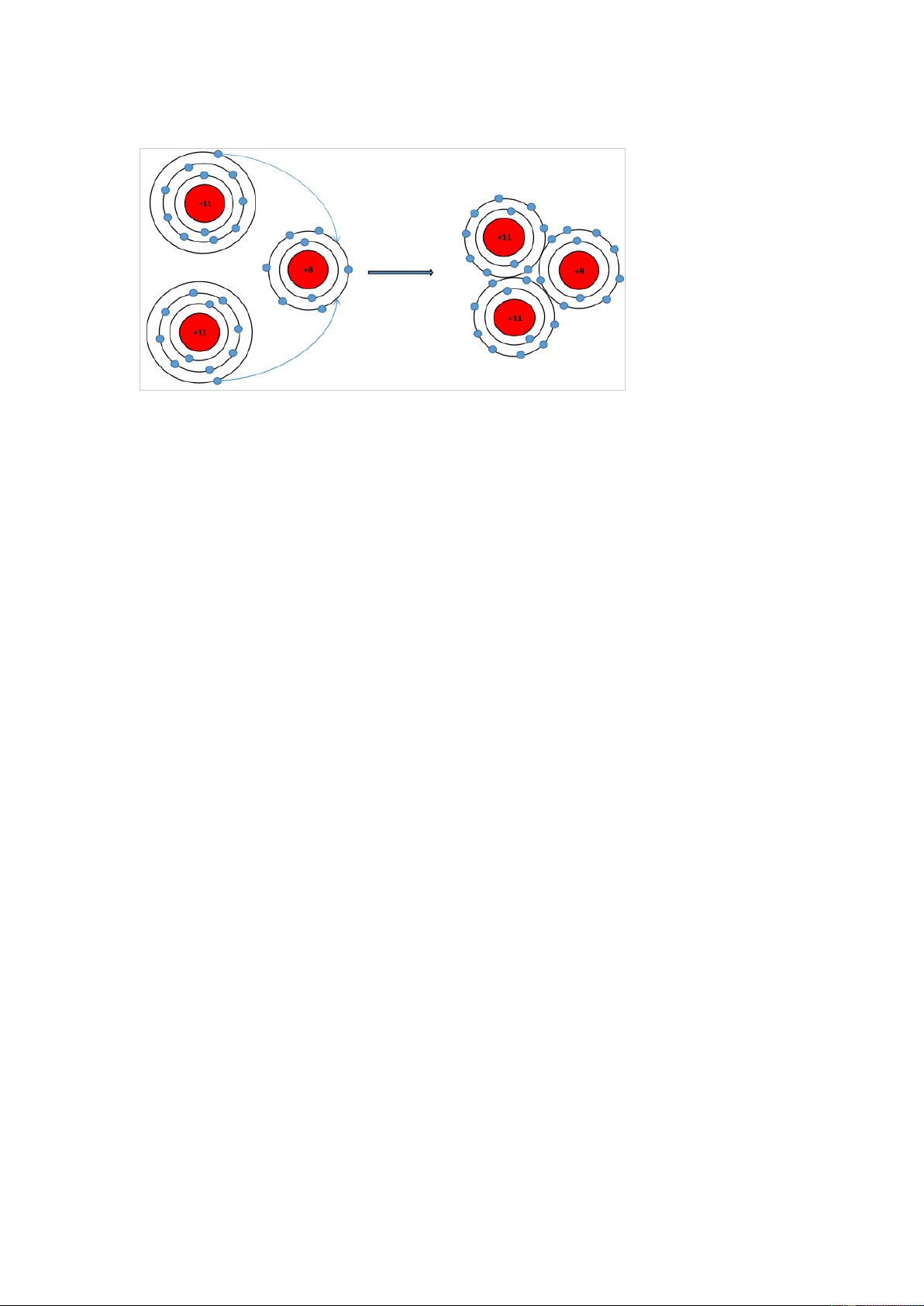
bày sự hình thành liên kết ion trong phân tử sodium oxide. Gợi ý đáp án
Nguyên tử Na (Z = 11): 1s22s22p63s1 ⇒ Có 1 electron ở lớp ngoài cùng
⇒ Có xu hướng nhường 1 electron để đạt cấu hình electron của khí hiếm tạo thành ion Na+
- Nguyên tử O (Z = 8): 1s22s22p4 ⇒ Có 6 electron ở lớp ngoài cùng
⇒ Có xu hướng nhận 2 electron để đạt cấu hình electron của khí hiếm tạo thành ion O2-
⇒ Nguyên tử O nhận 2 electron của hai nguyên tử Na tạo thành ion là O2-.
- Hai ion Na + và 1 ion O2- liên kết với nhau tạo thành phân tử Na2O




