






































Preview text:
Kiểm Nghiệm
Các Dạng Thuốc Đặc Biệt
PGS.TS. Nguyễn Đức Tuấn
Bộ môn Hóa Phân Tích – Kiểm Nghiệm
Khoa Dược – Đại học Y Dược TPHCM Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Kiểm Nghiệm Các Dạng Thuốc Đặc Biệt Mục tiêu
Trình bày được định nghĩa, phân loại và yêu cầu chất lượng của thuốc dán và thuốc khí dung Nội dung Thuốc dán
Thuốc dán thấm qua da
Thuốc dán tác dụng tại chỗ
Một vài ví dụ về thuốc dán Thuốc khí dung
Các dạng thuốc khí dung
Yêu cầu chất lượng của thuốc thành phẩ m
Một số chỉ tiêu kiểm nghiệm thành phần thuốc khí dung
Một vài ví dụ về thuốc khí dung Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Kiểm Nghiệm Các Dạng Thuốc Đặc Biệt
Tài liệu tham khảo chính 1. BP 2010, pp. 2667-2668
2. Dược điển Việt Nam IV (2009), tr. PL-15, 16, 17, 24, 25, 26, 148, 182, 185, 258, 266, 360
3. USP 32 (2009), pp. 204, 225, 2091, 3533
4. Võ Xuân Minh, Nguyễn Văn Long (2006), Kỹ thuật bào chế và sinh dược học các dạng
thuốc, tập 2, tr. 39-41
5. Lê Quan Nghiệm, Huỳnh Văn Hóa (2007), Bào chế và sinh dược học, tập 2, tr. 382-384 6. Quyết định của B
ộ trưởng Bộ y tế số 3113 /1999/QĐ-BYT ngày 11 tháng 10 nă m 1999
ban hành tiêu chuẩn “Giới hạn vi khuẩn, nấm mốc trong mỹ phẩm và phương pháp thử
kích ứng trên da”, tr. 10-13 Nguyễn Đức Tuấn Đại học Y Dược TPHCM Thuốc Dán
Thuốc dán thấm qua da Thuốc dán tác dụn g tại chỗ Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da
Chế phẩm mềm dẻo với những kích cỡ khác nhau
Chứa một hoặc nhiều hoạt chất
Được dán trên những vùng da nguyên vẹn
Đưa hoạt chất thấm qua da vào hệ thống tuần hoàn gây tác
dụng phòng hoặc điều trị Cấu tạo
Lớp màng nền bao phủ bên ngoài
Lớp chứa hoạt chất có bề mặt bắt dính
Lớp bảo vệ: bao phủ bề mặt bắt dính, gỡ bỏ dễ dàng trước khi dán lên da Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da
Lớp màng nền
Thường không thấm nước và hoạt chất
Có nhiệm vụ hỗ trợ và bảo vệ lớp chứa hoạt chất
Có thể có cùng kích thước với lớp chứa hoạt chất hoặc lớn hơn
(mép viền xung quanh của lớp màng nền được bao phủ bởi những
chất dễ dàng bắt dính khi dán lên da để đảm bảo sự kết dính của thuốc dán lên da) Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da
Lớp chứa hoạt chất
Chứa một hoặc nhiều hoạt chất cùng với các tá dược
Có thể là một lớp duy nhất hoặc nhiều lớp khung rắn hoặc khung xốp (matrix) nửa rắn
hoặc kiểu bể chứa (reservoir) nửa rắn Khung xốp Thành phầ
n và cấu trúc khung xốp xác định kiểu khuếch tán của hoạt chất qua da
Có thể chứa các chất giúp dễ dàng kết dính khi dán lên da Bể chứa
Một lớp màng kiểm soát (polymer) sự giải phóng và khuếch tán hoạt chất từ chế phẩm
Các chất giúp dễ dàng kết dính khi dán, có thể bao phủ
một phần hoặc một vài vị trí trên màng kiểm soát
hoặc chỉ xung quanh viền của lớp màng nền Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da
Lớp bảo vệ Lớp nhựa dẻo hoặ c kim loại dát mỏng Khi bóc lớp bả o v :
ệ không được kéo theo lớp chứa hoạt chất hoặ c các chất giúp kết dính từ miếng dán Yêu cầ u chung
Dán lên vùng da khô, sạch và nguyên vẹn
Dễ dàng dính lên da bởi một lực nh ẹ nhàng Có thể bóc ra d
ễ dàng mà không làm tổn thương da hoặc
Chỉ tách ra được lớp bảo vệ
Không gây mẫn cảm hoặ c kích ứn
g da, thậm chí trong những lần dùng lặp lại Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng
Phải đạt các yêu cầu qui định trong chuyên luận riêng và
các yêu cầ sau u Tính chất
Độ đồng đều hàm lượng
Độ đồng đều khối lượng lớp chứa hoạt chất
Độ đồng đều diện tích
Định tính, định lượng Độ hòa tan
Độ kích ứng (Thử tính kích ứng)
Dư lượng dung môi hòa tan chất kết dính
Dư lượng của nguyên liệu tạo chất kết dính Lực kết dính Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng Tính chấ t
Phải đồng nhất, có độ bắt dính thích hợp (dễ dính và dễ bóc), không gây kích ứn g da
Độ đồng đều hàm lượng
Nếu như không có chỉ dẫn khác trong chuyên luận riêng, tiến hành trên 10 đơn vị riêng
rẽ được lấy bất kỳ. Chế phẩm đem kiểm tra đạt yêu cầu phép thử nếu
Hàm lượng trung bình của 10 đơn vị không nằm ngoài giới hạn từ 90% đến 110% so
với hàm lượng ghi trên nhãn và
Không có đơn vị nào có hàm lượng nằm ngoài giới hạn từ 75% đến 125% so với hàm lượng trung bình Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng
Độ đồng đều khối lượng lớp chứa hoạt chất
Nếu phép thử độ đồng đều hàm lượng đã được tiến hành với tất cả các hoạt chất có
trong thuốc dán qua da thì không cần phải thử độ đồng đều khối lượng Tiến hành
Lấy 20 đơn vị bấ tkỳ
Xác định khối lượng lớp chứa hoạt chất của từng đơ
n vị và tính khối lượng trung bình
của lớp chứa hoạt chất
Cân từng đơn vị đã được loại bỏ lớp bảo vệ (m ) 1
Dùng hỗn hợp dung môi hữu cơ phù hợp để rữa hết lớp keo chứa hoạt chất, làm
khô, cân lại khối lượng lớp nền (m ) 2
Khối lượng lớp chứa hoạt chất: m1 - m2 Yêu cầu
Không quá 2 đơn vị có khối lượng lệch ra ngoài 5% so với khối lượng trung bình và
Không có đơn vị nào có khối lượng lệch ra ngoài 10% so với khối lượng trung bình Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng
Độ đồng đều diện tích Tiến hành
Lấy 20 đơn vị bất kỳ
Đo diện tích của từng đơn vị, tính diện tích trung bình: bóc lớp màng bảo vệ của từng
đơn vị, đo và tính diện tích của lớp chứa hoạt chất Yêu cầu
Không quá 2 đơn vị có diện tích lệch ra ngoài 5% so với diện tích trung bình và
Không có đơn vị nào có diện tích lệch ra ngoài 10% so với diện tích trung bình
Định tính, định lượng
Theo qui định trong chuyên luận riêng
Độ kích ứng (Thử tính kích ứng)
Tiến hành theo quy định hiện hành về “Phương pháp thử tính kích ứng trên da áp dụng
cho các sản phẩm dùng trong y tế và mỹ phẩm” (tài liệu tham khảo số 6) Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng Độ hòa tan
Phương pháp thử nghiệm thích hợp được yêu cầu theo từng chuyên luận riêng
Thiết bị kiểu giỏ quay, kiểu cánh khuấy hoặc kiểu dòng chảy có thể được sử dụng
Sự giải phóng hoạt chất qua màng cũng được sử dụng
Màng cellulose hoặc silicon
Phải không ảnh hưởng đến động học của giải phóng hoạt chất từ miếng thuốc dán
Màng có thể được xử lý một cách phù hợp trước khi thử nghiệm, được lưu giữ
trong môi trường thích hợp để sử dụng cho thử nghiệm trong 24 giờ Tiến hành
Đặt bề mặt phóng thích hoạt chất của miếng thuốc dán lên màng, tránh sự hình thành bọt khí
Điều kiện thử nghiệm và các yêu cầu tiến hành theo chuyên luận riêng Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng
Độ hòa tan: xác định độ hòa tan của thuốc dán thấm qua da scopolamin 1,5 mg
Thiết bị: kiểu cánh khuấy
Môi trường: 300 ml nước. Nhiệt độ môi trường: 32 ± 0,3oC
Tốc độ quay: 45 vòng/phút
Thời gian: 72 giờ. Thời điểm lấy mẫu: 1, 6, 24, 36, 72 giờ
Hàm lượng scopolamin phóng thích được xác định bằng HPLC Yêu cầu: Thời gian % scopolamin Thời gian % scopolamin (giờ) phóng thích (giờ) phóng thích 1 20% - 25% 36 65% - 75% 6 28% - 33% 72 ≥ 80% 24 48% - 53% Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da – Yêu cầu chất lượng
Độ hòa tan: xác định độ hòa tan của thuốc dán thấm qua da scopolamin 1,5 mg
Kết quả: % scopolamin giải phóng Thời
% scopolamin phóng thích gian TB SD RSD (giờ) 1 2 3 4 5 6 1 24,00 23,90 24,00 24,00 24,00 24,00 23,98 0,04 0,17% 6 30,30 31,10 30,80 30,70 30,90 30,40 30,70 0,30 0,99% 24 49,00 50,00 49,00 50,50 48,30 50,80 49,60 0,98 1,98% 36 74,30 69,90 74,60 70,20 65,50 70,20 70,78 3,36 4,74% 72 87,00 86,50 86,90 86,50 84,30 84,50 85,95 1,22 1,42% Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da Bảo quản
Nếu không có qui định khác Bao bì kín Nhiệt độ phòng Tránh ánh sáng Nhãn
Theo đúng qui định về Hướng dẫn ghi nhãn thuốc của Bộ Y tế Nơi dán thuốc
Tổng hàm lượng hoạt chất có trong một đơn vị
Liều phóng thích cho mỗi đơn vị thời gian
Diện tích bề mặt phóng thích Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da Estradiol (BP 2010, trang 2667)
Hoạt chất: estradiol hemihydrat
Cấu tạo: kiểu khung xốp (matrix) hoặc bể chứa (resorvoir)
Tùy thuộc vào cấu tạo của lớp hoạt chất, chỉ tiêu độ giải phóng hoạt chất
estradiol sẽ được thực hiện theo phương pháp thử nghiệm thích hợp
Chế phẩm phải đạt các yêu cầu qui định trong chuyên luận thuốc dán thấm
qua da và các yêu cầu sau đây: Định tính Tạp chất liên quan
Độ đồng đều hàm lượng Định lượng Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da Estradiol (BP 2010, trang 2667) Định tính
Bản mỏng silicagel F254 (10 x 10 cm) Pha độn :
g aceton – dicloromethan (2:8, tt/tt)
Chuẩn bị mẫu
Dung dịch (1): Loại b
ỏ lớp bảo vệ, rạch thành khía b
ề mặt bắt dính, che lại bằng len
thủy tinh. Cho miếng thuốc dán vào ống ly tâm, thêm methanol vừa đủ để được dung dịch
có chứa 2 mg estradiol/5 ml methanol, siêu âm và lắc trong 15„, lọc qua giấy lọc bằng sợi
thủy tinh (loại Whatman GF/C), lọc tiếp qua màng lọc 0,45 m
Dung dịch (2): dung dịch đối chiếu estradiol hemihydrat 0,04% trong ethanol tuyệt đối Tiến hành
Chấm mỗi dung dịch khoảng 10 l, khai triển sắc ký khoảng 7 cm. Lấy bản mỏng ra, để
khô tự nhiên khoảng 5„ ,phun dung dịch H 50% và 110 2SO4 sấy
oC trong 10„. Để nguội và soi bản mỏng dưới đè n UV 366 nm Yêu cầ u
Dung dịch (1) có vết chính tương ứn
g về màu sắc, v ịtrí và kích thước với vết chính của dung dịch (2) Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da Estradiol (BP 2010, trang 2667)
Tạp chất liên quan
Chuẩn bị mẫu
Dung dịch (1): Loại bỏ lớp bảo vệ khỏi 10 miếng thuốc dán, rạch thành khía bề mặt bắt dính, che
lại bằng len thủy tinh. Cho các miếng thuốc dán vào trong 1 bình cầu, thêm pha động vừa đủ để thu
được dung dịch có nồng độ estradiol 0,01% (kl/tt), siêu âm 10„, lắc tiếp 1 giờ, lọc qua giấy lọc bằng
sợi thủy tinh (loại Whatman GF/C). Nếu dịch lọc không trong, lọc tiếp qua màng lọc 0,45 m
Dung dịch (2): pha loãng 100 lần từ dung dịch (1) với pha động
Điều kiện sắc ký
Cột pha đảo C18 (250 x 4,6 mm; 10 m) (cột Nucleosil C18 thích hợp nhất); Pha động: acetonitril –
nước (35:65, tt/tt); Tốc độ dòng: 2 ml/phút; Bước sóng phát hiện: 280 nm; Thể tích tiêm mẫu: 50 l Tiến hành
Tiêm lần lượt dung dịch (1) và (2), mỗi dung dịch tiêm 2 lần. Phép thử chỉ có giá trị khi tỷ số chiều
cao của pic estradiol trong dung dịch (2) so với nhiễu đường nền lớn hơn 10 Yêu cầ u
Trong sắc ký đồ của dung dịch (1), diện tích pic của bất kỳ pic phụ nào không được lớn hơn diện tích
pic của estradiol trong dung dịch (2) (1%) và tổng diện tích pic của các pic phụ trong sắc ký đồ của
dung dịch (1) không được lớn hơn hai lần diện tích pic của estradiol trong sắc ký đồ của dung dịch
(2) (2%). Loại bỏ pic của diethyltoluamid Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da Estradiol (BP 2010, trang 2667)
Độ đồng đều hàm lượng
Chuẩn bị mẫu
Dung dịch mẫu thử: Loại bỏ lớp bảo vệ khỏi 1 miếng thuốc dán, rạch thành khía bề mặt bắt dính,
che lại bằng len thủy tinh. Cho miếng thuốc dán vào trong 1 bình cầu, thêm pha động vừa đủ để thu
được dung dịch có nồng độ estradiol 0,01% (kl/tt), siêu âm 10„, lắc tiếp 1 giờ, lọc qua giấy lọc bằng
sợi thủy tinh (loại Whatman GF/C), lọc tiếp qua màng lọc 0,45 m
Dung dịch mẫu đối chiếu: sử dụng pha động, pha loãng 10 lần dung dịch estradiol hemihydrat
0,1% (kl/tt) trong acetonitril
Điều kiện sắc ký
Giống chỉ tiêu tạp chất liên quan. Thể tích tiêm mẫu: 20 l Tiến hành
Tiêm lần lượt dung dịch mẫu thử và đối chiếu. Tính diện tích pic của estradiol trong sắc ký đồ của
mỗi dung dịch. Hàm lượng estradiol trong một miếng thuốc dán được tính dựa vào hàm lượng tinh
khiết của estradiol hemihydrat trong dung dịch mẫu đối chiếu Yêu cầ u
Chế phẩm đem kiểm tra đạt yêu cầu phép thử nếu hàm lượng trung bình của 10 đơn vị không nằm
ngoài giới hạn từ 90% đến 110% so với hàm lượng ghi trên nhãn và không có đơn vị nào có hàm
lượng nằm ngoài giới hạn từ 75% đến 125% so với hàm lượng trung bình Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán thấm qua da Estradiol (BP 2010, trang 2667)
Định lượng
Sử dụng kết quả trung bình t
ừ 10 kết quả đạt được khi tiến hành thử độ đồng đều hàm lượng Yêu cầu
Hàm lượng estradilol trong một miếng thuốc dán qua da không được nằm ngoài
giới hạn từ 90,0% - 110,0% so với hàm lượng ghi trên nhãn Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Kết quả kiểm nghiệm SCOPOLAMIN TTS 1,5 mg STT CHỈ TIÊU YÊU CẦU KẾT QUẢ 1 Tính chất
Miếng dán hình vuông, kích thước 2,25 cm x 2,25 Đạt
cm, lớp nền chứa dược chất ở trên, phía dưới là lớp bả
o vệ. Không có bọt khí, không có tinh thể
dược chất kết tinh trong lớp chứa hoạt chất 2
Độ đồng đều diện tích
± 5% so với diện tích trung bình miếng dán Đạ t 3
Độ đồng đều hàm lượng
hàm lượng trung bình của 10 đơn vị không nằm Đạt
ngoài giới hạn từ 90% đến 110% so với hàm
lượng ghi trên nhãn và không có đơn vị nào có
hàm lượng nằm ngoài giới hạn từ 75% đến 125%
so với hàm lượng trung bình 4 Định tính Scopolamin HBr Đún g 5 Độ hòa tan
Phải đạt theo qui định Đạ t 6 Định lượng
90,0% - 110,0% so với hàm lượng ghi trên nhãn Đạ ( t 100,6%) 7 Kích ứng da Không kích ứng Đạ t Nguyễn Đức Tuấn Đại học Y Dược TPHCM
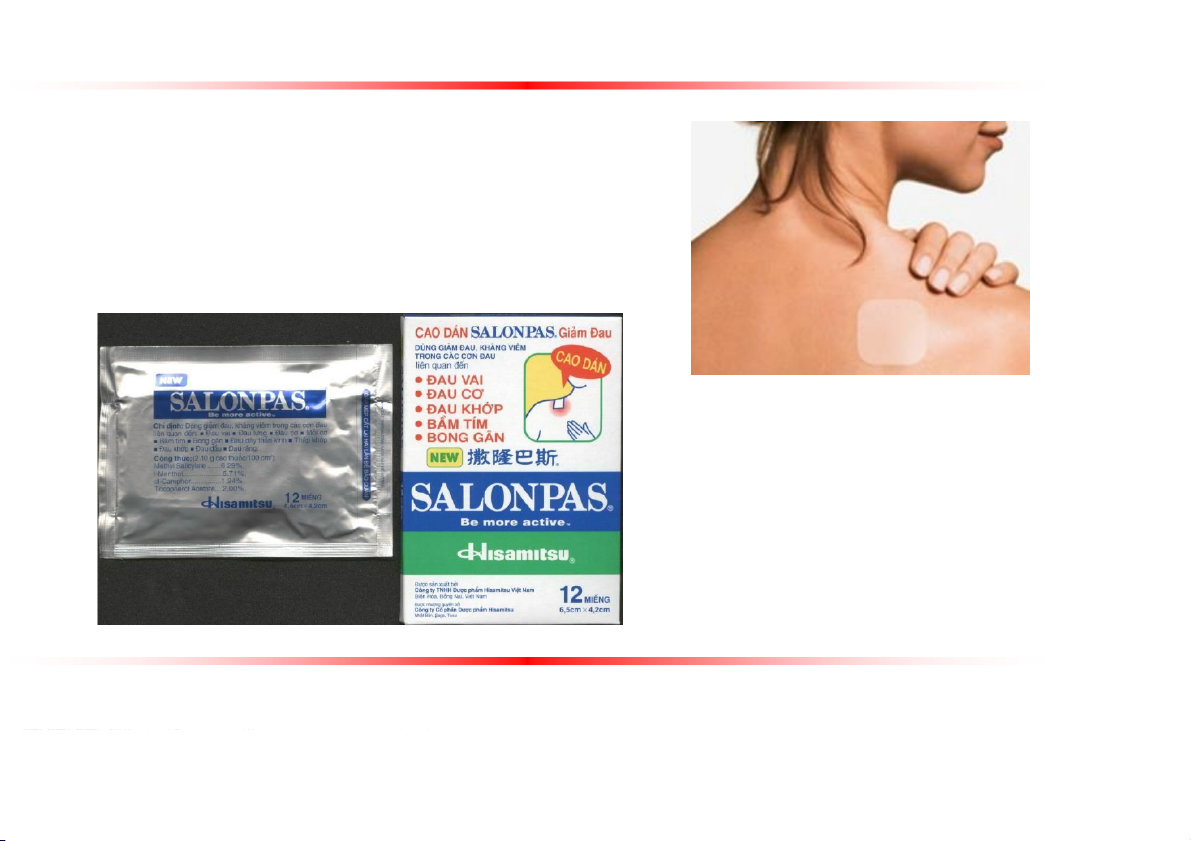
Thuốc dán tác dụng tại chỗ
Chế phẩm có chứa một hoặc nhiều dược chất
Trải đều hoặc dính trên một lớp vải hoặc một lớp phim dẻo và có tính bắt dính trên da Được dán trên da
Dược chất và các thành phần khác hầu như không thấm qua da để đi vào hệ
tuần hoàn chung, chỉ phát huy tác dụng tại chỗ Cấu tạo
Tương tự thuốc dán thấm qua da Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán tác dụng tại chỗ – Yêu cầu chất lượng
Phải đạt các yêu cầu qui định trong chuyên luận riêng và các yêu cầ sau u Tính chất
Độ đồng đều hàm lượng
Định tính, định lượng Độ hòa tan
Độ kích ứng (Thử tính kích ứng)
Dư lượng dung môi hòa tan chất kết dính
Dư lượng của nguyên liệu tạo chất kết dính Lực kết dính Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán tác dụng tại chỗ Bảo quản
Nếu không có qui định khác Bao bì kín Nhiệt độ phòng Tránh ánh sáng Nhãn
Theo đúng qui định về Hướng dẫn ghi nhãn thuốc của Bộ Y tế Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc dán tác dụng tại chỗ – Cao dán acid salicylic (USP 32, tr. 3533)
Hỗn hợp đồng nhất của acid salicylic, được trải trên lớp màng nền bằng giấy, vải bông
hoặc một vật liệu thích hợp khác
Yêu cầu: Hàm lượng acid salicylic trong lớp chứa hoạt chất không được nằ m ngoài giới hạn từ 90,0% đế
n 110,0% so với hàm lượng ghi trên nhãn Định lượng
Cân CXK một miếng cao dán (đã loại bỏ lớp bảo vệ) tương ứng với 500 mg acid salicylic (m ) 1
Cắt nhỏ, cho vào bình cầu, thêm 50 ml CHCl ,
3 lắc đến khi miếng cao dán rã hoàn toàn
Gạn dịch CHCl , rửa lớp lần rửa tiếp với chứa 3 nền 2 x 25 ml CHCl , 3 50 ml alcol có 1 ml NH OH 4 6N, rửa với 40 ml alcol
Làm khô lớp nền, cân (m ). Tính 2
khối lượng lớp chứa hoạt chất (m - m ) 1 2
Lọc dịch chiết CHCl qua miếng 3
vải bông sạch, rửa cắn còn lại với 10 ml alcol, lọc dịch rửa qua
miếng vải bông, dùng đũa thủy tinh ép miếng vải bông để lấy hết dịch lọc
Lắc dịch lọc với NaOH 1N 3 lần x 10 ml, rửa tiếp dịch lọc với nước 2 lần x 25 ml, cho tất cả vào
bình định mức 500 ml, thêm nước tới vạch, lắc đều
Định lượng bằng phương pháp brom. Áp dụng kỹ thuật chuẩn độ thế, chỉ thị hồ tinh bột. Thực
hiện tương tự đối với một mẫu trắng
Một mL dung dịch brom 0,1N tương đương với 2,302 mg acid salicylic Nguyễn Đức Tuấn Đại học Y Dược TPHCM Thuốc khí dung
Dạng bào chế mà trong quá trình sử dụng, hoạt chất được phân tán thành
những hạt nhỏ trong không khí do thuốc được nén qua đầu phun bởi một luồng
khí đẩy ở áp suất cao để tới v ịtrí tác dụng
Dùng ngoài da, tóc, műi - họng, răng miệng hoặc tai, ...
Hay dùng để hít theo đường hô hấp
Có tác dụng tại chỗ hoặc tác dụng toàn thân Các dạn g thuốc khí dung Dạng hoàn chỉnh Kiểu piston Dùng quả bóp Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung dạng hoàn chỉnh
Bao gồm thuốc, chai, l
ọ kín chứa thuốc có gắn đầu phun cùng với van và khí đẩy
được nén ở áp suất thích hợp Khi nhấn đầ
u phun, thuốc sẽ tự động đẩy ra khỏi đầu van
Van: không phân liều, nhưng nếu cần thiết thuốc phải gắn van phân liều chính xác
Thuốc: thường ở thể lỏng (dung dịch, hỗ n dịch, nh ű tương)
Đồ đựng thuốc
Chai, lọ, bình được chế tạo đặc biệt để có thể gắn kết với các bộ phận gồm ống
dẫn thuốc, van, đầu phun và nắp đậy
Chế bằng vật liệu thích hợp nh
ư thủy tinh, nhựa ,kim loại hoặc phối hợ p Khí đẩy
Nén thuốc qua đầu phun
Lượng khí nén đóng trong thuốc phải đảm bảo đủ để đẩy hết liều lượng thuốc
Hỗn hợp các loại khí: carbonic, nitơ hoặc hydrocarbon và dẫn chất halogen của
hydrocarbon. Hai nhóm sau thường dùng ở dạn g khí nén hóa lỏng
Lưu ý: kiểu đóng thuốc dưới áp lực cao của khí đẩy (thuốc bọt, thuốc lỏng để xoa da, sirô thuốc và mỹ phẩ . m ..) Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung kiểu piston
Dạng thuốc khí dung chưa hoàn chỉnh
Không nén sẵn khí đẩy như thuốc hoàn chỉnh
Gắn van kiểu piston để người dùng tự bơm nén
không khí để đẩy thuốc
Khi nhấn, piston hoạt động như van một chiều chỉ cho
khí đi vào, sau vài lần ấn áp suất đạt tới mức nhất định, van m ở cho thuốc phun ra
Tiếp tục nhấn piston, chu kỳ phát thuốc được lặp lại Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung dùng quả bóp
Đựng trong đồ đựn g riêng Khi dùng thuốc đượ c cho vào một đầ u phun có
gắn quả bóp (bằng nhựa hoặc cao su)
Khi bóp, không khí sẽ nén với áp lực đủ đ ể đẩy thuốc ra khỏi đầu phun Đầu phun
Có hình dạng khác nhau, tùy trường hợp
cho thuốc qua miệng hoặc mũi...
Dụng cụ tạo khí dung cho cá nhân hay
được dùng trong bệnh viện bằng cách nối
chung với máy nén khí trị liệu khí dung
Thiết bị khác (máy rung động siêu âm, máy
dùng điện thế) tạo ra thuốc khí dung đ ể xông hít Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Yêu cầu chất lượng của thuốc thành phẩm
Đạt yêu cầu chất lượng theo chuyên luận riêng
Tiêu chuẩn áp dụng cho thuốc khí dung hoàn chỉnh gồm: Áp suất khí nén, c ỡ
hạt và phân bố c
ỡ hạt khi phun thuốc, khả năng phân liều của van, tốc độ phun
Đặc tính an toàn: Điểm bắt lửa của thuốc khi phun, khả năng chịu áp lực của bình, độ kín của bao bì
Nếu dung môi dùng trong khí dung có chứa ethanol thì phả ixây dựng tiêu chuẩn và
phương pháp định lượng hàm lượng ethanol trong thuốc
Thuốc thành phẩm phải đáp ứng các tiêu chuẩn chung về nồng độ, hàm lượng
hoạt chất,...
Thuốc khí dung phải được sản xuất trong điều kiện đảm bảo chất lượng chung và phù
hợp với đường sử dụng thuốc; phải kiểm tra giới hạn vi sinh vật. Thuốc sử dụng cho
vết thương phải vô khuẩn (Dược điển Việt Nam IV, phụ lục 13.6 “Thử giới hạ n nhiễm
khuẩn”, trang PL-258 và phụ lục 13.7 “Thử vô khuẩn”, trang PL-266). Chất liệu của đồ
đựng thuốc phải lựa chọn đúng quy định Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Chế phẩm đặc biệt đóng trong bình có áp suất cao
Nhiều phép thử cần thiết để đảm bảo an toàn cho quá trình bảo quả n và sử dụn g
Một số chỉ tiêu kiểm nghiệm về vật lý, hóa học và sinh học như sau
Điểm bắt lửa (nhiệt độ bốc cháy)
Áp suất khí nén (áp suất hơi)
Định tính và định lượng tỷ lệ các khí đẩy Tỷ trọng Độ ẩm
Diện tích nền phun (diện tích tiếp xúc của dòng khí dung)
Độ chính xác phân liều
Khối lượng trung bình của liều thuốc
Khối lượng thuốc không kể bì
Độ bền của bọt xốp
Kích thước tiểu phân
Độ kín của đồ đựng (tốc độ rò rỉ thuốc) Chất lượng của van Tốc độ phun thuốc
Các phép thử sinh học Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Điểm bắt lửa (nhiệt độ bốc cháy)
Điểm cháy của hầu hế tcác khí đẩ y
Được xác định bằn g dụn g cụ chuẩn
Đặt thuốc ở -25oC, sau đó đặt vào dụng cụ thử, chất lỏng trong dụng cụ được
tăng từ từ nhiệt độ đến khi hơi phun ra bốc cháy, nhiệt đ
ộ lúc này là điểm bắt lử a
Áp suất khí nén (áp suất hơi) Dùng áp kế có đầ u phù hợp với van đ ể xác định áp suất d ư trong bình
Định tính và định lượng tỷ lệ các khí đẩy Sắc ký khí Tỷ trọng
Phương pháp dùng picnomet (DĐVN IV, phụ lục 6.5, trang PL-148) Độ ẩm
Phương pháp Karl Fischer (DĐVN IV, phụ lục 10.3, trang PL-185) hoặ c
Phương pháp khác được qui định trong DĐVN IV, phụ lục 9.6, trang PL-182 Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Diện tích nền phun (diện tích tiếp xúc của dòng khí dung)
Đánh giá, so sánh sự phun thuốc có đồng nhất giữa các lô nguyên liệu khác nhau hoặc van ở các lô khác nhau Có ý nghĩa đặ c biệt khi dùng ngoài
Phun thuốc lên băng giấy quay có tẩm chất liệu màu để kiểm tra, so sánh diện tích và
độ đậm của khối lượng các tiểu phân phun ra
Độ chính xác phân liều
Theo nguyên tắc: một liều thuốc được phun vào dung môi hoặc vật liệu có khả năng hòa tan hay hấ
p thu dược chất, sau đó đem định lượng
Khối lượng trung bình của liều thuốc
Cân bình thuốc trước và sau khi phun một số liều
Hiệu số khối lượng hai lần cân là khối lượng thuốc tương ứng với liều thuốc
Suy ra khối lượng trung bình của liều thuốc
Chỉ cho biết lượng thuốc mỗi lần mở van đẩ y ra Lượn
g thuốc này có thể không được dẫ
n hoàn toàn vào nơi cần tác dụn g
Dùng dụng cụ hô hấ p nhân tạo đ
ể xác định liều thuốc được hấp thu đố ivới bệnh nhân Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Khối lượng thuốc không kể bì
Xác định trong quá trình đóng thuốc với các bình chứa đ ã cân bì sẵn Thành phẩ : m kiểm tra bằn g cách m
ở bình thuốc, loại bỏ hết thuốc và khí đẩy
Hiệu số khối lượng cân bình lúc chưa mở và bao bì bình thuốc sau khi mở là khối
lượng thuốc không kể bì
Độ bền của bọt xốp Nhớt kế quay
Đo thời gian nhúng sâu của vật nặn g vào khối bọ t
Thời gian để que thử rơi ra khỏi khối bọt Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Kích thước tiểu phân
Kính hiển vi, máy đế
m cho các dạng thuốc như thuốc bột, hỗ n dịch, … Áp dụn
g phân tích kích thước tiểu phân của thuốc khí dung
Kính hiển vi, máy đếm: có thể không xác định đúng đượ
c trạng thái phân tán ban
đầu của các tiểu phân thuốc phun ra khỏi bình do có sự tập hợp lại của các tiểu phân
khi phân tích ở trạng thái tĩnh
Dụng cụ phân tích kích thước tiểu phân theo tầng va chạm (cascade impactor) thích hợ
p dùng cho việc đánh giá kích thước khí động học (aerodynamic size) của
các tiểu phân thuốc khí dung Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Kích thước tiểu phân
Các tiểu phân thuốc khí dung
Lượng thuốc trên mỗi đĩa được định
lượng bằng UV-Vis, sắc ký thích hợ p Tầng 0
Sự phân bố khối lượng thuốc là một hàm Vòng đệm kín
số của đường kính khí động học của tiểu Đĩa gom giữ tiểu phân
phân, có thể được tính từ đường chuẩn cho Tầng đầu tiên các đĩa Đĩa gom tầng 2
Đường chuẩn cho từng đĩa đượ c lập từ Các tầng tiếp theo các thuốc khí dung đơ n phân tán trong điều Tầng cuối cùng
kiện chuẩn để biết cỡ kích thước tiểu phân Đĩa gom được gom trên đĩa Màng lọc
Dụng cụ thường phân tích các tiểu phân Dụng cụ phân tích kích
thuốc khí dung từ 0,1 m đế n 30 m
thước tiểu phân theo tầng Hút chân không Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Một số chỉ tiêu kiểm nghiệm
Độ kín của đồ đựng (tốc độ rò rỉ thuốc)
Điều kiện áp suất cao, khí đẩy có thể thoát ra, làm giảm khối lượng thuốc
Thử nghiệm với mẫu 12 bình, đặ ttrong điều kiện qui định trong 36 giờ Xác định s
ự giảm khối lượng thuốc trong mỗi giờ, suy ra phân xuất giảm trong 1 năm Yêu cầ u
Mức rò rỉ giới hạn nhỏ hơn hoặc bằng 3,5%/năm
Không có bình nào vượt qua 5%/năm
Thay phương pháp trên, tiến hành đơn giản hơn: dụng cụ đo khí rò rỉ (eudiometer)
Chất lượng của van
Được nhận xét qua tổng hợp các kết quả khả năng phân liều, độ mịn hạt, tốc độ phân thuốc,…
Tốc độ phun thuốc
Lấy 4 bình, phun thuốc trong 5 giây ở 25 1oC, tư thế bình đứn g
Cân bình, xác định lượng thuốc phát ra trong mỗi giây
Các phép thử sinh học
Định lượng sinh học, đánh giá hiệu lực điều trị, xác định độ độc được tiến hành nh ư các
chế phẩm thuốc thông thường Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung – Bảo quản – Nhãn thuốc
Phải để thuốc khí dung xa tầm tay trẻ em
Thuốc khí dung sử dụng khí đẩy hydrocarbon hoặc dẫn chất halogenohydrocarbon:
phải tuân thủ các quy định hiện hành
Thuốc khí dung thành phẩm
Dán nhãn có nộ idung phù hợp với quy chế chung
Cần có những lưu ý, cảnh báo riêng biệt cần thiết cho người sử dụng ở từng loại thuốc
khí dung như “Không được phun trực tiếp vào mắt hoặc niêm mạc”
Thuốc khí dung dùng để hít
Khi hít phải thận trọng, phải thực hiện theo những chỉ dẫn cần thiết của đơ n thuốc
hoặc hướng dẫn của thầy thuốc
Không nên tự dùng thuốc khí dung đ
ể hít nếu không được chỉ định vì có thể ngạt thở
hoặc nguy hiểm đến tính mạng
Thuốc khí dung là chế phẩm đóng gói khí nén ở áp suất cao
Không để gần lử a hoặc nhiệt đ ộ cao từ 500C trở lên Không đốt, không đ
è nén, không chọc vật nhọ n vào thuốc Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091)
Hỗn dịch được phân tán trong alcol và khí đẩy thích hợp
Đựng trong đồ chứa chịu được áp lực cao của khí đẩy
Chế phẩm phải đạt các yêu cầu qui định trong chuyên luận thuốc khí dung và
các yêu cầu sau đây Định tính
Hàm lượng alcol
Độ chính xác phân liều (Độ đồng đều hàm lượng của mỗi lần phun
thuốc hay khả năng phân liều của van)
Định lượng Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091) Định tính
Bản mỏng silicagel 0,25 mm (20 x 20 cm); Pha độn
g cloroform–aceton–nước (50:50:1)
Dung dịch mẫu thử
Hòa tan 3,1 g acid boric, 203 mg magnesi clorid và 860 mg natri hydroxyd trong
nước để thu được 1000 ml dung dịch
Hòa tan 50 mg phosphatase kiềm trong 50 ml dung dịch đệm ở trên (pH 9)
Hút chính xác 5 ml dung dịch thu được, cho vào một ống nghiệm 50 ml (có nắp đậy
thủy tinh) có chứa sẳn 5 ml dung dịch thử được chuẩn bị trong phép thử định lượng
Ủ ống nghiệm ở 37oC trong 45‟, lắc với 25 ml methylen clorid trong 2‟
Cách thủy đến cắn 15 ml dịch chiết CH . Hòa cắn 2Cl2 trong 1 ml CH2Cl2
Dung dịch mẫu đối chiếu: dung dịch chứa 300 g chất đối chiếu dexamethason trong 1 ml methylen clorid
Tiến hành: chấm mỗi dung dịch khoảng 5 l, khai triển sắc ký khoảng ¾ chiều dài bản. Phun dung dịch H 50% và 105 C cho khi màu nâu 2SO4 sấy o đến vết hoặc đen xuất hiện
Yêu cầu: dung dịch mẫu thử có vết chính tương ứn
g về màu sắc, vị trí và kích thước
với vết chính của dung dịch mẫu đối chiếu Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091)
Hàm lượng alcol
Áp dụng phương pháp sắc ký khí, thử theo chuyên luận chung
“Định lượng alcol”, phương pháp IIa, trang 225, USP 32 Yêu cầ u
Hàm lượng alcol trong chế phẩm không được nằm ngoài giới hạ n 1,7% - 2,3% ethanol Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091)
Độ chính xác phân liều
Dung dịch mẫ
u chuẩn: cân chính xác khoảng 10,0 mg dexamethason chuẩn, cho vào bình định
mức 10 ml, thêm alcol vừa đủ đến vạch, lắc đều. Hút chính xác 1 ml dung dịch thu được, cho vào
bình định mức 100 ml, thêm dung dịch H 0,1N
đến vạch, lắc đều. Dung dịch thu được 2SO4 vừa đủ
có nồng độ khoảng 10 g/ml
Dung dịch mẫu thử: phun một liều thuốc khuyến cáo thấp nhất vào trong dụng cụ lấy mẫu, sau
đó tháo chai thuốc ra khỏi dụng cụ lấy mẫu. Rửa dụng cụ lấy mẫu với dung dịch H 0,1N hai 2SO4
lần, mỗi lần 5 ml. Cho dịch rửa vào ống ly tâm 50 ml có chứa sẳn 15 ml methylen clorid đã được
làm lạnh vài phút trước đó trong buồng aceton lạnh và khô. Đậy nắp ống ly tâm, lắc đều, thỉnh
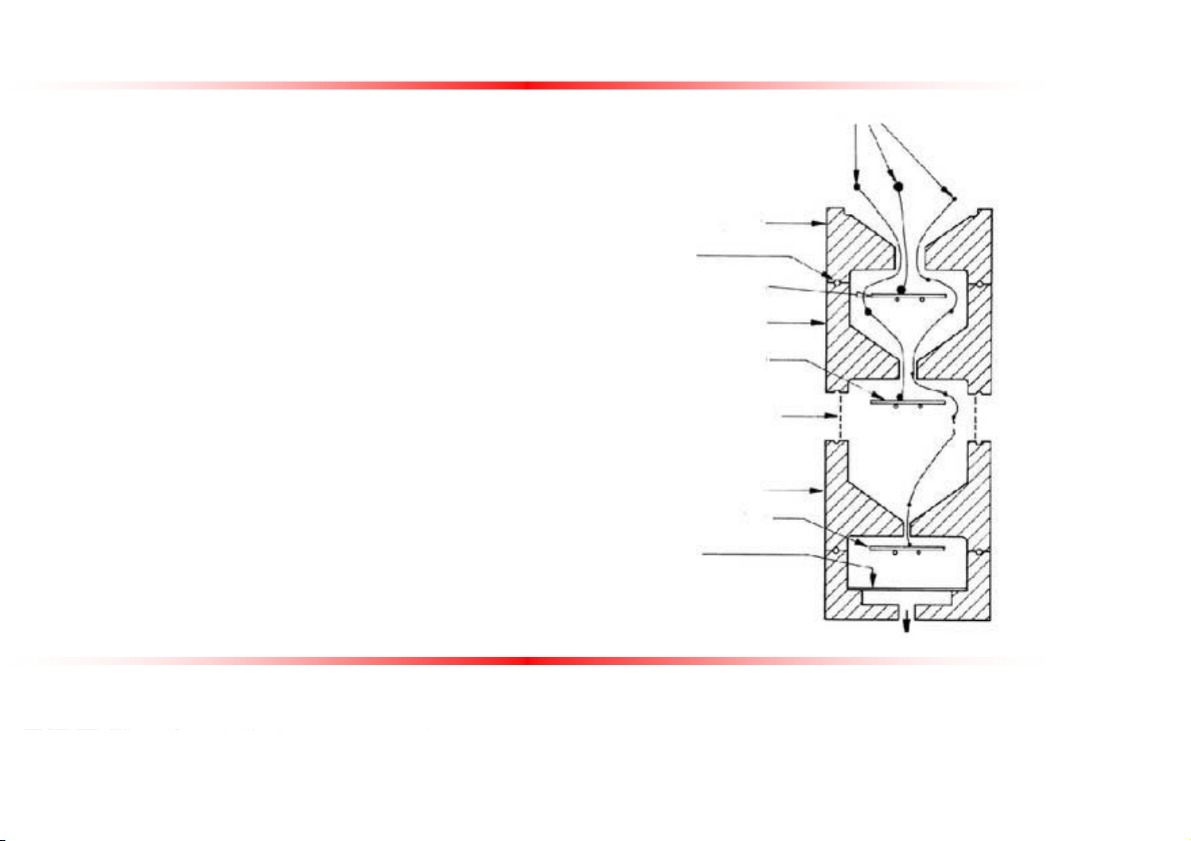
thoảng cân bằng áp suất bên ngoài. Để yên cho hai pha tách lớp hoàn toàn. Pha thân nước chính là dung dịch mẫu thử Giá lọc Thiết bị tiếp hợp Màng lọc với bộ phận tạo Khoen chữ O chân không Thiết bị tiếp hợp Nắp Ống
Dụng cụ lấy mẫu trong thử chứa
nghiệm độ chính xác phân liều mẫu Nắp
Đầu phun thuốc có van phân liều Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091)
Độ chính xác phân liều Tiến hành
Lần lượt thêm 2 ml dung dịch H
0,1N vào 10 ml dung dịch mẫu chuẩn và mẫu thử, 2SO4 lắc đều
Đo độ hấp thu hai dung dịch thu được ở bước sóng 239 nm, sử dụng H2SO4 0,1N làm mẫu trắng
Hàm lượng dexamethason phosphat ( g) trong mỗi liều phun thuốc thấp nhất được tính theo công thức :
X = 10(472,45/392,47)(CN)(A ) u/As Trong đó
X : hàm lượng dexamethason phosphat ( g).
472,45 và 392,47 lần lượt là PTL của dexamethason phosphat và dexamethason
C : nồng độ dung dịch mẫu chuẩn ( g/ml)
N : số lần phun thuốc để đạt được liều phun thuốc thấp nhất A và A u
s lần lượt là độ hấp thu của dung dịch mẫu thử và mẫu chuẩn Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091)
Độ chính xác phân liều Yêu cầ :
u Trong 10 liều phun thuốc đem thử của 1 đơn vị thành phẩ m
Có không quá một liều có hàm lượng dexamethason phosphat nằ m ngoài giới hạ n từ 75% đế n 125% và
Không có liều nào có hàm lượng nằ m ngoài giới hạ n từ 65% đế n 135% của hàm
lượng dexamethason phosphat qui định trong mỗi liều phun
Nếu hai hoặc ba liều có hàm lượng nằm ngoài giới hạn từ 75% đến 125%, nhưng ở
trong giới hạn từ 65% đến 135% của hàm lượng dexamethason phosphat qui định trong mỗi liều phun
Thử lại trên 2 đơn vị thành phẩm khác và tiếp tục thử nghiệm với 10 liều phun thuốc cho mỗi đơ n v ịthành phẩ m
Nếu có không quá 3 liều trong tổng số 30 liều đem thử có hàm lượng nằm
ngoài giới hạn từ 75% đế n 125% và
Không có liều nào có hàm lượng nằ
m ngoài giới hạn từ 65% đến 135% của
hàm lượng dexamethason phosphat qui định trong mỗi liều phun Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091) Định lượng
Dung dịch mẫ
u chuẩn: cân chính xác khoảng 40,0 mg dexamethason chuẩn, cho vào bình định
mức 50 ml, thêm alcol vừa đủ đến vạch, lắc đều. Hút chính xác 5 ml dung dịch thu được, cho vào
bình định mức 500 ml, thêm dung dịch H 0,1N
đến vạch, lắc đều. Dung dịch thu được 2SO4 vừa đủ
có nồng độ khoảng 8 g/ml
Dung dịch mẫu thử
Cân chính xác 1 đơn vị thành phẩm (khối lượng W gam), vào aceton và khô 1 đặt buồng lạnh
trong 60‟. Lấy thành phẩm ra khỏi buồng và tháo van phân liều ra bằng kìm cắt dây điện, giữ cẩn
thận các bộ phận đã tháo ra
Hòa tan thuốc trong đồ đựng bằng 20 ml dung dịch H 0,1N (được lần, 2SO4 chia làm 4 mỗi lần 5
ml). Cho dịch thu được vào cốc có mỏ đã được làm lạnh trước đó. Sấy khô đồ đựng và tất cả các
bộ phận ở 105oC trong 2 giờ, làm nguội và cân (khối lượng W gam) 2
Cốc có mỏ được làm ấm đến nhiệt độ phòng. Sau khi khí đẩy đã được bay hơi, cho dung dịch
trong cốc có mỏ vào bình định mức 200 ml, tráng cốc có mỏ bằng dung dịch H 0,1N, sau 2SO4 đó thêm H 0,1N 2SO4
vừa đủ tới vạch, lắc đều
Cho 20 ml dung dịch thu được vào một ống ly tâm, thêm 10 ml methylen clorid, lắc kỹ trong 1
phút và ly tâm. Hút chính xác 10 ml dịch ly tâm, cho vào bình định mức 100 ml, thêm H 0,1N 2SO4
vừa đủ tới vạch, lắc đều Nguyễn Đức Tuấn Đại học Y Dược TPHCM
Thuốc khí dung để hít dexamethason natri phosphat (USP 32, trang 2091) Định lượng Tiến hành
Đo độ hấp thu dung dịch mẫu chuẩn và mẫu thử ở bước sóng 239 nm, sử dụng H 2SO4 0,1N làm mẫu trắng
Hàm lượng dexamethason phosphat (mg) trong một gam chế phẩ m được tính theo công thức
C = 2(472,45/392,47)(Au/A )[C/(W -W s 1 2)] Trong đ ó
C : hàm lượng dexamethason phosphat (mg)
472,45 và 392,47 lần lượt là PTL của dexamethason phosphat và dexamethason C : nồng đ
ộ dung dịch mẫu chuẩn ( g/ml) A và A u
s lần lượt là độ hấp thu của dung dịch mẫu thử và mẫu chuẩn Yêu cầ u
Hàm lượng dexamethason natri phosphat trong chế phẩ m không được nằ m ngoài giới hạn
90% - 110% so với hàm lượng qui về dexamethason phosphat ghi trên nhãn Nguyễn Đức Tuấn Đại học Y Dược TPHCM