












Preview text:
SƠ LƯỢC VỀ PHỨC CHẤT
A. TÓM TẮT LÝ THUYẾT I. KHÁI NIỆM
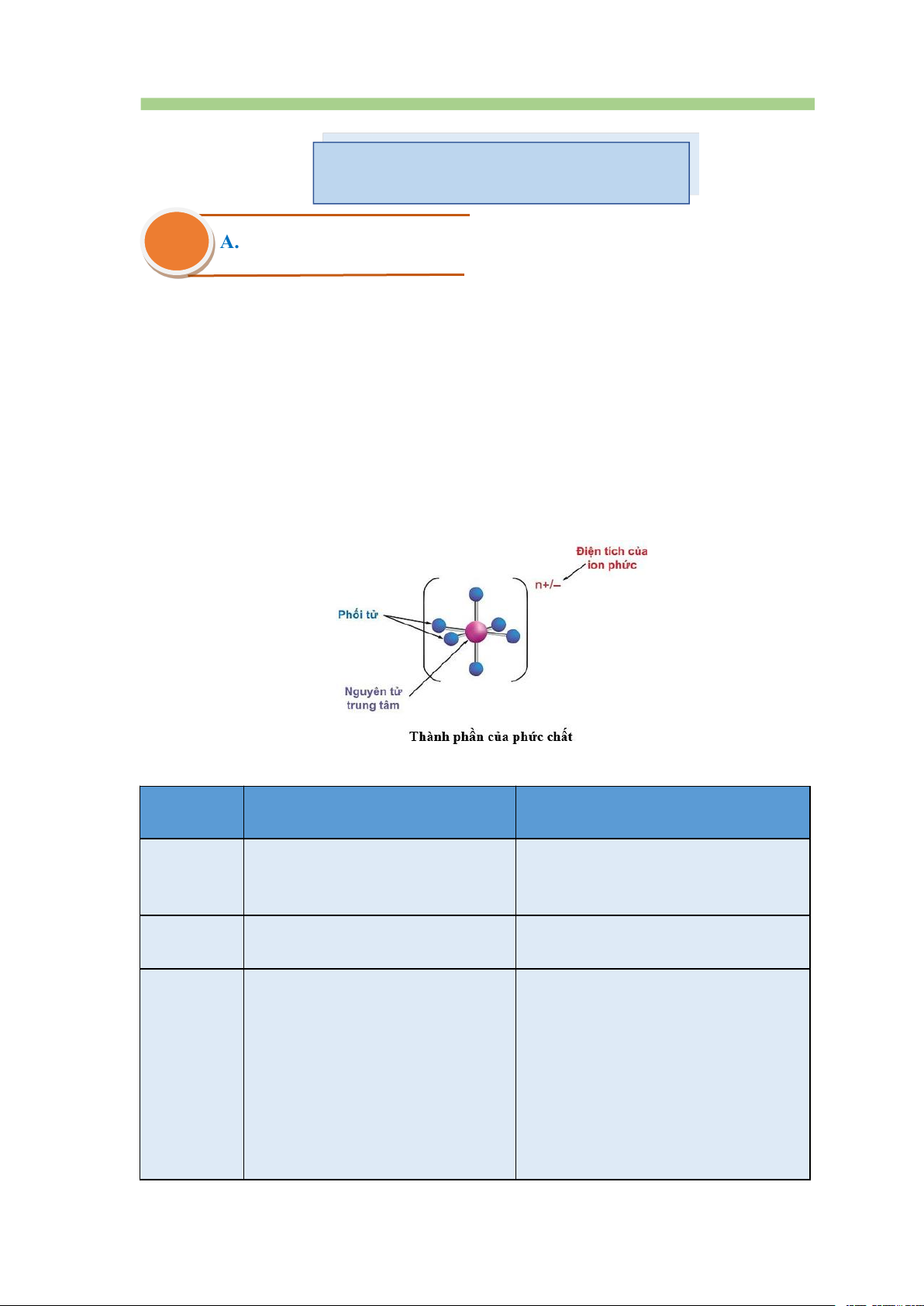
Phức chất đơn giản thường có một nguyên tử trung tâm liên kết với các phối tử
bao quanh, được đặt trong dấu ngoặc vuông. Liên kết giữa nguyên tử trung tâm và
phối tử trong phức chất là liên kết cho – nhận.
Phối tử là phân tử hoặc anion đã cho cặp electron chưa liên kết (hay cặp electron hoá trị riêng).
Nguyên tử trung tâm là cation kim loại hoặc nguyên tử kim loại có orbital trống đã
nhận cặp electron chưa liên kết của phối tử. Một số ví dụ: Phức chất [Ag(NH3)2]+ [CoF6]3- Nguyên tử trung tâm Ag+ Co3+ Phối tử NH3 F−
Giải thích Liên kết trong phức chất Liên kết trong phức chất [CoF6]3-
sự hình [Ag(NH3)2]+ được hình thành do được hình thành do phối tử F- cho
thành liên phối tử NH3 cho cặp electron cặp electron chưa liên kết vào AO
kết trong chưa liên kết vào AO trống của trống của nguyên tử trung tâm
phức chất nguyên tử trung tâm Ag+. Co3+. Chú ý:
+ Trong thực tế, có những phức chất có nhiều hơn một nguyên tử trung tâm; có
những phức chất chỉ có một phối tử.
+ Theo IUPAC, khi viết công thức hoá học của phức chất, nên hướng nguyên tử
cho cặp electron hoá trị riêng trong phối tử về phía nguyên tử trung tâm.
Ví dụ, nên viết [Fe(OH2)6]2+ thay vì [Fe(H2O)6]2+.
II. MỘT SỐ DẠNG HÌNH HỌC CỦA PHỨC CHẤT
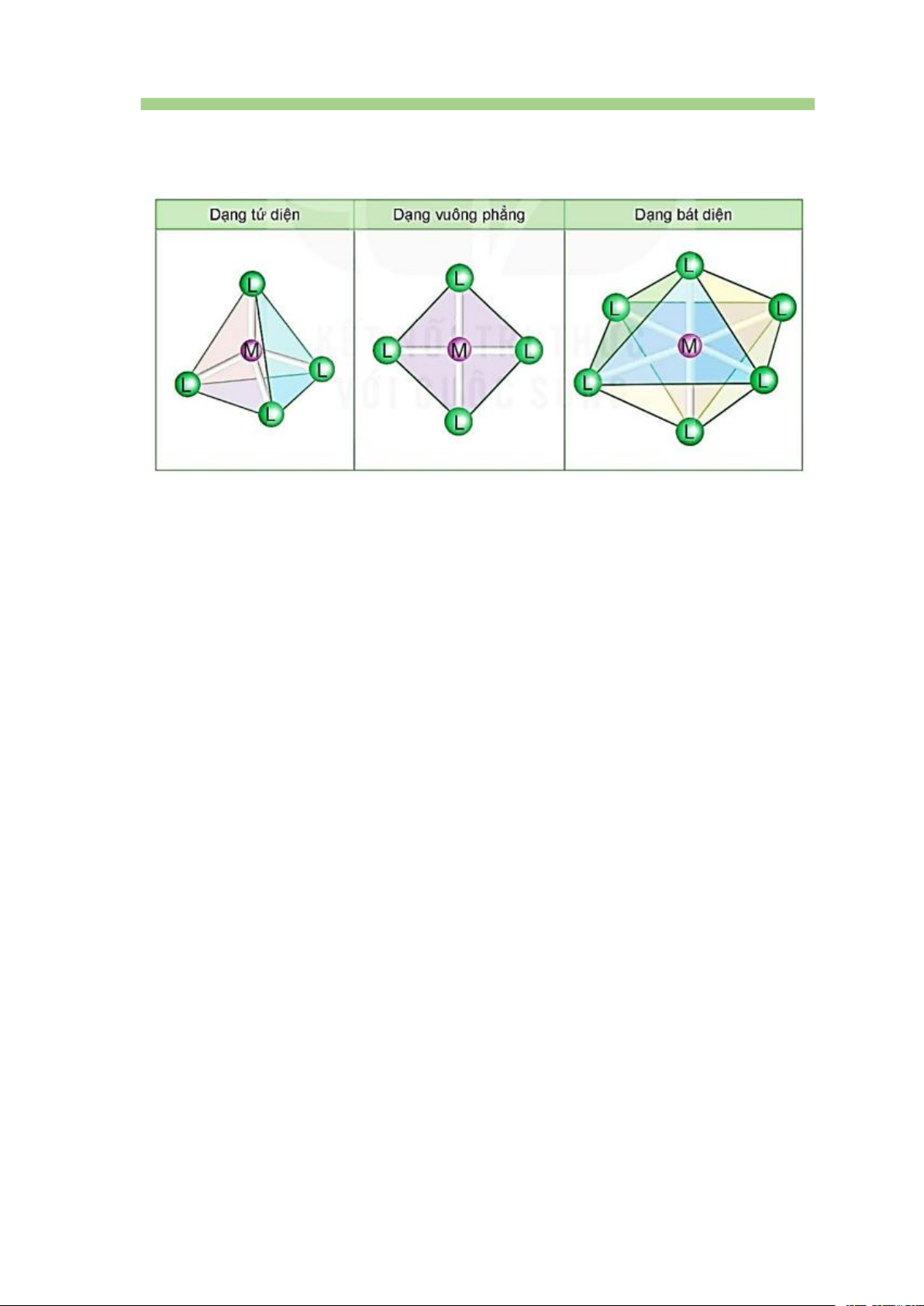
Trong phức chất [MLn] (điện tích đã được lược bỏ), các phối tử L sắp xếp xác
định xung quanh các nguyên tử trung tâm M tạo ra các dạng hình học khác nhau,
phổ biến nhất là dạng tứ diện, vuông phẳng và bát diện.
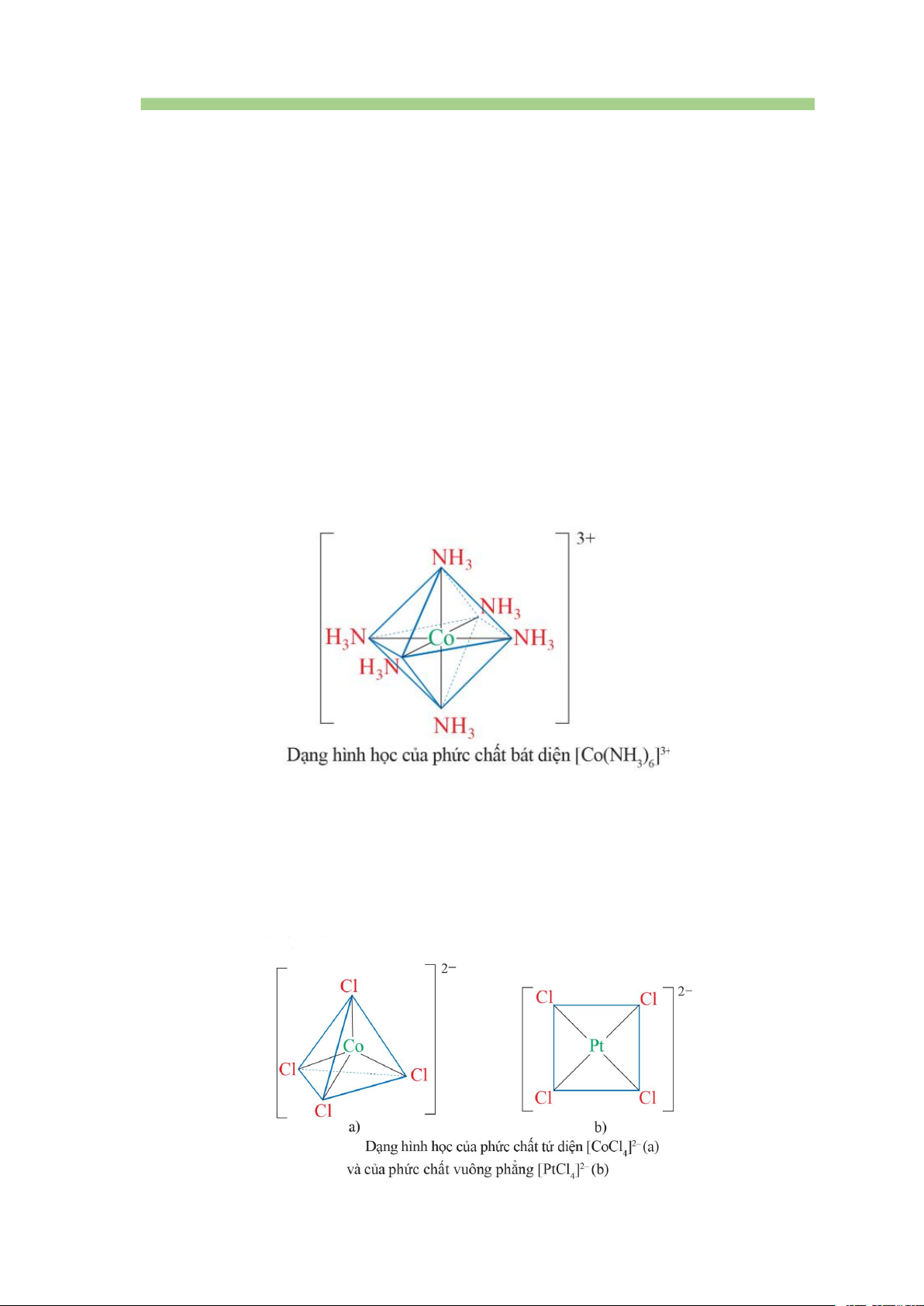
Ví dụ: [Co(NH3)6]3+ là phức chất bát diện, với dạng hình học như sau:
Trong phức chất này, các phối tử chiếm vị trí 6 đỉnh, còn nguyên tử trung tâm
nằm ở tâm của hình bát diện.
Phức chất [CoCl4]2- là phức chất tứ diện (a); phức chất [PtCl4]2- là phức chất vuông phẳng (b):
Một số dạng hình học phổ biến của phức chất [MLn]
III. SỰ HÌNH THÀNH PHỨC CHẤT CỦA ION KIM LOẠI CHUYỂN TIẾP TRONG DUNG DỊCH
1. Sự hình thành phức chất aqua của kim loại chuyển tiếp trong dung dịch
Khi tan trong nước, muối của các kim loại chuyển tiếp phân li thành các ion. Sau
đó, cation kim loại chuyển tiếp (Mn+) thường nhận các cặp electron hoá trị riêng từ
các phân tử H2O để hình thành các liên kết cho – nhận, tạo ra phức chất aqua. Phương trình tổng quát: n
M (aq) mH O(l)
[M (OH ) ]n aq m ( ) 2 2 Với:
+ n là giá trị điện tích của cation kim loại M. + m là số phối tử H2O.
+ [M(OH2)m]n+ là công thức tổng quát của phức chất aqua của Mn+.
- Ví dụ: Khi cho copper(II) sulfate vào nước thì hình thành phức chất bát diện với
các phối tử là 6 phân tử H₂O. Theo phương trình:
Cu2+(aq) + 6H2O(l) → [Cu(OH2)6]2+(aq)
2. Dấu hiệu của phản ứng tạo phức chất trong dung dịch
Các phản ứng tạo thành phức chất thường có một số dấu hiệu dễ quan sát như: sự
biến đổi màu sắc (phổ biến nhất), sự hoà tan, sự kết tủa … Ví dụ: Quá trình
Dấu hiệu tạo thành phức chất Sản phẩm Cho nước vào ống nghiệm
Chất rắn màu trắng bị hoà tan, 2
[Cu(OH ) ] (aq) chứa CuSO
tạo thành dung dịch có màu 2 6 4 khan, màu trắng. xanh.
Thêm tiếp vài giọt dung Xuất hiện kết tủa màu xanh [Cu(OH) (OH ) ](s) dịch ammonia. nhạt. 2 2 4
Thêm tiếp ammonia đến Kết tủa màu xanh nhạt bị hoà 2
[Cu(NH ) (OH ) ] (aq) dư
tan, dung dịch chuyển từ màu 3 4 2 2
xanh nhạt sang màu xanh lam.
3. Phản ứng thay thế phối tử trong phức chất
- Ở những điều kiện phù hợp, các anion và phân tử như OH-, X- (halide), NH3 …
có thể trở thành phối tử để thay thế một, một số hoặc tất cả các phối tử trong phức chất.
- Sự thay thế phối tử thường tạo thành phức chất bền hơn so với phức chất ban đầu. Ví dụ:
[Ni(OH2)6]2+(aq) + 6NH3(aq) → [Ni(NH3)6]2+ (aq) + 6H2O (l)
4. Ứng dụng của phức chất
Xác định hàm lượng cation kim loại chuyển
Ứng dụng dựa vào phản ứng tiếp trong dung dịch tạo phức chất
Hấp thụ và loại bỏ các cation kim loại nặng,
độc ra khỏi cơ thể ở dạng phức chất
Làm vật liệu, chất tạo màu trong sản xuất
Ứng dụng dựa vào đặc điểm, Làm thuốc, chất dinh dưỡng
tính chất của phức chất
Làm chất chỉ thị màu cho các quá trình phản
ứng, xúc tác cho một số phản ứng
B. CÂU HỎI LUYỆN TẬP
PHẦN I. CÂU HỎI TRẮC NGHIỆM KHÁCH QUAN
Câu 1. Thành phần của phức chất gồm có
A. nguyên tử trung tâm. B. phối tử.
C. phân tử trung tâm và phối tử.
D. nguyên tử trung tâm và phối tử.
Câu 2. Phần tử có thể trở thành phối tử trong phức chất là
A.Anion hoặc phân tử trung hòa có cặp electron hóa trị riêng.
B. Anion có kích thước lớn.
C.Phân tử trung hòa có hoặc không có cặp electron hóa trị riêng.
D.Cation kim loại chuyển tiếp có các orbital trống.
Câu 3. Phần tử có thể trở thành nguyên tử trung tâm trong phức chất khi chúng
sử dụng các orbital trống để nhận cặp electron hóa trị riêng từ phối tử. Các phần tử đó là
A.Tất cả các cation kim loại.
B. Nguyên tử hoặc cation của một số kim loại.
C.Các nguyên tử nguyên tố chuyển tiếp dãy thứ nhất.
D.Các cation kim loại của nguyên tố chuyển tiếp dãy thứ nhất.
Câu 4. Cho phát biêu sau: “Phức chất đơn giản thường cỏ một . .(1). . lièn kết
với các phối tử bao quanh. Liên kết giữa nguyên từ trung tâm và phôi tử trong
phức chất là liên kết . .(2) ”.
Cụm từ cần điền vào (1) và (2) lần lượt là
A.Cation kim loại, ion.
B. Nguyên từ kim loại, cho - nhận.
C. Nguyên từ trung tâm, cho - nhận. D. Phối tử, ion.
Câu 5. Nguyên tử trung tâm của các phức chất [PtCl4]2- và [Fe(CO)5] lần lượt là A. Pt4+ và Fe2+. B. Pt2+ và Fe2+. C. Cl và CO. D. Pt2+ và Fe.
Câu 6. Để trở thành phối từ trong phức chất thì phân tư hoặc anion cần có
A. Các orbital trống.
B. Cặp electron hoá trị riêng.
C. Ít nhất 4 orbital trống.
D. Ít nhất hai cặp electron hoá trị riêng.
Câu 7. Theo thuyết Liên kết hóa trị, tương tác giữa phối tử và nguyên tử trung tâm trong phức chất là
A. Liên kết cộng hóa trị kiểu cho – nhận. B. Liên kết ion.
C. Tương tác van der Waals.
D. Liên kết hydrogen.
Câu 8. Khi hòa tan hợp chất CoCl2 vào nước thì hình thành phức chất aqua có
dạng hình học là bát diện. Công thức của phức chất đó là A. [Co(OH2)6] 3+. B. [Co(OH2)6]2+.
C. [CoCl2(OH2)4]. D. [CoCl2(OH2)4]2+.
Câu 9. Số oxi hoá của nguyên tử trung tâm trong phức chất [RhCl(NH3)5](NO3)2 là A. +3. B. 0. C. +4. D. +2.
Câu 10. Phức chất nào sau đây chứa ion phức có số phối trí là 4? A.[Zn(NH3)4]2+. B.[Ag(NH3)2]+. C.[Co(NH3)6]3+. D.[Ni(CN)4]2-
Câu 11. Trong phức chất [Cr(H2O)6]Cl3, ion phức có dạng hình học gì? A. Hình vuông. B. Lập phương. C. Hình bát diện. D. Hình tứ diện
Câu 12. Trong phức chất [Zn(NH3)4]2+, ion phức có dạng hình học gì? A. Hình vuông. B. Lập phương. C. Hình bát diện. D. Hình tứ diện.
Câu 13. Phức chất nào sau đây có cấu trúc tứ diện? A. [Pt(NH3)4]2+. B. [Zn(NH3)4]2+. C.[Fe(H2O)6]+. D. [Co(H2O)6]3+.
Câu 14. Phức chất nào sau đây có dạng bát diện? A. [PtCl4]2-. B. [Ni(NH3)4]2+. C. [Co(NH3)6]3+. D. [Ag(NH3)2]+.
Câu 15. Phức chất nào sau đây có dạng vuông phẳng là A. [Cu(NH3)4]2+. B. [Zn(NH3)4]2+. C. [Fe(H2O)6]+. D. [Co(H2O)6]3+.
Câu 16. Khi phức chất tạo thành sẽ không có hiện tượng nào? A. Khí thoát ra.
B. Sự thay đổi màu sắc.
C. Sự xuất hiện kết tủa.
D. Kết tủa bị hòa tan.
Câu 17. Mô tả nào không đúng khi nói về phức chất [Co(NH3)6]3+?
A. Có điện tích +3.
B. Nguyên tử trung tâm là Co. C. Phối tử là NH3.
D. Số phối tử là 6.
Câu 18. Mô tả nào không đúng khi nói về phức chất [Zn(OH)4]2-?
A. Có điện tích -2.
B. Nguyên tử trung tâm là Zn2+. C. Phối tử là H2O.
D. Số phối tử là 4.
Câu 19. Mô tả nào không đúng khi nói về phức chất [Fe(CO)5]?
A. Không mang điện tích.
B. Nguyên tử trung tâm là Fe2+. C. Phối tử là CO.
D. Số phối tử là 5.
Câu 20. Phức chất nào có màu xanh lam đặc trưng? A. [Ni(NH3)6]2+ B. [Co(NH3)6]3+ C. [Fe(CN)6]3- D. [Cu(NH3)4]2+
Câu 21. Phức chất [Co(NH3)6]3+ có màu: A. Hồng đỏ. B. Vàng nâu. C. Xanh tím. D. Lục nhạt.
Câu 22. Hemoglobin trong máu gồm ion M2+ liên kết với popyrin và một phân tử
protein có tên globin tạo thành phức chất bát diện, phức này có nhiệm vụ vận
chuyển oxygen từ phổi đến các mô và CO2 từ các mô về phổi. M là kim loại: A. Fe. B. Pb. C. Co. D. Ni.
Câu 23. Cho carbon monoxide liên tục đi qua nickel (Ni) nung nóng ở 800C.
thu được phức chất [Ni(CO)4] ở thể khí. Tiếp tục dẫn [Ni(CO)4] qua khu vực có
nhiệt độ khoảng 1000C, phức chất [Ni(CO)4] phân huỷ thu được nickel tinh khiết.
Quá trình này được ứng dụng đã tinh chế nickel. Số oxi hoá của nickel trong phức chất [Ni(CO)4] là A. +2. B. +1. C. -1. D. 0.
Câu 24. Công thức feroxen hay bicyclopentadienyl có dạng M(C5H5)2 được dùng
làm thuốc chữa bệnh thiếu máu. Kim loại M trong công thức trên là A. Fe. B. Cu. C. Co. D. Ni.
Câu 25. Dạng hình học của phức chất [Ni(CN)4]2- là A. Tứ diện. B. Vuông phẳng C. Hình vuông D. Bát diện
Câu 26. Phức chất [Fe(CN)6]4- không có các tính chất nào sau đây?
A. Sắt có số oxi hóa là +2.
B. Phức chất này bền vững.
C. Số phối tử của sắt là 6.
D. Phức chất này có tính oxi hóa mạnh.
Câu 27. Chất nào sau đây có thể tạo phức với NH3? A. NaCl. B. K2SO4. C. CuSO4. D. Ba(NO3)2.
Câu 28. Phức chất [Cu(NH3)4]2+ không có tính chất nào sau đây?
A. Cu có số oxi hóa +2.
B. Có dạng hình học tứ diện C. Có màu xanh lam.
D. Số phối tử của Cu là 4.
Câu 29. Ứng dụng không phải của phức chất [Cu(NH3)4(OH2)2]2+ là
A. Xác định sự có mặt hàm lượng cation Cu2+ trong dung dịch dựa vào phản
ứng tạo phức chất [Cu(NH3)4(OH2)2]2+ có màu xanh lam.
B. Dùng để tinh chế và phân tích trọng lượng phân tử của cellulose do có khả năng hòa tan cel ulose.
C. Dùng làm thuốc chữa bệnh thiếu máu.
D. Làm chất tạo màu, thuốc nhuộm vải do có màu xanh lam đặc trưng.
Câu 30. Phức Na3[Co(NO3)6] được sử dụng nhiều trong phòng thí nghiệm để nhận
biết một số cation kim loại Những phát biểu nào sau đây về phức chất Na3[Co(NO3)6] là đủng?
A. Có liên kết cho - nhận và liên kết ion trong phân tử.
B. Phức có dạng hình học là tứ diện
C. Có nguyên tử trung tâm là natri (sodium) và cobalt.
D. Nguyên từ trung tâm có số oxi hoá là +2.
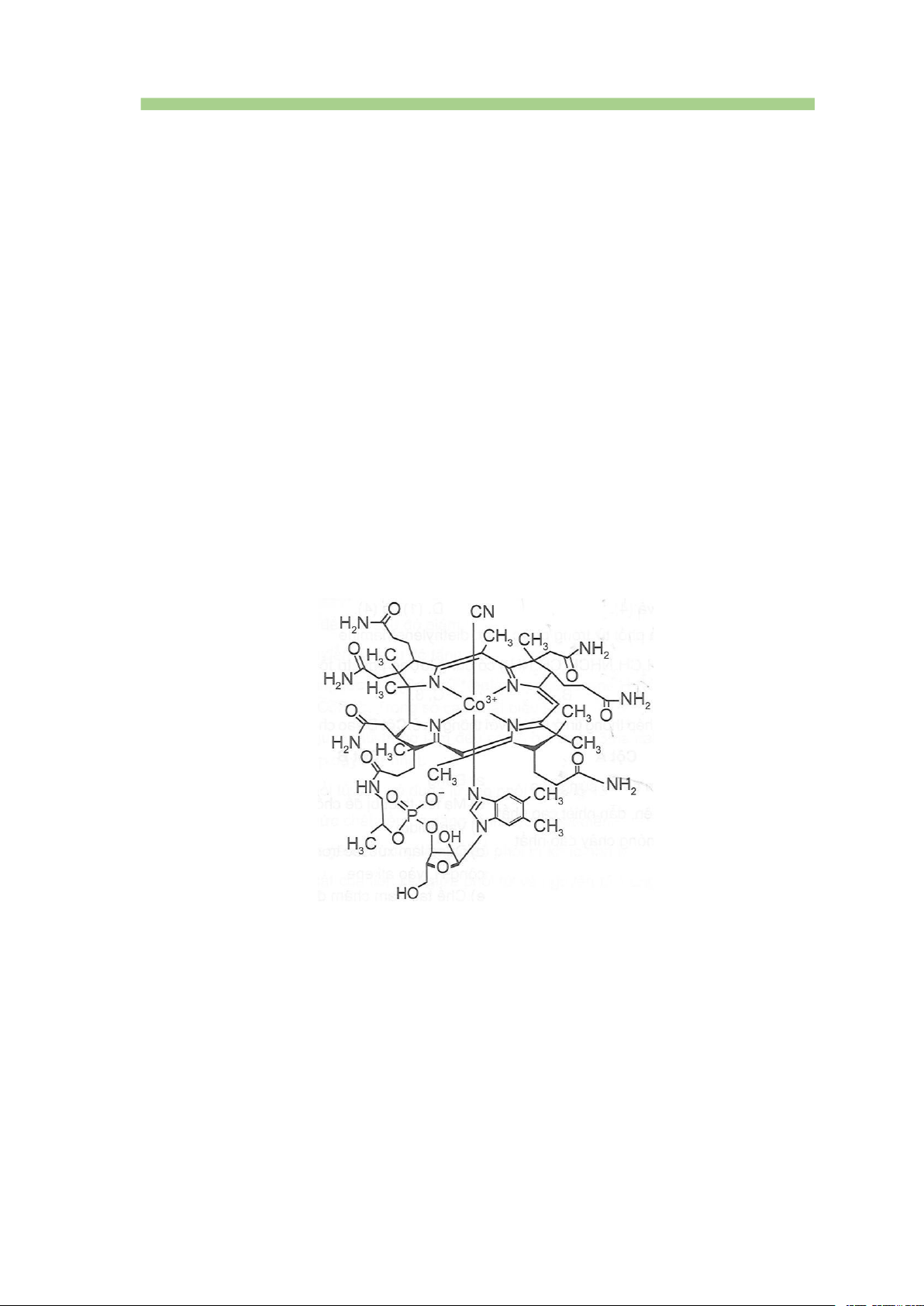
Câu 31. Quan sát CTCT của vitamin B2 cho ở dưới đây nhận xét nào là sai.
A. Vitamin B2 là phức chất do có ion trung tâm và phối tử
B. Ion trung tâm là Co3+, phối tử là các nguyên tử N
C. Ion trung tâm có dạng hình học bát diện
D. liên kết giữa ion Co3+ và các phối tử là liên kết cho - nhận
Câu 32. CuSO4 khan màu trắng, khi hoà tan trong nước, các phân tử nước liên
kết với ion Cu2+ tạo phức chất aqua [Cu(H2O)6]2+. Dấu hiệu nào chứng tỏ phức
chất aqua được tạo thành?
A. Có sự thay đổi màu sắc từ trắng thành xanh nhạt.
B. Có sự thay đổi màu sắc từ trắng thành xanh lam.
C. Có kết tủa màu xanh tạo thành.
D. Có sự thay đổi màu sắc từ trắng thành vàng.
Câu 33. Phản ứng nào dưới đây không phải là phản ứng thay thế phối tử trong phức chất?
A. [Co(OH2)6]3+(aq) + 6NH3(aq) ⟶[Co(NH3)6]3+(aq) + 6H2O(l)
B. 2Na[Au(CN)2](aq) + Zn(s) ⟶ Na2[Zn(CN)4](aq) + 2Au(s)
C. [Co(OH2)6]2+(aq) + 4Cl−(aq) ⇌ [CoCl4]2−(aq) + 6H2O(l)
D. [Ni(OH2)6]2+(aq) + 6NH3(aq) ⇌ [Ni(NH3)6]2+(aq) + 6H2O (l)
Câu 34. Khi cho dung dịch ammonia dư vào dung dịch chứa phức chất
[Ni(OH2)6]2+ và anion Cl- thì có phản ứng sau:
[Ni(OH2)6]2+(aq) + 6NH3(aq) ⇌ [Ni(NH3)6]2+(aq) + 6H2O (l) (*)
Phát biểu nào dưới đây là không đúng?
A. Trong điều kiện của phản ứng (*), phức chất [Ni(NH3)6]2+(aq) kém bền
hơn phức chất [Ni(OH2)6]2+(aq).
B. Phản ứng (*) là phản ứng thế phối tử.
C. Dung dịch sau phản ứng có pH > 7.
D. Trong phản ứng không có sự thay đổi số oxi hoá của các nguyên tố.
Câu 35. M là kim loại chuyển tiếp dãy thứ nhất. Phát biểu nào dưới đây không đúng?
A. Trong nước, cation của kim loại M (có hoá trị n) thường tồn tại ở dạng phức chất aqua [M(OH2)6]n+.
B. Các phức chất aqua [M(OH2)6]n+ thường có màu.
C. Trong nhiều phức chất aqua [M(OH2)6]n+, số phối tử thường là 6 .
D. Phức chất aqua [M(OH2)6]n+ không tan trong nước.
Câu 36. Phát biểu nào sau đây về phức chất bát diện [Cu(OH2)6]2+ không đúng?
A. Nguyên tử trung tâm được hình thành từ quá trình cation Cu2+ sử dụng 6 orbital
trống để nhận các cặp electron hoá trị riêng của các phân tử H2O.
B. Số oxi hoá của nguyên tử trung tâm là +2 .
C. Số liên kết cho - nhận giữa phối tử và nguyên tử trung tâm cũng là hoá trị phổ biến của đồng.
D. Mỗi phân tử nước chỉ sử dụng 1 cặp electron chưa liên kết của nó để tạo liên kết
cho - nhận với cation Cu2+.
Câu 37. Những phát biểu nào dưới đây không đúng?
A. Phản ứng tạo thành phức chất thường kèm theo sự biến đổi về màu sắc, sự xuất
hiện kết tủa, hòa tan kết tủa.
B. Phức chất tạo thành phải bền hơn so với chất tham gia phản ứng.
C. Quá trình hoà tan copper(II) chloride trong nước có diễn ra phản ứng hình thành phức chất.
D. Quá trình hoà tan potassium permanganate KMnO4 trong nước có diễn ra phản
ứng hình thành phức chất.
Câu 38. Phát biểu nào sau đây không đúng về phức chất?
A. Phức chất đơn giản thường có một nguyên từ trung tâm liên kết với các phối tử bao quanh.
B. Phức chất có thể mang điện tích hoặc không mang điện tích.
C. Liên kết giữa nguyên tử trung tâm và phối tử trong phức chất là liên kết ion.
D. K2[PtCl4] hoặc anion [PtCl4]2- đều được xếp vào loại phức chất.
Câu 39. Cho các chất có công thức: CuCl2, NH3, [CuCl4]2- . Phát biểu nào sau đây là không đúng?
A. Do không có liên kết cộng hoá trị theo kiểu cho - nhận trong phân tử nên CuCl2
không phải là phức chất.
B. Do có nguyên tử trung tâm là nguyên tố kim loại, đồng thời các phối tử xung
quanh liên kết với nguyên tử trung tâm bằng liên kết cho - nhận nên [CuCl4]2- là phức chất.
C. Dù có các nguyên tử H xung quanh N, nhưng NH3 không phải là phức chất.
D. Do nguyên tố đồng có hoá trị II nên quanh nguyên tử Cu trong CuCl2 và trong
[CuCl4]2- đều có 2 liên kết.
Câu 40. Chọn phát biểu đúng để giải thích sự hình thành liên kết trong phức [Ag(NH3)2]+
A. Liên kết trong phức chất [Ag(NH3)2]+ được hình thành do phối tử NH3 cho cặp
electron chưa liên kết vào AO trống của nguyên tử trung tâm Ag+
B. Liên kết trong phức chất [Ag(NH3)2]+ được hình thành do phối tử NH3 cho cặp
electron đã liên kết vào AO trống của nguyên tử trung tâm Ag+
C. Liên kết trong phức chất [Ag(NH3)2]+ được hình thành do phối tử NH3 tạo liên
kết ion với nguyên tử trung tâm Ag+
D. Liên kết trong phức chất [Ag(NH3)2]+ được hình thành do nguyên tử trung tâm
Ag+ cho cặp electron chưa liên kết vào AO trống của phối tử NH3
NỘI DUNG CÂU HỎI SBT
Câu 1. [CTST - SGK] Trong phức chất, giữa phối tử và nguyên tử trung tâm có
loại liên kết nào sau đây ? A. Ion. B. Hydrogen. C. Cho-Nhận. D. Kim loại.
Câu 2. [CTST - SBT] Nhận xét nào sau đây là không đúng?
A.Nguyên tử trung tâm chỉ có thể là cation kim loại.
B. Thành phần của phức chất có nguyên tử trung tâm và phối tử.
C.Phối tử còn cặp electron chưa liên kết, có khả năng cho nguyên tử trung tâm.
D.Liên kết giữa phối tử và nguyên tử trung tâm là liên kết cho – nhận.
Câu 3. [CTST - SBT] Nhận định nào sau đây là đúng?
A.Phức chất chỉ có dạng hình học là bát diện.
B. Phức chất luôn chứa cầu ngoại.
C.Phức chất có các dạng hình học khác nhau.
D.Một phức chất có thê tồn tại ở các dạng hình học khác nhau.
Câu 4. [CTST - SBT] Cho các nhận định sau:
(1) Kiểu lai hoá của nguyên tử trung tâm sẽ quyết định dạng hình học của phức chất.
(2) Cation Ni2+ chỉ có thế tạo phức chất bát diện.
(3) Cầu nội của phức chất có thể mang điện tích dương, âm hoặc không.
(4) Phối tử chỉ có thể là anion hoặc phân tử trung hoà.
(5) Cầu ngoại của phức chất thường mang điện tích âm.
(6) Nguyên tử trung tâm là các nguyên tố nhóm Ba
(7) Phức chất có các dạng hình học phổ biến là tứ diện, vuông phẳng và bát diện.
(8) Nguyên tử trung tâm không thể là các nguyên tố phi kim. Số nhận định đúng là A. 2. B. 3. C. 4. D. 5.
Hướng dẫn trả lời
Các nhận định đúng là:
(1) Kiểu lai hoá của nguyên tử trung tâm sẽ quyết định dạng hình học của phức chất.
(3) Cầu nội của phức chất có thể mang điện tích dương, âm hoặc không.
(7) Phức chất có các dạng hình học phổ biến là tứ diện, vuông phẳng và bát diện.
Câu 5. [CTST - SBT] Với phối tử Cl- , tất cả các ion nào sau đây sẽ là nguyên tử
trung tâm trong phức chất tứ diện? A. Cu2+, Ni2+, Mn2+. B. Fe3+, Cr3+, Co3+. C. Cr3+, Co3+, Sc3+. D. Ni2+, Cu2+, Zn2+.
Câu 6. [CTST - SBT] Dung dịch phức chất aqua không thể có màu xanh là A. [Cr(H₂O)6]3+. B. [Zn(H₂O)6]2+. C. [Ni(H₂O)6]2+. D. [Cu(H₂O)6]2+.
Câu 7. [CTST - SBT] Phức chất nào sau đây có dạng hình học không phải là tứ diện? A. [CuCl4]2-. B. [CoCl4]2-. C. [PdCl4]2-. D. [FeCl4]-.
Câu 8. [CTST - SBT] Nhỏ từng giọt dung dịch sodium hydroxide cho đến dư vào
dung dịch aluminium chloride, dấu hiệu chứng tỏ đã tạo ra phức chất chứa phối từ OH- là
A. kết tủa bị hoà tan
B. dung dịch bị chuyên từ không màu sang có màu.
C. kết tủa keo trắng tạo thành.
D. dung dịch bị mất màu.
Hướng dẫn trả lời PTHH:
3NaOH + AlCl3→ 3NaCl + Al(OH)3↓ Al(OH)3 + NaOH → Na[Al(OH)4]
Al(OH)3 là kết tủa keo trắng. Khi tạo phức, kết tủa Al(OH)3 tan, tạo dung dịch Na[Al(OH)4] không màu.
Câu 9. [CTST - SBT] Phức chất có dạng hình học không phải tứ diện là A. [CoBr4]2-. B. [PtBr4]2-. C. [AI(OH)4]-. D. [FeCl4]-.
Câu 10. [CTST-SBT] Cho các phức chất: [Cr(en)3]3+ (en là ethylenediamine,
H2NCH2CH2NH2), [Ti(H2O)6]3+, [CoF6]3-. Trong số các phát biểu sau:
(1) Các nguyên tử trung tâm đều có số oxi hóa +3, là cation kim loại chuyển tiếp dãy thứ nhất.
(2) Các phối tử đều có dung lượng phối trí bằng 1.
(3) Các phức chất đều có dạng hình học là bát diện.
(4) Các nguyên tử trung tâm có số phối trí khác nhau.
(5) Bản chất của liên kết giữa phối tử và nguyên tử trung tâm đều là liên kết cho − nhận.
(6) Liên kết cho − nhận là các liên kết σ. A. 1. B. 2. C. 3. D. 4.
Hướng dẫn trả lời (1) Đúng.
(2) Sai vì phối tử ethylenediamine có dung lượng phối trí bằng 2. (3) Đúng.
(4) Sai vì các nguyên tử trung tâm có số phối trí bằng 6. (5) Đúng. (6) Đúng.
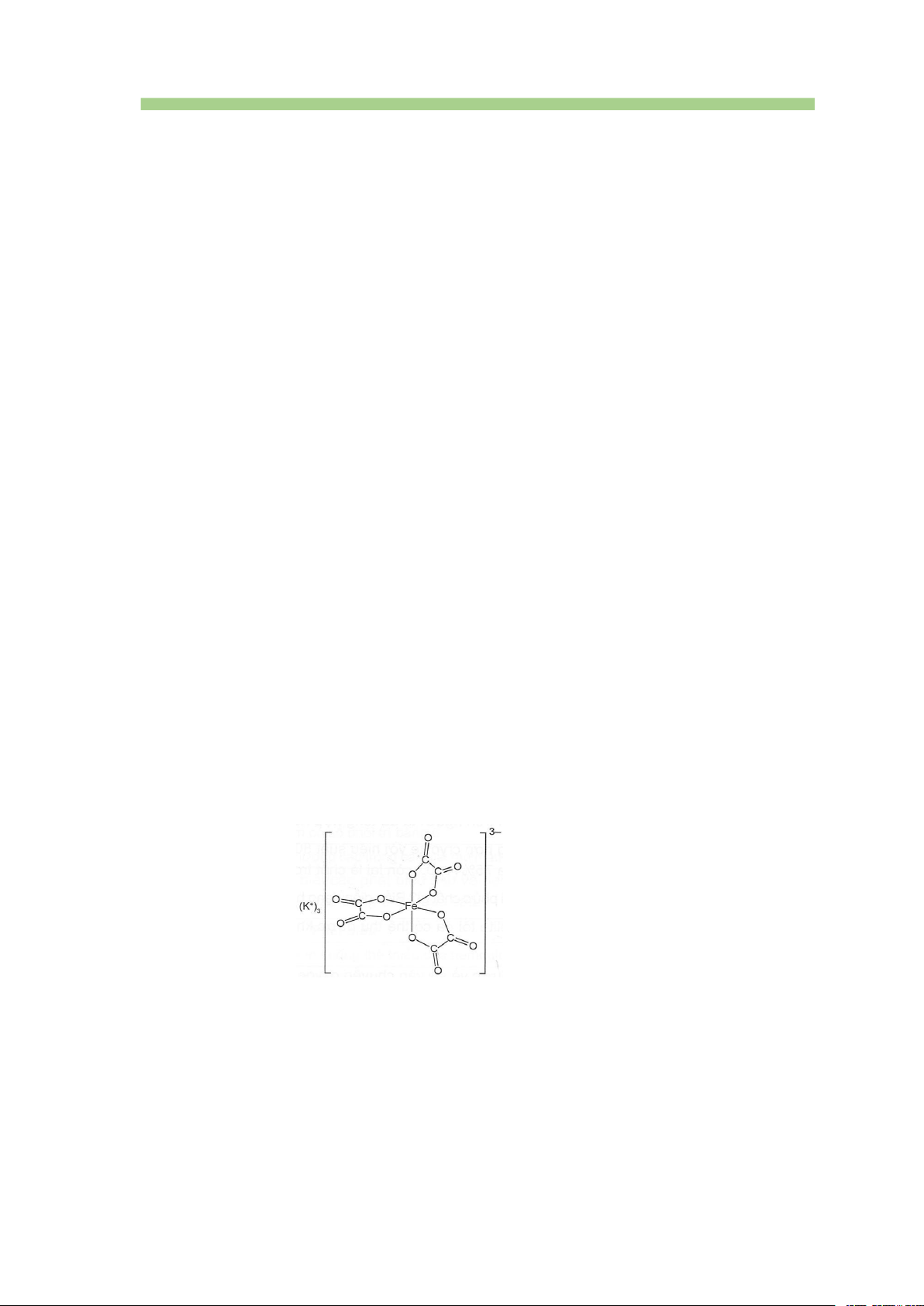
Câu 11. [CTST-SBT] Nhìn vào phức chất được biểu diễn như hình dưới, một bạn
học sinh có nhận xét sau:
(1) Số phối trí của nguyên tử trung tâm bằng 6.
(2) Dạng hình học của phức chất là tứ diện.
(3) Dung lượng phối trí của phối tử bằng 2.
(4) Số oxi hóa của nguyên tử trung tâm bằng +2.
(5) Các nhận xét đúng là A. (1) và (3). B. (2) và (3). C. (2) và (4). D. (1) và (4).
Hướng dẫn trả lời (1) Đúng.
(2) Sai vì dạng hình học của phức chất là bát diện. (3) Đúng.
(4) Sai vì số oxi hóa của nguyên tử trung tâm bằng +3.
Câu 12. [CTST-SBT] Khi là phối tử trong phức chất, diethylenetriamine (dien,
H2NCH2CH2HNCH2CH2NH2) có dung lượng phối trí tối đa là A. 1. B. 2. C. 3. D. 4.
Hướng dẫn trả lời
Phối tử diethylenetriamine còn 3 cặp electron chưa tham gia liên kết trên 3 nguyên
tử N có thể cho nguyên tử trung tâm hình thành 3 liên kết σ nên dung lượng phối
trí tối đa của phối tử này là 3.
Câu 13. [KNTT - SBT] Phối tử trong phức chất [PtCl4]2- và [Fe(CO)5] là A. Cl và C B. Pt và Fe C. Cl– và CO D. Cl và CO
Câu 14. [KNTT - SBT] Số lượng phối tử có trong mỗi phức chất [PtCl4]2- và [Fe(CO)5] là A. 4 và 5. B. 5 và 6. C. 5 và 2. D. 1 và 2.
Câu 15. [KNTT - SBT] Nguyên tử trung tâm của các phức chất [PtCl4]2- và [Fe(CO)5] lần lượt là A. Pt4+ và Fe2+. B. Pt2+ và Fe2+. C. Cl và CO. D. Pt2+ và Fe.
Câu 16. [KNTT - SBT] Điện tích của phức chất [PtCl4]2 và [Fe(CO)5] lần lượt là A. +2 và +5. B. +2 và 0. C. -1 và 0. D. -2 và 0.
Câu 17. [KNTT - SBT] Công thức tổng quát của phức chất (với nguyên tử trung
tâm M và phối tử L) có dạng tứ diện và bát diện lần lượt là A. [ML2] và [ML4]. B. [ML4] và [ML6]. C. [ML6] và [ML2]. D. [ML6] và [ML4].
Câu 18. [KNTT - SBT] Chọ phát biểu đúng nhất về dạng hình học có thể có của
phức chất có dạng tổng quát [ML4] A. Tứ diện. B. Bát diện. C. Vuông phẳng.
D. Tứ diện hoặc vuông phẳng.
Câu 19. [KNTT - SBT] Phức chất [Cu(H2O)6]2+ có dạng hình học là A. Vuông phẳng. B. Tứ diện. C. Bát diện. D. Đường thẳng.
Câu 20. [KNTT - SBT] Chọn đáp án đúng nhất sau về liên kết trong phức chất [PtCl4]2-
A. Là liên kết cộng hóa trị được hình thành do sự cho cặp electron chưa liên kết từ
phối tử Cl– vào nguyên tử trung tâm Pt2+.
B. Là liên kết cộng hóa trị được hình thàn do sự cho cặp electron chưa liên kết từ
nguyên tử trung tâm Pt2+vào phối tử Cl–.
C. Là liên kết tĩnh điện giữa nguyên tử trung tâm Pt2+ và phối tử Cl–.
D. Là liên kết cộng hóa trị được hình thành do sự ghép đôi cặp electron của phối tử
Cl– và nguyên tử trung tâm Pt2+ . Hướng dẫn trả lời
Liên kết trong phức chất [PtCl4]2- là liên kết cộng hóa trị được hình thành do sự
cho cặp electron chưa liên kết từ phối tử Cl– vào nguyên tử trung tâm Pt2+ .
Câu 21. [KNTT - SBT] Điện tích của nguyên tử trung tâm trong phức chất
[Co(NH3)6]3+ và [FeF6]3- lần lượt là A. +3 và +3 B. +3 và +2. C. +6 và -6. D. +3 và -3.
Câu 22. [KNTT - SBT] Dạng hình học có thể có của phức chất [FeF6]3- là A. Tứ diện. B. Bát diện. C. Vuông phẳng.
D. Tứ diện hoặc vuông phẳng.
Câu 23: [KNTT-SBT] Số lượng phối tử trong phức chất [PtCl4(NH3)2] là A. 6 B. 2 C. 4 D. 7.
Câu 24: [KNTT-SBT] Xét phức chất [PtCl4(NH3)4]2+ và [ FeF6]3- Phát biểu nào sau đây đúng?
A. Số lượng phối tử có trong mỗi phức chất lần lượt là 4 và 6.
B. Điện tích của mỗi phức chất lần lượt là +4 và + 3.
C. Nguyên tử trung tâm mỗi phức chất là Pt4+ và Fe3+.
D. Cả 2 phức chất đều ít tan trong nước.
Câu 25: [KNTT-SBT] Phức chất của Cr (0) có dạng hình học bát diện chỉ chứa
phối tử CO có cp6ng thức hóa học là A. [Cr(CO)4] B. [Cr(CO)6] C. [Cr(CO)4]2+ D. [Cr(CO)6]2+
Câu 26. [CD - SBT] Cho phát biểu sau: “Phức chất đơn giản thường có
một . .(1). . liên kết với các phối tử bao quanh. Liên kết giữa nguyên tử trung tâm
và phối tử trong phức chất là liên kết . .(2) ”.
Cụm từ cần điền vào (1) và (2) lần lượt là
A. cation kim loại, ion.
B. nguyên tử kim loại, cho — nhận.
C. nguyên tử trung tâm, cho — nhận. D. phối tử, ion.
Câu 27. [CD - SBT] Theo thuyết Liên kết hoá trị, để trở thành phối tử trong phức
chất thì phân tử hoặc anion cần có
A. các orbital trống.
B. cặp electron hoá trị riêng.
C. ít nhất 4 orbital trống.
D. ít nhất hai cặp electron hoá trị riêng.
Câu 28. [CD - SBT] Cho các chất có công thức: CuCl2, NH3, [CuCl4]2-. Phát biểu
nào sau đây là không đúng?
A. Do không có liên kết cộng hoá trị theo kiểu cho – nhận trong phân tử nên CuCl2
không phải là phức chất.
B. Do có nguyên tử trung tâm là nguyên tố kim loại, đồng thời các phối tử xung
quanh liên kết với nguyên tử trung tâm bằng liên kết cho – nhận nên, [CuCl4]2-là phức chất.
C. Dù có các nguyên tử H xung quanh N, nhưng NH3 không phải là phức chất.
D. Do nguyên tố đồng có hoá trị II nên quanh nguyên tử Cu trong CuCl2 và trong,
[CuCl4]2-đều có 2 liên kết.
Câu 29. [CD - SBT] Phát biểu nào sau đây không đúng về phức chất?
A. Phức chất đơn giản thường có một nguyên tử trung tâm liên kết với các phối tử bao quanh.
B. Phức chất có thể mang điện tích hoặc không mang điện tích.
C. Liên kết giữa nguyên tử trung tâm và phối tử trong phức chất là liên kết ion.
D. K,[PtCl4] hoặc anion [PtCl4]- đều được xếp vào loại phức chất
PHẦN II. CÂU HỎI TRẮC NGHIỆM ĐÚNG SAI
Câu 1. Phức chất là một khái niệm quan trọng trong lĩnh vực hóa học, phức chất
thường có cấu trúc phức tạp.
a) Phức chất là hợp chất có chứa nguyên tử trung tâm (kí hiệu là M) và các phối tử
(kí hiệu là L). Phức chất là thành phần có mang điện tích.
b) Nguyên tử trung tâm của phức chất là cation kim loại hoặc nguyên tử kim loại liên
c) kết với các phối tử.
d) Phối tử của phức chất là anion, cation hoặc phân tử. Hướng dẫn trả lời
Phức chất là hợp chất có chứa nguyên tử trung tâm (thường được kí hiệu là M) và
các phối tử (thường được kí hiệu là L). Trong đó, nguyên tử trung tâm là cation
kim loại hoặc nguyên tử kim loại liên kết với các phối tử. Phối tử là anion hoặc
phân tử. Phức chất có thể mang điện tích hoặc không mang điện tích. a, c đúng b, d sai
Câu 2. Thuốc thử Tollens có công thức [Ag(NH3)2]OH, có khả năng tham gia
phản ứng tráng bạc với aldehyde.
a) Nguyên tử trung tâm của thuốc thử Tollens là Ag(NH3)2.
b) Cation [Ag(NH3)2]+ được gọi là cầu nội của thuốc thử Tollens và quyết định tính chất của nó.
c) Nguyên tử trung tâm là Ag, phối tử là NH3.
d) Phối tử của thuốc thử Tollens là NH3 và OH.
Hướng dẫn trả lời
Phức chất là phân tử hoặc ion trong đó có nguyên tử trung tâm liên kết với các
phối tử bao quanh bởi liên kết cho nhận: phối tử cho cặp electron chưa liên kết vào
orbital trống của nguyên tử trung tâm.
Phức chất [Ag(NH3)2]OH có cấu tạo gồm: Nguyên tử trung tâm là Ag, phối tử là NH3. → b, c đúng → a, d sai
Câu 3. Phức chất cis-[Pt(NH3)2Cl2] một hợp chất vô cơ có khả năng ức chế các tế
bào ung thư như ung thư tinh hoàn, buồng trứng, bàng quang và các khối u ở đầu
và cổ. Mỗi phát biểu sau là đúng hay sai? a) Ion trung tâm là Pt b) Phối tử là NH3
c) Ion trung tâm là Pt2+, phối tử là NH3 và Cl-.
d) Phức có dạng hình học là vuông phẳng Hướng dẫn trả lời
Phức chất cis-[Pt(NH3)2Cl2] có ion trung tâm là Pt2+, phối tử là NH3 và Cl-. → c, d đúng → a, b sai
Câu 4. Metalloporphyrin có cấu trúc tương tự heme và được sử dụng việc kiểm
soát chứng tăng bilirubin máu ở trẻ sơ sinh ( chứng này gây ra bệnh vàng da ở trẻ
sơ sinh). Metalloporphyrin có công thức như sau
Mỗi phát biểu sau là đúng hay sai?
a) Ion trung tâm của phức Metalloporphyrin là Fe
b) Số phối trí của phức là 4.
c) Metalloporphyrin là muối kép không phải là phức chất.
d) Liên kết trong phức Metalloporphyrin được tạo thành do nguyên tử N cho cặp
electron chưa liên kết vào orbital trống của nguyên tử Fe. Hướng dẫn trả lời → b, d đúng
→ a sai Ion trung tâm của phức Metalloporphyrin là Fe2+
→ c sai Metalloporphyrin là muối kép không phải là phức chất → là phức chất
Câu 5. Trong dung dịch, hầu hết các ion kim loại chuyển tiếp đều có màu. Các ion
kim loại chuyển tiếp tồn tại trong nước dưới dạng phức chất.
a) Phức chất có thể mang điện tích hoặc không mang điện tích.
b) Liên kết giữa phối tử và nguyên tử trung tâm của phức chất là liên kết cho – nhận.
c) Nguyên tử trung tâm liên kết với các phối tử tạo thành cầu ngoại của phức chất.
d) Cầu ngoại quyết định tính chất hóa học của phức chất.
Hướng dẫn trả lời → a, b đúng
→ c sai Nguyên tử trung tâm liên kết với các phối tử tạo thành cầu ngoại của phức chất → Cầu nội
→ d sai Cầu ngoại quyết định tính chất hóa học của phức chất → Cầu nội
Câu 6. Phức chất có nhiều dạng hình học khác nhau, dạng hình học của phức chất
được xác định bằng thực nghiệm.
a) Phức chất mà nguyên tử trung tâm tạo 6 liên kết với các phối tử được gọi là phức chất bát diện.
b) Trong phức bát diện, nguyên tử trung tâm nằm ở các đỉnh của hình bát diện.
c) Phức tứ diện hoặc phức vuông phẳng thì nguyên tử trung tâm tạo 4 liên kết với các phối tử.
d) Phức chất tam giác là loại phức rất ít phổ biến.
Hướng dẫn trả lời → a, c, d đúng
→ b sai Trong phức bát diện, nguyên tử trung tâm nằm ở các đỉnh của hình bát diện → trung tâm
Câu 7. Phức chất có trong một số thành phần quan trọng của sinh vật như
hemoglobin, chất diệp lục. Một số phức chất có vai trò quan trọng trong điều trị bệnh ung thư.
a) Chất tạo phức có thể là ion (cation hoặc anion) hay nguyên tử và thường
được gọi chung là nguyên tử tạo phức.
b) Điện tích của cầu nội là tổng điện tích của các ion ở trong cầu nội. Cầu nội
có thể là cation, anion hoặc phân tử trung hòa điện.
c) Những ion nằm ngoài và ngược dấu với cầu nội tạo nên cầu ngoại.
d) Phức chất có thể có hoặc không có cầu nội.
Hướng dẫn trả lời
→ a sai Chất tạo phức có thể là ion (cation hoặc anion) hay nguyên tử và thường
được gọi chung là nguyên tử tạo phức → (anion)
→ d sai Phức chất có thể có hoặc không có cầu nội → cầu ngoại
Câu 8. Trong các nhận xét sau, nhận xét nào đúng, nhận xét nào sai?
a) Trong y học, nhiều phức chất có khả năng chữa trị hoặc kiểm soát bệnh (như
cisplatin là phức dùng làm thuốc chữa bệnh ung thư).
b) Phản ứng tạo thành phức chất trong dung dịch thường không có hiện tượng gì.
c) Phức chất của Mg2+ cấu tạo nên chlorophyll hay chất diệp lục, có vai trò quan
trọng trong quá trình quang hợp của cây xanh, thực vật có màu xanh là do có chứa chlorophyll.
d) Phức chất [Ag(NH3)2]+ được gọi là thuốc thử Tollens dùng để phân biệt aldehyde với ketone.
Hướng dẫn trả lời → a, c, d đúng
→ b sai Phản ứng tạo thành phức chất trong dung dịch thường không có hiện tượng gì.
Câu 9 [SBT –CD]. Cho các phát biểu sau đây về nguyên tử trung tâm trong phức chất?
a) Nguyên tử trung tâm trong phức chất là cation kim loại hoặc nguyên tử kim
loại đã nhận cặp electron hoá trị riêng của phân tử hoặc anion
b) Cation tạo nguyên tử trung tâm trong phức chất [Co(OH2)6]3+ là Co3+.
c) Nguyên tử trung tâm trong phức chất là các nguyên tố kim loại chuyển tiếp.
d) Nguyên tử trung tâm trong phức chất [Ni(CO)4] được hình thành từ quá trình
cation Ni2+ sử dụng các orbital trống để nhận các cặp electron hoá trị của các phân tử CO.
Hướng dẫn trả lời
Phát biểu không đúng là: (c), (d). Phát biểu đúng: (a), b)
Phát biểu (c) sai vì: Có phức chất mà nguyên tử trung tâm là nguyên tố s, p.
Phát biểu (d) sai vì: Phức chất [Ni(CO)4] hình thành từ quá trình nguyên tử Ni
nhận các cặp electron hoá trị riêng của 4 phân tử CO.
Hướng dẫn trả lời
Câu 10. Phức chất bao gồm nguyên tử trung tâm và các phối tử, có thể mang
điện tích hoặc không mang điện tích.
a) Phức chất [Co(NH3)6]3+ có điện tích là +3, nguyên tử trung tâm là Co, phối tử là NH3.
b) Phức chất [Fe(CO)5] là phức trung hòa, không mang điện tích.
c) F là nguyên tử trung tâm của phức chất [CoF6]3-.
d) Phức chất [PtCl2(NH3)2] có phối tử là PtCl2.
Hướng dẫn trả lời → a, b đúng
→ c sai F là nguyên tử trung tâm của phức chất [CoF6]3- → Co3+
→ d sai Phức chất [PtCl2(NH3)2] có phối tử là Cl−, NH3
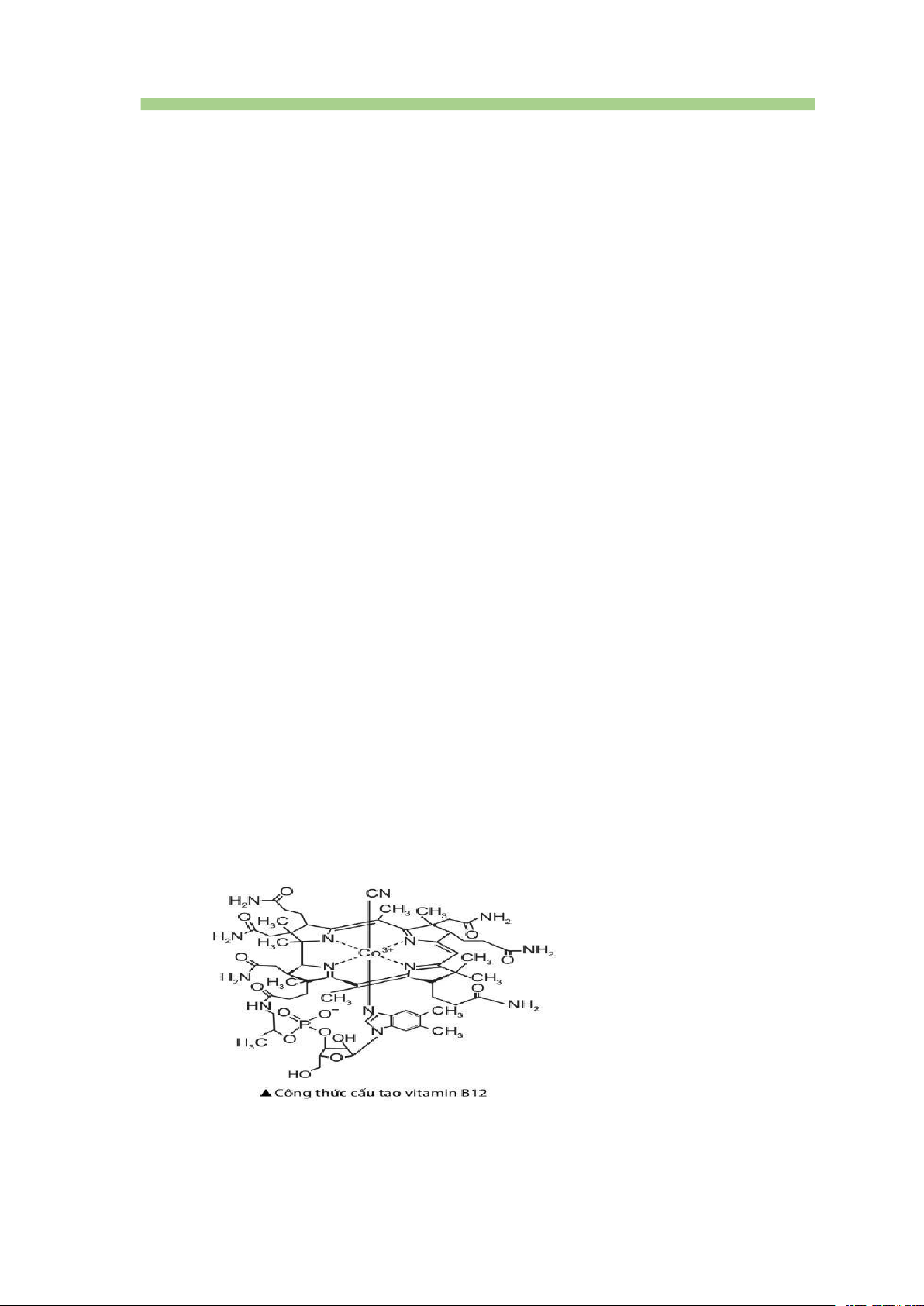
Câu 11. [CTST-SBT] Vitamin B12 có công thức cấu tạo được mô tả như hình dưới.
Em hãy cho biết phát biểu sau đúng hay sai?
a) Trong công thức cấu tạo có nhiều nhóm chức amide.
b) Vitamin B12 có nguyên tử trung tâm là Co(0).
c) Nguyên tử trung tâm có số phối trí bằng 6.
d) Vitamin B12 có hàm lượng cao trong các loại rau màu đỏ. Hướng dẫn trả lời
a) Đúng vì vitamin B12 có nhiều nhóm –CO-NH2.
b) Sai vì vitamin B12 có nguyên tử trung tâm là Co3+. c) Đúng.
d) Sai vì vitamin B12 có hàm lượng cao trong các loại rau củ như nấm hương, rau
chân vịt, củ dền, rong biển. ., tức là có nhiều loại rau không có màu đỏ vẫn chứa nhiều vitamin B12.
Câu 12. [CTST-SBT] Em hãy cho biết các phát biểu sau về heme B là đúng hay sai?
a) Heme B là thành phần không thể thiếu của hemoglobin.
b) Heme B là phức chất của Fe(III).
c) Heme B giúp cung cấp oxygen đến các tế bào và mô trong cơ thể
d) Máu của các loài giáp xác có chứa nhiều heme B. Hướng dẫn trả lời a) Đúng.
b) Sai vì heme B là phức chất của Fe(II). c) Đúng.
d) Sai vì máu của các loài giáp xác có chứa nhiều protein hemocyanin tạo ra màu
xanh lam đặc trưng; máu của các loài động vật cấp cao mới chứa nhiều heme B.
Câu 13. [CTST-SBT] Em hãy cho biết phát biểu sau về chlorophyll đúng hay sai?
a) Chlorophyll chỉ được tìm thấy trong thực vật.
b) Chlorophyll đóng vai trò là chất xúc tác cho quá trình quang hợp.
c) Trong chất diệp lục chỉ chứa một loại chlorophyll.
d) Chlorophyll là thành phần quan trọng trong chất diệp lục. Hướng dẫn trả lời
a) Sai vì chlorophyll còn được tìm thấy trong tảo, vi khuẩn lam… b) Đúng.
c) Sai vì có nhiều loại chlorophyll như chlorophyll a, chlorophyll b, … d) Đúng.
Câu 14. [KNTT - SBT] Xét phức chất [CoCl2(NH3)4]+
a) Nguyên tử trung tâm trong phức chất là CO2+.
b) Các phối tử có trong phức chất là Cl– và NH3
c) Số lượng phối tử trong phức chất là 6.
d) Điện tích của phức chất là +3. Hướng dẫn trả lời
a. Sai vì nguyên tử trung tâm là Co3+. b. Đúng. c. Đúng.
d. Sai vì điện tích của phức chất là +1.
Câu 15. [KNTT - SBT] Xét phức chất [ZnCl4]2+
a) Số lượng phối tử trong phức chất là 2.
b) Liên kết trong phức chất được hình thành là do phối tử Cl– cho cặp electron
chưa liên kết vào nguyên tử trung tâm Zn2+ .
c) Điện tích của phức chất là +3.
d) Phức chất có thể có dạng hình học bát diện. Hướng dẫn trả lời
a. Sai vì số lượng phối tử trong phức chất là 4. b. Đúng.
c. Sai vì điện tích của phức chất là +2.
d. Sai vì phức chất có thể có dạng hình học tứ diện hoặc vuông phẳng.
Câu 16. [KNTT - SBT] Xét phức chất [Ni(NH3)6]2+
a) Phức chất có thể có dạng hình học tứ diện hoặc vuông phẳng.
b) Liên kết trong phức chất được hình thành là do phối tử NH3 cho cặp eletron
chưa liên kết vào nguyên tử trung tâm Ni+.
c) Nguyên tử trung tâm trong phức là Ni2+.
d) Điện tích của phức chất là +2 Hướng dẫn trả lời
a. Sai vì có 6 phối tử nên phức chất có dạng hình học là bát diện.
b. Sai vì nguyên tử trung tâm không phải Ni+ mà là Ni2+.
c. Đúng. Nguyên tử trung tâm trong phức là Ni2+.
d. Đúng. Điện tích của phức chất là +2.
Câu 17. [KNTT - SBT] Trong dung dịch Fe3+ tạo phức chất aqua có dạng hình học bát diện.
a) Công thức hóa học của phức chất là [Fe(H2O)6]2+ .
b) Phức chất có điện tích là +2.
c) Số lượng phối tử trong phức chất là 6.
d) Liên kết trong phức chất được hình thành là do phối tử H2O cho cặp electron
chưa liên kết vào nguyên tử trung tâm Fe3+. Hướng dẫn trả lời
a. Sai vì công thức hóa học của phức chất là [Fe(H2O)6]3+ .
b. Sai vì điện tích của phức chất là +3. c. Đúng. d. Đúng.
Câu 18. [KNTT-SBT] Thí nghiệm xác định nồng độ muối Fe2+ bằng phương pháp
chuẩn độ với dung dịch thuốc tím (KMnO4) xảy ra theo phương trình hóa học sau:
10FeSO4 + 2KMnO4 + 8H2SO4 →→ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
a) Dung dịch thuốc tím được cho vào bình tam giác khi chuẩn độ.
b) Dung dịch muối Fe2+ được cho vào burette khi chuẩn độ.
c) Phản ứng xảy ra là phản ứng oxi hóa-khử.
d) Khi kết thúc chuẩn độ, dung dịch trong bình tam giác có màu hồng tồn tại bền
trong khoảng 20 giây là của lượng rất nhỏ KMnO4 dư. Hướng dẫn trả lời
a. Sai, thuốc tím là chất chuẩn độ được cho vào burette khi chuẩn độ.
b. Sai, dung dịch muối Fe2+ được cho vào bình tam giác khi chuẩn độ.
c. Đúng. Phản ứng xảy ra là phản ứng oxi hóa-khử.
d. Đúng. Khi kết thúc chuẩn độ, dung dịch trong bình tam giác có màu hồng tồn
tại bền trong khoảng 20 giây là của lượng rất nhỏ KMnO4 dư.
Câu 19. [KNTT-SBT] Phức chất có nguyên tử trung tâm Co2+, chứa 4 phối tử Cl- và 2 phối tử NH3.
a) Công thức hóa học của phức chất là [CoCl4(NH3)2]2-.
b) Phức chất có dạng hình học bát diện.
c) Phức chất có điện tích là +2.
d) Nguyên tử trung tâm Co2+ nhận 6 cặp electron chưa liên kết từ các phối tử. Hướng dẫn trả lời
a. Đúng. Công thức hóa học của phức chất là [CoCl4(NH3)2]2-.
b. Đúng. Phức chất có dạng hình học bát diện.
c. Sai. Phức chất này có điện tích là -2.
d. Đúng. Nguyên tử trung tâm Co2+ nhận 6 cặp electron chưa liên kết từ các phối tử.
Câu 20. [CD - SBT] Những phát biểu nào sau đây là không đúng về nguyên tử
trung tâm trong phức chất?
a) Nguyên tử trung tâm trong phức chất là cation kim loại hoặc nguyên tử kim loại
đã nhận cặp electron hoá trị riêng của phân tử hoặc anion.
b) Cation tạo nguyên tử trung tâm trong phức chất [Co(OH2)6]3+ là Co3+.
c) Nguyên tử trung tâm trong phức chất là các nguyên tố kim loại chuyển tiếp.
d) Nguyên tử trung tâm trong phức chất [Ni(CO)4] được hình thành từ quá trình
cation Ni2+ sử dụng các orbital trống để nhận các cặp electron hoá trị của các phân tử CO. Hướng dẫn trả lời
Phát biểu không đúng là: (c), (d).
Phát biểu (c) sai vì: Có phức chất mà nguyên tử trung tâm là nguyên tố s, p.
Phát biểu (d) sai vì: Phức chất [Ni(CO)4] hình thành từ quá trình nguyên tử Ni
nhận các cặp electron hoá trị riêng của 4 phân tử CO.
Câu 21. [CD - SBT] Theo thuyết Liên kết hoá trị, những phát biểu nào sau đây là không đúng?
a) Phối tử là các phân tử hoặc anion đã cho một hoặc một số cặp electron hoá trị riêng.
b) Các phần tử gồm NH3, N2, H2, OH- , Cl- đều có thể trở thành phối tử trong phức chất.
c) Có phối tử là anion và phối tử là phân tử trong phức chất [Cu(NH3)4(OH2)2]2+.
d) Khi tham gia quá trình tạo phức chất, phân tử ethylenediamine H2N-CH2-CH2-
NH2, sử dụng hai cặp electron hoá trị riêng để tạo 2 liên kết cho - nhận. Hướng dẫn trả lời
Các phát biểu không đúng là: (b), (c), (d).




