








Preview text:
Biên soạn: Cao Minh Hiếu – HC19KSTN.
Tài liệu tham khảo:
1. Vũ Bá Minh. (2013). Quá trình và thiết bị Công nghệ Hóa học và Thực
phẩm, tập 3. TP HCM: NXB Đại học Quốc gia.
2. LDDT – TYB. Mass Transfer Theory Final Revision.
3. Bài giảng được biên soạn bởi thầy Mai Thanh Phong và thầy Trần Tấn Việt.
4. Bài giảng được biên soạn bởi thầy Trịnh Văn Dũng. 1 HẤP THU
Câu 1. Định nghĩa quá trình hấp thu? Mục đích của quá trình hấp thu?
Hấp thu là quá trình hút khí bằng chất lỏng, dùng để tách các cấu tử khí bằng dung môi. Chất bị hấp thu: khí.
Chất hấp thu (dung môi): lỏng.
Khí trơ: khí không bị hấp thu.
Mục đích của quá trình hấp thu: Thu hồi cấu tử quý, làm sạch khí, tách hỗn hợp thành
nhiều cấu tử riêng biệt.
Câu 2. Nêu một vài ứng dụng thực tế của quá trình hấp thu?
- Sản xuất nước có gas: hấp thu CO2 vào trong chất lỏng.
- Làm sạch khí SO2: sử dụng dung dịch Na2SO3 để lấy lượng SO2 vào trong.
- Sản xuất H2SO4 bằng cách cho hơi SO3 đi vào bồn chứa nước.
Câu 3. Nêu một quá trình hấp thu được rộng rãi trong đời sống và sản xuất?
Làm sạch nước bằng Ca(OH)2: hấp thu acid từ đất trồng cây lâu năm để đất không bị
chua và nghèo dinh dưỡng.
Câu 4. Phân biệt quá trình hấp thụ và nhả hấp thụ? Hấp thu Nhả hấp thu
Các phân tử khí khuếch tán đi vào trong chất Các phân tử khí trong dung dịch đi ra khỏi lỏng. dung dịch.
Câu 5. Phân loại các quá trình hấp thu
Tiêu chí phân loại Đặc điểm 2
Theo bản chất hóa học
- Hấp thu hóa học: có phản ứng giữa khí và lỏng.
- Hấp thu vật lý: không có phản ứng giữa khí và lỏng.
Theo chiều chuyển động của khí Khí => Lỏng: Hấp thu.
Lỏng => Khí: Nhả hấp thu.
=> Quá trình xảy ra thuận nghịch.
Theo chiều chuyển động của hai pha
Xuôi chiều, ngược chiều, chéo chiều.
Theo tính chọn lọc
Hấp thu tuyệt đối (chỉ hấp thu một cấu tử).
Hấp thu tương đối (hấp thu nhiều cấu tử).
Theo áp suất làm việc
Áp suất thấp, thường, cao.
Theo nhiệt độ
Đẳng nhiệt, đa biến nhiệt.
Câu 6. Các nguyên tác cơ bản khi lựa chọn dung môi? Nguyên tắc Mục đích
Độ hòa tan chọn lọc
Chỉ hòa tan một số cấu tử, không hòa tan được
cấu tử khác (hoặc tan rất ít).
Độ nhớt thấp
Để giảm trở lực, tăng hệ số truyền khối
Nhiệt dung riêng nhỏ
Tiết kiệm năng lượng hoàn nguyên
Nhiệt độ sôi khác xa cấu tử hòa tan
Dễ hoàn nguyên qua chưng cất 3
Nhiệt độ đóng rắn thấp
Không tạo kết tủa, không ăn mòn thiết bị Ít bay hơi
Rẻ, dễ kiếm, không độc
Câu 7. Tại sao khi lựa chọn dung môi cho quá trình hấp thụ cần chú trọng đến tính
hòa tan chọn lọc của dung môi? Để đảm bảo dung dịch chỉ chứa đúng cấu tử cần hấp thu.
Câu 8. Thế nào là độ hòa tan cân bằng của khí trong lỏng? Đơn vị?
Khí hòa tan trong lỏng sẽ tạo thành hỗn hợp 2 cấu tử.
Tại T = const, độ hòa tan của khí phụ thuộc vào áp suất theo định luật Henry.
𝑃𝑖 = 𝑘𝐻 × 𝑥𝑖
𝑃𝑖 là áp suất hơi riêng phần của khí trên bề mặt chất lỏng.
𝑘𝐻 là hằng số Henry (cùng đơn vị với áp suất),
𝑥𝑖 là phần mol của khí trong dung dịch.
Câu 9. Vẽ sơ đồ và thuyết minh quá trình hấp thu, chú thích đầy đủ.
Ta xét quá trình hấp thu ammoniac trong không khí vào nước:
Gọi x, y là nồng độ của ammoniac trong pha lỏng và pha khí.
𝑣𝑡, 𝑣𝑛 là vận tốc pha khí đi vào lỏng và lỏng đi vào khí.
Ban đầu: 𝑥 = 0, 𝑦 > 0.
- 𝒗𝒕 > 𝒗𝒏 => xảy ra qua trình hấp thu. Khi đó y giảm dần, x tăng dần. 4
- Khi: 𝒙 = 𝒙∗, 𝒚 = 𝒚∗, 𝒗𝒕 = 𝒗𝒏, quá trình hấp thu đạt cân bằng. Đây là giới hạn của quá trình.
- 𝒗𝒕 < 𝒗𝒏, quá trình nhả hấp thu xảy ra. Khi đó y tăng dần, x giảm dần.
Câu 10. Các yếu tố ảnh hưởng đến quá trình hấp thu?
Nhiệt độ: Vì 𝑘𝐻 = 𝑓(𝑇) nên hằng số Henry tăng => phần mol 𝑥𝑖 giảm => độ hấp thu giảm.
Áp suất: Khi áp suất tăng => 𝑥𝑖 tăng => độ hấp thu tăng.
Chiều chuyển động của hai pha: động lực quá trình hấp thu ngược chiều lớn hơn động lực xuôi chiều.
Chiều cao thiết bị: Vì hấp thu là quá trình tỏa nhiệt nên khi chiều cao thiết bị tăng =>
nhiệt lượng tăng => nhiệt độ tăng => độ hấp thu giảm.
=> Để quá trình hấp thu xảy ra tốt, ta nên tiến hành ở nhiệt độ thấp, áp suất cao và cho
hai dòng đi ngược chiều.
Câu 11. Trình bày nguyên lý hoạt động của tháp mâm? Ưu và nhược điểm của tháp mâm.
Pha lỏng đi từ trên xuống, pha khí đi từ dưới lên. Hai pha tiếp xúc và trao đổi chất với
nhau tại mỗi bậc (mâm). Ưu điểm
- Hiệu quả truyền khối tốt hơn tháp đệm.
- Sử dụng được với cả lưu lượng cao hoặc thấp.
- Sử dụng được khi có lẫn hạt rắn.
- Đáp ứng được nhiều yêu cầu đặc biệt. Nhược điểm
- Trở lực cao hơn tháp đệm.
- Không phù hợp khi có quá nhiều cặn. 5 CHƯNG CẤT
Câu 1. Định nghĩa thế nào là quá trình chưng cất?
Chưng cất là quá trình dùng để tách các cấu tử của một hỗn hợp lỏng cũng như hỗn hợp
khí – lỏng thành các cấu tử riêng biệt dựa vào độ bay hơi khác nhau (ở cùng một nhiệt độ,
áp suất hơi bão hòa của các cấu tử khác nhau).
Khi chưng cất, ta thu được nhiều sản phẩm và thường thì bao nhiêu cấu tử sẽ thu được bấy nhiêu sản phẩm.
Trong trường hợp hỗn hợp gồm hai cấu tử, quá trình chưng cất sẽ cho:
- Sản phẩm đỉnh: cấu tử có độ bay hơi lớn (một ít cấu tử có độ bay hơi bé).
- Sản phẩm đáy: cấu tử có độ bay hơi bé (một ít cấu tử có độ bay hơi lớn).
Câu 2. Nêu một vài ví dụ về việc ứng dụng chưng cất trong đời sống và sản xuất? Trong sản xuất:
Ứng dụng trong ngành công nghiệp lọc dầu: nguyên liệu dầu thô và khí thiên nhiên được
đi qua tháp chưng cất nhiều bậc, tạo ra các dòng sản phẩm khác nhau có ứng dụng khác nhau. Trong đời sống:
Dùng để chưng rượu, tách tinh dầu…
Câu 3. Phân biệt quá trình chưng cất và quá trình cô đặc?
Giống nhau: đều xảy ra sự bay hơi. Khác nhau:
Chưng cất: tất cả dung môi và chất tan đều bay hơi (các cấu tử đều hiện diện trong hai pha).
Cô đặc: chỉ có dung môi bay hơi, chất tan không bay hơi. 6
Câu 4. Nêu các phương pháp phân loại, các phương pháp chưng cất và phạm vi
ứng dụng của từng phương pháp?
Các phương pháp phân loại:
Theo số cấu tử
- Hai cấu tử: ethanol – nước, acetone – nước…
- Nhiều cấu tử: dầu mỏ, tinh dầu… Theo áp suất
- Áp suất thường: dễ thực hiện, thường được dùng để chưng rượu, acid…
- Áp suất thấp: nhiệt độ sôi của hỗn hợp giảm => thường
dùng để chưng các hợp chất dễ bị biến tính nhiệt.
- Áp suất cao: tách các hỗn hợp không thể hóa lỏng ở
nhiệt độ thường (sản xuất O2 và N2 từ không khí). Theo số bậc
Chưng một bậc (còn gọi là chưng đơn giản) hoặc nhiều bậc.
Theo phương pháp cấp nhiệt Trực tiếp hoặc gián tiếp.
Theo thiết bị sử dụng
Tháp chêm, tháp mâm, tháp màng…
Các phương pháp chưng và phạm vi ứng dụng:
Chưng đơn giản (một bậc)
Các cấu tử có độ bay hơi rất khác nhau => tách sơ
bộ hoặc làm sạch các cấu tử khỏi tạp chất.
Chưng bằng hơi nước trực tiếp Tách các hỗn hợp gồm các chất khó bay hơi và tạp
chất không bay hơi => ứng dụng trong trường hợp
chất được tách không tan vào nước. 7
Chưng chân không
Dùng trong trường hợp cần hạ thấp nhiệt độ sôi của
cấu tử. Dùng cho các cấu tử trong hỗn hợp dễ bị phân
hủy ở nhiệt độ cao hoặc nhiệt độ sôi quá cao. Chưng cất
Phương pháp phổ biến nhất dùng để tách hoàn toàn
hỗn hợp các cấu tử hòa tan một phần hoặc hòa tan
hoàn toàn vào nhau.
Câu 5. Thế nào là quá trình chưng cất lôi cuốn hơi nước?
Chưng cất lôi cuốn hơi nước là quá trình cấu tử trong hỗn hợp bị lôi cuốn theo hơi nước
trong quá trình sôi. Chưng cất lôi cuốn hơi nước được áp dụng phổ biến để tách tinh dầu.
Câu 6. Ưu nhược điểm của chưng cất lôi cuốn hơi nước? Ưu điểm: - Giá thành rẻ.
- Sử dụng được nhiều loại nguồn nhiệt khác như điện, củi…
Nhược điểm: thời gian chưng lâu.
Câu 7. Thế nào là độ bay hơi tương đối? Viết biểu thức?
Độ bay hơi 𝛼 tương đối (hay hệ số tách) là tỉ số giữa áp suất hơi bão hòa của hai cấu tử
trong hỗn hợp, hoặc tỉ số giữa tỉ số nồng độ của A và B trong pha hơi với tỉ số nồng độ của A và B trong pha lỏng. 𝑦𝐴 𝑦 𝑃0 𝛼 𝐵 𝐴 𝐴𝐵 = 𝑥 = 𝐴 𝑃0 𝑥 𝐵 𝐵 8 𝑦 𝑥 𝛼 0 0 𝐴 𝐴
𝐴𝐵 > 1 => 𝑃𝐴 > 𝑃𝐵 ℎ𝑎𝑦 >
=> A dễ sôi hơn B => chưng cất được. 𝑦𝐵 𝑥𝐵 𝑦 𝑥 𝑎 0 0 𝐴 𝐴
𝐴𝐵 < 1 => 𝑃𝐴 < 𝑃𝐵 ℎ𝑎𝑦 >
=> B dễ sôi hơn A => chưng cất được. 𝑦𝐵 𝑥𝐵 𝛼 = 1 => 𝑃0 0
𝐴 = 𝑃𝐵 => hỗn hợp cùng nhiệt độ sôi => không chưng cất được. 𝑦 𝑥
Hay 𝐴 = 𝐴 => hỗn hợp đẳng phí => không chưng cất được. 𝑦𝐵 𝑥𝐵
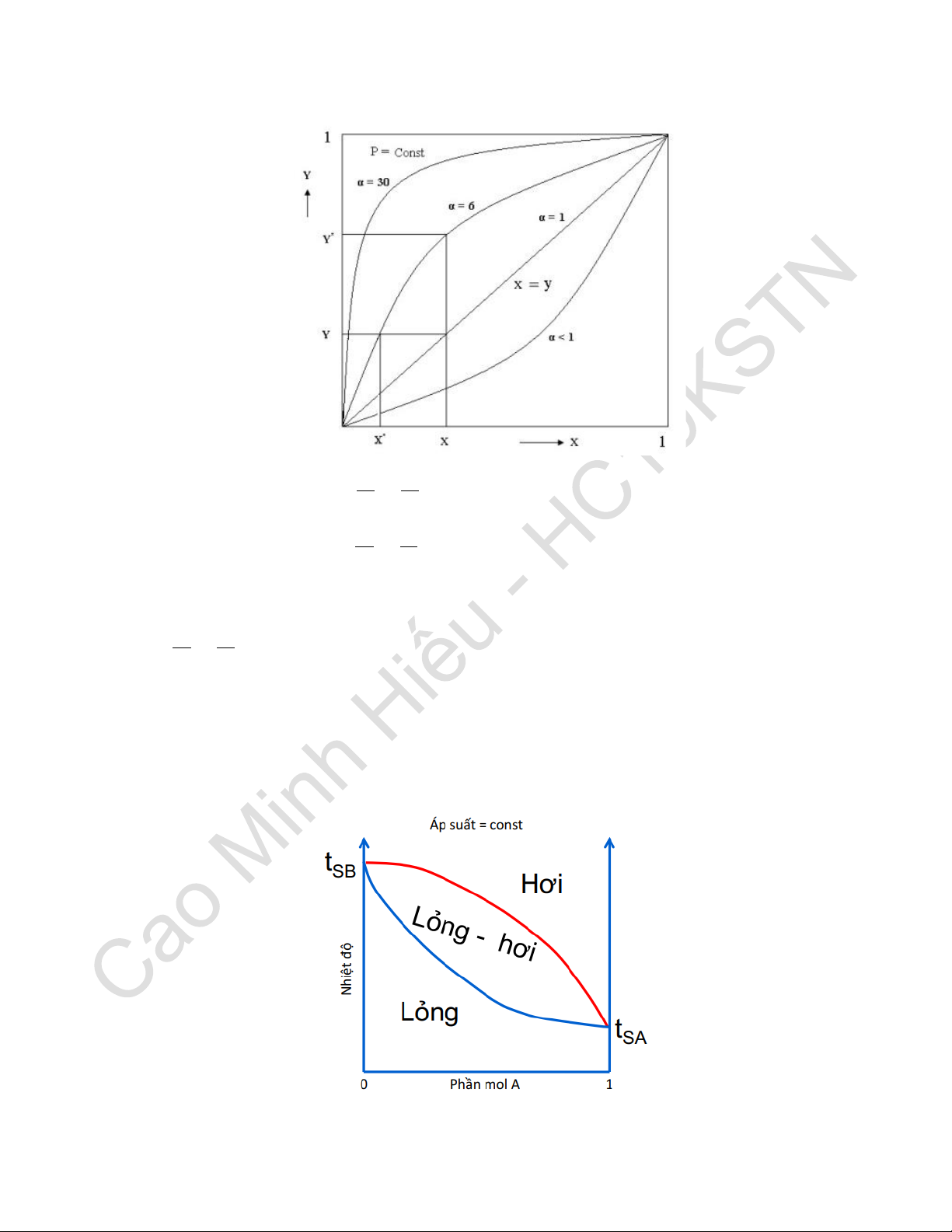
Câu 8. Thiết lập cân bằng lỏng hơi của hỗn hợp 2 cấu tử ở áp suất cố định? Viết
định luật Raoult cho hỗn hợp lý tưởng?
Đồ thị nhiệt độ - phần mol ở áp suất P = const: 9
Với hỗn hợp lý tưởng, ta có định luật Raoult: 𝑃 0 𝐴 = 𝑃𝐴 × 𝑥𝐴 𝑃 0 0
𝐵 = 𝑃𝐵 × 𝑥𝐵 = 𝑃𝐵 × (1 − 𝑥𝐴) 𝑃 = 𝑃 0 0
𝐴 + 𝑃𝐵 = 𝑃𝐴 × 𝑥𝐴 + 𝑃𝐵 × (1 − 𝑥𝐴)
Độ bay hơi tương đối: 𝑦𝐴 𝑦 𝑃0 𝛼 𝐵 𝐴 𝐴𝐵 = 𝑥 = 𝐴 𝑃0 𝑥 𝐵 𝐵
Thành phần của hỗn hợp trong pha hơi: 𝑃 𝑃0 × 𝑥 𝑦 𝐴 𝐴 𝐴 𝐴 = = 𝑃 𝑃0 0
𝐴 × 𝑥𝐴 + 𝑃𝐵 × (1 − 𝑥𝐴) 𝑃 𝑃0 × 𝑥 𝑦 𝐵 𝐵 𝐵 𝐵 = = 𝑃 𝑃0 0
𝐴 × 𝑥𝐴 + 𝑃𝐵 × (1 − 𝑥𝐴) Chia tử và mẫu cho 𝑃0
𝐵 của phương trình 𝑦𝐴: 𝛼 × 𝑥 𝑦 𝐴 𝐴 =
𝛼 × 𝑥𝐴 + 1 − 𝑥𝐴
Ta được phương trình đường cân bằng: 𝛼 × 𝑥 𝑦 𝐴 𝐴 = 1 + 𝑥𝐴 × (𝛼 − 1)
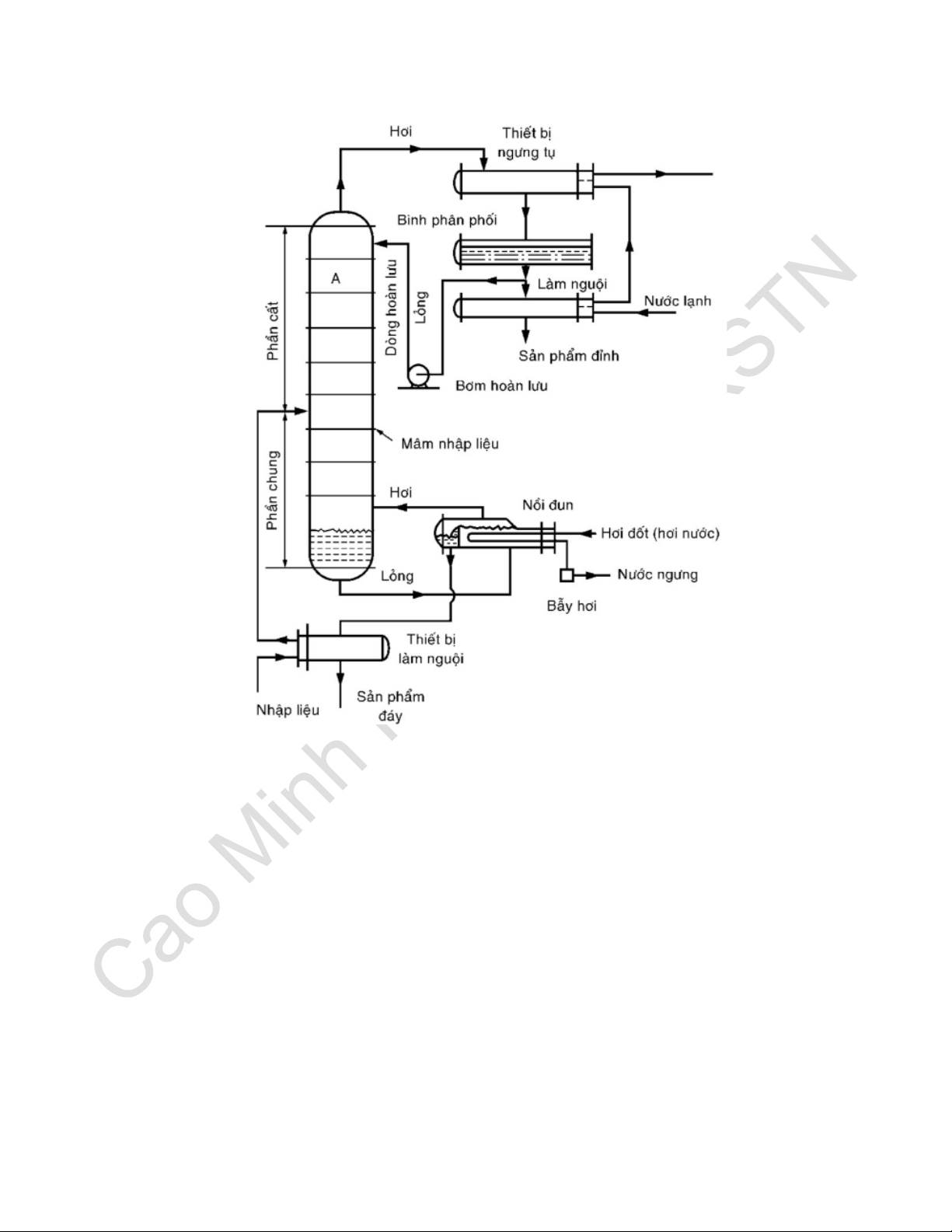
Câu 9. Vẽ sơ đồ quy trình chưng cất liên tục? 10
Nguyên tắc làm việc:
Pha lỏng đi từ trên xuống có nồng độ cấu tử dễ bay hơi giảm dần.
Pha khí đi từ dưới lên có nồng độ cấu tử dễ bay hơi tăng dần.
Nồng độ các cấu tử thay đổi theo chiều cao của tháp, nhiệt độ sôi cũng thay đổi tương
ứng với sự thay đổi nồng độ.
Trên mỗi mâm xảy ra quá trình truyền khối giữa pha lỏng và pha hơi. Một phần cấu tử
dễ bay hơi chuyển từ pha lỏng vào pha hơi và một ít chuyển từ pha hơi vào pha lỏng. 11
Lặp lại nhiều lần bốc hơi và ngưng tụ, cuối cùng trên đỉnh tháp ta thu được cấu tử dễ
bay hơi ở dạng nguyên chất và ở đáy tháp ta thu được cấu tử khó bay hơi ở dạng nguyên chất.
Theo lý thuyết, số mâm của tháp bằng số bậc thay đổi nồng độ.
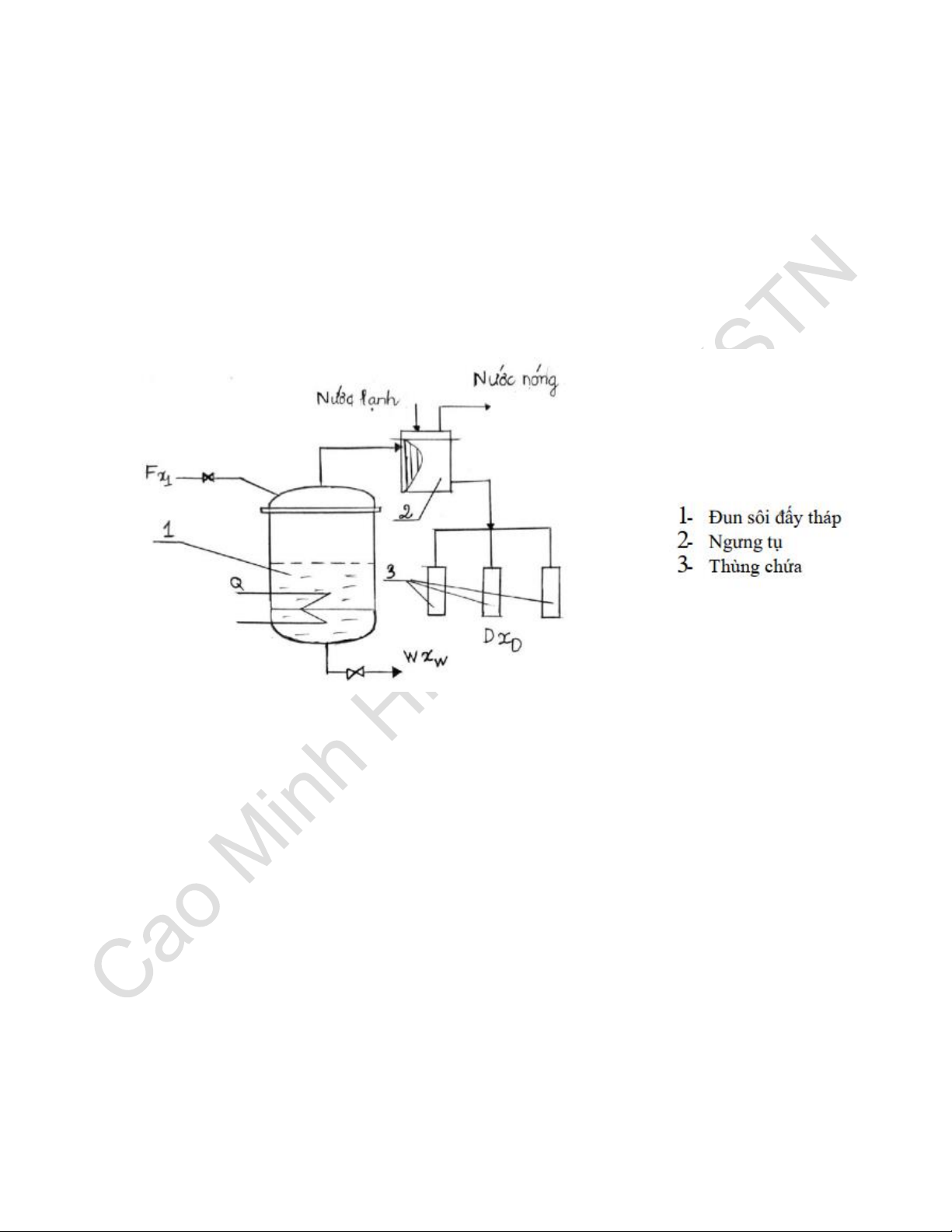
Câu 10. Thuyết minh quy trình chưng một bậc, kể rõ các thiết bị chính trong quy
trình? Ưu, nhược điểm và khắc phục? Ứng dụng của quy trình này?
Hỗn hợp được cho vào nồi đun 1 và được gia nhiệt. Phần hơi bay lên được dẫn sang
thiết bị ngưng tụ 2. Sau quá trình ta thu được:
Sản phẩm đỉnh: lượng lỏng có nồng độ cấu tử dễ bay hơi 𝑥𝐷 cao.
Sản phẩm đáy: lượng lỏng có nồng độ cấu tử khó bay hơi 𝑥𝑊 cao. Ứng dụng:
- Sử dụng chưng một bậc khi nhiệt độ sôi 2 cấu tử khác xa nhau.
- Sản phẩm có độ tinh khiết không cao. - Tách sơ bộ hỗn hợp.
Ưu điểm: đơn giản, vốn đầu tư thấp, công nghệ linh động… 12 Nhược điểm:
- Nồng độ sản phẩm thấp, không đều.
- Hiệu suất, năng suất thấp.
- Tốn nhân công, chi phí năng lượng.
- Khó cơ giới hóa, tư động hóa. Khắc phục:
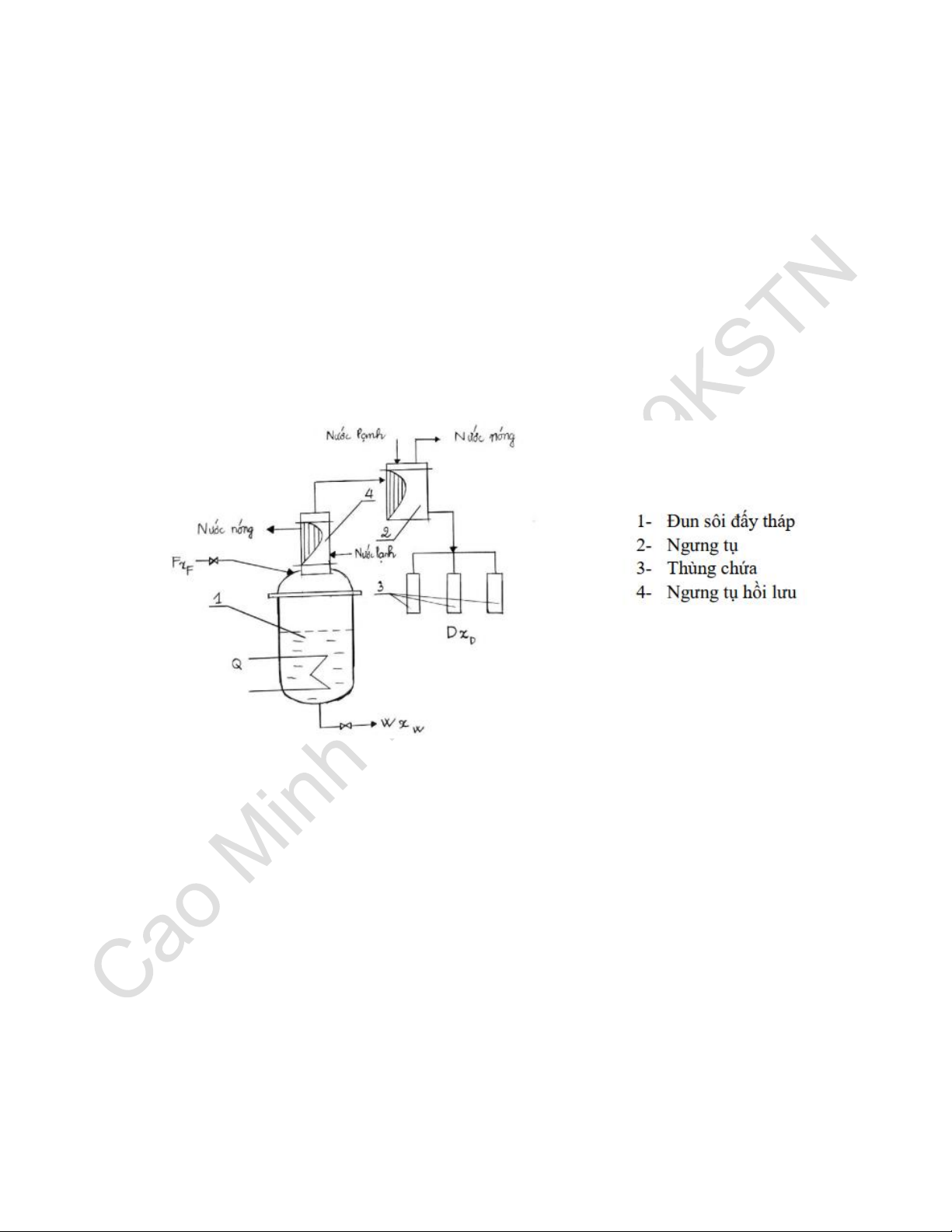
- Để tăng nồng độ sản phẩm đỉnh, gắn thêm thiết bị ngưng tụ hồi lưu:
- Sử dụng lại sản phẩm đáy để chưng cất.
- Chưng đơn giản nhiều lần có thiết bị ngưng tụ ở mỗi bậc.
- Sử dụng nồi chồng lên nhau => tháp chưng luyện.
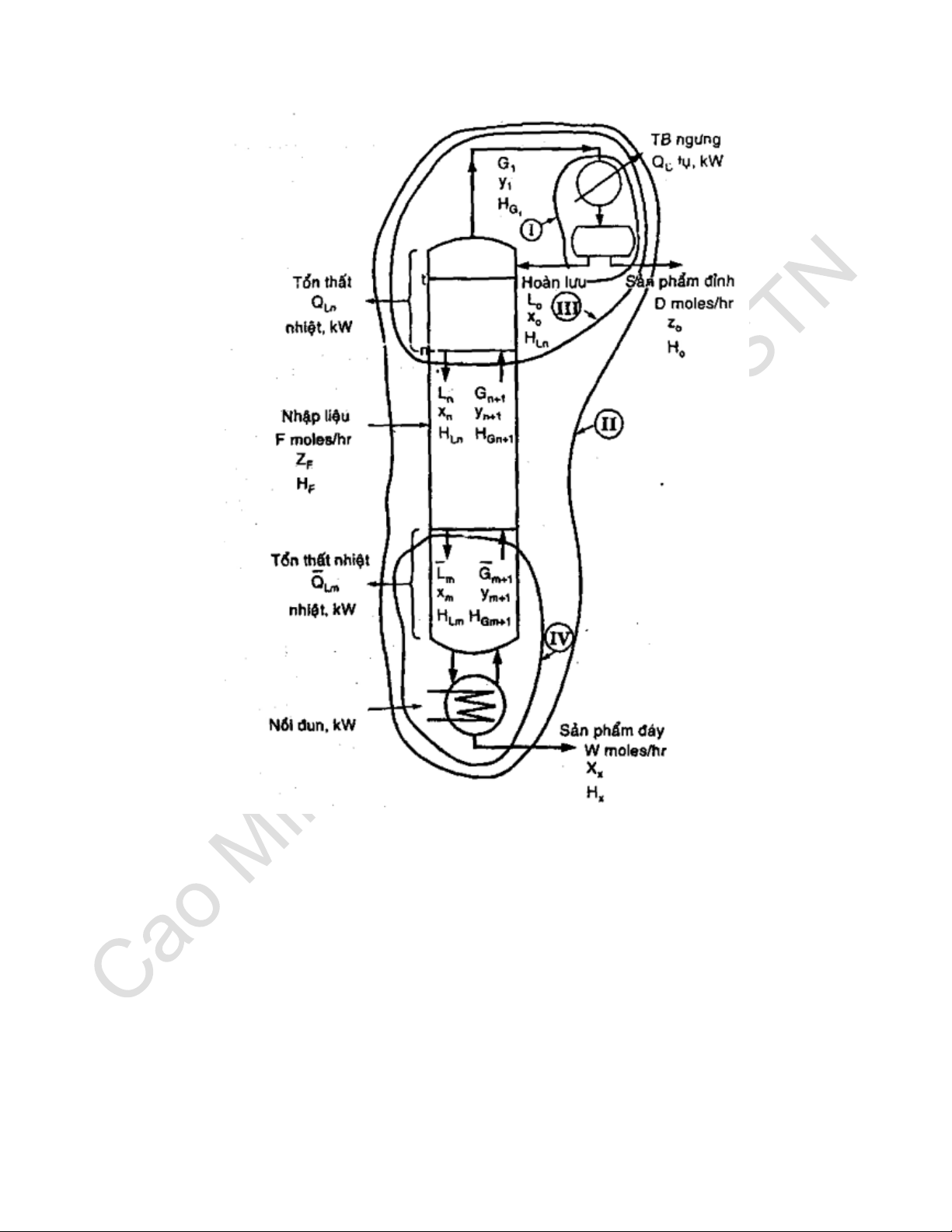
Câu 11. Thiết lập phương trình cân bằng vật chất cho quá trình chưng cất liên tục? 13
Hình: Cân bằng vật chất và năng lượng cho tháp chưng cất
Cân bằng vật chất: 𝐹 = 𝐷 + 𝑊 Trong đó:
𝐹 là suất lượng mol nhập liệu (kmol / h).
𝐷 là suất lượng mol sản phẩm đỉnh (kmol / h). 14
𝑊 là suất lượng mol sản phẩm đáy (kmol / h).
Cân bằng cấu tử dễ bay hơi:
𝐹 × 𝑥𝐹 = 𝐷 × 𝑥𝐷 + 𝑊 × 𝑥𝑊
𝑥𝐹, 𝑥𝐷, 𝑥𝑊 là nồng độ phần mol cấu tử dễ bay hơi trong nhập liệu, sản phẩm đỉnh, sản
phẩm đáy (kmol / kmol hỗn hợp)
Câu 12. Thiết lập phương trình cân bằng năng lượng cho quá trình chưng cất liên tục?
Thiết bị gia nhiệt cho nhập liệu: 𝑄 = 𝐷 𝑆
1 × 𝑟1 = 𝐹 × 𝐶𝐹 × (𝑡𝐹 − 𝑡𝐹) + 𝑄𝑚
𝐷1 là lượng hơi đốt cần sử dụng.
𝑟1 là nhiệt hóa hơi của hơi đốt.
𝐹 là lưu lượng nhập liệu.
𝐶𝐹 là nhiệt dung riêng của nhập liệu.
𝑄𝑚 là năng lượng mất mát ra môi trường (𝑄𝑚 = 5 ÷ 10% × 𝑄)
Thiết bị ngưng tụ:
* Ngưng tụ hoàn toàn:
𝑄 = 𝐺𝑦 × 𝑟𝐷 = 𝐷 × (𝑅 + 1) × 𝑟𝐷 = 𝐺1 × 𝐶1 × (𝑡𝑟 − 𝑡𝑣) + 𝑄𝑚
* Ngưng tụ hồi lưu: 𝑄 = 𝐺 ′ ′
𝑥 × 𝑟𝐷 = 𝐷 × 𝑅 × 𝑟𝐷 = 𝐺1 × 𝐶1 × (𝑡𝑟 − 𝑡𝑣) + 𝑄𝑚
𝑟𝐷: nhiệt ngưng tụ của hỗn hợp hơi đỉnh tháp. 𝐺 ′ : lưu lượng nướ 1, 𝐺1 c cần làm lạnh. 𝐶 ’
1, 𝐶1: nhiệt dung riêng nước làm lạnh.
𝑡𝑣, 𝑡𝑟: nhiệt độ vào và ra nước giải nhiệt 15 𝑄 : năng lượ 𝑚
ng mất mát ra môi trường xung quanh (5÷10%Q).
Thiết bị làm lạnh:
* Thiết bị làm lạnh sản phẩm đỉnh:
𝑄 = 𝐷 × 𝐶𝐷 × (𝑡𝑆𝐷 − 𝑡𝐷) = 𝐺2 × 𝐶2 × (𝑡𝑟 − 𝑡𝑣) + 𝑄𝑚
* Thiết bị làm lạnh sản phẩm đáy:
𝑄 = 𝑊 × 𝐶𝑊 × (𝑡𝑆𝑊 − 𝑡𝑊) = 𝐺3 × 𝐶3 × (𝑡𝑟 − 𝑡𝑣) + 𝑄𝑚
𝐶𝐷: nhiệt dung riêng của hỗn hợp hơi đỉnh tháp.
𝐶𝑊 : nhiệt dung riêng của hỗn hợp hơi đáy tháp. 𝐺 : lưu lượng nướ 2, 𝐺3 c cần làm lạnh.
𝐶2, 𝐶3: nhiệt dung riêng nước làm lạnh.
𝑡𝑣, 𝑡𝑟: nhiệt độ vào và ra nước giải nhiệt. 𝑄 : năng lượ 𝑚
ng mất mát ra môi trường xung quanh, 5÷10%Q.
Cân bằng nhiệt lượng toàn tháp:
𝐷2 là lưu lượng hơi cần đun nóng.
𝑟2 là nhiệt hóa hơi của hơi đốt.
𝑄𝑚 là năng lượng mất mát ra môi trường xung quanh, 𝑄𝑚 = 5 ÷ 10% × 𝑄 16
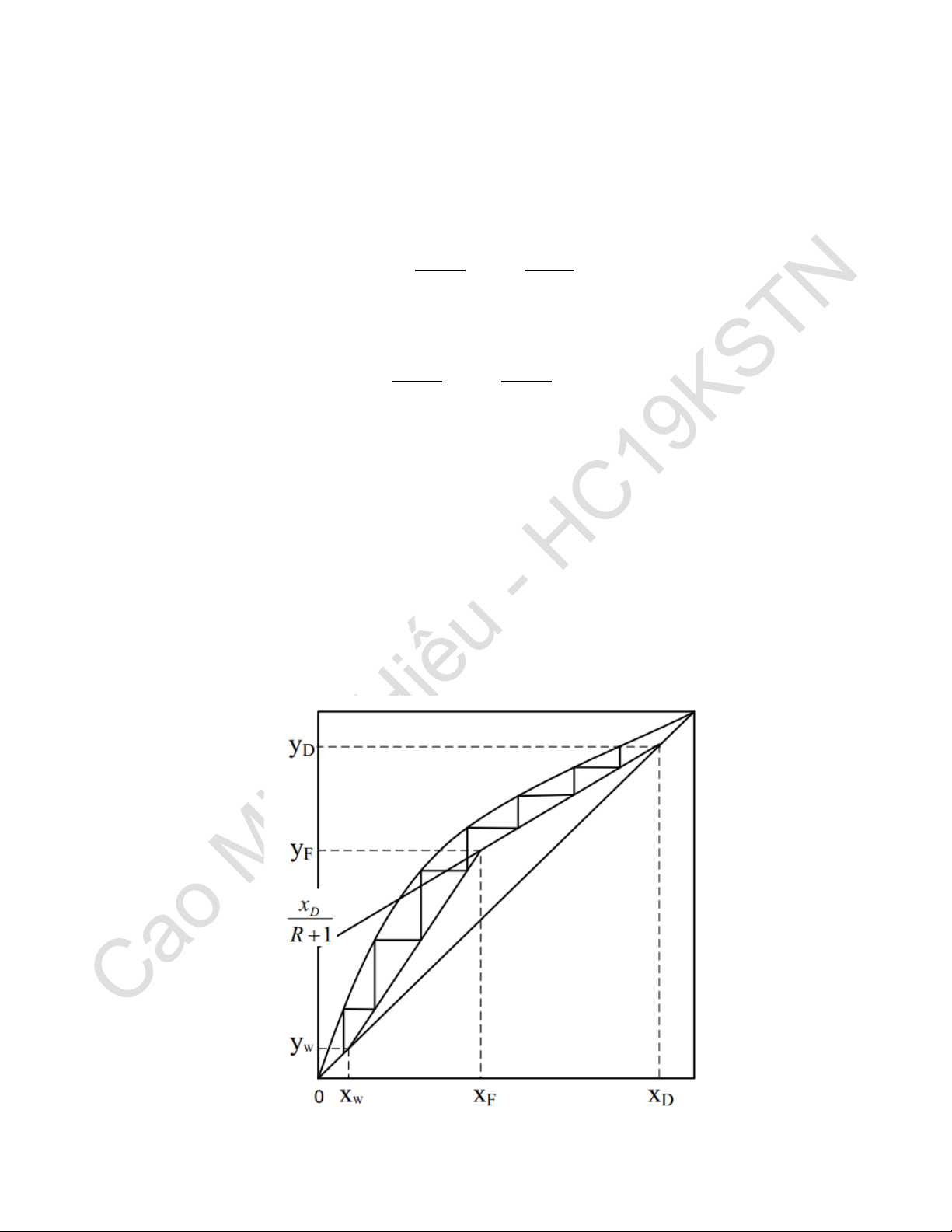
Câu 13. Cách xác định số mâm lý thuyết?
Bước 1: Vẽ đường cân bằng.
Bước 2: Vẽ đường làm việc phần chưng. 𝑹 𝒙 𝒚 = × 𝒙 + 𝑫 𝑹 + 𝟏 𝑹 + 𝟏
Bước 3: Vẽ đường làm việc phần cất. 𝑳 + 𝑹 𝑳 − 𝟏 𝒚 = × 𝒙 − × 𝒙 𝑹 + 𝟏 𝑹 + 𝟏 𝑫
Bước 4: Từ vị trí (𝑥𝐷, 𝑦𝐷) tại đường cất, ta kẻ ngang chạm đường cân bằng, sau đó kẻ
thẳng đứng xuống chạm đường làm việc, tạo thành các tam giác. Cứ như vậy cho đến khi
đạt bằng hoặc đi qua điểm (𝑥𝑊, 𝑦𝑊) thì dừng lại. Đếm số tam giác ta được số mâm lý thuyết cần tìm.
Câu 14. Cách xác định vị trí mâm nhập liệu?
Sau khi xác định số mâm lý thuyết, ta dựa vào giao điểm của đoạn chưng và đoạn cất,
ứng với số mâm thứ mấy thì đó là số mâm nhập liệu. 17
Dựa vào đồ thị, ta có thể thấy vị trí mâm nhập liệu tại (𝑥𝐹, 𝑦𝐹) ứng với mâm số 4 từ trên xuống.
Câu 15. Thế nào là chỉ số hoàn lưu? Thế nào là chỉ số hoàn lưu tối ưu? Cách xác
định chỉ số hoàn lưu?
Chỉ số hoàn lưu R là lượng lỏng hoàn lưu ứng với 1kmol sản phẩm đỉnh. 𝐿 𝑅 = 0 𝐷
𝐿0 là suất lượng mol hoàn lưu.
𝐷 là suất lượng mol sản phẩm đỉnh.
Chỉ số hoàn lưu tối ưu (R tối ưu) là chỉ số hoàn lưu dùng để thiết kế ứng với chi phí thấp nhất.
Có 3 cách xác định chỉ số hoàn lưu:
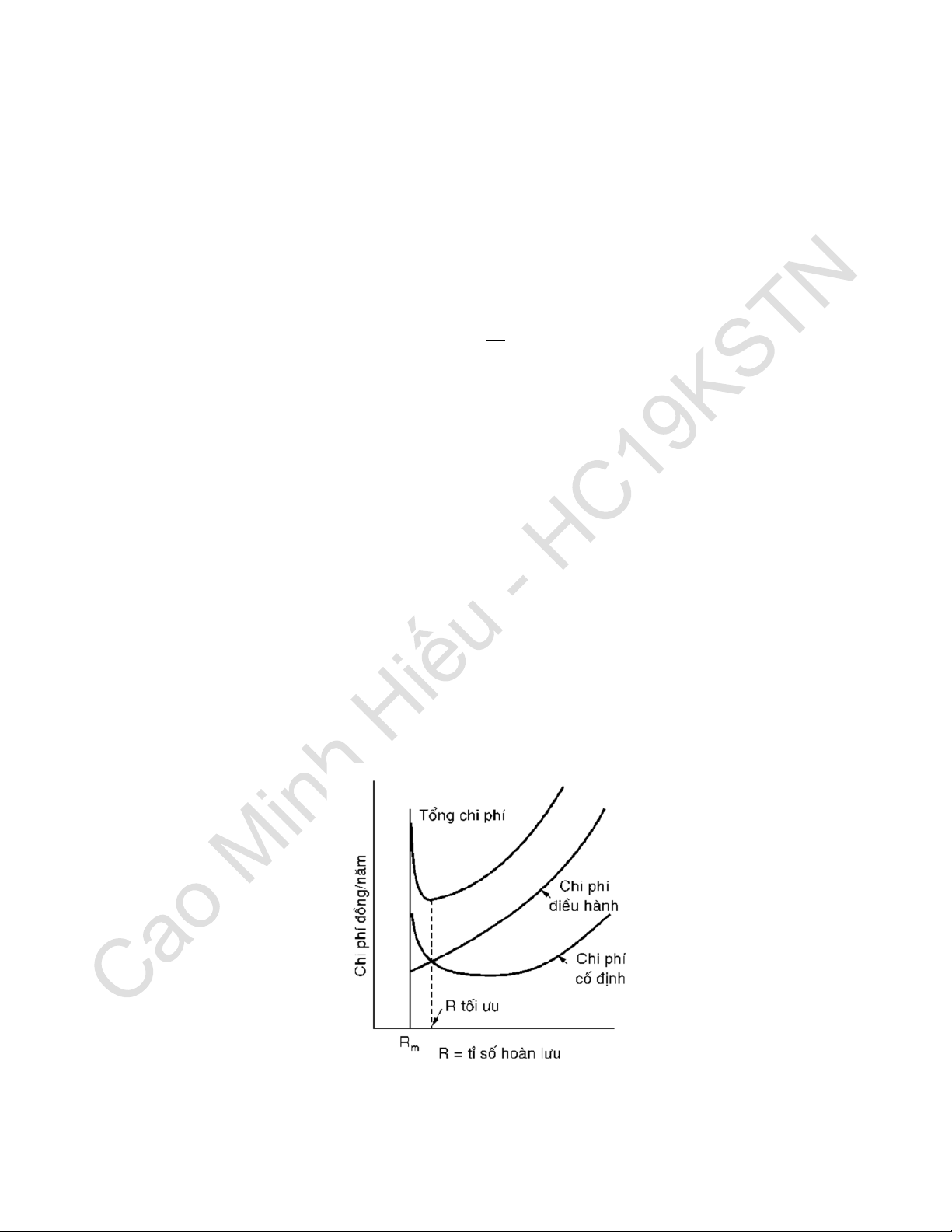
Cách 1: Xác định theo chỉ tiêu kinh tế - kỹ thuật: tổng chi phí của quá trình chưng cất là
nhỏ nhất (ta được R tối ưu).
𝑆𝑚𝑖𝑛 = 𝑆1 + 𝑆2 + 𝑆3
𝑆1 là chi phí cố định, 𝑆2 là chi phí điều hành, 𝑆3 là chi phí gián tiếp. 18
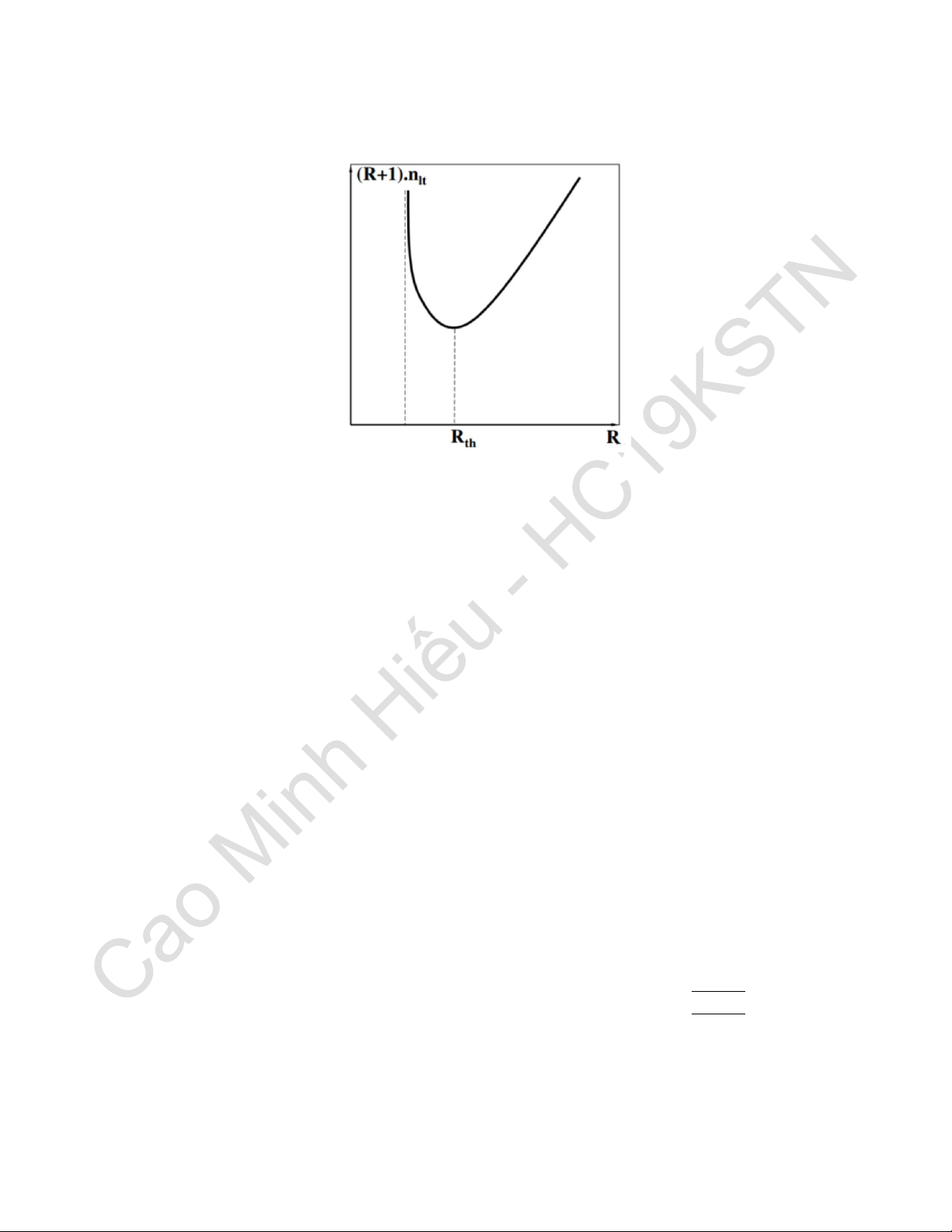
Cách 2: Xác định theo thể tích tháp nhỏ nhất: lập bảng 𝑅, 𝑛𝑙𝑡, 𝑉 (ta được R tối ưu).
Cách 3: Sử dụng công thức thực nghiệm
𝑅 = 𝑏 × 𝑅𝑚𝑖𝑛 với 𝑏 là hệ số dư.
𝑅 = 1.3 × 𝑅𝑚𝑖𝑛 + 0.3
Hoặc 𝑅 = (1.2 ÷ 2.5) × 𝑅𝑚𝑖𝑛
Chỉ số hoàn lưu là đại lượng có ảnh hưởng lớn đến quá trình chưng cất. Ảnh hưởng đến
chi phí vận hành, chi phí đầu tư và chất lượng sản phẩm. Khi R tăng:
- Lượng lỏng hồi lưu tăng => tăng chi phí bơm, xử lý lỏng.
- Lượng nước giải nhiệt tăng => tăng chi phí nhiên liệu cho thiết bị.
- Hệ số góc đường làm việc tăng => động lực quá trình tăng, số đĩa lý thuyết giảm.
- Khi R tăng đến vô cùng, đường làm việc sẽ là đường y = x, khi đó số đĩa lý thuyết là cực tiểu.
- 𝐺 = (𝑅 + 1) × 𝐷 => khi R tăng thì lượng hơi G tăng, mà 𝐷 = √ 𝐺 nên đường 0.785×𝑣
kính của tháp tăng => tốn chi phí mua / thuê đất và lắp đặt thiết bị.
Câu 16. Thế nào là chỉ số hoàn lưu tối thiểu? 19
Chỉ số hoàn lưu tối thiểu Rmin là chỉ số hoàn lưu ứng với động lực quá trình bằng 0
(đường làm việc cắt đường cân bằng tại (𝑥 ∗
𝐹, 𝑦𝐹)) và số mâm lý thuyết là vô cùng.
Có 2 cách xác định Rmin:
Cách 1: Dùng công thức 𝑥 ∗ 𝑅 𝐷 − 𝑦𝐹 𝑚𝑖𝑛 = 𝑦∗𝐹 − 𝑥𝐹
𝑥𝐷 là nồng độ phần mol cấu tử dễ bay hơi trong sản phẩm đỉnh.
𝑥𝐹 là nồng độ phần mol cấu tử dễ bay hơi trong nhập liệu. Từ 𝑥 ∗
𝐹 ta tra số liệu đường cân bằng => 𝑦𝐹
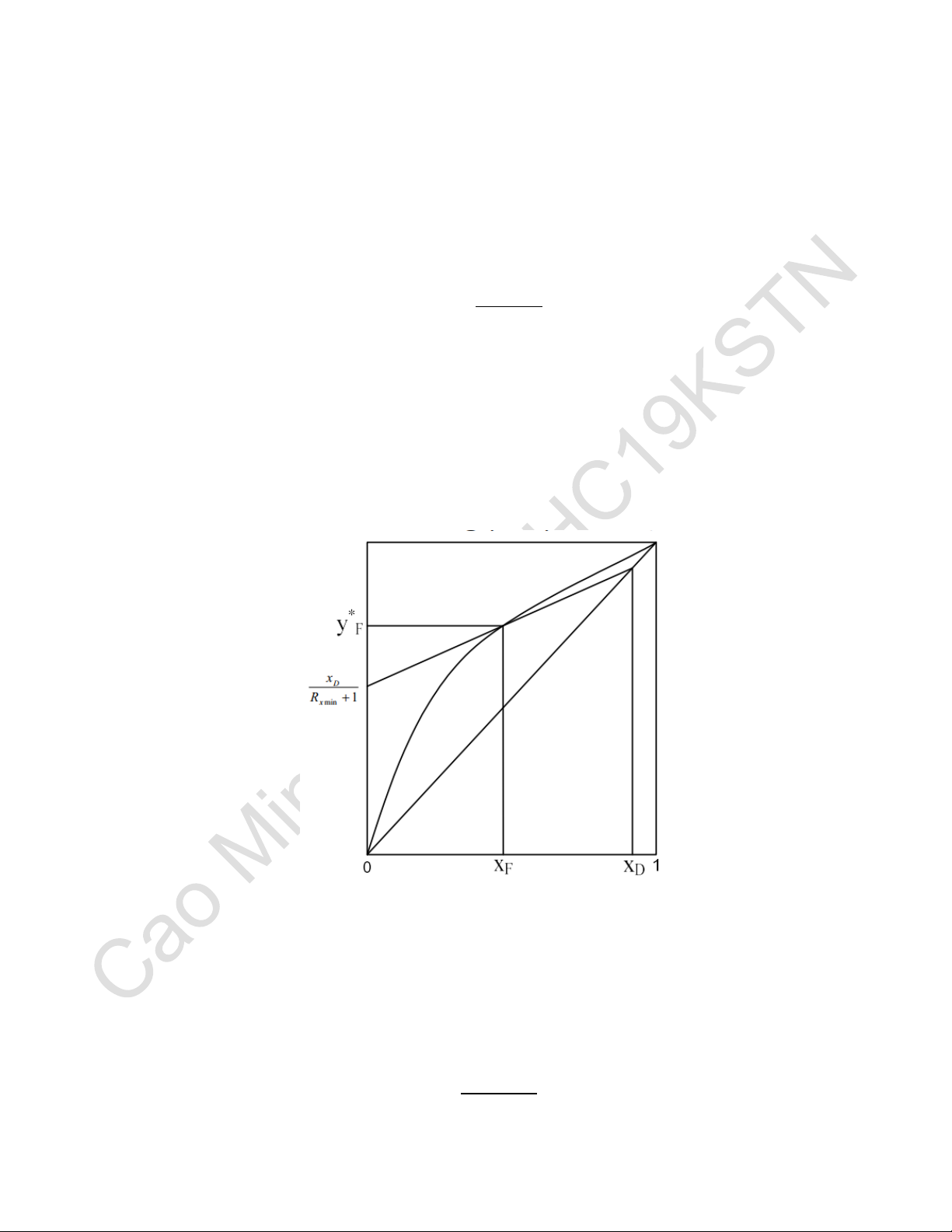
Cách 2: Xác định bằng đồ thị Bước 1: Từ 𝑥 ∗
𝐹 gióng thẳng đứng lên trên, cắt đường cân bằng tại 𝑦𝐹 (áp dụng cho trường
hợp nhập liệu là hỗn hợp lỏng sôi). Bước 2: Từ điểm (𝑥 ∗ ∗
𝐷, 𝑦𝐷) dựng đường thẳng cắt (𝑥𝐹, 𝑦𝐹) cắt trục tung tại điểm (0, 𝑦0).
Điểm đó được xác định bằng công thức: 𝑥 𝑦∗ 𝐷 0 = 𝑅𝑚𝑖𝑛 + 1 20



