! "
#$%
& Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ ' đến '(Mỗi câu hỏi
thí sinh chỉ chọn một phương án.
'&Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng
% một electron chung. ) sự cho – nhận electron.
chỉ một cặp electron chung. * một hay nhiều cặp electron chung.
'Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng
% số electron. ) số lớp electron. số electron hóa trị. * số e lớp ngoài cùng.
'+Nguyên tố R ở nhóm A, nguyên tử R có phân lớp electron ngoài cùng là 4s
1
. Số hiệu nguyên tử
của nguyên tố R là
% 19 hoặc 24 hoặc 29. ) 19. 29. * 24.
'!Cấu hình electron nguyên tử nào sau đây của nguyên tố kim loại?
% 1s
2
. ) 1s
2
2s
2
2p
6
. 1s
2
2s
2
2p
5
. * 1s
2
2s
2
2p
6
3s
2
.
'"Cho các nguyên tố:
8
X,
11
R,
6
Y. Bán kính nguyên tử của các nguyên tố tăng dần theo thứ tự
% X < Y < R. ) Y < X< R. R < X< Y. * R < Y< X.
',Dãy các chất nào sau đây sắp xếp theo chiều tăng tính base
% NaOH<Al(OH)
3
<Mg(OH)
2
. ) Mg(OH)
2
<NaOH<Al(OH)
3
.
Al(OH)
3
<NaOH<Mg(OH)
2
. * Al(OH)
3
<Mg(OH)
2
<NaOH.
'-Nguyên tử nguyên tố X có tổng số electron trên phân lớp p là 11. Hãy cho biết cấu hình electron
lớp ngoài cùng của nguyên tử X và kiểu xen phủ các orbital trong nguyên tử để tạo ra phân tử X
2
?
% 3s
2
3p
5
, kiểu xen phủ trục p-p. ) 3s
2
3p
5
, kiểu xen phủ bên p-p.
3s
1
, kiểu xen phủ s-s. * 3s
2
3p
5
, kiểu xen phủ s-p.
'(&Trong các hợp chất sau đây, hợp chất nào là hợp chất ion?
% H
2
O ) H
2
S KBr * NH
3
'.Cấu hình electron lớp ngoài cùng của nguyên tử X có dạng ns
2
np
3
. Trong hợp chất cao nhất với
oxygen, X chiếm 43,662% về khối lượng. Phần trăm của X trong hợp chất với hydrogen là
% 91,176%. ) 17,648%. 82,352%. * 8,824%.
' Hạt nhân nguyên tử X có 17 proton và 20 neutron. Ký hiệu nguyên tử X là
%
20
37
X
. )
17
37
X
.
17
20
X
. *
17
54
X
.
'Công thức Lewis của phân tử O
2
là
% O = O ) # O = O# #
. .
O
. .
=
. .
O
. .
# *
. .
O
. .
=
. .
O
. .
'Cho độ âm điện các nguyên tố K(0,82); O(3,44); Cl(3,16); H(2,20); N(3,04). Hợp chất có liên
kết cộng hóa trị phân cực mạnh nhất là
% KCl ) Cl
2
O
7
NH
3
* H
2
O
'+Chất nào sau đây có cả liên kết ion, liên kết CHT phân cực và liên kết cho nhận?
% HNO
3
) NaNO
3
NaOH * K
2
CO
3
'!Nguyên tố X thuộc nhóm A trong bảng tuần hoàn. Oxide cao nhất của X có công thức hóa học là
XO
3
. Số electron lớp ngoài cùng của X là
% 8 ) 6 3 * 2
'"X, Y, Z là 3 nguyên tố thuộc cùng chu kì của bảng tuần hoàn. Biết oxide của X khi tan trong
nước tạo thành một dung dịch làm hồng quỳ tím, Y phản ứng với nước tạo thành một dung dịch làm xanh
giấy quỳ tím, còn Z phản ứng được với cả dung dịch acid và dung dịch kiềm. Nếu xếp theo trật tự tăng
dần độ âm điện thì trật tự đúng sẽ là
% Y<Z<X. ) Z<Y<X. X<Y<Z. * X<Z<Y.
',Chất nào sau đây đều có liên kết hydrogen giữa các phân tử?
% SiH
4
; CH
4
. ) H
2
O; HF. PH
3
; NH
3
. * H
2
S; HCl.
/01

'-&Cho 9,0g hỗn hợp 2 kim loại A, B hòa tan hoàn toàn trong dung dịch HCl dư thu được 7,437 lít
khí H
2
(đkc). A, B thuộc 2 chu kì liên tiếp nhau và thuộc nhóm IIA. A, B là các nguyên tố
A. Be, Ca. B. Ca, Sr. C. Be, Mg. D. Mg, Ca.
'(Cho các phát biểu sau
a. Liên kết ion là liên kết được hình thành bỡi lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
b. Trong phân tử C
2
H
2
có một liên kết ba.
c. Mỗi cặp electron góp chung tạo nên hai liên kết cộng hóa trị.
d. Độ âm điện của một nguyên tử đặc trưng cho khả năng nhường electron của nguyên tử đó khi hình
thành liên kết hóa học.
e. Liên kết giữa nguyên tử C và O phân cực nên phân tử CO
2
phân cực.
Số phát biểu 20là
A. 1 B. 3 C. 4 D. 2
& Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4.Trong mỗi ý a), b), c), d) ở mỗi
câu, thí sinh chọn đúng hoặc sai.(Đ – S)
' Nguyên tố X được sử dụng làm vật liệu máy bay, ô tô, tên lửa, tàu vũ trụ. Trong bảng tuần hoàn,
X thuộc chu kì 3, nhóm IIIA.
0 X có tính kim loại mạnh hơn Mg(Z=12).
3 Oxide cao nhất của X có công thức hóa học X
2
O
3
.
Hợp chất hydroxide của X có công thức hóa học X(OH)
3
.
4 Hydroxide của X có tính base mạnh.
'Khí CO
2
có trong khí quyển và sự gia tăng hàm lượng CO
2
là nguyên nhân chính gây ra hiệu ứng
nhà kính. Cho độ âm điện của nguyên tử C là 2,55 và O là 3,44.
0Phân tử CO
2
là phân tử không phân cực.
3. Phân tử CO
2
có 2 xen phủ s-p và 2 xen phủ p-p.
Trong phân tử CO
2
có 2 liên kết σ và 2 kiên kết π.
4Trong phân tử CO
2
có 4 cặp e hóa trị riêng chưa tham gia liên kết.
'+Nguyên tố Y là kim loại cứng nhất, dùng trong dao cắt kính và ở ô số 24 của bảng tuần hoàn.
a. Y có 6 e hóa trị và là nguyên tố kim loại.
b. Y là nguyên tố d.
c. Y ở chu kì 4 của bảng tuần hoàn.
d. Ở trạng thái cơ bản, Y có 6 e ở phân lớp s.
'!Cho 5 nguyên tố A, X, Y, Z, T theo thứ tự thuộc 5 ô liên tiếp nhau trong bảng tuần hoàn các
nguyên tố hóa học, có số hiệu nguyên tử tăng dần. Tổng số hạt mang điện trong 5 nguyên tử của 5 nguyên
tố trên bằng 100.
0 Nguyên tố A là oxygen và T là nguyên tố Magnesium.
3 A, X, Y thuộc loại là nguyên tố p.
Z, T thuộc cùng một nhóm.
4 Z, T thuộc loại là nguyên tố phi kim.
&# Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
'# Trong tự nhiên, bromine có 2 đồng vị là
79
Br có hàm lượng 50,7% còn lại là
81
Br. Nguyên tử khối
trung bình của bromine là bao nhiêu?
'Cho các chất sau: NaCl, H
2
O, K
2
O, BaCl
2
, CaF
2
, HCl, NH
4
NO
3
. Có bao nhiêu chất chứa liên kết
ion?
'+Tổng số cặp electron dùng chung giữa các nguyên tử trong phân tử ethylene (C
2
H
4
) là bao nhiêu?
'!Hợp chất khí với hydrogen của nguyên tố X có công thức XH
4
, được sử dụng làm tác nhân ghép
nối để bám dính các sợi như sợi thủy tinh và sợi carbon. Oxide cao nhất của X chứa 53,3% oxygen về
/01

khối lượng, thường được dùng để sản xuất cửa sổ, lọ thủy tinh. Hãy cho biết giá trị nguyên tử khối trung
bình của X là bao nhiêu?
'" Trong sản xuất thịt chế biến sẵn, người ta thường bổ sung một hợp chất có công thức dạng X
2
Y để
ức chế sự sinh sôi phát triển của vi khuẩn trong thịt, giúp thịt lâu hư, tránh các trường hợp ngộ độc thực
phẩm do thịt bị ôi thiu. Phân tử X
2
Y có tồng số proton là 23. Biết X, Y ở hai nhóm A liên tiếp trong cùng
một chu kì. Phần trăm khối lượng của Y trong oxide cao nhất của Y là bao nhiêu?
', Hợp chất X có công thức là A
2
B có tổng số hạt (p, n, e) là 92, trong đó số hạt mang điện nhiều hơn
số hạt không mang điện là 28. Nguyên tử nguyên tố A có số proton nhiều hơn so với nguyên tử nguyên tố
B là 3. Số hạt mang điện của nguyên tử A là ?
555555555555555565555555555555555
7789%
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 * 10 )
2 ) 11 *
3 ) 12 %
4 * 13 )
5 % 14 )
6 * 15 %
7 % 16 )
8 17 *
9 % 18 )
:# Điểm tối đa của 01 câu hỏi là 1 điểm
- Thí sinh chỉ lựa chọn chính xác 01 ý trong 1 câu hỏi được =>?
- Thí sinh chỉ lựa chọn chính xác 02 ý trong 1 câu hỏi được =">?
- Thí sinh chỉ lựa chọn chính xác 03 ý trong 1 câu hỏi được =">?
- Thí sinh lựa chọn chính xác cả 04 ý trong 1 câu hỏi được >?
' @AB ;<;CDEF ' @AB ;<;CDEF
a E + a
b b
c E c
d E d E
a ! a
b E b
c c E
d d E
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 -.=.(, 4 (
2 " 5 + =!+
3 , 6
Lưu ý: Phần nhận biết HS trả lời đáp án khác nhưng đúng vẫn cho điểm tối đa
/01+

;<;GHI14J
& Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ ' đến '(Mỗi câu hỏi
thí sinh chỉ chọn một phương án.
'&Liên kết cộng hóa trị là liên kết hóa học được hình thành giữa hai nguyên tử bằng
) một electron chung. B. sự cho – nhận electron.
C. chỉ một cặp electron chung. D. một hay nhiều cặp electron chung.
'Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng
) số electron. B. số lớp electron. C. số electron hóa trị. D. số e lớp ngoài cùng.
'+Nguyên tố R ở nhóm A, nguyên tử R có phân lớp electron ngoài cùng là 4s
1
. Số hiệu nguyên tử
của nguyên tố R là
) 19 hoặc 24 hoặc 29. B. 19. C. 29. D. 24.
'!Cấu hình electron nguyên tử nào sau đây của nguyên tố kim loại?
) 1s
2
. B. 1s
2
2s
2
2p
6
. C. 1s
2
2s
2
2p
5
. D. 1s
2
2s
2
2p
6
3s
2
.
'"Cho các nguyên tố:
8
X,
11
R,
6
Y. Bán kính nguyên tử của các nguyên tố tăng dần theo thứ tự
) X < Y < R. B. Y < X< R. C. R < X< Y. D. R < Y< X.
',Dãy các chất nào sau đây sắp xếp theo chiều tăng tính base
) NaOH<Al(OH)
3
<Mg(OH)
2
. B. Mg(OH)
2
<NaOH<Al(OH)
3
.
C. Al(OH)
3
<NaOH<Mg(OH)
2
. D. Al(OH)
3
<Mg(OH)
2
<NaOH.
'-Nguyên tử nguyên tố X có tổng số electron trên phân lớp p là 11. Hãy cho biết cấu hình electron
lớp ngoài cùng của nguyên tử X và kiểu xen phủ các orbital trong nguyên tử để tạo ra phân tử X
2
?
) 3s
2
3p
5
, kiểu xen phủ trục p-p. B. 3s
2
3p
5
, kiểu xen phủ bên p-p.
C. 3s
1
, kiểu xen phủ s-s. D. 3s
2
3p
5
, kiểu xen phủ s-p.
'(&Trong các hợp chất sau đây, hợp chất nào là hợp chất ion?
) H
2
O B. H
2
S C. KBr D. NH
3
'.Cấu hình electron lớp ngoài cùng của nguyên tử X có dạng ns
2
np
3
. Trong hợp chất cao nhất với
oxygen, X chiếm 43,662% về khối lượng. Phần trăm của X trong hợp chất với hydrogen là
) 91,176%. B. 17,648%. C. 82,352%. D. 8,824%.
' Hạt nhân nguyên tử X có 17 proton và 20 neutron. Ký hiệu nguyên tử X là
)
20
37
X
. B.
17
37
X
. C.
17
20
X
. D.
17
54
X
.
'Công thức Lewis của phân tử O
2
là
A. O = O B. # O = O# C. #
. .
O
. .
=
. .
O
. .
# D.
. .
O
. .
=
. .
O
. .
'Cho độ âm điện các nguyên tố K(0,82); O(3,44); Cl(3,16); H(2,20); N(3,04). Hợp chất có liên
kết cộng hóa trị phân cực mạnh nhất là
) KCl B. Cl
2
O
7
C. NH
3
D. H
2
O
'+Chất nào sau đây có cả liên kết ion, liên kết CHT phân cực và liên kết cho nhận?
) HNO
3
B. NaNO
3
C. NaOH D. K
2
CO
3
'!Nguyên tố X thuộc nhóm A trong bảng tuần hoàn. Oxide cao nhất của X có công thức hóa học là
XO
3
. Số electron lớp ngoài cùng của X là
) 8 B. 6 C. 3 D. 2
'"X, Y, Z là 3 nguyên tố thuộc cùng chu kì của bảng tuần hoàn. Biết oxide của X khi tan trong
nước tạo thành một dung dịch làm hồng quỳ tím, Y phản ứng với nước tạo thành một dung dịch làm xanh
giấy quỳ tím, còn Z phản ứng được với cả dung dịch acid và dung dịch kiềm. Nếu xếp theo trật tự tăng
dần độ âm điện thì trật tự đúng sẽ là
) Y<Z<X B. Z<Y<X C. X<Y<Z D. X<Z<Y
',Chất nào sau đây đều có liên kết hydrogen giữa các phân tử?
) SiH
4
; CH
4
B. H
2
O; HF C. PH
3
; NH
3
D. H
2
S; HCl
'-&Cho 9,0g hỗn hợp 2 kim loại A, B hòa tan hoàn toàn trong dung dịch HCl dư thu được 7,437 lít
khí H
2
(đkc). A, B thuộc 2 chu kì liên tiếp nhau và thuộc nhóm IIA. A, B là các nguyên tố
/01!

B. Be, Ca B. Ca, Sr C. Be, Mg D. Mg, Ca
'(Cho các phát biểu sau
f. Liên kết ion là liên kết được hình thành bỡi lực hút tĩnh điện giữa các ion mang điện tích trái dấu
g. Trong phân tử C
2
H
2
có một liên kết ba
h. Mỗi cặp electron góp chung tạo nên hai liên kết cộng hóa trị
i. Độ âm điện của một nguyên tử đặc trưng cho khả năng nhường electron của nguyên tử đó khi hình
thành liên kết hóa học
j. Liên kết giữa nguyên tử C và O phân cực nên phân tử CO
2
phân cực.
Số phát biểu 20là
B. 1 B. 3 C. 4 D. 2
& Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4.Trong mỗi ý a), b), c), d) ở mỗi
câu, thí sinh chọn đúng hoặc sai.(Đ – S)
' Nguyên tố X được sử dụng làm vật liệu máy bay, ô tô, tên lửa, tàu vũ trụ. Trong bảng tuần hoàn,
X thuộc chu kì 3, nhóm IIIA.
0 X có tính kim loại mạnh hơn Mg(Z=12).
3 Oxide cao nhất của X có công thức hóa học X
2
O
3
.
Hợp chất hydroxide của X có công thức hóa học X(OH)
3
.
4 Hydroxide của X có tính base mạnh.
'Khí CO
2
có trong khí quyển và sự gia tăng hàm lượng CO
2
là nguyên nhân chính gây ra hiệu ứng
nhà kính. Cho độ âm điện của nguyên tử C là 2,55 và O là 3,44.
0Phân tử CO
2
là phân tử không phân cực.
3. Phân tử CO
2
có 2 xen phủ s-p và 2 xen phủ p-p.
Trong phân tử CO
2
có 2 liên kết σ và 2 kiên kết π.
4Trong phân tử CO
2
có 4 cặp e hóa trị riêng chưa tham gia liên kết.
'+Nguyên tố Y là kim loại cứng nhất, dùng trong dao cắt kính và ở ô số 24 của bảng tuần hoàn.
a. Y có 6 e hóa trị và là nguyên tố kim loại.
b. Y là nguyên tố d.
c. Y ở chu kì 4 của bảng tuần hoàn.
d. Ở trạng thái cơ bản, Y có 6 e ở phân lớp s.
'!Cho 5 nguyên tố A, X, Y, Z, T theo thứ tự thuộc 5 ô liên tiếp nhau trong bảng tuần hoàn các
nguyên tố hóa học, có số hiệu nguyên tử tăng dần. Tổng số hạt mang điện trong 5 nguyên tử của 5 nguyên
tố trên bằng 100.
0 Nguyên tố A là oxygen và T là nguyên tố Magnesium.
3 A, X, Y thuộc loại là nguyên tố p.
Z, T thuộc cùng một nhóm.
4 Z, T thuộc loại là nguyên tố phi kim.
HI14J1K
Gọi số hạt proton của A là Z
=> của X là Z+1; của Y là Z+2; của Z là Z+3; của T là Z+4
Theo bài ra ta có: 10Z + 20 = 100 => Z = 8.
=> A là
8
O&; X là
9
F&; Y là
10
Ne&; Z là
11
Na&; T là
12
Mg
A(Z=8): 1s
2
2s
2
2p
4
=> nguyên tố p ( có 6 electron lớp ngoài cùng nên thuộc loại nguyên tố phi kim)
X(Z= 9): 1s
2
2s
2
2p
5
=> nguyên tố p (có 7 electron lớp ngoài cùng nên thuộc loại nguyên tố phi kim).
Y(Z= 10): 1s
2
2s
2
2p
6
=> nguyên tố p (có 8 electron lớp ngoài cùng nên thuộc loại nguyên tố khí hiếm).
Z (Z=11): 1s
2
2s
2
2p
6
3s
1
=> nguyên tố s (có 1 electron lớp ngoài cùng nên thuộc loại nguyên tố kim loại,
thuộc nhóm IA).
T (Z=11): 1s
2
2s
2
2p
6
3s
2
=> nguyên tố s (có 2 electron lớp ngoài cùng nên thuộc loại nguyên tố kim loại,
thuộc nhóm IIA).
0 Nguyên tố A là oxygen và T là nguyên tố Magnesium. => Đúng
/01"

3 A, X, Y thuộc loại là nguyên tố p. => Đúng
Z, T thuộc cùng một nhóm => Sai
4 Z, T thuộc loại là nguyên tố phi kim. => Sai
&# Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
'# Trong tự nhiên, bromine có 2 đồng vị là
79
Br có hàm lượng 50,7% còn lại là
81
Br. Nguyên tử khối
trung bình của bromine là bao nhiêu?
HI14J1K
)/
5
'Cho các chất sau: NaCl, H
2
O, K
2
O, BaCl
2
, CaF
2
, HCl, NH
4
NO
3
. Có bao nhiêu chất chứa liên kết
ion?
'+Tổng số cặp electron dùng chung giữa các nguyên tử trong phân tử ethylene (C
2
H
4
) là bao nhiêu?
HI14J1K
L!MN6>OC!P<FQMN6>R5CP<F
'!Hợp chất khí với hydrogen của nguyên tố X có công thức XH
4
, được sử dụng làm tác nhân ghép
nối để bám dính các sợi như sợi thủy tinh và sợi carbon. Oxide cao nhất của X chứa 53,3% oxygen về
khối lượng, thường được dùng để sản xuất cửa sổ, lọ thủy tinh. Hãy cho biết giá trị nguyên tử khối trung
bình của X là bao nhiêu?
HI14J1K
SR1TU
!
2V/0W4UX
:/YWV1Z#"+=+5 suy ra X=28
'" Trong sản xuất thịt chế biến sẵn, người ta thường bổ sung một hợp chất có công thức dạng X
2
Y để
ức chế sự sinh sôi phát triển của vi khuẩn trong thịt, giúp thịt lâu hư, tránh các trường hợp ngộ độc thực
phẩm do thịt bị ôi thiu. Phân tử X
2
Y có tồng số proton là 23. Biết X, Y ở hai nhóm A liên tiếp trong cùng
một chu kì. Phần trăm khối lượng của Y trong oxide cao nhất của Y là bao nhiêu?
HI14J1K
[1</U
\ZQZ
U
]
\
5+CF
LZ%M6</1N^=0L
U
G
\
5CFP
\
G
U
5C+F
SCFQCF1K/0
U
5(CXF=
\
5-CFR1TX
Từ (1) và (3) giải ra P
X
, P
y
lẻ (loại)
', Hợp chất X có công thức là A
2
B có tổng số hạt (p, n, e) là 92, trong đó số hạt mang điện nhiều hơn
số hạt không mang điện là 28. Nguyên tử nguyên tố A có số proton nhiều hơn so với nguyên tử nguyên tố
B là 3. Số hạt mang điện của nguyên tử A là ?
HI14J1K
_`;a/11VMb%Q==<
;a/11VMb)Q==<
3Q/0=0L#!<]]<]5.
!<]<GG5(
/01,

G<5+
EV/0<5=<5(
cdV2ea01>Af0%Q]5
! "
#$%
& Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến '(Mỗi câu hỏi thí
sinh chỉ chọn một phương án.
'&Hạt mang điện trong hạt nhân nguyên tử là:
% Electron. ) Proton.
Neutron. * Neutron và electron.
'Cho các nguyên tử Những nguyên tử nào cùng thuộc một nguyên tố hóa học?
% X và Y. ) Y và Z. X và Z. *X, Y và Z.
'+Nitrogen trong thiên nhiên là hỗn hợp gồm hai đồng vị là (99,63%) và (0,37%). Nguyên tử khối
trung bình của nitrogen là:
%. 14,7. ) . 14,0. . 14,4. *. 13,7.
'!Sự phân bố electron theo ô orbital nào dưới đây là đúng?
% gg ) g g g gh g *. gg g g
'" Một nguyên tố R có cấu hình electron: 1s
2
2s
2
2p
6
3s
2
3p
4
, công thức hợp chất của R với hydrogen và công
thức oxide cao nhất là:
A. RH
2
, RO. B. RH
2
, RO
3
.& C. RH
2
, RO
2
. D. RH
5
, R
2
O
5
.
', Cấu hình electron nào sau đây không phải của kim loại?
% 1s
2
2s
2
2p
6
3s
2
3p
6
3d
6
4s
2
. ) 1s
2
2s
2
2p
6
3s
2
3p
5
.
1s
2
2s
2
2p
6
3s
2
. * 1s
2
2s
2
2p
6
3s
2
3p
1
.
'- Ion nào sau đây NR1 là ion đơn nguyên tử?
% Al
3+
. ) NO
3
-
. Br
-
. * Ca
2+
.
'( Sắp xếp tính base của NaOH, Mg(OH)
2
, Al(OH)
3
theo chiều giảm dần là:
% NaOH, Mg(OH)
2
, Al(OH)
3
) Al(OH)
3
, Mg(OH)
2
, NaOH
Mg(OH)
2
, Al(OH)
3
, NaOH
* Mg(OH)
2,
NaOH, Al(OH)
3
'.Vị trí của nguyên tử nguyên tố X có Z= 20 trong bảng tuần hoàn là:&
%Chu kì 4, nhóm VIIB.
)Chu kì 4, nhóm VIIIB.
Chu kì 4,nhóm IIA.
*Chu kì 3, nhóm IIB.
' Nguyên tố Ca có số hiệu nguyên tử là 20. Phát biểu nào sau đây về Ca làZNR1&đúng?
/01-
%Số electron ở vỏ nguyên tử của nguyên tố Ca là 20.
)Vỏ của nguyên tử Ca có 4 lớp electron và lớp ngoài cùng có 2 electron.
Hạt nhân của nguyên tố Ca có 20 proton.
*Nguyên tố Ca là một phi kim.
' Nguyên tử của nguyên tố A có tổng số electron ở phân lớp p là 5, Vị trí của nguyên tố A trong bảng tuần
hoàn là:
% Nhóm VA, chu kì 3. ) Nhóm VIIA, chu kì 2.
Nhóm VIIB, chu kì 2 . *Nhóm VIA, chu kì 3.
' Liên kết ion được tạo thành giữa?
% Hai nguyên tử kim loại.
) Hai nguyên tử phi kim.
Một nguyên tử kim loại điển hình và một nguyên tử phi kim điển hình.
* Ba nguyên tử trở lên.
'+ Nguyên tử của nguyên tố X có cấu hình electron 1s
2
2s
2
2p
6
3s
2
3p
6
4s
1
, nguyên tử của nguyên tố Y có cấu
hình electron 1s
2
2s
2
2p
5
. Liên kết hóa học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết nào?
%Kim loại. )Cộng hóa trị có cực. Ion. *Cộng hóa trị không cực.
'! Công thức cấu tạo nào sau đây là công thức Lewis?
% ) *
'" Dãy nào sau đây gồm các chất mà phân tử đều chỉ có liên kết cộng hóa trị phân cực?
%O
2
, H
2
O, NH
3
)H
2
O, HCl, H
2
S
HCl, N
2
, H
2
S *HCl, Cl
2
, H
2
O
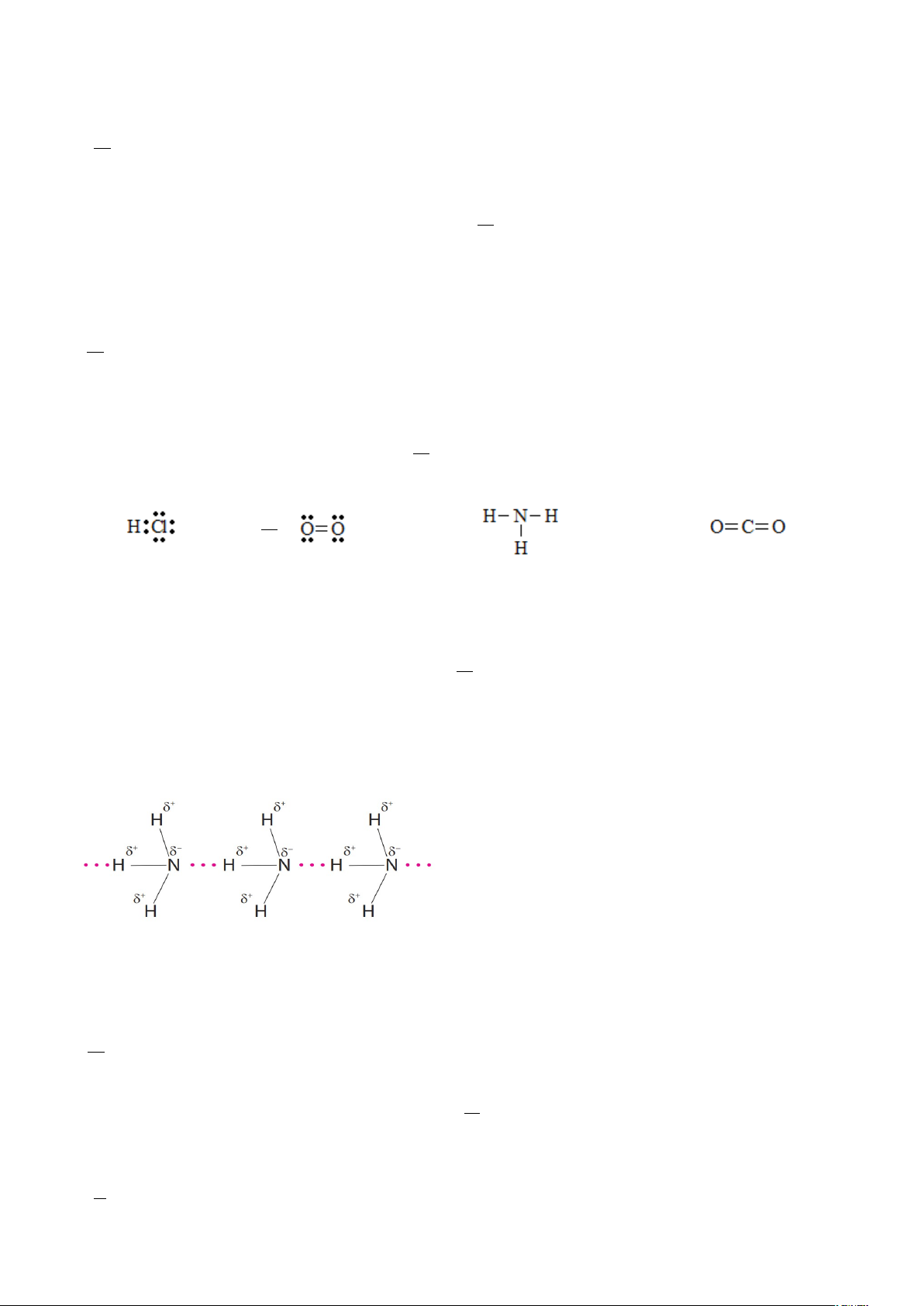
', Cho sơ đồ liên kết giữa các phân tử NH
3
:
Trong sơ đồ trên, đường nét đứt( i) đại diện cho:
%Zliên kết cộng hóa trị có cực.
)Zliên kết ion.
Zliên kết cho – nhận.
*Zliên kết hydrogen.
'-Cation M
2+
có cấu hình electron 1s
2
2s
2
2p
6
3s
2
3p
6
. Cấu hình electron của nguyên tử M là?
%1s
2
2s
2
2p
6
3s
2
)1s
2
2s
2
2p
6
3s
2
3p
6
4s
2
1s
2
2s
2
2p
6
3s
2
3p
4
*1s
2
2s
2
2p
6
3s
2
3p
2
'(Phân tử nào sau đây có chứa liên kết ba?
%
N
2
)
NH
3
H
2
O *
C
6
H
6
/01(

& Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4.Trong mỗi ý a), b), c), d) ở mỗi câu, thí
sinh chọn đúng hoặc sai.(Đ – S)
'# Cấu hình electron của:
- Nguyên tử X: 1s
2
2s
2
2p
6
3s
2
3p
6
4s
1
- Nguyên tử Y: 1s
2
2s
2
2p
6
3s
2
3p
4
0 Nguyên tử X chứa 19 electron.
3 Số hiệu nguyên tử của Y là Z
Y&
= 16.
Trong nguyên tử X lớp electron ở mức năng lượng cao nhất là lớp M (n=3).
4 Nguyên tử Y có 4 e lớp ngoài cùng ⇒ Y là nguyên tố kim loại
'Cho các phát biểu sau:
a. Các cặp nguyên tử và
18
40
Ar
, và là đồng vị của nhau.
b. Mg có 3 đồng vị , , ; Cl có 2 đồng vị , . Vậy có 9 loại phân tử MgCl
2
khác
tạo nên từ các đồng vị của 2 nguyên tố đó.
c. Oxygen có 3 đồng vị , , và carbon có hai đồng vị là: , . Vậy có 12 loại phân tử khí
CO
được tạo thành giữa carbon và oxygen.
d. Đồng vị là những nguyên tử của cùng một nguyên tố, có số proton bằng nhau và số neutron bằng nhau
'+ X, Y là những nguyên tố có số đơn vị điện tích hạt nhân lần lượt là 6, 17. Công thức và liên kết hợp chất tạo
thành từ X và Y là:
0XY và liên kết cộng hóa trị.
3X
4
Y và liên kết ion.
XY
2
và liên kết ion.
4XY
4
&và liên kết cộng hóa trị.
'! Cho các phát biểu sau:
a. Tất cả hạt nhân nguyên tử của các nguyên tố đều luôn có 2 loại hạt cơ bản là proton và neutron.
b. Khối lượng nguyên tử tập trung ở lớp vỏ electron.
c. Trong nguyên tử, số electron bằng số proton.
d. Trong hạt nhân nguyên tử, hạt mang điện là proton và electron.
&# Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
'R thuộc chu kì 3 nhóm VA của bảng tuần hoàn. Cho biết cấu hình electron của R có bao nhiêu electron p ?
' Cho các nguyên tố: Mg (12); Al (13); Si (14); P (15); Ca (20). Các nguyên tố thuộc cùng một chu kì?&
'+ Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang
điện là 12 hạt. Nguyên tố X có số khối là?
/01.

'! Trong tự nhiên Chlorine có hai đồng vị bền: chiếm 24,23% tổng số nguyên tử, còn lại là .
Thành phần % theo khối lượng của trong HClO
4
là?
'" Các chất mà phân tử chỉ có liên kết cộng hóa trị phân cực:NaCl,O
2
, H
2
O, HCl, Cl
2
, CaBr
2
, HF
' , Trong nhóm A, theo chiều tăng của điện tích hạt nhân, tính kim loại biến đổi theo chiều nào?
. & & & & & & & & & & & & & &
555555555555555565555555555555555
7789%
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 ) 10 *
2 11 )
3 ) 12
4 ) 13
5 ) 14 )
6 ) 15 )
7 ) 16 *
8 % 17 )
9 18 %
:# Điểm tối đa của 01 câu hỏi là 1 điểm
- Thí sinh chỉ lựa chọn chính xác 01 ý trong 1 câu hỏi được =>?
- Thí sinh chỉ lựa chọn chính xác 02 ý trong 1 câu hỏi được =">?
- Thí sinh chỉ lựa chọn chính xác 03 ý trong 1 câu hỏi được =">?
- Thí sinh lựa chọn chính xác cả 04 ý trong 1 câu hỏi được >?
' @AB ;<;CDEF ' @AB ;<;CDEF
a + a E
b b E
c E c E
d E d
a E ! a E
b b E
c c
d E d E
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 có 9 e thuộc phân lớp p 4
8,92%
2 Mg, Al,Si,P 5 H
2
O, HCl, HF
3 Nguyên tố X có số khối là A = 27 6 Tăng dần. & & & & & & & & & & & & & &
&# Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
'R thuộc chu kì 3 nhóm VA của bảng tuần hoàn. Cho biết cấu hình electron của R có bao nhiêu electron p ?
R thuộc chu kì 3 ⇒ Có 3 lớp electron.
R thuộc nhóm VA ⇒ Có 5 electron lớp ngoài cùng
⇒ Cấu hình electron của R: 1s
2
2s
2
2p
6
3s
2
3p
3
&⇒ có 9 e thuộc phân lớp p.
' Cho các nguyên tố: Mg (12); Al (13); Si (14); P (15); Ca (20). Các nguyên tố thuộc cùng một chu kì?&
Mg, Al,Si,P
/01

'+ Nguyên tử của nguyên tố X có tổng số hạt là 40. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang
điện là 12 hạt. Nguyên tố X có số khối là?
{
2 Z+N =40
2Z−N =12
⇔
{
Z=13
N =14
Vậy nguyên tố X có số khối là A = Z + N = 13 + 14 = 27
'! Trong tự nhiên chlorine có hai đồng vị bền: chiếm 24,23% tổng số nguyên tử, còn lại là . Thành
phần % theo khối lượng của trong HClO
4
là?
A
Cl
=
37.24,23+35.75,77
100
= 35,4846 →%m C
17
37
l=
37.0,2423
1+64+4.35,4846
=8,92 %
'" Các chất mà phân tử chỉ có liên kết cộng hóa trị phân cực:
0=O
2
, H
2
O, HCl, Cl
2
, CaBr
2
, HF. H
2
O, HCl, HF
', Trong nhóm A, theo chiều tăng của điện tích hạt nhân, tính kim loại biến đổi theo chiều nào?
Tăng dần. & & & & & & & & & & & & & &
Lưu ý: Phần nhận biết HS trả lời đáp án khác nhưng đúng vẫn cho điểm tối đa
+
! "
#$%
& Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến '(Mỗi câu hỏi thí
sinh chỉ chọn một phương án.
'Các nguyên tử của cùng một nguyên tố hoá học là đồng vị của nhau có sự khác nhau về
% số khối . ) số proton.
số electron. *điện tích hạt nhân.
'Kí hiệu phân lớp electron nào sau đây sai?
% 1s. ) 2p. 2d. *3p.
'+#Bảng tuần hoàn hiện nay có số cột, số nhóm A và số nhóm B lần lượt là:
%16, 8, 8. )18, 8, 8. 18, 8, 10. *18, 10, 8.
'!#Nguyên tử của nguyên tố X có cấu hình electron là 1s
2
2s
2
2p
6
3s
2
3p
3
. X có công thức oxide cao
nhất là
%XO
2.
. )X
2
O
5
. X
2
O
3
. *XO
3
.
'"#Phát biểu nào 20 khi nói về neutron?
%Có khối lượng lớn hơn khối lượng electron.
)Có khối lượng lượng bằng khối lượng proton.
Không mang điện.
*Tồn tại trong hạt nhân nguyên tử.
',#Phát biểu nào sau đây NR1 đúng?
%Số khối của hạt nhân bằng tổng số proton và số neutron.
)Trong nguyên tử, số đơn vị điện tích hạt nhân bằng số proton và bằng electron.
Nguyên tố hóa học là những nguyên tử có cùng số đơn vị điện tích hạt nhân.
*Số hiệu nguyên tử bằng số neutron trong hạt nhân nguyên tử.
/01

'-#Vì sao các nguyên tử lại liên kết với nhau thành phân tử?
%Để mỗi nguyên tử trong phân tử đạt tới cấu electron ổn định, bền vững.
)Để lớp ngoài cùng của mỗi nguyên tử trong phân tử có nhiều electron độc thân nhất.
Để mỗi nguyên tử trong phân tử đều đạt 8 electron ở lớp ngoài cùng.
*Để tổng số electron ngoài cùng của các nguyên tử trong phân tử là 8.
'(#Hạt nhân nguyên tử nguyên tố X có 24 hạt, trong đó số hạt mang điện là 12. Số electron trong X
là
%12. )6. 24. *13.
'.#Điều nào dưới đây >j1khi nói về ion Cl
-
?
%Được tạo thành khi nguyên tử chlorine (Cl) nhận vào 1 proton. )Có chứa 18 proton.
Có chứa 18 electron. *Trung hoà về điện.
' #Trong Bảng tuần hoàn các nguyên tố, con số trên đầu mỗi ký hiệu hóa học biểu thị thông tin về
^#1VMe/1
%Số khối của nguyên tố. )Số thứ tự nhóm của nó.
Số thứ tự chu kỳ của nguyên tố. *Số hiệu nguyên tử của nguyên tố.
'#Kí hiệu chung của mọi nguyên tử là , trong đó A, X và Z lần lượt là
%số khối, kí hiệu nguyên tố, số hiệu nguyên tử.
)số khối, số hiệu nguyên tử, kí hiệu nguyên tố.
số hiệu nguyên tử, số khối, kí hiệu nguyên tố.
*số hiệu nguyên tử, kí hiệu nguyên tố, số khối.
'#Quan sát hình bên dưới và cho biết nguyên tố Phosphorus có bao nhiêu proton?
^#1VMe2</2
%30. )15. 3. *10.
'+#Trong nguyên tử, loại hạt có khối lượng NR1 đáng kể so với các hạt còn lại là
%electron. )neutron. neutron và electron. *proton.
'!#Cấu hình electron nguyên tử của nguyên tố nitrogen (Z= 7) là
%1s
2
2s
2
2p
4
. )1s
2
2s
2
. 1s
2
2s
2
2p
6
3s
2
. *1s
2
2s
2
2p
3
.
'"#Nguyên tử của nguyên tố X có cấu hình electron: 1s
2
2s
2
2p
6
3s
2
3p
5
. X thuộc nhóm
%VA )IIIA IA. *VIIA
',Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
% NH
3
. ) H
2
O. HF. *PH
3
.
'-Trong chất và phân tử Cl
2
, N
2
, O
2
có tổng số liên kết σ và liên kết π lần lượt là
% 0 và 4. ) 2 và 2. 3 và 3. *4 và 0.
'(Cho bảng số liệu sau:
/01

Phát biểu nào sau đây sai?
% Do có liên kết hydrogen giữa các phân tử nên HF có nhiệt độ sôi cao hơn hydrogen còn lại.
) Trong phân tử chỉ có các liên kết cộng hóa trị.
Nguyên tử H và các nguyên tử Halogen góp 1 e tạo liên kết.
*Liên kết F-H trong phân tử HF là liên kết ion.
& Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4.Trong mỗi ý a), b), c), d) ở mỗi
câu, thí sinh chọn đúng hoặc sai.(Đ – S)
'#Soudime (
11
Na) và Magienime (
12
Mg) thuộc chu kì 3 trong bảng tuần hoàn các nguyên tố
hóa học.
0 Na và Mg đều có 3 electron hóa trị.
3 Dựa vào mức độ phản ứng của Na và Mg với nước ở điều kiện thường, có thể so sánh được độ hoạt
động hóa học giữa Na với Mg.
Tính base của sodium hydroxide yếu hơn tính base của magnesium hydroxide.
4Khi phản ứng với Cl
2
, Na và Mg đều tạo ra hợp chất ion.
' ZCho độ âm điện của N bằng 3,04; của H bằng 2,2; của C bằng 2,55; của O bằng 3,44.
0&Phân tử NO
2
và NH
3
tuân theo quy tắc octet; CH
4
và H
2
O vi phạm quy tắc octet .
3&Dung dịch NH
3
có thể tạo được tối đa 4 loại liên kết hydrogen.
&Nhiệt độ sôi của H
2
O cao hơn nhiều so với CH
4
nhờ có liên kết hydrogen.
4&Nguyên tử C trong phân tử CH
4
còn một cặp electron chưa tham gia liên kết.
'+#Cho biết chlorine (Cl có Z=17)
0Cấu hình electron lớp ngoài cùng của nguyên tử Cl là 2s
2
2p
5
.
3Liên kết hóa học trong phân tử Cl
2
là liên kết cộng hóa trị không phân cực.
Cl là phi kim vì có 5 e ở lớp ngoài cùng
4Trong chu kỳ 7 Clo là nguyên tố có độ âm điện lớn nhất nên tính phi kim mạnh nhất.
'!# Cho K có Z = 19
a. Cấu hình electron lớp ngoài cùng của K là 4s
1.
b. Liên kết hóa học trong K
2
O là liên kết ion.
c. Cho 0,1 mol K tác dụng với H
2
O dư thu được 2,479 lit khí ở điều kiện chuẩn.
d. Trong các phản ứng hóa học K có khả năng nhận thêm 1e tạo cấu hình bền của khí hiếm.
&# Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
'Cho 6 nguyên tố có số hiệu nguyên tử lần lượt là 9, 11, 17, 18, 19 và 20. Trong số các nguyên tố
trên có bao nhiêu nguyên tố phi kim?
'Có bao nhiêu hợp chất tạo được liên kết Hidrogen trong dãy các chất sau: NH
3
, HF, HCl, PH
3
, C-
2
H
5
OH?
'+Một nguyên tố tạo hợp chất khí với hydrogen có công thức RH
3
, được sử dụng để trung hoà các
thành phần acid của dầu thô, bảo vệ thiết bị không bị ăn mòn trong ngành công nghiệp dầu khí. Nguyên tố
này chiếm 25,93% về khối lượng trong oxide cao nhất. % khối lượng của nguyên tố R trong hợp chất khí
với hydrogen là bao nhiêu&?
'!Có bao nhiêu hợp chất chỉ chứa liên kết cộng hoá trị trong dãy các chất sau: NH
3
, CaO, PCl
3
,
H
2
S, NaOH, O
2,
HCl?
'". Cho nguyên tử các nguyên tố sau: Na (Z=11), K (Z=19), Mg (Z=12), F (Z=9), Al (Z=13), S
(Z=16). Có bao nhiêu nguyên tử có xu hướng hình thành lớp vỏ bền vững như Ne.
/01+

',[Ne=0V<[NeHk1CE#022E</F fV6>Hk2b4l1>mW;>n
<'bNe=1VMSNef0;oQQHk1;>p1nbền của một nguyên tố. Phổ
khối của neon được biểu diễn như ở hình bên.
/l13?nQHk1<:/Ym2e1VMbf0S1>q1n=/lQ3?nr
2es01VMbNeCFf0t>p1nI>Aucủa các ion đồng vị tương ứng C>Auv
f0;>p1n>m3w1]F
1VMbNe/13^f0Qx
77
:t'>j1 =">
Câ
u
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18
ĐA A C B B B D A A C D A B A D D D C D
:?e>0t'Q>HS chọn đúng 1 ý là 0,1đ, 2 ý là 0,25đ, 3 ý là 0,5đ, 4 ý là 1đ
Câu Lệnh hỏi Đáp án (Đ/S) Câu Lệnh hỏi Đáp án (Đ/S)
1 A S 3 A S
B Đ B Đ
C S C S
D Đ D S
2 A S 4 A Đ
B Đ B Đ
C Đ C S
D S D S
:t'>j1 =">
Câu 1 2 3 4 5 6
Đáp án 2 3 82,3 5 4 20,19
!
! "
#$%
& Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến '(Mỗi câu hỏi thí
sinh chỉ chọn một phương án.
'# Nhà khoa học nào đã phát hiện ra neutron?
% Chadwick. ) Rutherford. Thomson. * Bohr.
'Đặc điểm của electron là
% mang điện tích dương và có khối lượng.)mang điện tích âm và có khối lượng.
không mang điện và có khối lượng.* mang điện tích âm và không có khối lượng.
'+Cặp nguyên tử nào sau đây có cùng số neutron?
% và ) và
Mg
12
24
và
Si
14
28
. *
N
7
14
và
O
8
16
.
'!: Hình ảnh mô hình nguyên tử các đồng vị của nguyên tử Hydrogen được cho dưới đây. Các đồng vị này
khác nhau về&
/01!

% Số proton. ) Số neutron. Số electron. * Số hiệu nguyên tử.
'" Lớp electron thứ 3 có bao nhiêu phân lớp
% 1. ) 2. 3. * 4.
',Nguyên tử N có 7 proton, nguyên tử H có 1 proton. Số lượng hạt proton và electron trong ion NH
4
+
là:
%11 proton và 10 electron. ) 11 proton và 11 electron.
10 proton và 11 electron. * 10 proton và 10 electron.
'-Trong tự nhiên, oxygen có 3 đồng vị
16
O,
17
O,
18
O. Có bao nhiêu loại phân tử O
2
?
% 3. ) 6. 9. * 12.
'(Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử X là 3p
1
. Số hiệu nguyên tử của nguyên tố X
là
%13 )14 12 *11
'.Một nguyên tố R có cấu hình electron: 1s
2
2s
2
2p
3
, công thức oxide cao nhất và hợp chất khí với hydrogen và
lần lượt là:
%R
2
O
5
, RH
5
. )R
2
O
3
, RH. R
2
O
7
, RH. *R
2
O
5
, RH
3
.
' Trong cùng một nhóm A, theo chiều tăng của điện tích hạt nhân, độ âm điện thường
%giảm xuống. ) tăng lên.
biến đổi không theo quy luật. * không thay đổi.
'Chromium được sử dụng nhiều trong luyện kim để chế tạo hợp kim chống ăn mòn và đánh bóng bề mặt.
Nguyên tử chromium có cấu hình electron viết gọn là [Ar]3dd
5
4s
1
. Vị trí chromium trong bảng tuần hoàn là
%ố số 17, chu kì 4, nhóm IA )ố số 24, chu kì 4, nhóm VIB
. ố số 24, chu kì 3, nhóm VB *. ố số 27, chu kì 4, nhóm IB
'Nguyên tố nào trong số các nguyên tố sau đây có công thức oxide cao nhất ứng với công thức R
2
O
5
?
%Mg. )Al. Si. *P.
'+Cation X
2+
(ion dương) có cấu hình electron ở lớp vỏ ngoài cùng 2p
6
. Cấu hình electron của nguyên tử X
là:
% 1s
2
2s
2
2p
2
) . 1s
2
2s
2
2p
6
3s
2
1s
2
2s
2
2p
4
* 1s
2
2s
2
2p
5
'!Cho các nguyên tố . Các nguyên tố thuộc cùng chu kì là
% Mg, Al, Si ). Mg, Al, Ca . Mg, Al, Si, P *. Mg, Al, Si và Ca
'"Số lượng cặp electron dùng chung trong các phân tử H
2
, O
2
, N
2
, F
2
lần lượt là
% 1,2,3,4 ) 1,2,3,1 2,2,2,2 * 1,2,2,1
',Liên kết hóa học trong phân tử nào sau đây là liên kết ion?
% HClO. ) Cl
2
. KCl. * HCl.
'-Điều nào sau đây đúng khi nói về liên kết hydrogen liên phân tử ?
% Lực hút tĩnh điện giữa nguyên tử H (thường trong các liên kết H – F; H – N , H – O ở phân tử này) với một
trong các nguyên tử có độ âm điện mạnh (thường là N, O, F) ở một phân tử khác.
) Là lực hút giữa các phân tử khác nhau.
Là lực hút tĩnh điện giữa các ion trái dấu.
* Là lực hút giữa các nguyên tử trong một hợp chất cộng hóa trị.
'(Chất nào có chứa liên kết ba?%. Cl
2
. ). CH
4
. CO
2
* . N
2
& Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 1 đến câu 4.Trong mỗi ý a), b), c), d) ở mỗi
câu, thí sinh chọn đúng hoặc sai.(Đ – S)
'# Sulfur dạng kem bôi được sử dụng để điều trị mụn trứng cá. Nguyên tử sulfur có phân lớp
electron ngoài cùng là
0Hạt nhân nguyên tử sulfur có 16 electron.
3Sulfur nằm ở chu kì 3 và là một phi kim.
/01"
Oxide cao nhất của Sulfur là SO
2
.
4Sulfurcó độ âm điện lớn hơn nguyên tố phosphorus.
': Nguyên tử của một nguyên tố có cấu hình electron như sau:
(1)1s
2
2s
2
2p
1
(2)1s
2
2s
2
2p
4
(3)1s
2
2s
2
2p
6
3s
2
3p
1
(4)1s
2
2s
2
2p
6
3s
2
3p
5
0(1) và (2) cùng chu kỳ, (3) và (4) cùng chu kỳ
3(1) và (3) cùng nhóm, (2) và (4) cùng nhóm
(2) và (4) là phi kim, (1) và (3) là kim loại
4(2) và (3) là phi kim, (1) và (4) là kim loại
'+: Nguyên tử của nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khí hiếm
argon khi tham gia hình thành liên kết hóa học?
0Sulfur.
3Oxygen.
Fluorine.
4Chlorine.
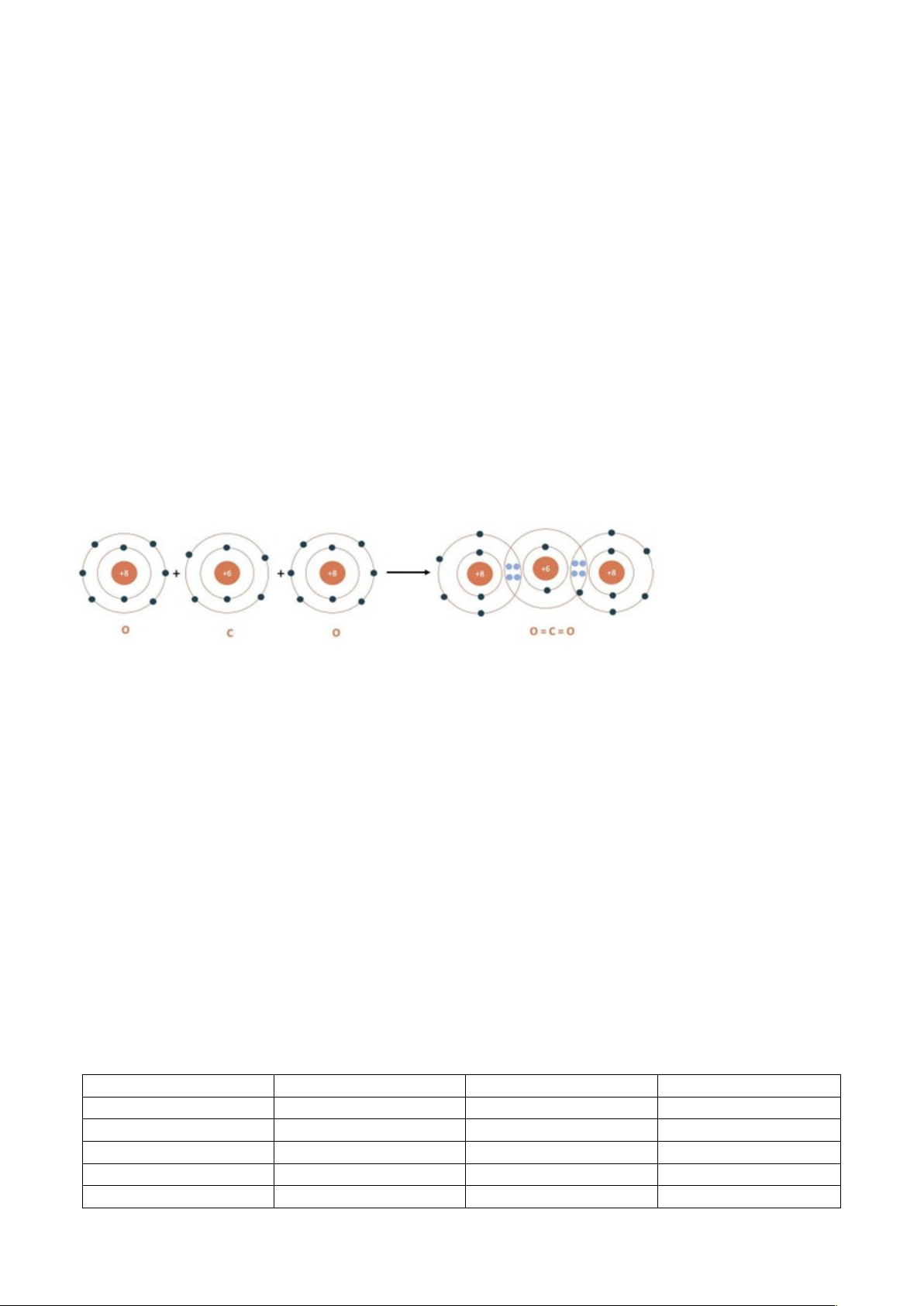
'!: Cho sơ đồ biểu diễn sự hình thành liên kết trong phân tử khí carbon dioxide.
0LiênkếtgiữanguyêntửOvàClàliênkết phâncực.
3Phân tử carbon dioxide số liên kết σ và liên kết π lần lượt là 2 và 2.
PhântửCO
2
khôngphâncực do tổng momen lưỡng cực trong phân tử bằng không
4Giữa nguyên tử C với mỗi nguyên tử O có 2 cặp electron chung
&# Câu hỏi trắc nghiệm yêu cầu trả lời ngắn. Thí sinh trả lời từ câu 1 đến câu 6.
'Số hiệu nguyên tửcủa các nguyên tố X, A, M, Q lần lượt là 6, 7, 20, 19. Trong số các nguyên tố
trên có bao nhiêu nguyên tố là kim loại?
'Hợp chất khí với hydrogen của nguyên tố X có công thức XH
4
, được sử dụng làm tác nhân ghép
nối để bám dính các sợi như sợi thủy tinh và sợi carbon. Oxide cao nhất của X chứa 53,3% oxygen về
khối lượng, thường được dùng để sản xuất cửa sổ, lọ thủy tinh. Tính nguyên tử khối của X?
'+Cho các chất sau: NaCl, H
2
O, K
2
O, BaCl
2
, CaF
2
, HCl, NH
4
NO
3
. Số phân tử có liên kết ion là ?
'!Để đạt quy tắc octet, nguyên tử Na (Z=11) đã nhường bao nhiêu electron?
'"Tổng số cặp electron dùng chung giữa các nguyên tử trong phân tử ethylene (C
2
H
4
) là bao nhiêu?
',Cho các chất sau: NH
3
, HCl, HF, CH
3
COOH, CH
3
OH. Có bao nhiêu chất tạo được liên kết
hydrogen?
77
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 % 10 %
2 ) 11 )
3 % 12 *
4 ) 13 )
5 14
/01,

6 % 15 )
7 ) 16
8 % 17 %
9 * 18 *
:#
' @AB ;<;CDEF ' @AB ;<;CDEF
a E + a
b b E
c E c E
d d
a ! a
b E b
c c
d E d
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 4
2 ( 5 ,
3 " 6 !
77&
'#
UCy5,F
%Cy5-F
zCy5.F
Cy5 F
Chỉ có Q có 1 electron lớp ngoài cùng, M có 2 eletron lớp ngoài cùng.
=> M, Q là kim loại.
'#Ta có: hợp chất khí với hydrogen của nguyên tố X có công thức XH
4
=> công thức oxide cao nhất của X là XO
2
Ta có: Oxide cao nhất của X chứa 53,3% oxygen về khối lượng
=>
'+Cho các chất sau: NaCl, H
2
O, K
2
O, BaCl
2
, CaF
2
, HCl, NH
4
NO
3
. Số phân tử có liên kết ion là ?
HI14JZ# NaCl, K
2
O, BaCl
2
, CaF
2
, NH
4
NO
3
.
'"Công thức electron của C
2
H
4
',Cho 4 chất NH
3,
HF, CH
3
COOH, CH
3
OH tạo được liên kết hydrogen.
"
! "
#$%
/01-
&'/{1Am<HO1;|0`u2/K}S'>6'(t'
Bu2r`~<HO1;
'&Hạt mang điện trong hạt nhân nguyên tử là
%proton và electron. )proton.
neutron. *proton và neutron.
'#ZDãy nào dưới đây gồm các đồng vị của cùng một nguyên tố hóa học?
% . ) . . * .
'+# Các nguyên tố trong cùng chu kỳ
% Có cùng số lớp electron. ) Có cùng số electron ở lớp vỏ ngoài cùng của chúng.
Có tính chất hóa học tương tự nhau. * Có cùng số điện tích hạt nhân.
'!# Trong một nhóm khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân bán kính nguyên
tử
% Tăng. ) Giảm. Không đổi. * Không có quy luật.
'"# Trong Bảng tuần hoàn các nguyên tố, con số trên mỗi ký hiệu hóa học biểu thị thông tin về
^+!1VMe/1
% Số thứ tự chu kỳ của nguyên tố. ) Số thứ tự nhóm của nó.
Số hiệu nguyên tử của nguyên tố. * Số khối của nguyên tố.
',# Bảng tuần hoàn hiện nay có số chu kì và số hàng ngang lần lượt là
%7 và 9. )7 và 8. 7 và 7. *6 và 7.
'-# Trong một chu kì, khi đi từ trái sang phải theo chiều tăng dần của điện tích hạt nhân, giá trị nào
dưới đây giảm dần?
% Độ âm điện ) Tính kim loại. Tính phi kim. * Số lượng lớp
electron.
'(: Theo •V{3;bthì nguyên tử có xu hướng đạt cấu trúc bền giống như:
%Kim loại kiềm gần kề. )Kim loại kiềm thổ gần kề.
Nguyên tử halogen gần kề. *Nguyên tử khí hiếm gần kề.
'.# Trong nguyên tử, electron hóa trị là các electron
%Độc thân. )Ở phân lớp ngoài cùng.
Ở obitan ngoài cùng. *Tham gia tạo liên kết hóa học.
' # Điền từ vào dấu (…)
Khi một electron được thêm vào hoặc bị loại bỏ khỏi nguyên tử, nguyên tử đó sẽ trở thành một...
%ion. )liên kết. cation. *phân tử.
'# Cặp nguyên tử nào dưới đây liên kết với nhau tạo hợp chất cộng hoá trị?
%H và He. )Na và F. Li và F. *H và Cl.
'# Vì sao HF có nhiệt độ sôi cao hơn hẳn so với HCl, HBr và HI?
%HF có phân tử khối lớn nhất. )HF có liên kết hydrogen.
HF có tương tác van der Waals lớn nhất. *HF là hợp chất phân cực nhất.
'+# Nguyên tử của nguyên tố X có cấu hình electron 1s
2
2s
2
2p
6
3s
2
, nguyên tử của nguyên tố Y có cấu
hình electron 1s
2
2s
2
2p
5
. Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết
%kim loại. )cộng hoá trị. ion. *cho nhận.
'!# Cho dãy các chất methane (CH
4
), ethane (C
2
H
6
), propane (C
3
H
8
) và butane (C
4
H
10
). Chất có nhiệt
độ sôi thấp nhất là
% methane. ) propane. ethane. * butane.
'"#Cấu hình electron hóa trị của nguyên tử R ở trạng thái cơ bản là ns
2
np
1
. Phát biểu nào sau đây là
20?
% R thuộc khối nguyên tố p. ) R nằm ở nhóm IIIA trong bảng tuần hoàn.
Công thức oxide cao nhất của R có dạng R
2
O
3
. * R là một nguyên tố phi kim.
/01(

',# Nguyên tố R có công thức oxide cao nhất là RO
2
. Công thức của hợp chất khí với hydrogen là
%RH
3
. )RH
4
. H
2
R. *HR.
'-# Nguyên tử X có Z = 15. Trong bảng tuần hoàn, nguyên tố X thuộc chu kì
%4. )2. 5. *3.
'(# Hợp chất khí tạo bởi nguyên tố R với hydrogen là RH, trong oxide cao nhất R chiếm 58,86% về
khối lượng, nguyên tố R là
%Br. )F. I. *Cl.
&'/{1A>j120u2/K}S'>6'!/1t€0F=3F=F=4F•
t'=u2`>j1P20CGEF
'# Cho nguyên tử sunfua (lưu huỳnh) có Z = 16, N = 16)
a. Số khối của nguyên tử sunfua là 16.
b. Sunfua là một nguyên tố phi kim do có 6 electron thuộc lớp ngoài cùng.
c. Ở trạng thái cơ bản, nguyên tử sunfua có số orbital chứa eletron là 8.
d. Trong bảng tuần hoàn các nguyên tố sunfua nằm ở chu kì 3.
'# Aluminium có rất nhiều ứng dụng trong cuộc sống. Aluminium được dùng để sản xuất các thiết bị
và dụng cụ sinh hoạt như nồi, chảo, các đường dây tải điện, các loại cửa,… đặc biệt dùng trong công nghệ
sản xuất vỏ máy bay do nhẹ, bền. Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tử Aluminium
thuộc chu kì 3 và nhóm IIIA.
a. Trong hạt nhân nguyên tử Aluminium có 13 hạt proton.
b. Nguyên tử Aluminium có 3 lớp electron.
c. Nguyên tố Aluminium có có tính kim loại mạnh hơn nguyên tố có số hiệu 11.
d. oxide cao nhất của Aluminium có công thức Al
2
O
3
là basic oxide.
'+#Cho 2 nguyên tố X và Y có số hiệu nguyên tử lần lượt là 11 và 8.
a. Số electron hoá trị của X và Y lần lượt là 1 và 2.
b. Hợp chất tạo thành giữa X và Y có liên kết ion và có công thức là X
2
Y.
c. Hợp chất tạo thành giữa X và Y là chất khí tan tốt trong nước.
d. Khi tạo thành hợp chất, nguyên tử X nhường 2 electron và nguyên tử Y nhận 2 electron.
'!# Ammonia là chất khí không màu có mùi khai là xốc. Amonia là chất trung gian
trong sản xuất phân bón. Công thức Lewis của Ammonia hình bên
a. Phân tử Ammonia chứa 3 liên kết cộng hoá trị phân cực, cặp elctron dùng chung
lệch về phía nguyên tử hidrogen.
b. Trong phân tử amonia nguyên tử nitrogen còn 1 cặp electron chưa liên kết nên có khả năng hình thành
liên kết cho nhận.
c. Khí Ammonia tan tốt trong nước do hình thành liên kết hydrogen với các phân tử nước.
d. Liên kết giữa nguyên tử N và H được hình thành do sự xen phủ của orbital s và p gọi là liên kết .
&#'B/{1AVM:/K}1{u2/K}S'>6',
'# Trong tự nhiên Ga có 2 đồng vị là
69
Ga (60,1%) và
71
Ga (39,9%). Tính nguyên tử khối
trung bình của Ga?
'# Nguyên tử của nguyên tố oxygen có ba đồng vị là&:
8
16
O;
8
17
O và
8
18
O&. Nguyên tử
của nguyên tố nitrogen có 2 đồng vị là và . Tính số hợp chất N
2
O tạo ra từ các đồng vị
trên?
'+# X thuộc nhóm IVA, phần trăm khối lượng của X trong hợp chất khí với hydrogen là 75%.
Tính phần trăm khối lượng của X trong oxide cao nhất? ( Lấy 3 chữ số sau dấu phẩy)
'!# X, Y là hai nguyên tố liên tiếp trong một chu kì (Z
X
< Z
Y
) và có tổng số điện tích hạt nhân là 29.
Cho biết số thứ tự chu kì của X và Y?
/01.

'"# Cho dãy các chất: N
2
, H
2
, NH
3
, NaCl, HCl, H
2
O. Có bao nhiêu chất trong dãy mà phân tử chỉ chứa
liên kết cộng hóa trị có cực?
',# Có bao nhiêu phát biểu đúng trong các phát biểu sau?
(a) Tương tác van der Waals yếu hơn liên kết hydrogen.
(b) Liên kết đôi được tạo nên từ 2 liên kết σ.
(c) Liên kết hydrogen làm tăng nhiệt độ nóng chảy và nhiệt độ sôi của nước.
(d) trong dung dịch HF và H
2
O có thể tạo ra ít nhất 4 kiểu liên kết hydrogen
555555555555555565555555555555555
77
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 ) 10 %
2 11 *
3 % 12 )
4 % 13
5 14 %
6 % 15 *
7 ) 16 )
8 * 17 *
9 * 18 %
:# Điểm tối đa của 01 câu hỏi là 1 điểm
- Thí sinh chỉ lựa chọn chính xác 01 ý trong 1 câu hỏi được =>?
- Thí sinh chỉ lựa chọn chính xác 02 ý trong 1 câu hỏi được =">?
- Thí sinh chỉ lựa chọn chính xác 03 ý trong 1 câu hỏi được =">?
- Thí sinh lựa chọn chính xác cả 04 ý trong 1 câu hỏi được >?
' @AB ;<;CDEF ' @AB ;<;CDEF
a E + a E
b b
c E c E
d d E
a ! a E
b b
c E c
d E d E
:# Mỗi câu trả lời đúng được 0,25 điểm
' ;<; ' ;<;
1 ,.=-.( 4 +
2 . 5 +
3 -=-+ 6 +
Lưu ý: Phần nhận biết HS trả lời đáp án khác nhưng đúng vẫn cho điểm tối đa
,
! "
#$%
/01
Bấm Tải xuống để xem toàn bộ.