




Preview text:
CHUYÊN ĐỀ 1. ESTER, CHẤT BÉO VÀ XÀ PHÒNG
DẠNG 1. BÀI TOÁN PHẢN ỨNG ESTER HÓA CÓ HẰNG SỐ CÂN BẰNG
Dạng bài toán thường có liên quan đến hiệu suất, và thường là một ý nhỏ trong bài toán lớn liên quan.
Tuy nhiên việc cắt nhỏ thành các bài “nhỏ” hơn cũng sẽ giúp cho việc tư duy và dịnh hướng các chia nhỏ các
phần trong bài toán lớn. Khi giải dạng bài toán này thì tùy vào mức độ mà cho độ khó khác nhau. + 0
Phương trình tổng quát: H , t RCOOH + R 'OH ⎯⎯⎯ → ⎯⎯⎯ RCOOR '+ H O 2
Kiểu 1. Phản ứng ester hóa có cho hằng số KC.
Bước 1. Tìm số mol ban đầu các chất (hoặc nồng độ)
Bước 2. Lập bảng số liệu 3 dòng + 0 H ,t RCOOH + R 'OH ⎯⎯⎯ →
⎯⎯⎯ RCOOR ' + H O 2 Ban đầu Tham gia Cân bằng [RCOOR '][H O]
Bước 3. Dùng CT hằng số cân bằng KC: 2 K = C [RCOOH].[R 'OH] Lưu ý.
1. KC chỉ phụ thuộc t 0C. Khi tăng t 0C thì KC sẽ tăng.
2. Nếu trong dung dịch có nước (cho dưới dạng C%) thì [H2O] trong CT là tổng H2O trong dung dịch và H2O sinh ra do phản ứng.
3. Nếu acid hoặc alcohol tham gia 1 lúc 2 phương trình ester hóa thì [acid] hoặc [alcohol] trong CT là nồng
độ cân bằng chung cho cả 2 phản ứng.
4. Khi đã là bài toán tính H% thì một điều phải chú ý là các chất tham gia đều còn dư (không có chất nào hết).
5. Một số bài toán thì không đủ dữ liệu kết luận chất nào quyết định H% thì phải giải cả 2TH và kiểm tra
lại số liệu (số mol, H% đã cho) để chọn TH phù hợp 1
PHẦN TRẢ LỜI NGẮN
Câu 1. Cho 2 mol CH3COOH phản ứng với 3 mol C2H5OH trong môi trường acid với hiệu suất phản ứng ester
hóa đạt 66,67%. Hằng số cân bằng Kc của phản ứng có giá trị là bao nhiêu? Đáp án
Câu 2. Khi thực hiện phản ứng ester hóa 1 mol CH3COOH và 1 mol C2H5OH, lượng ester lớn nhất thu được là
2 mol. Để đạt hiệu suất cực đại là 90% (tính theo acid). Khi tiến hành ester hóa 1 mol CH3COOH cần số mol 3
C2H5OH là bao nhiêu? (biết các phản ứng ester hoá thực hiện ở cùng nhiệt độ). Đáp án
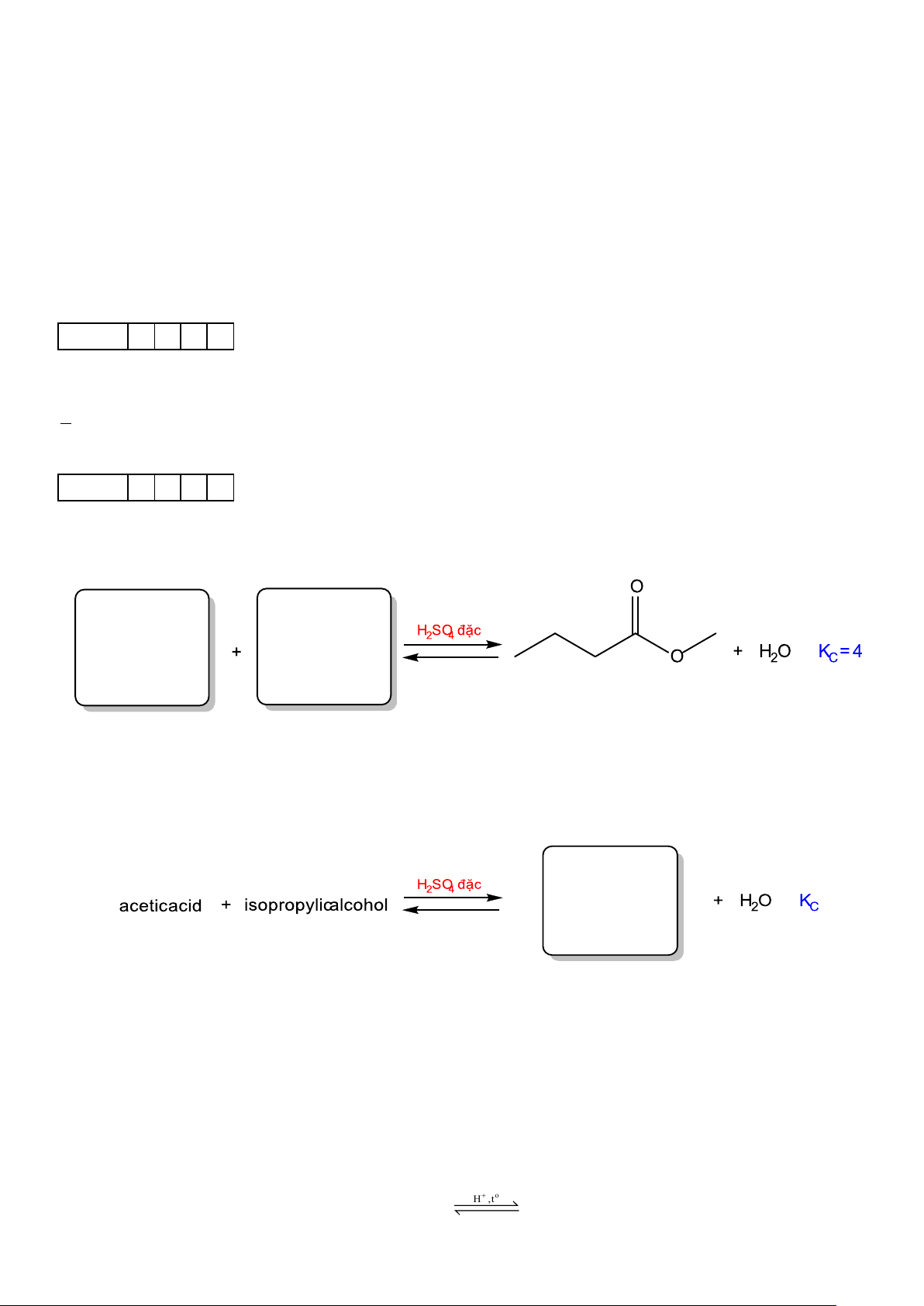
Câu 3. Methyl butyrate là ester tạo mùi đặc trưng của quả táo, cho phương trình điều chế methyl butyrate
bằng phương pháp ester hóa như sau:
a. Hãy vẽ CTCT của acid và alcohol tương ứng vào ô trống.
b. Ở 25°C, cho biết nồng độ ban đầu của acid là 1 M. Khi phản ứng đạt trạng thái cân bằng, nồng độ của methyl
butyrate là 0,93M. Hãy tính nồng độ ban đầu của alcohol.
Câu 4. Cho acid acetic tác dụng với isopropylic alcohol theo phản ứng thuận nghịch sau:
Nếu ban đầu người ta cho 1 mol acetic acid tác dụng với 1 mol isopropylic alcohol thì cân bằng sẽ đạt được
khi có 0,6 mol ester được tạo thành. Lúc đó người ta thêm 1 mol acetic acid vào hỗn hợp phản ứng, cân bằng
sẽ bị phá vỡ và chuyển đến trạng thái cân bằng mới.
a. Vẽ CTCT của ester tạo thành vào ô trống (dạng thu gọn nhất)
b. Khi cân bằng mới được thiết lập thì số mol alcohol là bao nhiêu ở thời điểm cân bằng?
Câu 5. Carboxylic acid X đơn chức có tác dụng kháng khuẩn nhẹ, được sử dụng trong điều trị một số loại
bệnh. Kết quả phân tích nguyên tố (theo khối lượng) cho thấy X chứa 53,33% oxygen. Ethanol phản ứng với
X trong môi trường H2SO4 đặc tạo thành chất hữu cơ Y theo phương trình hoá học sau: + o C H ,t
2H5OH(l) + X(l) Y(l) + H2O(l) 2
Ở nhiệt độ t 0C, giá trị KC của phản ứng trên là 3,4. Nếu cho 46,0 gam ethanol phản ứng với 60,0 gam X trong
bình dung tích 1 L ở t 0C thì khối lượng Y thu được ở trạng thái cân bằng là bao nhiêu gam? (làm tròn kết quả
đến hàng đơn vị) (Coi tổng thể tích của hệ phản ứng không đổi). Đáp án
PHẦN TRẮC NGHIỆM ĐÚNG SAI.
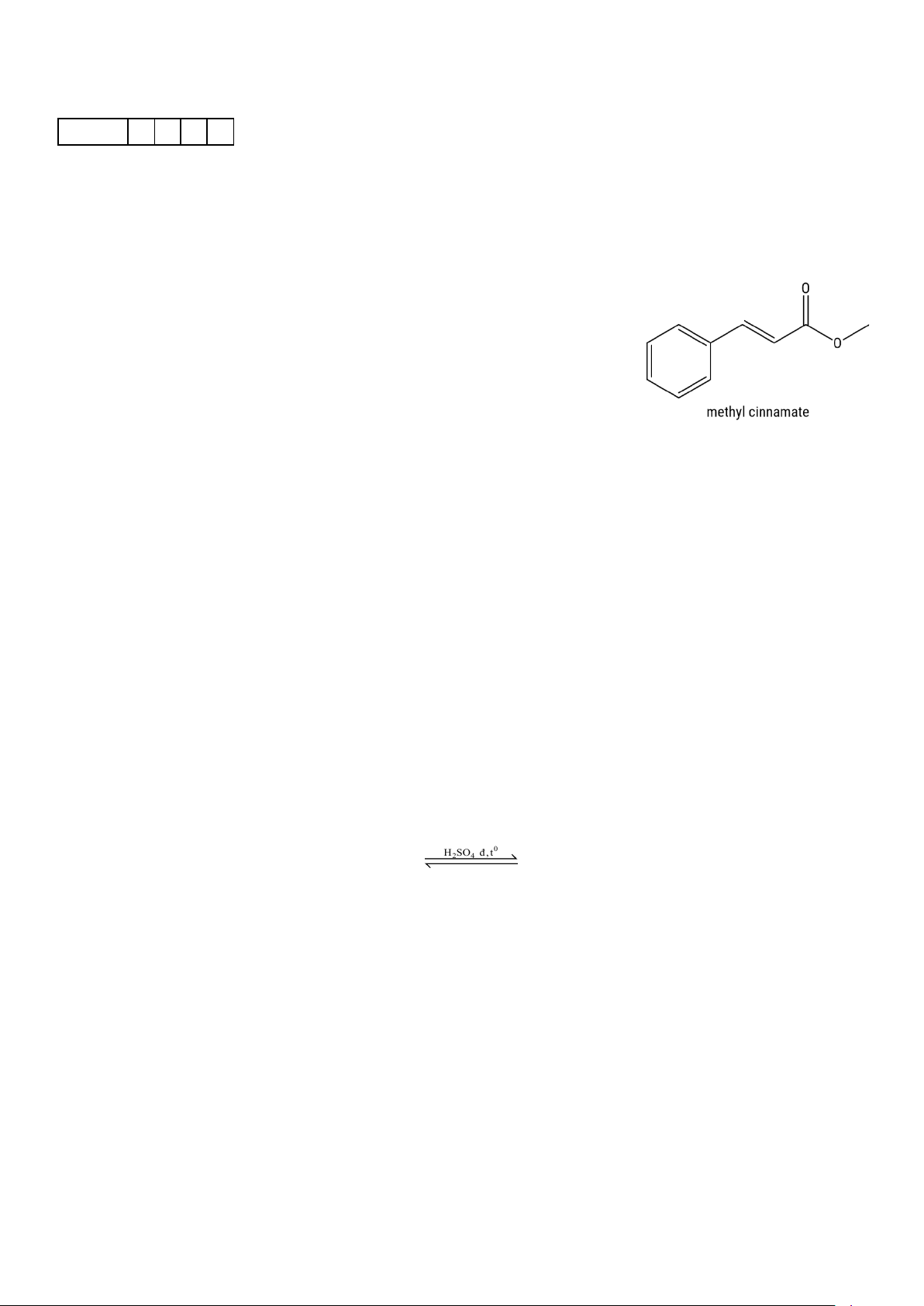
Câu 1. Methyl cinnamate là một ester có công thức cấu tạo dưới đây và có
mùi thơm của dâu tây (strawberry) được sử dụng trong ngành công nghiệp
hương liệu và nước hoa. Để điều chế 16,2 gam ester methyl cinnamate người
ta cho 29,6 gam cinnamic acid (C6H5CH=CH-COOH) phản ứng với lượng dư methyl alcohol (CH3OH). Cho các phát biểu sau:
a. Methyl cinnmate phản ứng với dung dịch NaOH, khi đun nóng theo tỉ lệ mol 1: 1.
b. Methyl cinnmate có đồng phân hình học.
c. Hiệu suất phản ứng ester hóa theo cinnamic acid trong trường hợp này là 60%.
d. Methyl cinnmate có công thức phân tử là C10H10O2.
Câu 2. Cho salicylic acid (2-hydroxybenzoic acid) phản ứng với methyl alcohol có mặt sulfuric acid làm xúc
tác, thu được methyl salicylate (C8H8O3) dùng làm chất giảm đau (có trong miếng dán giảm đau khi vận động
hoặc chơi thể thao). Cho các phát biểu sau:
a. Công thức cấu tạo của salicylic acid là o-HOC6H4COOH.
b. Phản ứng giữa salicylic acid với methyl alcohol có mặt H2SO4 đặc làm xúc tác là phản ứng thuận nghịch.
c. Methyl salicylate có thể tác dụng tối đa với NaOH theo tỷ lệ mol là 1: 1.
d. Nhiệt độ sôi của methyl salicylate cao hơn của salicylic acid.
Câu 3. Methyl salicylate (chất X) thường được kết hợp với các loại tinh dầu khác dùng làm thuốc bôi ngoài
da, thuốc xoa bóp, cao dán giảm đau, chống viêm. X được tổng hợp từ salicylic acid và methanol theo phản ứng sau: 0 o-HO-C H2SO4 đ,t
6H4-COOH + CH3OH o-HO-C6H4-COOCH3 + H2O Cho các phát biểu sau:
a. Công thức phân tử của X là C8H7O3.
b. X có thể tác dụng tối đa với KOH theo tỷ lệ mol là 1: 2.
c. X là hợp chất hữu cơ tạp chức.
d. Để sản xuất được 3,04 triệu miếng dán salonpas (mỗi miếng chứa 1,8 mg methyl salicylate) thì khối lượng
salicylic acid cần dùng là 6,21 kg. Biết hiệu suất tổng hợp tính theo salicylic acid là 80%
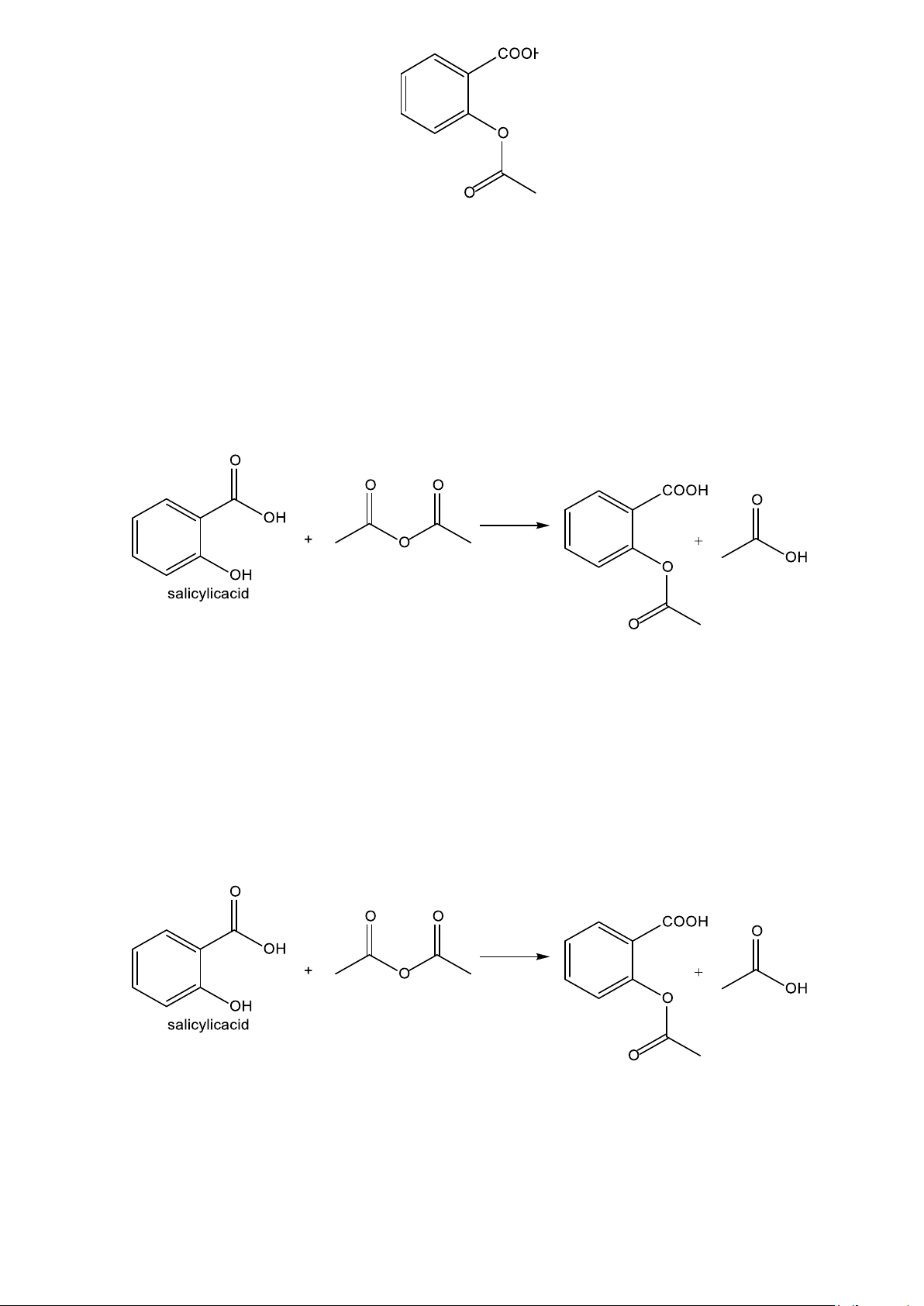
Câu 4. Aspirin được sử dụng làm thuốc giảm đau, hạ sốt. Sau khi uống, aspirin bị thủy phân trong cơ thể tạo
ra salicylic acid. Công thức cấu tạo của aspirin như sau 3 Cho các phát biểu sau:
a. Công thức phân tử của aspirin là C7H6O3.
b. 1 mol aspirin phản ứng tối đa với dung dịch chứa 3 mol NaOH đun nóng.
c. Aspirin là ester được điều chế bằng phản ứng giữa carboxylic acid và alcohol tương ứng.
d. Phản ứng thủy phân aspirin trong cơ thể là phản ứng một chiều.
Câu 5. “Aspirin 81” là một loại thuốc chống đột quỵ, trong mỗi viên có chứa 81 mg aspirin. Aspirin được tổng
hợp bằng cách đun hỗn hợp salicylic acid và anhydride acetic khi có mặt xúc tác sulfuric acid đặc theo phương trình hóa học sau:
Hỗn hợp sau phản ứng được làm lạnh để tạo tinh thể aspirin. Sau đó tiến hành lọc, rửa, làm khô sản phẩm.Cho các phát biểu sau:
a. Phản ứng tổng hợp aspirin là phản ứng ester hóa.
b. Sử dụng phương pháp chiết để tách aspirin ra khỏi hỗn hợp sau phản ứng.
c. 1 mol aspirin tác dụng tối đa với 3 mol NaOH trong dung dịch.
d. Để tổng hợp aspirin đủ để sản xuất 1 triệu viên “aspirin 81” thì acần dùng ít nhất 621 gam salicylic acid.
Câu 6. Acetylsalicylic acid còn được gọi là aspirin - hoạt chất chính trong các thuốc giảm đau, hạ sốt, chống
viêm. Trong quá trình điều chế, aspirin được tách ra khỏi hỗn hợp bằng phương pháp kết tinh. Một nhóm học
sinh thực hiện thí nghiệm tổng hợp aspirin theo phương trình hóa học sau:
+ Chuẩn bị: Dụng cụ: bình cầu 100 mL, cốc thủy tinh, đũa thủy tinh, đèn cồn, phễu lọc, giấy lọc.
Hóa chất: 2 gam salicylic acid, 4 mL anhydride acetic lỏng (d = 1,08 g/ml), 3-4 giọt H3PO4 đặc làm xúc tác. - Tiến hành:
Bước 1. Cho salicylic acid vào bình cầu, thêm anhydride acetic và H3PO4 đặc. Đun cách thủy ở khoảng nhiệt
độ 60oC - 70°C trong 15 phút.
Bước 2. Thêm nước cất lạnh vào bình phản ứng, aspirin kết tinh nhanh dưới đáy bình 4
Bước 3. Lọc lấy kết tinh, rửa bằng nước lạnh rồi sấy khô tinh thể trong tủ sấy ở 50oC trong 30 phút.
Bước 4. Đem cân tinh thể đã sấy khô thu được 1,8 gam aspirin. Cho các phát biểu sau:
a. Hiệu suất của phản ứng tổng hợp aspirin nhỏ hơn 70%.
b. Nhiệt độ bay hơi của aspirin cao hơn 70°C.
c. Acetylsalicylic acid có chứa nhóm chức ester.
d. H3PO4 đặc vừa là chất xúc tác vừa là chất hút nước để cân bằng chuyển dịch theo chiều thuận.
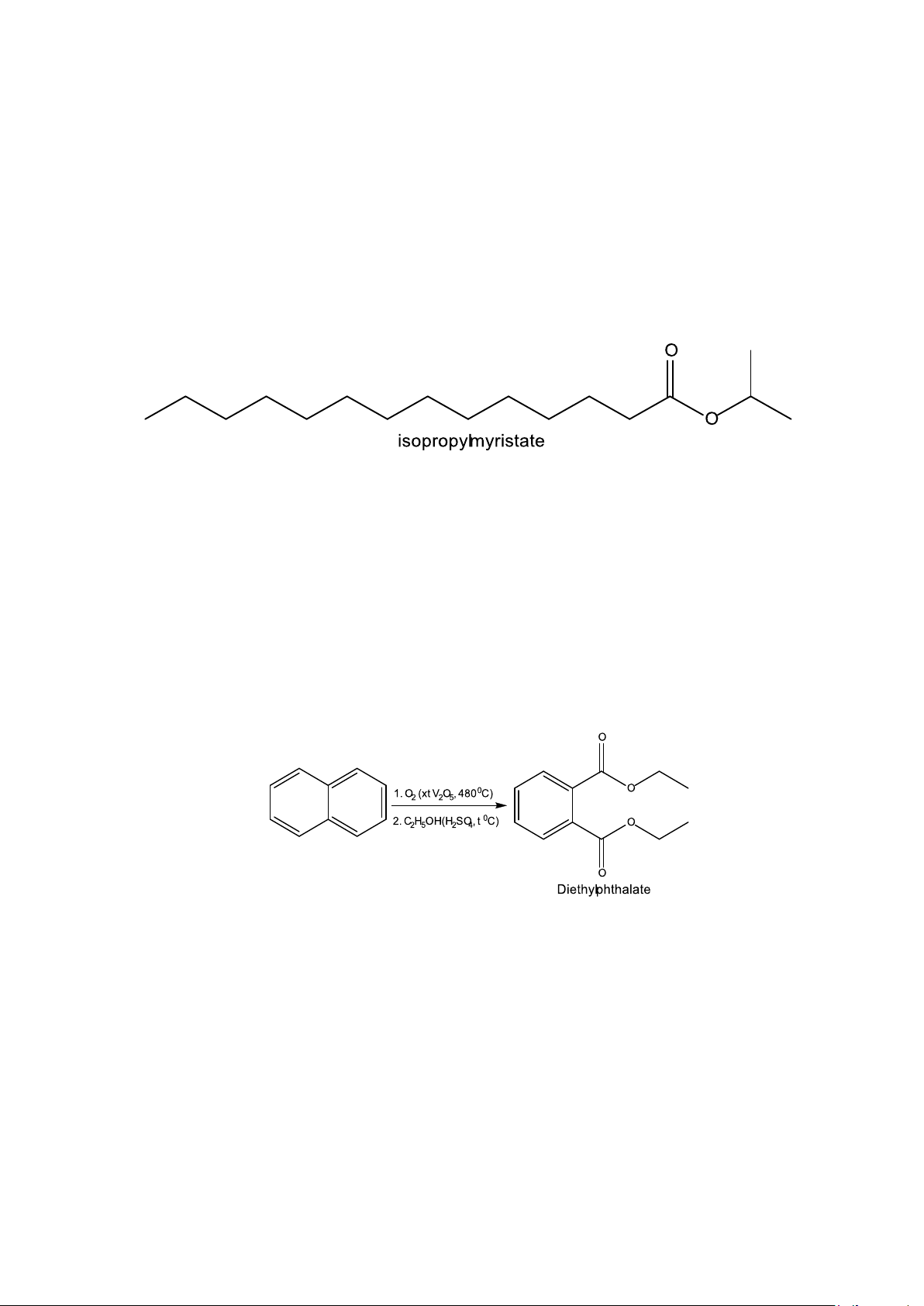
Câu 7. Isopropyl myristate là một ester thường được sử dụng trong kem dưỡng da, dầu tẩy trang và sản phẩm
chăm sóc tóc như một chất làm mềm, chất kết dính và chất tăng hương thơm vì khả năng thẩm thấu tốt mà
không gây nhờn rít. Ester này được tạo ra từ phản ứng giữa acid béo bão hòa myristic và isopropyl alcohol.
Công thức khung phân tử của isopropyl myristate như sau: Cho các phát biểu sau:
a. Công thức phân tử của isopropyl myristate là C17H34O2.
b. Để điều chế 5,4 gam isopropyl myristate trong một sản phẩm mỹ phẩm cần 4,56 gam isopropyl alcohol (giả
sử hiệu suất phản ứng là 80%).
c. Một lọ kem dưỡng da có thể tích thực là 100 mL cho biết thành phần có chứa 3% isopropyl myristate theo
khối lượng. Giả sử khối lượng riêng của kem dưỡng da đã cho là 0,85 g/mL. Lượng ester cần dùng để sản xuất
500 lọ kem trên là 1,275 kg.
d. Isopropyl myristate là một chất béo bão hòa.
Câu 8. Diethyl phthalate (DEP) là chất lỏng không màu, có vị đắng và mùi khó chịu được dùng để sản xuất
thuốc diệt côn trùng bảo vệ cho vật nuôi. Điều chế DEP qua 2 bước như sau: Cho các phát biểu sau:
a. Diethyl phthalate (DEP) được điều chế từ naphthalene.
b. DEP thuộc loại hợp chất ester 2 chức.
c. Công thức phân tử của DEP là C12H16O4.
d. Có thể thu được 109,35 kg thuốc DEP từ 192 kg naphthalene. Biết hiệu suất các phản ứng (1) và (2) lần lượt là 75% và 60%.
Câu 9. Methyl benzoate là một chất lỏng, không màu, có mùi dễ chịu và được sử dụng trong nước hoa) Nhóm
học sinh A tiến hành điều chế methyl benzoate trong phòng thí nghiệm như sau:
- Cho 12,2 gam benzoic acid và 20 mL methanol (khỏi lượng riêng 0,79 g/mL) vào bình cầu đáy tròn, lắc đều hỗn hợp.
- Thêm 3,0 mL sulfuric acid đậm đặc vào, lắc nhẹ để các chất trộn đều với nhau.
- Cho cá từ vào bình cầu, gắn bình cầu vào ống sinh hàn rồi tiền hành đun nóng trên máy khuấy từ gia 5 nhiệt trong 1 giờ.
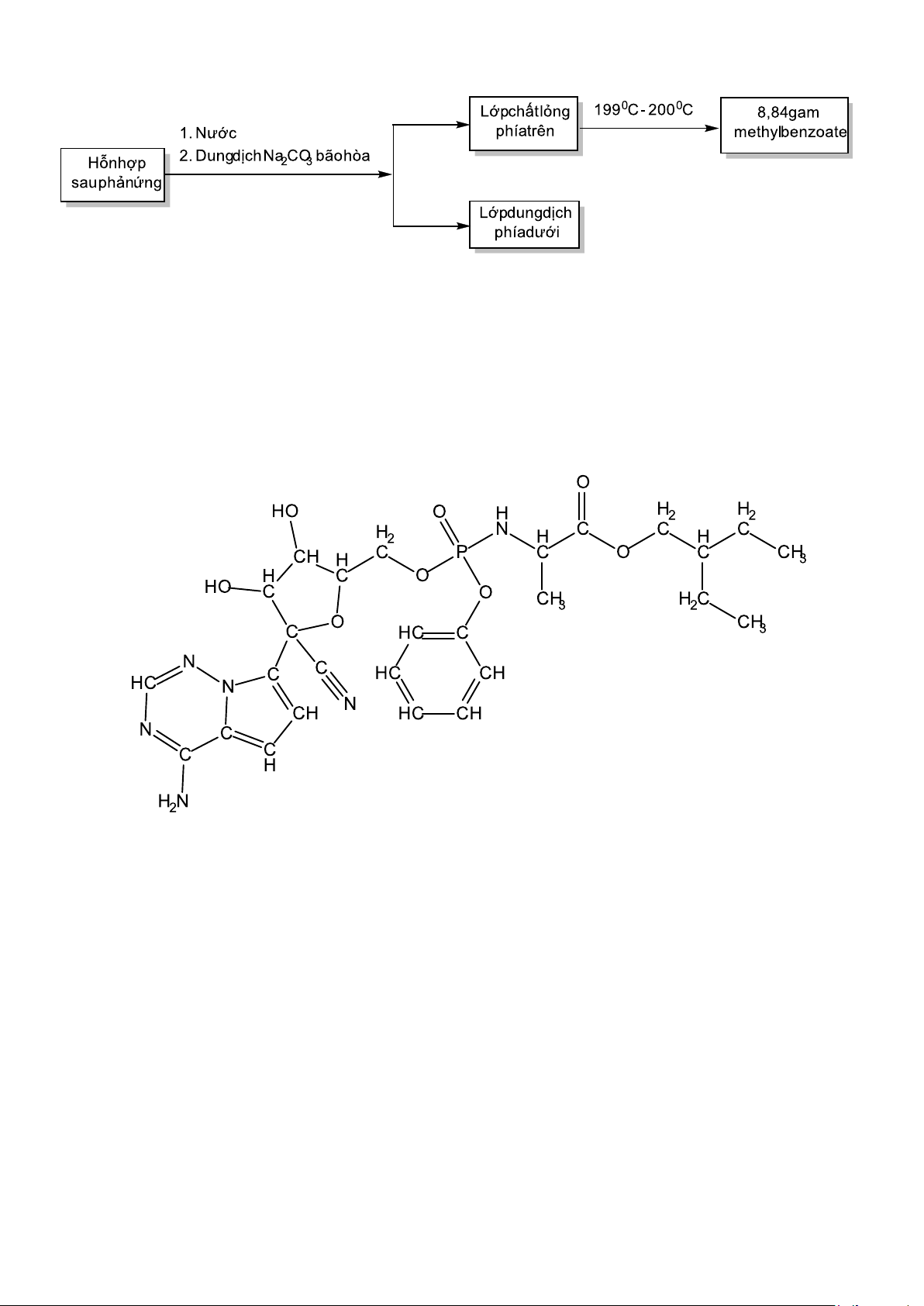
Để tách được methyl benzoate khỏi hỗn hợp, nhóm học sinh tiến hành theo sơ đồ sau: 0 H SO ,t C
a. Phương trình xảy ra là C 2 4 d ⎯⎯⎯⎯→
6H5COOH + CH3OH ⎯⎯⎯⎯ C6H5COOCH3 + H2O.
b. Vai trò của sulfuric acid trong thí nghiệm là xúc tác và hút nước làm cân băng chuyến dịch sang phải.
c. Việc thêm dung dịch Na2CO3 vào là để pha loãng sulfuric acid còn dư.
d. Hiệu suất của phản ứng ester hóa là 70%.
Câu 10. Remdesivir (kí hiệu: R) là thuốc chống virus được dùng rất thành công để khống chế dịch MERS-
CoV năm 2012. Remdesivir đã được cấp phép sử dụng điều trị SARS-CoV-2 ở người và vẫn đang tiếp tục được
cải tiến để tạo ra thuốc đặc trị. Phân tử R có công thức cấu tạo như sau:
a. Công thức phân tử của R là C27HxNyOzP. Giá trị của x, y, z lần lượt là 35 ; 8 ; 6
b. Biết khối lượng mol phân tử của R là MR = 602 g/mol. Phần trăm khối lượng các nguyên tố carbon trong R là 56%.
c. Tổng số liên kết π của R là 10.
d. Đun nóng R trong môi trường kiềm thu được hỗn hợp sản phẩm trong đó có chứa chất Y. Biết Y có tính
chất hóa học rất giống với ethyl alcohol. Công thức cấu tạo của Y là (CH3CH2)2CHCH2OH.
Câu 11. Trong ngành công nghiệp thực phẩm, các chất phụ gia như chất bảo quản, chất tạo màu và hương liệu
được sử dụng phổ biến nhằm cải thiện chất lượng sản phẩm. Chất bảo quản E211 (thành phần là muối
monosodium của acid hữu cơ đơn chức, có vòng benzene) thường dùng trong các loại nước giải khát có tính acid nhẹ.
Chất E211 khi sử dụng trong các loại nước giải khát chứa acid ascorbic (vitamin C) thì sẽ sinh ra benzene- một
chất độc có khả năng gây ung thư. Trong một nghiên cứu của hội Hóa Học HCM để khảo sát ảnh hưởng của
nhiệt và ánh sáng mặt trời, nhóm nghiên cứu đã mang một số mẫu nước giải khát đem phơi ngoài nắng trong
thời gian 3 tuần lễ. Kết quả cho thấy hàm lượng benzene trong các loại nước giải khát dạng lon nhôm thì tăng
rất ít còn trong loại nước giải khát dạng chai thủy tinh (nhựa trong) thì tăng cao. 6 Cho các phát biểu sau:
a. Cho thành phần phần trăm các nguyên tố trong E211 như sau Nguyên tố C H O Na
Thành phần phần trăm nguyên tố (%) 58,33 3,47 22.23 15,97
Công thức cấu tạo của E211 là C6H5CH2COONa.
b. Phản ứng giữa E211 và vitamin C là phản ứng oxi hóa khử.
c. Để giảm thiểu nồng độ benzene trong nước giải khát thì tránh sử dụng E211 và vitamin đồng thời. Ngoài ra
cần trữ nước ngọt trong mát, tránh ánh nắng mặt trời.
d. Một cơ sở bị phát hiện pha loãng sản phẩm nước cam (chứa chất bảo quản E211) bằng cách thêm vitamin C
tổng hợp. Cho biết thể tích mỗi chai nước cam là 350 mL (khối lượng riêng của nước cam là 1,04 g/mL), sau
khi pha loãng thì nồng độ E211 trong nước cam 0,12% (theo khối lượng) xuống còn 0,03%. Lượng benzene đã
sinh ra là 177,5 miligam. Biết phản ứng sinh benzene xảy ra theo phương trình: E211 + C6H8O6 ⎯⎯ →C6H6 + CO2 + C6H7O6Na. 7
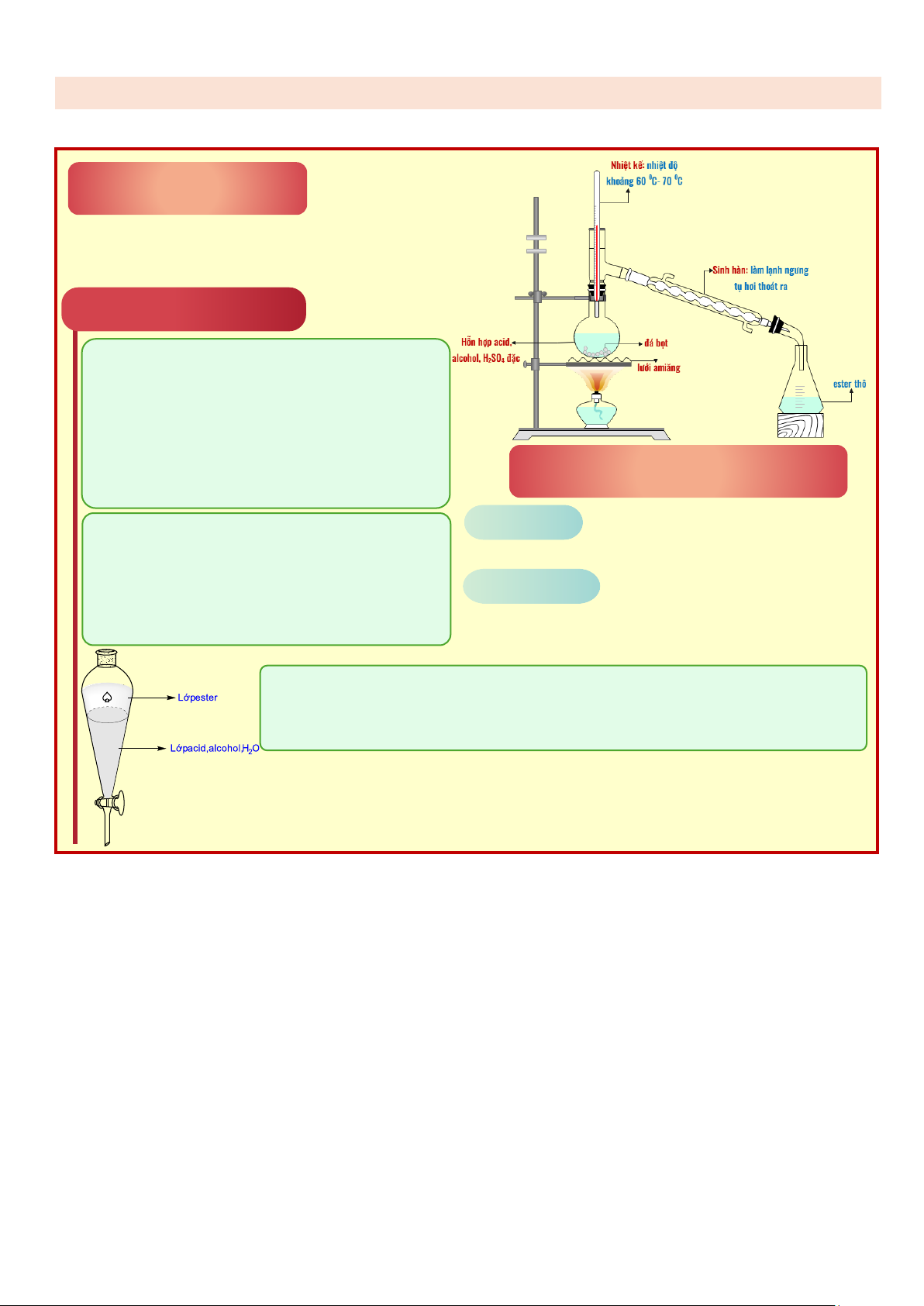
DẠNG 2. BÀI TẬP VỀ THAO TÁC THÍ NGHIỆM ĐIỀ U CHỀ ĐA SỐ ỀSTỀR PHẢN ỨNG ESTER HÓA 0 H2SO4 đ,t ⎯⎯⎯⎯→
R–CỐỐ-H + R’ỐH ⎯⎯⎯⎯ R–CỐỐ-R’ + H2Ố VAI TRÒ CÁC
CHA T VÀ LƯU Ý
Acid và alcohol nguyên chất: hạn chế sự mặt của H2O, tăng hiệu suất.
H2SO4 đặc: chất xúc tác (được sử dụng nhiều trong CN)
NaCl bão hòa (thêm vào bình chứa ester thô): làm tăng tỉ
khối của hỗn hợp lỏng (giảm độ tan của ester) nên ester
ĐIỀ U CHỀ MỐ T SỐ ỀSTỀR ĐA C dễ tách lớp hơn.
Đá bọt, silicagen : để hỗn hợp sôi đều, tránh sôi cục bộ BIỀ T Không đun sôi: Vinyl acetate
acid, alcohol dễ bay hơi (đun nhẹ) 0 Không thay H (C 3 H COO)2 Zn,t
2SO4 đặc bằng loãng hoặc HCl, HNO3
CH3CỐỐH + C2H2 ⎯⎯⎯⎯⎯⎯ →
Không thay NaCl bão hòa bằng HCl: vì HCl dễ bay hơi. CH3CỐỐCH=CH2 Phenyl acetate
CaCl2 dùng hút alcohol, H2O. Tắt đèn cồn rồi mới tháo (CH
ống dẫn khí để tránh ester chưa thoát ra bốc cháy. 3CỐ)2 + C6H5ỐH ⎯⎯ →CH3CỐỐC6H5 + CH Anhydride acetic phenol 3CỐỐH
Hỗn hợp thu được sau phản ứng: có mùi thơm (của ester).
Phương pháp chiết: dùng tách lấy ester ra khỏi hỗn hợp lỏng với dung môi không phân cực,
không tan trong nước như diethyl ether (không dùng acetone vì acetone tan trong nước). 8
PHẦN TRẢ LỜI NGẮN
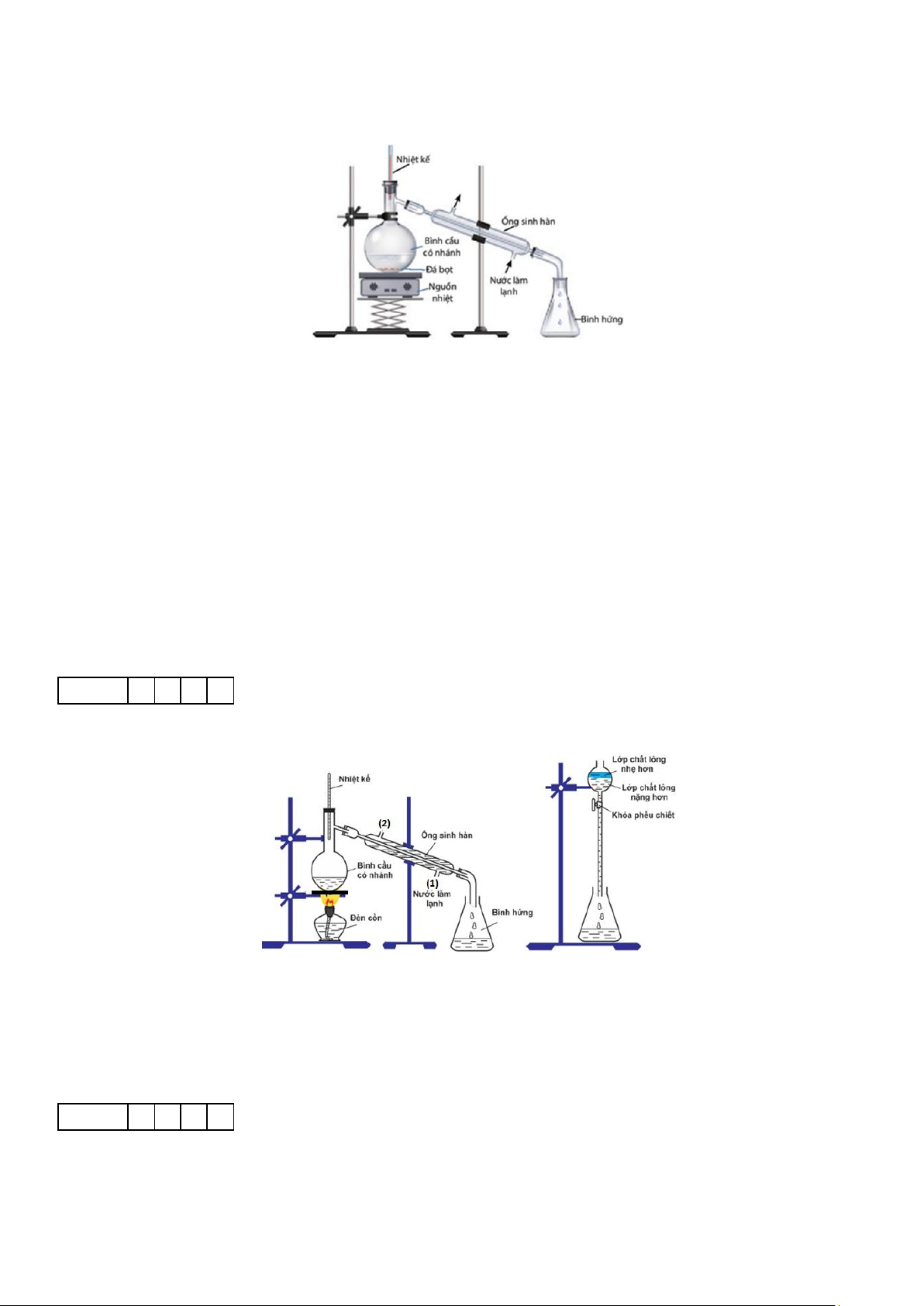
Câu 1. Tiến hành thí nghiệm chưng cất ethyl alcohol theo các bước sau :
Bước 1: Cho khoảng 100 mL dung dịch ethyl alcohol 30° vào bình cầu 250 mL, thêm đá bọt vào bình cầu.
Bước 2: Lắp dụng cụ thí nghiệm như hình bên
Bước 3: Tiến hành chưng cất và thu lấy phân đoạn chất lỏng có nhiệt độ sôi khoảng 75 – 80°C vào bình tam
giác. Dùng ống đong đo thể tích chất lỏng chưng cất được.
Cho các phát biểu sau về thí nghiệm trên :
(1) Nhiệt kế dùng để đo nhiệt độ của bình cầu.
(2) Phương pháp sử dụng trong thí nghiệm trên là phương pháp chưng cất ở áp suất thường.
(3) Do nhiệt độ sôi của ethyl alcohol thấp hơn nước, vì vậy chất lỏng thu được ở bình tam giác thành phần chỉ có ethyl alcohol.
(4) Sinh hàn có tác dụng để ngưng tụ hơi thành chất lỏng.
(5) Cho đá bọt vào bình cầu làm tăng sự đối lưu giúp cho chất lỏng không trào lên khi đun nóng.
(6) Ngoài phương pháp chưng cất để tách ethyl alcohol ta còn có thể sử dụng phương pháp kết tinh.
Các phát biểu đúng gồm những phát biểu nào? (Liệt kê theo thứ tự từ nhỏ đến lớn, ví dụ 123; 234;.). Đáp án
Câu 2. Hình vẽ sau minh họa sơ đồ điều chế isoamyl acetate trong phòng thí nghiệm: Cho các phát biểu sau:
(a). Phản ứng xảy ra trong thí nghiệm trên là phản ứng một chiều.
(b). Nhiệt kế giúp để kiểm soát nhiệt độ trong bình cầu có nhánh.
(c). Trong phễu chiết, lớp chất lỏng nhẹ hơn là isoamyl acetate.
(d). Hợp chất hữu cơ trong bình hứng đều có phổ hồng ngoại IR có số sóng hấp thụ đặc trưng của liên kết OH.
Có bao nhiêu phát biểu là đúng? Đáp án
Câu 3. Một nhóm học sinh đã thực hiện phản ứng điều chế ethyl acetate từ nguyên liệu ban đầu từ acetic acid
và ethanol trong phòng thí nghiệm. Khi phản ứng kết thúc, nhóm đã thu được hỗn hợp sản phẩm gồm ethyl
acetate và acetic acid, ethanol dư theo phương trình hóa học: 9 + 0 CH H ,t ⎯⎯⎯ → 3COOH + C2H5OH ⎯⎯ ⎯ CH3COOC2H5 + H2O
Nhóm đã dùng dung môi hữu cơ diethyl ether (C2H5OC2H5) để chiết ethyl acetate ra khỏi hỗn hợp sau phản
ứng. Cho biết nhiệt độ sôi các chất như sau: Chất Acetic acid Ethanol Ethyl acetate Diethyl ether
Nhiệt độ sôi (0C) 118 78,3 77,1 34,6 Cho các phát biểu sau:
(a) Diethyl ether là dung môi chiết lí tưởng trong thí nghiệm trên vì ethyl acetate tan tốt trong dung môi này,
còn acetic acid và ethanol lại tan tốt trong dung môi nước.
(b) Bằng phương pháp chưng cất đơn giản, ta có thể tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
(c) Do diethyl ether có nhiệt độ sôi thấp hơn nhiều so với ethyl acetate (34,6°C so với 77,1°C) nên có thể thu
được ethyl acetate sau khi chiết bằng cách dùng đèn cồn đun nhẹ cho dung môi diethyl ether bay hơi.
(d) Để an toàn, ta có thể dùng nước nóng liên tục tưới lên bình cầu trong phương pháp chưng cất đơn giản để
tách ethyl acetate ra khỏi dung môi diethyl ether sau khi chiết.
Có bao nhiêu phát biểu là đúng? Đáp án 10
PHẦN TRẮC NGHIỆM ĐÚNG SAI.
Câu 1. Trong phòng thí nghiệm, ethyl acetate được điều chế từ acetic acid và ethanol, xúc tác H2SO4 đặc, theo mô hình thí nghiệm sau:
Biết nhiệt độ trong bình cầu (4) giữ ở mức 65-70°C, nhiệt độ trong ống sinh hàn (3) duy trì ở 25°C. Sau thí
nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của acetic acid, ethanol và ethyl acetate. Cho biết
số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết
O-H (alcohol) O-H (carboxylic acid) C=O (ester, carboxylic acid) Số sóng (cm-1) 3650 - 3200 3300 - 2500 1780 - 1650
a. Chất lỏng trong bình hứng (5) có ethyl acetate.
b. Vai trò của ống sinh hàn (3) để ngưng tụ hơi; nước vào từ (1), nước ra ở (2).
c. Nhiệt độ phản ứng ở bình cầu (4) càng cao thì phản ứng điều chế ethyl acetate xảy ra càng nhanh.
d. Dựa vào phổ hồng ngoại, phân biệt được acetic acid, ethanol và ethyl acetate.
Câu 2. Cho bảng nhiệt độ sôi (°C) đo ở áp suất 1 atm như sau: Chất C2H5OH CH3COOH H2O CH3COOC2H5 H2SO4 Nhiệt độ sôi 78,3 118 100 77 337
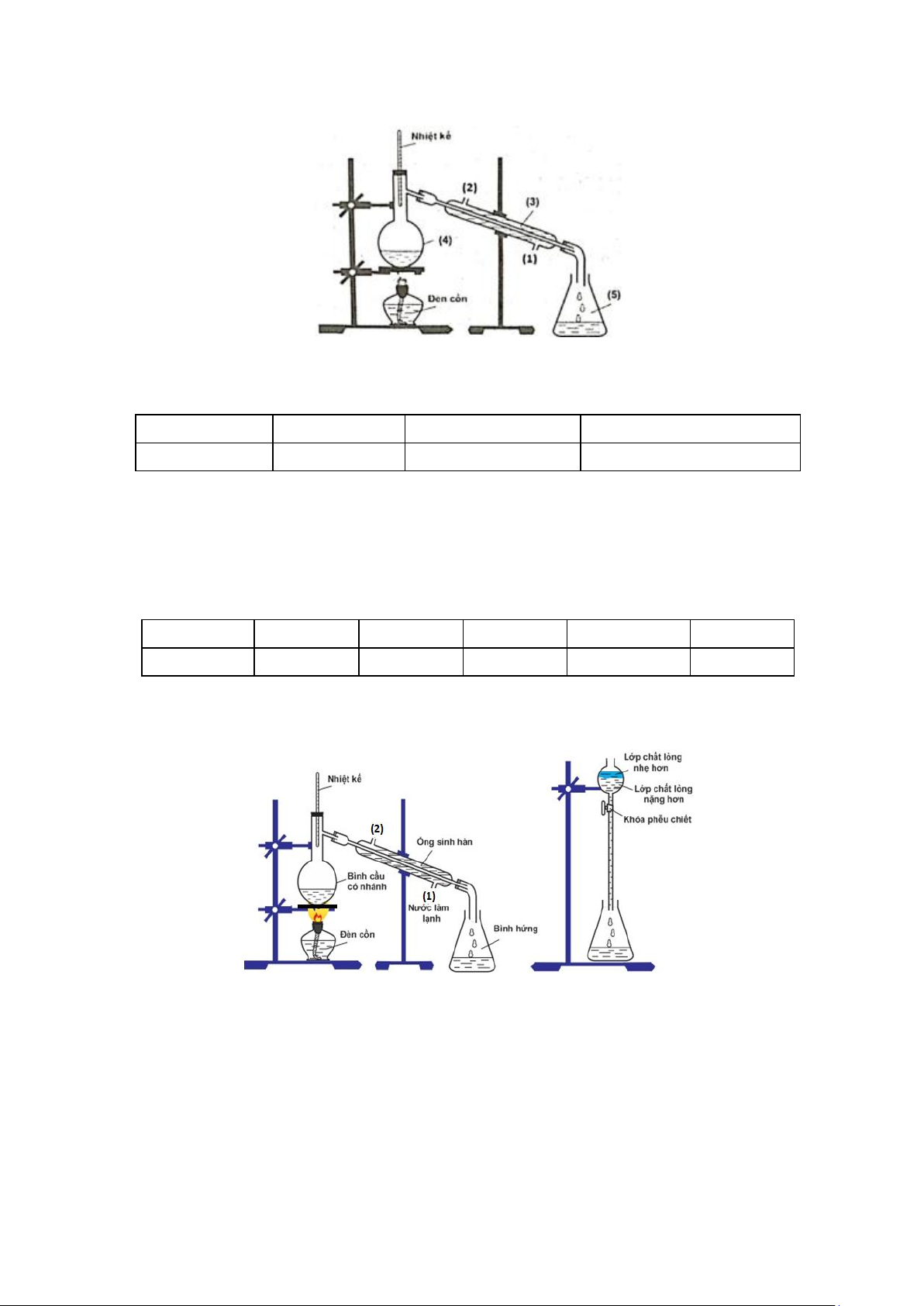
Ethyl acetate được điều chế bằng cách đun nóng hỗn hợp gồm acetic acid, ethanol và dung dịch H2SO4 98%,
đựng trong bình cầu có nhánh. Nhiệt độ bếp được thiết lập ở 80°C. Mô hình điều chế và tách ethyl acetate được thực hiện như sau:
a. Phản ứng điều chế ethyl acetate từ các nguyên liệu trên được gọi là phản ứng ester hóa.
b. Dung dịch H2SO4 đặc có vai trò làm chất xúc tác làm tăng hiệu suất của phản ứng.
c. Trong quá trình phản ứng, phần hơi tách ra từ bình cầu có nhánh sang bình hứng chủ yếu gồm ethyl acetate và nước.
d. Nếu thiết lập nhiệt độ bếp ở 150°C sẽ thu được nhiều sản phẩm ester hơn ở bình hứng.
Câu 3. Benzyl acetate là một ester có mùi thơm dễ chịu, thường được dùng trong nước hoa và mỹ phẩm.
Benzyl acetate được điều chế bằng cách đun hồi lưu hỗn hợp nguyên liệu và H2SO4 đậm đặc trong 1,5 giờ. Sau
đó, hỗn hợp sản phẩm được xử lí bằng nước, dung dịch Na2CO3 10% và NaCl bão hòa để tách và tinh chế ester. Cho các phát biểu sau: 11
a. Sau khi thêm NaCl, hỗn hợp bị tách thành hai lớp, phần chất lỏng phía dưới chứa benzyl acetate.
b. Benzyl acetate tan tốt trong nước nên cần thêm NaCl bão hòa để tách sản phẩm.
c. Nguyên liệu của phản ứng trên gồm có phenol và acetic acid.
d. Na2CO3 được thêm vào để trung hòa acid trong hỗn hợp.
Câu 4. Isoamyl acetate thường được sử dụng làm chất phụ gia để tạo mùi chuối trong thực phẩm hoặc được
dùng làm hương liệu nhân tạo. Một học sinh tiến hành điều chế isoamyl acetate theo các bước sau:
Bước 1: Cho vào bình cầu 26,4 mL isoamyl alcohol (d = 0,81 g/mL), 40 mL acetic acid (d =1,049 g/mL) và 2,5
mL H2SO4 đậm đặc, cho thêm vào bình vài viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng đứng vào miệng bình
cầu. Sau đó đun nóng bình cầu trong khoảng 1,5 giờ.
Bước 2: Sau khi đun, để nguội rồi rót sản phẩm vào phễu chiết, thêm 50 mL nước cất vào phiễu, lắc đều rồi để
yên khoảng 5 phút, lúc đó chất lỏng tách thành hai lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
Bước 3: Cho từ từ dung dịch Na2CO3 10% vào phần chất lỏng thu lấy ở bước 2 và lắc đều cho đến khi không
còn khí thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hòa rồi để yên khi đó chất lỏng tách thành hai lớp. Chiết
lấy phần chất lỏng phía trên, thu được 26,0 mL isoamyl acetate (d = 0,876 g/mL). Cho các phát biểu sau:
a. Biết tổng lượng isoamyl acetate bị thất thoát ở bước 2 và 3 là 5% so với lượng thu được ở trên, hiệu suất
phản ứng ester hóa ở bước 1 bằng 72,1 %.
b. Việc lắp ống sinh hàn ở bước 1 nhằm mục đích hạn chế sự thất thoát chất lỏng ra khỏi bình cầu.
c. Tiến hành đo phổ khối lượng (MS) của isoamyl acetate sẽ xuất hiện peak ion phân tử có m/z = 130
d. Thêm dung dịch Na2CO3 ở bước 3 nhằm mục đích loại bỏ acid lẫn trong isoamyl acetate.
Câu 5. Điều chế ethyl acetate trong phòng thí nghiệm được tiến hành như sau:
Bước 1: Cho khoảng 5 mL ethanol và 5 mL acetic acid tuyệt đối vào ống nghiệm, lắc đều hỗn hợp.
Bước 2: Thêm khoảng 2 mL dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
Bước 3: Đặt ống nghiệm vào cốc nước nóng (khoảng 60 0C – 70 0C) trong khoảng 5 phút, thỉnh thoảng lắc đều hỗn hợp.
Bước 4: Lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp rồi rót sang ống nghiệm khác chứa 10 mL
dung dịch muối ăn bão hòa thì thấy chất lỏng trong ống nghiệm tách thành hai lớp, lớp trên có mùi thơm đặc trưng.
Bước 5: Đem đo phổ hồng ngoại (IR) của chất lỏng có mùi thơm đặc trưng.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết O-H (alcohol) O-H (carboxylic acid) C=O (ester, carboxylic acid) C-O (ester) Số sóng (cm-1) 3650-3200 3300-2500 1780-1650 1300-1000
a. Trên phổ hồng ngoại của chất mùi thơm xuất hiện peak có số sóng 3500 cm-1 chứng tỏ sản phẩm chưa tinh khiết.
b. Sulfuric acid đặc vừa là chất xúc tác, vừa có tác dụng hút nước, làm tăng hiệu suất tạo ester.
c. Phản ứng xảy ra trong bước 3 theo phương trình: 0 H SO ,60−70 C CH 2 4 ⎯⎯⎯⎯⎯→
3COOH(l) + C2H5OH(l) ⎯⎯⎯⎯⎯ CH3COOC2H5(l) + H2O(l)
d. Dung dịch NaCl bão hoà làm giảm độ tan của ester trong nước để ester dễ dàng tách lớp nổi lên trên tốt hơn.
Câu 6. Khi nghiên cứu đặc điểm của phản ứng ester hoá để tổng hợp ethyl acetate, một nhóm học sinh dự đoán
“nhiệt độ càng cao, hiệu suất phản ứng ester hoá càng cao”. Từ đó nhóm học sinh tiến hành thí nghiệm tổng
hợp ethyl acetate với nồng độ ethyl alcohol và acetic acid không đổi nhưng thay đổi nhiệt độ phản ứng để kiểm
tra dự đoán trên như sau: 12
• Bước 1: Cho 32,5 mL ethyl alcohol, 30,0 mL acetic acid và 10,5 mL H2SO4 đặc vào bình cầu, lắc đều.
• Bước 2: Lắp ống sinh hàn hồi lưu vào bình phản ứng và đun trên bếp cách thuỷ có điều chỉnh nhiệt độ ở nhiệt
độ 60°C trong 60 phút. Tắt bếp và để nguội bình phản ứng.
• Bước 3: Chưng cất tách hỗn hợp sản phẩm, tách ethyl acetate bằng phễu chiết, rửa sạch, làm khô bằng CaCl2 khan.
• Bước 4: Tiến hành chưng cất lại ethyl acetate bằng hệ sinh hàn ở khoảng nhiệt độ 77°C, thu ethyl acetate và
đong thể tích ethyl acetate thu được bằng ống đong.
Lặp lại thí nghiệm trên, chỉ thay đổi nhiệt độ ở bước 2 lần lượt là 65; 70; 75; 80; 85. Nhóm học sinh ghi lại thể
tích ethyl acetate thu được với thời gian thí nghiệm tương ứng và kết quả ở bảng sau: Nhiệt độ (°C) 60 65 70 75 80 85
Thể tích ethyl acetate (mL) 25,8 30,5 35,1 39,8 36,6 32,9 Cho các phát biểu sau:
a. Theo kết quả thí nghiệm trên, thể tích ethyl acetate thu được ở 70°C là nhiều nhất.
b.Với các giá trị nhiệt độ khảo sát, phản ứng ester hoá tạo ethyl acetate ở 80°C có hiệu suất cao hơn ở 60°C.
c. Số liệu cho thấy phản ứng có nhiệt độ tối ưu ở 75°C, sau đó hiệu suất tổng hợp ethyl acetate giảm.
d. Từ kết quả thí nghiệm, kết luận được khi nhiệt độ tăng thì hiệu suất phản ứng ester hoá càng tăng.
Câu 7. Phản ứng thủy phân ester trong môi trường kiềm được biểu diễn như sau:
R-COO-R' + NaOH → RCOONa + R'OH
Một nhóm học sinh dự đoán “nồng độ NaOH càng lớn thì tốc độ phản ứng thủy phân càng lớn”. Từ đó, học
sinh tiến hành thí nghiệm ở nhiệt độ không đổi (60°C) nhưng thay đổi nồng độ NaOH để kiểm tra dự đoán trên như sau:
• Bước 1: Thêm 4 mL ethyl acetate (d = 0,9 g/mL) vào một ống nghiệm chứa 20 mL dung dịch NaOH nồng độ
C (mol/L). Các giá trị nồng độ này không giống nhau giữa các thí nghiệm.
• Bước 2: Ngâm ống nghiệm trong nồi nước nóng (nhiệt độ nước khoảng 60°C) và đo thời gian cho đến khi
phần chất lỏng trong ống nghiệm trở lên đồng nhất.
Kết quả thí nghiệm được cho ở bảng sau:
Nồng độ NaOH (mol/L) 4,0 3,6 3,2 2,8 2,4 2,0
Thời gian hỗn hợp đồng nhất (phút) 5,2 6,0 7,0 8,2 9,5 11,0 Cho các phát biểu sau:
a. Sau bước 1, phần chất lỏng trong các ống nghiệm tách thành hai lớp.
b. Phản ứng thủy phân ethyl acetate xảy ra ở bước 2 của các thí nghiệm.
c. Phản ứng thủy phân hoàn toàn tại thời điểm hỗn hợp trong ống nghiệm đồng nhất.
d. Kết quả thí nghiệm chứng tỏ dự đoán của học sinh ban đầu là chính xác. 13
DẠNG 3. BÀI TOÁN LIÊN QUAN KIẾN THỨC PHỔ.
PHƯƠNG PHÁP GIẢI BÀI TOÁN LIÊN QUAN
Bước 1. Xác định CTPT của hợp chất
- Cho phổ khối MS: thông thường tín hiệu peak có m/z lớn nhất chính là M+ và MHCHC = M+ (đây chỉ là sự gán
ghép tạm thời của SGK, trên thực tế giải phổ MS thì M+ chưa chắc là ion có m/z lớn nhất.) Lập CT phân tử m m m m m C H O N HCHC = = = = 1 2x 1y 16z 14t M Dùng công thức như sau: HCHC C H O N ... ⎯⎯ → x y z t %C %H %O %N 100 = = = = 12x 1y 16z 14t M HCHC
Bước 2. Xác định nhóm chức chính bằng phổ IR.
Bảng tín hiệu peak trên IR Hợp chất
Liên kết hấp thụ Số sóng hấp thụ (cm-1)
Hình dạng peak cơ bản Alcohol O-H 3500- 3200
Peak tù, to rộng, mạnh C-H 2830 - 2695 Aldehyde
Peak nhỏ (thường trùng với hydrocarbon) C=O 1740 - 1685
Peak nhọn, trung bình hoặc mạnh Ketone C=O 1715-1666
Peak nhọn, trung bình hoặc mạnh C=O 1715-1690 Carboxylic
Peak nhọn, trung bình hoặc mạnh acid O-H 3300- 2500
Peak to kéo dài, mạnh 14 C=O 1750 - 1715
Peak nhọn, trung bình Ester C - O 1300 -1000
Peak nhọn, hẹp trung bình -NH2 (amine bậc 1) Amine N-H 3300-3000 -NH- (amine bậc 2) Vòng thơm 1800
Dãy peak yếu, đặc trưng 15
PHẦN TRẢ LỜI NGẮN
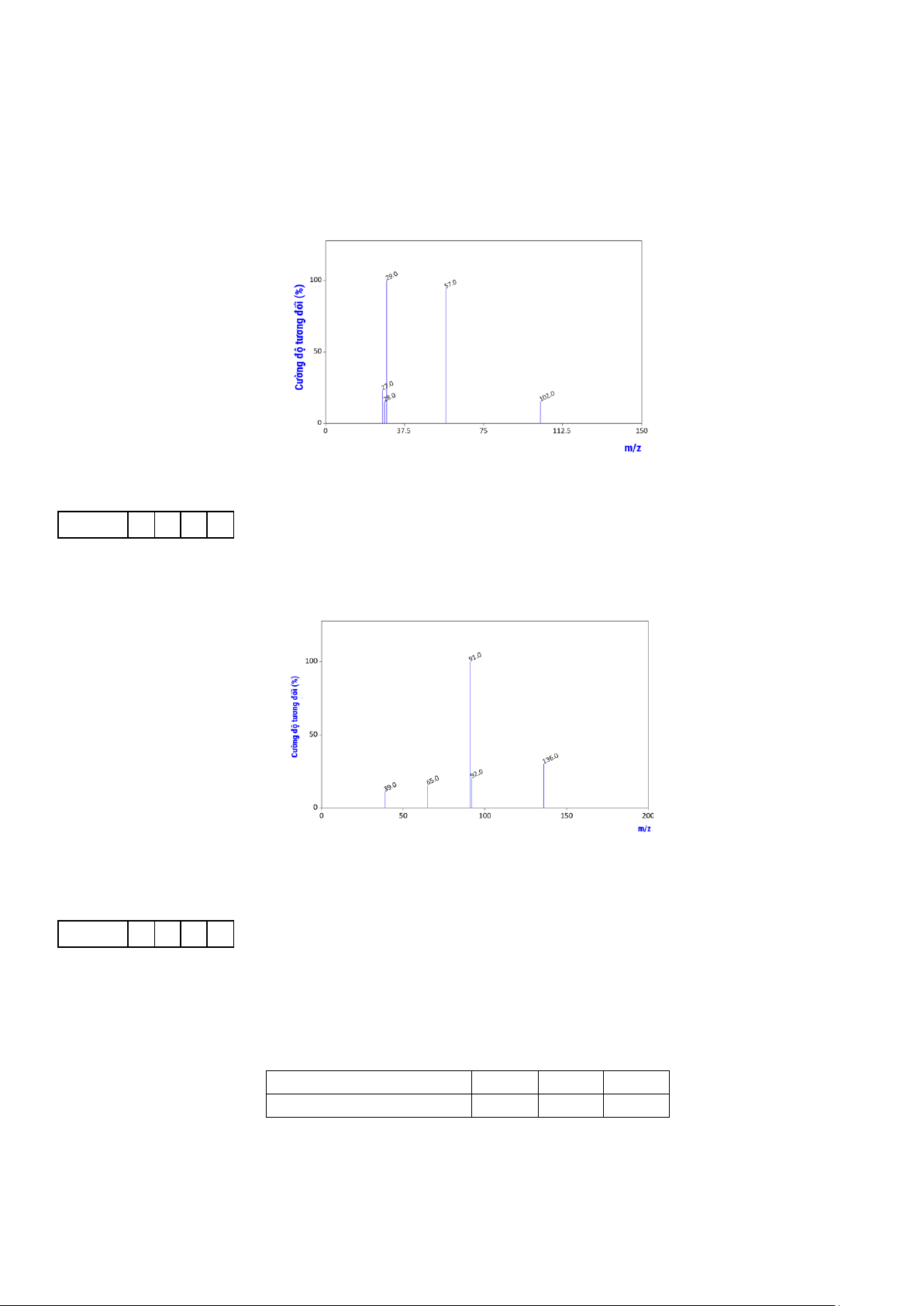
Câu 1. Cho ester đơn chức có phổ MS như sau:
Bằng phương pháp phổ NMR 13C và 1H thì thấy trong ester trên có tỷ lệ số nhóm CH3 : CH2 là 1 : 1.
Có bao nhiêu nhóm methylene trong công thức cấu tạo của X? Đáp án
Câu 2. Cho ester X có phần trăm về khối lượng C và H lần lượt là 70,59% và 5,88%, còn lại là O.
Hình ảnh dưới đây là kết quả phổ MS của X:
Khi phân tích bằng phổ NMR 1H của X thì cho kết quả như sau: X có 2 loại nguyên tử H trong đó có 5H nằm trong vòng benzene
Có bao nhiêu nhóm methyl trong công thức cấu tạo của X? Đáp án
Câu 3. Hợp chất E được điều chế từ alcohol X và carboxylic acid Y (biết Y là hợp chất tạp chức chứa vòng
benzene). E có trong thành phần của một số thuốc giảm đau, xoa bóp, cao dán,. dùng để điều trị đau lưng, căng cơ, bong gân,.
Thành phần về khối lượng các nguyên tố trong E như sau: Nguyên tố C H O
Phần trăm về khối lượng 63,16 5,26 31,58
Phân tích E bằng phổ IR cho kết quả sau:
+ peak đặc trưng của liên kết C=O (số sóng 1750-1735 cm-1),
+ liên kết C-O (số sóng 1300-1000 cm-1)
+ peak đặc trưng của liên kết O-H (số sóng 3650-3200 cm-1). 16
Từ phổ MS, xác định được E có phân tử khối là 152 amu. (1) X là methyl alcohol.
(2) Tổng số nguyên tử trong phân tử E là 20.
(3) Y có nhóm -OH và -COOH.
(4) Nếu lấy 1 mol Y tác dụng NaOH thì số mol NaOH cần để phản ứng vừa đủ là 2 mol.
Có bao nhiêu phát biểu là đúng? Đáp án
Câu 4. Điều chế ethyl acetate trong phòng thí nghiệm được tiến hành như sau:
- Bước 1: Cho khoảng 5 mL ethanol và 5 mL acetic acid tuyệt đối vào ống nghiệm, lắc đều hỗn hợp.
- Bước 2: Thêm khoảng 2 mL dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
- Bước 3: Đặt ống nghiệm vào cốc nước nóng (khoảng 60 °C – 70 °C) trong khoảng 5 phút, thỉnh thoảng lắc
đều hỗn hợp. Sau đó lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp rồi rót sang ống nghiệm khác
chứa 10 mL dung dịch muối ăn bão hòa thì thấy chất lỏng trong ống nghiệm tách thành hai lớp, lớp trên có mùi
thơm đặc trưng. Phản ứng xảy ra trong thí nghiệm theo phương trình hoá học sau:
CH3COOH(l) + C2H5OH(l)
CH3COOC2H5(l) + H2O(l) KC = 4
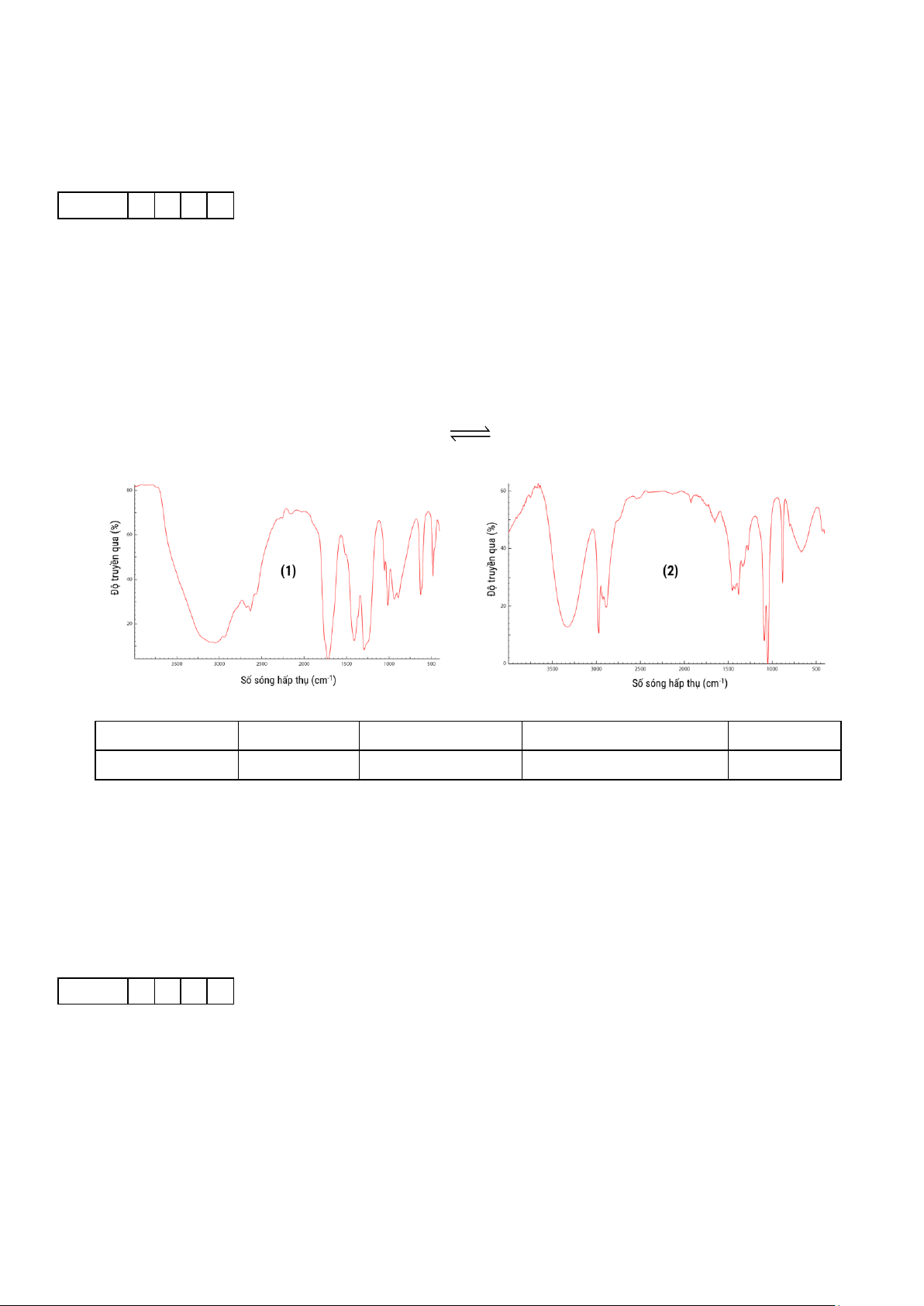
Cho phổ IR của hai hợp chất hữu cơ trong phản ứng trên như hình dưới đây.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết
O–H (alcohol) O–H (carboxylic acid) C=O (ester, carboxylic acid) C–O (ester) Số sóng (cm–1) 3650 – 3200 3300 – 2500 1780 – 1650 1300 – 1000 Cho các phát biểu sau:
(a). Phổ IR trong hình 1 là của C2H5OH, hình 2 là của CH3COOH.
(b). Sulfuric acid đặc vừa là chất xúc tác, vừa có tác dụng hút nước, làm tăng hiệu suất tạo ester.
(c). Ban đầu, nếu cho 0,625 mol acetic acid tác dụng với 1 mol ethanol thì khi đạt đến trạng thái cân bằng, hiệu
suất phản ứng ester hóa là 75%.
(d). Dung dịch NaCl bão hoà giúp ester tạo thành tách lớp nổi lên trên tốt hơn.
(e). Phản ứng hóa học xảy ra trong thí nghiệm trên là phản ứng thủy phân ester.
Có bao nhiêu phát biểu đúng? Đáp án 17
PHẦN TRẮC NGHIỆM ĐÚNG SAI.
Câu 1. Đun nóng hỗn hợp gồm ethyl alcohol, acetic acid và sulfuric acid đặc ở điều kiện thích hợp để tổng
hợp ra ester E. Sau một thời gian phản ứng thì thu được hỗn hợp X. Tiến hành tách được chất E từ X. Cho các
thông số tính chất vật lý sau: Chất
Khối lượng riêng (g.mL-1) Độ tan trong 100 g
Nhiệt độ sôi (oC) nước(g) H2O 1,00 100 C2H5OH 0,79 ∞ 78 CH3COOH 1,05 ∞ 118 CH3COOC2H5 0,90 2 77
a. Phản ứng ester hóa giữa ethyl alcohol và acetic acid là phản ứng một chiều.
b. Để tách E ra khỏi X, sử dụng phương pháp chưng cất sẽ phù hợp hơn phương pháp chiết.
c. Phổ IR của E có peak hấp thụ đặc trưng của liên kết C=O và C-O.
d. Ở phản ứng trên có sự tách OH từ phân tử acetic acid và H từ phân tử ethyl alcohol.
Câu 2. Một học sinh tiến hành tổng hợp ethyl butyrate (thành phần chính tạo mùi dứa) từ butyric acid và
ethanol theo phương trình hóa học sau: H 2SO4 ,t
CH CH CH COOH + C H OH CH CH CH COOC H + H O 3 2 2 2 5 3 2 2 2 5 2
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của butyric acid, ethanol và ethyl
butyrate. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết O-H (alcohol) O-H (carboxylic acid) C=O (ester, carboxylic acid) Số sóng (cm-1) 3650-3200 3300-2500 1780-1650
a. Dựa vào phổ hồng ngoại, phâ biệt được butyric acid, ethanol và ethyl butyrate.
b. Ethyl butyrate có cùng công thức phân tử với isopropyl acetate.
c.Phản ứng tổng hợp trong thí nghiệm này là phản ứng ester hóa.
d. Phổ hồng ngoại có số sóng hấp thụ ở 1730 cm-1 mà không có số sóng hấp thụ đặc trưng của liên kết O-H là phố của ethyl butyrate.
Câu 3. Ethyl benzoate là hợp chất chính tạo mùi thơm của quả anh đào (cherry). Một học sinh tiến hành tổng
hợp ethyl benzoate từ benzoic acid và ethyl alcohol theo phương trình hoá học sau: H 2SO4 ,t
C H COOH + C H OH C H COOC H + H O 6 5 2 5 6 5 2 5 2
Sau thí nghiệm, tiến hành phân tách sản phẩm. Ghi phổ hồng ngoại của ethyl benzoate, benzoic acid và ethyl
alcohol. Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết O-H (alcohol) O-H (carboxylic acid) C=O (ester, carboxylic acid) Số sóng (cm-1) 3650 - 3200 3300 – 2500 1780 - 1650
a. Phổ hồng ngoại có số sóng hấp thụ đặc trưng ở 3391 cm-1 là phổ của ethyl alcohol.
b. Phổ hồng ngoại có số sóng hấp thụ đặc trưng ở 1726 cm-1 mà không có số sóng hấp thụ đặc trưng của liên
kết O-H là của ethyl benzoate.
c. Dựa vào phổ hồng ngoại phân biệt được benzoic acid, ethyl alcohol và ethyl benzoate.
d. Phản ứng ester hoá ở trên có sự tách nguyên tử H từ phân tử benzoic acid và nhóm OH từ phân tử ethyl alcohol.
Câu 4. Ba hợp chất hữu cơ đơn chức X, Y, Z đều mạch hở, phân tử đều chứa C, H, O. Phổ khối lượng của X,
Y, Z đều có peak ion phân tử có giá trị m/z = 60. Kết quả phân tích bằng phổ IR như sau: 18
• Phổ hồng ngoại của X có peak ở số sóng hấp thụ 3360 cm-1 nhưng không có số sóng hấp thụ ở vùng 1780 cm-1-1600 cm-1
• Phổ hồng ngoại của Y có peak nhọn ở số sóng hấp thụ ở 1720 cm-1 nhưng không có peak ở vùng 3600 cm-1 – 2500 cm-1.
• Phổ hồng ngoại của Z có peak to, rộng ở vùng 2950 cm-1 và peak nhọn ở vùng 1715 cm-1.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết O–H (alcohol) O–H (carboxylic acid) C=O (ester, carboxylic acid) Số sóng (cm-1) 3650 – 3200 3300 – 2500 1780 – 1650
a. Y và Z là đồng phân của nhau.
b. X là propyl alcohol hoặc isopropyl alcohol.
c. Y là acetic acid, Z là methyl formate.
d. Nhiệt độ sôi của ba chất tăng dần theo thứ tự là Y < X < Z.
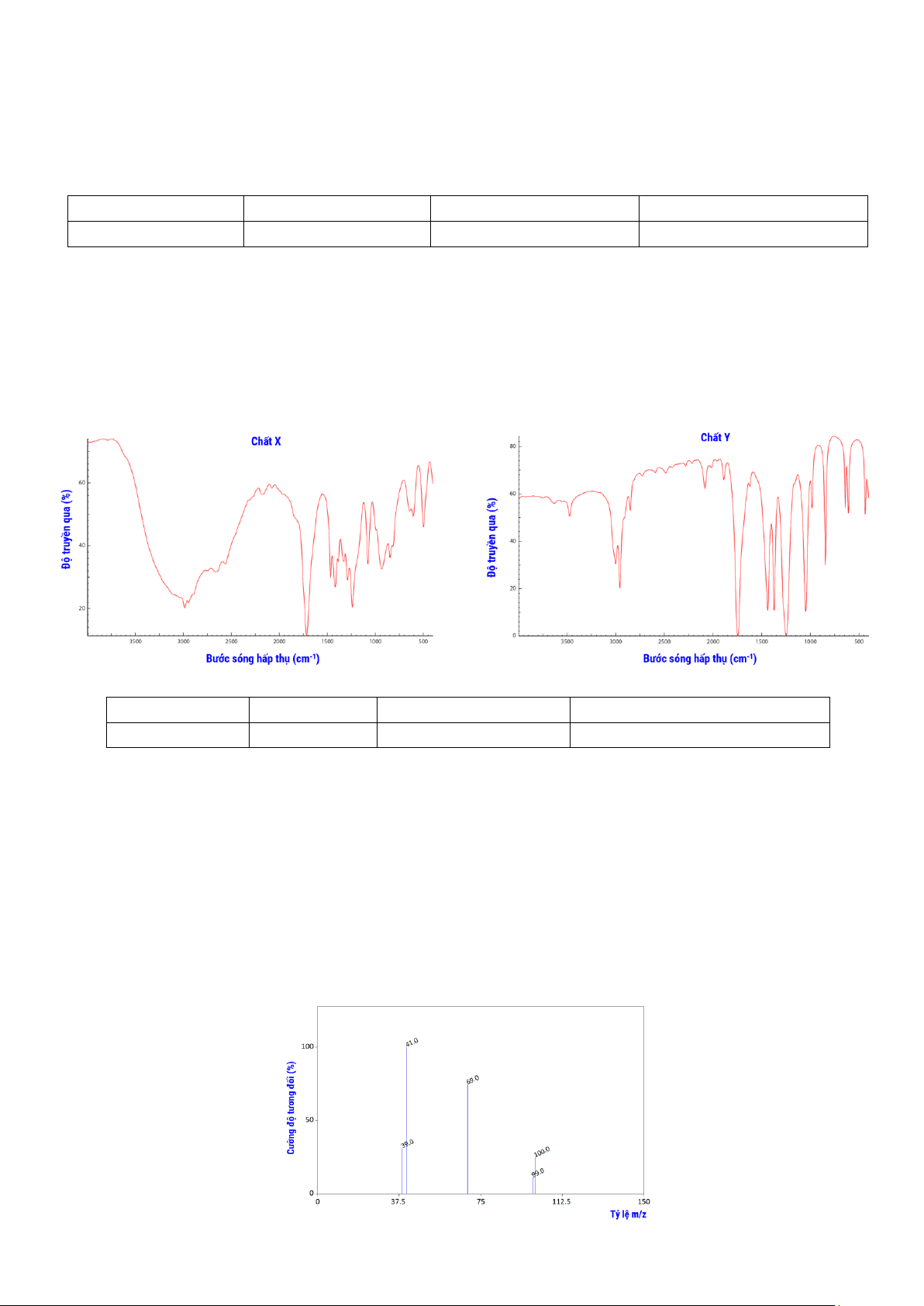
Câu 5. Cho 2 chất hữu cơ X, Y đều đơn chức, có cùng công thức phân tử C3H6O2. Phổ hồng ngoại của X, Y
được trình bày sau đây:
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau: Liên kết
O-H (alcohol) O-H (carboxylic acid) C=O (carboxylic acid và ester) Số sóng (cm-1) 3600-3300 3300-2500 1750-1735
a. X và Y là đồng phân của nhau.
b. X hoặc Y có thể có công thức cấu tạo CH3COCH2OH.
c. Phổ hồng ngoại của X có peak hấp thụ ở 1725 cm-1 và peak hấp thụ rộng ở vùng 3 600 – 3 200 cm-1 nên X là propionic acid.
d. Y là ester vì phổ hồng ngoại của Y có peak hấp thụ ở 1750 cm-1 nhưng không có peak hấp thụ đặc trưng
của liên kết O-H trong alcohol hoặc carboxylic acid.
Câu 6. Phân tích phần trăm khối lượng các nguyên tố của ester X cho thấy X chứa 60% carbon, 8% hydrogen,
còn lại là oxygen. Thủy phân X trong môi trường acid thu được methyl alcohol (Y) và carboxylic acid Z. Phổ
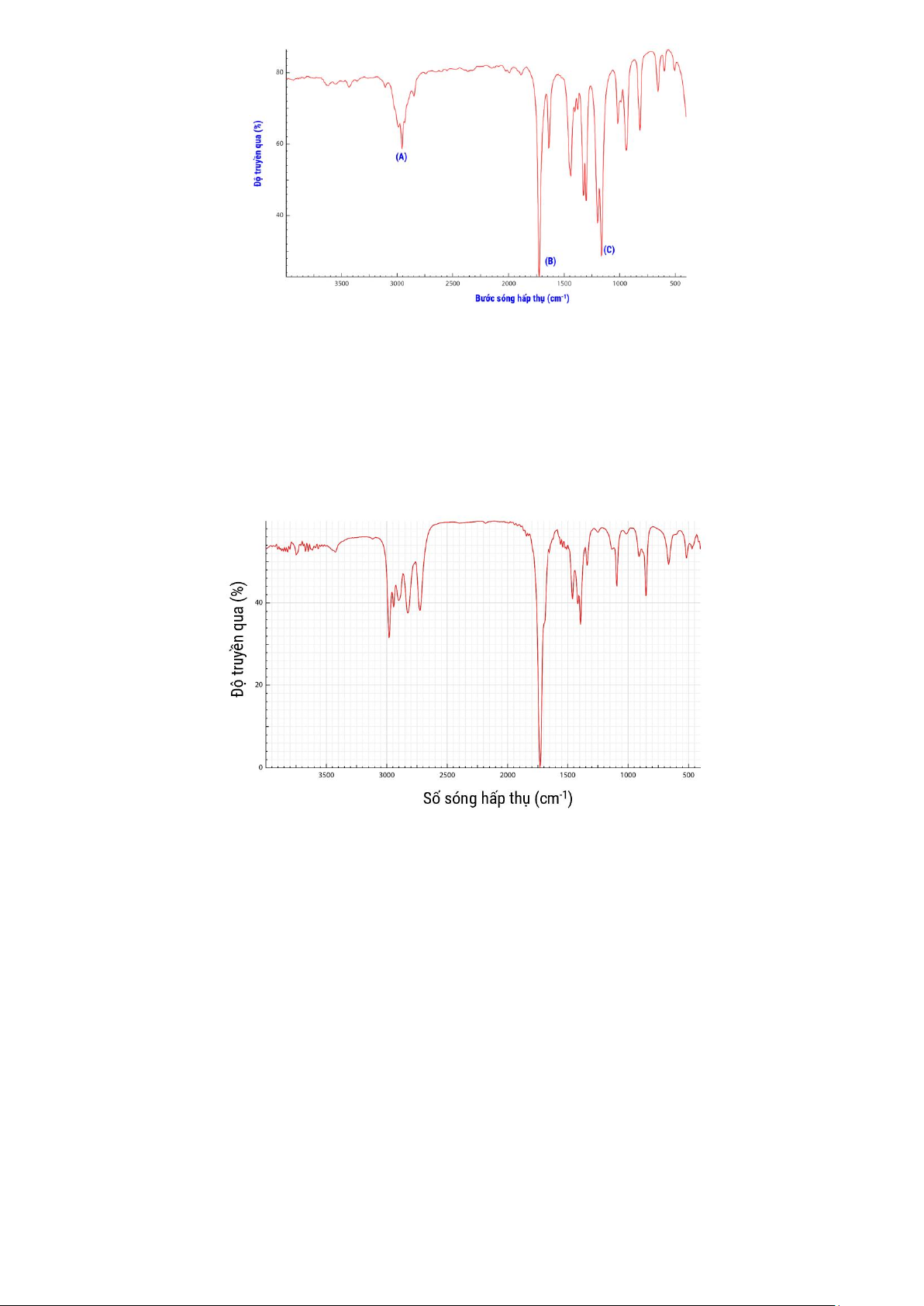
khối lượng và phổ hồng ngoại của X được cho trong hình dưới đây: 19
a. Khối lượng phân tử của X là 100.
b. Tổng số nguyên tử hydrogen và oxygen trong phân tử X là 12.
c. Tín hiệu hấp thụ đặc trưng cho liên kết C=O (ester) của X trên phổ hồng ngoại là điểm B.
d. Điều chế X trong phòng thí nghiệm bằng cách đun nóng 0,099 mol alcohol Y với 8,00 mL carboxylic acid Z
(D = 1,02 g/mL), có dung dịch H2SO4 đặc làm xúc tác, thu được 5,58 gam ester X. Hiệu suất của phản ứng ester
hóa là 50% (kết quả làm tròn đến hàng đơn vị). Cho H = 1, C = 12, O = 16.
Câu 7. Hợp chất hữu cơ X no, mạch hở, công thức phân tử là C3H6O và phổ IR của chất X như sau:
Mối quan hệ các hợp chất X, Y, Z, T được biểu diễn bằng các phương trình: (1) X LiAlH4 ⎯⎯⎯→ Y (2) X + Br2 + H2O ⎯⎯ → Z + 2HBr 0 H SO đ, t C (3) Y + Z 2 4 ⎯⎯⎯⎯⎯ → ⎯⎯⎯⎯ T + H2O Cho các phát biểu sau:
a. Dựa trên phổ IR có thể xác định X là acetone.
b. Ester T có danh pháp thay thế là propyl propionate.
c. Hợp chất X thể hiện tính oxi hóa ở phản ứng (1) và tính khử ở phản ứng (2).
d. Hợp chất X, Y, Z tan được trong nước vì đều có khả năng tạo liên kết hydrogen với nước.
Câu 8. Hợp chất hữu cơ X có phần trăm khối lượng C và H lần lượt là 68,04%, 7,22%, còn lại là O. Hình ảnh
dưới đây là kết quả chụp phổ khối lượng (MS) của X: 20

