
Preview text:
HỘI CÁC TRƯỜNG THPT CHUYÊN
KÌ THI CHỌN HỌC SINH GIỎI KHU VỰC MỞ RỘNG
HỘI CÁC TRƯỜNG THPT CHUYÊN
KHU VỰC DH & ĐB BẮC BỘ NĂM HỌC 2011- 2012
KHU VỰC DH & ĐB BẮC BỘ
MÔN THI: HÓA HỌC LỚP 11
Ngày thi: 21 tháng 4 năm 2012 ĐỀ CHÍNH THỨC
(Thời gian làm bài 180 phút không kể thời gian giao đề)
Đề thi gồm 3 trang Câu 1: (2,5 điểm)
1. Cho các chất BF3, CF4, NH3.
a. Viết công thức Lewis và cho biết dạng hình học của các phân tử trên.
b. Các chất trên, chất nào đóng vai trò là axit, bazơ theo Lewis? 2. Cho phản ứng: 3378
Fe3O4 (r) + H2 (k) 3 FeO (r) + H2O (k) (1) có: lgKp = - + 3,648. T 748 FeO −
(r) + H2 (k) Fe(r) + H2O(k) (2) có: lgKp = + 0,573. T
a. Xác định H0; S0 của (1) và (2) giả thiết rằng H0; S0 không phụ thuộc vào nhiệt độ.
b. Trong một bình kín dung tích không đổi tại nhiệt độ 10000C, ban đầu có 0,1 mol Fe3O4,
người ta 0,4 mol cho H2 vào. Xác định thành phần của hệ tại thời điểm cân bằng. Câu 2: (2,5 điểm)
1. A là một hợp chất của nitơ và hiđro với tổng số điện tích hạt nhân bằng 10. B là một oxit của
nitơ, chứa 36,36% oxi về khối lượng.
a. Xác định các chất A, B, D, E, G và hoàn thành các phương trình phản ứng: A + NaClO ⎯⎯
→ X + NaCl + H2O ; A + Na 1:1 ⎯⎯→ G + H2 X + HNO2 ⎯⎯ → D + H2O ; G + B ⎯⎯ → D + H2O D + NaOH ⎯⎯ → E + H2O
b. Viết công thức cấu tạo của D và nêu các tính chất hóa học đặc trưng của D.
2. Để định lượng đồng người ta hoà tan 1,080 gam quặng đồng trong môi trường thích hợp tạo
muối đồng (II), rồi thêm KI dư. Sau đó chuẩn độ iot giải phóng ra hết 15,65 ml Na2S2O3
0,0950M. Tính % khối lượng Cu trong quặng.
Câu 3: (2,5 điểm)
1. Điện phân dung dịch X chứa NiSO4 0,02M và CoSO4 0,01M trong axit H2SO4 0,5M ở 250C,
dùng điện cực Pt với dòng điện I = 0,2A.
a. Viết phương trình phản ứng xảy ra ở các điện cực, tính thế của các cặp oxi hóa khử ở từng điện
cực và cho biết hiệu thế tối thiểu phải đặt vào hai cực để quá trình điện phân bắt đầu xảy ra.
b. Cation nào bị điện phân trước? Khi cation thứ hai bắt đầu điện phân thì nồng độ của cation thứ nhất còn bao nhiêu?
2. Nếu điện phân dung dịch chứa NiSO4 0,02M; CoSO4 0,01M và NaCN 1M thì kim loại nào sẽ
tách ra trước? Có thể tách hai kim loại ra khỏi nhau bằng phương pháp điện phân dung dịch này
không? Biết rằng một ion được coi là tách hoàn toàn khỏi dung dịch khi nồng độ ion của nó còn
lại trong dung dịch nhỏ hơn 10-6 M. 1
Cho biết ở 250C, Eo Ni2+/Ni = - 0,233V; Eo Co2+/Co = - 0,277V; Eo O2,H+/H2O = 1,23V; PO2= 0,2 atm.
Các phức chất: [Co(CN)6]4- có lg1 = 19,09; [Ni(CN)4]2- có lg2 = 30,22.
Quá thế của H2/Pt đủ lớn để quá trình điện phân H+ và nước tại catot không xảy ra. Câu 4: (2,5 điểm)
1. Tiến hành chuẩn độ dung dịch CH3COOH (0,15M) bằng dung dịch NaOH (0,10M), người ta lấy
10 ml mẫu cho vào bình tam giác và thêm 2-3 giọt dung dịch chất chỉ thị sau đó nhỏ từ từ từng
giọt dung dịch NaOH từ buret và lắc đều đến khi chỉ thị chuyển màu. Cho pK(CH3COOH) = 4,76.
a. Tính pH tại điểm tương đương của phép chuẩn độ.
b. Tính thể tích dung dịch NaOH đã thêm nếu sử dụng chất chỉ thị:
• Metyl da cam (pT = 4,4).
• phenolphtalein (pT = 9,0).
2. Cho phản ứng: 2A(k) + B(k) ⎯⎯
→ C(k) (1) tại 4000C có năng lượng hoạt động hóa học (năng
lượng hoạt hóa) là 140 KJ/mol; khi có mặt chất xúc tác, năng lượng hoạt hóa giảm còn 60 KJ/mol.
a. So sánh tốc độ phản ứng khi có chất xúc tác với tốc độ phản ứng khi không có chất xúc tác?
b. Ở nhiệt độ bao nhiêu (trong điều kiện không có chất xúc tác) tốc độ của (1) bằng tốc độ của
phản ứng ở 4000C có xúc tác trên.
Câu 5: (2,5 điểm)
1. a. Sáu chất có công thức phân tử C4H8O, đều quang hoạt và có các tính chất vật lý thông thường
khác nhau (nhiệt độ nóng chảy, nhiệt độ sôi ...). Hãy biểu diễn cấu trúc của chúng.
b. Năm chất cũng có công thức phân tử C4H8O, đều không quang hoạt nhưng có các tính chất vật lý
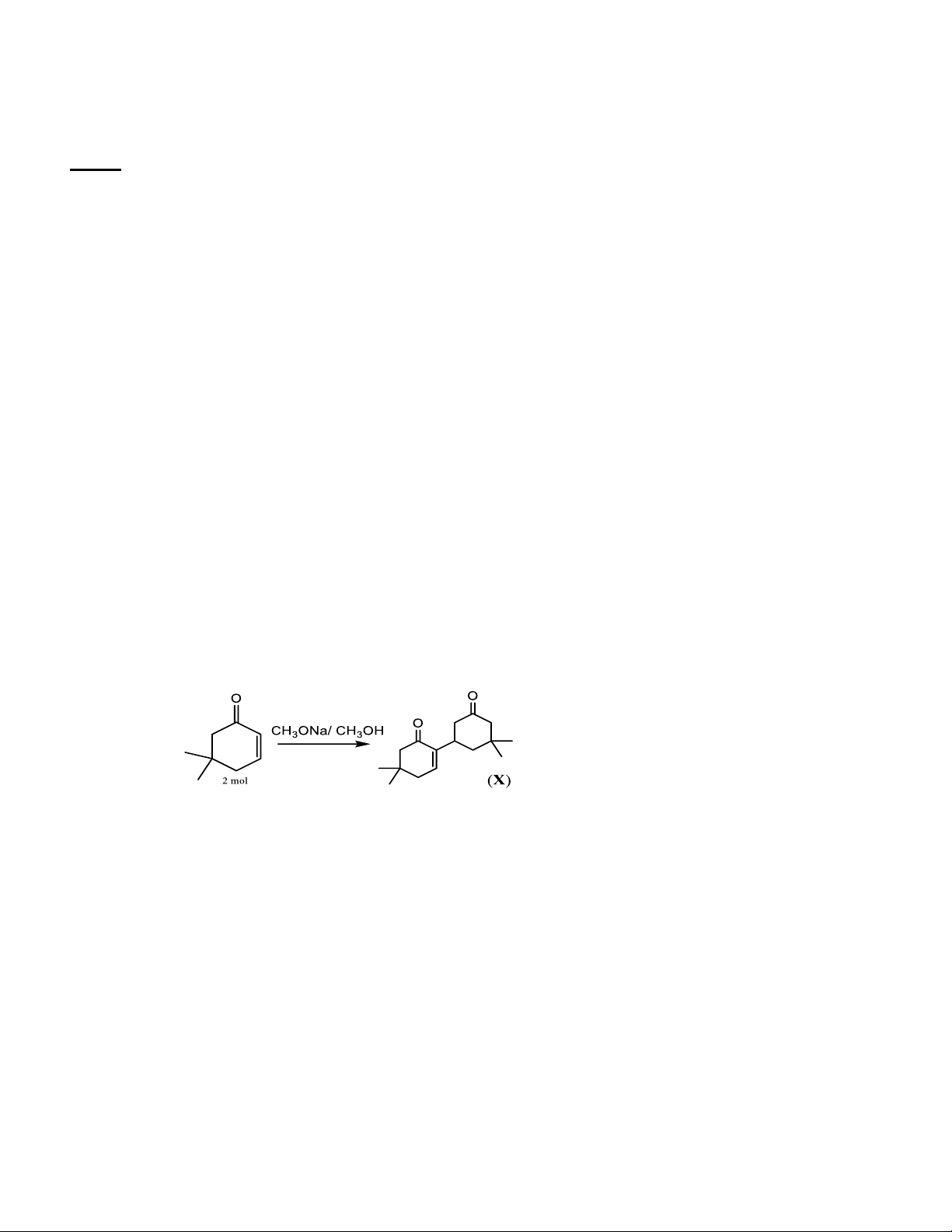
thông thường khác nhau (nhiệt độ nóng chảy, nhiệt độ sôi ...). Hãy biểu diễn cấu trúc của chúng. 2. Cho sơ đồ
a/ Đề nghị cơ chế chi tiết quá trình hình thành X.
b/ Trong quá trình tạo ra (X) còn sinh ra 4 sản phẩm phụ (X1, X2, X3 và X4) là đồng phân cấu tạo
của X. Hãy biểu diễn cấu tạo của chúng.
Câu 6: (2,5 điểm)
1. Có 5 lọ không nhãn được kí hiệu từ A đến E chứa riêng lẻ 5 hợp chất thơm sau:
C6H5COCH2CH3, C6H5COOH, C6H5COCH3, C6H5CH(OH)CH3 và C6H5CHO. Dựa vào các
kết quả thí nghiệm sau đây nhận biết hóa chất có trong mỗi lọ:
- Cho vào mỗi lọ 1 giọt dung dịch K2Cr2O7/H2SO4 rồi lắc đều. Sau vài phút thấy lọ A và C
biến đổi dung dịch màu da cam thành xanh lục.
- Cho vào mỗi chất một ít dung dịch NaOH loãng thì chỉ riêng lọ B tan được.
- Khi cho tác dụng với I2 trong dung dịch kiềm thì lọ A và E cho kết tủa vàng.
- Lọ C, D và E đều tác dụng với 2,4-đinitrophenylhydrazine cho kết tủa đỏ, da cam.
2. So sánh tính axit của các chất dưới đây và giải thích ngắn gọn. 2
a. Axit bixiclo[1.1.1]pentan-1-cacboxylic (A) và axit 2,2-đimetyl propanoic (B)
b. C6H5CO2H (E), C6H5CO3H (F) và C6H5SO3H (G) c. COOH COOH , COOH , HO COOH M OH HO N P Q
Câu 7: (2,5 điểm)
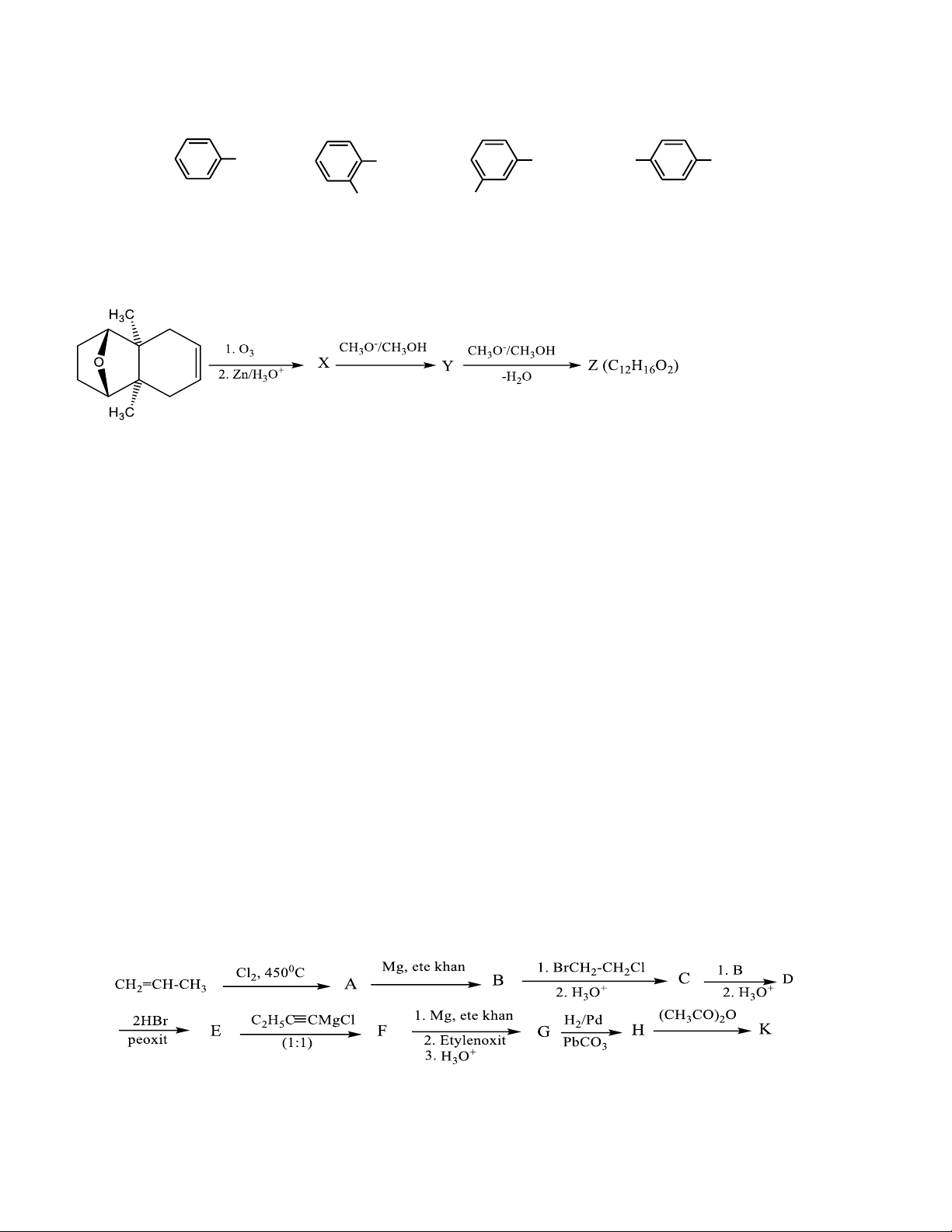
1. Cho sơ đồ chuyển hóa :
a. Biểu diễn cấu tạo của X, Y, Z.
b. Biểu diễn 1 cấu trúc của Y và cho biết cấu hình tuyệt đối của các nguyên tử cacbon bất đối.
2. Chất A có CTPT là C8H16O và có phản ứng Iođofom nhưng không cộng được H2. Khi đun A
với H2SO4 đặc ở 170oC ta thu được hỗn hợp X trong đó có 3 chất B, C và D có cùng CTPT là
C8H14 , đều không có đồng phân hình học. Nếu ozon phân khử hoạc oxy hóa hỗn hợp X thì sản
phẩm thấy xuất hiện xiclopentanon.
a. Xác định công thức cấu tạo của A, B, C, D.
b. Trình bày cơ chế chuyển A thành B, C, D.
Câu 8: (2,5 điểm)
1. Thủy phân hợp chất A (C13H18O2) trong môi trường axit HCl loãng cho hợp chất B (C11H14O). Chất
B cũng được tạo ra khi cho cumen tác dụng với axetylclorua (xúc tác AlCl3). Khi B phản ứng với
brom trong NaOH, sau đó axit hóa thì thu được axit C. Nếu đun nóng B với hỗn hợp hiđrazin và
KOH trong glicol thì cho hiđrocacbon D. Mặt khác, B tác dụng với benzanđehit trong dung dịch
NaOH loãng (có đun nóng) thì tạo thành E (C18H18O). Cho E tác dụng NaBH4 được hợp chất F.
Cho F tác dụng với Br2/CCl4 thu được G.
a. Hãy cho biết công thức cấu tạo của các hợp chất từ A đến G.
b. Từ 1 cấu hình của F, cho biết cấu hình của G.
2. Tetrađec-11-enyl axetat là chất dẫn dụ của sâu đục hạt ngô. Một đồng phân hình học của chất
này (K) được tổng hợp theo sơ đồ dưới đây:
a. Biểu diễn cấu tạo của các chất từ A đến K.
b. Để có sản phẩm là đồng phân hình học của K, cần điều chỉnh giai đoạn nào trong sơ đồ tổng hợp trên?
…………………………. Hết …..……………………… 3




