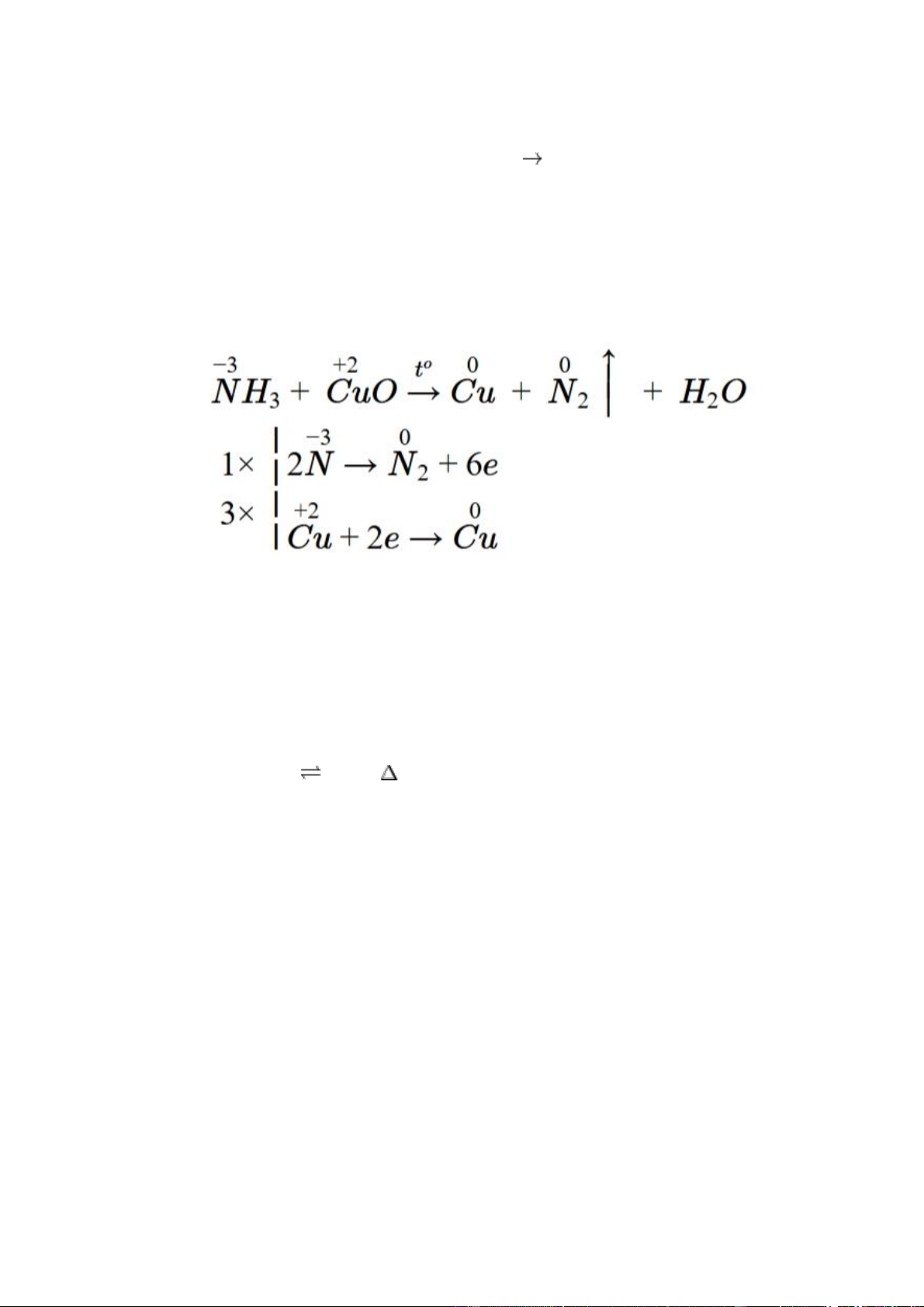







Preview text:
Cân bằng phương trình hoá học NH3 + CuO → Cu + N2 + H2O
1. Cân bằng phương trình hóa học NH3 + CuO Cu + N2 + H2O
2NH3 + 3CuO → 3Cu + N2↑ + 3H2O
- Điều kiện phương trình hóa học giữa NH3 và CuO Điều kiện: đun nóng.
- Cách cân bằng phản ứng:
Phản ứng hoá học được cân bằng:
2NH3 + 3CuO → 3Cu + N2↑ + 3H2O
2. Bài tập vận dụng
Câu 1: Cho cân bằng hóa học (trong bình kín) sau:
N2(khí) + 3H2 (khí) 2NH3; H = -92kJ/mol
Có bao nhiêu yếu tố làm cho cân bằng dịch chuyển theo chiều thuận ? A. 3 B. 4 C. 5 D. 2 Hướng dẫn giải: Đáp án đúng là: D Các yếu tố: 1, 4.
+ (1): Thêm lượng N2 hoặc H2 → cân bằng dịch chuyển theo chiều làm giảm N2/ H2(chiều thuận)
+ (2): Thêm NH3→ cân bằng dịch chuyển theo chiều làm giảm NH3 (chiều nghịch)
+ (3): 𝛥𝐻 = -92 < 0 → phản ứng thuận là tỏa nhiệt → tăng nhiệt độ làm cân bằng chuyển
dịch theo chiều thu nhiệt (chiều nghịch)
+ (4): Tăng áp suất của phản ứng → cân bằng dịch chuyển theo chiều giảm áp suất (chiều thuận)
+ (5): Chất xúc tác không làm ảnh hưởng đến cân bằng hóa học
Câu 2: Oxi hóa NH3 bằng CrO3 sinh ra N2, H2O và Cr2O3. Số phân tử NH3 tác dụng với một phần tử CrO3 là: A. 3 B. 1 C. 4 D. 2 Hướng dẫn giải:
Đáp án đúng là đáp án B
2NH3 + 2CrO3 N2 + 3 H2O + Cr2O3
Thì ta có: 1 phân tử NH3 phản ứng với 1 phân tử CrO3
Câu 3: Hỗn hợp X gồm N2 và H2 có tỉ khối so với hidro là 6,2. Dẫn X đi qua bình đựng
bột Fe rồi nung nóng biết rằng hiệu suất tổng hợp NH3 đạt 40% thì thu được hỗn hợp Y. Tỉ
khối của hỗn hợp khí Y hidro là: A. 14,76 B. 18,23 C. 7,38 D. 13,48 Hướng dẫn giải: Đáp án đúng là: C
Câu 4: Hợp chất nào sau đây nitơ có số oxi hóa là -3: A. NO B. N2O C. HNO3 D. NH4Cl2 Hướng dẫn giải:
Đáp án đúng là đáp án D
Câu 5: Hỗn hợp X gồm N2 và H2 có tỉ lệ mol là 1: 4. Nung hỗn hợp X ở điều kiện thích
hợp để phản ứng xảy ra, Biết hiệu suất phản ứng là 40%. PHần trăm theo thể tích của amoniac
Nh3 trong hỗn hợp thu được sau phản ứng là: A. 16,04% B. 17,04% C. 18,04% D. 19,04% Hướng dẫn giải:
Đáp án đúng là đáp án D
Câu 6: Chất nào sau đây có thể làm khô khí NH3 có lẫn hơi nước: A.Có ba P2O5 B. H2SO4 đặc C. CuO bột D. NaOH rắn
Câu 7: Có ba dung dịch mất nhãn: NaCl; Nh4Cl; NaNO3. Dãy hóa chất nào sau đây có thể
phân biệt được và dung dịch: A. Phenolphtalein và NaOH B. Cu và HCl
C. Phenolphtalein; Cu và H2SO4 loãng
D. Quỳ tím và dung dịch AgNO3 Hướng dẫn giải
Đáp án đúng là đáp án D
Câu 8: Cho 4 lít N2 và 14 lít H2 vào bình phản ứng ở điều kiện thích hợp, hỗn hợp thu
được sau phản ứng có thể tích bằng 16,4% (thể tích các khí được đo ở cùng điều kiện). Hiệu suất phản ứng là: A. 30% B. 20% C. 17,14% D. 34,28 % Hướng dẫn giải
Đáp án đúng là đáp án B
Câu 9: Muối Nh4HCO3 thuộc loại: A. muối hỗn tạp B. muối trung hòa C. muối axit D. muối kép Hướng dẫn giải:
Đáp án đúng là đáp án C
Câu 10: Chất nào sau đây là khô khí NH3 tốt nhất: A. HCl B. H2SO4 C. CaO D. HNO3 Hướng dẫn giải:
Đáp án đúng là đáp án C
Nguyên tắc chung cần ghi nhớ:
- Chất làm khô là chất có khả năng hút ẩm mạnh
- Chất làm khô không tác dụng không hòa tan với khí (cả khi có nước)
- Trong quá trình làm khô khí thì không giải phóng khí khác.
Câu 11: Có các dung dịch riêng biệt không nhãn dán: NH4NO3, Al(NO3)3, (NH4)2SO4.
Để phân biệt các dung dịch trên người ta dùng dung dịch: A. NaOH B. BaCl2 C. NaHSO4 D. Ba(OH)2 Hướng dẫn giải
Đáp án đúng là đáp án D
Cho lần lượt tới dư các thuốc thử vào các mẫu thử: A.
- NH4NO3 và (NH4)2SO4: sủi bọt khí không màu, mùi khai.
- Al(NO3)3: kết tủa keo trắng rồi tan thì chỉ nhận được Al(NO3)3. Suy ra loại B.
- NH4NO3 và Al(NO3)3: không hiện tượng
(NH4)2SO4: kết tủa trắng chỉ nhận được (NH4)2SO4. Suy ra loại
C. Không mẫu thử nào có hiện tượng. Suy ra loại D.
- NH4No3: sủi bọt khí không màu, mùi khai
- Al(NO3)3: Kết tủa keo trắng rồi tan
- (NH4)2SO4: kết tủa trắng không tan.
Suy ra nhận được cả 3 dung dịch
Câu 12: Nhận xét nào dưới đây không đúng về muối amoni?
A. Muối amoni kém bền với nhiệt
B. Tất cả muối amoni tan trong nước
C. Các muối amoni đều là chất điện li mạnh
D. Dụng dịch của các muối amoni luôn có môi trường bazo Hướng dẫn giải: Đáp án đúng là D
Câu 13: Trộn 300 ml dung dịch NaNo2 2M với 200ml dung dịch NH4Cl 2M rồi đun nóng
cho đến khi phản ứng xảy ra hoàn toàn. Thể tích khí thu được ở điều kiện tiêu chuẩn là: A. 22,4 lít B. 13,44 lít C. 8,96 lít D. 1,12 lít Hướng dẫn giải
Đáp án đúng là đáp án C
Câu 14: Hợp chất X tan trong nước tạo dung dịch không màu. Dung dịch này không tạo
kết tủa với dung dịch BaCl2, khi phản ứng với NaOH tạo ra khí có mùi khai, khi phản ứng với
dung dịch HCl tạo ra khí đục nước vôi trong và làm mất màu dung dịch thuốc tím. Chất này là: A.NH4HSO3 B. Na2SO3 C. NH4HCO3 D. (NH4)2CO3 Hướng dẫn giải: Đáp án đúng là: A
Câu 15: Để tách riêng NH3 ra khỏi hỗn hợp gồm N2, H2, NH3 trong công nghiệp người ta đã:
A. cho hỗn hợp qua nước vôi trong dư.
B. cho hỗn hợp qua bột CuO nung nóng
C. nén và làm lạnh hỗn hợp để hóa lỏng NH3
D. cho hỗn hợp qua dung dịch H2SO4 đặc. Hướng dẫn giải: Đáp án đúng là C
Trong công nghiệp, để tách riêng NH3 ra khỏi hỗn hợp gồm N2, H2, Nh3 người đem nén
và làm lạnh hỗn hợp khí thì chỉ có NH3 hóa lỏng và tách ra.
Câu 16: Tính bazơ của NH3 do:
A. trên N còn cặp electron tự do
B. phân tử có 3 liên kết cộng hóa trị phân cực
C. NH3 tan được nhiều trong nước
D. NH3 tác dụng với nước tạo NH4OH Hướng dẫn giải: Đáp án đúng là A
Câu 17: Hỗn hợp X gồm NH4Cl và (NH4)2SO4. Cho X tác dụng với dung dịch Ba(OH)2
dư, đun nhẹ thu được 9,32 gam kết tủa và 2,24 lít khí thoát ra. Hỗn hợp X có khối lượng là: A. 5,28 gam B. 6,60 gam C. 5,35 gam D. 6,35 gam Hướng dẫn giải: Đáp án đúng là D
Câu 18: Cho 2,3 gam Na vào 200 ml dung dịch (NH4)2SO4 1M. Đun nóng thu được V
khí (điều kiện tiêu chuẩn). Giá trị của V là: A. 1,12 B. 2,24 C. 3,36 D. 10,08 Hướng dẫn giải: Đáp án đúng là C
Câu 19: Nhận xét nào dưới đây không đúng về muối amoni?
A. Muối amoni kém bền với nhiệt
B. Tất cả muối amoni tan trong nược
C. Các muối amoni đều là chất điện li mạnh
D. Dung dịch của các muốsi amoni luôn có môi trường bazơ Hướng dẫn giải
Đáp án đúng là đáp án D
3. Củng cố lý thuyết
- Hiện tượng phản ứng giữa CuO và NH3
Khi dẫn khí NH3 đi qua ống đựng bột CuO đun nóng thì chất rắn chuyển từ màu đen của CuO sang màu đỏ của Cu.
- Tính chất hóa học của NH3
+ Amoniac có tính bazơ yếu
Amoniac do tính bazơ nên dung dịch amoniac làm cho quỳ tím hóa xanh còn dung dịch
phenolphtalein từ màu chuyển thành hồng.
+ Amoniac phản ứng với nước
NH3 + H2O to⇄NH4+ + OH-
+ Amoniac phản ứng với axit → Muối amoni
Thí dụ: NH3 (khí) + HCl (khí) → NH4Cl (khói trắng)
+ Amoniac tác dụng với dung dịch muối của các kim loại mà hidroxit không tan → bazơ và muối
2NH3 + MgCl2 + 2H2O → Mg(OH)2↓ + 2NH4Cl
* Chú ý: Với muối của Cu2+, Ag+ và Zn2+ có kết tủa sau đó kết tủa tan do tạo phức chất
tan: [Cu(NH3)4](OH)2; [Ag(NH3)2]OH; [Zn(NH3)4](OH)2.
Thí dụ: ZnSO4 + 2NH3+ 2H2O → Zn(OH)2↓ + (NH4)2SO4
- Amoniac có tính khử mạnh
+ Amoniac tác dụng với O2 4NH3 + 5O2 → 4NO↑ + 6H2O
+ Amoniac tác dụng với Cl2 2NH3 + 3Cl2 → N2↑ + 6HCl
+ Amoniac tác dụng với oxit của kim loại
3CuO + 2NH3 → Cu + 3H2O + N2↑




