








Preview text:
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ Mã HP: CH3323
PHẦN I: Các phương pháp phân tích quang phổ Khối lượng: 2 (2-1-0-4)
Chương 1. Đại cương về các phương pháp quang phổ Lý thuyết: 30 tiết
Chương 2. PP phổ hấp thụ phân tử Bài tập: 15 tiết
Chương 3. PP phổ phát xạ nguyên tử
Chương 4. PP phổ hấp thụ nguyên tử
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/1
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/2 1 2
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ
Tài liệu học tập & tham khảo
PHẦN II: Các phương pháp phân tích điện hóa • Tiếng Việt:
CHƯƠNG 5: Phương pháp điện phân 1. Bài giảng
CHƯƠNG 6: PP phân tích điện thế
2. Từ Văn Mặc, Các phương pháp phân tích dung
CHƯƠNG 7: Phương pháp Von- Ampe
công cụ, NXB ĐHQG Hà Nội, 2004.
PHẦN III: Các phương pháp tách chất
3. Từ Văn Mặc, Phân tích hóa lý - phương pháp
CHƯƠNG 8: Phương pháp chiết
phổ nghiệm nghiên cứu cấu trúc phân tử, NXB
Khoa học và Kỹ thuật, 2003.
Chương 9. Phương pháp sắc ký
3. Trần Tứ Hiếu, Phân tích trắc quang-Phổ hấp
Chương 10. Phương pháp sắc lỏng hiệu năng cao
thụ UV-Vis, NXB ĐHQG Hà Nội, 2008.
Chương 11. Phương pháp sắc ký khí
4. Hồ Viết Quý (2012), Cơ sở hóa học phân tích
hiện đại – Tập 4, NXB ĐH Sư phạm
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/3
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/4 3 4
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ
PHẦN I: Các PP phân tích quang phổ
Tài liệu học tập & tham khảo
Chương 1. Đại cương về các phương pháp quang phổ
5. Hồ Viết Quý (2012), Cơ sở hóa học phân tích hiện
đại – Tập 4, NXB ĐH Sư phạm
Quang phổ: ánh sáng được phân giải thành các bước
6. Phạm Hùng Việt (2003), Cơ sở lý thuyết của
sóng thành phần của nó để tạo ra phổ quang học.
phương pháp sắc ký khí, NXB Khoa học và Kỹ thuật.
Phương pháp quang phổ (spectroscopy): nhóm các • Tiếng Anh:
phương pháp nghiên cứu tương tác giữa vật chất và
1. Douglas A. Skoog, Donald M. West, F. James bức xạ điện từ.
Holler, Stanley R. Crouch (2004), Fundamentals of
Analytical Chemistry, 8th edition, Thomson, USA.
2. Daniel C. Harris (2006), Quantitative analytical
chemistry, 7th edition. W. H. Freeman, New York
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/5
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/6 5 6
1.1. Giới thiệu chung về phương pháp phổ ứng
1.2. Tính chất chung của bức xạ điện từ dụng trong phân tích. Định nghĩa:
Ánh sáng vừa có tính sóng vừa có tính hạt.
PP phân tích quang phổ là tên gọi chung cho một
Tương ứng với lưỡng tính sóng – hạt có 2 thuyết:
nhóm các phương pháp phân tích công cụ dựa trên
thuyết sóng điện từ của Maxwell và thuyết lượng tử
những tính chất quang học của nguyên tử, ion, phân
(hay thuyết hạt) của Planck-Einstein.
tử và nhóm phân tử bị kích thích.
Lý thuyết về quang phổ được xây dựng trên cơ sở của
PP phân tích quang phổ là phương pháp PTCC được cả 2 thuyết nói trên.
sử dụng rộng rãi để nghiên cứu cấu trúc phân tử, định tính và định lượng.
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/7
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/8 7 8
1.2. Tính chất chung của bức xạ điện từ
1.2. Tính chất chung của bức xạ điện từ
1.2.1. Thuyết sóng về ánh sáng
1.2.1. Thuyết sóng về ánh sáng
• Theo thuyết sóng của Maxwell (1865) thì ánh sáng
hay bức xạ nói chung có bản chất là sóng điện từ,
phát sinh từ nguồn sáng, xuất hiện do chuyển động
tuần hoàn của các điện tích.
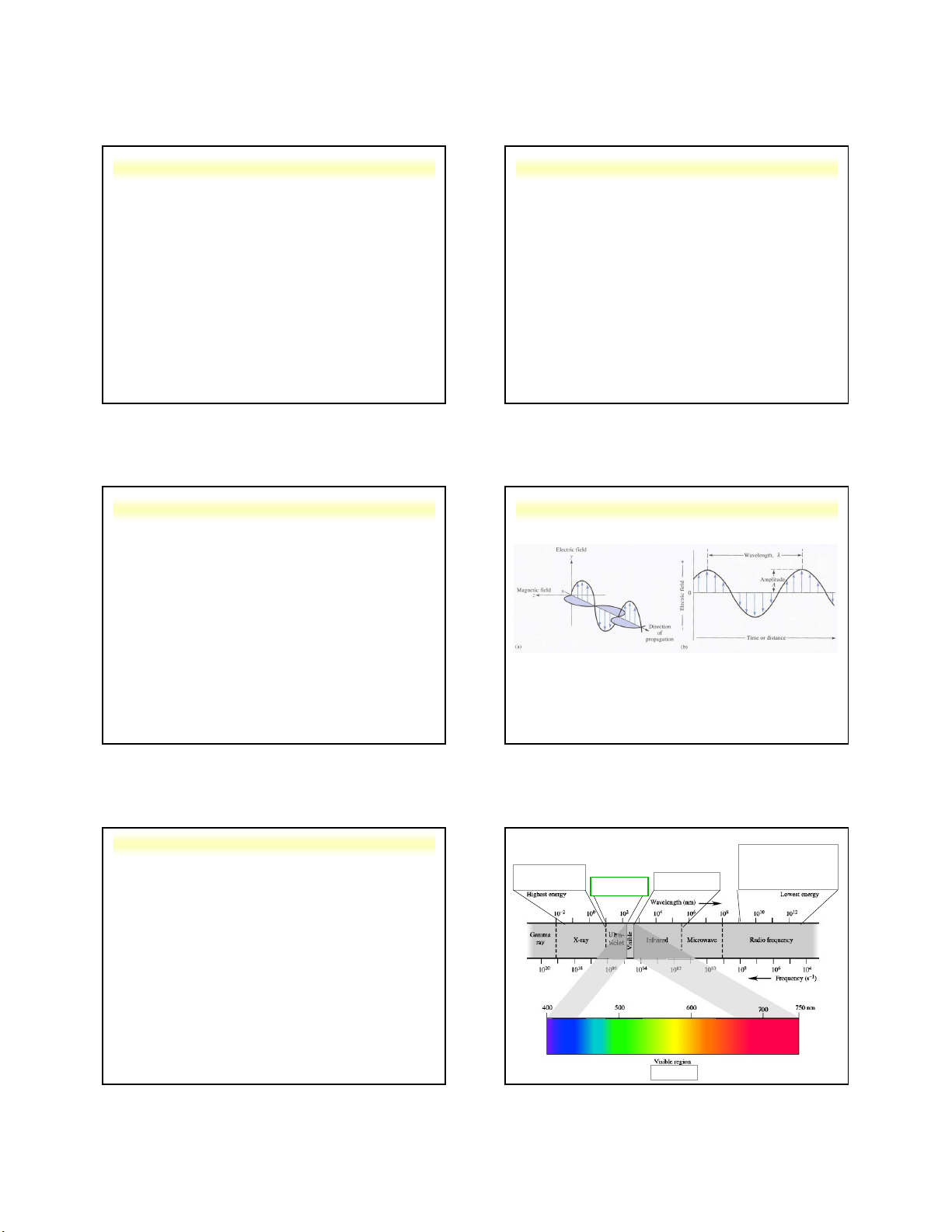
• Trong sóng điện từ, điện trường E và từ trường H
luôn luôn có phương vuông góc với nhau và vuông góc với phương truyền.
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/9
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/10 9 10
1.2. Tính chất chung của bức xạ điện từ
Miền sóng (hay quang phổ) của bức xạ điện từ Sóng Radio: NMR,
1.2.1. Thuyết sóng về ánh sáng Tia X (phổ ESR (trong từ
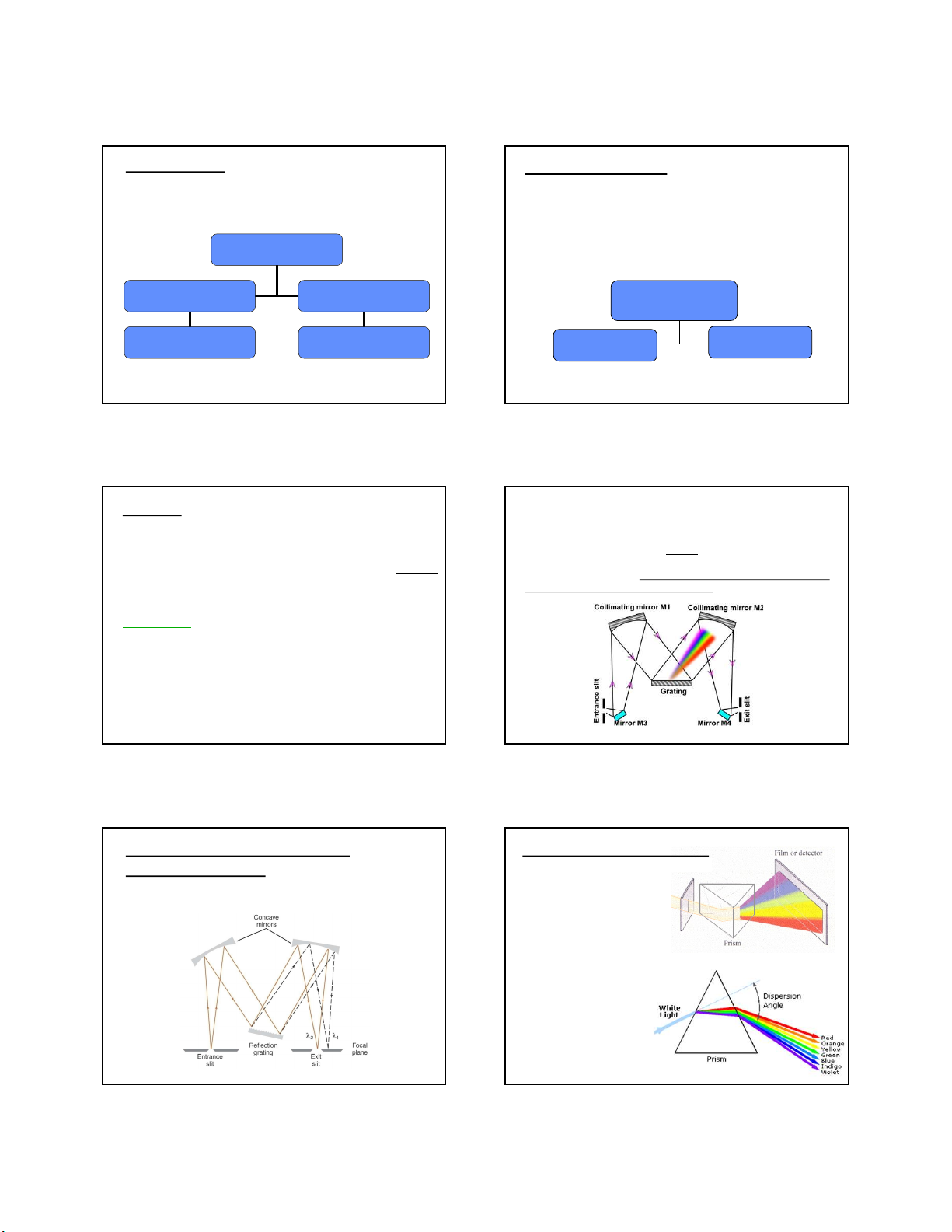
• Quãng đường mà sóng điện từ lan truyền được Rơnghen) Tử ngoại Hồng ngoại trường)
trong một chu kỳ T (chu kỳ dao động của điện
trường hay từ trường) được gọi là độ dài sóng . λ = cT (nm)
c là vận tốc truyền sóng (c = 3108 m/s trong chân không)
• Tần số ν cho biết số chu kỳ hay số dao động trong một đơn vị thời gian. ν = 1/T = c / λ (Hz)
• Bức xạ điện từ còn được đặc trưng bởi số sóng, với: ῡ = 1 / λ (cm-1) Khả kiến
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/11
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/12 11 12
1.2. Tính chất chung của bức xạ điện từ
1.3. Sự tương tác giữa bức xạ điện từ và vật chất
1.2.2. Thuyết lượng tử về ánh sáng
• Khi các bức xạ điện từ tương tác với các phân tử
• Theo thuyết lượng tử Planck (1900), ánh sáng hay
vật chất, có thể xảy ra theo hai khả năng: trạng thái
bức xạ nói chung gồm những lượng tử năng lượng
năng lượng của phân tử thay đổi hoặc không thay đổi.
được gọi là photon, phát đi từ nguồn sáng.
Khi có sự thay đổi năng lượng thì phân tử có thể hấp
thụ hoặc bức xạ (thứ cấp) năng lượng. = hν (J)
• Nếu gọi trạng thái năng lượng ban đầu của phân tử
h: hằng số Planck (h = 6,63×10-34 Js)
là E1, sau khi tương tác là E2,
• Theo hệ thức Einstein: E = mc2, photon có một khối E = E
lượng m (tính hạt của ánh sáng) tính theo hệ thức: 2 – E1
+ E = 0: năng lượng không thay đổi khi tương tác với m = h/c bxđt
+ E > 0: hấp thụ năng lượng
+ E < 0: phát xạ năng lượng
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/13
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/14 13 14
1.3. Sự tương tác giữa bức xạ điện từ và vật chất
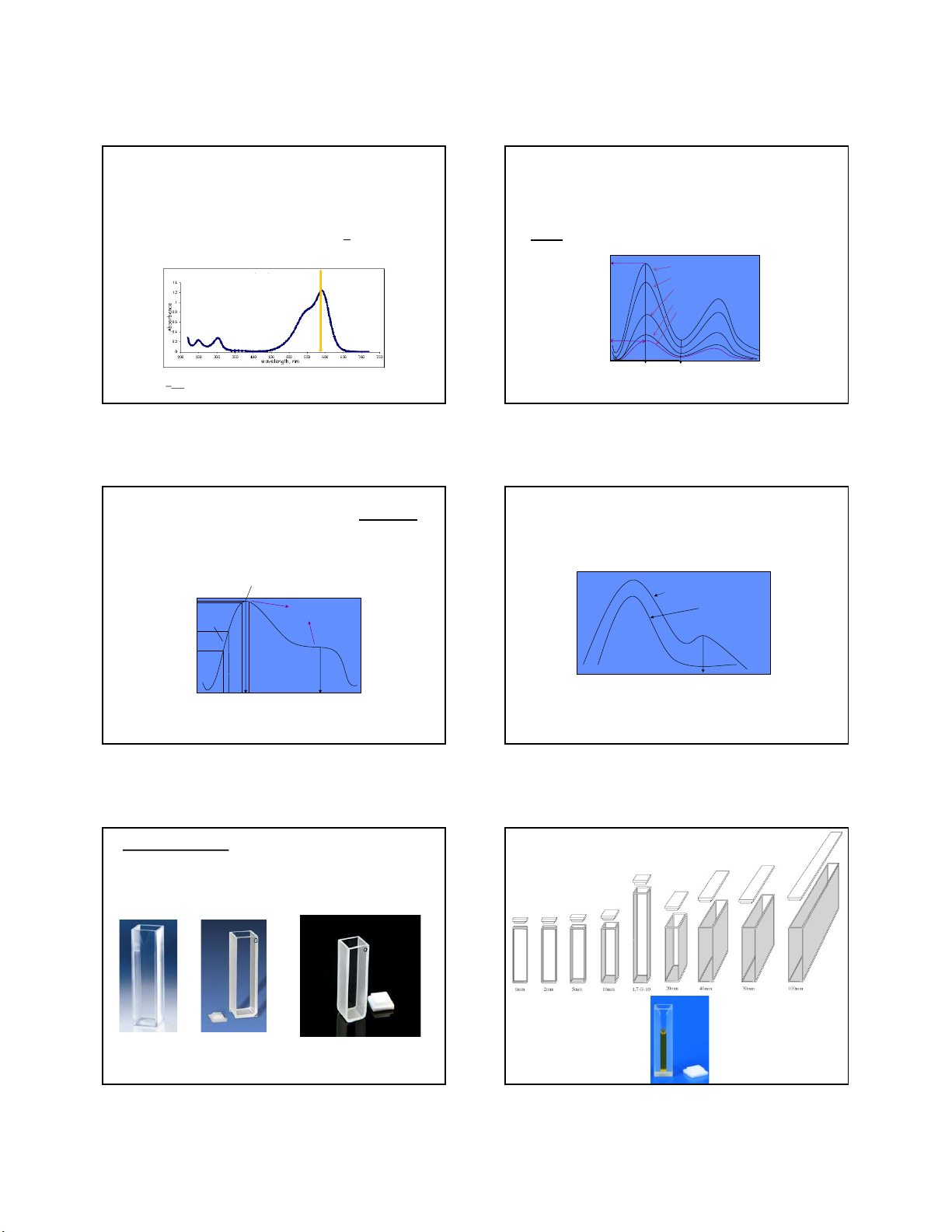
Miền phổ theo độ dài sóng: Bức xạ điện từ Dải bước sóng
Kiểu dịch chuyển lượng tử
• Vùng tử ngoại: 10 - 380 nm
Vùng tử ngoại gần (Near-UV hay Quartz-UV) trong Tia gama 0,005 – 1,4 Ȧ Hạt nhân
các phép phân tích từ 200 đến 380 nm Tia X 0,1 – 100 Ȧ Electron lớp trong
• Vùng khả kiến (VIS): 380 - 780nm. Tử ngoại chân không 10 – 180 nm Electron hóa trị
• Vùng hồng ngoại (IR): 0.78μm - 300 μm. (xa)
- Vùng hồng ngoại gần (Near-InfraRed, NIR): 0.80μm Tử ngoại, khả kiến 180 – 780 nm Electron hóa trị - 2.5 μm. Hồng ngoại 0,78 – 16 m
Dao động, quay của phân tử
- Vùng hồng ngoại xa (Far-InfraRed, FIR) từ 2.5μm Vi sóng 0,75 – 3,75 mm Quay của phân tử đến 16 μm. Radio, vô tuyến 1 cm – 10 m
Spin của electron, hạt nhân trong từ trường
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/15
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/16 15 16
Tương tác của bức xạ điện từ với phân tử
Tương tác của bức xạ và sự xuất hiện phổ
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/17
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/18 17 18
2.1. Sự tạo thành phổ hấp thụ phân tử (phổ UV-
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ Vis)
• Các phân tử ở điều kiện bình thường tồn tại ở trạng
PHẦN I: Các PP phân tích quang phổ
thái cơ bản bền vững có năng lượng thấp. Khi chúng
Chương 2: Phương pháp phổ hấp thụ phân tử UV-Vis
được cung cấp năng lượng, ví dụ như khi chiếu
chùm bức xạ vùng tử ngoại – khả kiến (UV-Vis), thì
các điện tử hóa trị (liên kết) trong phân tử sẽ hấp
thụ năng lượng của nguồn bức xạ và chuyển lên
trạng thái kích thích có năng lượng cao hơn.
• Sự chuyển dời electron giữa 2 trạng thái (2 obitan)
được gọi là sự dịch chuyển điện tử.
• Cùng với sự dịch chuyển điện tử thì phân tử có sự
dịch chuyển cảm ứng bức xạ là sự dao động và quay.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/19
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/20 19 20
2.1. Sự tạo thành phổ hấp thụ phân tử (phổ UV-
2.1. Sự tạo thành phổ hấp thụ phân tử (phổ UV- Vis) Vis)
• Năng lượng tổng cộng E của 1 phân tử được viết như sau:
• Phổ hấp thụ phân tử UV-Vis là phổ xuất hiện do sự E = Eđt + Edđ + Eq
tương tác của các điện tử hóa trị trong phân tử hay
Eđt: là năng lượng của các e trong các obitan ở lớp vỏ của phân
nhóm phân tử với bức xạ điện từ vùng UV-Vis. tử;
• Thực chất, phổ UV-Vis gồm những dải hấp thụ được
Edđ: là năng lượng các dao động giữa các nguyên tử trong toàn
tạo ra do rất nhiều vạch có khoảng cách rất gần bộ phân tử; nhau (phổ đám).
Eq: là năng lượng ứng với sự quay của phân tử quanh trọng tâm của chúng
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/21
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/22 21 22
2.1. Sự tạo thành phổ hấp thụ phân tử (phổ UV- Vis)
2.2. Định luật cơ bản về sự hấp thụ bức xạ điện từ
2.2.1. Định luật Bouguer-Lambert-Beer Pierre Bouguer Johan Lambert August Beer (1698-1758) (1728-1777) (1825-1863) Investigated Extended the Applied Lambert’s absroption vs. concepts developed concepts to solutions of thickness of by Bouguer different concentrations medium
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/23
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/24 23 24 Định luật Beer
• Khi chiếu một chùm tia sáng đơn sắc đi qua một môi
trường vật chất thì cường độ của tia sáng ban đầu I0 sẽ
bị giảm đi chỉ còn là I do các hiện tượng hấp thụ (phần
chính), phản xạ và tán xạ.
• Nếu môi trường vật chất là dung dịch chất mẫu nồng
độ C đựng trong cuvet có bề dày b, thì độ hấp thụ A
của các phân tử trong dung dịch chất mẫu,
• Chia lớp dung dịch thành những lớp vô cùng mỏng A = log (I0/I) = bC
thiết diện S có bề dày là dx.
là hệ số hấp thụ mol (hệ số hấp thụ phân tử gam).
• Px: năng lượng của bxđt tới thiết diện S trong 1 đơn vị thời gian.
• Ánh sáng khi đi qua lớp dx giảm cường độ mất dPx.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/25
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/26 25 26 Định luật Beer Định luật Beer
• Dựa trên sự hấp thụ năng lượng của bxđt bởi chất
• Thiết diện S có thể được biểu diễn qua đại lượng thể - dPx/Px = dS/S tích và bề dày Trong đó:
dS/S là tỉ lệ của diện tích hấp thụ trên thiết diện S, tỉ lệ với số S=V/b (cm2)
hạt (đơn vị) hấp thụ có trong dS n/V = C
dS=adn với a là hằng số, dn số hạt (đơn vị) hấp thụ trong dS a/2,303
n là tổng số hạt (đơn vị) hấp thụ trong mẫu P anb P dP n adn o log b . C . x P 2.30 V 3 P S P x o 0 P an o ln P S P an o log P . 2 30 S
3 Nguyễn X. Trường – ANACHEM-SCE-HUST-2/27
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/28 27 28
2.2.2. Tính chất của độ hấp thụ quang
2.2.2. Tính chất của độ hấp thụ quang
• Độ hấp thụ quang có tính chất cộng tính hay định
• Ý nghĩa vật lý của :
luật Beer-Lambert có thể áp dụng cho hỗn hợp chất
là độ hấp thụ quang của dung dịch có nồng độ 1 M
(nếu không có sự tương tác giữa các chất)
đựng trong cuvet có bề dày 1 cm.
Atot=SAx = 1.b.C1 + 2.b.C2 + … n.b.Cn
đặc trưng cho bản chất của chất nghiên cứu (phụ
Hệ quả: Amẫu = Achất nc + Aso sánh
thuộc vào bản chất của chất nghiên cứu) và phụ hay A
thuộc vào bước sóng của ánh sáng tới. chất nc = Amẫu - Aso sánh Trong đó, A
• Thứ nguyên của là: l.mol-1cm-1 hay cm2.mmol-1
so sánh là độ hấp thụ quang của dung
dịch trống (mẫu trắng – blank). Dung dịch so sánh
• Hệ số hấp thụ phân tử k = /6,0231020 (cm2)
được chuẩn bị sao cho có thành phần như dung
dịch mẫu đo nhưng không chứa nghiên cứu.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/29
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/30 29 30
Một số đại lượng dùng trong phổ UV-Vis:
2.2.3. Đại lượng đặc trưng cho sự hấp thụ ánh sáng
• Độ truyền quang - % T: % T = I/I 0 100 • Độ hấp thụ quang A A = log(I0/I) = - logT
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/31
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/32 31 32
2.3. Giới hạn của định luật Beer
Cân bằng hóa học dịch chuyển
2.3.1. Các nguyên nhân làm cho sự hấp thụ ánh sáng • Ảnh hưởng của H+
không tuân theo định luật Beer
• Ảnh hưởng của ion lạ
• Cân bằng hóa học dịch chuyển
• Sự phân ly của phức khi pha loãng
• Ánh sáng không đơn sắc
• Bxđt xuất hiện ngẫu nhiên (tản mạn) do hệ thiết bị (stray light)
• Cuvet không đồng nhất
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/33
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/34 33 34 Ánh sáng không đơn sắc
Bxđt xuất hiện ngẫu nhiên: Stray light
• Bxđt có nhiều hơn một bước sóng
• Bxđt xuất hiện ngẫu nhiên tạo nên bởi sự tán xạ và phản
xạ ánh sáng trên bề mặt của cách tử nhiễu xạ, thấu kính,
gương, kính lọc, cửa sổ cuvet... (đến detector nhưng không qua mẫu)
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/35
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/36 35 36 Cuvet không đồng nhất
2.3. Giới hạn của định luật Beer
2.3.2. Độ chính xác của phép đo
• Cuvet chứa mẫu trắng (blank) và mẫu thực tế
A = b.C = log(1/T) = 0,434 ln(1/T) không đồng nhất Lấy đạo hàm theo T dC/dT = -0,434/Tb Thay b = A/C ta có:
dC/C = -0,434/A (dT/T) = 0,434/logT (dT/T) (1)
Giá trị T mà tại đó sai số tương đối về nồng độ là nhỏ
nhất được xác định bằng cách lấy đạo hàm của (1) và cho bằng 0.
Tìm được T = 0,368 hay A = 0,434 và dC/C = - 2,72 dT
Nếu sai số của phép đo T là 0,1% thì sai số tương đối xác
định nồng độ sẽ là 0,27%.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/37
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/38 37 38
2.3. Giới hạn của định luật Beer
2.4. Máy quang phổ hấp thụ phân tử UV-Vis
2.3.2. Độ chính xác của phép đo Sơ đồ khối
Thông thường giá trị A nên nằm trong khoảng 0,2 – 0,8
ứng với T = 0,65 – 0, 16 (65% - 16%). (1) Nguồn sáng (2) Bộ chọn sóng (3) Cuvet chứa mẫu (4) Detectơ
(5) Khuyếch đại và ghi tín hiệu
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/39
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/40 39 40
2.4. Máy quang phổ hấp thụ phân tử UV-Vis
2.4. Máy quang phổ hấp thụ phân tử UV-Vis
Phổ hấp thụ phân tử UV-Vis
Các bộ phận chính của máy
Phổ UV-Vis là dạng đồ thị với: quang phổ trục tung: A, , log, T 1. Nguồn sáng
trục hoành: bước sóng , tần số , số sóng.
2. Bộ chọn bước sóng (kính lọc, bộ đơn sắc) 3. Cuvet chứa mẫu 4. Detector 5. Bộ đọc tín hiệu
Máy quang phổ 1 (single
beam) và 2 (double beam) chùm tia
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/41
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/42 41 42 2.4.1- Nguồn sáng
2.4.2. Bộ chọn bước sóng
Nguồn sáng của máy quang phổ UV-Vis là nguồn sáng liên tục.
Trường hợp lý tưởng bxđt ra khỏi bộ chọn bước sóng là đơn sắc
• Phát bức xạ điện từ với tất cả các bước sóng trong vùng phổ sử (1 bước sóng) dụng
• Nguồn bức xạ ổn định và có cường độ lớn
Không có bộ chọn bước sóng nào có thể làm việc lý tưởng, tức
là bxđt ra khỏi bộ chọn bước sóng là 1 chùm tia Nguồn sáng liên tục
Thiết bị càng tốt thì chùm tia thu được càng hẹp
Bxđt vùng khả kiến và hồng ngoại Bộ chọn bước Bxđt vùng UV gần sóng Đèn Tungsten Đèn Deuterium Kính lọc Bộ đơn sắc 320-2500 nm 200-400 nm
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/43
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/44 43 44 b- Bộ đơn sắc a- Kính lọc
Bộ đơn sắc được sử dụng nếu muốn quét phổ (có thể dễ dàng thay đổi
bước sóng của bxđt cho khoảng mong muốn).
• Kính lọc cho qua những chùm tia nhất định (độ rộng bước sóng cỡ ~ 50 nm).
Có thể được sử dụng cho vùng UV/Vis.
• Loại kính lọc đơn giản nhất là kính lọc hấp thụ (colored
Bộ đơn sắc gồm khe đo (slits), gương (mirror), thấu kính (lense), cách glass filters).
tử nhiễu xạ (grating) hoặc lăng kính (prism).
• Kính lọc thường được sử dụng cho vùng khả kiến. Nhược điểm
• Kính lọc không phải là bộ phận chọn bước sóng tốt.
Vì kính lọc cho qua chùm tia có độ rộng bước sóng
khá lớn có thể gây sai lệch định luật Beer.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/45
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/46 45 46
b1-Bộ đơn sắc sử dụng cách tử nhiễu xạ
b2- Bộ đơn sắc sử dụng lăng kính
Cách tử nhiễu xạ phản xạ
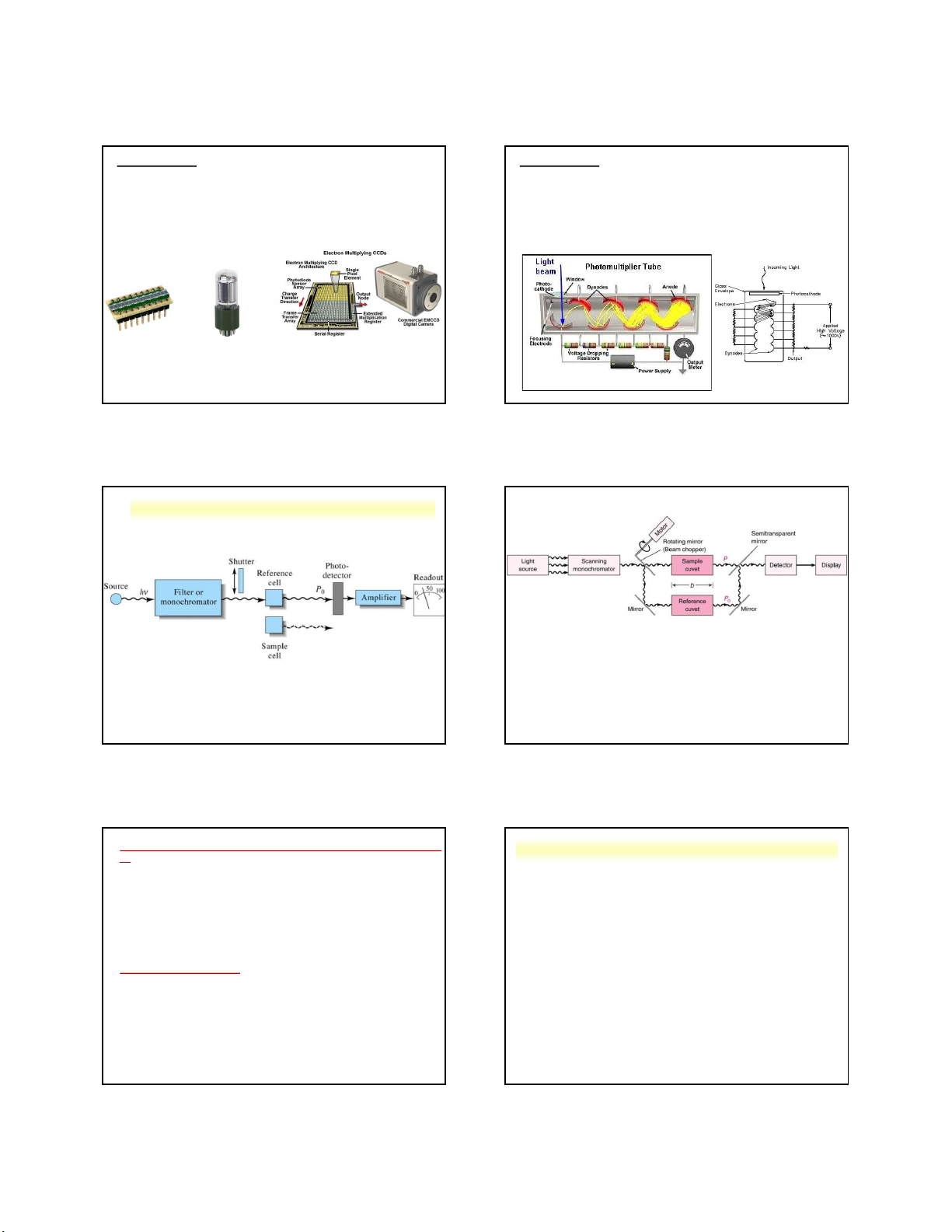
Độ tán sắc bởi lăng kính
Quay cách tử nhiễu xạ phản xạ cho phép chỉ 1 bước sóng (2)
phụ thuộc vào độ khúc xạ ánh qua bộ đơn sắc sáng
Tia tím với năng lương cao
hơn (bước sóng ngắn hơn) bị
nhiễu xạ (bẻ cong) nhiều nhất
Bức xạ đỏ với năng lương
nhỏ hơn (bước sóng dài hơn)
bị nhiễu xạ (bẻ cong) ít nhất
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/47
Nguyễn X. Trường – ANACHEM-SCE-HUST-2 4 / 8 48 47 48
Lựa chọn bước sóng phân tích
Đo độ hấp thụ quang tại bước sóng Phép đo đ
max thì có thể đo được
ộ hấp thụ thường được thực hiện tại 1 bước
nồng độ chất phân tích nhỏ nhất với độ chính xác tốt.
sóng cố định. Khi 1 bước sóng được chọn cho mục đích
phân tích định lượng, 3 yếu tố sau cần phải lưu ý:
Ví dụ so sánh nồng độ tối thiểu của chất phân tích tại max
1. Bước sóng lựa chọn cho độ nhạy cao nhất. max hoặc bước (10-5 M) và 1.
sóng tại đó hệ số hấp thụ tương đối lớn. 10-2 M 10-3 M λ e max c n 10-4 M a rb 5x10-5 M so 10-5 M b A max 1
λmax – bước sóng tại đó sự hấp thụ là lớn nhất wavelength
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/49
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/50 49 50
2. Tốt nhất nên chọn bước sóng mà tại đó độ hấp thụ không thay đổ
đáng kể khi bước sóng thay đổi nhỏ. Tức là tỉ số A / nhỏ.
3. Nếu dung dịch có chứa nhiều cấu tử hấp thụ, nếu có thể chọn
bước sóng tại đó cấu tử quan tâm hấp thụ lớn ngược lại cấu tử
Ví dụ: Tại băng (dải) A A / 0
gây nhiễu không hấp thụ hoặc ít hấp thụ.
Tại băng (dải) B A / lớn (độ đúng của phép đo giảm) Band A sample A Broad horizontal ce n Interfering bands a species e Band B rb c n so a A b shoulder A rb so b A m wavelength wavelength m
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/51
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/52 51 52 2.4.3- Bộ chứa mẫu
Mẫu lỏng thường được chứa trong cuvet. Cuvet
Cuvet nhựa, thủy tinh cho vùng khả kiến
Cuvet thạch anh cho vùng UV, Vis Semi micro cuvet Nhựa Thủy tinh Thạch anh
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/53
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/54 53 54 2.4.4- Detector 2.4.4- Detector
Là bộ phận chuyển đổi tín hiệu quang thành tín hiệu điện. Ống nhân quang
Detector phải nhạy, đáp ứng nhanh cho 1 khoảng bước sóng mong muốn.
Electron giải phóng ra từ catot nhạy sáng kéo theo (thúc đẩy) các
Tín hiệu điện tạo ra bởi detector phải tỉ lệ thuận với độ truyền quang.
electron khác từ các dynode.
Nếu quá trình này được lặp lại vài lần thì có hơn 106 electrons được
giải phóng khi 1 photon tác động lên catot đầu tiên. Diode quang Ống nhân quang CCD camera
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/55
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/56 55 56
Sơ đồ khối của máy quang phổ 2 chùm tia
Sơ đồ khối của máy quang phổ 1 chùm tia
Ánh sáng đi qua mẫu thực tế hoặc mẫu so sánh (mẫu trắng) nhờ vào bộ chia bxđt (beam chopper)
Khi ánh sáng qua mẫu detector đo P. Ngược lại khi ánh sáng qua mẫu trắng detector đo P0.
Bộ chia bxđt lặp lại vài lần/s mạch điện tử tự động so sánh P và P0 để tính
toán độ hấp thụ và độ truyền quang.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/57
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/58 57 58
Ưu điểm của máy quang phổ 2 chùm tia so với máy quang phổ 1 chùm
2.5. Phân tích bằng phương pháp phổ UV-Vis tia
Máy quang phổ 1 chùm tia không tiện ích vì:
2.5.1. Nguyên tắc của phép đo:
1. Mẫu trắng và mẫu phải được đo lần lượt.
• Hòa tan chất phân tích trong một dung môi phù
2. Nếu muốn đo tại nhiều bước sóng khác nhau, mẫu trắng phải được
hợp, hoặc cho chất nghiên cứu, thường là ion kim
đo ứng với mỗi bước sóng (với máy không có chức năng quét theo
loại, tác dụng với thuốc thử hữu cơ trong dung môi bước sóng).
thích hợp để tạo ra hợp chất (phức chất) có phổ UV- Vis nhạy. Máy quang phổ 2 chùm tia
• Chiếu vào dung dịch mẫu chứa chất nghiên cứu
1. Độ hấp thụ của mẫu được tự động so sánh với mẫu trắng.
(đựng trong cuvet) 1 chùm sáng có bước sóng phù
2. Tự động hiệu chỉnh sự thay đổi cường độ của nguồn sáng và sự
hợp để chất nghiên cứu hay sản phẩm của nó hấp
thay đổi đáp ứng của detector với thời gian hoặc bước sóng bởi vì 2
thụ bức xạ để tạo thành phổ UV-Vis.
chùm tia được so sánh và đo tại cùng 1 thời điểm.
• Thu, phân ly phổ đó và chọn bước sóng cần đo rồi
3. Tự động quét và ghi phổ (absorbance vs. wavelength).
ghi lại giá trị độ hấp thụ quang A.
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/59
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/60 59 60
2.5.2. Phương pháp định lượng
2.5.2. Phương pháp định lượng
a. Phương pháp một điểm chuẩn
a. Phương pháp một điểm chuẩn (single-point standardization)
b. Phương pháp đường chuẩn S
c. Phương pháp thêm chuẩn A = kA. CA kA = Sstd / Cstd Csamp = Ssamp / kA
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/61
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/62 61 62
a. Phương pháp một điểm chuẩn (single-point standardization)
a. Phương pháp một điểm chuẩn (single-point standardization) Nhược điểm: -
Sai số khi xác định kA dẫn đến sai số khi tính toán Csamp -
Giá trị thực nghiệm kA được xác định chỉ dựa trên
1 giá trị nồng độ chất phân tích -
Sử dụng kA để tính toán nồng độ chất phân tích
nghiễm nhiên đã giả thiết mối quan hệ tuyến tính
giữa tín hiệu đo và nồng độ chất phân tích. Điều này thường không đúng.
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/63
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/64 63 64
a. Phương pháp một điểm chuẩn (single-point standardization)
2.5.2. Phương pháp định lượng • Ưu điểm
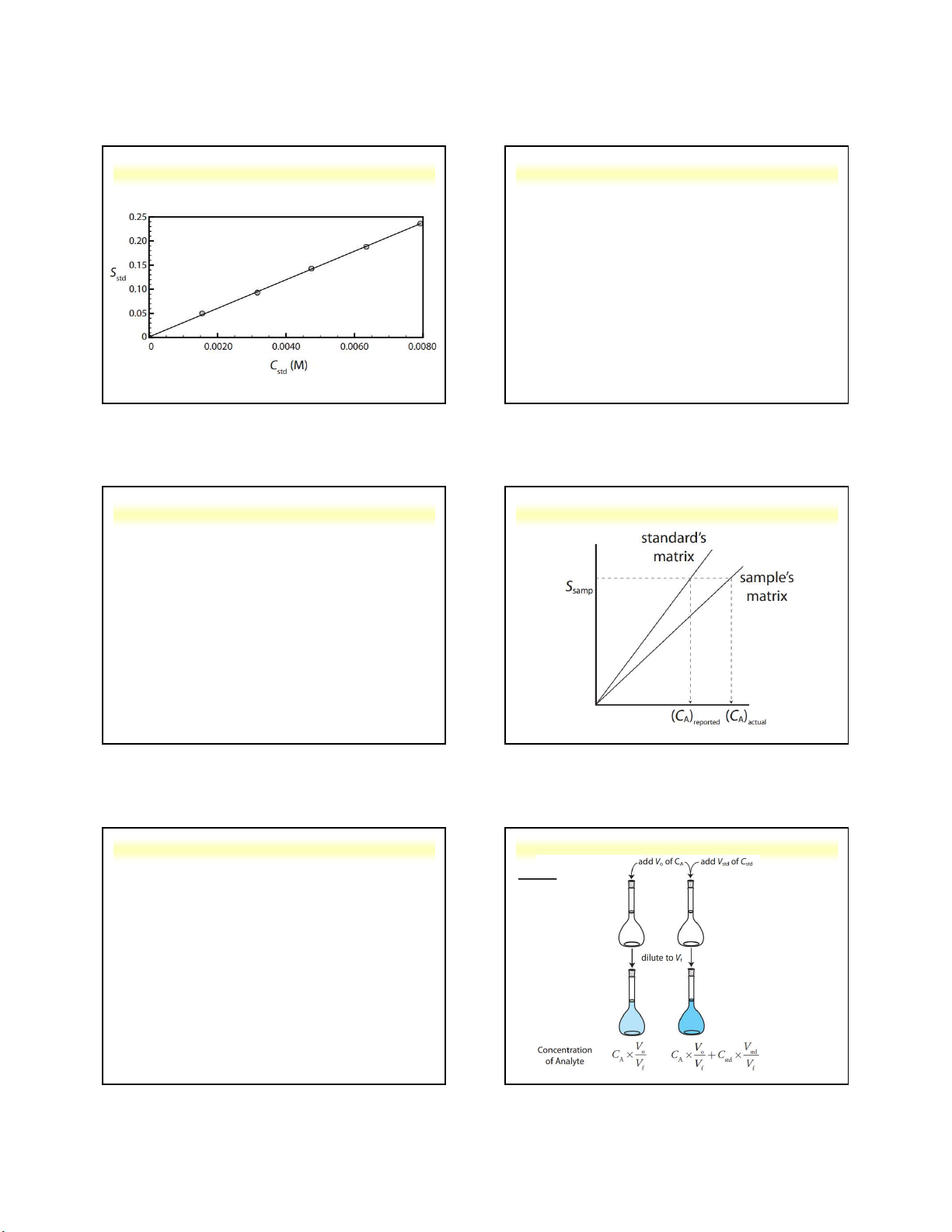
b. Phương pháp đường chuẩn (multiple-point
- Mặc dù có nhiều nhược điểm nhưng phương pháp standardization)
một điểm chuẩn vẫn được dùng khá phổ biến nếu
- Chuẩn bị một dãy mẫu chuẩn (đã biết nồng độ) của
nồng độ chất chuẩn và nồng độ chất phân tích
chất phân tích trong cùng điều kiện với mẫu phân không khác nhau nhiều
tích như chất nền, môi trường pH, ...
- Không tốn nhiều thời gian phân tích.
- Đo phổ UV-Vis của mẫu chuẩn và mẫu phân tích
- Xác định kA từ hệ số góc của đường chuẩn (Sstd – Cstand)
- Từ giá trị Sx (Ax) của mẫu phân tích suy ra nồng độ Cx của mẫu phân tích
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/65
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/66 65 66
b. Phương pháp đường chuẩn (multiple-point
b. Phương pháp đường chuẩn (multiple-point standardization) standardization) • Ưu điểm
- Giảm thiểu được sai số khi xác định Csamp
- kA là biến độc lập với nồng độ chất phân tích trong
khoảng nồng độ xây dựng đường chuẩn
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/67
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/68 67 68
b. Phương pháp đường chuẩn (multiple-point
b. Phương pháp đường chuẩn (multiple-point standardization) standardization) • Nhược điểm
- Chấp nhận giả thiết là nền mẫu không ảnh hưởng
đến việc xác định kA từ đường chuẩn. Nhưng, thực tế
nền mẫu thực và mẫu xây dựng đường chuẩn là khác nhau.
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/69
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/70 69 70
2.5.2. Phương pháp định lượng
c1. Thêm chuẩn một điểm (single standard addition) Ví dụ 1:
c. Phương pháp thêm chuẩn (standard additions)
Ưu điểm: Loại bỏ được sự ảnh hưởng của nền mẫu phân tích (spike)
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/71
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/72 71 72
c1. Thêm chuẩn một điểm (single standard addition)
c1. Thêm chuẩn một điểm (single standard addition) Ví dụ 2: (spike)
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/73
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/74 73 74
c1. Thêm chuẩn một điểm (single standard addition)
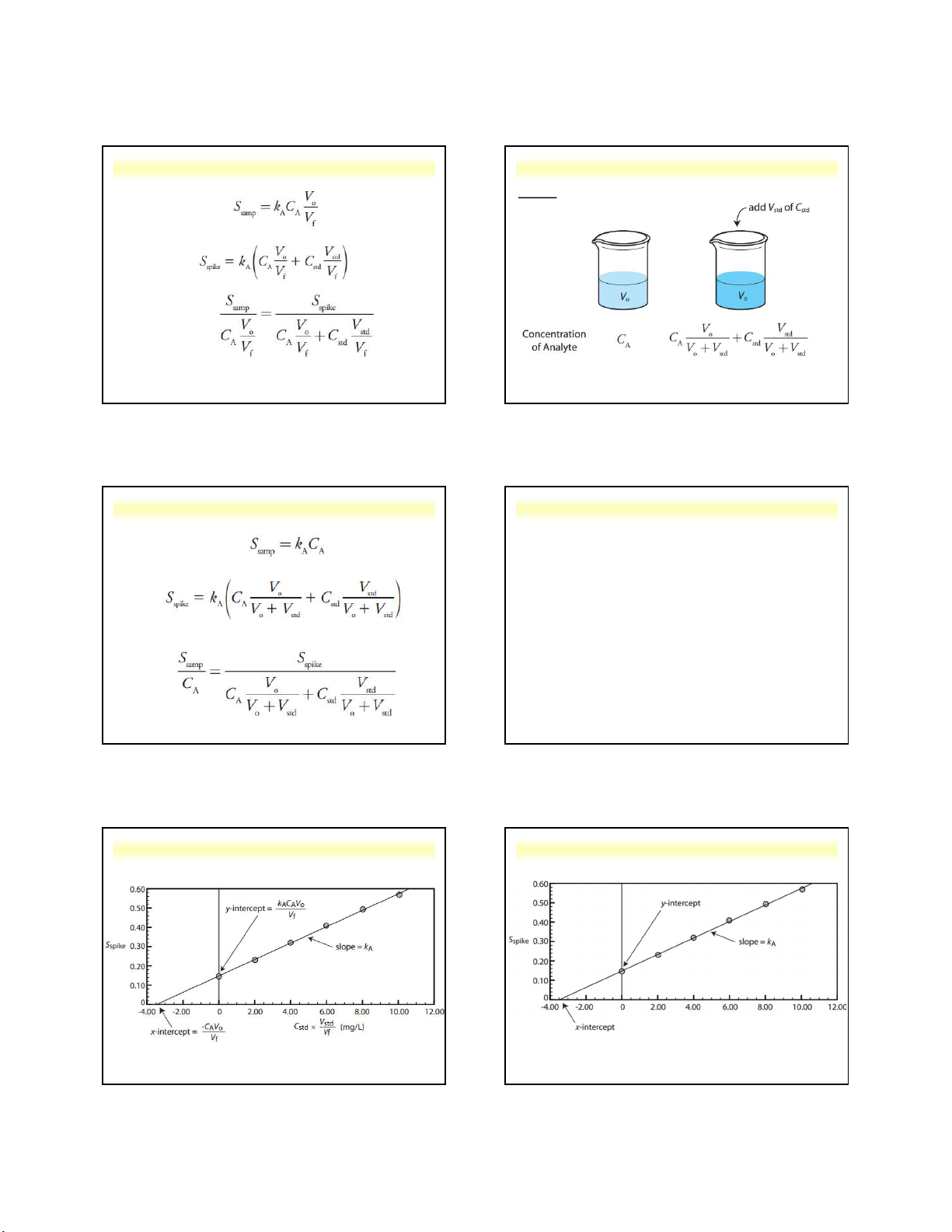
c2. Đường thêm chuẩn – thêm chuẩn nhiều điểm (multiple standard additions)
• Chuẩn bị một dãy mẫu phân tích nồng độ chưa biết CA với thể tích V0
• Thêm lần lượt vào dãy mẫu phân tích trên một thể
tích thay đổi Vstd của chất chuẩn phân tích có nồng độ Cstd
• Thêm nước (dung môi) đến vạch mức thể tích Vf
• Đo phổ UV-Vis của tất cả dãy mẫu trên
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/75
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/76 75 76
c2. Đường thêm chuẩn – thêm chuẩn nhiều điểm
c2. Đường thêm chuẩn – thêm chuẩn nhiều điểm (multiple standard additions) (multiple standard additions) Vstd
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/77
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/78 77 78
c2. Đường thêm chuẩn – thêm chuẩn nhiều điểm
2.6. Ứng dụng của pp phổ UV-Vis (multiple standard additions)
2.6.1. Phân tích định lượng
Phổ hấp thụ phân tử UV-Vis là một trong những công
cụ hữu hiệu để phân tích định lượng
Khả năng áp dụng rộng:
- Một số lớn các hợp chất hữu cơ, vô cơ (phức),
phân tử sinh học hấp thụ trong vùng UV-Vis nên có
thể phân tích định lượng trực tiếp.
- Nhiều hợp chất không hấp thụ vùng UV-Vis có thể
phân tích gián tiếp sau khi dẫn xuất hóa bằng phương pháp hóa học.
Nguyễn X. Trường – ANACHEM-SCE-HUST-1/79
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/80 79 80
2.6. Ứng dụng của pp phổ UV-Vis
Độ nhạy cao 10-6-10-4 M
2.6.2. Một số ứng dụng khác của phổ UV-Vis
Độ chọn lọc ở mức trung bình đến cao.
Xác định thành phần của phức Độ chính xác cao M + nX = MX n = [MXn]/[M][X]n
Sai số tương đối về nồng độ khoảng từ 1% đến 3%
a. Phương pháp dãy đồng phân tử gam
Dễ thao tác, thực hiện nhanh, xử lý số liệu dễ dàng
Gọi nồng độ ban đầu của M là CM, của X là CL; nồng cân và thuận tiện bằng của phức là Cp. Cp ( 1) (C C ).(C nC )n M p L p
Giá trị cực đại Cp được xác định bằng cách lấy đạo hàm
Cp theo CM và CL và cho bằng 0. Cp max khi CL = nCM
Hay độ hấp thụ của phức Amax khi nX/(nX+nM) = n/n+1
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/81
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/82 81 82
2.6. Ứng dụng của pp phổ UV-Vis
a. Phương pháp dãy đồng phân tử gam
2.6.2. Một số ứng dụng khác của phổ UV-Vis
Xác định thành phần của phức M + nX = MX n = [MXn]/[M][X]n
a. Phương pháp dãy đồng phân tử gam Tiến hành:
- Pha các dung dịch ion M và X có nồng độ mol/l như nhau.
- Chuẩn bị dãy đồng phân tử gam bằng cách trộn các
dung dịch theo thể tích khác nhau, nhưng tổng thể tích không đổi.
- Đo A ở 1 giá trị đã chọn.
- Xây dựng đồ thị A – phần mol X, tại vị trí trên trục
hoành của cực đại thì nX/(nX+nM) = n/n+1 n
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/83
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/84 83 84
2.6. Ứng dụng của pp phổ UV-Vis
b. Phương pháp đường cong bão hòa
2.6.2. Một số ứng dụng khác của phổ UV-Vis
Xác định thành phần của phức
M + nX = MXn = [MXn]/[M][X]n
b. Phương pháp đường cong bão hòa Tiến hành:
- Chuẩn bị dãy dung dịch có nồng độ của thuốc thử
thay đổi còn tất cả các cấu tử khác đều như nhau.
- Đo A ở 1 giá trị đã chọn.
- Xây dựng đồ thị A – CL/CM, tại vị trí trên trục
hoành của điểm gãy thì n = CL/CM
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/85
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/86 85 86
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ
PHẦN I: Các PP phân tích quang phổ
Chương 3: Phương pháp phổ phát xạ nguyên tử
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/87 87




