




Preview text:
lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB NỘI DUNG [1] – Tập 3, Chương NHẬN XÉT 9: trang 226 – 252 CHUNG [2] – Chương 16: trang 282 – 291 I. ĐƠN CHẤT [3] – Phần III, 1. Tính chất vật lý 2. Chương 1: trang Tính chất hóa học 374 – 394 II. HỢP CHẤT 1. Các hợp chất +1 2. Các hợp chất +2 3.
Các hợp chất +3 TÀI LIỆU lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB NHẬN XÉT CHUNG
- Cấu hình electron của 2 lớp ngoài cùng:
(n-1)s2 (n-1)p6 (n-1)d10 ns1
Gây ra hiệu ứng chắn kém Kém bền hơn cấu hình hơn cấu hình (n 2(n-1)p6 (n-1)s2 (n-1)p6 tạo các -1)s
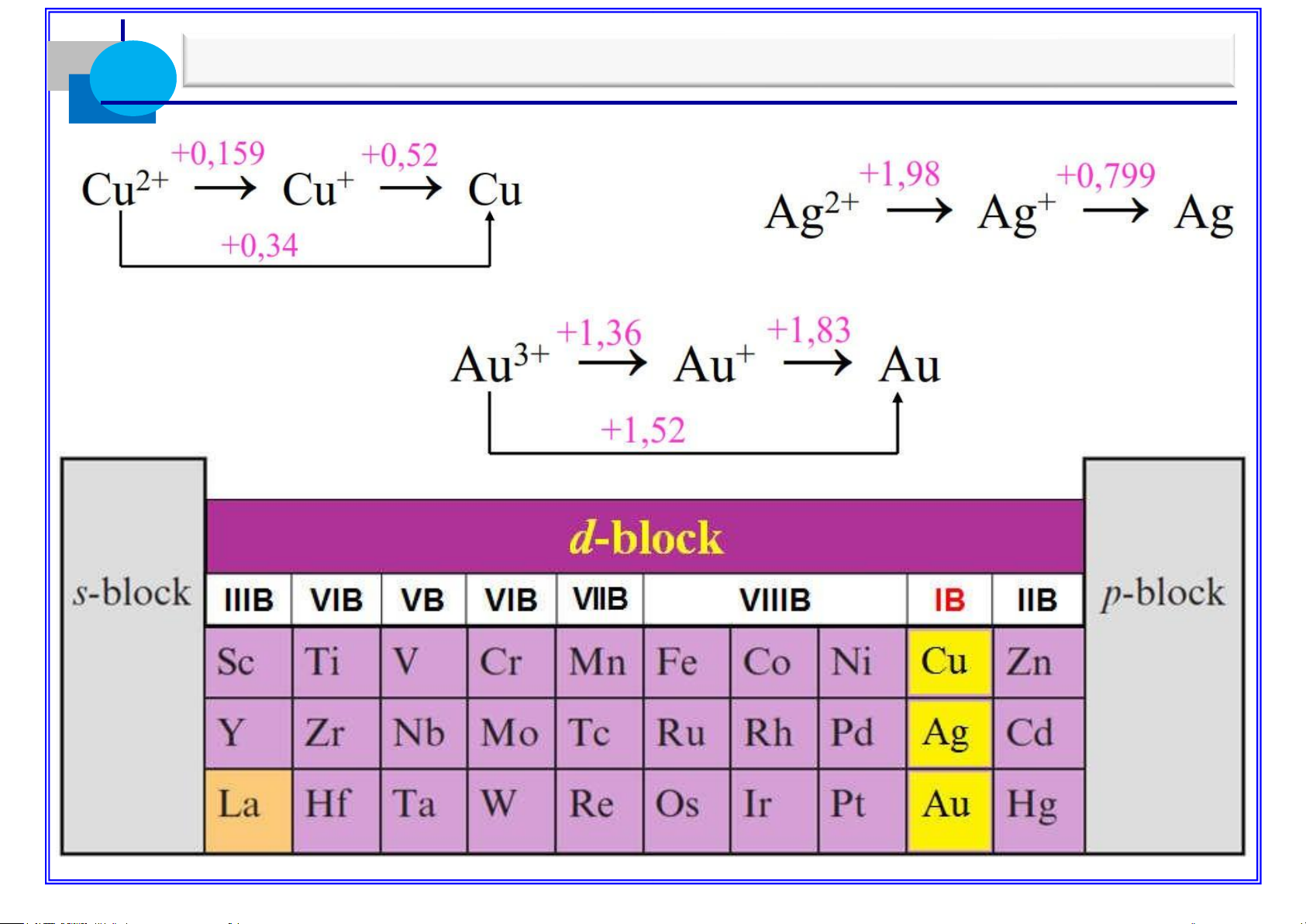
mức độ hoạt động IB < IA
hợp chất có số OXH > +1 lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB IB Cu Ag Au Rk,(Å) 1,28 1,44 1,44 I1, (eV) 7,72 7,57 9,22 I2, (eV) 20,29 21,50 20,50 I3, (eV) 36,9 34,82 30,50 IA K Rb Cs Rk,(Å) 2,36 2,53 2,74 I1, (eV) 4,32 4,16 3,58 lOMoAR cPSD| 58702377
Cu Au: tính KL , khả năng tạo phức , các hợp
chất số OXH cao đều có màu, hợp chất tan đều độc. lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB I ĐƠN CHẤT
1 Tính chất vật lý Kim Tonc, oC Tos, oC Tỷ Độ cứng
Độ dẫn điện Độ dẫn nhiệt loại khối (thang Mohr) (Hg = 1) (Hg = 1) Cu 1083 2543 8,94 3,0 57 36 Ag 960,6 2167 10,50 2,7 59 49 Au 1073,4 2880 19,32 2,5 40 35 lOMoAR cPSD| 58702377
- Dễ tạo hợp kim với nhau và với kim loại khác
- Dễ tạo hỗn hóng với Hg
- Rất dễ kéo sợi, dát mỏng (nhất là Au). lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB
2 Tính chất hóa học
- Kim loại kém hoạt động và hoạt tính Cu Au: +
Tác dụng với oxi không khí 2Cu + O2 + 2H2O 2Cu(OH)2 t0thường lOMoAR cPSD| 58702377 Cu(OH)2 + Cu Cu2O + H2O nếu không khí có H2S: 4Ag + 2H2S + O2 2Ag2S + 2H2O lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB
Tác dụng với axit:
+ Cu tác dụng với axit HCl, H2SO4 loãng có O2kk
Cu + H2SO4loãng + 1/2O2kk CuSO4 + H2O
+ Cu, Ag tác dụng với axit HI, H2SO4đđ, HNO3 Cu + HI CuI + 1/2H2 lOMoAR cPSD| 58702377
3Ag + 4HNO3loãng 3AgNO3 + NO + 2H2O + Cu,
Ag, Au tác dụng với nước cường thủy, dd HCl bão
hòa clo, dd CN- trong không khí, HCN đậm đặc
Au + HNO3 + 4HCl H[AuCl4] + NO + 2H2O 2Au + 3Cl2 + 2HCl 2H[AuCl4]
4Au + 8KCN + 2H2O + O2 4K[Au(CN)2] + 4KOH lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB II HỢP CHẤT
1 Các hợp chất (+1)
✓ Các oxyt E2O: đều là chất rắn, ít tan trong nước,
tan một phần trong dd kiềm đặc.
Cu2O + 2NaOHđặc 2Na[Cu(OH)2] -
Cu2O và Ag2O tan trong dd NH3đđ : lOMoAR cPSD| 58702377
Cu2O + 4NH3 + H2O 2[Cu(NH3)2]OH
Ag2O + 4NH3 + H2O 2[Ag(NH3)2]OH
- Cu2O bền nhiệt, Ag2O và Au2O kém bền nhiệt lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB
Điều chế oxyt E2O:
2CuSO4 + 4NaOH + C6H12O6 Cu2O + C6H12O7 + 2H2O + 2Na2SO4
2AgNO3 + 2NaOH Ag2O + 2NaNO3 + H2O
2AuCl + 2KOH Au2O + 2KCl + H2O
✓ Các hydroxit EOH: đều kém bền lOMoAR cPSD| 58702377 2EOH E2O + H2O lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB
✓ Các muối Cu(+1), Au(+1): không tan trong nước,
ở trạng thái ẩm không bền bị phân hủy, tan trong HClđặc 2CuCl (r) → CuCl2 + Cu (r)
3AuCl (r) → AuCl3 + 2 Au (r) lOMoAR cPSD| 58702377
✓ Các muối Ag(+1): bền trong dung dịch. Bị phân
hủy dưới tác dụng ánh sáng với mức độ khác nhau:
2AgBr → 2Ag + Br2 các halogenua dễ
bị phân cực hóa bởi Ag+ lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB
✓ Phức chất của E(+1):
- phức cation amiacat rất bền CuCl + 2NH3 [Cu(NH3)2]Cl
Ag2O + 4NH3 + H2O 2[Ag(NH3)2]OH
- phức anion phổ biến hơn và bền CuCl + HCl H[CuCl2] lOMoAR cPSD| 58702377
AgBr + 2Na2S2O3 Na3[Ag(S2O3)2] + NaBr lOMoAR cPSD| 58702377
CHƯƠNG XIV: CÁC NGUYÊN TỐ PHÂN NHÓM IB
2 Các hợp chất (+2) – Cu(+2) ✓ CuO:
- Tạo thành khi đốt nóng Cu với không khí hoặc nhiệt phân Cu(OH)2.