







Preview text:
Phần I: Các phương pháp phân tích quang học
Chương 3. Phương pháp phổ phát xạ nguyên tử
(Atomic Emission Spectroscopy (AES) Tran Thi Thuy
Department of Analytical Chemistry
School of Chemical Engineering – Hanoi University of Science and Technology (HUST) Outline 3.1 Giới thiệu
3.2 Nguyên tắc phương pháp phổ phát xạ nguyên tử AES
3.3 Phân tích bằng phương pháp AES
3.4 Các yếu tố ảnh hưởng đến độ chính xác AES
3.5 Ứng dụng của phương pháp AES 3.6 Bài tập 9/22/2020 2 HUST SCE 3.1 Giới thiệu
Trong quang phổ nguyên tử, một chất bị phân hủy
thành các nguyên tử trong ngọn lửa, trong lò hay trong
plasma (plasma là một loại khí đủ nóng để chứa các
ion và electron tự do). Mỗi nguyên tố được xác định
bằng cách đo hấp thụ hoặc phát bức xạ của các
nguyên tử khí ở vùng tử ngoại hoặc trông thấy. 3 HUST SCE 3.1 Giới thiệu
Ví dụ, để xác định các
nguyên tố vi lượng trong
một chiếc răng, các phần
nhỏ của răng được bốc hơi (ablated) bởi một
xung lazer và bị cuốn vào một plasma. Plasma ion
hóa một số các nguyên tử
và chúng đi vào phổ khối,
ở đó các ion được tách
theo khối lượng và được định lượng.
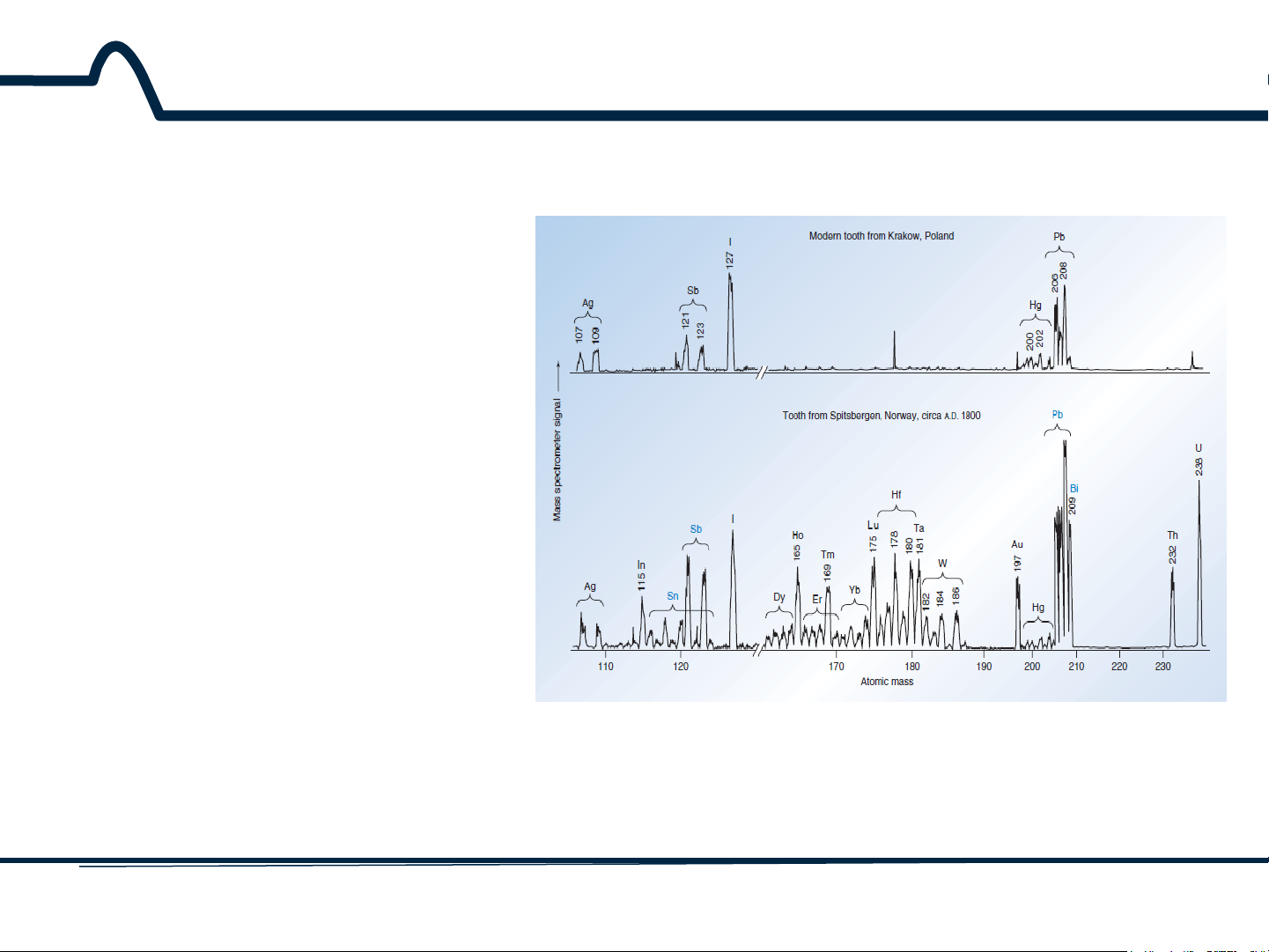
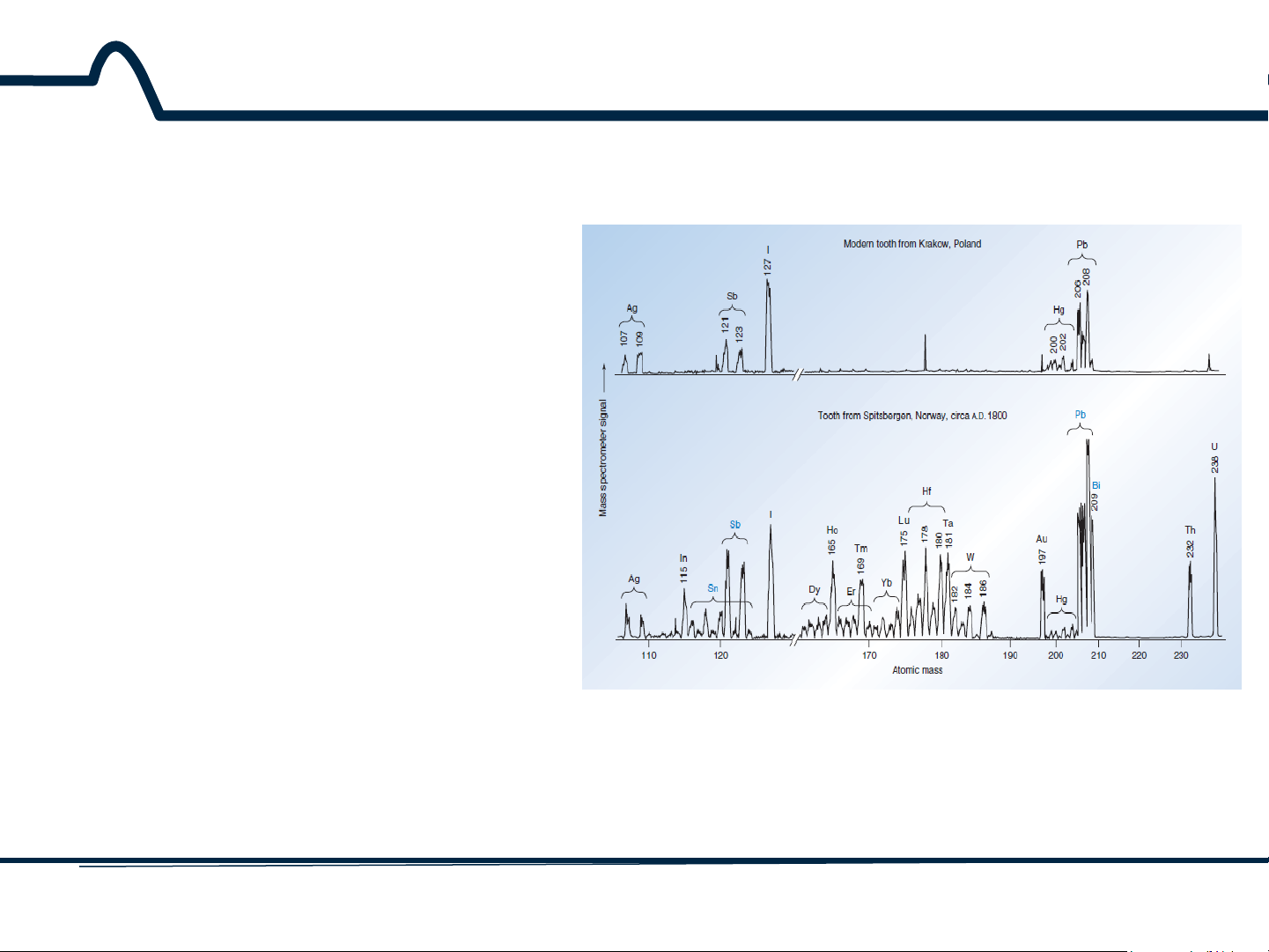
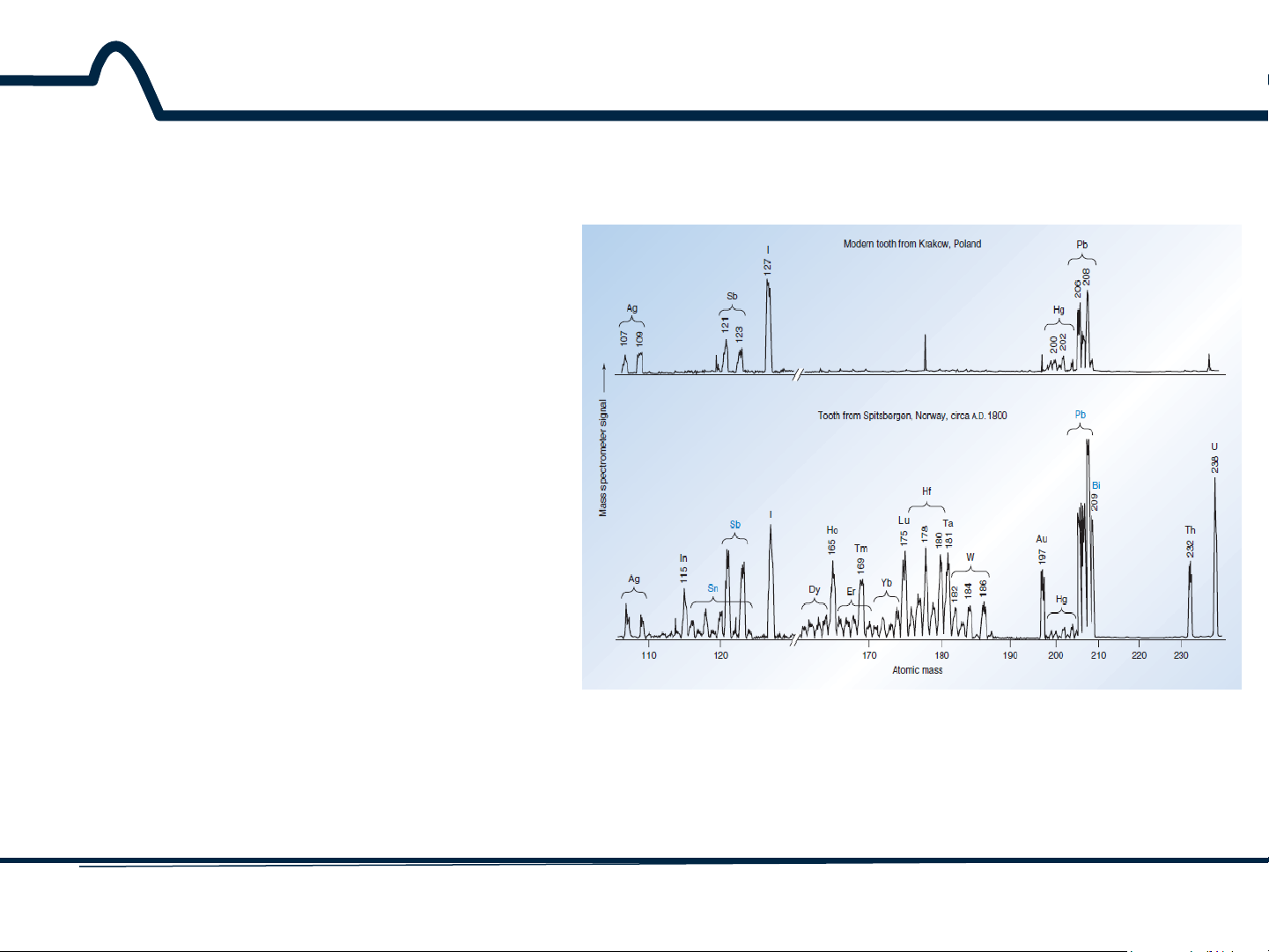
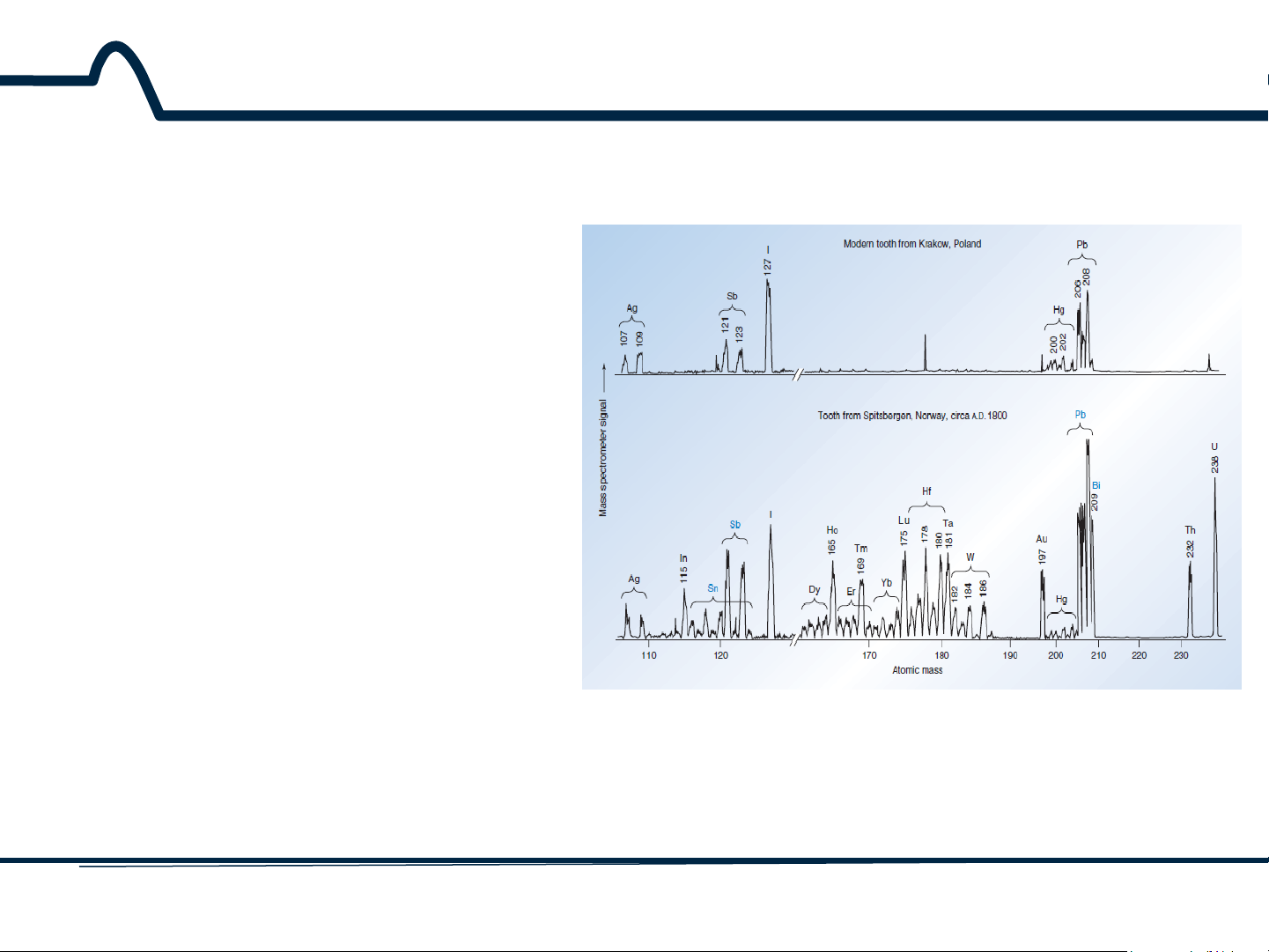
Hình 3.1. Phổ phát xạ của các vết nguyên tố của một chiếc răng từ một người đàn ông
hiện đại và từ một người sống bán đảo phía Tây Bắc Scandinavia cách đây 200 năm 4 HUST SCE 3.1 Giới thiệu
Các yếu tố được đưa vào
răng từ chế độ ăn uống
hoặc khi hít phải. Phổ khối
lượng cho thấy vết nguyên
tố được đo bằng laser - ion
hóa plasma – khối phổ của
ngà răng của răng từ một
người hiện đại và một người
đã sống ở Bắc Âu những năm 1800 sau công nguyên.
Độ tương phản rất nổi bật.
Hình 3.1. Phổ phát xạ của các vết nguyên tố của
một chiếc răng từ một người đàn ông hiện đại và từ
một người sống bán đảo phía Tây Bắc Scandinavia cách đây 200 năm 5 HUST SCE 3.1 Giới thiệu
Răng của người sống cách
đây khoảng 200 năm trước
có chứa một lượng đáng kể
của thiếc và bismuth, trong
đó nó gần như vắng mặt
trong các răng hiện đại.
Răng của người sống cách đây khoảng 200 năm có
chứa nhiều chì và antimon
hơn các răng hiện đại. Thiếc
và chì là thành phần của
hợp kim thiếc, nó được sử
dụng trong các dụng cụ nấu Hình 3.1.
ăn và đồ dùng. Bismuth và
Phổ phát xạ của các vết nguyên tố của
một chiếc răng từ một người đàn ông hiện đại và từ
antimon cũng có thể đến từ
một người sống bán đảo phía Tây Bắc Scandinavia thiếc. cách đây 200 năm 6 HUST SCE 3.1 Giới thiệu
Thậm chí còn nổi bật hơn
trong các răng của người
sống cách đây khoảng 200
năm trước là sự phong phú
của đất hiếm (dysprosium, holmium, erbium, thulium, ytterbium, và Lutetium) và
các yếu tố tantali, vonfram,
vàng, thori và urani. Khoáng
sản đất hiếm được tìm thấy ở Scandinavia (trong thực
tế, nhiều nguyên tố đất
Hình 3.1. Phổ phát xạ của các vết nguyên tố của
một chiếc răng từ một người đàn ông hiện đại và từ
hiếm được phát hiện).
một người sống bán đảo phía Tây Bắc Scandinavia cách đây 200 năm 7 HUST SCE 3.1 Giới thiệu
Giới hạn định lượng: µg/g - pg/g
Giảm nồng độ bằng pha loãng, hoặc có thể đo trực tiếp.
Độ chính xác của quang phổ nguyên tử, thường là 1-2%, là
không tốt như một số phương pháp hóa học ướt. Các thiết
bị đắt tiền, nhưng các thiết bị lại có sẵn rộng rãi.
Các mẫu cần xác định, mẫu chuẩn, và mẫu trống có thể
được đưa vào theo hệ bơm mẫu tự động, là một bàn xoay
tự động xoay mỗi mẫu vào vị trí để phân tích. Thiết bị có
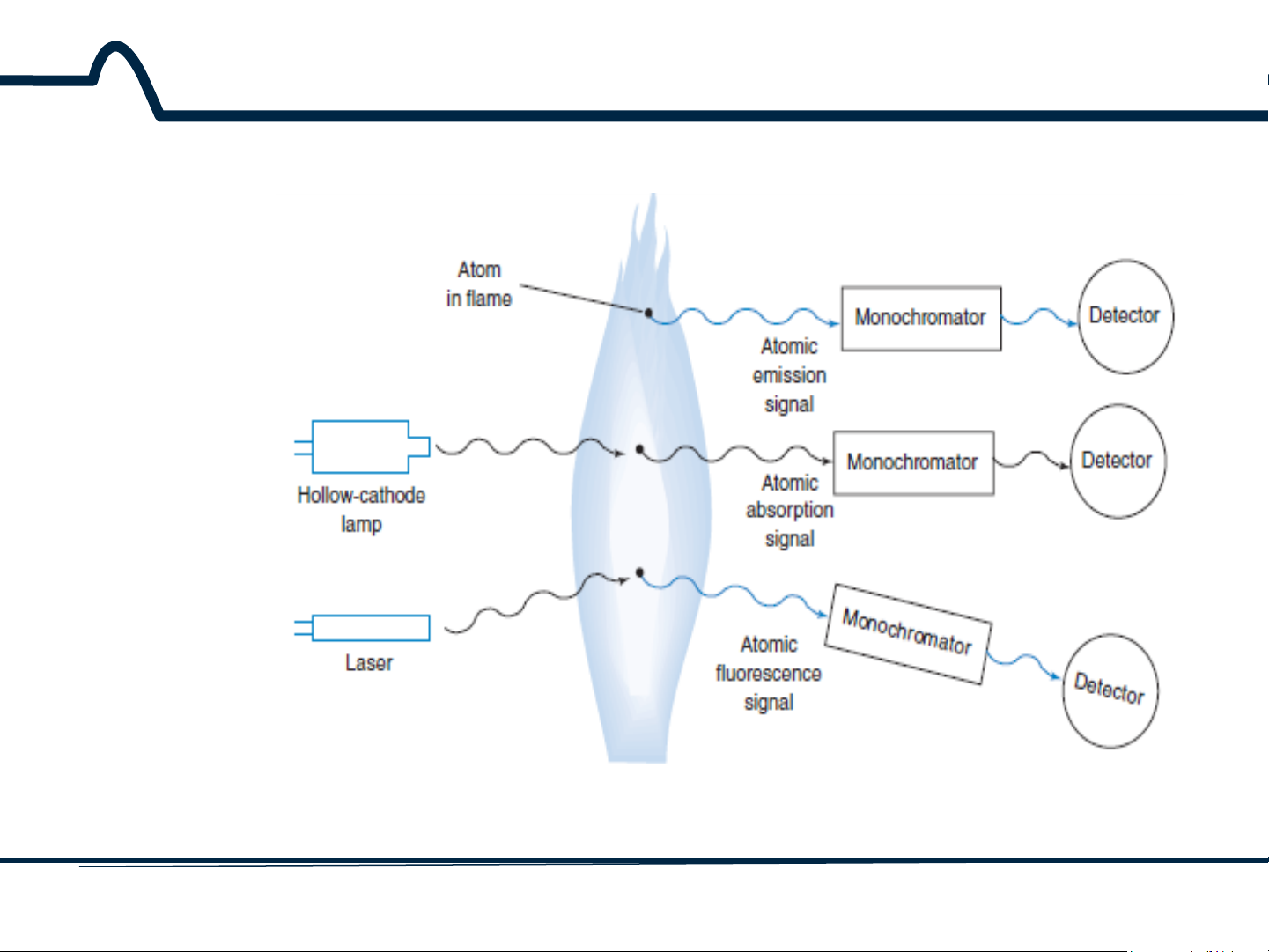
thể chạy trong nhiều giờ mà không cần sự can thiệp của con người. 8 HUST SCE 3.1 Giới thiệu Ngọn lửa
Hình 3.2. Các loại phổ nguyên tử 9 HUST SCE 3.1 Giới thiệu
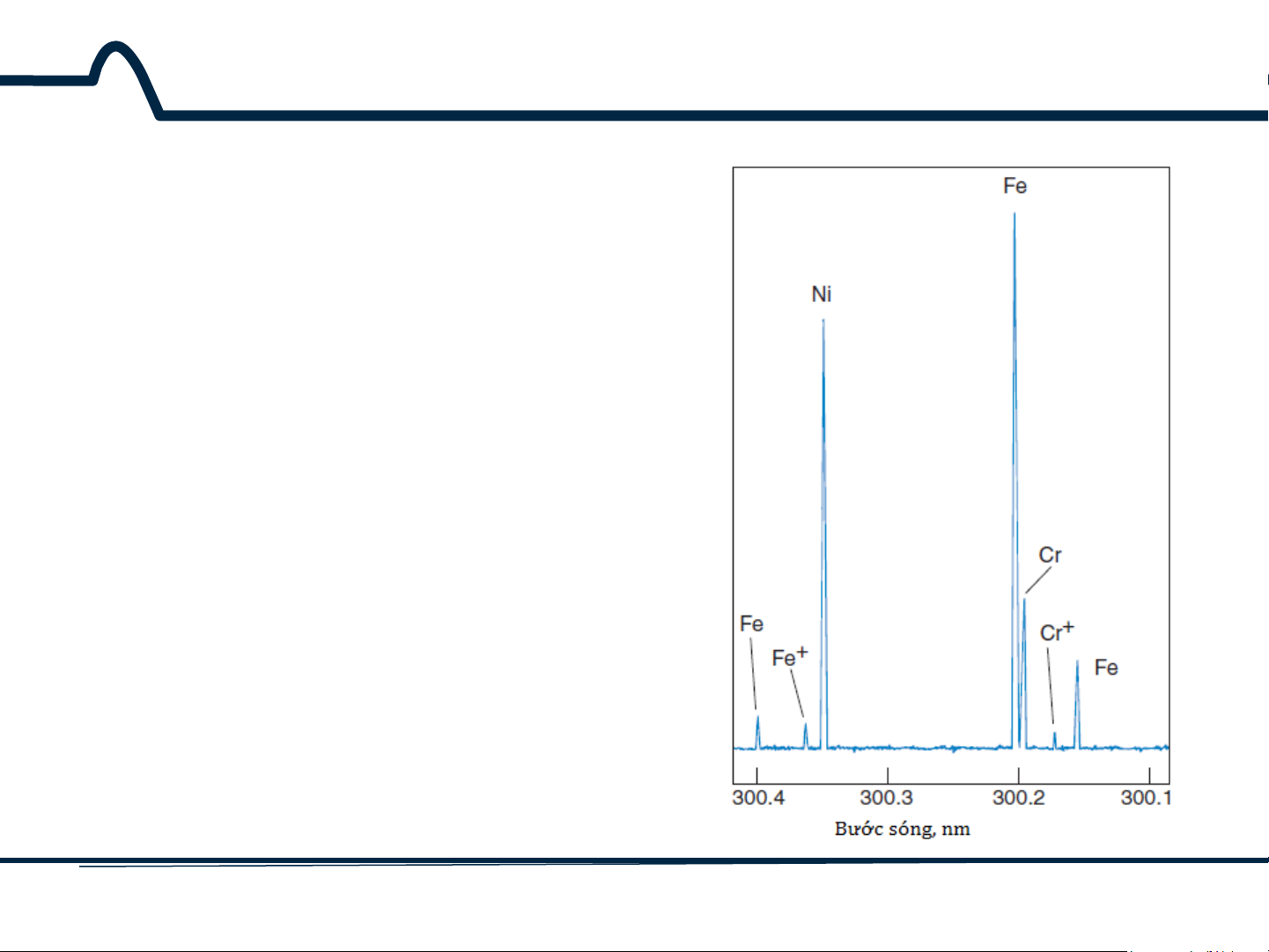
Phổ phát xạ nguyên tử của
đèn catot rỗng của thép chứa
Fe, Ni và Cr. Độ phân giải của
bộ tán sắc là 0,001 nm, có thể
so sánh độ rộng của vạch phổ
Hình 3.3. Phổ phát xạ nguyên tử
của đèn catot rỗng của thép 10 HUST SCE
3.2. Nguyên tắc phương pháp phổ phát xạ nguyên tử AES
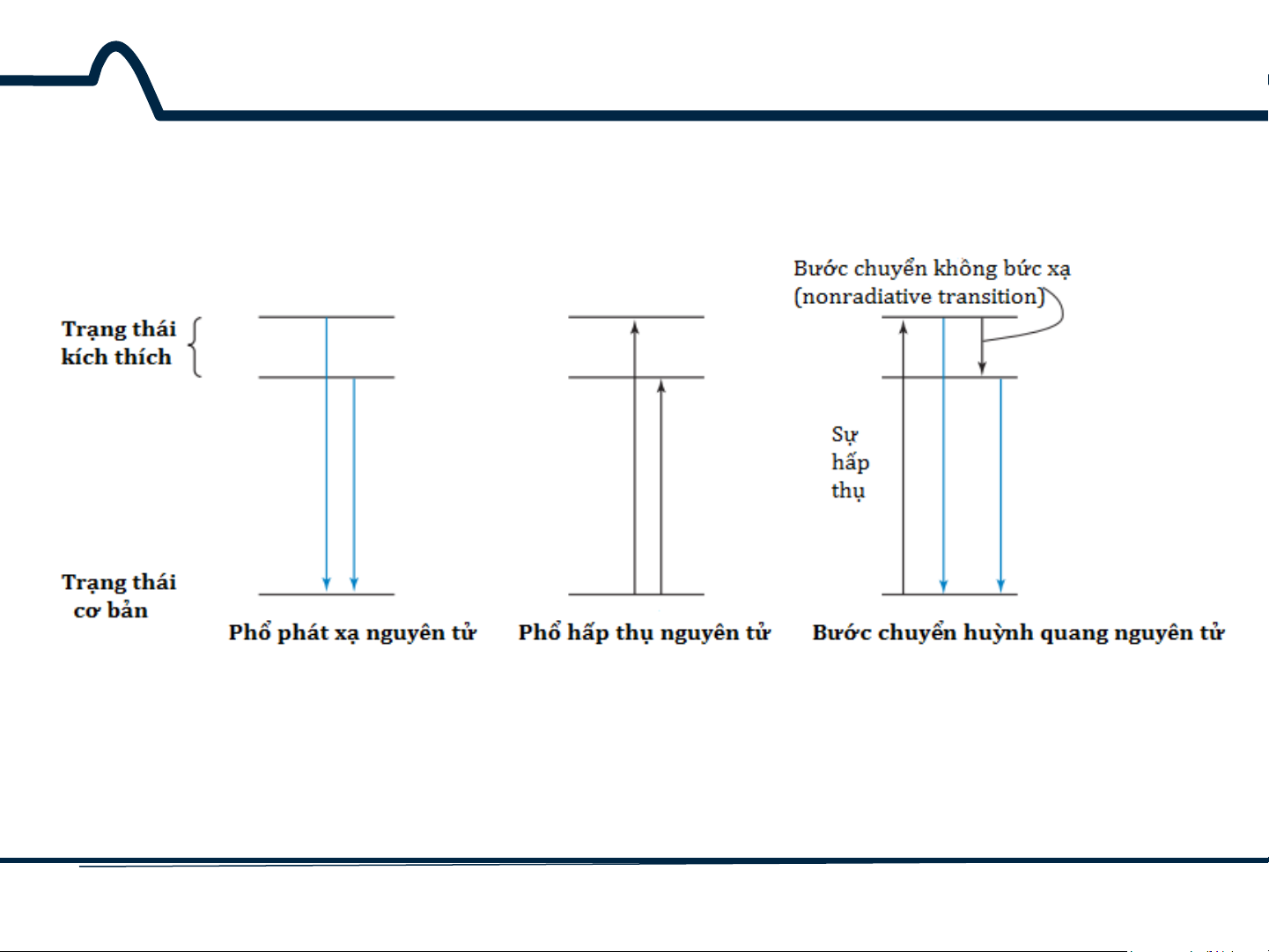
3.2.1. Sự tạo thành phổ AES
Hình 3.4. Quá trình hấp thụ và phát xạ của một nguyên tử 11 HUST SCE
3.2.2. Tính đa dạng của phổ AES
-Nhóm phổ vạch: Đó là phổ của nguyên tử và ion. Nhóm phổ vạch này của các nguyên tố
hóa học hầu như thường nằm trong vùng phổ từ 190-1000nm (vùng UV-VIS). Chỉ có một
vài nguyên tố á kim hay kim loại kiềm mới có một số vạch phổ nằm ngoài vùng này.
-Nhóm phổ đám: Đó là phổ phát xạ của các phân tử và nhóm phân tử. Ví dụ phổ của phân
tử MeO, CO và nhóm phân tử CN. Các đám phổ này xuất hiện thường có một đầu đậm và
một đầu nhạt. Đầu đậm ở phía sóng dài và nhạt ở phía sóng ngắn. Trong vùng tử ngoại thì
phổ này xuất hiện rất yếu và nhiều khi không thấy. Nhưng trong vùng khả kiến thì xuất
hiện rất đậm, và làm khó khăn cho phép phân tích quang phổ vì nhiều vạch phân tích của
các nguyên tố khác bị các đám phổ này che lấp.
- Phổ nền liên tục: Đây là phổ của vật rắn bị đốt nóng phát ra, phổ của ánh sáng trắng và
phổ do sự bức xạ riêng của điện tử. Phổ này tạo thành một nền mờ liên tục trên toàn dải
phổ của mẫu, nhạt ở sóng ngắn và đậm dần về phía sóng dài. Phổ này nếu quá đậm thì
cũng sẽ cản trở phép phân tích. 12 HUST SCE
3.2.3. Các loại vạch phổ đặc trưng của một nguyên tố
Trong tập hợp các vạch phổ đó, thì mỗi loại nguyên tử hay ion lại có một
số vạch đặc trưng riêng cho nó. Các vạch phổ đó được gọi là các vạch
phổ phát xạ đặc trưng của loại nguyên tố ấy.
Ví dụ: Khi bị kích thích:
nguyên tử Al phát ra vạch đặc trưng trong vùng UV: 308,215; 309,271nm.
nguyên tử Cu phát ra vạch đặc trưng trong vùng UV: 324,754; 327,396nm.
Chính nhờ các vạch phổ đặc trưng này người ta có thể nhận biết được sự
có mặt hay vắng mặt của một nguyên tố nào đó trong mẫu phân tích qua
việc quan sát phổ phát xạ của mẫu phân tích, và tìm xem có các vạch
phổ đặc trưng của nó hay không, nghĩa là dựa vào các vạch phổ phát xạ
đặc trưng của từng nguyên tố để nhận biết chúng. Đó là nguyên tắc của
phương pháp phân tích quang phổ phát xạ định tính. 13 HUST SCE
3.2.3. Các loại vạch phổ đặc trưng của một nguyên tố
Các vạch phổ đặc trưng phải thỏa mãn một số điều kiện sau đây:
- Những vạch phổ này phải rõ ràng và không trùng lẫn với các vạch của
nguyên tố khác, nhất là nguyên tố nồng độ lớn.
- Nó phải là những vạch phổ nhạy, để có thể phát hiện được các nguyên
tố trong mẫu với nồng độ nhỏ (phân tích lượng vết).
- Việc chọn các vạch phổ chứng minh cho một nguyên tố phải xuất phát
từ nguồn năng lượng đã dùng để kích thích phổ của mẫu phân tích, vì
trong nguồn kích thích có năng lượng thấp thì phổ của nguyên tử là chủ
yếu và vạch nguyên tử của nó thường là những vạch nhạy. Ngược lại,
trong nguồn kích thích giầu năng lượng (ICP) thì phổ của Ion là chủ yếu.
Cho nên phải tùy thuộc vào nguồn năng lượng đã dùng để kích thích phổ
mà chọn vạch chứng minh là vạch nguyên tử hay vạch ion cho phù hợp. 14 HUST SCE
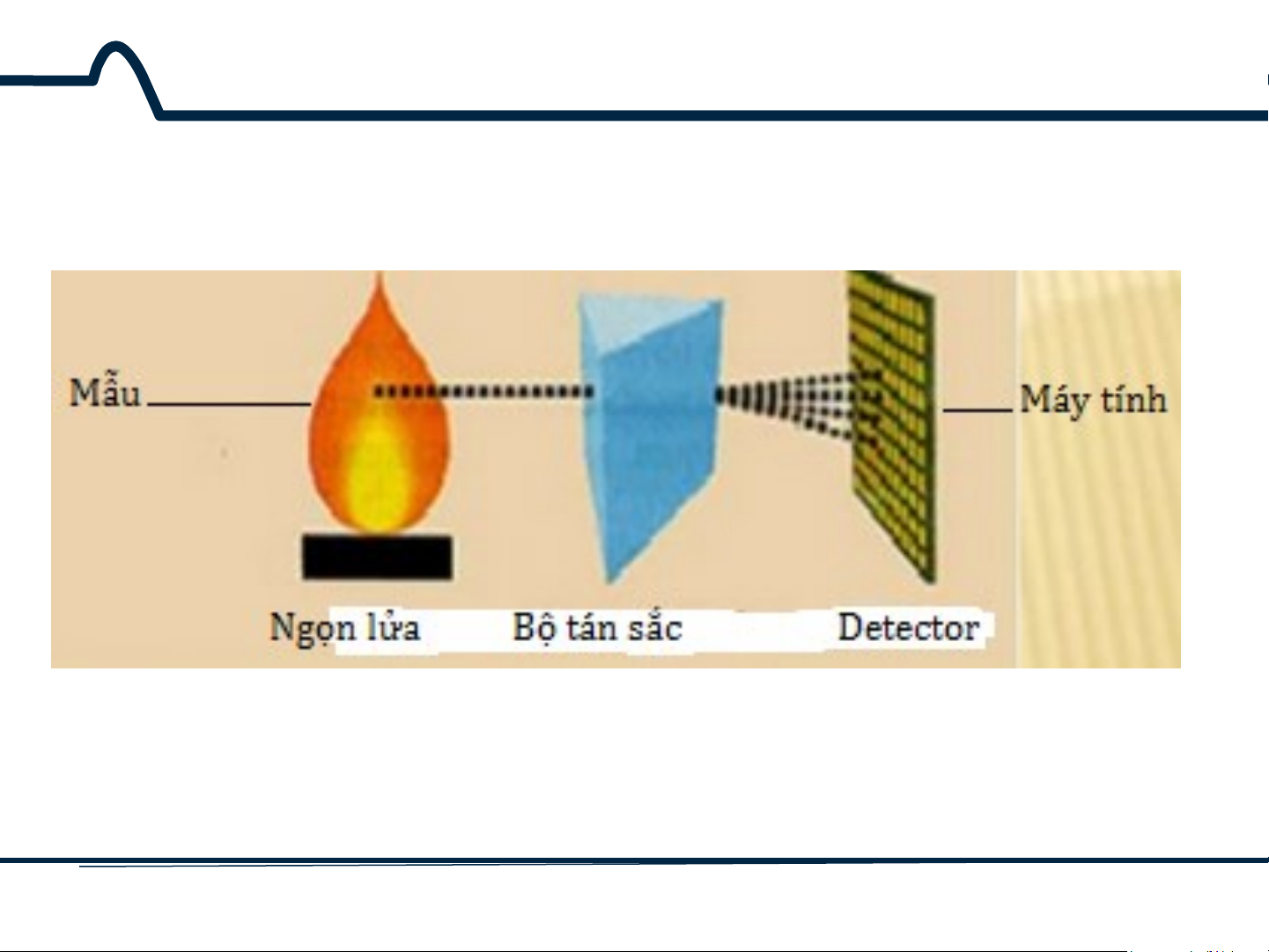
3.2.4. Sơ đồ thiết bị AES
Hình 3.5. Sơ đồ thiết bị phát xạ nguyên tử 15 HUST SCE
3.2.4. Sơ đồ thiết bị AES Nguồn: + Ngọn lửa + Lò điện
+ Cảm ứng cao tần plasma (ICP) 16 HUST SCE
3.2.4. Sơ đồ thiết bị AES Ngọn lửa
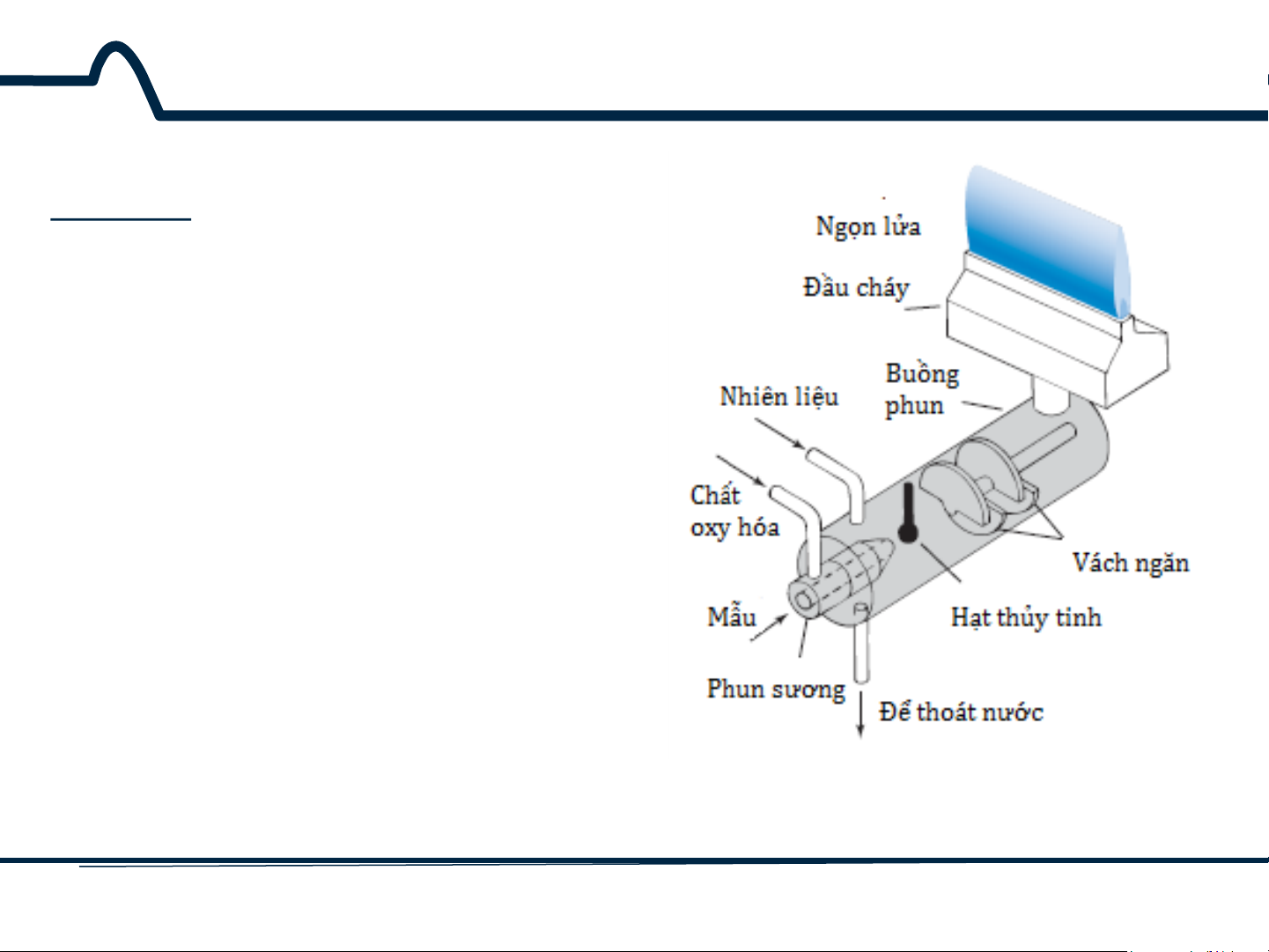
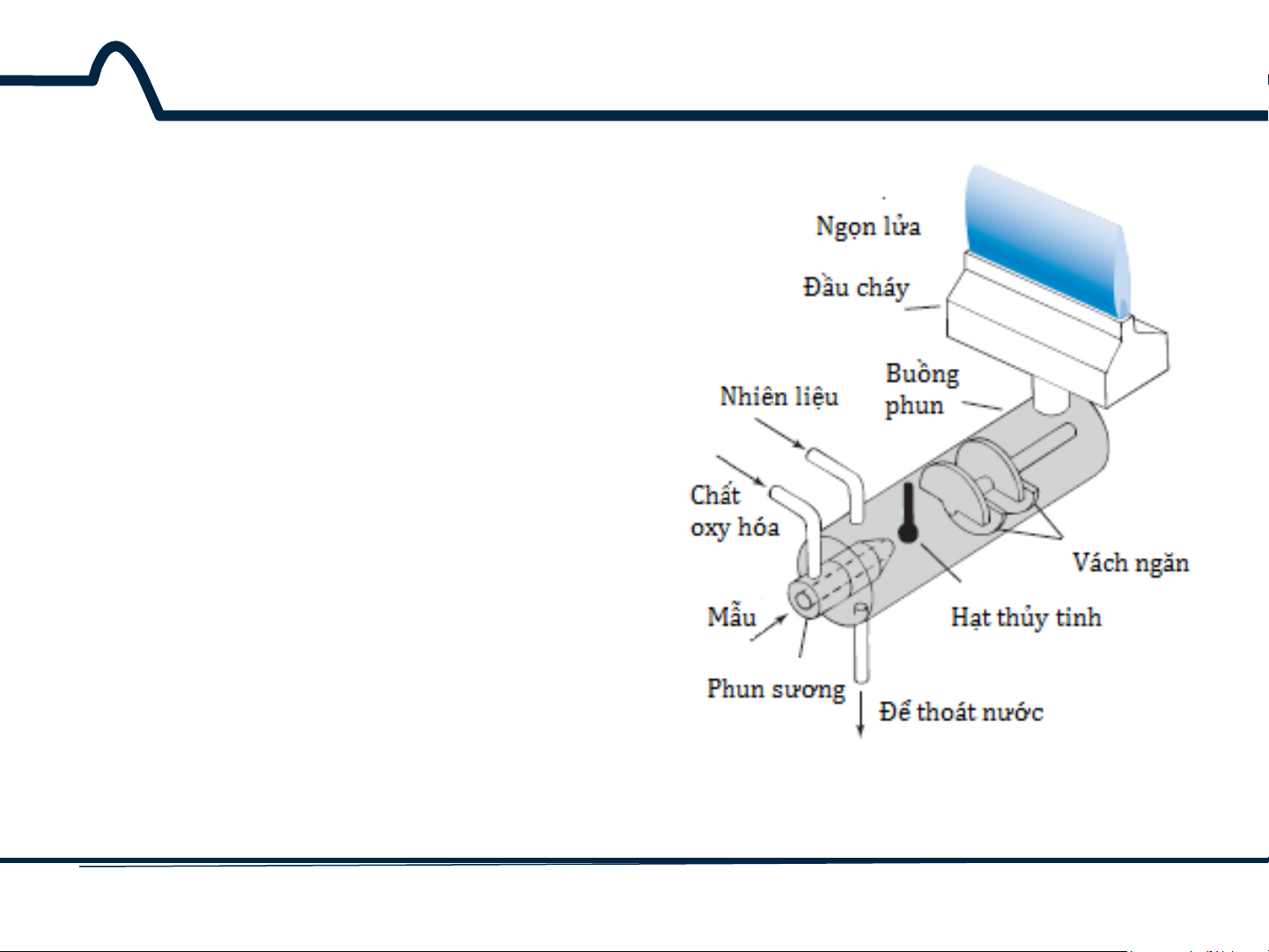
Hầu hết các quang phổ kế ngọn
lửa sử dụng Premix Burner
Nhiên liệu, chất oxy hóa,
và mẫu được trộn lẫn
trước khi đưa vào ngọn
lửa. Dung dịch mẫu được hút vào máy phun sương bởi dòng chất oxy hóa
(thường là không khí) qua mao quản của kim bơm mẫu. Hình 3.6. Premix Burner 17 HUST SCE
3.2.4. Sơ đồ thiết bị AES
Chất lỏng bị phá ra dưới
dạng sương mù khi rời khỏi mao quản. Quá trình phun
được định hướng bật vào
một hạt thủy tinh, khi đó
những giọt phá vỡ thành các
hạt nhỏ hơn. Sự hình thành
của các giọt nhỏ được gọi là xông (nebulization).
Sự phân tán tốt của chất
lỏng hay rắn trong khí được gọi là aerosol.
Hình 3.6. Premix Burner 18 HUST SCE
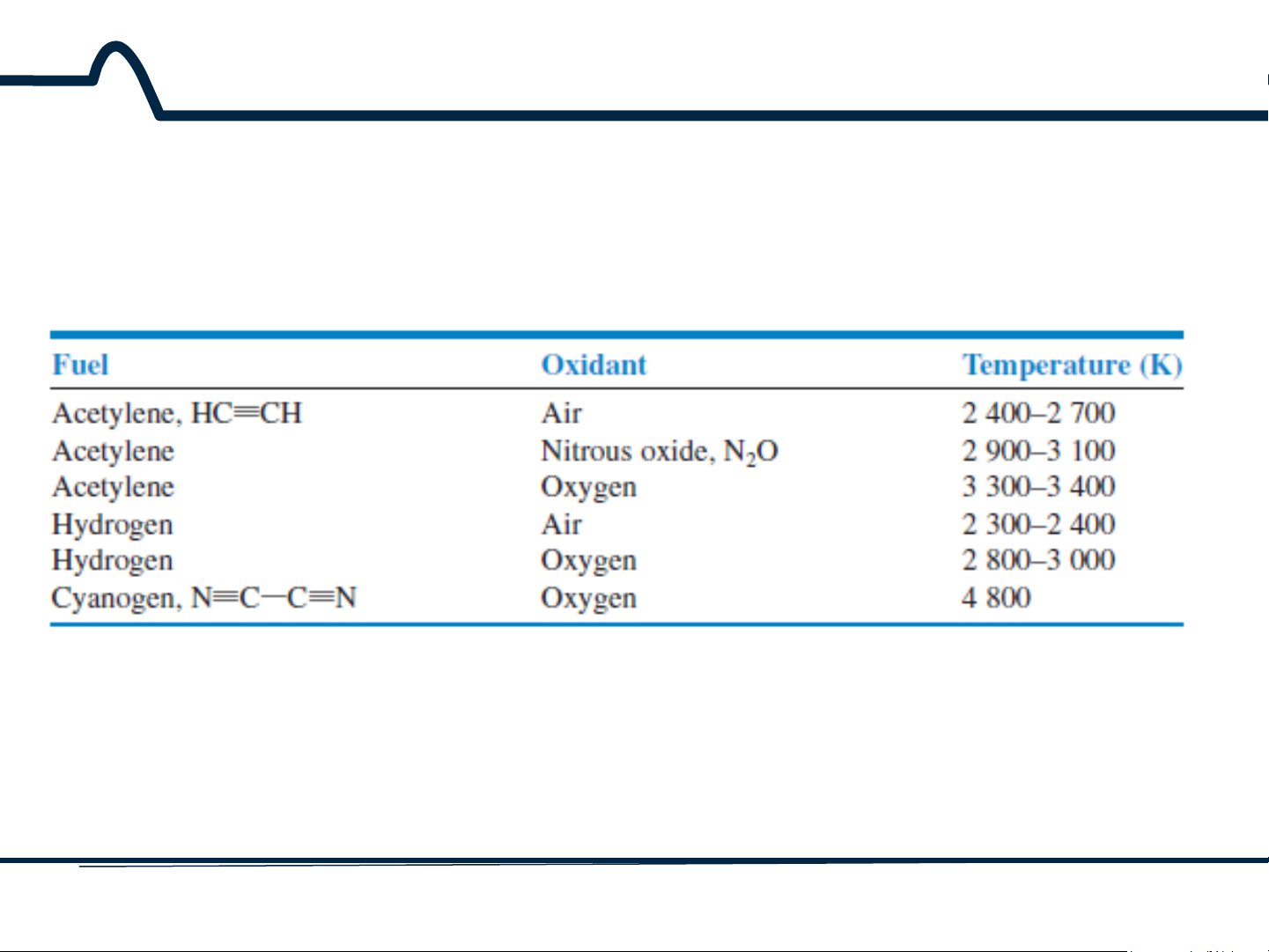
3.2.4. Sơ đồ thiết bị AES
Bảng 1. Nhiệt độ cao nhất của ngọn lửa 19 HUST SCE
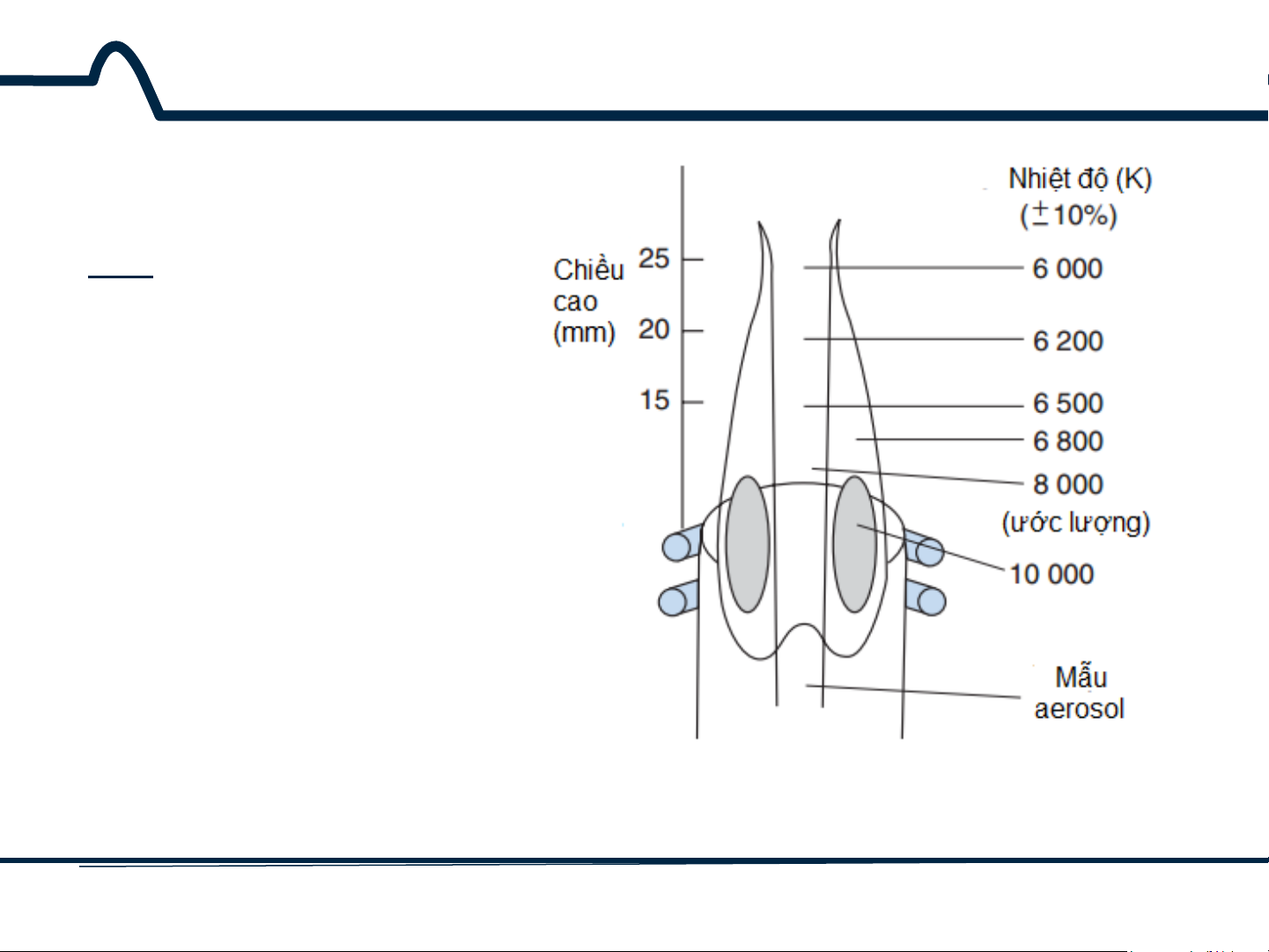
3.2.4. Sơ đồ thiết bị AES ICP
Phân tích đồng thời đa nguyên tố, ICP đã phổ biến, và đã thay thế phổ phát xạ nguyên tử dùng ngọn lửa. Tuy nhiên, chi phí mua và vận hành của ICP thì đắt hơn khi dùng ngọn lửa.
Hình 3.7. Nhiệt độ của thiết bị ICP 20 HUST SCE




