

Preview text:
PHƯƠNG PHÁP PHÂN TÍCH CÔNG CỤ
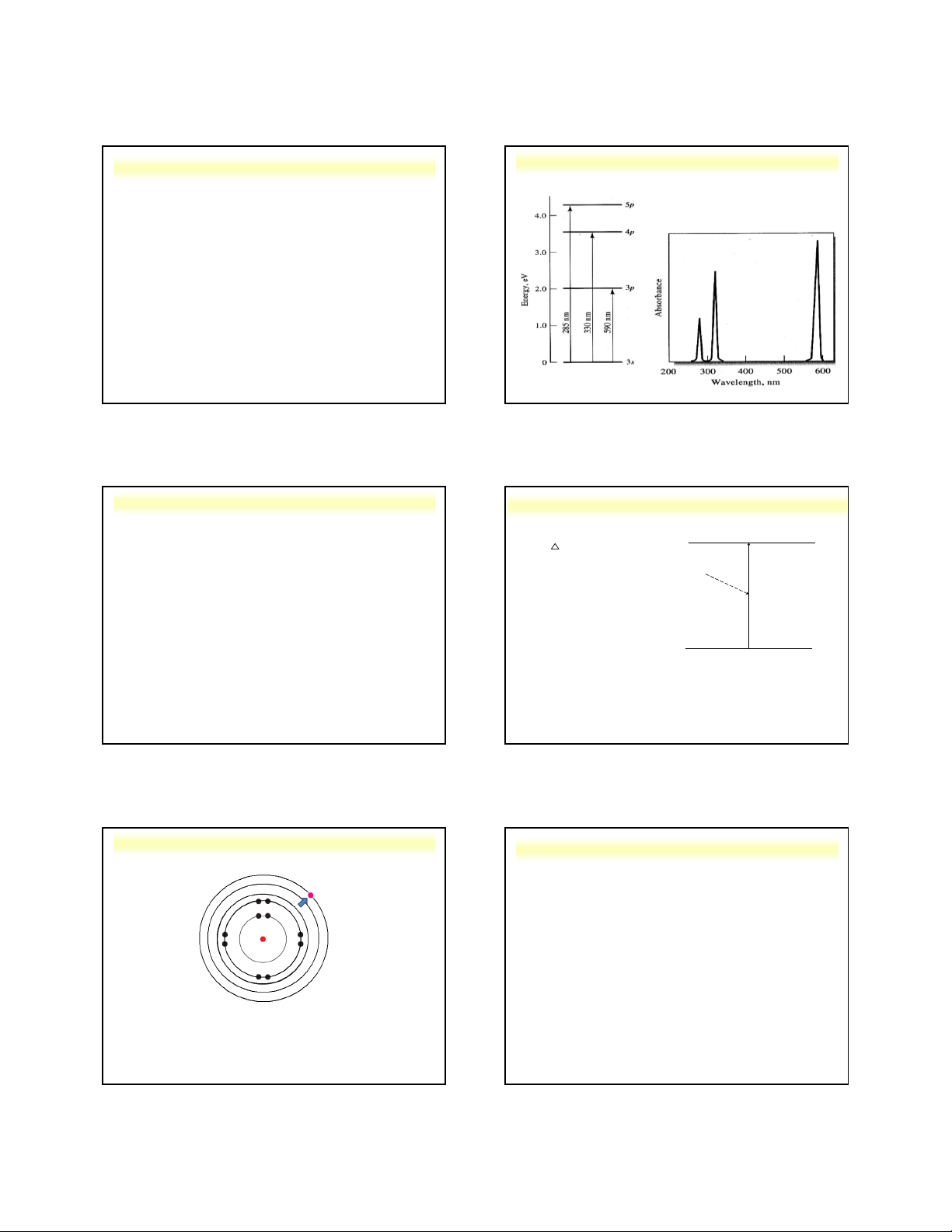
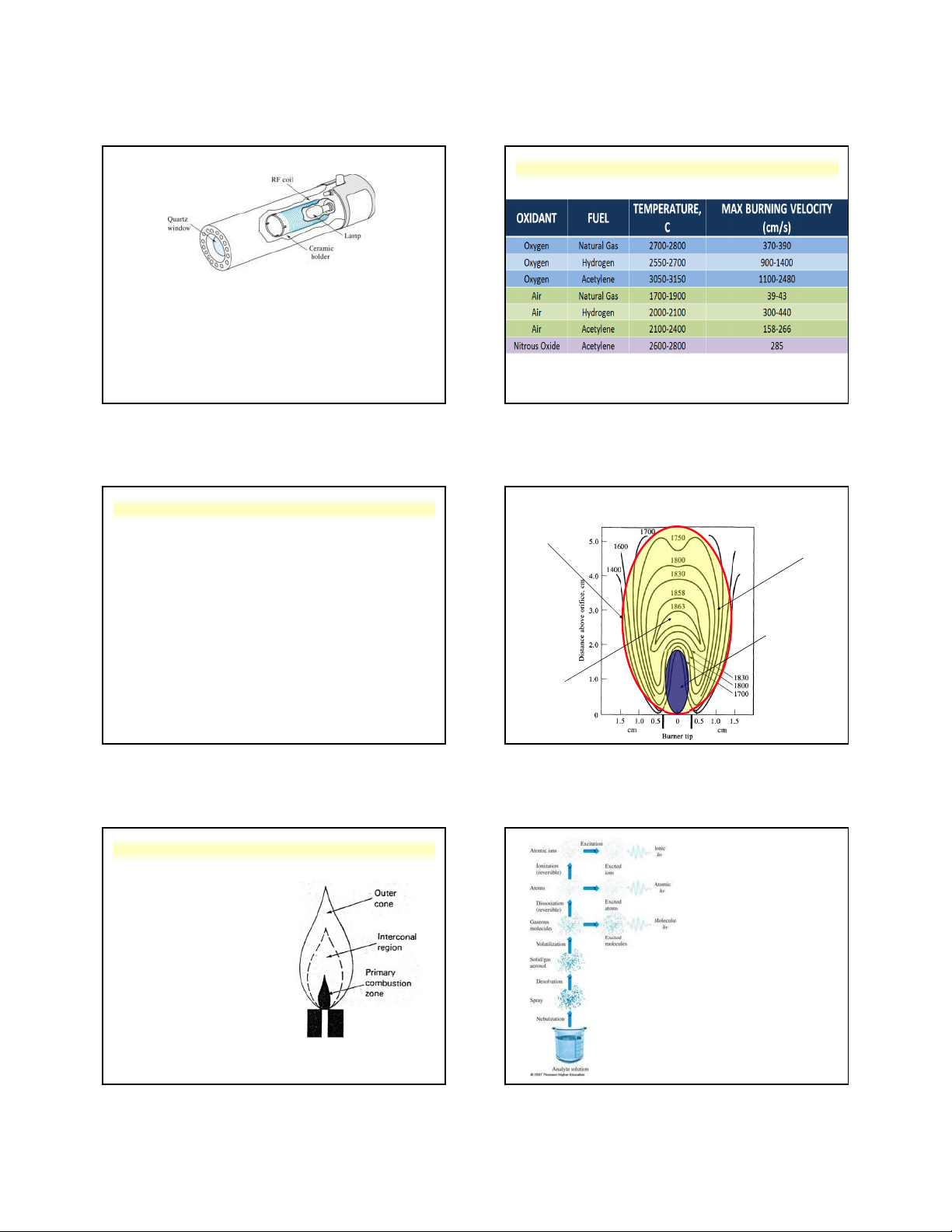
4.1. Sự xuất hiện phổ hấp thụ nguyên tử
PHẦN I: Các PP phân tích quang phổ
Chương 4: Phương pháp phổ hấp thụ nguyên tử
Nguyễn X. Trường – ANACHEM-SCE-HUST-2/139
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/142 139 142
4.1. Sự xuất hiện phổ hấp thụ nguyên tử
4.2. Sự hấp thụ ánh sáng của nguyên tử
Khi nguyên tử ở trạng thái hơi tự do bị kích thích
bởi bxđt có tần số xác định (ứng đúng với những E E = E - E 2 2 1
bức xạ quang học phát xạ), nó sẽ chuyển sang trạng = hn
thái kích thích có mức năng lượng cao hơn. Phổ sinh hn = c /ν
ra trong quá trình này gọi là phổ hấp thụ nguyên tử. = hc/(E - E ) 2 1
E = trạng thái kích thích 2 E = trạng thái cơ bản 1 h = hằng số Planck E1
ν = tần số sóng kích thích e- A = lg(I /I) = K x N x L 0 a
K : là hệ số hấp thụ nguyên tử đặc trưng cho từng bước sóng hấp a thụ của mỗi nguyên tố
N: nồng độ nguyên tử tự do ở trạng thái hơi
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/140
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/143
L: bề dày của lớp hấp thụ 140 143
4.1. Sự xuất hiện phổ hấp thụ nguyên tử
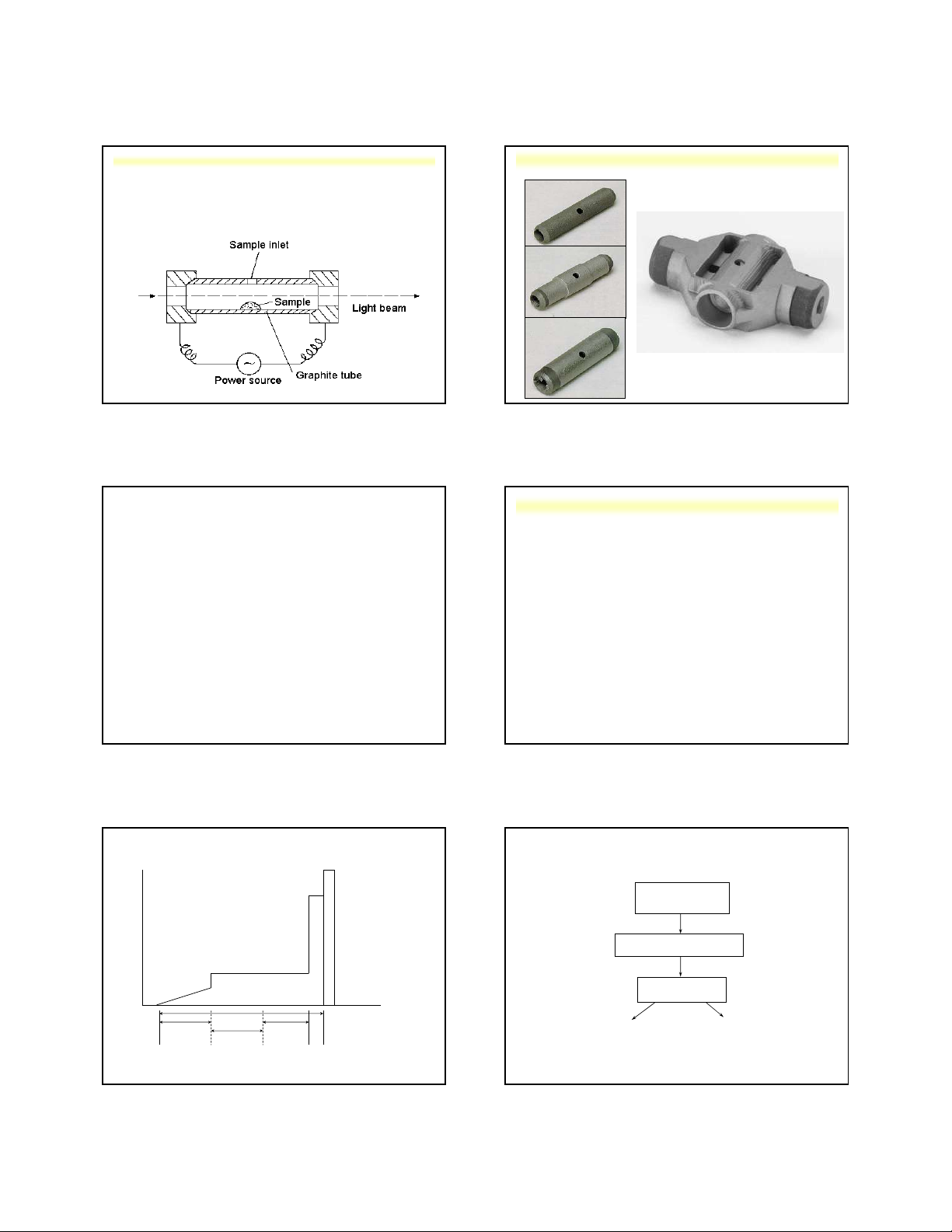
4.3. Nguyên tắc của phép đo phổ hấp thụ nguyên tử Na: 1s22s22p63s1 Nguyên tắc:
1. Hóa hơi và nguyên tử hóa mẫu
2. Chiếu chùm tia sáng bx đặc trưng của nguyên tố
cần phân tích qua đám hơi nguyên tử hóa.
3. Thu, phân li chọn 1 vạch phổ hấp thụ của nguyên
tố cần nghiên cứu để đo cường độ. Nguyên t Ng ử uyên tửNa Naở ở tr tr ạ ạ ng ng thái thái c kíơ b ch ản thích
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/144 141 144 Hệ thống AAS
4.5.1. Nguồn phát bức xạ đơn sắc
1. Đèn catot rỗng – Hollow-Cathode Lamp (HCL)
2. Đèn phóng điện không điện cực – Electroless Discharge Lamp (EDL)
3. Nguồn phát bức xạ đã được biến điệu: laser, ...
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/145
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/148 145 148
4.4. Cường độ vạch phổ hấp thụ nguyên tử
4.5.1. Nguồn phát bức xạ đơn sắc A = lg(I /I) = K x N x L λ 0 a Yêu cầu:
• BX đơn sắc phải là các tia bức xạ nhạy đối với
nguyên tố cần phân tích. Tần số của bức xạ (bước
• F là tốc độ dẫn mẫu vào hệ thống nguyên tử hóa (ml/phút),
sóng) ứng đúng với những tia bức xạ mà nó có thể
• W là hiệu suất sol hóa mẫu,
phát ra trong quá trình phát xạ.
• s là hiệu suất nguyên tử hóa,
• Chùm tia sáng phải có cường độ ổn định, lặp lại
• n0 là số phân tử khí ở nhiệt độ ban đầu, T0,
được trong các lần đo khác nhau trong cùng điều
• nT là số phân tử khí ở nhiệt độ T của ngọn lửa nguyên tử hóa,
kiện và phải điều chỉnh được để có cường độ cần
• Q là tốc độ của dòng khí mang mẫu vào buồng sol hóa (lít/phút),
thiết trong mỗi phép đo.
• C là nồng độ của nguyên tố phân tích có trong dung dịch mẫu. Aλ = a. Cb
a: gọi là hằng số thực nghiệm
b: gọi là hằng số bản chất (0 < b ≤ 1)
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/146
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/149 146 149
4.5. Sơ đồ khối và nguyên lý hoạt động của máy Đèn catot rỗng
Anot được chế tạo bằng kim loại trơ và bền nhiệt như Pt, W,…
quang phổ hấp thụ nguyên tử
Catot được chế tạo có dạng hình ống rỗng và chính bằng kim
loại cần phân tích với độ tinh khiết cao ( > 99,9 %).
Hiện nay, có cả đèn kép đôi, kép ba hay kép 6 nguyên tố (Cu+Mn+Cr+Fe+Co+Ni).
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/147
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/150 147 150
Đèn Phóng Điện Không Điện Cực
Nhiệt độ của ngọn lửa
Nguồn năng lượng cảm ứng tạo ra ở tần số cao 100 kHz – 100 MHz (radiofrequency)
Chất trong đèn là vài mg kim loại hay muối kim loại dễ
bay hơi của nguyên tố phân tích.
Nguồn bức xạ mạnh hơn đèn catot rỗng gấp 10 lần
Sử dụng cho những nguyên tố kém nhạy với đèn catot
rỗng như As, Se, Te, Hg, Pb, …Nguyễn X. Trường –ANACHEM-SCE-HUST-6/151
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/154 151 154
4.5.2. Các kỹ thuật nguyên tử hoá mẫu
Nguyên tử hóa mẫu: Là quá trình hoá hơi và nguyên secondary
tử hoá chất phân tích thành nguyên tử tự do. interzonal
(a) Ngọn lửa (Flame AAS : F-AAS)
(b) Không ngọn lửa (Electrothermal Atomization - ETA-AAS)
- Lò graphit AAS (Graphite Furnace - GFAAS) Primary zone
- Hydrua hóa (Hydride Vapor Generator - HVG)
- Hoá hơi lạnh (Mercury Vapor Unit - MVU) Maximum temperature 5-155
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/152 152 155 VD: dung dịch muối KCl a. Ngọn lửa KCl K+ + Cl- s aq aq 1. Bay hơi dung môi
Ngọn lửa tạo thành do sự K+ + Cl- KCl aq aq s
kết hợp của khí oxi hoá
2. Chất rắn chảy và hóa hơi
(không khí, NO ,…) và khí KCl KCl s g 2 3. Nguyên tử hóa đốt (H , acetylen,…). 2 KCl K + Cl g g g
4. Nguyên tử bị kích thích hoặc
ion hóa (hấp thụ năng lượng do va chạm) K K* K K+ + 1e
5. Nguyên tử bị kích thích (hấp thụ bức xạ) K K* …
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/153
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/156 153 156 b. Không ngọn lửa
Cuvet để nguyên tử hoá mẫu •
Nguyên tử hóa sử dụng lò graphit (GF-AAS)
Là quá trình nguyên tử hóa bằng nhiệt điện.
Dạng mẫu: lỏng hoặc rắn, được nạp trực tiếp vao hệ thống
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/157
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/160 157 160
Các quá trình khi nguyên tử hóa bằng lò graphit b. Không ngọn lửa
1a. Quá trình làm khô mẫu - Loại dung môi •
Nguyên tử hóa sử dụng bộ tạo hydrua (HVG-AAS)
- Việc lựa chọn nhiệt độ phụ thuộc vào nhiệt độ bay hơi của dung
môi, không quá cao tránh xảy ra hiện tượng bắn mẫu. -
Sử dụng để xác định các nguyên tố dễ hóa hơi như
- Thông thường ở nhiệt độ khoảng 110OC Se, As, Sn, Sb, Te, Bi.
2a. Quá trình tro hóa -
Các nguyên tố được chuyển về dạng hơi kim loại bằng
- Các hợp chất hữu cơ bị tro hóa hoặc chuyển thành H O, CO , và 2 2
cách cho phản ứng với NaBH trong môi trường axit: 4
các hợp chất vô cơ bay hơi.
H Se; AsH , H Te, SbH , SnH , … 2 3 2 3 4
- Nhiệt độ đủ cao để loại các hợp chất bay hơi mà không làm mất chất phân tích.
3a. Quá trình nguyên tử hóa
- Thường ở nhiệt độ khoảng 2000 – 3000oC 4a. Quá trình làm sạch
- Nhằm làm bay hơi các chất bẩn như các kim loại hoặc muối còn
lại nằm trong ống graphit.
- Thông thường nhiệt độ làm sạch sẽ cao hơn nhiệt độ nguyên tử hóa khoảng 200oC
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/158
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/161 158 161
Các bước thay đổi nhiệt độ trong lò Hydrua hoá (HVG) Làm sạch Nguyên tử hoá Se, As, Sn, Sb, Te ) C Bi o độ ( t Hoá hơi Hydrua Nhiệ Tro hoá Làm khô Nguyên tử hoá Thời gian (s) Outer gas (Ar) Inner gas (Ar) Ngọn lửa Nhiệt Inner gas (O ) 2 0 20 35 50 54
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/159
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/162 159 162 Hydrid hoá (HVG)
Hoá hơi lạnh (Mercury Vapor Unit - MVU) BH - + 3H O + H+ H BO + 4H (hidro mới sinh) 4 2 3 3 2 3BH - + 3H + + 4H AsO 4AsH + 3H O + 3H BO 4 3 3 3 2 3 3
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/163
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/166 163 166 Hydrid hoá (HVG) 4.5.3. Bộ đơn sắc 1. Cách tử nhiễu xạ
2. Hệ thống truyền ánh sáng (khe vào, gương, thấu kính, khe ra) 4.5.4. Detector Ống nhân quang
Nguyên lý và cấu tạo của Bộ đơn sắc và Detector xem chương 2 3BH - 4 +3H+ +4H3AsO3 3H3BO3 + 4AsH3 + 3H20
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/164
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/167 164 167 b. Không ngọn lửa
4.6. Phân tích định lượng bằng phổ hấp thụ nguyên tử •
Bộ hóa hơi lạnh phân tích thủy ngân (MVU-AAS)
- Các phương pháp phân tích trực tiếp -
Ion Hg2+ trong dung dịch bị khử thành Hg nguyên tố
- Các phương pháp phân tích gián tiếp: sử dụng để
(dễ bay hơi) bằng SnCl ở nhiệt độ phòng. 2
phân tích các nguyên tố không có phổ AAS.
Sn2+ + Hg2+ = Hg0 + Sn4+
+ Thông qua việc đo phổ của 1 kim loại có phổ nhạy, -
Thích hợp cho phân tích thủy ngân trong môi nước và
KL này có khả năng tương tác với chất phân tích môi trường.
theo 1 phản ứng hóa học định lượng như: phản ứng -
Giới hạn phát hiện có thể đạt 0,1 ppb.
tạo kết tủa, tạo phức ít phân ly, …
+ Dựa theo hiệu ứng tăng hay giảm cường độ vạch phổ
AAS của 1 nguyên tố KL khi cho KL này tác dụng
với chất phân tích phù hợp.
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/165
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/168 165 168
4.7. Các yếu tố gây ảnh hưởng đến quá trình đo phổ
4.6. Phân tích định lượng bằng phổ hấp thụ nguyên tử
hấp thụ nguyên tử Ưu điểm:
• Ảnh hưởng của các cation
- Độ nhạy và độ chọn lọc cao. Có thể xác định ~ 60
Trong dung dịch phân tích, ngoài nguyên tố cần xác định
nguyên tố hóa học, độ nhạy ~10-4-10-5%.
còn chứa nhiều cation lạ. Ảnh hưởng của các cation có thể
có hiệu ứng dương, hiệu ứng âm hoặc vừa có hiệu ứng
- Tốn ít nguyên liệu mẫu, tiết kiệm thời gian, trong
dương vừa có hiệu ứng âm ở các nồng độ khác nhau.
nhiều trường hợp không phải làm giàu.
Để loại trừ ảnh hưởng của các cation sử dụng một số biện
- Kết quả phân tích ổn định, sai số nhỏ (<15%). pháp sau: Nhược điểm:
* Chọn điều kiện xử lý mẫu phù hợp để loại các nguyên tố
lạ ra khỏi dung dịch phân tích
- Chỉ cho biết thành phần nguyên tố của chất ở trong
* Chọn các thông số máy đo thích hợp
mẫu phân tích mà không chỉ ra trạng thái liên kết.
* Chọn điều kiện thí nghiệm và điều kiện nguyên tử hoá mẫu thích hợp
* Thêm vào mẫu chất phụ gia phù hợp để loại trừ ảnh
hưởng của các cation như: LaCl , SrCl , AlCl . 3 3 3
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/169
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/172 169 172
4.7. Các yếu tố gây ảnh hưởng đến quá trình đo phổ
4.6. Phân tích định lượng bằng phổ hấp thụ nguyên tử
hấp thụ nguyên tử
Đối tượng và khả năng ứng dụng: •
Ảnh hưởng của các anion
- Phân tích lượng vết các kim loại và một số phi kim
+ Ảnh hưởng của các anion về cơ bản cũng tương tự
(Si, P, S, …) trong các loại mẫu khác nhau của các
như ảnh hưởng của các loại axít. Chỉ có 2 anion
ClO - và CH COO- là gây hiệu ứng dương, còn các
chất vô cơ và hữu cơ. 4 3
anion khác gây hiệu ứng âm theo thứ tự Cl- < NO - < 3
- Phân tích các loại mẫu quặng, đất, đá, nước khoáng,
CO 2- < PO 3- < F-. 3 4
các mẫu y học, sinh học, các sản phẩm nông nghiệp,
+ Ảnh hưởng của các anion không lớn như các
cation, nên để loại trừ ảnh hưởng của các anion ta
rau quả, thực phẩm, nước uống, các nguyên tố vi
chỉ cần trong mỗi phép đo phải cho nồng độ của các
lượng trong phân bón, trong thức ăn gia súc, ...
anion trong mẫu phân tích và trong mẫu chuẩn như nhau là được.
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/170
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/173 170 173
4.7. Các yếu tố gây ảnh hưởng đến quá trình đo phổ
4.7. Các yếu tố gây ảnh hưởng đến quá trình đo phổ
hấp thụ nguyên tử
hấp thụ nguyên tử
• Ảnh hưởng của nồng độ axít và loại axít trong dung •
Ảnh hưởng của một loạt yếu tố khác như: dịch mẫu
+ Thành phần nền của mẫu, dung môi hữu cơ, độ
nhớt và sức căng bề mặt của dung dịch mẫu, sự ion
Nồng độ axít làm thay đổi độ nhớt của dung dịch, do
hoá, sự kích thích phổ phát xạ, sự chen lấn của vạch
anion gốc axít quyết định. Các axít càng khó bay hơi
phổ, sự hấp thụ của nền,…
thường càng làm giảm cường độ vạch phổ. Các axít
+ Để thu được kết quả tốt, khi làm thí nghiệm phải
dễ bay hơi gây ảnh hưởng ít. Axít làm giảm độ hấp
khống chế để dung dịch phân tích và dung dịch
chuẩn phải được tiến hành trong cùng điều kiện và
thụ theo thứ tự HCl < HNO < H SO < H PO < HF. 3 2 4 3 4
tiến hành đo với các thông số tối ưu hoàn toàn như
(thường dùng HCl, HNO 1%) 3 nhau.
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/171
Nguyễn X. Trường – ANACHEM-SCE-HUST-6/174 171 174




