














Preview text:
Chương 7
Phương pháp phân tích vôn-ampe
(Voltammetry)
7.1. Cơ sở của phương pháp 2
7.1.1. Đặc điểm chung
Phương pháp phân tích vôn-ampe là nhóm các phương pháp dựa vào
đường cong vôn-ampe, hay còn gọi là đường cong phân cực, là đường
cong biểu diễn mối quan hệ giữa cường độ dòng điện với điện thế khi
tiến hành điện phân dung dịch phân tích.
Quá trình điện phân được thực hiện trong một bình điện phân đặc biệt,
trong đó có một điện cực có diện tích bé hơn điện tích của điện cực kia
nhiều lần. Điện cực có diện tích bé được gọi là vi điện cực. Quá trình
khử (hay oxy hóa) chủ yếu xảy ra trên vi điện cực.
7.1. Cơ sở của phương pháp 3
7.1.1. Đặc điểm chung
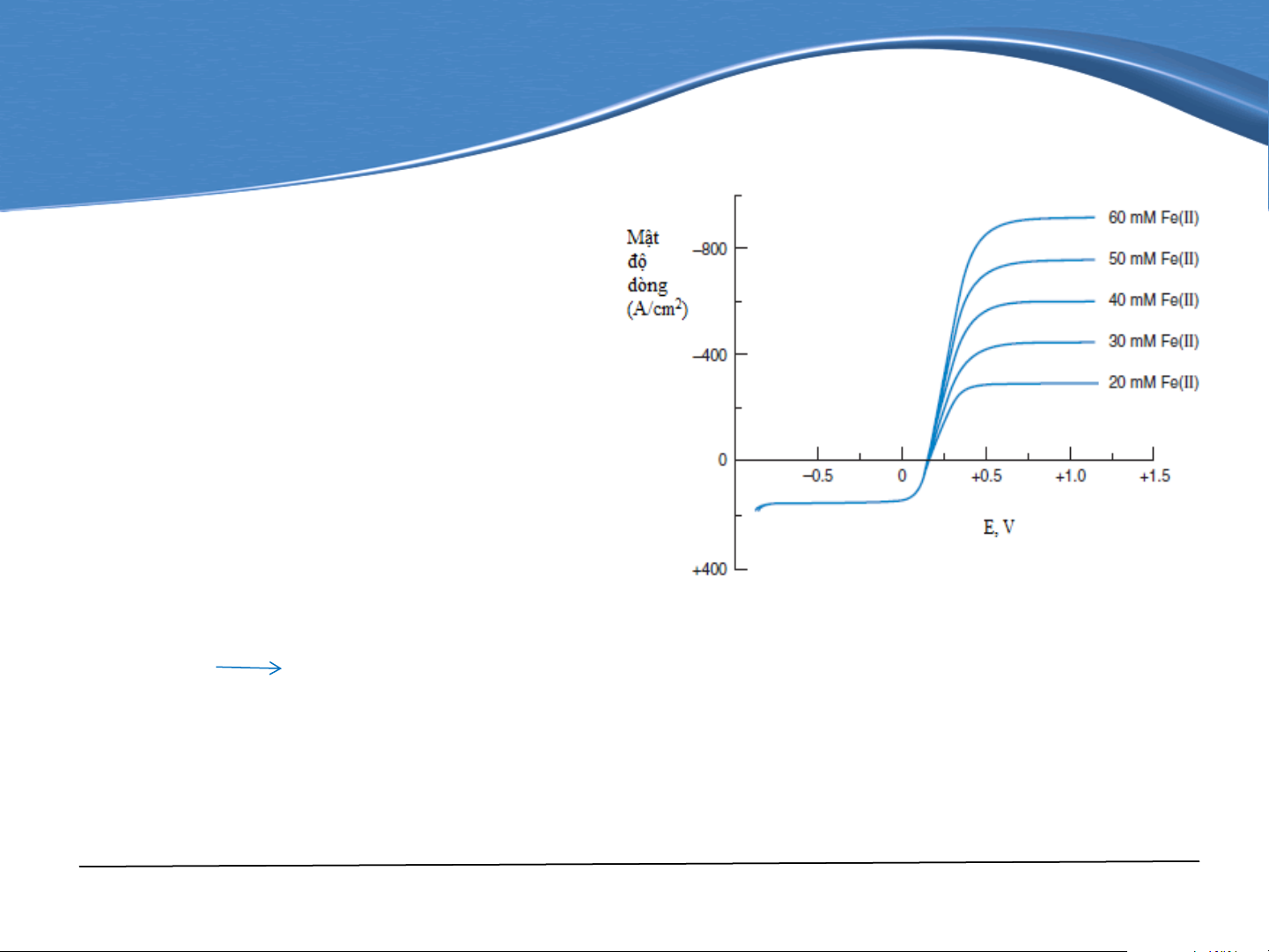
Đường cong vôn-ampe trên hình 7-1
là đường cong mô tả mối quan hệ
dòng và thế của điện cực làm việc
trong quá trình oxy hóa hay khử của hỗn hợp Fe(CN) 3– 4– 6 /Fe(CN)6 xảy ra
trên điện cực đĩa quay.
Theo qui ước, dòng là dương khi
chất phân tích bị khử trên điện cực
làm việc. Giới hạn của dòng khuếch
tán cho quá trình oxy hóa Fe(CN) 4– 6
xảy ra ở điện thế lớn hơn 0,5V (điện
cực so sánh là calomen bão hòa). 4– 3–
Hình 7-1. Đường cong vôn-ampe cho hỗn hợp Fe(CN)6 Fe(CN)6 + e–
10 mM K3Fe(CN)6 và 20-60mM K4Fe(CN)6 trong Ferroxyanide
Ferricyanide
dung dịch Na2SO4 0,1M trên điện cực đĩa quay
(xyanua sắt II)
(xyanua sắt III)
cacbon thủy tinh. Tốc độ quay 2000
Ở vùng này, dòng được điều khiển bởi tốc 4–
vòng/phút, điện thế quét 5mV/s
độ khuếch tán của Fe(CN)6 tới điện cực.
7.1. Cơ sở của phương pháp 4
7.1.1. Đặc điểm chung
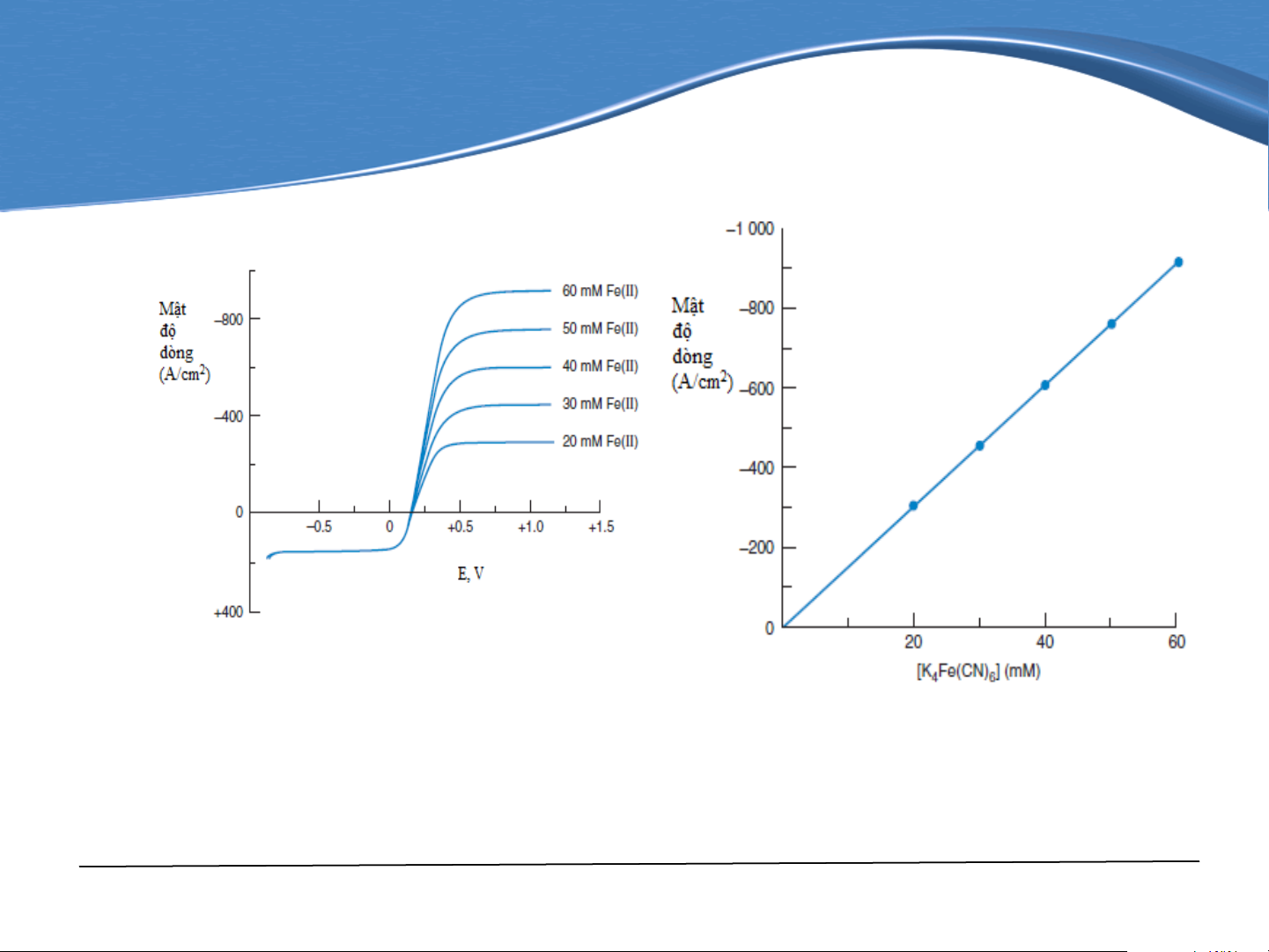
Hình 7-1. Đường cong vôn-ampe cho hỗn hợp
10 mM K3Fe(CN)6 và 20-60mM K4Fe(CN)6 trong
Hình 7-2. Sự phụ thuộc dòng giới hạn
dung dịch Na2SO4 0,1M trên điện cực đĩa quay
vào nồng độ K4Fe(CN)6
cacbon thủy tinh. Tốc độ quay 2000
vòng/phút, điện thế quét 5mV/s
7.1. Cơ sở của phương pháp 5
7.1.1. Đặc điểm chung
Việc ứng dụng đường cong điện phân cực vào mục đích
phân tích đã được nhà bác học người Tiệp Khắc Heyrovski
tìm ra vào năm 1922. Do phát minh về phương pháp phân
tích dựa vào đường cong điện phân cực và những đóng góp
xây dựng phát triển phương pháp phân tích, năm 1959
Heyrovski được tặng giải thưởng Nobel về hóa học.
Dùng phương pháp vôn-ampe người ta có thể xác định được
nhiều ion vô cơ, hợp chất hữu cơ. Quá trình phân tích có thể
được thực hiện trong môi trường nước và cả môi trường
không nước. Phép phân tích có thể được thực hiện với độ
nhạy, độ chọn lọc và độ chính xác rất cao.
7.1. Cơ sở của phương pháp 6
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
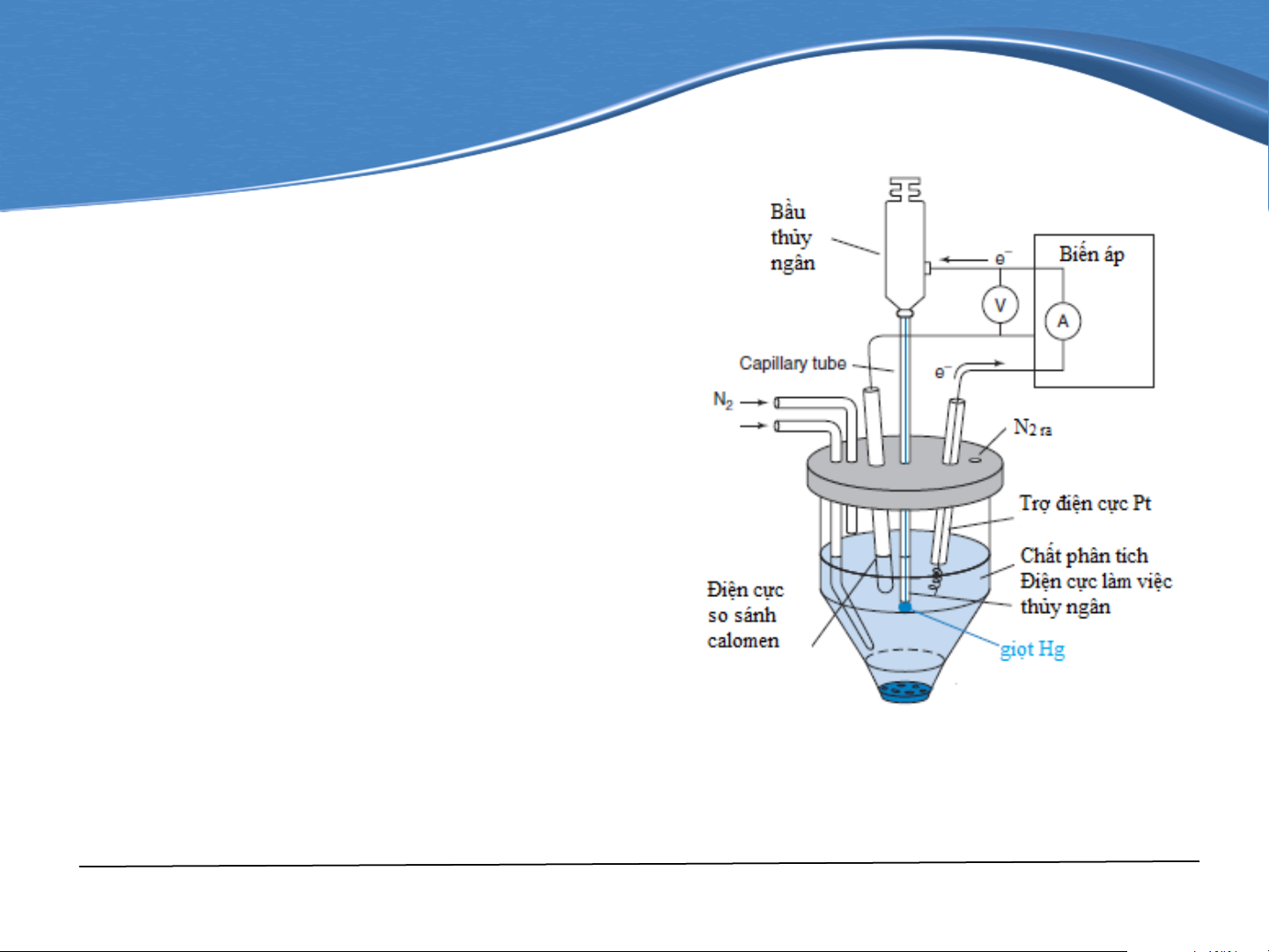
Phương pháp vôn-ampe dựa trên quá
trình điện phân với điện cực giọt thủy
ngân được gọi là phương pháp cực phổ (hình 7-3).
Hình 7-3. Thiết bị vôn-ampe với điện cực làm việc Hg
7.1. Cơ sở của phương pháp 7
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Một số lượng lớn các phản ứng được nghiên cứu với điện cực thủy ngân là các
phản ứng khử. Ở bề mặt điện cực Pt, sự khử H+ xảy ra với nhiều chất phân tích.
2H+ + 2e– → H2(khí) E° = 0,000V
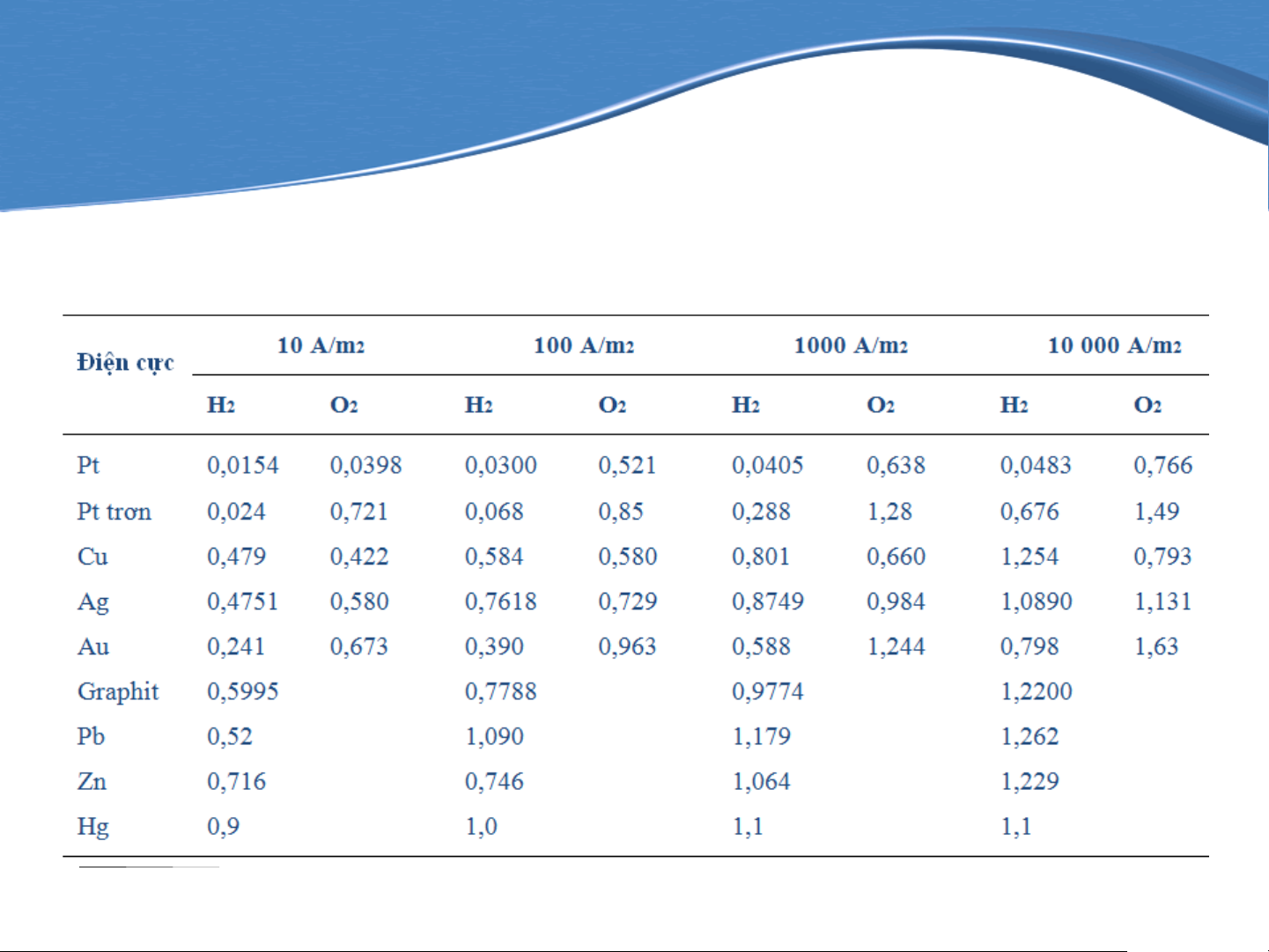
Bảng 7-1 chỉ ra rằng quá thế cho sự thoát H2 trên bề mặt điện cực Hg là rất lớn.
Trong môi trường trung tính hay kiềm, thậm chí các cation kim loại kiềm (nhóm I)
bị khử dễ dàng hơn H+. Hơn nữa, sự khử của một ion kim loại trên điện cực Hg ở
dạng hỗn hống là dễ dàng hơn sự khử trên bề mặt điện cực rắn. K+ + e– → K(rắn) E° = –2,936 K+ + e– + Hg → K(hỗn hống Hg) E° = –1,975 V
7.1. Cơ sở của phương pháp 8
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Điện cực thủy ngân không thuận lợi cho việc nghiên cứu phản ứng oxy hóa bởi vì
Hg dễ bị oxy hóa trong môi trường không tạo phức ở thế gần 0,25V (được so sánh
với điện cực calomen bão hòa). Nếu nồng độ Cl– là 1M, Hg bị oxy hóa gần giá trị
0V bởi vì Hg(II) được ổn định bởi Cl– do tạo phức:
Hglỏng + 4Cl– ⇋ + 2e–
Để nghiên cứu các phản ứng oxy hóa bằng phương pháp vôn-ampe, các điện cực
làm việc như Pt, Au, C hay kim cương trong dung dịch nền thích hợp được sử dụng.
7.1. Cơ sở của phương pháp 9
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Bảng 7-1. Quá thế (V) của quá trình thoát khí ở các mật độ dòng khác nhau ở 25°C
7.1. Cơ sở của phương pháp 10
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Ta nghiên cứu quá trình điện phân trên catot là điện cực thủy ngân, còn anot là
điện cực có diện tích lớn ví dụ điện cực calomen. Vì điện cực calomen có diện
tích bề mặt lớn hơn diện tích điện cực giọt Hg rất nhiều nên quá trình điện cực
chủ yếu xảy ra trên điện cực giọt Hg. Vì điện cực Hg là catot nên người ta gọi đây
là phân cực catot. Nếu trong dung dịch không có các chất có khả năng bị khử
dưới tác dụng của dòng điện, cường độ dòng điện I sẽ tỉ lệ với điện thế đặt vào
hai cực (định luật Ohm).
I là cường độ dòng điện chạy qua bình điện phân;
E là điện thế giáng vào hai cực;
R là điện trở của bình điện phân;
Từ (7-1) cho thấy cường độ I phụ thuộc tuyến tính với điện thế đặt vào hai cực bình điện phân.
7.1. Cơ sở của phương pháp 11
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Khi có các chất tham gia phản ứng khử trên catot Hg trong miền điện thế nghiên
cứu, dạng đường cong I-E sẽ thay đổi. Khi điện thế giáng vào hai cực của bình
điện phân đạt đến giá trị điện thế khử của ion nghiên cứu, trên điện cực giọt thủy
ngân có thể tạo thành hỗn hống:
Mn+ + ne– + Hg ⇋ M(Hg) (7-2)
7.1. Cơ sở của phương pháp 12
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Điện thế của điện cực giọt Hg khi xảy ra quá trình thuận nghịch 7-2 tính theo phương trình Nernst:
Ca (Camalgam) là nồng độ của hỗn hống (M);
γa là hệ số hoạt độ của hỗn hống;
CM là nồng độ của ion kim loại bị khử tại lớp dung dịch ở sát bề mặt của điện cực, M;
γM là hệ số hoạt độ của ion kim loại M trong dung dịch;
aHg là hoạt độ của thủy ngân trong hỗn hống
E° là thế điện cực tiêu chuẩn của điện cực, V
7.1. Cơ sở của phương pháp 13
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Do kết quả của phản ứng (7-2), khi cường độ dòng điện bắt đầu tăng thì nồng độ
ion kim loại ở lớp dung dịch sát bề mặt điện cực giảm. Tuy nhiên, do hiện tượng
khuếch tán, các ion kim loại ở sâu bên trong dung dịch sẽ tiến đến lớp dung dịch
ở sát bề mặt điện cực. Vì vậy cường độ dòng điện sẽ phụ thuộc tốc độ khuếch
tán, mà tốc độ khuếch tán ion lại phụ thuộc hiệu số nồng độ ở sâu bên trong
dung dịch và nồng độ CM ở sát bề mặt điện cực.
7.1. Cơ sở của phương pháp 14
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Trong thành phần dòng điện chạy qua bình điện phân, ngoài dòng điện sinh ra do
sự khuếch tán ion kim loại đến sát bề mặt điện cực và gây ra phản ứng điện cực,
người ta gọi đó là dòng khuếch tán, còn có thành phần dòng điện sinh ra do sự
dịch chuyển các ion đến các điện cực do tác dụng của điện trường dù các ion này
không tham gia phản ứng điện cực. Người ta gọi dòng điện sinh ra đơn thuần do
sự dịch chuyển các ion không tham gia quá trình điện cực là dòng dịch chuyển.
Dòng dịch chuyển cản trở việc đo thành phần dòng khuếch tán (đặc trưng cho ion
nghiên cứu) nên người ta phải loại bỏ dòng dịch chuyển khi phân tích theo
phương pháp vôn-ampe. Để giảm và đi đến loại bỏ dòng dịch chuyển, người ta có
thể đưa thêm vào dung dịch phân tích một chất điện ly trơ (không tham gia phản
ứng điện cực) có nồng độ lớn hơn nồng độ ion nghiên cứu nhiều lần. Người ta
gọi đây là chất điện ly nền. Cation của chất điện ly nền sẽ chắn tác dụng của điện
trường và làm dòng dịch chuyển thực tế bằng không.
7.1. Cơ sở của phương pháp 15
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Điện thế phân hủy của chất điện ly thực tế bằng hiệu đại số của điện thế anot và catot: E = Ea – Ek (7-5)
Khi dùng điện cực calomen làm anot thì thế anot Ea thực tế không thay đổi khi có
dòng điện nhỏ chạy qua bình điện phân. Thực vậy, quá trình anot trên calomen
chính là sự oxy hóa thủy ngân kim loại thành ion Hg+ và chuyển Hg+ vào dung dịch:
2Hg ⇋ 2Hg+ + 2e– (7-6)
Nhưng dung dịch của điện cực calomen lại có ion Cl– với nồng độ không thay đổi
(thường là dung dịch KCl bão hòa hoặc dung dịch KCl 3M) nên lập tức sẽ xuất hiện kết tủa calomen.
2Hg+ + 2Cl– ⇋ Hg2Cl2↓ (7-7)
7.1. Cơ sở của phương pháp 16
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Nồng độ ion Cl– luôn luôn không thay đổi và do đó nồng độ Hg+ không đổi và thế
điện cực Ea trong suốt quá trình điện phân không đổi, Ea = const. Nếu trong
trường hợp này ta chấp nhận Ea = 0 V vì diện tích bề mặt của anot quá lớn so với
diện tích của catot nên phân cực catot không đáng kể) thì thế bắt đầu điện phân là:
E = –Ek hay Ek = –E
Điện thế này gọi là điện thế thoát kim loại (hay thế khử) của ion kim loại trong điều
kiện đang xét. Điện thế thoát kim loại phụ thuộc vào nồng độ ion kim loại bị khử.
Nồng độ ion kim loại càng bé càng khó bị khử, thì điện áp đặt vào bình điện phân
có thể bắt đầu quá trình điện phân phải càng lớn.
7.1. Cơ sở của phương pháp 17
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Khi tăng điện thế đặt vào catot (điện thế đặt vào bình điện phân) thì nồng độ CM ở
phương trình (7-4) sẽ giảm dần, dù rằng trong quá trình điện phân luôn có các kim
loại mới ở lớp bên sâu trong dung dịch bổ sung đến sát bề mặt điện cực do hiện
tượng khuếch tán. Nhưng sẽ đến lúc ứng với điện thế E nào đó, vận tốc khử kim
loại sẽ bằng vận tốc khuếch tán và nồng độ CM ở lớp dung dịch sát bề mặt điện
cực bằng không CM = 0.
Quá trình điện phân ở đây thường xảy ra với cường độ dòng bé (thường bé hơn
10–5A) nên nồng độ dung dịch sâu bên trong của dung dịch thực tế không đổi và
bằng CM°. Cường độ dòng chạy qua bình điện phân lúc bấy giờ đạt giá trị không
đổi Id dù cho có tiếp tục tăng điện thế đặt vào bình điện phân.
Ứng dụng phương trình (7-4) với CM = 0 ta có: Id = KM× CM° (7-8)
7.1. Cơ sở của phương pháp 18
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại: Dòng I
d theo (7-8) được gọi là dòng giới hạn. Thay Id vào 7-4 ta có:
7.1. Cơ sở của phương pháp 19
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
Sự hình thành sóng cực phổ của một ion kim loại:
Việc tạo thành dòng không Faraday có thể do mấy nguyên nhân:
Khi nhún g điện cực vào dung dịch, trên bề mặt sẽ xuất hiện lớp điện kép.
Lớp điện kép có thể xem như một tụ điện, khi tụ này phóng điện sẽ tiêu
thụ một lượng điện nào đó. Khi tăng điện thế đặt vào hai điện cực, điện
dung của tụ này sẽ tăng lên. Dòng phóng điện của tụ lại tạo nên một
thành phần của dòng không Faraday gọi là dòng tụ điện. Ngoài dòng tụ
điện, dòng dịch chuyển như đã nêu ở trên cũng là thành phần dòng không Faraday.
Trong thực tế phân tích, dòng dịch chuyển có thể được loại bỏ nhờ tác
dụng của nền cực phổ là dung dịch các chất điện ly mạnh, trơ có nồng độ lớn.
Tất cả các vấn đề vừa mô tả trên đây giải thích dạng đặc biệt của đường cong I-E.
7.1. Cơ sở của phương pháp 20
7.1.2. Quá trình xảy ra trên điện cực thủy ngân
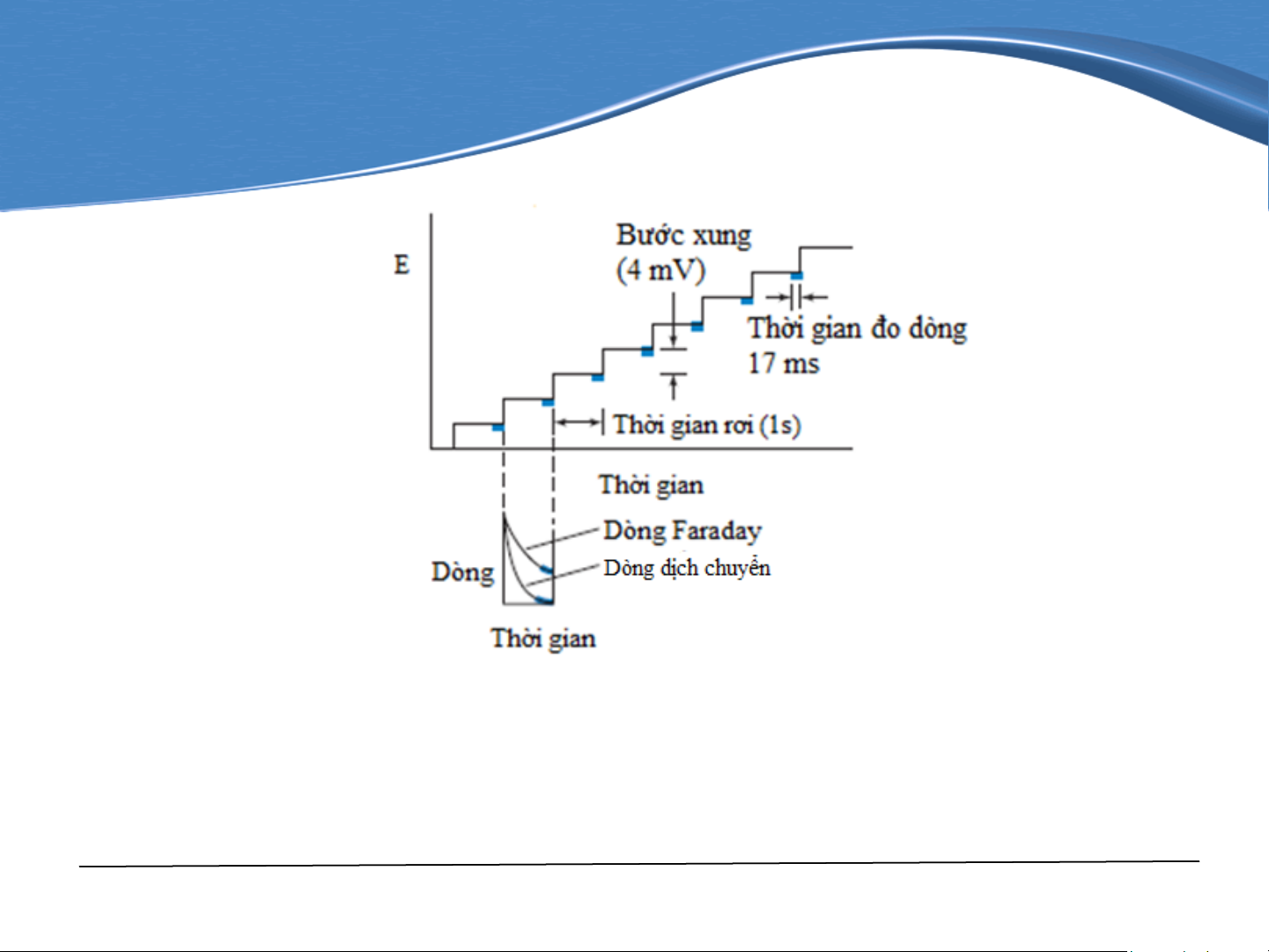
Hình 7-4. Quét thế dạng bậc thang. Dòng được đo ở
miền được tô đậm màu xanh.




