















Preview text:
12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
PHẦN 3: PHƯƠNG PHÁP TÁCH-CHIẾT
PHẦN 3: PHƯƠNG PHÁP TÁCH-CHIẾT
Chương 8: Phương pháp chiết Mở đầu
I. Chiết lỏng-lỏng (liquid – liquid extraction LLE)
8.1. Những khái niệm cơ bản
Tách là nhóm các phương pháp hóa học, vật lý và hóa lý
a. Định luật phân bố Nernst
nhằm đi từ một hỗn hợp phức tạp hỗn hợp đơn giản - Hằng số phân bố KD từng chất. A(1) ⇌ A(2) [ ] A
Tách có thể dùng để tinh chế hoặc nghiên cứu, xác định (2) K
thành phần của một hỗn hợp. D [ ] A )1 (
[A](1), [A](2) : Nồng độ chất A trong dung môi (1) và (2).
Thông thường dung môi (1) là nước, dung môi (2) là dung môi hữu cơ.
Với một hợp chất chiết xác định thì KD chỉ phụ thuộc vào nhiệt
độ và bản chất dung môi.
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 1 4
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
PHẦN 3: PHƯƠNG PHÁP TÁCH-CHIẾT
b. Hằng số phân bố điều kiện D – Hệ số phân bố
Tách hỗn hợp không đồng nhất
Hỗn hợp có ít nhất 2 pha không hòa lẫn vào nhau. Ví dụ: nhũ tương, hỗn dịch.
Khi A tồn tại ở nhiều dạng khác nhau
Lọc, ly tâm: áp dụng cho hỗn dịch
Thay đổi nhiệt độ, pH, lắng, gạn: áp dụng cho nhũ
tổng nđộ các dạng của A trong pha hữu cơ tương. D =
Tách hỗn hợp đồng nhất
tổng nđộ các dạng của A trong pha nước
- Chia cắt pha: hỗn hợp đồng nhất hỗn hợp không đồng
nhất. Ví dụ: kết tủa,…
D không phải là hằng số mà phụ thuộc vào điều kiện thực - Chuyển pha: nghiệm.
Chuyển một chất từ pha này sang pha khác: chiết, thẩm thấu, sắc ký
Biến đổi trạng thái: cất, thăng hoa
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 2 5
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
PHẦN 3: PHƯƠNG PHÁP TÁCH-CHIẾT c. Hằng số chiết Mở đầu n+ + Me + nHR MeR nH (8.1) (nc) (hc) n(hc) (nc)
Chiết là phương pháp dùng dung môi (đơn hay hỗn hợp) + n [MeR ][H ] n(hc)
để tách lấy một chất hay một nhóm các chất từ hỗn hợp K (8.2) ch n+ n [Me ][HR ] cần nghiên cứu. (nc) (hc)
Chiết là một phương pháp tách bằng chuyển pha dựa vào
sự phân bố của chất tan trong hai pha A và B. Phân loại chiết: - Chiết lỏng – lỏng
- Chiết lỏng rắn (chiết pha rắn)
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 3 6 1 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
d. Phần trăm chiết – Hiệu suất chiết
Thí dụ 1: Hệ số phân bố của I2 giữa CCl4 và H2O là 85. Tính nồng độ I2
Phần trăm chiết – E (%): là số % chất tan bị tách ra khỏi pha nước (đi vào
còn lại trong pha nước nếu ta đem 50,0ml dung dịch I2 chiết bằng CCl4
pha hữu cơ) sau 1,2,… lần chiết. theo các cách sau:
1. Chiết 1 lần bằng 50,0ml CCl4 Quan hệ giữa E và D
2. Chiết 2 lần mỗi lần bằng 25,0ml CCl 4 X .V
3. Chiết 5 lần mỗi lần bằng 10,0ml CCl hc hc E = 4 100 (8.3) X .V + X .V
Thí dụ 2: Hệ số phân bố của 1 hợp chất D=5. Giả thiết chiết 1g chất đó hc nc hc nc
ra khỏi 20ml pha nước bằng 20ml một dung môi hữu cơ. Hỏi: Chia cho X .V : hc
1. Sau lần chiết thứ nhất lượng chất còn lại là bao nhiêu? nc [X]
2. Muốn chiết được 99,9% thì phải chiết bao nhiêu lần? hc [X] D nc E 100 100 (8.4) [X] V V hc nc nc D+ [X] V V nc hc hc
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 7 10
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
d. Phần trăm chiết – Hiệu suất chiết e. Hệ số tách
Tính lượng chất tan còn lại sau lần chiết thứ nhất, thứ n và tính số lần
Nếu có 2 chất A và B cùng bị chiết bởi một dung môi, hệ số
chiết để đạt được một yêu cầu nào đó.
phân bố của A là DA, của B là DB thì khả năng tách 2 chất A và
Giả sử: w là lượng chất tan có trong V
B ra khỏi nhau được biểu diễn bởi hệ số tách .
nc (lượng chất tan ban đầu).
w1: là lượng chất tan còn lại ở pha nước sau 1 lần chiết
wn: là lượng chất tan còn lại ở pha nước sau n lần chiết D [ ] A [B] A hc hc = : (8.5) D [ ] A [B] B nc nc D w-w1 E= 100 100 Vnc w D+ Vhc D w-w = w 1 Vnc D+ Vhc
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 8 11
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH V
8.2. Phân loại các hệ chiết nc V V
Các chất có thể chiết được bằng dung môi hữu cơ: hc nc w w w 1 V
- Các chất vô cơ đơn giản có liên kết cộng hóa trị: nc D.V +V hc nc D+ V + I2, Br2, … hc + Halogenua: HgCl n
2, HgI2, GeCl4, AsBr3, SbI3, … V nc w = w
- Phức axit kim loại: HFeCl4, HSbCl6, HInBr4, HAuBr4, H2Hg(SCN)4, … n D.V +V
- Hợp chất hữu cơ ít phân ly: axit, bazơ hữu cơ yếu hc nc
- Muối nội phức (phức của ion kim loại với thuốc thử hữu cơ) - Tập hợp ion
Thông thường chia ra 2 loại hệ chiết:
- Chiết các hợp chất nội phức: Phức tạo bởi ion kim loại liên kết với ít
nhất hai nguyên tử của phân tử phối tử.
- Chiết tập hợp ion: Phức tạo bởi cation hữu cơ và các anion vô cơ như MnO - - - - - -
4 , IO4 , ClO4 , RuO4 , TeO4 , BF4 hoặc các anion phức kiểu SnCl 2- 2- 2- 6 , CdCl4 , ZnCl4 , …
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 9 12 2 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
8.3. Cơ chế chiết các ion kim loại b. Chiết liên hợp ion
a. Chiết các hợp chất nội phức a- + a- + MeX + a.Y MeX .aY
Cho ion kim loại Men+ tạo phức với phối tử R- sau đó đem chiết bằng (n+a) (n+a) dung môi hữu cơ.
cation hữu cơ tập hợp ion HR MeR (hc) n(hc) Cân bằng chiết:
Tập hợp ion (liên hợp ion) được chiết bằng dung môi hữu cơ thích hợp. hc KHR Dphức nc
Ví dụ: Chiết tetraphenylasoni perenat, phức liên hợp được chiết bằng ete + Men+ ↔ MeRn(nc) HR β (nc) ↔ H+ + R- C H As ReO C H As.ReO 6 5 4 6 5 K 4 4 4 a,HR Giả thiết: -
Dùng dư thuốc thử hữu cơ HR
-Đặc điểm: Biểu thức liên hệ giữa phần trăm chiết và các thông số thực - MeR
nghiệm thường phức tạp và khó khăn do 2 nguyên nhân:
n chủ yếu tan vào pha hữu cơ
Việc chiết các phức liên hợp ion thường được tiến hành trong dung dịch n+ + Me + nHR M eR nH (8.6)
chứa lượng lớn các chất điện ly nên có sự khác nhau khá lớn giữa nồng (nc) (hc) n(hc) (nc) độ và hoạt độ. n + n + [MeR ][H ]
Thành phần dung dịch phức tạp, nên số các phản ứng phụ tham gia vào n(hc) [H ] K D (8.7)
quá trình hình thành các phức ion liên hợp nhiều, làm cho mối quan hệ ch n+ n [Me ][HR ] [HR ] (nc) (hc) (hc)
của các thông số chiết trở nên rất phức tạp.
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 13 16
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
8.4. Các yếu tố ảnh hưởng quá trình chiết ion kim loại a.
Ảnh hưởng của nồng độ axit. Từ hệ thức (8.7) có: n [HR ] (hc) D K (8.8) ch + [H ] Từ hệ thức (8.4) có: 8 - hydroxyquinoline axetylaxeton V 1 nc D E (8.9) V 100 E
- Thuốc thử 8 – hydroxylquinoline
- Thuốc thử axetylaxeton tan tốt trong hc So sánh (8.8) và (8.9) có:
tan tốt trong rượu, benzen, clorofom,…
nước, ete, benzen, clorofom, CCl4,… n
- Thường dùng 8 – hydroxylquinoline
- Dùng axetylaxeton làm thuốc thử [HR ] (hc) V 1 nc
1,5% trong clorofom; có thể chiết
có thể chiết được hơn 60 nguyên K E (8.10) ch + [H ] V 100 E
được hơn 50 nguyên tố: Pd, Mo,
tố: Pb, Sc, Al, Th, La, Fe, Cu,… hc
W, V, Tl, Zr, Ga, In, Fe, Cu, Ti, Bi,
Lấy logarit 2 vế của hệ thức (8.10) có: Ni, … Vnc npH = lgE + lg
lg(100 E) lg K nlg[HR] (8.11) V ch hc hc
Bằng phương trình (8.11) có thể tính được pH trong pha nước cần thiết
để hiệu suất chiết đạt như ý muốn.
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 14 17
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH dithizon
- Thuốc thử dithizon tan tốt trong CCl4, clorofom,…
- Dùng dithizon có thể chiết được
Natri dietyl dithiocacbamat (DDTK)
các nguyên tố: Pd, Au, Hg, Ag, Zn,
Cd, Pb, In, Zn, Cu, Pt, Bi, Co, …
- Thuốc thử DDTK tan tốt trong nước.
- Dùng DDTK có thể chiết được các
nguyên tố: Bi, Co, Cu, Tl, Ni, Cd, Pb, …
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 15 18 3 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH MeR MeRn n (hc) 1 1 D = (hc) K D = K MeR + [Me ] [Me ] n+ D,MeRn n+ [Me ] [Me ] 1 n n+ D,MeRn n+ (nc) 1 MeR + 1 n MeR (nc) MeR n n (nc) (nc) K K D,MeRn (8.12) D,MeRn (8.18) 1 1 1 1 - n n R - R 1,n (nc) 1,n (nc) Mặt khác: Mặt khác: K [HR] K [HR] K [HR] K [HR] - a,HR (nc) a,HR (hc) [R ] = = (8.13) - a,HR (nc) a,HR (hc) [R ] = = (8.19) (nc) + + [H ] K [H ] (nc) + + [H ] K [H ] (nc) D,HR (nc) D,HR
Từ phương trình (8.12) và (8.13) có:
Từ phương trình (8.18) và (8.19) có: K K D,MeRn D (8.14) D,MeRn D (8.20) n n + 1 K [H ] + 1 K [H ] D,HR nc 1 D,HR nc 1 K [HR] K [HR] 1,n a,HR (hc) 1,n a,HR (hc)
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 19 22
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
• Thí dụ 4: Chiết một ion kim loại bằng thuốc thử là axit hữu cơ ở điều
• Thí dụ 5: Chiết thori axetylxetonat bằng benzen ở điều kiện như
kiện như sau: Ka = 5,0.10-5. KD,phức = 7104; KD,HA = 1104. ß =
sau: Ka = 1,17.10-9. KD,phức = 315; KD,thuốc thử = 5,95. ß1 = 7.107; ß1,2 =
2,51016. Tính E ở pH = 1 nếu 100,0ml ion kim loại nồng độ 1,010-6
3,8.1015; ß1,3 = 7,2.1021; ß1,4 = 7,2.1026. Tính E ở pH = 6 nếu nồng
được chiết với 10,0ml HA nồng độ 0,1 mM. Lặp lại tính toán ở pH =
độ cuối cùng của axetylaxeton trong pha hữu cơ là 10-3M; Vhc/Vnc = 3. 1/5. Đáp số:
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 20 23
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
c. Ảnh hưởng của chất tạo phức (phối tử lạ)
b. Ảnh hưởng của nồng độ tác nhân chiết (nồng độ phối tử)
Xét trường hợp trong pha nước, ngoài phức MeRn còn tồn tại các
Xét đến các dạng phức bậc thấp giữa ion kim loại với phối tử tạo phức dạng phức MX, MX2, MXk,… HR trong pha nước.
Hằng số phân bố điều kiện D: MeRn MeR (hc) n (hc) D = (8.15) D = (8.21) i=k MeR + MeX n i MeR i=n-1 + MeR (nc) (nc) n i (nc) (nc) i=0 i=0
Tương tự phương trình 8.20 ta cũng có: i=n-1 in MeR 1 n+ -
[Me ](1 [R ]i) (8.16) i 1, (nc) i K i=0 i 1 D,MeRn D (8.22) n Đặt: + 1 K [H ] D,HR nc 1 in 1 1 K [HR] - 1 [R ]i (8.17) 1,n a,HR (hc) 1,i i 1 Trong đó: 1 ik - 1 [X ]i (8.23) 1,k i 1
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 21 24 4 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
• Thí dụ 6: Chiết Cu2+ 10-4M bằng dithizon được hòa tan trong CCl4
• Thí dụ 7: Hằng số phân bố KD của axit yếu HA giữa pha nước và
có mặt EDTA 10-2M. Tính hằng số phân bố điều kiện D ở pH=2.
dietylete là 800. Hằng số phân ly axit Ka=1,5.10-5. Tính nồng độ axit Biết:
HA còn lại trong pha nước nếu ta lấy 50,0ml axit HA 0,050M chiết
Hằng số bền của phức Cu2+ và EDTA là 1018,8; K
bằng 25,0ml dietylete ở pH=2,0. a = 3.10-5. KD,phức =
7.104; KD, thuốc thử = 1,1.104; β = 5.1022.
Đáp số: [HA]nc = 1,25.10-4M.
• Thí dụ 8: Hằng số phân bố KD của axit yếu HA giữa pha nước và
hexan là 3. Hằng số phân ly axit Ka=1,0.10-5. Tính % chiết nếu ta lấy
50,0ml axit HA 0,025M chiết bằng 50,0ml hexan ở pH=3,0. Lặp lại với pH = 5,0 và pH = 7,0.
• Thí dụ 9: Hằng số phân bố KD của bazơ yếu B giữa pha nước và
pha hữu cơ là 5. Hằng số bazơ Kb=1,0.10-4. Tính % chiết nếu ta lấy
25,0ml bazơ B 0,025M chiết bằng 50,0ml dung môi hữu cơ ở pH=9,0.
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 25 28
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
d. Hiệu ứng muối (hiệu ứng cường chiết) 8.6. Kỹ thuật chiết
• Hiệu ứng muối là hiệu ứng tăng phần trăm chiết của nguyên tố cần 8.6.1. Phương pháp chiết
chiết bằng cách thêm vào dung dịch chiết các chất điện ly mạnh.
• Chiết gián đoạn: sau 1 lần chiết, tách
• Thêm vào hệ chiết dung dịch chất điện ly mạnh sẽ làm tăng hằng số
lấy pha hữu cơ rồi lại thêm dung môi phân bố điều kiện.
hữu cơ vào pha nước, lặp đi lặp lại
• Khi thêm muối (NaCl, KCl, CaCl2, CH3COONa…) vào hệ chiết lỏng-
thao tác này nhiều lần cho đến khi đạt
lỏng thì cân bằng lỏng-lỏng trong dung dịch bị thay đổi do lực ion yêu cầu về tách tăng.
Trong trường hợp hệ số phân bố bé thì
• Các ion sẽ bị solvat hóa (hidrat hóa), làm cho các hợp chất hữu cơ
cách chiết gián đoạn sẽ khó khăn và mất
bị tách ra khỏi pha nước. Do đó tăng hiệu quả của quá trình chiết. thời gian.
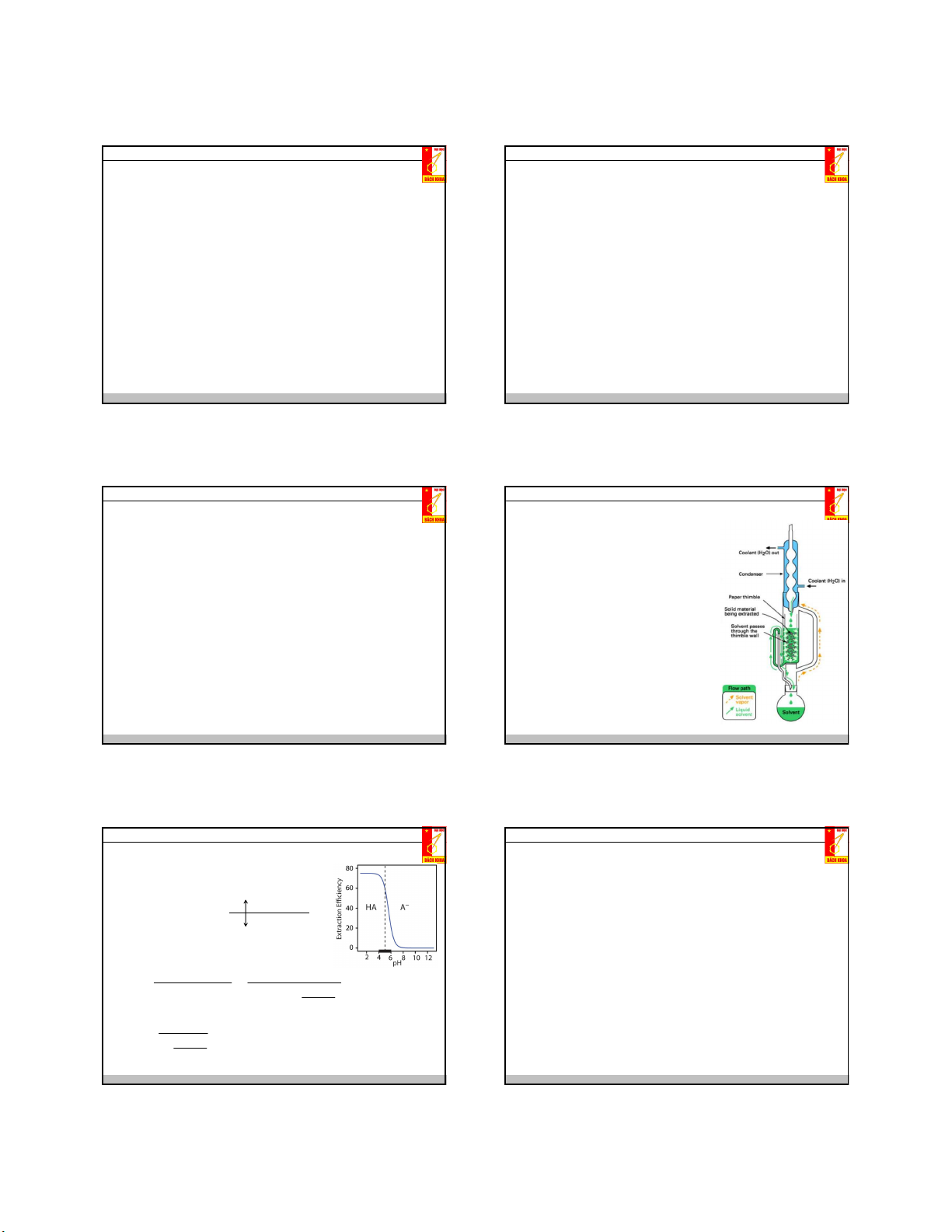
• Chiết liên tục: chiết Soxhlet
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 26 29
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
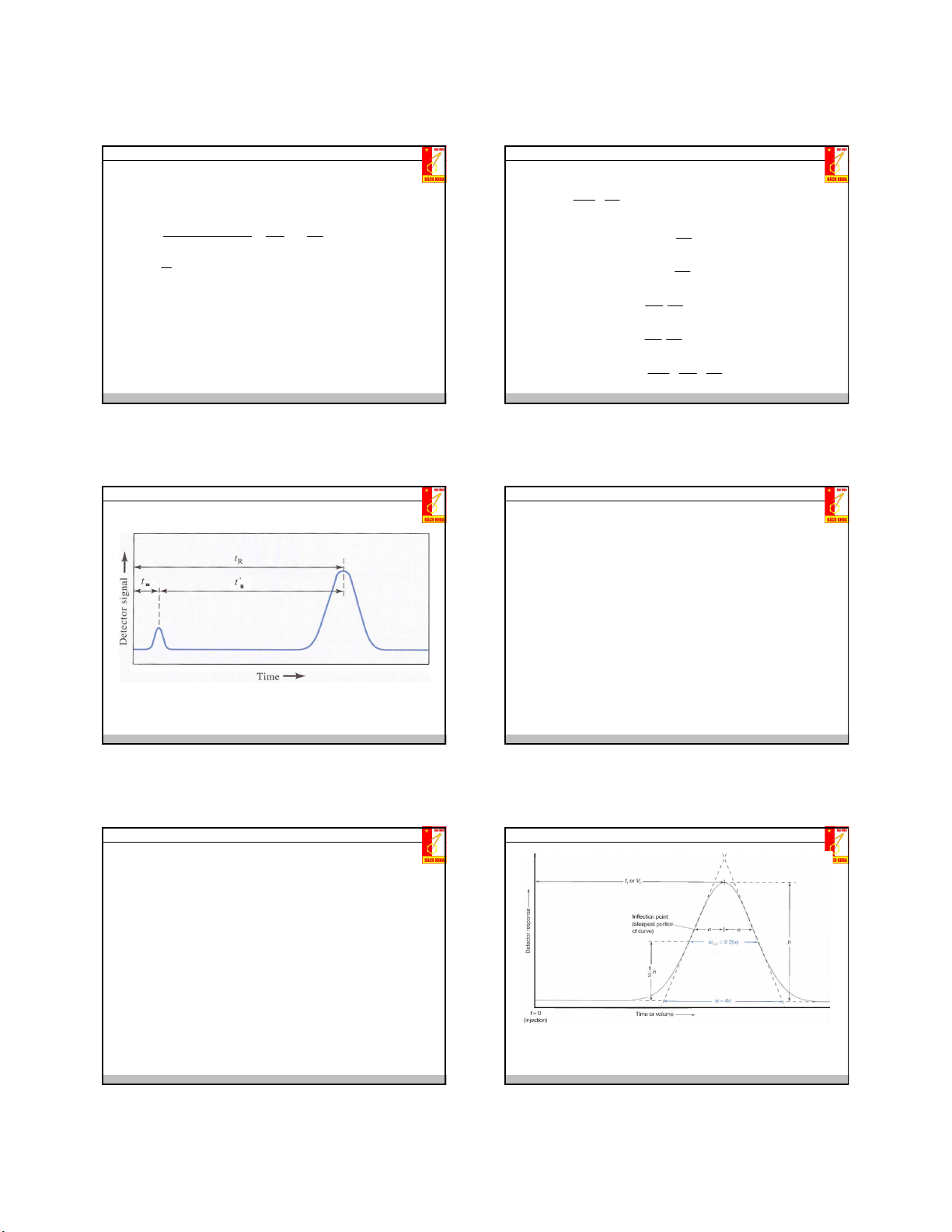
8.5. Cân bằng chiết một axit hữu cơ 8.6. Kỹ thuật chiết
Axit HR không phân ly trong pha hữu cơ 8.6.2. Chọn dung môi Cân bằng chiết: HA
• Chọn dung môi sao cho hệ số phân bố của chất tan lớn. (hc) hc K
• Chú ý đến độ nhớt, tỷ trọng, mức độ tan lẫn vào nhau giữa 2 pha HA nc
• Chọn dung môi sao cho quá trình giải chiết sau này dễ dàng HA(nc) ↔ H+ + A- Ka,HA [HA] [HA] (hc) (hc) D = (8.24) HA - [HA] [A ] Ka (nc) (nc) [HA] (1 ) (nc) [H ](nc) K D HR (8.25) HA Ka 1 [H](nc)
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 27 30 5 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH 8.6. Kỹ thuật chiết
PHẦN 3: PHƯƠNG PHÁP TÁCH-CHIẾT 8.6.3. Chất trợ chiết
Chương 8: Phương pháp chiết
• Là các chất điện ly làm tăng khả năng chiết
II. Chiết pha rắn (solid phase extraction – SPE)
• Chất trợ chiết thường dùng với nồng độ cao, gây trở ngại cho việc
- Mẫu ở trạng thái lỏng được lọc qua một lớp chất rắn
xử lý pha nước sau này, do đó phải chọn loại muối có thể dễ dàng
loại bỏ khỏi dung dịch khi cần (VD muối amoni,...)
(chất chiết) có khả năng hấp phụ: hạt nhỏ, xốp đk 25 – 70 m.
- Các chất quan tâm sẽ dịch chuyển theo những tốc độ
khác nhau và phân bố trên bề mặt chất hấp phụ.
- Mỗi chất sẽ được rửa giải ra khỏi bề mặt chất hấp phụ bằng dung môi rửa giải
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 31 34
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH 8.6. Kỹ thuật chiết
PHẦN 3: PHƯƠNG PHÁP TÁCH-CHIẾT 8.6.4. Rửa phần chiết
Chương 8: Phương pháp chiết
• Sau khi tách, trong phần chiết không tránh khỏi có lẫn tạp chất, do II. Chiết pha rắn
đó cần rửa phần chiết (thường là lắc với dung dịch nước có chất trợ chiết, pH, ... thích hợp) 8.7. Cột chiết pha rắn
Cột tách chiết pha rắn có cấu trúc theo nhiều dạng:
- Dạng cột nhồi sẵn: đây là dạng được sử dụng phổ biến nhất.
cột 61 cm hay dung lượng chiết 100 – 600 mg
- Dạng phiến, đĩa: dày 1-2 mm, đk 3-4 cm - Dạng sợi
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 32 35
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH 8.6. Kỹ thuật chiết II. Chiết pha rắn 8.6.5. Giải chiết 8.7. Cột chiết pha rắn
• Khi cần tiến hành tiếp các quá trình phân tích với chất đã chiết được
Phân loại cột tách theo cơ chế chiết SPE: nhưng trong pha nước.
- Cơ chế tương tác hấp phụ của chất rắn
• Giải chiết tức là chuyển chất đã tách được từ pha hữu cơ sang pha
+ Cột pha thuận (Normal Phase - NP): silica trung tính và nhôm oxit nước.
+ Cột pha đảo (Revered Phase - RP): silica thường được alkyl hóa
nhóm –OH bằng nhóm –C8, C18,…
• Thường dùng các dung dịch thích hợp như dung dịch axit mạnh,
Được sử dụng nhiều nhất dùng để phân tích các chất không phân
làm bay hơi dung môi sau đó hòa tan bã bằng nước,...
cực và phân cực vừa (pha động sử dụng là chất phân cực)
- Cơ chế trao đổi ion (Cationit/Anionit): ví dụ chiết các cation kim loại và anion
+ Cột cation, anion, cặp ion
- Cơ chế liên hợp phân tử: thêm một thuốc thử tạo
phức liên hợp với chất phân tích có trong mẫu
phân tích để có được phức liên hợp phân tử
- Rây: sàng lọc phân tử theo kích thước
- Hấp phụ khí (purge and trap extraction)
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 33 36 6 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH II. Chiết pha rắn II. Chiết pha rắn
8.8. Các bước tiến hành SPE
8.10. Ưu điểm của SPE so với LLE
- Bước 1: Hoạt hóa cột chiết - Tiêu tốn ít dung môi
- Bước 2: Đưa mẫu lên cột - Tiêu tốn ít thời gian
- Bước 3: Rửa cột để loại các chất cản trở (hoặc rửa - Cho nền mẫu sạch
giải cấu tử cần quan tâm nếu như chất cản trở bị lưu
- Dễ dàng trong việc tự động hóa
giữ mạnh hơn nằm lại trên cột). - Ít bị nhiễm bẩn
- Bước 4: Rửa giải các cấu tử quan tâm nếu chúng bị - Cho độ thu hồi cao
lưu giữ mạnh hơn các chất cản trở đã được rửa giải
- Sử dụng cho nhiều chất phân tích khác nhau trong một ra ở bước trên. lần tách chiết.
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017 37 40
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH II. Chiết pha rắn
Chương 9: Phương pháp tách sắc ký 8.9. Ứng dụng •
Sắc ký là phương pháp tách chất dựa vào sự phân bố khác nhau của
- Làm sạch mẫu: ống pha rắn được xem như là “một ống
chúng giữa 2 pha, pha động và pha tĩnh.
lọc hoá học”, nó lưu trữ các cấu tử cần quan tâm, còn các
cấu tử khác được rửa ra, hoặc ngược lại các cấu tử quan
tâm bị rửa ra còn các cấu tử cản trở bị lưu giữ lại.
- Làm giàu mẫu: ống pha rắn được sử dụng để tập trung
chất phân tích từ những dung dịch rất loãng (lượng vết).
Sự làm giàu lượng vết đặc biệt có lợi khi nồng độ chất
phân tích nằm dưới giới hạn xác định của phương pháp.
- Phân đoạn các cấu tử: Dùng các dung môi rửa giải có ái
lực khác nhau để rửa giải các hợp chất có độ phân cực
khác nhau ra thành các phân đoạn. Sự phân đoạn có lợi
khi ta muốn phân tích những cấu tử khác nhau của cùng một mẫu phân tích
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 38 41
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH II. Chiết pha rắn
Chương 9: Phương pháp tách sắc ký 8.9. Ứng dụng
9.1. Phân loại: các dạng sắc ký cơ bản Cách bố trí pha
- Phân tích các dư lượng thuốc BVTV và thuốc kháng sinh Dạng sắc ký Pha động Pha tĩnh Cơ chế phân tách tĩnh trong thực phẩm. Khí
- Chiết pha rắn cho các mẫu nước. Khí – hấp phụ khí rắn cột hấp phụ Khí – lỏng khí lỏng cột phân bố
- Phân tích các loại thuốc trong mẫu sinh học, … Lỏng Lỏng – rắn lỏng rắn cột hấp phụ Lỏng – lỏng lỏng lỏng cột phân bố Lỏng – nhựa trao đổi lỏng rắn cột trao đổi ion Lớp mỏng (bản mỏng) lỏng rắn lớp mỏng hấp phụ lỏng lỏng lớp mỏng phân bố Điện di lỏng rắn cột
sự di chuyển của cấu tử mang
điện trong điện trường Giấy lỏng lỏng giấy sắc ký phân bố Rây (sắc ký gel) Lỏng lỏng Cột theo KT phân tử
Nguyễn Xuân Trường Phương pháp tách - chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 39 42 7 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 9: Phương pháp tách sắc ký
Chương 9: Phương pháp tách sắc ký
9.1.1. Phân loại dựa trên hình dạng pha tĩnh
9.2. Những đại lượng cơ bản của phương pháp tách sắc ký
- Sắc ký trên giấy: pha tĩnh thường là nước được giữ trong sợi xenlulo a. Hệ số phân bố K của tờ giấy
D và sự di chuyển các chất phân tích
- Sắc ký lớp mỏng (bản mỏng): pha tĩnh là chất hấp phụ được hòa thành A A s m
nhũ dịch sau đó trải lên phiến kính thành một lớp mỏng, rồi sấy khô để A hoạt hóa. s K D
- Sắc ký cột: Chất liệu làm pha tĩnh được nhồi vào cột. Tùy loại chất liệu Am
tạo cột mà có tất cả các loại sắc ký theo nguyên lý (hấp phụ, phân bố,
trao đổi ion, rây phân tử). Ngoài ra tùy áp lực trên cột trong quá trình sắc
[A]m: Nồng độ chất A trong pha động ký mà phân chia thành:
[A]s: Nồng độ chất A trong pha tĩnh
+ Sắc ký cột mở: Cột thủy tinh làm sắc ký không có khả năng chịu lực.
Áp lực trên cột là áp suất thường.
+ Sắc ký lỏng cao áp (HPLC): Cột sắc ký được làm bằng thủy tinh hoặc
bằng thép chịu lực. Pha động được bơm vào cột với áp lực cao trong hệ thống sắc ký kín.
+ Sắc ký cột mao quản: sắc ký khí, sắc ký điện di, …
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 43 46
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 9: Phương pháp tách sắc ký
b. Sự liên hệ giữa tốc độ di chuyển của chất tan và K
9.1.2. Phân loại dựa trên đặc tính pha tĩnh (cơ chế của D quá trình phân tách) Số mmol A trong pha động
- Sắc ký hấp phụ: sự phân tách các chất là do ái lực khác f =
nhau của chất phân tách đối với chất hấp phụ là chất rắn
Tổng số mmol A trong toàn cột (pha cố định).
- Sắc ký trao đổi ion: sự phân tách các ion là do các ion có
f: tỷ lệ thời gian trong pha động
ái lực khác nhau với các trung tâm trao đổi ion (nhóm A .Vm m f =
chứa ion) trên chất rắn là pha cố định. Các chất trao đổi A .V + A .V m s m s
ion thông thường nhất là các nhựa trao đổi ion.
- Sắc ký phân bố: Các chất được phân tách dựa trên sự
Vm, Vs: thể tích của pha động và pha tĩnh tương ứng.
phân bố khác nhau của mỗi chất hòa tan vào 2 pha lỏng
Chia cả tử số và mẫu số cho [A]m.Vm
không trộn lẫn (hoặc pha khí – pha lỏng). Mỗi chất có hệ 1 1 f = =
số phân bố riêng trong một hệ dung môi nhất định. ' Vs 1 + k 1 + K . D Vm
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 44 47
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 9: Phương pháp tách sắc ký V ' s (k = K
, gọi là thừa số dung tích) D
9.1.2. Phân loại dựa trên đặc tính pha tĩnh (cơ chế của quá trình Vm phân tách) 1 U.
- Sắc ký lọc gel: các chất được phân tách trên cơ sở kích thước và hình Vận tốc UA = U.f = (cm/s) ' 1+k
dạng của các phân tử trong mẫu phân tích. Những phân tử lớn của
pha lỏng không qua được các lỗ gel nên di chuyển qua các chỗ trống, ' (k 0 nên f 1 và U U)
đường đi ngắn hơn nên di chuyển nhanh, ra khỏi cột trước. Các phân A
tử nhỏ chui qua các lỗ của hạt gel, đường đi vòng vèo, dài hơn nên di chuyển chậm.
Nhận xét: Khi KD hoặc k' càng lớn thì thời gian chất tan ở pha
- Sắc ký ái lực: Giá thể là chất giá có phân tử lớn, trơ, trên đó gắn một
động càng ít, nói cách khác là chất tan di chuyển càng chậm.
chất ái lực sinh học đặc hiệu với một loại cấu tử hòa tan của mẫu
phân tích. Tương tác đặc hiệu sinh học thường là các phản ứng kiểu
enzym- cơ chất, kháng nguyên- kháng thể.
- Sắc ký điện di: các chất (cấu tử mang điện) được phân tách dựa trên
tốc độ di chuyển khác nhau của chúng (do kích thước và điện tích)
trong điện trường thế cao (5 - 30 kV). Cột mao quản thường dùng là silica, teflon, …
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 45 48 8 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH e. Hệ số tách α
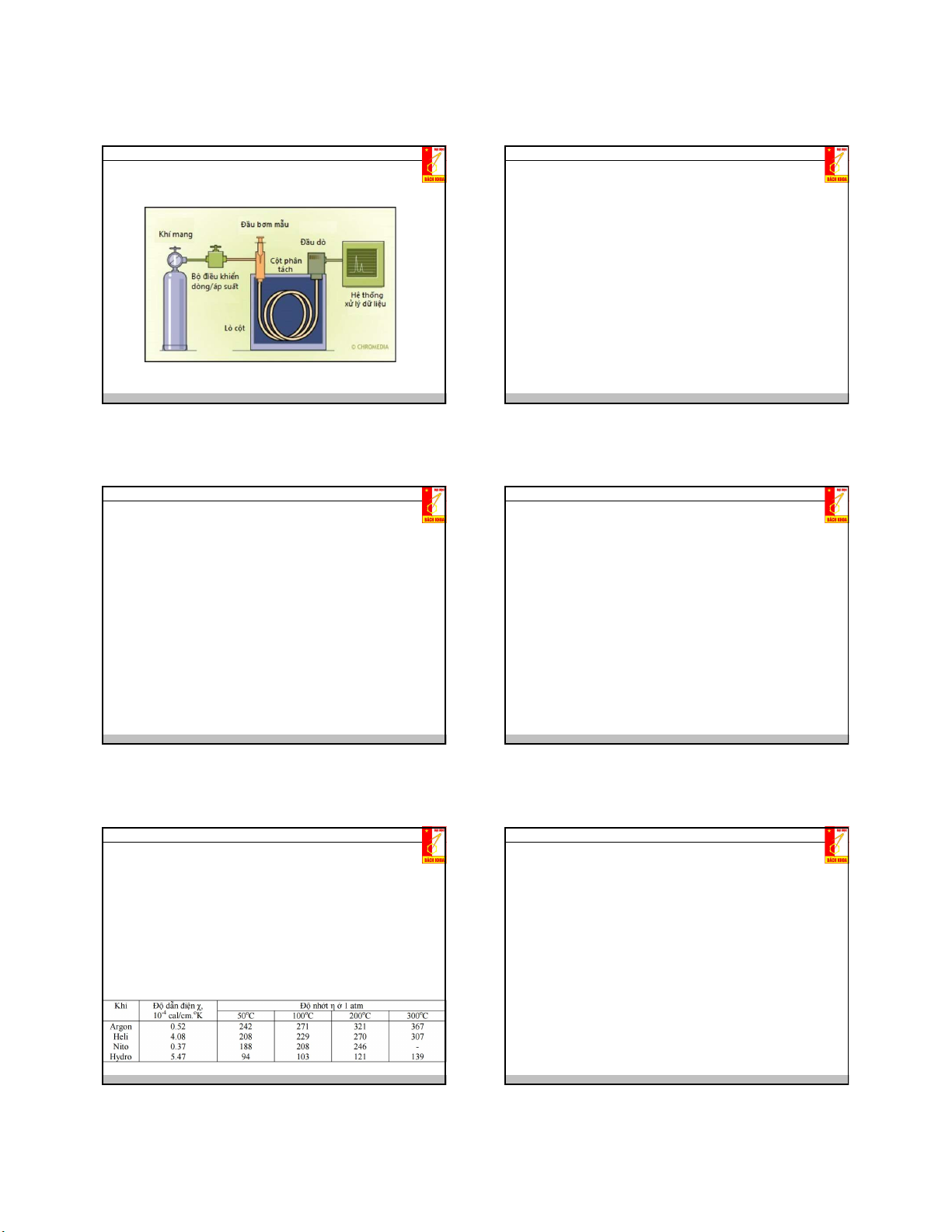
c. Thời gian lưu tr và thời gian lưu hiệu chỉnh t’r K k
Thời gian lưu là thời gian tính từ lúc bắt đầu bơm mẫu vào đầu cột tới khi pic DA A' α= =
đạt giá trị cực đại. K k DB B' chiều dài cột (cm) L L V t s rA = = = (1+k’A) Mặt khác: t' =t .K . vận tốc của A (cm/s) U RA m DA A U Vm L t =
là thời gian cấu tử không lưu giữ trên cột, còn gọi là thời gian chết. V m s U t' =t .K . RB m DB V t m rA = tm (1 + k’A ) t' V RA m
Thời gian lưu hiệu chỉnh: t’ K = . rA = trA - tm DA t V m s t' V RB m K = . DB t V m s K t' k' DA RA A α= = = K t' k' DB RB B
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 49 52
Bộ môn Hóa phân tích – Viện KTHH
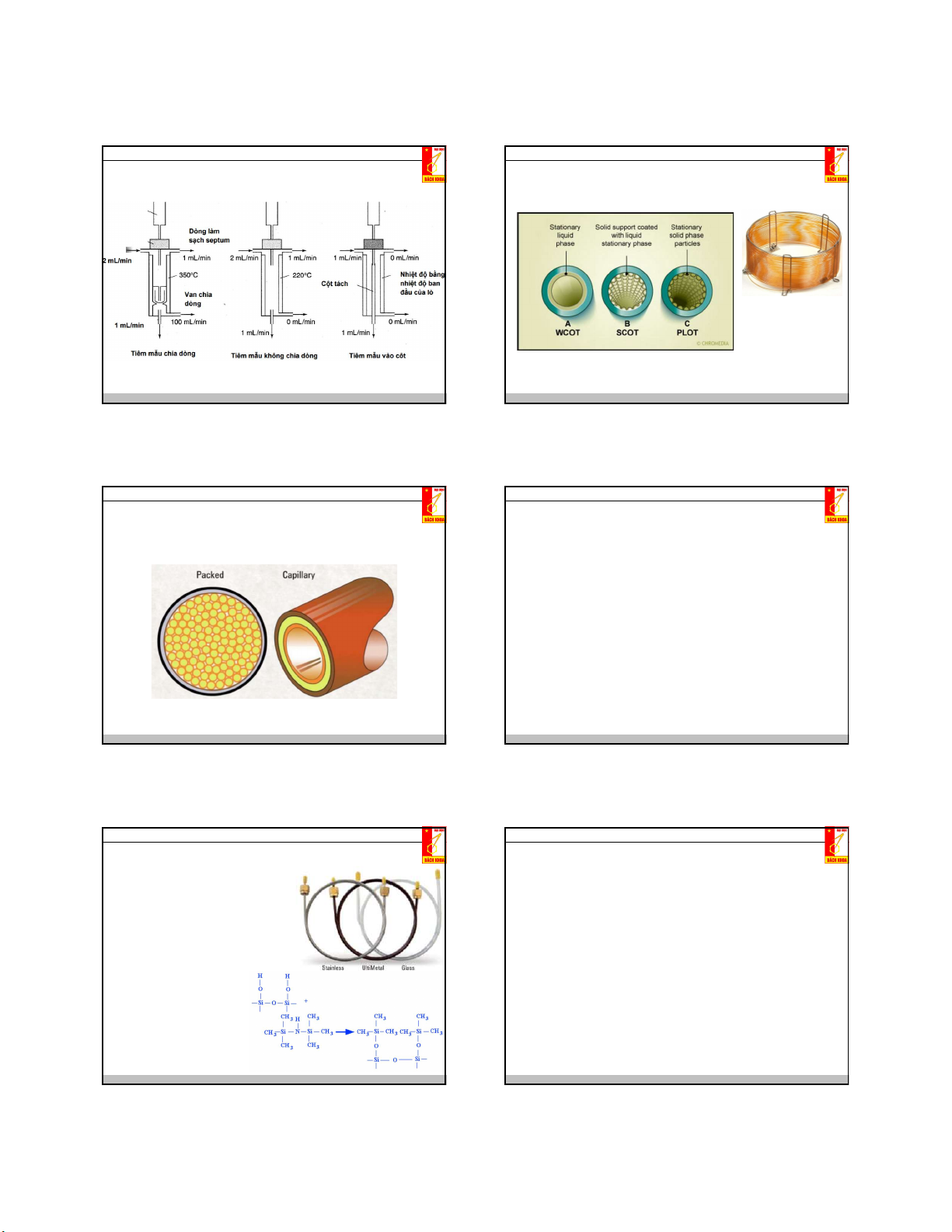
Bộ môn Hóa phân tích – Viện KTHH g. Pic sắc ký (sắc đồ)
Diện tích nằm dưới đường cong của A biểu thị tích phân v2 Diện tích = Adv = mmol A 1 vt2 Diện tích = Sdt.mmol=R .mmolA A 1 t
(S tín hiệu của detetor như hàm số của thời gian)
RA: tín hiệu ứng với chất phân tích A (số của giấy đồ thị đối với mỗi mmol của A).
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 50 53
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
d. Thể tích lưu VR và thể tích lưu hiệu chỉnh V’R VRA = tRA.F VRA là thể tích lưu
F là tốc độ chảy của pha động, ml/s Vm = tm .F
Vm là thể tích trống của cột (bất kỳ thể tích nào trong cột mà
không bị pha tĩnh chiếm sẽ bị pha động chiếm).
V’RA = VRA - Vm = tm (1+k’A ).F – Vm = Vm .k’A = Vm . KDA . Vs /Vm = KDA .Vs Vg = V’RA/VS = KDA
Vg là thể tích lưu riêng hay thể tích đặc trưng riêng cho cấu tử
(thể tích dung dịch rửa giải để rửa chất phân tích trong 1 đơn vị
thể tích hay trọng lượng của pha tĩnh) W: độ rộng đáy pic
V’RA = VRA – Vm = (tRA – tm)F = t’RA.F
W1/2: độ rộng đáy pic đo ở nửa độ cao
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 51 54 9 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
9.3. Sự giãn rộng vùng mẫu, phương trình van Deemter b. Độ phân giải R a. Lý thuyết đĩa
R=1: Hai cấu tử A và B tách khỏi nhau đạt 95%
Đĩa lý thuyết và cách xác định số đĩa lý thuyết bằng TN
R=1,5: Hai cấu tử A và B tách khỏi nhau đạt 99,8%
Gọi n là số đĩa lý thuyết, σ là độ lệch chuẩn (đại lượng đặc trưng cho độ rộng
Giá trị R=1,5 thì gọi là độ phân giải đường nền. của pic): T Đ σ n K K
Nếu tính theo hệ số phân bố thì R ~ D , 2 D , 1 , trong đó K n D,2 > KD,1 K
Mặt khác, thời gian lưu t D,2 R ~ n nên: t n t n +1
Như vậy, R phụ thuộc vào độ chênh lệch tương đối giữa hai hệ số R R 2 hay n ( ) phân bố. n
Thông thường chiều ngang W được đo bằng thực nghiệm và W = 4σ 2 2 2 t t t R n 16. R 5,54. R W / 4 W W 1/2
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 55 58
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chiều cao đĩa lý thuyết H L H= (cm) n
Gọi neff là số đĩa lý thuyết hiệu dụng: 2 2 2 t -t t' t .k' R m R m n =16 =16. =16. eff W W W 2 2 2 t t k' k' R R t = n =16. . =n. m eff 2 1+k' W 1+k'2 k'+1
Chiều cao đĩa lý thuyết hiệu dụng: L H = eff neff
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 56 59
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH b. Độ phân giải R Thí dụ 1: 2t -t
Hai chất tan A và B được tách bằng sắc ký với các thông số sau: RB RA R= W +W
chiều dài cột L= 3.2m, tRA = 280s, tRB = 300s, wA = 15s, wB = 14s, tm = A B 10s. Tính:
1.Tính số đĩa lý thuyết, chiều cao đĩa lý thuyết
tRB – tRA = ΔtR (ΔZ) là sự chênh lệch về thời gian lưu (cũng có thể dùng
2.Tính số đĩa lý thuyết hiệu dụng, chiều cao đĩa lý thuyết hiệu dụng
thể tích lưu ΔVR = VRB – VRA)
3.Tính độ phân giải R của phép tách sắc ký
4.Tính độ phân giải nếu thay cột có chiều dài là 400cm.
½(WA + WB) là tổng bán chiều rộng pic đo bằng giây hoặc ml t ~ n R tR ~ n hay R ~ n W ( ) ~ n W
Nhận xét: Phương pháp tăng độ phân giải sẽ đơn giản là dùng cột dài hơn.
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 57 60 10 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH c. Lý thuyết động học H = H1 + H2 + H3
- H1 là đại lượng khuếch tán xoáy, đặc trưng cho độ đồng
đều cả hạt nhồi, đường kính hạt nhồi, khả năng nạp cột. H =2λ.d 1 p
λ là hệ số nạp cột, nếu nạp cột tốt nó có giá trị bằng 1,5
dp là đường kính hạt nhồi (cm)
- H2 là đại lượng khuếch tán theo chiều dọc. H2 = B/U
B = 2γ.Dm là đại lượng đặc trưng cho hệ số khuếch tán của chất tan
trong pha động và hệ số đường đi của nó. H2 = 2γ.Dm /U
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 61 64
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Xét cực tiểu của chiều cao đĩa lý thuyết:
- H3 là đại lượng đặc trưng cho quá trình chuyển khối lượng. B H A C.U H3 = (Cs + Cm).U U Trong đó: B B 2 H ' (theoU ) C 0 U + k.df C = 2 opt U C s Ds H A 2 BC min k: hệ số
Thí dụ 2: Một phép sắc ký sử dụng cột dài 36m, chạy đơn chất chuẩn ở
Ds: hệ số khuếch tán của chất tan trong pha tĩnh (cm2s-1) 3 TN như sau:
df : chiều dày pha tĩnh (cm) TN U (cm/s) tR (s) W (s) 2 β.d 1 10 300 20 + p C = 2 20 250 16 m Dm 3 30 150 10
β: hệ số thực nghiệm, có giá trị từ 0,5 – 1
Dm: hệ số khuếch tán của chất tan trong pha động (cm2s-1)
Xác định vận tốc tối ưu, số đĩa lý thuyết, chiều cao đĩa lý thuyết cho cột
khi vận hành ở vận tốc tối ưu đó.
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 62 65
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
9.4. Phân tích bằng phương pháp tách sắc ký
Tổng hợp lại, H có biểu thức tổng quát là: a. Phân tích định tính 2 2 2γ.D K.d d p m f H = 2λd + + +β. .U
Dựa vào đại lượng đặc trưng thời gian lưu giữ t p U D D Ri của các s m
chất. tRi đặc trưng cho mỗi chất tan Xi trong một hệ pha xác
Vậy, chiều cao tương đương của đĩa lý thuyết phụ thuộc định.
vận tốc dòng của pha động U được mô tả bằng phương Nguyên tắc: trình van Deemter. B
- Chạy sắc ký và ghi sắc đồ của bộ mẫu chuẩn, xác định thời H=A+ +C.U gian lưu t U
Ri của từng chất chuẩn.
- Sau đó chạy sắc ký của mẫu phân tích và xác định thời A=H1
gian lưu của từng pic sắc ký trong sắc ký đồ của mẫu phân B=2.γ.Dm tích. C=C +C s m
- So sánh thời gian lưu của các pic sắc ký có trong bộ mẫu
chuẩn với sắc ký đồ của mẫu phân tích. Nếu có bộ thư viện
chất chuẩn thì càng dễ dàng.
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017 63 66 11 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
9.4. Phân tích bằng phương pháp tách sắc ký
Chương 10: Phương pháp sắc ký lỏng
b. Phân tích định lượng
10.1. Giới thiệu kỹ thuật sắc ký lỏng
Dựa vào đại lượng diện tích (S) hoặc chiều (H) cao pic sắc
- Phương pháp tách sắc ký dựa vào sự hấp phụ và giải ký:
hấp phụ xảy ra liên tục hoặc sự phân bố của chất giữa 2 H = k.C b b pha: x hoặc S = k.Cx Trong đó:
+ Pha tĩnh là chất rắn hoặc chất lỏng: lưu giữ chất phân
k là hằng số của điều kiện thực nghiệm; tích.
b- hằng số bản chất, 0 + Pha động là chất lỏng (một hoặc hỗn hợp nhiều chất):
hòa tan và di chuyển chất phân tích.
- Phương pháp ngoại chuẩn: đường chuẩn, thêm chuẩn, …
- Phương pháp nội chuẩn:
+ Để định lượng một cấu tử X cần phải chọn một chất chuẩn S
sao cho: pic của X và S tách rời nhau và gần nhau.
+ Tiến hành pha các hỗn hợp có tỷ lệ về lượng X và S biết trước
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 67 70
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
9.4. Phân tích bằng phương pháp tách sắc ký
Chương 10: Phương pháp sắc ký lỏng
b. Phân tích định lượng 10.2. Phân loại
- Phương pháp nội chuẩn:
- Sắc ký lỏng áp suất thường (sắc ký cổ điển)
+ Chạy sắc ký đo diện tích các pic, lập tỷ số diện tích tương ứng,
- Sắc ký lỏng áp suất cao (sắc ký lỏng hiệu năng cao –
rồi lập đường chuẩn tương đối. HPLC)
Dựa trên trạng thái pha tĩnh
- Lỏng: Sắc ký lỏng – lỏng (LLC)
- Rắn: sắc ký lỏng – rắn (LSC)
Dựa vào bản chất của quá trình sắc ký - SK phân bố - SK pha thường (NP) + S - SK pha đảo (RP)
c/Ss và Wc/Ws tương ứng là tỷ lệ diện tích và tỷ lệ về lượng
của cặp cấu tử cần xác định X và chuẩn nội S. - SK trao đổi ion (IE) - SK ghép cặp ion (IP)
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 68 71
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
9.4. Phân tích bằng phương pháp tách sắc ký
Chương 10: Phương pháp sắc ký lỏng
10.3. Nguyên tắc của hệ thống máy HPLC
c. Phân tích bán định lượng
Coi tổng diện tích của tất cả các pic sắc ký của các chất có trong mẫu là 100 %:
Stot = S1 + S2 + …+ Sn = 100 %
Từ đó tính được % của các chất có trong mẫu phân tích.
Ưu điểm: nhanh và không cần có dãy mẫu chuẩn. Hạn chế:
- Trong mẫu có những chất mà detector không phát hiện được.
- Đã coi giới hạn phát hiện LOD của các chất là như nhau.
Nguyễn Xuân Trường Phương pháp tách chiết 04/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 69 72 12 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 10: Phương pháp sắc ký lỏng 10.3.1. Bình chứa dung môi 10.3.3. Van bơm mẫu
- Cần lọc dung môi qua màng lọc 0.45 µm trước khi sử + Kiểu bơm mẫu bằng tay
dụng. Đầu của ống nhựa trong bình chứa dung môi cần + Kiểu bơm tự động phải có đầu lọc.
- Cần loại bỏ không khí hòa tan hoặc các bọt không khí
trong dung môi vì khí hòa tan có thể làm biến dạng các pic
và làm nhiễu đường nền. Loại bỏ bằng cách chạy siêu âm,
hoặc sục khí trơ như Ar, N2, …
- Rửa giải với hệ dung môi hoặc rửa giải gradient thường
dùng 2, 3 hoặc 4 bình dung môi khác nhau và là hỗn hợp
của các loại dung môi trên được trộn với tỷ lệ biến đổi theo
chương trình lập trước.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 73 76
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 10: Phương pháp sắc ký lỏng 10.3.2. Bơm cao áp 10.3.4. Cột tách
- Bơm pha động vào cột tách
- Cột được làm bằng vật liệu thép không rỉ (thép Cr-Ni-Mo) với
- Điều khiển tốc độ dòng, áp suất của pha động
mặt trong của cột được làm nhẵn.
+ Cột tách có thể chịu đến 200 bar nhưng thường chỉ sử dụng áp - Kích thước phổ biến:
suất trong cột khoảng 20 đến 100 bar. Áp suất trong cột phụ
+ ĐK ngoài bằng 6.35 mm (1/4 in.)
thuộc vào chiều dài cột, kích thước hạt của pha tĩnh, độ nhớt và + ĐK trong 4.6 mm
tốc độ dòng của pha động. + Chiều dài: 10 - 25 cm.
+ Bơm không bị ảnh hưởng bởi bất kỳ loại dung môi nào:
- Cột được nhồi các hạt có đk 3,4,5,10 µm.
Bơm tốc độ dòng hằng định (constant flow pump): bơm
Chất nhồi trong cột thường là silicagen
kiểu syringe đẩy dung môi liên tục, khi hết dung môi trong ống
hoặc silicagen có bọc hoặc gắn hóa học
bơm (khoảng 250 ml) thì dừng lại để nạp lại.
một màng mỏng chất hữu cơ. Ngoài ra còn dùng Al2O3, hạt
Bơm kiểu piston thì đẩy hút luân phiên. Loại này được
polime xốp, hạt chất trao đổi ion.
dùng phổ biến vì có nhiều ưu điểm
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 74 77
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 10: Phương pháp sắc ký lỏng 10.3.3. Van bơm mẫu 10.3.4. Detector
- Dùng van tiêm mẫu có một vòng mẫu (sample loop) có dung - UV-Vis
tích khác nhau từ 5 đến 500 µl. - Huỳnh quang
- Mẫu được bơm bằng xilanh vào vòng mẫu. Sau đó chuyển van - Đo độ dẫn
từ vị trí nạp mẫu (load) đến vị trí tiêm mẫu (inject ) nối vòng mẫu - Đo chỉ số khúc xạ
với dòng chảy của pha động. Một lượng mẫu chính xác trong - Khối phổ
vòng mẫu sẽ được vận chuyển vào cột tách.
10.3.5. Bộ ghi và phần mềm xử lý tín hiệu
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 75 78 13 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 10: Phương pháp sắc ký lỏng
10.4. Quá trình tách trong sắc ký lỏng
10.5. Phương pháp tiến hành sắc ký
Quá trình tách phụ thuộc vào 3 tương tác chính:
10.5.3. Phương pháp thế đẩy
+ Sự tương tác và cân bằng của chất phân tích với pha tĩnh
+ Mẫu được cho vào cột, dùng dung môi rửa giải có ái lực với
+ Sự tương tác và cân bằng của chất phân tích với pha động
pha tĩnh mạnh hơn bất kì một cấu tử nào của hỗn hợp tách để
+ Sự tương tác của pha động và pha tĩnh
đẩy các cấu tử cần tách thoát ra khỏi cột.
+ Cấu tử thoát ra khỏi cột đầu tiên là cấu tử tương tác yếu nhất
với pha tĩnh, sau đó đến các cấu tử khác có ái lực với pha tĩnh tăng dần.
+ Phương pháp này tạo nên các dải rửa giải không hoàn toàn
được tách khỏi nhau: có dải thu được chất nguyên chất nhưng có
dải giữa các dải nguyên chất thì gồm hỗn hợp của chúng.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 79 82
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
10.5. Phương pháp tiến hành sắc ký
10.5.1. Phương pháp rửa giải
+ Kỹ thuật rửa giải được sử dụng rộng rãi nhất trong các phương pháp sắc kí hiện nay.
+ Một lượng nhỏ hỗn hợp mẫu được đưa vào cột, pha động có ái lực
với pha tĩnh bé hơn so với bất kì cấu tử cần tách có trong mẫu.
+ Các cấu tử cần tách di chuyển với tốc độ chậm hơn so với chất rửa giải.
+ Các cấu tử được rửa giải theo trật tự ái lực của chúng nhưng tốc độ
di chuyển tương đối của chúng phụ thuộc vào tương tác 3 thành phần
giữa chúng với pha động, với pha tĩnh và giữa pha động với pha tĩnh.
+ Pha động có thể không thay đổi thành phần dung môi trong suốt quá
trình rửa giải (rửa giải đẳng dòng); có thể thay đổi dung môi rửa giải
sau một thời gian định trước (rửa giải theo từng giai đoạn); cũng có thể
không thay đổi các dung môi tạo nên pha động nhưng thay đổi nồng độ
của các thành phần có trong pha động sau một thời gian định trước (rửa giải gradient).
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 80 83
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 10: Phương pháp sắc ký lỏng
10.5. Phương pháp tiến hành sắc ký
10.6. Chọn điều kiện sắc ký
10.5.2. Phương pháp tiền lưu 10.6.1. Lựa chọn pha tĩnh
+ Hỗn hợp cần tách gồm các chất A, B và C được cho chảy liên tục vào
- Dựa vào các tài liệu, dược điển, thành phần và tính chất của
phần trên của cột, trong đó A là cấu tử có ái lực yếu nhất với pha tĩnh.
các chất có trong mẫu phân tích ta chọn cột sắc ký phù hợp: cột
+ Do các cấu tử A, B và C bị lưu giữ trên cột, nên trước hết từ cột chảy
pha thuận (NP), cột pha đảo (RP), cột CN, cột NH
ra chỉ có dung môi. A do có lực tương tác trên cột yếu nhất sẽ di 2,… Cột pha thuận (NP):
chuyển xuống dưới còn các cấu tử có ái lực mạnh hơn A bị pha tĩnh
giữ ở phần trên của cột.
+ Pha tĩnh: silicagel trung tính; trên bề mặt hoạt động của nó có
+ Do dung dượng có hạn của pha tĩnh nên khi vượt dung lượng này thì
chứa các nhóm –OH phân cực ưa nước.
cấu tử A sẽ di chuyển dọc theo cột và ra khỏi cột ở dạng nguyên chất
+ Dùng để tách các chất không phân cực hay ít phân cực.
sau đó là hỗn hợp của các thành phần tiếp theo A+B rồi A+B+C.
+ Ví dụ: Lichrosorb Si 40, Si 60, …
+ Phương pháp tiền lưu ít được dùng do không thực hiện được việc
+ Pha động: dung môi không phân cực hay ít
tách hoàn toàn các cấu tử, đặc biệt khi sử dụng sự tách sắc kí vào mục
phân cực như methanol, benzene, acetonitrile, đích phân tích. chloroform,…
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 81 84 14 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
10.6. Chọn điều kiện sắc ký 10.6.1. Lựa chọn pha tĩnh Cột pha đảo (RP):
+ Pha tĩnh: silicagel đã alkyl hóa; trên bề mặt hoạt động nguyên
tử H bị thay thế trong nhóm -OH bị thay thế bằng các mạch
cacbon thẳng (C8, C18) hay cacbon mạch vòng (phenyl).
+ Dùng để tách các chất không phân cực, ít phân cực hay các
chất phân cực có thể tạo cặp ion.
+ Ví dụ: Lichrospher RP8, C18 ODS, Nucleosil C18, …
+ Pha động: dung môi phân cực như methanol, acetonitrile, nước,
các loại dung dịch đệm, hỗn hợp của các dung môi-đệm,…
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 85 88
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 11: Phương pháp sắc ký khí
10.6. Chọn điều kiện sắc ký
11.1. Giới thiệu kỹ thuật sắc ký khí 10.6.1. Lựa chọn pha tĩnh
Sắc ký khí (GC) là phương pháp sắc ký được sử dụng để
Cột silicagel trên nền mạch cacbon (silicagel biến tính):
tách và phân tích các hợp chất bay hơi mà không làm
+ Dùng để tách các chất phân cực.
phân hủy thay đổi chúng.
- Cơ sở để tách bằng sắc kí khí là sự phân bố của chất giữa hai pha:
+ Pha tĩnh có bề mặt tiếp xúc lớn;
+ Pha động là khí thấm qua toàn bề mặt pha tĩnh.
- Nếu pha tĩnh là rắn thì gọi là sắc kí khí-rắn.
+ Chất rắn nhồi cột thường là silicagel, rây phân tử hoặc than hoạt tính.
+ Quá trình tách chủ yếu là hấp phụ.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 86 89
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 10: Phương pháp sắc ký lỏng
Chương 11: Phương pháp sắc ký khí
10.6. Chọn điều kiện sắc ký
11.1. Giới thiệu kỹ thuật sắc ký khí
10.6.2. Lựa chọn pha động
- Nếu pha tĩnh là lỏng, gọi là sắc kí khí-lỏng.
Mục đích: chọn được pha động có khả năng rửa giải hoàn toàn các
+ Chất lỏng bao bọc quanh bề mặt một chất rắn trơ, gọi là
chất có trong mẫu, tách tốt, pic cân đối. Ngoài ra, thời gian phân tích
phù hợp nhằm tiết kiệm dung môi hóa chất,…
chất mang, tạo nên một lớp phim mỏng. Yêu cầu:
+ Quá trình tách là sự phân bố của chất trong và ngoài lớp
+ Pha động trơ với pha tĩnh đã chọn, không làm biến đổi hóa học pha phim mỏng.
tĩnh (vd pH làm việc 2 < pH < 9).
+ Hòa tan được chất phân tích (không làm kết tủa các chất có trong cột).
+ Bền theo thời gian (ít nhất trong suốt thời gian phân tích mẫu).
+ Độ tinh khiết cao (dung môi cho HPLC hoặc hóa chất tinh khiết phân tích).
+ Nhanh đạt cân bằng trong quá trình sắc ký.
+ Phù hợp với loại detector
+ Kinh tế (không quá đắt và hiếm).
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 87 90 15 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí
11.2. Nguyên tắc của hệ thống máy GC
11.2.1. Hệ thống cung cấp khí mang Khí mang:
+ Độ giảm áp suất tỉ lệ với độ nhớt của khí mang nên cần
chọn khí mang có độ nhớt thấp cho cột mao quản và cột nhồi chặt.
+ Khi lựa chọn cần chú đến detector đang sử dụng:
. Detector đo độ dẫn cần phải sử dụng khí mang có độ dẫn
cao như H2, He. Khí He có ưu điểm không nguy hiểm.
. Detector ion hóa ngọn lửa thường sử dụng khí mang N2 do rẻ và không nhuy hiểm.
. Detector cộng kết điện tử thường dùng khí mang là N2.
. Detector khối phổ phải dùng khí mang là He.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 91 94
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí
11.2.1. Hệ thống cung cấp khí mang
11.2.2. Hệ thống bơm mẫu (bộ tiêm mẫu)
- Các khí mang phải trơ về mặt hóa học như He, Ar, N
- Bộ tiêm mẫu là bộ phân đưa mẫu vào dòng khí mang liên tục. 2, CO
Bộ tiêm mẫu là một bộ phận gắn liền với đầu cột.
2 và H2 và việc chọn lựa khí mang thường được quyết
định bởi loại detector sử dụng.
- Sử dụng một bơm tiêm mẫu vi lượng (microsyringe) để tiêm một
mẫu lỏng hoặc khí qua một đệm cao su silicon (septum) chịu
- Hệ thống cung cấp khí mang bao gồm các bộ điều chỉnh
nhiệt vào một buồng hóa hơi (injector).
áp suất (pressure regulators), các thiết bị đo áp suất
+ Đối với các cột tách thông thường, cỡ mẫu thường thay đổi từ
(gauges), và thiết bị đo tốc độ dòng. một vài đến 20µl.
- Hệ thống khí mang còn chứa một bộ lọc phân tử để tách
+ Cột mao quản đòi hỏi lượng mẫu đưa vào nhỏ hơn nên hệ
nước và các chất nhiễm bẩn khác. Tốc độ dòng được
thống chia dòng mẫu được thiết kế sao cho chỉ một phần nhỏ
kiểm soát bởi các van điều chỉnh áp suất lắp ở các bình
lượng mẫu được tiêm đi vào cột, phần còn lại được thải ra ngoài. chứa khí mang.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 92 95
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí
11.2.1. Hệ thống cung cấp khí mang
11.2.2. Hệ thống bơm mẫu (bộ tiêm mẫu)
- Áp suất của khí vào thiết bị nằm trong khoảng từ 10 đến
+ Tiêm mẫu có chia dòng (split injection):
50 psi để có tốc độ dòng từ khoảng 30 đến 150 ml/ph đối
. Phù hợp cho mẫu có các cấu tử phân tích có nồng độ lớn hơn
với cột nhồi; và khoảng từ 1 đến 25 ml/ph đối với cột mao
0.1% mẫu. Việc tiêm toàn bộ mẫu sẽ làm quá tải cột có đường quản.
kính 0.32 mm hoặc nhỏ hơn.
. Tỉ lệ của mẫu không được đưa vào cột được gọi là tỉ số chia
- Nói chung, nếu áp suất đi vào thiết bị không đổi thì tốc độ
dòng (split ratio) có giá trị từ 50:1 đến 600:1.
dòng sẽ không đổi. Để đo tốc độ dòng khí người ta dùng
+ Tiêm mẫu không chia dòng (splitless injection):
thiết bị đo tốc độ dòng (flowmeter).
. Phù hợp cho phân tích lượng vết những cấu tử có nồng độ nhỏ Khí mang: hơn 0.01% mẫu
. Cách tiêm này có khoảng 80 % mẫu được đưa vào cột.
. Nhiệt độ của buồng tiêm mẫu cho chế độ không chia dòng giữ
thấp hơn (< 220oC) so với chế độ chia dòng vì mẫu bị lưu giữ lâu
hơn trong buồng tiêm mẫu và tránh mẫu bị phân hủy nhiệt.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 93 96 16 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí
11.2.2. Hệ thống bơm mẫu (bộ tiêm mẫu) 11.2.3. Cột sắc ký Cột mao quản
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 97 100
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.3. Cột sắc ký 11.2.3. Cột sắc ký
2 loại: cột nhồi và cột mao quản Cột mao quản
+ Cột mao quản dài 15 - 100 m; đk trong rất nhỏ 0.10 - 0.53 mm.
+ Cột được chế tạo từ thủy tinh oxit tinh khiết nấu chảy, bền và
chịu được nhiệt độ cao đến 350oC.
+ Cột mao quản mở có lớp phim mỏng tráng trên thành ống cho
độ phân giải cao hơn, thời gian phân tích ngắn hơn và độ nhạy
cao hơn cột nhồi nhưng chúng có dung lượng thấp hơn.
+ Cột mao quản mở hẹp cho độ phân giải cao hơn cột mao quản
mở rộng hơn, nhưng chúng đòi hỏi áp suất cao hơn để hoạt động
và có dung lượng nhỏ hơn.
+ Lớp phim mỏng lỏng pha tĩnh dày từ 0.1 - 5 µm.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 98 101
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.3. Cột sắc ký 11.2.3. Cột sắc ký Cột nhồi Cột mao quản
+ Cột mao quản có các hạt rắn chất mang phủ một lớp pha tĩnh lỏng
+ Cột thường được làm
được gắn trên bề mặt bên trong của cột.
bằng thép không rỉ, nicken,
+ Diện tích bề mặt của cột loại này tăng nên có dung lượng lớn hơn thủy tinh cột phủ lớp phim mỏng. . đk 3 - 6 mm Chỉ số lưu Kovats (KI) . chiều dài 1 - 5 m.
+ Thể tích lưu tuyệt đối trong các phép đo thường ít được sử dụng vì
+ Cột nhồi chứa các hạt
chúng phụ thuộc vào rất nhiều yếu tố: lưu lượng dòng, chiều dài cột,
chất mang rắn được phủ lượng pha tĩnh, …
một lớp pha tĩnh lỏng hoặc
+ Kovats đề nghị chọn dãy đồng đẳng n-paraffin làm dãy chuẩn
bản thân hạt rắn là pha tĩnh.
nhằm xác định thể tích lưu tương đối.
. Chất mang rắn silanol đã
+ Chỉ số lưu KI của cấu tử khác được xác định bằng cách so sánh
được metyl hóa để giảm
thời gian lưu của nó với với thời gian lưu của hai n-ankan, trong đó
liên kết hydro với các chất
một cấu tử được rửa giải ra trước còn cấu tử kia được rửa giải ra phân cực
sau chất nghiên cứu trong những điều kiện sắc kí cụ thể.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 99 102 17 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.3. Cột sắc ký 11.2.4. Detector Chỉ số lưu Kovats (KI)
11.2.4.1. Detector dẫn nhiệt Trong đó,
n, N: số nguyên tử C trong ankan thứ nhất và thứ hai;
t’X, t’n, t’N: thời gian lưu hiệu chỉnh của cấu tử X, ankan thứ nhất và thứ hai tương ứng.
+ Chỉ số lưu KI làm chuẩn hóa các biến thiết bị trong sắc ký khí,
cho phép các số liệu lưu giữ được tạo trong những hệ thống sắc
ký khác nhau có thể so sánh được.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 103 106
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.4. Detector 11.2.4. Detector - Dẫn nhiệt (TCD)
11.2.4.2. Detector ion hóa ngọn lửa (FID) - Ion hóa ngọn lửa (FID)
Detector FID là một trong những detector
- Cộng kết điện tử (ECD)
có độ nhạy cao, cao hơn TCD 100 -1000 - Khối phổ (MS) lần. Nguyên tắc:
+ Dựa trên sự biến đổi độ dẫn điện của
ngọn lửa được tạo bởi hỗn hợp khí H2 và
O2 trong không khí đặt trong một điện
trường (buồng điện cực).
+ Do nhiệt độ cao của ngọn lửa, các chất
hữu cơ từ cột tách bị ion hóa. Các ion tạo
thành được chuyển về các bản điện cực
trái dấu. Kết quả tạo thành dòng điện giữa
hai điện cực. Dòng điện này đi qua điện trở
đo R. Sự sụt thế sẽ được khuếch đại rồi đưa ra máy ghi.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 104 107
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.4. Detector 11.2.4. Detector
11.2.4.1. Detector dẫn nhiệt
11.2.4.2. Detector ion hóa ngọn lửa (FID)
+ Độ dẫn nhiệt không đủ nhạy khi phân tích tách với cột mao quản mở có Ứng dụng:
đường kính cột < 0.53 mm.
+ Thích hợp nhất với các hợp chất hữu cơ chứa cacbon.
+ Detector đo độ dẫn nhiệt sử dụng cho cột mao quản đk 0.53 mm và cho các
+ Một số hợp chất không thể phát hiện bằng detector này như: CO, cột nhồi. Nguyên tắc:
CO2, axit formic, formaldehit, NOx, NH3, hợp chất halogen, CS2, H2S,
+ Đo liên tục độ dẫn nhiệt của khí mang (tinh khiết hoặc có chứa các cấu tử H2O.
mẫu cần tách) giữa buồng đo và buồng so sánh.
+ Khí linh động (trọng lượng phân tử nhỏ) tốc độ chuyển động càng cao, dẫn nhiệt càng tốt.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 105 108 18 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.4. Detector
11.3. Phân tích bằng sắc ký khí
11.2.4.3. Detector cộng kết điện tử (ECD) 11.3.2. Chuẩn bị mẫu Nguyên tắc:
- Cần phải làm “sạch” mẫu trước khi đưa vào cột.
+ Dựa trên đặc tính của các chất có khả
- Kết hợp nhiều phương pháp như vi chiết pha rắn, chiết lỏng -
năng cộng kết các điện tử tự do trong pha
lỏng, chiết rắn - lỏng, sự giải hấp nhiệt các các cấu tử dễ bay hơi khí.
để cô lập những cấu tử cần phân tích trong mẫu phức tạp từ Ứng dụng: những chất cản trở.
+ Các phân tử chứa halogen, cacbonyl liên
+ Nếu ta không làm “sạch” mẫu thì sắc ký đồ thu được sẽ chứa
hợp, nitril, hợp chất nitro, và hợp chất cơ
rất nhiều pic kém phân giải và các cấu tử không bay hơi sẽ còn kim.
giữ trong cột và phá hủy các cột đắt tiền.
+ Nó tương đối kém nhạy với các phân tử
hợp chất hydrocacbon, các rượu và xeton.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 109 112
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí 11.2.4. Detector
11.3. Phân tích bằng sắc ký khí
11.2.4.4. Detector khối phổ (MS) 11.3.3. Chọn detector
11.2.4.5. Một số loại khác
Các detector nhạy cho phân tích siêu vết chỉ đáp ứng với một loại
Nito-phospho (NPD), quang hóa ion (PID), ion hóa phóng xung hợp chất nào đó.
(PDD), ion hóa nhiệt (TID), cực tím chân không (VUV), hồng
- Detector được sử dụng rộng rải nhất là detector khối phổ nhưng
ngoại (IRD), ion hóa Heli (HID), độ dẫn điện phân (ELCD), … đắt tiền.
- Detector ion hóa ngọn lửa cũng là loại được dùng phổ biến nhất
nhưng nó chỉ đáp ứng tốt cho hợp chất chứa mạch cacbon dài hoặc các hydrocacbon.
- Detector dẫn nhiệt phổ biến nhất nhưng nó không đủ nhạy cho
những cột mao quản mở có độ phân giải cao.
- Detector ECD thích hợp cho các hợp chất chứa halogen,
cacbonyl liên hợp, nitril, và hợp chất nitro.
- Nếu chỉ cần biết những thông tin định tính để nhận diện các chất
rửa giải, nên chọn detector khối phổ và hồng ngoại.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 110 113
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí
11.3. Phân tích bằng sắc ký khí
11.3. Phân tích bằng sắc ký khí
11.3.1. Mục tiêu phân tích 11.3.4. Chọn cột tách
- Xác định mục tiêu của phép phân tích
Pha tĩnh, đường kính cột và chiều dài cột
+ phân tích định tính hay định lượng? Chọn pha tĩnh
+ Độ phân giải và thời gian phân tích?
+ Các pha tĩnh không phân cực được sử dụng nhiều.
+ Có cần hy sinh độ phân giải để rút ngắn thời gian phân tích?
+ Pha tĩnh có độ phân cực trung bình được sử dụng hầu hết
+ Cần phân tích định lượng chỉ một cấu tử hay nhiều cấu tử trong
những phép tách mà pha tĩnh không phân cực không thể thực mẫu? hiện.
+ Đối với những hợp chất phân cực cao thì cần cột phân cực mạnh.
+ Các đồng phân quang học và những hợp chất có cấu trúc hình
học gần giống nhau đòi hỏi những pha tĩnh đặc biệt cho phép tách này.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 111 114 19 12/21/20
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí
Chương 11: Phương pháp sắc ký khí
11.3. Phân tích bằng sắc ký khí
11.3. Phân tích bằng sắc ký khí 11.3.4. Chọn cột tách
11.3.6. Chương trình hóa nhiệt độ và áp suất
Đường kính cột và bề dày của lớp phim ảnh hưởng đến độ Ưu điểm phân giải:
+ Giảm thời gian tiến hành phân tích và tang giới hạn phát hiện.
+ Độ phân giải cao nhất có thể đạt được bởi những cột hẹp nhất
+ Chương trình hóa nhiệt độ cũng có thể giúp rửa sạch một cột bị
với pha tĩnh mỏng nhất.
nhiễm bẩn các cấu tử có nhiệt độ sôi cao trong những lần tiêm
+ Các cột hẹp và lớp phim mỏng đặc biệt thích hợp cho việc tách trước.
các hỗn hợp của các chất có nhiệt độ sôi cao.
+ Chương trình hóa nhiệt độ thường thiết lập nhiệt độ cho cột
+ Tuy nhiên, các cột hẹp có lớp phim mỏng có dung lượng mẫu
tách tương ứng với nhiệt độ của cấu tử có nhiệt độ sôi thấp nhất,
rất thấp, đòi hỏi những detector có độ nhạy cao.
thích hợp là dưới 90oC. Sau đó nhiệt độ được nâng lên theo tốc
+ Các cột mở rộng và có lớp phim dày phù hợp cho các detector
độ chọn trước cho đến nhiệt độ cuối cùng tương ứng với nhiệt độ
đo độ dẫn điện và hồng ngoại. Chúng có dung lượng cao và có
của cấu tử có điểm sôi cao nhất.
thích hợp với các hợp chất dễ bay hơi nhưng cho độ phân giải
thấp và thời gian lưu giữ lâu.
+ Nếu một cột đáp ứng hầu hết những yêu cầu đặt ra nhưng
không đủ độ phân giải thì dung cột dài hơn cùng loại.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 115 118
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí Câu C
1: hương 11: Phương pháp sắc ký khí
11.3. Phân tích bằng sắc ký khí
a. Bản chất sự hành thành phổ phát xạ nguyên tử?
11.3.5. Chọn phương pháp tiêm mẫu
b. Tính tỷ lệ số nguyên tử Na ở trạng thái kích thích và
Chế độ tiêm mẫu chia dòng:
trạng thái cơ bản (Nm/N0) nếu nhiệt độ của nguồn
+ Phù hợp cho những mẫu phân tích có nồng độ cao hoặc phân
nguyên tử hóa là 21000C. Cho biết các hằng số: h = 6.62 tích khí.
x 10-34 J.s; c = 3 x 108 m/s; k = 1.38 x 10-23 J/K; và gm/g0
Chế độ tiêm mẫu không chia dòng: = 6/2;
+ Phù hợp cho những dung dịch rất loãng. em = 330.00 nm.
+ Cho độ phân giải tốt nhưng trong phân tích định lượng có thể
Câu 2: Nồng độ Cu(II) trong một mẫu nước biển được
có các hợp chất kém bay hơi bị mất trong quá trình tiêm.
xác định bằng phương pháp von-ampe hòa tan anot
+ Các mẫu chứa chất phân tích < 100 ppm có thể phân tích với
những cột có chiều dày lớp phim < 1µm ở chế độ tiêm mẫu không
theo cách thêm chuẩn một điểm. chia dòng.
- 50,0 mL dung dịch mẫu chứa Cu2+ cho Ipic là 0,868
+ Những mẫu chất phân tích 100-1000 ppm đòi hỏi lớp phim dày A. hơn 1µm.
- Nếu thêm vào mẫu trên 10,0 mL dung dịch Cu2+
chuẩn nồng độ 5,0 ppm thì Ipic là 2,52 A.
Tính nồng độ (ppb) của Cu2+ trong mẫu phân tích.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 116 119
Bộ môn Hóa phân tích – Viện KTHH
Bộ môn Hóa phân tích – Viện KTHH
Chương 11: Phương pháp sắc ký khí Câu C
1: hương 11: Phương pháp sắc ký khí
11.3. Phân tích bằng sắc ký khí
a. Nêu các loại dòng cực phổ?
11.3.5. Chọn phương pháp tiêm mẫu
b. Tính tỷ lệ số nguyên tử Cd ở trạng thái kích thích và
Tiêm mẫu trên cột (on-column injection):
trạng thái cơ bản (Nm/N0) nếu nhiệt độ của nguồn
+ Phù hợp cho phân tích định lượng và cho những hợp chất kém
nguyên tử hóa là 45000C. Cho biết các hằng số: h = 6.62 bền nhiệt.
x 10-34 J.s; c = 3 x 108 m/s; k = 1.38 x 10-23 J/K; và gm/g0
+ Độ phân giải thấp và không thể sử dụng cho những cột có = 6/2;
đường kính nhỏ hơn 0.25 mm. em = 228.80 nm..
Câu 2: Bằng phương pháp điện phân có thể tách Cu và
Cd khỏi nhau hay không? Nếu dung dịch CuSO4 và
CdSO4 cùng nồng độ 0,01 M, pH = 0; và biết:
E0(O2,4H+/2H2O) = 1,23 V; A = + 0,40 V; E0(Cu2+/Cu) =
0,34 V; E0(Cd2+/Cd) = - 0,40 V; K = 0,0 V.
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017
Nguyễn Xuân Trường Phương pháp tách - chiết 4/2017 117 120 20




