











Preview text:
lOMoAR cPSD| 47205411 Enzym
1. Trình bày được thành phần cấu tạo, danh pháp, phân
loại enzym và coenzym có minh họa. - Định nghĩa:
Enzym là chất xúc tác sinh học/cơ thể sống, có bản chất là protein. - Đặc điểm:
o Làm tăng tốc độ pư: 109 đến 1020 o
Tính đặc hiệu cao o Hoạt động của E được điều hòa -
Danh pháp: Tên E = tên S và/ tên pư + ase. -
Phân loại: theo hiệp hội enzym quốc tế (EC: Enzym commission) chia làm 6 nhóm:
Oxydoreductase: oxy hóa khử
E oxi hóa khử - oxidoreductase: xt cho pư oxi hóa và pư khử, các pư có sự trao đổi H hoặc electron
- Dehydrogenase: sử dụng các phân tử không phải oxy ( NAD+, NADP+ ,FAD,...) là chất nhận e. VD: lactat dehydrogenase
- Oxidase: sử dụng oxi như là chất nhận điện tử.
- Reductase: xúc tác cho pư khử.
VD glutathion reductase G-S-S-G + NADPH + H+ → 2 GSH + NADP+
- Peroxidase: sử dụng H2O2 làm chất nhận e: 2GSH + H2O2 → GS–SG + 2H2O ( Glutathion peroxidase)
- Catalase: 2 H2O2 → 2 H2O + O2
- Oxygenase: chuyển nguyên tử O vào cơ chất
Transferase: vận chuyển nhóm
E vận chuyển nhóm (transferase) AX + B A + BX
- Các aminotransferase: chuyển nhóm –NH2 từ aa vào acid cetonic.
VD: aspartat transaminase (AST), alanin transaminase (ALT)
- Transcetolase, transaldolase: vận chuyển đơn vị 2C và 3C.
- Các acyl-, methyl-, glucosyl- transferase, phosphorylase. VD: glycogen phosphorylase,... lOMoAR cPSD| 47205411
- Kinase: vận chuyển gốc Pi từ ATP vào cơ chất
VD hexokinase xt: G + ATP → G6P + ADP
- Thiolase: chuyển nhóm CoASH vào cơ chất
- Polymerase: vận chuyển các nucleotid Hydrolase: thủy phân
E thủy phân (hydrolase) AB + H2O → AH + BOH
Các esterase, glycosidase, protease, phosphatase, phospholipase, amidase, desaminase, nuclease
G6P + H2O → G + Pi (xt G-6-phosphatase).
Lyase: phân cắt, bão hòa hoặc tạo liên kết đôi. - Liên kết C-C: - Liên kết C-O:
HOOC-CHOH-CH2-COOH → HOOC-CH=CH-COOH + H2O (malat) (fumarat)
Enzym: Fumarase (fumarat hydratase)/ malat hydro-lyase
- Liên kết C-N: L-aspartat → fumarat + NH3
Enzym: aspartat amoni-lyase (aspartase) Isomerase: đồng phân
Enzym đồng phân: xt cho phản ứng biến đổi giữa các dạng đồng phân. - Racemase - Epimerase
- Isomerase: làm thay đổi cấu trúc của phân tử
VD: Phosphohexose isomerase: G-6-P ↔ F-6-P
- Mutase: vận chuyển nhóm P nhưng không làm thay đổi cấu trúc. lOMoAR cPSD| 47205411
VD: Phosphoglycerat mutase: 3-Phosphoglycerat ↔ 2-Phosphoglycerat Ligase: tổng hợp
Emzym tổng hợp (ligase hoặc synthetase)
Xt cho pư hình thành liên kết C-C, C-O, C-N, C-S có sử dụng năng lượng (ATP,...)
2. Trình bày được cấu trúc phân tử và tính đặc hiệu của enzym
Cấu trúc phân tử của enzym:
Thành phần cấu tạo: E chia làm 2 loại
- Enzym đơn giản: là những protein thuần
- Enzym phức tạp: ngoài phần protein (apoenzym) còn có thành phần khác không phải là protein (cofactor)
- Cofactor : ion kim loại ( Mg2+, Zn2+,...) hoặc là hợp chất hữu cơ - coenzym. Tính đặc hiệu •
Enzym chỉ xúc tác một hoặc một nhóm phản ứng đặc trưng trên cơ chất cụ thể. •
Được minh họa bằng liên kết đặc hiệu E-S (enzyme-substrate) qua các liên kết yếu (tĩnh
điện, hydro, Van der Waals)
3. Giải thích được các đặc tính của trung tâm hoạt động và
cơ chế hoạt động của enzym
Trung tâm hoạt động (TTHĐ) của enzym. - Cấu tạo:
+ gồm các aa có nhóm hóa học hoạt tính cao: -SH (Cys) , -OH (Ser,Thr, Tyr), -NH2(Lys), COOH
Trp (Glu,Asp), nhóm indol (Trp),....
+ trong nhiều trường hợp: ion KL, coenzym
- Một E có thể có 1 hay nhiều TTHĐ
- Vai trò: gắn đặc hiệu với S, xúc tác phản ứng biến đổi S thành P.
- TTHĐ của E gắn với S theo 2 thuyết: lOMoAR cPSD| 47205411
+ Thuyết “ổ khóa – chìa khóa”
+ Thuyết “ tiếp xúc cảm ứng”
4. Phân tích được động học của enzym một cơ chất, có
chất ức chế cạnh tranh và không cạnh tranh. Không có chất ức chế
- Mô hình Michaelis–Menten:
- Km là hằng số Michaelis – phản ánh ái lực giữa enzym và cơ chất.
Chất ức chế cạnh tranh
- Gắn vào trung tâm hoạt động. -
Km tăng, Vmax không đổi.
Chất ức chế không cạnh tranh -
Gắn tại vị trí khác trung tâm hoạt động. -
Km không đổi, Vmax giảm.
5. Giải thích được các yếu tố ảnh hưởng đến hoạt động và
nguyên lý điều hòa hoạt động enzym
Các yếu tố ảnh hưởng -
[S] (cơ chất) tăng → v tăng (đến ngưỡng bảo hòa). -
[E] (enzym) tăng → v tăng tuyến tính. -
Nhiệt độ, pH: có ngưỡng tối ưu riêng biệt. -
Chất hoạt hóa/ức chế, ánh sáng, siêu âm…. Điều hòa hoạt động enzym
1. Điều hòa hoạt tính:
o Dị lập thể (allosteric): thay đổi cấu hình trung tâm hoạt động.
o Hoạt hóa zymogen, thay đổi hóa trị (phosphoryl hóa…). lOMoAR cPSD| 47205411
2. Điều hòa tổng hợp enzym:
o Enzym cấu trúc vs. enzym cảm ứng.
6. Trình bày được một số ứng dụng của enzym trong thực tế Y học chẩn đoán:
o ALT, AST: bệnh gan o ACP: ung thư tuyến tiền liệt o G6PD: thiếu máu tan huyết Dược phẩm:
o Alteplase – tiêu huyết khối.
o α-chymotrypsin – chống viêm, giảm phù nề.
Nghiên cứu phát triển thuốc:
o Enzym chuyển hóa thuốc, kháng sinh, độc chất (ADH, ALDH) Chu trình Krebs
1. Bản chất của sự hô hấp tế bào và hoạt động của chuỗi hô hấp tế bào
Bản chất hô hấp tế bào -
Là quá trình oxy hóa sinh học các chất (glucid, lipid, protein) để tạo năng lượng ATP
dưới dạng hóa học mà không sinh nhiệt như đốt cháy vật lý. -
Gồm nhiều giai đoạn, xúc tác bởi hệ thống enzym phức tạp, không xảy ra trong một bước mà qua nhiều trung gian.
Chuỗi hô hấp tế bào (HHTB) -
Diễn ra tại màng trong ti thể – nơi các enzym và phức hợp vận chuyển điện tử được sắp xếp có tổ chức. -
Gồm 4 phức hợp chính:
1. Phức hợp I (NADH dehydrogenase): nhận e từ NADH.⁻
2. Phức hợp II (succinate dehydrogenase): nhận e từ FADH .⁻ ₂
3. Phức hợp III (ubiquinone-cytochrome c oxidoreductase). lOMoAR cPSD| 47205411
4. Phức hợp IV (cytochrome c oxidase): chuyển e cuối cùng cho O → H O.⁻ ₂ ₂ -
Chất nhận e cuối cùng là O⁻ ₂, tạo ra H O₂ và giúp tạo ra thế điện hóa để tổng hợp ATP.
2. Phosphoryl hóa, khử phosphoryl, hợp chất và liên kết giàu năng lượng Phosphoryl hóa
Là quá trình gắn nhóm phosphat vào phân tử hữu cơ (có thể sử dụng năng lượng từ ATP), xúc
tác bởi kinase hoặc phosphorylase. Khử phosphoryl
Là quá trình loại bỏ nhóm phosphat, xúc tác bởi enzym phosphatase, tỏa năng lượng.
Các hợp chất giàu năng lượng (ΔG° < -7 kcal/mol) 1.
Acyl phosphat (VD: 1,3-bisphosphoglycerat, ΔG° = -11,8) 2.
Enol phosphat (VD: phosphoenolpyruvat, ΔG° = -14,8) 3.
Guanido phosphat (VD: creatinphosphat, ΔG° = -10,3) 4.
Pyrophosphat (ATP, ΔG° = -7,3) 5.
Thioeste (Acetyl-CoA, ΔG° = -7,5). Vai trò của ATP -
Lưu trữ và cung cấp năng lượng cho các quá trình:
o Vận chuyển tích cực (Na /K ATPase)⁺ ⁺ o Co cơ
o Truyền tín hiệu nội bào
o Tổng hợp sinh học (VD: G + ATP → G-6P + ADP)
3. Cơ chế, điều hòa và vai trò của sự phosphoryl oxy hóa Cơ chế -
Phosphoryl oxy hóa là quá trình gắn phosphat vô cơ vào ADP để tạo ATP, đồng thời oxy
hóa khử NADH hoặc FADH₂. -
Xảy ra tại chuỗi HHTB, dựa trên sự chênh lệch điện thế màng ti thể (∆pH và ∆Ψ) – theo
thuyết thẩm thấu hóa học. lOMoAR cPSD| 47205411
Tỉ số P/O (ATP sinh ra trên mỗi nguyên tử O tiêu thụ) - NADH → 2.5 ATP - FADH₂ → 1.5 ATP
Enzym then chốt: ATP synthase -
Tổng hợp ATP từ ADP + Pi -
Có ái lực với ATP cao hơn ADP → phản ứng thuận chiều tạo ATP Điều hòa
Phụ thuộc vào: nhu cầu ATP, nồng độ ADP + Pi, và oxy sẵn có.
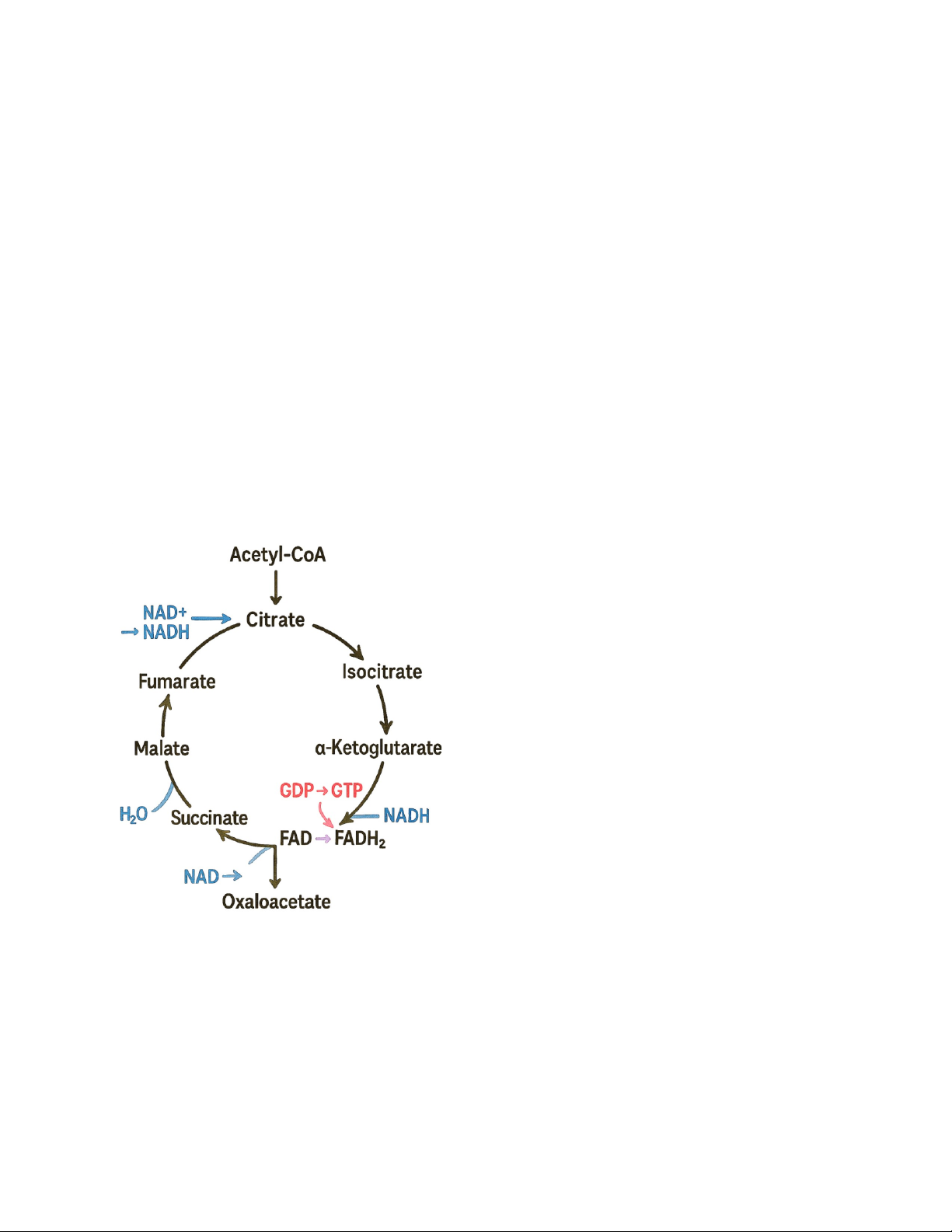
4. Các giai đoạn, kết quả, ý nghĩa và điều hòa chu trình Krebs
Các giai đoạn (8 bước chính) Kết quả 1 vòng Krebs -
3 NADH → 7.5 ATP - 1 FADH → 1.5 ATP₂ - 1 GTP ≈ 1 ATP -
Tổng cộng: ~10 ATP / 1 Acetyl-CoA. Điều kiện hoạt động
Hiếu khí – cần oxy để tái oxy hóa NADH và FADH₂ Điều hòa -
Qua các enzym chính như isocitrat
dehydrogenase và α-ketoglutarate dehydrogenase. -
Bị ảnh hưởng bởi nồng độ ATP/ADP, NADH/NAD và các chất trung gian.⁺ Ý nghĩa -
Giai đoạn thoái hóa chung cuối cùng của glucid, lipid, protein. -
Cung cấp năng lượng, chất trung gian cho các quá trình sinh tổng hợp khác:
αketoglutarat, oxaloacetat, succinyl-CoA, v.v. lOMoAR cPSD| 47205411 Hormon
1. Khái niệm, phân loại và cơ chế điều hòa bài tiết hormon Khái niệm hormon -
Là chất dẫn truyền thông tin hóa học, do tế bào nội tiết sản xuất,
đi theo đường máu để điều hòa hoạt động của các cơ quan khác. -
Đặc điểm: o Nồng độ thấp o T½ ngắn o Tác dụng thông qua
receptor đặc hiệu. Receptor hormon - Là protein có hai vùng:
o Vùng nhận diện hormon o
Vùng phát tín hiệu nội bào.
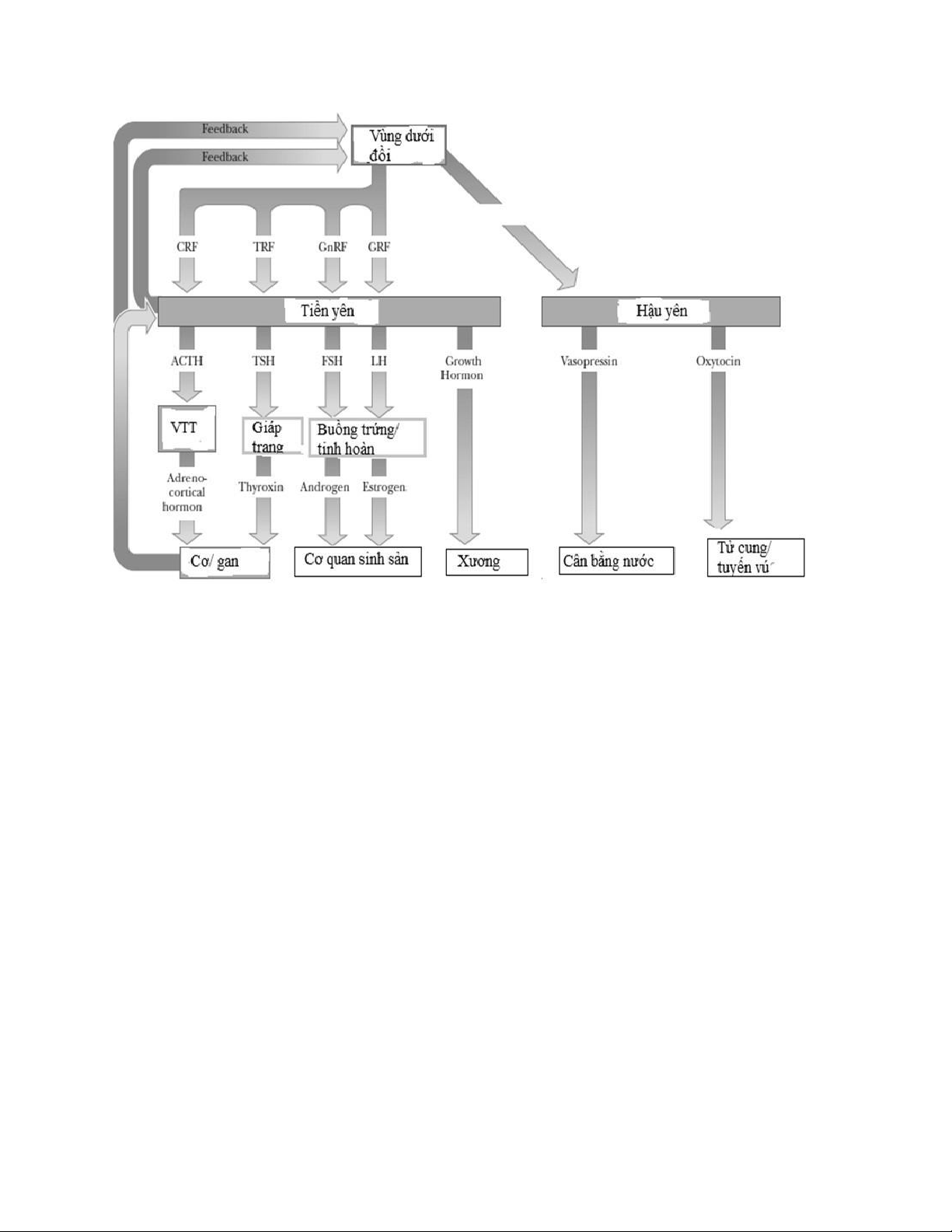
Các tuyến nội tiết chính
Vùng dưới đồi, tuyến yên, tuyến giáp, tuyến tùng, cận giáp, tuyến tuỵ, tuyến thượng thận, buồng
trứng, tinh hoàn, gan, nhau thai… lOMoAR cPSD| 47205411
Cơ chế điều hòa bài tiết hormon -
Điều hòa ngược âm tính (feedback âm): hormon ức chế tuyến sản xuất chính khi đã đủ. -
Điều hòa ngược dương tính (feedback dương): ít gặp, ví dụ hormon sinh dục nữ thúc
đẩy tuyến yên tiết LH trước rụng trứng. -
Kiểm soát qua chất chuyển hóa trung gian: VD glucose huyết điều khiển bài tiết insulin. Phân loại hormon - Theo cấu tạo:
o Peptid/Protein: VD hormon tuyến yên, tụy, cận giáp o Steroid: từ vỏ thượng
thận, tuyến sinh dục o Dẫn xuất acid amin: từ tuyến giáp, tủy thượng thận -
Theo cơ chế truyền tín hiệu:
o Nhóm I: receptor nội bào
o Nhóm II: receptor màng tế bào (phân chia theo chất truyền tin thứ 2: AMPv,
GMPv, Ca² /DAG, tyrosine kinase).⁺
2. Cơ chế truyền tín hiệu của hormon lOMoAR cPSD| 47205411
Hormon tác động qua receptor nội bào (nhóm I) -
Thường là steroid hoặc hormon tuyến giáp. -
Đi qua màng tế bào → gắn receptor trong bào tương hoặc nhân → tác động trực tiếp lên
DNA, điều hòa phiên mã gen.
Hormon tác động qua receptor màng tế bào (nhóm II) -
Gồm nhiều phân nhóm dựa trên chất truyền tin thứ hai (CTT2):
o IIA (AMPv): Adrenalin, Glucagon, Calcitonin
o IIB (GMPv): ANP o IIC (Ca² /DAG)⁺ :
TRH, Oxytocin o IID (phosphoryl hóa): Insulin, GH.
AMPv làm CTT2 – Ví dụ chi tiết:
Khi hormon gắn vào receptor màng → hoạt hóa G-protein → adenyl cyclase tạo AMP vòng →
kích hoạt protein kinase A → phosphoryl hóa nhiều enzyme nội bào.
3. Cấu tạo, tác dụng, điều hòa bài tiết và chuyển hóa của mỗi nhóm hormon Hormon protein và peptid
VD: GH, Insulin, Glucagon, Somatostatin, PTH -
Tác dụng: điều hòa tăng trưởng, đường huyết, canxi máu -
Điều hòa: phụ thuộc chất nền (glucose, canxi…) -
Chuyển hóa nhanh, tan trong nước, receptor màng. Hormon dẫn xuất acid amin -
Tuyến giáp (T3, T4): tăng chuyển hóa cơ bản, tăng hấp thu glucose, lipid, protein -
Tủy thượng thận (adrenalin, noradrenalin): tăng nhịp tim, huyết áp, giải phóng glucose -
T3 tác động mạnh hơn T4 dù T4 bền hơn và vận chuyển mạnh hơn. Hormon steroid -
Tổng hợp từ cholesterol, tan trong lipid, receptor nội bào. - Vỏ thượng thận: lOMoAR cPSD| 47205411
o Glucocorticoid: tăng đường huyết, chống viêm (Cortisol) o Mineralocorticoid: tăng
tái hấp thu Na , tăng huyết áp (Aldosteron⁺ ) o Androgen: hoạt động sinh dục nhẹ - Sinh dục:
o Estrogen (E1, E2, E3), Progestin: điều hòa chu kỳ kinh, tránh thai o Cơ chế tránh
thai tổng hợp: ức chế FSH, LH, không cho rụng trứng và làm tổ. - Chuyển hóa hormon steroid:
o Qua gan, tạo sản phẩm mất hoạt tính và tan tốt hơn nhờ liên hợp glucuronic acid.
4. Vận dụng kiến thức hormon để giải thích thuốc và tác dụng phụ
Thuốc tránh thai tổng hợp -
Gồm estrogen + progestin: o Ức chế rụng trứng o Ngăn cản trứng làm tổ o Làm dày
chất nhầy cổ tử cung → ngăn tinh trùng. Tác dụng phụ liên quan: -
Glucocorticoid (dùng lâu dài): Loãng xương, tăng đường huyết, giảm miễn dịch -
Insulin: Dễ gây hạ đường huyết nếu dùng quá liều -
Androgen: Dùng liều cao gây rối loạn nội tiết ở nữ Glucid
1. Phân loại – Cấu trúc – Tính chất – Vai trò sinh học và Ứng dụng của Glucid Phân loại: -
Monosaccharid: đường đơn (3–7C), gồm aldose và ketose. -
Oligosaccharid: gồm 2–14 monosaccharid, liên kết glycosid. - Polysaccharid:
o Thuần: tinh bột, glycogen, cellulose. o Phức tạp:
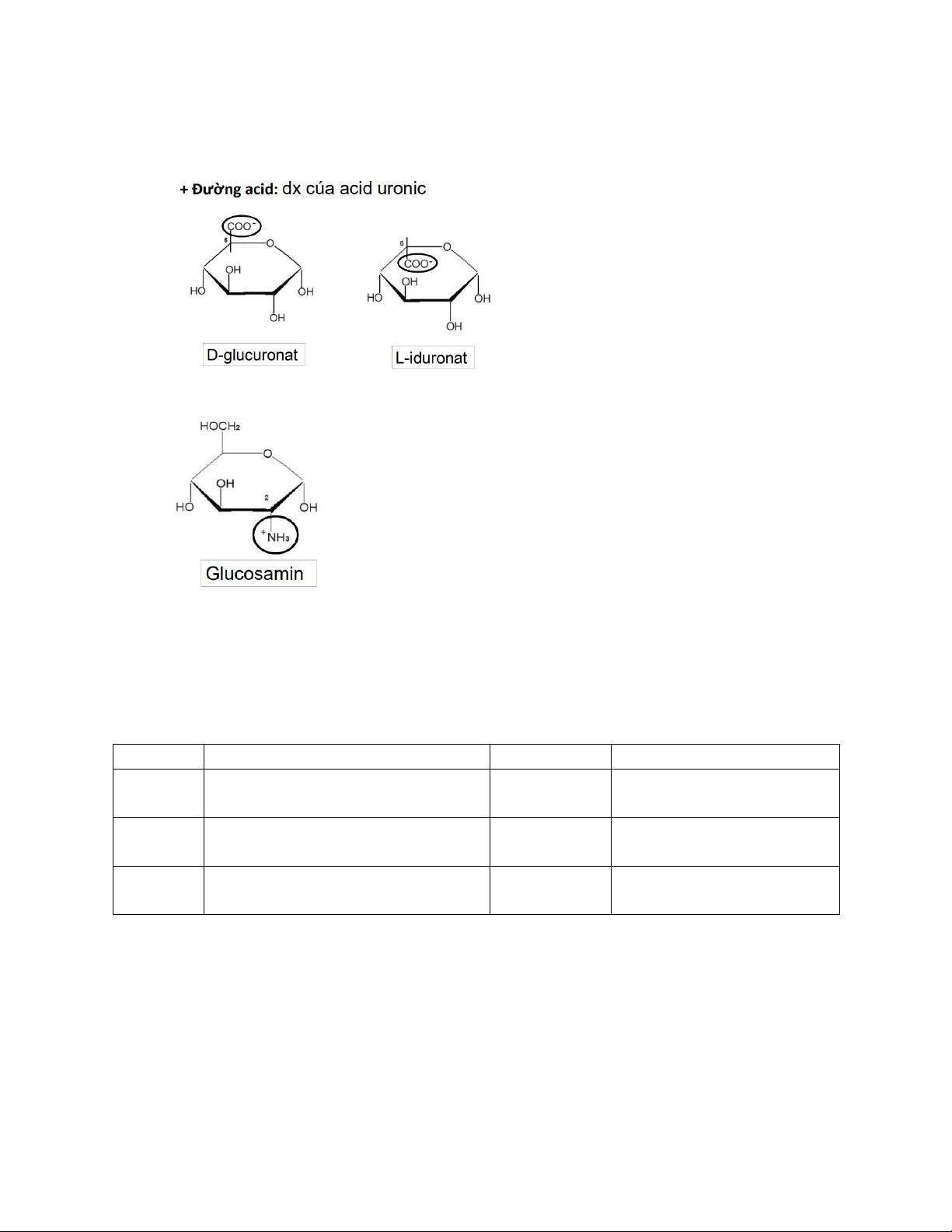
peptidoglycan, glycosaminoglycan, proteoglycan. lOMoAR cPSD| 47205411 Dẫn xuất monosaccharid -
Acid uronic (glucuronat, iduronat) -
Đường amin (glucosamin, galactosamin) -
Đường khử oxy, glycosid, N-/S-glycosid. Polysaccharid
1.Polysaccharid thuần (homopolysaccharid). -
Chỉ gồm 1 loại monosaccharid, ví dụ glucose Tên Cấu tạo Liên kết Vai trò α(1→4) & Tinh bột Amylose + Amylopectin
Dự trữ NL ở thực vật α(1→6)
Cấu trúc giống amylopectin nhưng α(1→4), Glycogen
Dự trữ NL ở động vật phân nhánh nhiều hơn α(1→6)
Cấu trúc thành TB thực vật, Cellulose Chuỗi β-glucose β(1→4) không tiêu hóa được
2. Polysaccharid phức tạp (heteropolysaccharid)
Gồm nhiều loại monosaccharid + nhóm phi glucid (protein, lipid…). -
Peptidoglycan: thành tế bào VK Gram (+) -
Glycosaminoglycan (GAGs):
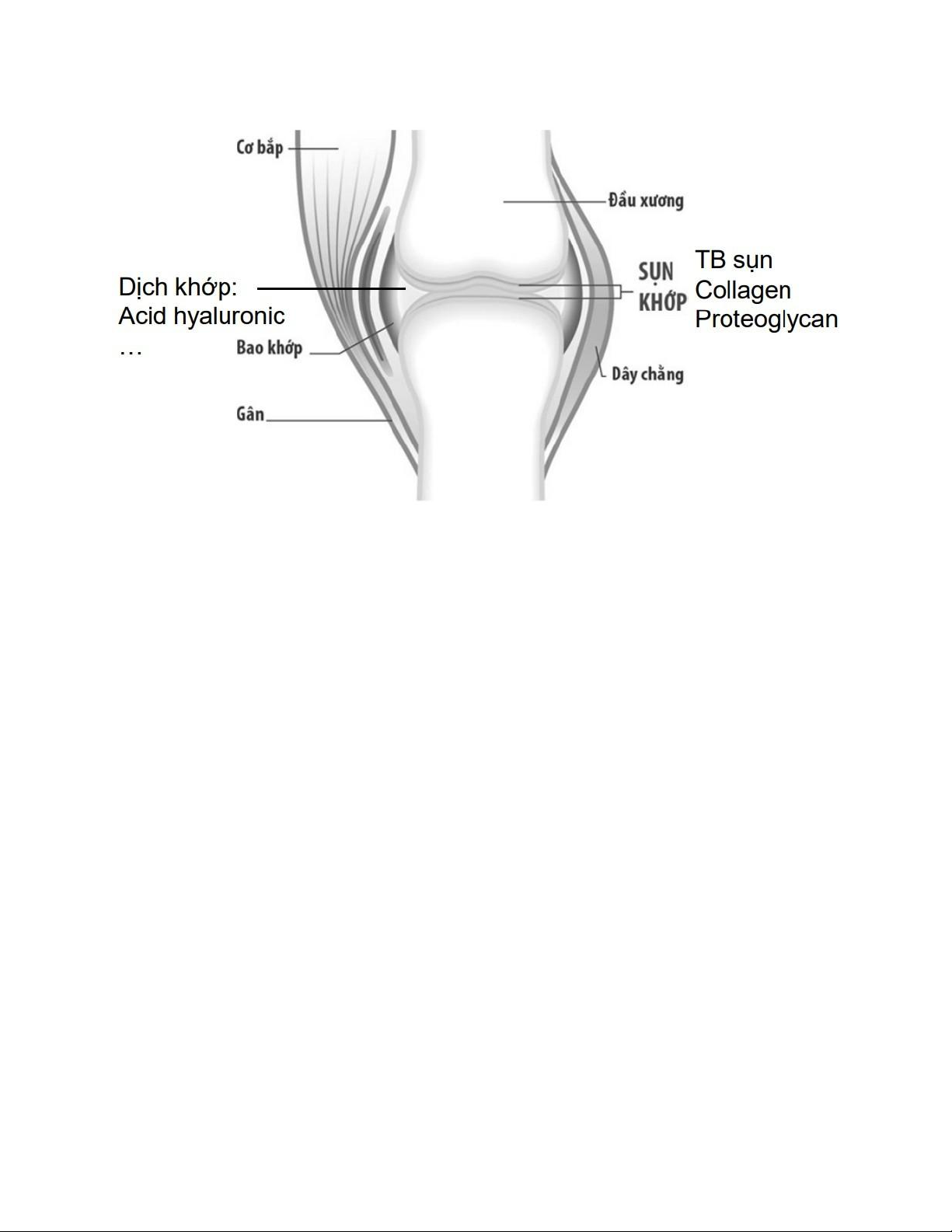
o Heparin, Acid hyaluronic, Chondroitin sulfat – cấu trúc mô liên kết, dịch khớp lOMoAR cPSD| 47205411 -
Proteoglycan: Protein lõi + GAGs, cấu trúc nền ngoại bào -
Glycoprotein/Glycolipid Tính chất nổi bật: -
Khả năng tạo liên kết glycosid, tính khử (ở đường có nhóm hemiacetal tự do). -
Có thể tạo dẫn xuất có hoạt tính sinh học.
Vai trò sinh học & Ứng dụng: -
Nguồn năng lượng chính (60% NL hằng ngày). -
Cấu trúc mô liên kết, dịch khớp, enzyme, miễn dịch (glycoprotein). -
Ứng dụng trong y học: dẫn xuất glucid dùng làm thuốc, xét nghiệm, vaccine, kháng sinh (VD: streptomycin).
2. Tiêu hóa và hấp thu Glucid Tiêu hóa -
Bắt đầu từ miệng (amylase nước bọt), chủ yếu ở ruột non. - Enzym tiêu hóa:
o α-Amylase: phân giải tinh bột → dextrin. o
Disaccharidase (lactase, sucrase, maltase): tạo monosaccharid. lOMoAR cPSD| 47205411 Hấp thu: -
Chủ yếu ở ruột non (tá tràng và hỗng tràng). - Cơ chế hấp thu:
o Khuếch tán thụ động: fructose, arabinose. o Vận chuyển
tích cực (SGLT1): glucose, galactose.
3. Diễn biến – Ý nghĩa các con đường thoái hóa, tổng hợp glucid và mối liên hệ A. Thoái hóa glycogen -
Thủy phân → G1P (90–93%) và glucose tự do (7%) - Enzym: phosphorylase,
debranching enzyme. B. Đường phân (glycolysis): -
Xảy ra ở bào tương, gồm 10 phản ứng -
Sản phẩm: 2 pyruvat + 2 ATP + 2 NADH -
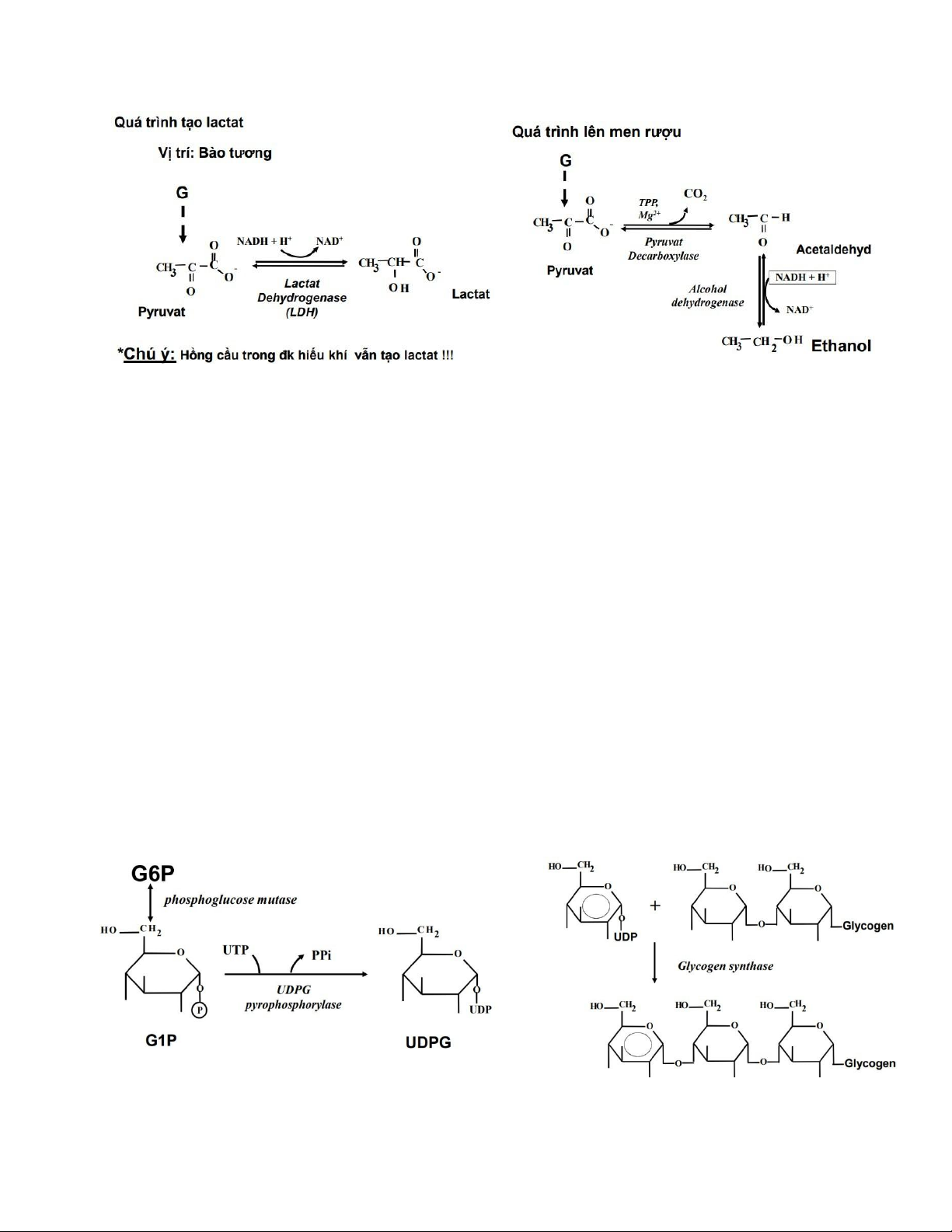
Trong hồng cầu: có nhánh chu trình Rapoport tạo 2,3-BPG giúp Hb nhả O .₂ C. Số phận Pyruvat: -
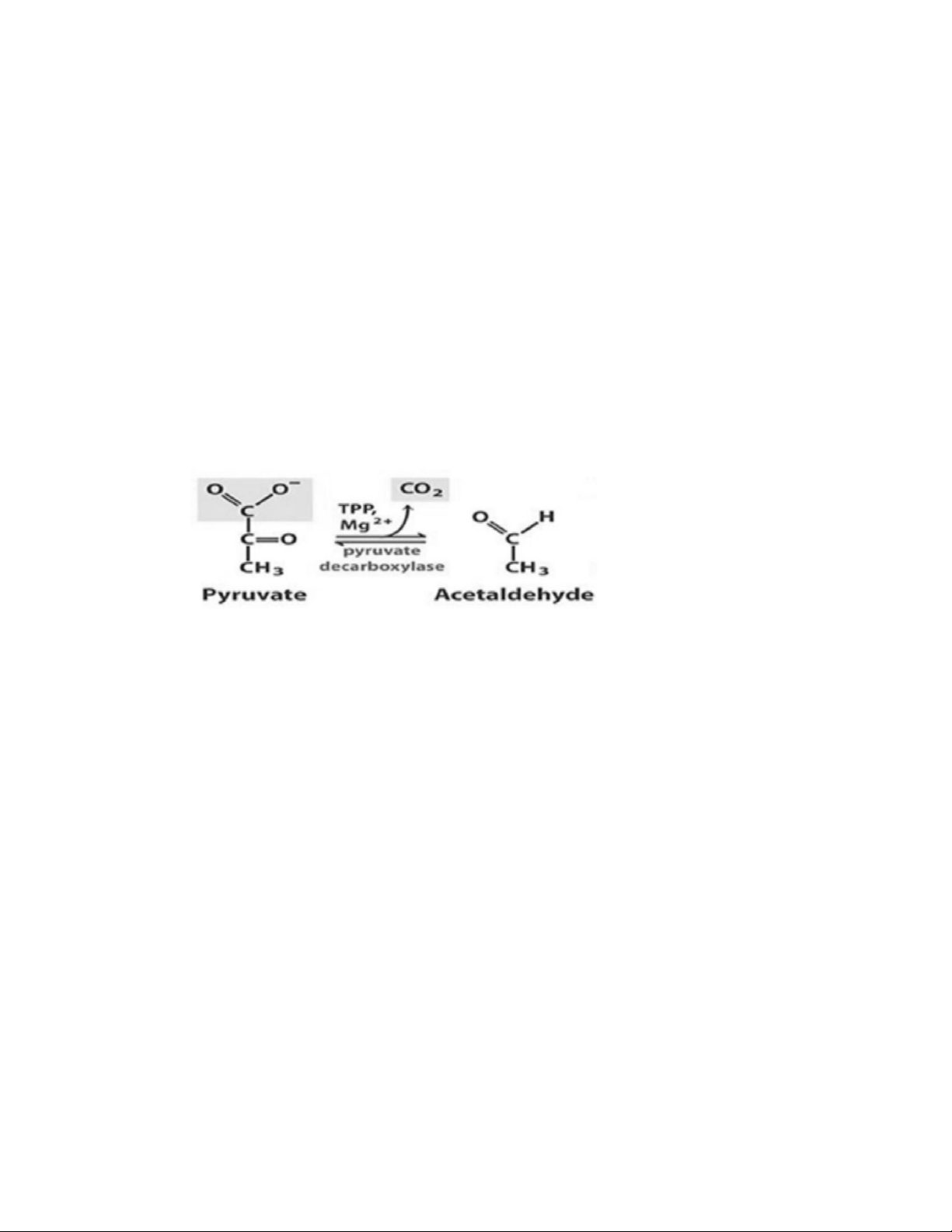
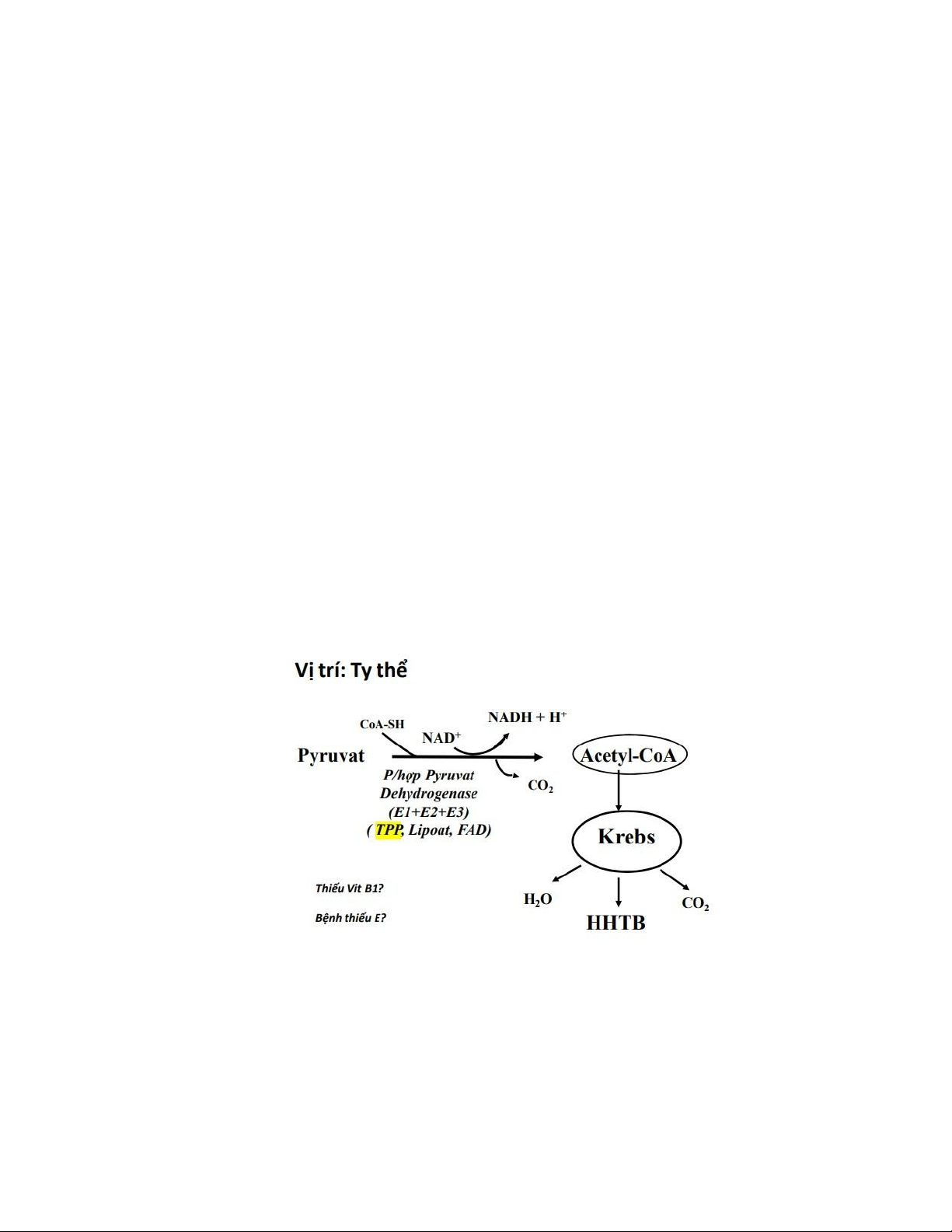
Hiếu khí: chuyển thành Acetyl-CoA → Krebs → CO , H O.₂ ₂ -
Kị khí: thành lactat (cơ, HC) hoặc ethanol (nấm men). lOMoAR cPSD| 47205411
D. Pentose phosphate pathway (PPP): -
Tạo NADPH và Ribose-5-phosphate - Quan trọng trong:
o Tổng hợp acid nucleic o Giải độc qua hệ thống glutathion -
Chiếm ưu thế ở: gan, mô mỡ, tuyến vú, thượng thận. E.
Đường uronic & ascorbic: -
Giải độc, tổng hợp chất nền (hyaluronat, chondroitin sulfat).
F. Tân tạo glucose (Gluconeogenesis): -
Xảy ra ở gan, thận -
Từ: pyruvat, lactat, acid amin glucogenic, glycerol, các đường khác - Liên hệ với chu
trình Cori, chu trình alanin. G. Tổng hợp glycogen: -
Từ G1P → UDP-glucose → gắn vào chuỗi glycogen lOMoAR cPSD| 47205411 -
Enzym: glycogen synthase, branching enzyme: amylo (1-4 ,1-6) transglycosylase.
4.Các cơ chế điều hòa chuyển hóa glucid Điều hòa tương hỗ -
Giữa: Đường phân ⟷ Tân tạo đường -
Tránh tạo chu trình vô ích -
Các enzym chủ chốt điều hòa:
o PFK-1 / F-1,6-BPase: điều hòa bởi ATP, AMP, F2,6BP o Pyruvat kinase /
Pyruvat carboxylase: điều hòa bởi Acetyl-CoA, F1,6BP.
Điều hòa đường huyết -
Gan, thận: điều chỉnh nồng độ glucose máu. - Hormone tham gia:
o Insulin: hạ đường huyết o Glucagon, adrenalin, cortisol, GH,
T3/T4: tăng đường huyết.
5. Giải thích rối loạn chuyển hóa trong Đái tháo đường tụy Cơ chế bệnh sinh
Do thiếu insulin hoặc giảm đáp ứng → rối loạn chuyển hóa: o
Thu nhận glucose vào tế bào o
Thoái hóa glucose → tế bào thiếu năng lượng o Thoái hóa
lipid → tạo acetyl-CoA dư thừa o Thể cetonic (do thiếu
oxaloacetat) o NADPH → tổn thương mô. Biểu hiện lâm sàng: - Tăng glucose máu và niệu - Nhiễm toan máu (do ceton) -
Dễ nhiễm trùng, mệt mỏi, sụt cân -
Biến chứng: suy thận, NMCT, hoại tử chi, đục thủy tinh thể... lOMoAR cPSD| 47205411 Lipid
1. Phân loại, cấu trúc, danh pháp, vai trò sinh học và ứng dụng của lipid Phân loại Lipid được chia thành: Loại Cấu tạo cơ bản Ví dụ Đơn giản Acid béo + Alcol
Glycerid (dự trữ năng lượng), Cerid, Sterid Phức tạp
Đơn giản + nhóm khác (P, glucid, S, Phospholipid, Glycolipid, N...) Lipoprotein... Tiền chất / dẫn
Acid béo, alcol, sterol, steroid, keton, Cholesterol, hormone vỏ thượng xuất aldehyd... thận... Cấu trúc tiêu biểu -
Triglycerid (TG): Glycerol + 3 acid béo → dự trữ năng lượng. -
Phospholipid: lipid màng, có đầu ưa nước – đuôi kỵ nước, đóng vai trò trong cấu trúc màng tế bào. -
Sterol (cholesterol): nền tảng tạo acid mật, hormone steroid, vitamin D. Vai trò sinh học -
Nguồn năng lượng cao (1g lipid → 9 kcal). -
Thành phần cấu trúc màng sinh học. -
Tiền chất tạo hormon, acid mật, vitamin tan trong dầu. -
Chất trung gian truyền tín hiệu (eicosanoid). Ứng dụng
- Trong điều trị (heparin lipid, dung môi thuốc, viên nang mềm). -
Ứng dụng xét nghiệm rối loạn lipid máu, bệnh lý chuyển hóa.
2. Trình bày quá trình tiêu hóa và hấp thu lipid Tiêu hóa -
Bắt đầu tại ruột non, có sự hỗ trợ của:
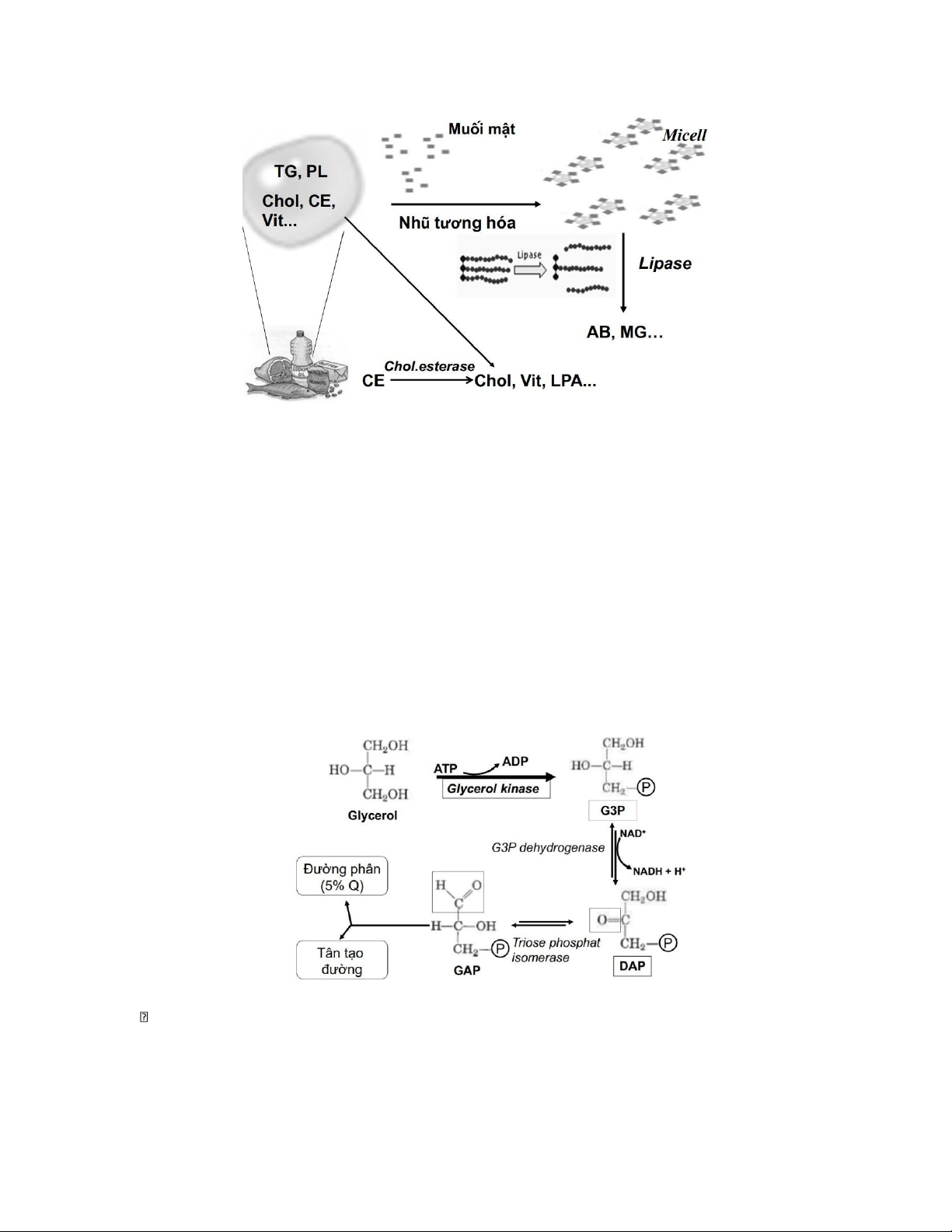
o Muối mật: nhũ tương hóa lipid. o Lipase tụy: thủy phân TG →
acid béo (AB), monoglycerid (MG). o Cholesterol esterase,
phospholipase: thủy phân CE, PL. lOMoAR cPSD| 47205411 Hấp thu -
Sản phẩm tiêu hóa (AB, MG, cholesterol…) → tạo micelle → khuếch tán vào tế bào ruột. -
Tái ester hóa thành TG, CE → chylomicron → hệ bạch huyết → máu.
3. Diễn biến – ý nghĩa của các con đường thoái hóa – tổng
hợp lipid và liên hệ chuyển hóa khác Thoái hóa lipid a. Glycerol:
Vào gan, thận → chuyển thành G3P → dùng cho tân tạo đường hoặc đường phân.
b. Acid béo (AB) – β-oxi hóa
Diễn ra tại ty thể → mỗi chu trình tạo: o 1 Acetyl-CoA o 1 NADH và 1
FADH₂ → năng lượng cao (14n – 6 ATP cho AB C )ₙ c. Thể cetonic -
Khi thiếu glucose (đói, ĐTĐ): Acetyl-CoA dư → tạo acetone, acetoacetat, βhydroxybutyrat lOMoAR cPSD| 47205411 -
Gan tổng hợp, ngoài gan sử dụng tạo năng lượng. Tổng hợp lipid
a. Tổng hợp acid béo -
Từ Acetyl-CoA và Malonyl-CoA → kéo dài chuỗi bởi enzyme FAS -
Tạo AB bão hòa, chuỗi chẵn (C16 – palmitic)
b. Tổng hợp triglycerid - Từ G3P + 3 Acyl-CoA -
Diễn ra chủ yếu ở gan, mô mỡ
b. Tổng hợp glycerophospholipid
Liên hệ với các con đường khác -
Acetyl-CoA là trung gian của Krebs, tổng hợp cholesterol, ceton, acid béo. -
Glycerol từ thoái hóa TG có thể tái sử dụng tạo glucose (tân tạo đường). -
Khi thiếu glucose: tăng β-oxi hóa, tăng cetonic (rối loạn ĐTĐ).
4. Phân tích được các yếu tố điều hòa chuyển hóa lipid
Điều hòa β-oxi hóa – tổng hợp acid béo -
Malonyl-CoA ức chế carnitin-acyl transferase I → ngăn AB vào ty thể - Hormone:
o Insulin: tăng tổng hợp AB, ức chế phân giải o Glucagon,
Adrenalin: kích hoạt HSL → tăng phân giải TG
5. Lipoprotein trong máu: nguồn gốc, cấu tạo, chức năng Loại
Nguồn gốc Thành phần chính Vai trò Chylomicro Ruột non TG ngoại sinh Vận chuyển lipid sau ăn n VLDL Gan TG nội sinh Phân phối TG tới mô LDL Từ VLDL Cholesterol Vận chuyển Chol tới mô HDL Gan, ruột Phospholipid Thu hồi Chol về gan
6.Giải thích cơ chế bệnh sinh và thuốc điều trị rối loạn chuyển hóa lipid
Xơ vữa động mạch (XVĐM) -
LDL bị oxy hóa (LDLm) → đại thực bào ăn → tế bào bọt → mảng xơ vữa -
Gây hẹp lòng mạch, nguy cơ NMCT, đột quỵ lOMoAR cPSD| 47205411
Thuốc điều trị rối loạn lipid máu -
Statin: ức chế HMG-CoA reductase → giảm tổng hợp cholesterol nội sinh -
Fibrat: giảm TG, tăng HDL -
Ezetimib: giảm hấp thu cholesterol -
Niacin: giảm LDL, tăng HDL Protein
1. Acid amin – cấu tạo, phân loại, tính chất và ứng dụng Khái niệm và cấu tạo -
Acid amin là dẫn xuất của acid hữu cơ, trong đó một hay nhiều nguyên tử hydro được
thay thế bằng nhóm amin (-NH )₂ . -
Tất cả acid amin chuẩn là L-α-amino acid, nghĩa là nhóm amin gắn tại vị trí α so với nhóm carboxyl. - Công thức tổng quát
Danh sách 20 acid amin chuẩn -
Được chia thành 2 bảng 10 tên, gồm các nhóm như Glycin (Gly), Alanin (Ala), Leucin
(Leu), Lysine (Lys), Tryptophan (Trp), v.v.




