










Preview text:
ÔN TẬP ĐẠI CƯƠNG KIM LOẠI
Câu 1. Ở điều kiện thường, kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất? A. Zn. B. Hg. C. Ag. D. Cu.
Câu 2. Kim loại nào sau đây được điều chế bằng phương pháp nhiệt luyện? A. Na. B. Al. C. Ca. D. Fe.
Câu 3. Tiến hành các thí nghiệm sau:
(a) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3.
(b) Để miếng tôn (sắt tráng kẽm) trong không khí ẩm.
(c) Nhúng thanh kẽm vào dung dịch H2SO4 loãng có nhỏ vài giọt dung dịch CuSO4.
(d) Đốt sợi dây sắt trong bình đựng khí oxi.
Trong các thí nghiệm trên, số thí nghiệm xảy ra ăn mòn điện hoá là A. 2. B. 3. C. 4. D. 1.
Câu 4. Tiến hành điện phân với điện cực trơ và màng ngăn xốp một dung dịch chứa m gam hỗn hợp
CuSO4 và NaCl cho đến khi nước bắt đầu bị điện phân ở cả hai điện cực thì dừng lại. Ở anot thu được
0,896 lít khí (đkc). Dung dịch sau khi điện phân có thể hòa tan tối đa 3,2 gam CuO. Giả sử hiệu suất của
quá trình điện phân là 100% và các khí không hoà tan trong nước. Giá trị của m là A. 11,94. B. 9,60. C. 5,97. D. 6,40.
Câu 5. Nung hỗn hợp X gồm a mol Mg và 0,25 mol Cu(NO3)2, sau một thời gian, thu được chất rắn Y và
0,45 mol hỗn hợp khí Z gồm NO2 và O2. Cho Y phản ứng vừa đủ với dung dịch chứa 1,3 mol HCl, thu
được dung dịch chỉ chứa m gam hỗn hợp muối clorua và 0,05 mol hỗn hợp khí T (gồm N2 và H2 có tỉ khối
so với H2 là 11,4). Giá trị của m gần nhất với giá trị nào sau đây? A. 82. B. 74. C. 72. D. 80.
Câu 6. Cho dãy các kim loại: Al, Cu, Fe, Ag. Số kim loại trong dãy phản ứng được với dung dịch H 2SO4 loãng là A. 1. B. 2. C. 3. D. 4.
Câu 7. Cho các nhận định sau:
(1) Trong các kim loại kiềm, xesi (Cs) có nhiệt độ nóng chảy thấp nhất.
(2) Độ dẫn điện của nhôm (Al) tốt hơn của đồng (Cu).
(3) Những kim loại có độ dẫn điện tốt thì cũng dẫn nhiệt tốt.
(4) Crom (Cr) là kim loại cứng nhất trong các kim loại.
(5) Wonfam (W) có nhiệt độ nóng chảy cao nhất trong các kim loại.
Số nhận định đúng là A. 5. B. 3. C. 4. D. 2.
Câu 8. Điện phân dung dịch hỗn hợp NaCl và 0,05 mol CuSO4 bằng dòng điện một chiều có cường độ 2A
(điện cực trơ, có màng ngăn). Sau thời gian t giây thì ngừng điện phân, thu được khí ở hai điện cực có tổng
thể tích là 2,352 lít (đktc) và dung dịch X. Dung dịch X hòa tan được tối đa 2,04 gam Al2O3. Giả sử hiệu suất
điện phân là 100%, các khí sinh ra không tan trong dung dịch. Giá trị của t là A. 9408. B. 7720. C. 9650. D. 8685.
Câu 9. Một học sinh nghiên cứu tính chất của ba dung dịch lần lượt chứa các chất A, B, C như sau:
- A tác dụng với B thu được kết tủa X, cho X vào dung dịch HNO3 loãng dư, thấy thoát ra khí không
màu hóa nâu ngoài không khí; đồng thời thu được kết tủa Y.
- B tác dụng với C thấy khí thoát ra, đồng thời thu được kết tủa.
- A tác dụng C thu được kết tủa Z, cho Z vào dung dịch HCl dư, thấy khí không màu thoát ra.
Các chất A, B và C lần lượt là
A. CuSO4, Ba(OH)2, Na2CO3.
B. FeCl2, AgNO3, Ba(OH)2
C. NaHSO4, Ba(HCO3)2, Fe(NO3)3.
D. FeSO4, Ba(OH)2, (NH4)2CO3.
Câu 10. Hòa tan hết 15,0 gam hỗn hợp X gồm Fe, Fe3O4, FeCO3 và Fe(NO3)2 trong dung dịch chứa NaHSO4
và 0,16 mol HNO3, thu được dung dịch Y và hỗn hợp khí Z gồm CO2 và NO (tỉ lệ mol tương ứng 1 : 4).
Dung dịch Y hòa tan tối đa 8,64 gam bột Cu, thấy thoát ra 0,03 mol khí NO. Nếu cho dung dịch Ba(OH)2
dư vào Y, thu được 154,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn và khí NO là sản phẩm khử
duy nhất của cả quá trình. Phần trăm khối lượng của Fe trong hỗn hợp X là A. 48,80%. B. 33,60%. C. 37,33%. D. 29,87%.
Câu 11. Dãy các ion xếp theo chiều giảm dần tính oxi hóa là.
A. Ag+, Cu2+, Fe3+, Fe2+ .
B. Ag+ , Fe3+, Cu2+, Fe2+.
C. Fe3+, Ag+, Cu2+, Fe2+.
D. Fe3+, Cu2+, Ag+, Fe2+.
Câu 12. Nhúng thanh Fe nặng m gam vào 300 ml dung dịch CuSO 4 1M, sau một thời gian, thu được dung
dịch X có chứa CuSO4 0,5M, đồng thời khối lượng thanh Fe tăng 4% so với khối lượng ban đầu. Giả sử thể
tích dung dịch không thay đổi và lượng Cu sinh ra bám hoàn toàn vào thanh sắt. Giá trị m là A. 24. B. 30. C. 32. D. 48.
Câu 13. Cho hỗn hợp rắn X gồm các chất có cùng số mol gồm BaO, NaHSO4, FeCO3 vào lượng nước dư,
lọc lấy kết tủa nung ngoài không khí đến khối lượng không đổi, thu được rắn Y chứa A. BaSO4. B. BaO và BaSO4. C. BaSO4 và Fe2O3.
D. BaSO4, BaO và Fe2O3.
Câu 14. Tiến hành điện phân dung dịch chứa 0,25 mol Cu(NO3)2 và 0,18 mol NaCl bằng điện cực trơ,
màng ngăn xốp với cường độ dòng điện không đổi tới khi khối lượng dung dịch giảm 21,75 gam thì dừng
điện phân. Cho m gam bột Fe vào vào dung dịch sau điện phân, kết thúc phản ứng, thấy thoát ra khí NO
(sản phẩm khử duy nhất) và còn lại 0,75m gam rắn không tan. Giá trị của m là A. 18,88. B. 19,33. C. 19,60. D. 18,66.
Câu 15. Cho 10,24 gam hỗn hợp X gồm Fe và Cu vào dung dịch chứa H2SO4 0,6M và NaNO3 đun nóng,
kết thúc phản ứng thu được dung dịch Y chỉ chứa các muối sunfat và 2,688 lít khí NO (sản phẩm khử duy
nhất; đktc). Cho Ba(OH)2 dư vào dung dịch Y, lọc lấy kết tủa nung ngoài không khí đến khối lượng không
đổi thu được 69,52 gam rắn khan. Giả sử thể dung dịch thay đổi không đáng kể. Nồng độ mol/l của
Fe2(SO4)3 trong dung dịch Y là A. 0,04M. B. 0,025M. C. 0,05M. D. 0,4M.
Câu 16. Tính chất hóa học đặc trưng của kim loại là A. tính bazơ. B. tính axit. C. tính oxi hóa. D. tính khử.
Câu 17. Chất nào sau đây kém bền với nhiệt? A. Na2CO3. B. BaCl2. C. Al(OH)3. D. K2SO4.
Câu 18. Điện phân dung dịch chứa 53,9 gam hỗn hợp muối NaCl và Cu(NO3)2 với điện cực trơ, màng ngăn
xốp, đến khi nước điện phân ở cả hai điện cực thì ngừng điện phân, tại thời điểm này thể tích khí sinh ở anot
gấp 1,5 lần thế tích khí thoát ra ở catot ở cùng điều kiện nhiệt độ và áp suất. Nhận xét nào sau đây không đúng?
A. Nếu cường độ dòng điện là 5 ampe thì thời gian điện phân là 3 giờ 13 phút.
B. Nếu điện phân với thời gian là 3 giờ 19 phút 26 giây với I=5 ampe rồi dừng lại thì khối lượng dung dịch giảm là 28,30 gam.
C. Khối lượng kim loại bám vào catot là 6,4 gam.
D. tỉ lệ mol hai muối NaCl : CuSO4 là 6 : 1.
Câu 19. Cho 36,24 gam hỗn hợp X gồm Fe, Fe3O4, Fe(NO3)2 vào dung dịch chứa 1,15 mol HCl và 0,04 mol HNO +
3, khuấy đều cho phản ứng xảy ra hoàn toàn thu được dung dịch Y (không chứa NH4 ) và 0,16
mol hỗn hợp khí Z gồm NO2 và NO. Cho dung dịch AgNO3 đến dư vào dung dịch Y thấy thoát ra 0,025
mol NO (sản phẩm khử duy nhất của N+5) , đồng thời thu được 173,125 gam kết tủa. Phần trăm số mol của
Fe có trong hỗn hợp ban đầu là A. 18,22%. B. 20,00%. C. 6,18%. D. 13,04%.
Câu 20. Trong các kim loại: Al, Mg, Fe và Cu, kim loại có tính khử mạnh nhất là A. Cu. B. Mg. C. Fe. D. Al.
Câu 21. Chất nào sau đây vừa phản ứng với dung dịch NaOH vừa phản ứng với dung dịch HCl? A. AlCl3. B. Al2(SO4)3. C. NaAlO2. D. Al2O3.
Câu 22. Cho 5 gam hỗn hợp X gồm Ag và Al vào dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn, thu
được 3,36 lít khí H2 (đktc). Phần trăm khối lượng của Al trong X là A. 54,0%. B. 49,6%. C. 27,0%. D. 48,6%.
Câu 23. Thực hiện các thí nghiệm sau:
(1) Cho lá kim loại Fe nguyên chất vào dung dịch CuSO4.
(2) Cho lá kim loại Al nguyên chất vào dung dịch HNO3 loãng, nguội.
(3) Đốt cháy dây Mg nguyên chất trong khí Cl2.
(4) Cho lá kim loại Fe-Cu vào dung dịch H2SO4 loãng.
Số thí nghiệm xảy ra ăn mòn hóa học là A. 4. B. 3. C. 2. D. 1.
Câu 24. Cho các phát biểu sau:
a (a) Hợp chất Fe(NO3)2 vừa có tính khử, vừa có tính oxi hóa.
b (b) Dung dịch Fe(NO3)2 tác dụng được với dung dịch HCl đặc.
c (c) Corinđon có chứa Al2O3 ở dạng khan.
d (d) Sục khí H2S vào dung dịch FeCl3 thu được kết tủa.
e (e) Na2CO3 là hóa chất quan trọng trong công nghiệp thủy tinh. Số phát biểu đúng là
A. 2. B. 5. C. 3. D. 4.
Câu 25. Hòa tan hoàn toàn hỗn hợp X gồm CuSO4 và KCl vào H2O, thu được dung dịch Y. Điện phân Y
(có màng ngăn, điện cực trơ) đến khi H2O bắt đầu điện phân ở cả hai điện cực thì dừng điện phân. Số mol
khí thoát ra ở anot bằng 4 lần số mol khí thoát ra từ catot. Giả sử các khí sinh ra không hoà tan trong nước.
Phần trăm khối lượng của CuSO4 trong X là A. 61,70%. B. 44,61%. C. 34,93%. D. 50,63%.
Câu 26. Cho hỗn hợp X gầm 0,12 mol CuO; 0,1 mol Mg và 0,05 mol Al2O3 tan hoàn toàn trong dung
dịch chứa đồng thời 0,15 mol H2SO4 (loãng) và 0,55 mol HCl, thu được dung dịch Y và khí H2. Nhỏ từ
từ dung dịch hỗn hợp Ba(OH)2 0,1M và NaOH 0,6M vào Y đến khi thu được khối lượng kết tủa lớn nhất,
lọc kết tủa đem nung đến khối lượng không đổi, thu được m gam chất rắn khan. Giá trị của m gần nhất
với giá trị nào sau đây? A. 48,54 B. 52,52.
C. 43,45. D. 38,72.
Câu 27. Kim loại nào sau đây không tác dụng với dung dịch FeCl3? A. Cu. B. Ni. C. Ag. D. Fe.
Câu 28. Kim loại nào sau đây không tác dụng với nước? A. K. B. Ca. C. Na. D. Be.
Câu 29. Nhúng thanh Zn vào dung dịch muối X, sau khi kết thúc phản ứng thu được dung dịch có khối
lượng giảm so với dung dịch ban đầu. X là A. Ni(NO3)2. B. AgNO3. C. Fe(NO3)3. D. Cu(NO3)2.
Câu 30. Tiến hành điện phân dung dịch chứa NaCl và 0,15 mol Cu(NO3)2 bằng điện cực trơ, màng ngăn xốp
với cường độ dòng điện không đổi I = 5A trong thời gian 6562 giây thì dừng điện phân, thấy khối lượng dung
dịch giảm 15,11 gam. Dung dịch sau điện phân hòa tan tối đa m gam bột Fe, phản ứng tạo ra khí NO (sản
phẩm khử duy nhất của N+5). Giả sử hiệu suất của quá trình điện phân là 100% và các khí không hoà tan
trong nước. Giá trị m là A. 2,80. B. 4,20. C. 3,36. D. 5,04.
Câu 31. Hỗn hợp rắn X gồm Mg, MgO, Fe3O4 và (trong đó oxi chiếm 21,951% khối lượng hỗn hợp). Dẫn
6,72 lít khí CO (đktc) đi qua ống sứ chứa 32,8 gam X, nung nóng. Sau một thời gian thu được hỗn hợp rắn
Y và hỗn hợp khí Z có tỉ khối so với H2 bằng 18. Hòa tan hết toàn bộ Y trong dung dịch HNO3 loãng, dư.
Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 122,7 gam muối và 4,48 lít (đktc) hỗn
hợp khí gồm NO và N2O có tỉ khối so với He là 8,375. Số mol HNO3 tham gia phản ứng là A. 1,7655. B. 1,715. C. 1,825. D. 1,845.
Câu 32. Phương pháp chung để điều ché các kim loại Na, Ca, Al trong công nghiệp là A. Thuỷ luyện.
B. Điện phân nóng chảy. C. Nhiệt luyện
D. Điện phân dung dịch.
Câu 33. Để khử hoá hoàn toàn 30 gam hỗn hợp rắn gồm CuO và Fe 2O3 bằng khí H2, thu được m gam
hỗn hợp kim loại và 4,5 gam H2O. Giá trị của m là A. 28 gam. B. 24 gam. C. 26 gam. D. 22 gam.
Câu 34. Cho Mg vào dung dịch hỗn hợp FeCl3 và CuCl2, đến khi phản ứng xảy ra hoàn toàn thu được dung
dịch X chứa 3 cation kim loại và chất rắn Y. Trong Y gồm A. Fe và Cu. B. Cu. C. Fe. D. Fe, Cu và Mg.
Câu 35. Cho thanh Fe nguyên chất lần lượt vào các dung dịch sau: HCl, CuSO4, FeCl3, H2SO4 có nhỏ vài
giọt dung dịch CuSO4. Số trường hợp mà Fe chủ yếu bị ăn mòn điện hóa là A. 4. B. 3. C. 2. D. 1.
Câu 36. Nung nóng 30,52 gam hỗn hợp gồm Ba(HCO3)2 và NaHCO3 đến khi khối lượng không đổi thu
được 18,84 gam rắn X và hỗn hợp Y chứa khí và hơi. Cho X vào lượng nước dư, thu được dung dịch Z. Hấp
thụ 1/2 hỗn hợp Y vào dung dịch Z, thu được dung dịch T chứa m gam chất tan. Giá trị của m là A. 14,64. B. 17,45. C. 16,44. D. 15,20.
Câu 37. Điện phân dung dịch X gồm FeCl2 và NaCl (tỉ lệ mol tương ứng là 1 : 2) với điện cực trơ màng
ngăn xốp thu được dung dịch Y chứa hai chất tan, biết khối lượng dung dịch X lớn hơn khối lượng dịch Y là
4,54 gam. Dung dịch Y hòa tan tối đa 0,54 gam Al. Mặt khác dung dịch X tác dụng với lượng dư dung dịch
AgNO3 thu được m gam kết tủa. Biết các phàn ứng xảy ra hoàn toàn. Giá trị m là A. 14,35. B. 17,59. C. 17,22. D. 20,46.
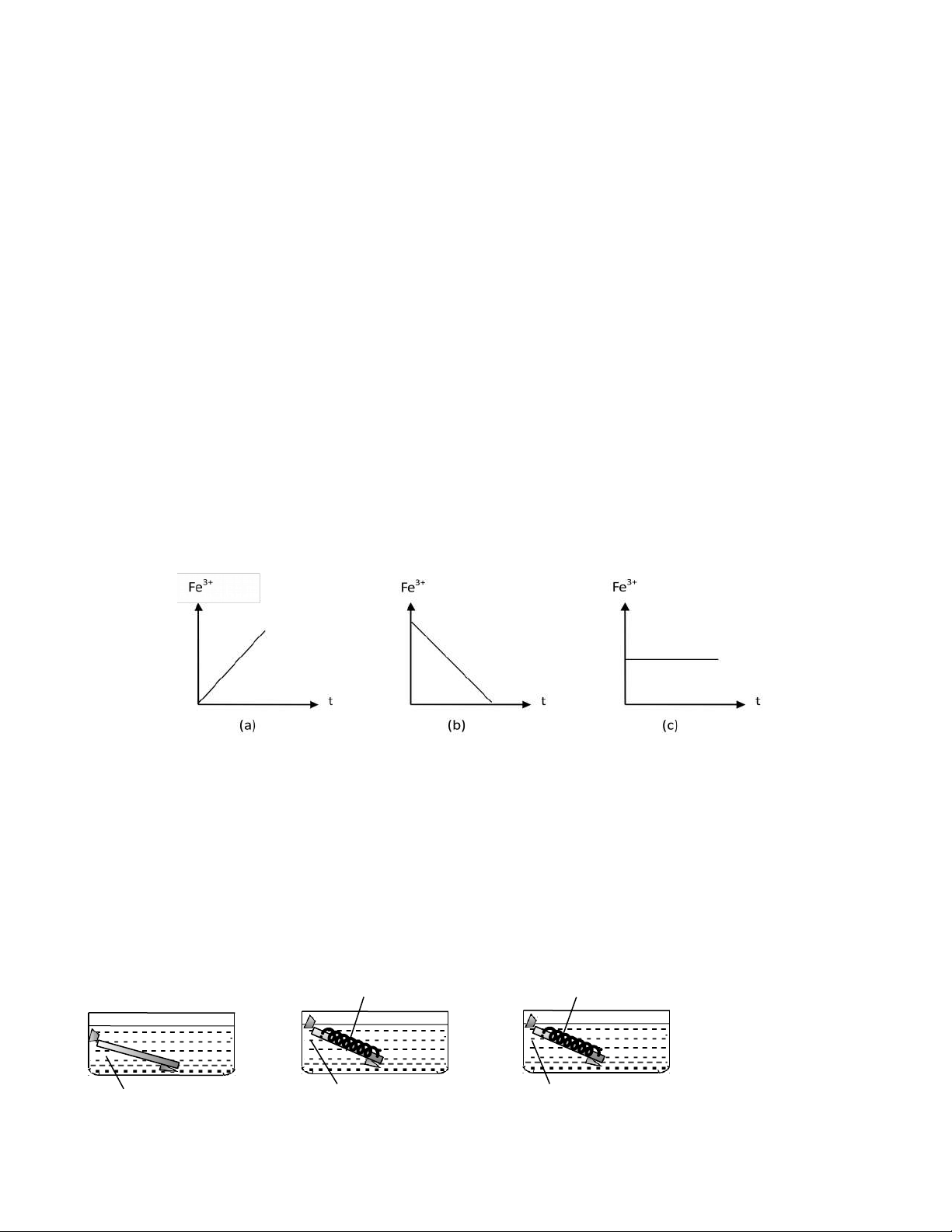
Câu 38. Cho 3 thí nghiệm sau:
(1) Cho từ từ dung dịch AgNO3 đến dư vào dung dịch Fe(NO3)2.
(2) Cho bột sắt từ từ đến dư vào dung dịch FeCl3.
(3) Cho từ từ dung dịch AgNO3 đến dư vào dung dịch FeCl3.
Trong mỗi thí nghiệm, số mol ion Fe3+ biến đổi tương ứng với đồ thị nào sau đây A. 1-a, 2-c, 3-b. B. 1-a, 2-b, 3-c. C. 1-b, 2-a, 3-c. D. 1-c, 2-b, 3-a.
Câu 39. Cho hỗn hợp X gồm FexOy, Fe, MgO, Mg. Cho m gam hỗn hợp X trên tác dụng với dung dịch
HNO3 dư thu được 6,72 lít hỗn hợp khí N2O và NO (dktc) có tỉ khối so với H2 là 15,933 và dung dịch Y. Cô
cạn dung dịch Y thu được 129,4 gam muối khan. Cho m gam hỗn hợp X tác dụng với dung dịch H2SO4 đặc
nóng dư thu được 15,68 lít khí SO2 (đktc, sản phẩm khử duy nhất) và dung dịch Z. Cô cạn dung dịch Z thu
được 104 gam muối khan. Giá trị gần nhất của m là A. 22,0. B. 28,5. C. 27,5. D. 29,0.
Câu 40. X là kim loại có nhiệt độ nóng chảy cao nhất, được sử dụng để làm sợi tóc bóng đèn thay thế cho
sợi than, sợi osimi. X là kim loại nào dưới đây? A. W. B. Cr. C. Cs. D. Ag.
Câu 41. Tiến hành thí nghiệm với 3 chậu nước như hình vẽ sau: Dây đồng Dây kẽm Đinh sắt Đinh sắt Đinh sắt Cốc 1 Cốc 2 Cốc 3
Đinh sắt trong cốc nào bị ăn mòn nhanh nhất? A. Cốc 3. B. Cốc 2 và 3. C. Cốc 2. D. Cốc 1.
Câu 42. Cho dãy các kim loại: Na, Cu, Fe, Zn, Ag. Số kim loại trong dãy phản ứng được với dung dịch HCl là A. 3. B. 2. C. 5. D. 4.
Câu 43. Cho 24,94 gam hỗn hợp gồm CuSO4 và KCl vào nước dư, thu được dung dịch X. Tiến hành điện
phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện I = 5A trong thời gian t giậy,
thấy khối lượng dung dịch giảm 9,7 gam. Nếu thời gian điện phân là 1,5t giây, khối lượng catot tăng 6,4
gam; đồng thời thu được dung dịch Y. Dung dịch Y hòa tan tối đa m gam Al2O3. Giá trị của m và t lần lượt là
A. 1,36 gam và 4632 giây.
B. 2,04 gam và 3088 giây.
C. 1,36 gam và 3088 giây.
D. 2,04 gam và 4632 giây.
Câu 44. Hòa tan hoàn toàn 8,66 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 bằng dung dịch chứa hỗn
hợp gồm 0,52 mol HCl và 0,04 mol HNO3 (vừa đủ), thu được dung dịch Y và 1,12 lít (đktc) hỗn hợp khí Z
gồm NO và H2 có tỉ khối hơi đối với H2 là 10,8. Cho dung dịch Y tác dụng với một lượng vừa đủ dung dịch
AgNO3 thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng dư dung dịch
NaOH, lọc kết tủa nung đến đến khối lượng không đổi thu được 10,4 gam chất rắn. Các phản ứng xảy ra
hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây? A. 75. B. 77. C. 79. D. 73.
Câu 45. Trong các ion sau đây, ion nào có tính oxi hóa mạnh nhất? A. Ag+. B. Cu2+. C. Zn2+. D. Ca2+.
Câu 46. Có 2 kim loại X, Y thỏa mãn các tính chất sau: Kim loại Dung dịch X Y HCl tác dụng tác dụng HNO3 đặc, nguội không tác dụng tác dụng
Các kim loại X, Y lần lượt là A. Mg, Fe. B. Fe, Mg. C. Fe, Cr. D. Fe, Al.
Câu 47. Cho các phát biểu sau:
(a) Nước cứng là nước có nhiều ion Ca2+ và Ba2+.
(b) Cho Ba vào dung dịch CuSO4 thì giải phóng ra kim loại Cu.
(c) Hỗn hợp tecmit dùng hàn đường ray xe lửa là hỗn hợp gồm Al và Fe2O3.
(d) Al(OH)3, Cr(OH)2, Zn(OH)2 đều là hiđroxit lưỡng tính.
(e) Na và Kali được dùng làm chất trao đổi nhiệt trong các lò phản ứng hạt nhân. Số phát biểu đúng là A. 1. B. 2. C. 3. D. 4.
Câu 48. Điện phân dung dịch chứa 0,2 mol CuSO4 và 0,12 mol NaCl bằng điện cực trơ, với cường độ
dòng điện không đổi I = 5A trong thời gian 4632 giây thì dừng điện phân. Nhúng thanh Mg vào dung dịch
sau điện phân, kết thúc phản ứng, khối lượng thanh Mg thay đổi như thế nào so với trước phản ứng. Giả
thiết hiệu suất điện phân là 100%. A. giảm 3,36 gam. B. tăng 3,20 gam. C. tăng 1,76 gam. D. không thay đổi.
Câu 49. Cho m gam hỗn hợp X gồm MgO, Mg, Na2O vào 415 ml dung dịch HNO3 1M, sau phản ứng thu
được dung dịch Y và 0,448 lít khí NO (đktc). Dung dịch Y phản ứng vừa đủ dung dịch chứa 0,295 mol
NaOH, thu được một lượng kết tủa, đun nóng kết tủa đến khối lượng không đổi thu được 4,4 gam rắn Z. Biết
các phản ứng xảy ra hoàn toàn. Giá trị m gần nhất với giá trị nào sau đây? A. 7,36. B. 8,82. C. 7,01. D. 8,42.
Câu 50. Hỗn hợp X gồm Mg, Al, Al2O3 và MgCO3 (trong đó oxi chiếm 25,157% về khối lượng). Hòa tan
hết 19,08 gam X trong dung dịch chứa 1,32 mol NaHSO4 và a mol HNO3, kết thúc phản ứng thu được
dung dịch Y chỉ chứa các muối trung hòa có khối lượng 171,36 gam và hỗn hợp khí Z gồm CO2, N2O,
H2. Tỉ khối của Z so với He bằng 7,5. Cho dung dịch NaOH dư vào Y, thu được 19,72 gam kết tủa. Giá trị của a là A. 0,10. B. 0,18. C. 0,16. D. 0,12.
Câu 51. Kim loại có khối lượng riêng lớn nhất là A. Cs. B. Os. C. Ca. D. Li.
Câu 52. Kim loại nào dưới đây không tan trong nước ở điều kiện thường? A. K. B. Cu. C. Na. D. Ca.
Câu 53. Tiến hành các thí nghiệm sau:
(1) Cho miếng kẽm vào dung dịch HCl loãng, có nhỏ thêm vài giọt CuSO4.
(2) Đốt dây thép trong bình đựng đầy khí oxi.
(3) Cho lá thép vào dung dịch ZnSO4.
(4) Cho lá nhôm vào dung dịch CuSO4.
Số trường hợp xảy ra sự ăn mòn điện hóa là A. 5. B. 4. C. 2. D. 3.
Câu 54. Cho m gam hỗn hợp Cu và Fe vào 200 ml dung dịch AgNO3 0,2M, sau một thời gian thu được 4,16
gam chất rắn X và dung dịch Y. Cho 5,2 gam Zn vào dung dịch Y, sau khi các phản ứng xảy ra hoàn toàn thu
được 5,82 gam chất rắn Z và dung dịch chỉ chứa một muối duy nhất. Giá trị của m gần nhất với giá trị nào sau đây? A. 1,75. B. 2,25. C. 2,00. D. 1,50.
Câu 55. Thực hiện các thí nghiệm sau:
(1) Đốt dây sắt trong khí clo.
(2) Đốt cháy hỗn hợp sắt và lưu huỳnh (trong điều kiện không có không khí).
(3) Cho sắt (II) oxit vào dung dịch axit sunfuric đặc nóng.
(4) Cho sắt vào dung dịch đồng (II) sunfat.
(5) Cho đồng vào dung dịch sắt (III) clorua.
(6) Cho oxit sắt từ tác dụng với dung dịch axit clohidric.
Số thí nghiệm tạo ra muối sắt (II) là A. 4. B. 3. C. 5. D. 2.
Câu 56. Cho các phát biểu sau:
(a) Các kim loại Na, K và Al đều phản ứng mạnh với nước.
(b) Dung dịch muối Fe(NO3)2 tác dụng được vớỉ dung dịch HCl.
(c) Than chì được dùng làm điện cực, chế tạo chất bôi trơn, làm bút chì đen.
(d) Hỗn hợp Al và NaOH (tỉ lệ số mol tương ứng 1:1) tan hoàn toàn trong nước dư.
(e) Người ta không dùng CO2 để dập tắt đám cháy magie hoặc nhôm. Số phát biểu đúng là A. 3. B. 4. C. 5. D. 2.
Câu 57. Điện phân 200 ml dung dịch X có chứa Cu(NO3)2 x mol/l và NaCl 0,06 mol/l với cường độ dòng
điện 2A. Nếu điện phân trong thời gian t giây ở anot thu được 0,448 lít khí. Nếu điện phân trong thời gian 2t
giây thì thể tích thu được ở 2 điện cực là 1,232 lít. Các khí đo ở điều kiện tiêu chuẩn và giả sử khí sinh ra
không hoà tan trong nước. Giá trị của x là A. 0,20. B. 0,15. C. 0,10. D. 0,25.
Câu 58. Phản ứng nào xảy ra ở catot trong quá trình điện phân MgCl2 nóng chảy?
A. Sự oxi hoá ion Mg2+. B. Sự khử ion Mg2+. C. Sự oxi hoá ion Cl-. D. Sự khử ion Cl-.
Câu 59. Oxit kim loại nào sau đây khi tan trong nước tạo thành dung dịch bazơ là A. NO2. B. K2O. C. CO2. D. P2O5.
Câu 60. Oxit nào sau đây là oxit bazơ? A. Al2O3. B. Cr2O3. C. CrO3. D. Fe2O3.
Câu 61. Cho các phát biểu sau:
(a) Muối kali đicromat có màu da cam.
(b) Phèn chua được dùng làm chất cầm màu trong ngành nhuộm vải.
(c) Các chất S, C, C2H5OH bốc cháy khi tiếp xúc với CrO3.
(d) Cr và Fe tác dụng với oxi đều tăng lên số oxi hóa +3.
(e) Nhiệt độ nóng chảy của các kim loại kiềm thổ giảm dần từ Be đến Ba. Số phát biểu đúng là A. 5. B. 4. C. 3. D. 2.
Câu 62. Điện phân 1 lít dung dịch X gồm Cu(NO3)2 0,6M và FeCl3 0,4M đến khi anot thoát ra 17,92 lít khí
(đktc) thì dừng lại. Lấy catot ra khỏi bình điện phân, khuấy đều dung dịch để phản ứng xảy ra hoàn toàn thì
thu được dung dịch Y. Giả thiết kim loại sinh ra đều bám lên catot, sản phẩm khử của N+5 (nếu có) là NO duy
nhất. Giá trị (mX – mY) gần nhất với giá trị nào sau đây? A. 92 gam. B. 102 gam. C. 99 gam. D. 91 gam.
Câu 63. Ion kim loại nào sau đây có tính oxi hóa yếu nhất? A. Fe3+. B. Mg2+. C. Ag+. D. Cu2+.
Câu 64. Chất nào sau đây không bị oxi hoá bởi H2SO4 đặc, nóng là A. Al. B. Fe3O4. C. FeCl2. D. CuO.
Câu 65. Cho 8,0 gam hỗn hợp bột X gồm Mg và Fe (tỉ lệ mol tương ứng 1 : 1) tác dụng hoàn toàn với 100
ml dung dịch CuSO4 0,5M, sau phản ứng thu được m gam kim loại. Giá trị của m là A. 11,60. B. 10,00. C. 6,80. D. 8,40.
Câu 66. Thực hiện các thí nghiệm sau:
(a) Nhúng thanh Fe nguyên chất vào dung dịch CuSO4.
(b) Cho bột Fe vào dung dịch HNO3 đặc, nguội.
(c) Đốt cháy dây kim loại Fe trong khí Cl2.
(d) Cho hợp kim Fe-Cu vào dung dịch H2SO4 loãng.
(e) Nhúng miếng tôn (Fe-Zn) vào dung dịch muối ăn.
Số thí nghiệm xảy ra ăn mòn kim loại là A. 3. B. 4. C. 2. D. 5.
Câu 67. Cho 14,35 gam muối MSO4.nH2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến
hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi trong thời
gian t giây, thấy khối lượng catot tăng m gam; đồng thời ở anot thu được 0,1 mol khí. Nếu thời gian điện
phân là 2t giây, tổng thể tích khí thoát ra ở 2 cực là 7,28 lít (đktc). Giả sử hiệu suất của phản ứng điện phân là 100%. Giá trị của m là A. 7,15. B. 7,04. C. 3,25. D. 3,20.
Câu 68. Hỗn hợp X gồm FeO và Fe3O4 có tỉ lệ mol tương ứng là 1 : 3. Cho một luồng CO đi qua ống sứ
đựng m gam X nung nóng, sau một thời gian thu được 6,96 gam hỗn hợp Y gồm Fe, FeO và Fe3O4. Hòa
tan hoàn Y trong dung dịch HNO3 dư thu được 2,24 lít (đkc) hỗn hợp Z gồm NO và NO2 (không có sản
phẩm khử khác của N+5), tỉ khối của Z so với metan là 2,725. Giá trị của m là A. 10,34. B. 6,82. C. 7,68. D. 30,40.
Câu 69. Nung nóng 25,5 gam hỗn hợp gồm Al, CuO và Fe3O4 trong điều kiện không có không khí, thu được
hỗn hợp rắn X. Chia X làm 2 phần bằng nhau. Phần 1 cho vào dung dịch NaOH loãng dư, thấy lượng NaOH
phản ứng là 6,8 gam; đồng thời thoát ra a mol khí H2 và còn lại 6,0 gam rắn không tan. Hòa tan hết phần 2
trong dung dịch chứa 0,4 mol H2SO4 và x mol HNO3, thu được dung dịch Y chỉ chứa các muối trung hòa có
tổng khối lượng là 49,17 gam và a mol hỗn hợp khí Z gồm NO, N2O và H2 (trong đó H2 có số mol là 0,02
mol). Các phản ứng xảy ra hoàn toàn. Giá trị của x là A. 0,09. B. 0,13. C. 0,12. D. 0,15.
Câu 70. Để điều chế Cu từ dung dịch CuSO4 theo phương pháp thuỷ luyện người ta dùng kim loại nào sau đây làm chất khử? A. Ca. B. Na. C. Ag. D. Fe.
Câu 71. Trong thí nghiệm nào sau đây xảy ra ăn mòn điện hóa?
A. Cho lá đồng nguyên chất vào dung dịch gồm Fe(NO3)3 và HNO3.
B. Để thanh thép đã sơn kín trong không khí khô.
C. Nhúng thanh kẽm nguyên chất vào dung dịch HCl.
D. Cho lá sắt nguyên chất vào dung dịch gồm CuSO4 và H2SO4 loãng.
Câu 72. Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn
sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). M là A. Mg. B. Ca. C. Fe. D. Al.
Câu 73. Cho các kim loại sau: Na, Al, Fe, Cu, Ag. Số kim loại khử được ion Fe3+ trong dung dịch là A. 3. B. 1. C. 4. D. 2.
Câu 74. Có các nhận xét sau về kim loại và hợp chất của nó:
(1) Nhôm vừa tan trong dung dịch HCl, vừa tan trong dung dịch NaOH.
(2) Mạ niken lên vật bằng sắt là phương pháp bảo vệ bề mặt.
(3) CaSO4 được gọi là thạch cao khan.
(4) Na, Ba đều kim loại kiềm thổ.
(5) Mg không phản ứng với nước ở bất kì nhiệt độ nào.
Trong các nhận xét trên, số nhận xét đúng là A. 2. B. 3. C. 4. D. 1.
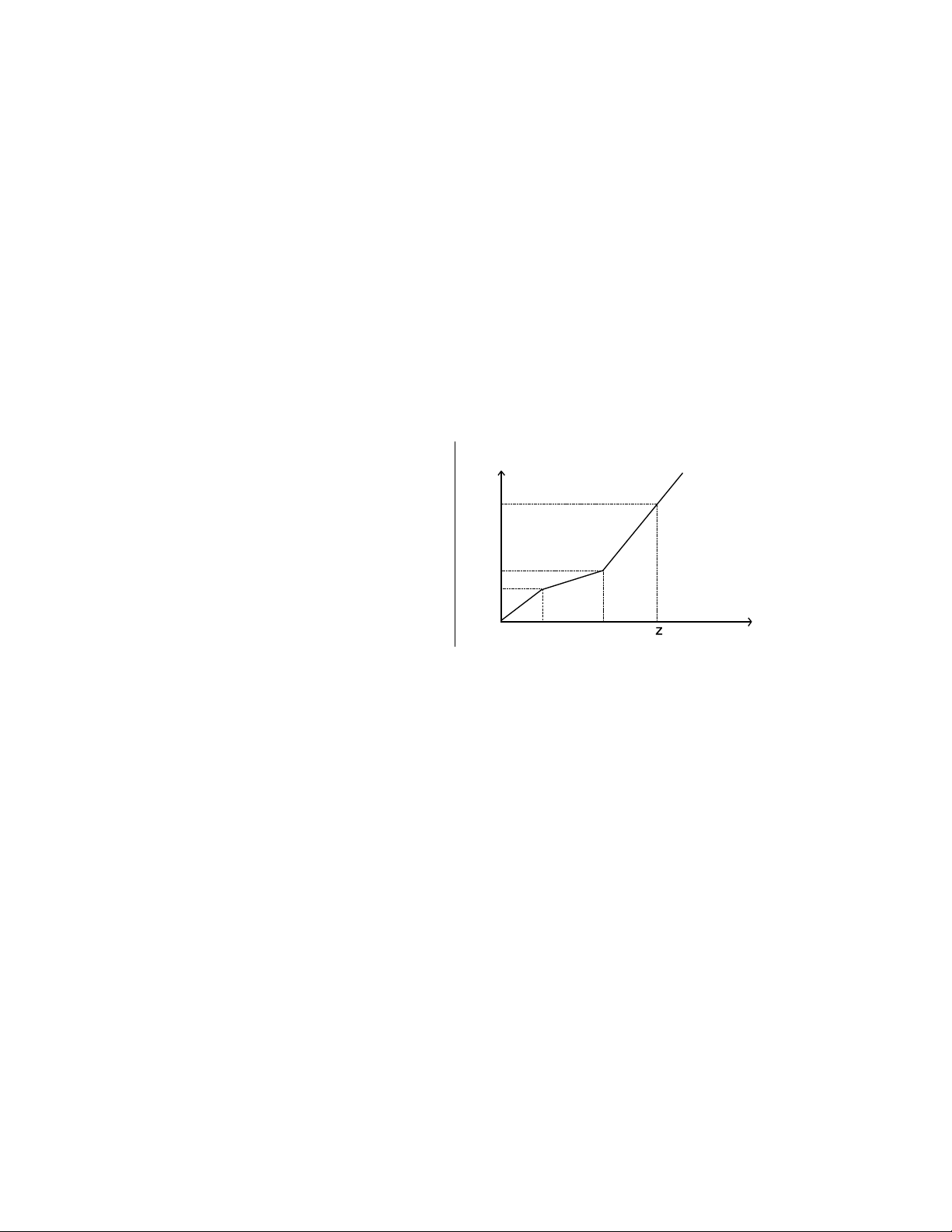
Câu 75. Điện phân dung dịch hỗn hợp CuSO4 và
Theåtích khí ôûñktc (lít)
KCl bằng dòng điện một chiều có cường độ 5A
(điện cực trơ, màng ngăn xốp, hiệu suất điện phân 3,248
100%, các khí sinh ra không tan trong dung dịch).
Toàn bộ khí sinh ra trong quá trình điện phân (ở cả
hai điện cực) theo thời gian được biểu diễn bằng 1,568
đồ thị bên. Giá trị của z là 0,896 A. 5790. B. 3860. C. 6755. D. 7720. 0 Thôiøgian (giaây) x y
Câu 76. Hoà tan hoàn toàn 7,9 gam hỗn hợp X gồm Mg, Al và Fe (tỉ lệ mol tương ứng là 2:2:1) bằng lượng
vừa đủ dung dịch chứa 0,815 mol HCl và x mol KNO3. Phản ứng kết thúc được 2,464 lít NO (đktc) và dung
dịch Y chỉ chứa muối clorua. Cho Y tác dụng với dung dịch AgNO3 dư thu được m gam kết tủa Giá trị của m
gần nhất với giá trị nào sau đây? A. 122,5. B. 118. C. 119. D. 117.
Câu 77. Tính chất nào sau đây không phải là tính chất vật lý chung của kim loại? A. Dẫn nhiệt. B. Cứng. C. Ánh kim. D. Dẫn điện.
Câu 78. Cặp chất không xảy ra phản ứng hoá học là
A. Cu và dung dịch FeCl3.
B. Fe và dung dịch HCl.
C. Fe và dung dịch FeCl3.
D. Cu và dung dịch FeCl2.
Câu 79. Cho các trường hợp bảo vệ kim loại sau đây:
(1) Tráng thiếc lên bề mặt vật bằng sắt (sắt tây).
(2) Gắn miếng kẽm kim loại vào chân vịt của tàu thuỷ để bảo vệ vỏ tàu.
(3) Mạ niken lên vật bằng sắt.
(4) Ngâm Na trong dầu hoả.
Số trường hợp kim loại được bảo vệ theo phương pháp điện hoá là A. 1. B. 3. C. 2. D. 4.
Câu 80. Cho các phát biểu sau:
(a) Để một miếng gang (hợp kim sắt – cacbon) ngoài không khí ẩm, sẽ xảy ra sự ăn mòn điện hóa.
(b) Kim loại cứng nhất là W (vonfram).
(c) Hòa tan Fe3O4 bằng dung dịch HCl vừa đủ, thu được dung dịch chứa 2 muối.
(d) Khi điện phân NaCl nóng chảy (điện cực trơ), tại catot xảy ra sự oxi hóa ion Na+.
(e) Không thể dùng khí CO2 để dập tắt đám cháy magie hoặc nhôm. Số phát biểu đúng là A. 3. B. 2. C. 1. D. 4.
Câu 81. Cho hỗn hợp X gồm CuO và NaOH có tỉ lệ số mol 1:1 tác dụng vừa đủ với dung dịch hỗn hợp
HCl 1M và H2SO4 0,5M thu được dung dịch Y chỉ chứa m gam hỗn hợp muối trung hòa. Điện phân dung
dịch Y với điện cực trơ màng ngăn xốp cường độ I = 2,68A đến khi khối lượng dung dịch giảm 20,225
gam mất t giây thì dừng lại, thu được dung dịch Z. Cho m gam Fe vào Z, sau khi phản ứng kết thúc thu
được 0,9675m gam hỗn hợp hai kim loại. Giá trị của t là A. 11523. B. 10684. C. 12124. D. 14024.
Câu 82. Cho m gam Mg vào 200ml dung dịch chứa AgNO3 2,5M và Cu(NO3)2 3M, sau một thời gian thu
được 80,8 gam hỗn hợp rắn X và dung dịch Y chỉ gồm 2 muối. Nhúng thanh sắt nặng 8,4 gam vào dung dịch
Y, sau khi các phản ứng xảy ra hoàn toàn, lấy thanh sắt, rửa sạch cân nặng 10 gam. Cho m gam Mg trên vào
dung dịch HNO3 đặc, nóng, dư không thấy khí thoát ra và thu được dung dịch Z. Khối lượng muối khan trong Z là A. 103,6. B. 106,3. C. 117,6. D. 116,7.
Câu 83. X, Y, Z, M là các kim loại. Thực hiện các thí nghiệm sau: Thí nghiệm 1
M dung dòch muoái cuûa X − −⟶ keát tuûa khí Thí nghiệm 2
X dung dòch muoái cuûa Y − −⟶ Y Thí nghiệm 3
X dung dòch muoái cuûa Z: khoâng xaûy ra phaûn öùng Thí nghiệm 4
Z dung dòch muoái cuûa M : khoâng xaûy ra phaûn öùng
Chiều tăng dần tính khử của các kim loại X, Y, Z, M là
A. Y < X < M < Z.
B. Z < Y < X < M. C. M < Z < X < Y.
D. Y < X < Z < M.
Câu 84. Cho 7,488 gam hỗn hợp rắn X gồm Fe, Fe3O4 và Fe(NO3)2 vào dung dịch chứa 0,3 mol HCl và
0,024 mol HNO3, khuấy đều cho các phản ứng xảy ra hoàn toàn thu được dung dịch Y (không chứa NH +
4 ) và 0,032 mol hỗn hợp khí Z gồm NO và N2O. Cho dung dịch AgNO3 đến dư vào dung dịch Y, sau
phản ứng thấy thoát ra 0,009 mol NO (sản phẩm khử duy nhất của N+5), đồng thời thu được 44,022 gam
kết tủa. Phần trăm khối lượng Fe trong hỗn hợp X có giá trị gần nhất với giá trị nào sau đây? A. 46,6%. B. 35,8%. C. 37,8%. D. 49,6%.
Câu 85. Kim loại nào sau đây không tác dụng với dung dịch H2SO4 loãng? A. Fe. B. Cu. C. Na. D. Mg.
Câu 86. Dẫn khí CO dư qua hỗn hợp bột gồm MgO, CuO, Al2O3 và Fe3O4, nung nóng. Sau khi các phản ứng
xảy ra hoàn toàn, thu được hỗn hợp rắn Y. Số oxit kim loại có trong Y là A. 3. B. 1. C. 4. D. 2.
Câu 87. Cho 5,4 gam Al vào dung dịch chứa 0,2 mol FeCl 3 và 0,3 mol HCl. Sau khi các phản ứng hoàn
toàn, thu được m gam chất rắn. Giá trị của m là A. 8,4. B. 2,8. C. 4,2. D. 5,6.
Câu 88. Cho các thí nghiệm sau:
(a) Cho bột Cu vào dung dịch FeCl3.
(b) Cho bột sắt vào dung dịch HCl và NaNO3.
(c) Cho miếng Na vào dung dịch CuSO4.
(d) Cho miếng Zn vào dung dịch AgNO3.
Số thí nghiệm có xảy ra hiện tượng ăn mòn điện hóa học là A. 3. B. 4. C. 2. D. 1.
Câu 89. Cho các phát biểu sau:
(a) Gang là hợp kim của sắt với cacbon, chứa từ 2-5% khối lượng cacbon.
(b) Các kim loại K, Al và Mg chỉ điều chế được bằng phương pháp điện phân nóng chảy.
(c) Dung dịch hỗn hợp FeSO4 và H2SO4 làm mất màu dung dịch KMnO4.
(d) Cr(OH)3 tan được trong dung dịch axit mạnh và kiềm.
(e) Tất cả các kim loại đều tác dụng được với khí oxi ở trong điều kiện thích hợp. Số phát biểu đúng là A. 5. B. 2. C. 3. D. 4.
Câu 90. Điện phân (với các điện cực trơ, màng ngăn) dung dịch chứa m gam hỗn hợp gồm Cu(NO3)2 và
NaCl bằng dòng điện có cường độ 2,68A. Sau thời gian 6h, tại anot thoát ra 4,48 lít khí (đktc). Thêm 20
gam bột sắt vào dung dịch sau điện phân, thu được khí NO (sản phẩm khử duy nhất của NO - 3 ) và 12,4
gam chất rắn gồm hai kim loại. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là A. 86,9. B. 77,5. C. 97,5. D. 68,1.
Câu 91. Kim loại nào sau đây có tính khử yếu hơn Cu là A. Ag. B. Fe. C. Na. D. Al.
Câu 92. Đốt hỗn hợp Fe và Cu trong bình chứa khí clo dư, thu được sản phẩm muối gồm A. FeCl2 và CuCl. B. FeCl2 và CuCl2. C. FeCl3 và CuCl. D. FeCl3 và CuCl2.
Câu 93. Tàu biển với lớp vỏ thép dễ bị ăn mòn bởi môi trường không khí và nước biển. Để bào vệ các tàu
thép ngoài việc sơn bỏ vệ, người ta còn gắn vào vỏ tàu một số tấm kim loại. Tấm kim loại đó là A. Thiếc. B. Đồng. C. Chì. D. Kẽm.
Câu 94. Cho các phát biểu sau:
(a) Khi điện phân dung dịch CuSO4 (điện cực trơ) tại anot H2O bị khử tạo ra khí O2.
(b) Để lâu hợp kim Fe-Cu trong không khí ẩm thì Fe bị ăn mòn điện hóa.
(c) Ở nhiệt độ cao, khí CO khử được Al2O3 tạo thành Al và khí CO2.
(d) Gang xám chủ yếu được dùng để đúc bệ máy, ống dẫn nước, cánh cửa,…
(e) Trong tự nhiên, crom chỉ tồn tại dưới dạng hợp chất. Số phát biểu đúng là A. 2. B. 5. C. 3. D. 4.
Câu 95. Cho 61,25 gam tinh thể MSO4.5H2O vào 300 ml dung dịch NaCl 0,6M thu được dung dịch X. Tiến
hành điện phân (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong
nước và sự bay hơi của nước) dung dịch X với cường độ dòng điện không đổi, trong thời gian t giây, thấy
khối lượng catot tăng m gam, đồng thời ở anot thu được 0,15 mol khí. Nếu thời gian điện phân là 2t giây,
tổng số mol khí thoát ra ở hai cực là 0,425 mol. Giá trị của m là A. 13,44. B. 11,80. C. 12,80. D. 12,39.
Câu 96. Cho a gam hỗn hợp X gồm Al, Al2O3, Mg, MgO, Fe, FeO, Fe2O3 và Fe3O4 (biết mX = 4,625mO)
tác dụng hết với dung dịch Y gồm NaHSO4 và NaNO3, thu được dung dịch Z chỉ chứa b gam muối trung
hòa 1,12 lít hỗn hợp khí T (đktc) gồm 2 khí không màu (trong đó có 1 khí hóa nâu trong không khí) có tỉ
khối của T so với H2 bằng 6,6. Cho từ từ dung dịch KOH vào 1/2 dung dịch Z đến khi kết tủa lớn nhất
thì dùng hết 0,21 mol KOH. Cho dung dịch BaCl2 vào một nửa dung dịch Z còn lại thu được 52,425 gam
kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị gần nhất của b là A. 48,9. B. 49,3. C. 59,8. D. 60,3.
Câu 97. Kim loại nào sau đây phản ứng được với dung dịch CuSO4 và dung dịch HNO3 đặc, nguội? A. Mg. B. Al. C. Fe. D. Ag.
Câu 98. Trong khí quyển có các chất sau: O2, Ar, CO2, H2O, N2. Những chất nào là nguyên nhân gây ra sự
ăn mòn kim loại phổ biến? A. O2 và H2O. B. CO2 và O2. C. CO2 và H2O. D. O2 và N2.
Câu 99. Cho hỗn hợp gồm Al và Fe vào dung dịch chứa Cu(NO3)2 và FeCl3, sau phản ứng hoàn toàn thu
được chất rắn X gồm hai kim loại và dung dịch Y chứa hai muối. Cation kim loại có trong dung dịch Y là A. Al3+. B. Al3+ và Cu2+. C. Fe2+. D. Al3+ và Fe2+.
Câu 100. Tiến hành điện phân dung dịch chứa m gam hỗn hợp gồm CuSO4 và KCl bằằng điện cực trơ, màng
ngằn xốốp với cường độ dòng điện khống đổi. Kếốt quả quá trình điện phân được ghi theo bảng sau: Thời gian Catot (-) Anot (+) t (giây)
Khối lượng tăng 10,24 gam
2,24 lít hỗn hợp khí (đktc) 2t (giây)
Khối lượng tăng 15,36 gam
V lít hỗn hợp khí (đktc)
Nhận định nào sau đây đúng?
A. Giá trị của V là 4,480 lít.
B. Giá trị của m là 44,36 gam.
C. Giá trị của V là 4,928 lít.
D. Giá trị của m là 43,08 gam.
Câu 101. Trộn m gam hỗn hợp X gồm Mg, Fe, Fe3O4, Cu và CuO (trong đó nguyên tố oxi chiếm 12,82%
theo khối lượng hỗn hợp X) với 7,05 gam Cu(NO3)2, thu được hỗn hợp Y. Hoà tan hoàn toàn Y trong
dung dich chứa đồng thời HCl; 0,05 mol KNO3 và 0,1 mol NaNO3. Sau khi các phản ứng xảy ra hoàn
toàn, thu được dung dịch Z chỉ chứa muối clorua và 3,36 lít (đktc) hỗn hợp khí T gồm N2 và NO. Tỉ khối
của T so với H2 là 14,667. Cho Z phản ứng với dung dịch Ba(OH)2 dư, kết thúc các phản ứng thu được
56,375 gam kết tủa. Giá trị của m gần nhất với giá trị nào sau đây? A. 30,5. B. 32,2. C. 33,3. D. 31,1.
Câu 102. Điện phân nóng chảy NaCl (với các điện cực trơ), tại catot xảy ra quá trình A. khử H2O. B. khử ion Na+. C. oxi hóa H2O. D. oxi hóa ion Cl-.
Câu 103. Phương trình hóa học nào sau đây sai?
A. 2Na + 2HCl → 2NaCl + H2.
B. Cu + 2HCl → CuCl2 + H2.
C. Zn + 2AgNO3 → Zn(NO3)2 + 2Ag.
D. Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4.
Câu 104. Giấy "bạc" được làm từ quá trình dát mỏng các miếng kim loại A. Cu. B. Al. C. Zn. D. Ag.
Câu 105. Thí nghiệm nào sau đây có xảy ra ăn mòn điện hóa học?
A. Cho miếng nhôm vào dung dịch NaOH.
B. Ngâm miếng hợp kim Fe-Cu trong dung dịch muối ăn.
C. Cho miếng Na vào dung dịch CuSO4.
D. Đốt miếng gang (hợp kim Fe-C) trong bình chứa khí oxi.
Câu 106. Điện phân (với điện cực trơ, màng ngăn) dung dịch chứa hỗn hợp gồm Cu(NO3)2 và 0,10 mol
NaCl bằng dòng điện một chiều có cường độ 2,68A. Sau t (h), thì màu xanh của dung dịch mất đi và thu
được dung dịch X. Dung dịch X hòa tan tối đa 1,92 gam Mg, sau phản ứng thu được 358,4 ml khí N2O (khí
duy nhất thoát ra, ở đktc). Giá trị của t là A. 2,0h. B. 3,0h. C. 2,5h. D. 1,5h.
Câu 107. Kim loại X là một kim loại quý, dẫn điện tốt nhất trong số các kim loại và có nhiều ứng dụng: làm
phim ảnh, gương cầu... X là A. Al. B. Ag. C. Cr. D. Fe.
Câu 108. Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy? A. Fe. B. Cu. C. K. D. Ag.
Câu 109. Cho 5,4 gam Mg vào 300 ml dung dịch CuSO4 0,5M. Sau khi phản ứng hoàn toàn, thu được m
gam chất rắn. Giá trị của m là A. 12,8. B. 9,6. C. 14,4. D. 11,4.
Câu 110. Tiến hành các thí nghiệm sau:
(a) Nhúng thanh đồng nguyên chất vào dung dịch FeCl3.
(b) Nhúng thanh sắt vào nước.
(c) Nhúng thanh bạc vào dung dịch H2SO4 loãng.
(d) Nhúng thanh nhôm vào dung dịch KOH.
Trong các thí nghiệm trên, số thí nghiệm xảy ra phản ứng ở điều kiện thường là A. 2. B. 3. C. 1. D. 4.
Câu 111. Hỗn hợp X chứa Mg, Fe, Cu, FeO, Fe2O3, Fe3O4 và CuO, trong đó oxi chiếm 3,5% khối lượng.
Đun nóng m gam X với 0,448 lít khí CO một thời gian thu được rắn Y và hỗn hợp khí Z có tỷ khối hơi
so với hiđro bằng 16. Hoà tan hết Y trong dung dịch chứa 1,3 mol HNO3, thu được dung dịch T chứa
84,72 gam muối và 2,688 lít hỗn hợp khí G chứa NO và N2. Biết G có tỷ khối hơi đối với hiđro bằng
89/6. Biết thể tích các khí đều đo ở đktc. Giá trị của m là A. 19,2. B. 12,8. C. 16,0. D. 32,0.
Câu 112. Điện phân dung dịch chứa 11,7 gam NaCl và x gam Cu(NO3)2 (điện cực trơ, màng ngăn xốp)
sau một thời gian thu được dung dịch X và khối lượng dung dịch giảm 25,5 gam. Cho thanh Mg (dư) vào
dung dịch X đến khi các phản ứng xảy ra hoàn toàn thấy khối lượng thanh Mg tăng 9,18 gam và thoát ra
0,56 lít khí NO, cô cạn dung dịch thu được m gam muối khan. Phát biểu nào sau đây đúng?
A. Dung dịch X có chứa NaOH.
B. Giá trị của x là 94.
C. Khối lượng Mg phản ứng là 9,84 gam.
D. Giá trị của m là 63,39.
Câu 113. Kim loại kiềm nào sau đây nhẹ nhất? A. Li. B. Na. C. K. D. Rb.
Câu 114. Cho 7,8 gam bột Zn vào 200 ml dung dịch AgNO3 1,0M. Sau khi phản ứng hoàn toàn thu được
m gam hỗn hợp kim loại. Giá trị của m là A. 29,4. B. 21,6. C. 22,9. D. 10,8.
Câu 115. Tiến hành các thí nghiệm sau:
(a) Nhúng thanh gang (hợp kim sắt và cacbon) vào dung dịch NaCl.
(b) Đốt dây sắt trong bình đựng đầy khí O2.
(c) Nhúng thanh Fe nguyên chất vào dung dịch FeCl3.
(d) Để miếng sắt tây (sắt tráng thiếc) trong không khí ẩm.
Trong các thí nghiệm trên, số thí nghiệm mà Fe bị ăn mòn điện hóa học là A. 3. B. 1. C. 4. D. 2.
Câu 116. Điện phân dung dịch X chứa đồng thời 0,04 mol HCl và a mol NaCl (điện cực trơ, màng ngăn
xốp, cường độ dòng điện không đổi, hiệu suất điện phân 100%) trong thời gian t giây thì thu được 1,344
lít hỗn hợp hai khí trên các điện cực trơ. Mặt khác, khi điện phân X trong thời gian 2t giây thì thu được
1,12 lít khí (đktc) hỗn hợp khí trên anot. Giá trị của a là A. 0,04. B. 0,02. C. 0,06. D. 0,01.
Câu 117. Nung m gam hỗn hợp A gồm Mg, FeCO3, FeS và Cu(NO3)2 (trong đó phần trăm khối lượng oxi
chiếm 47,818%) một thời gian, thu được chất rắn B (không chứa muối nitrat) và 11,144 lít hỗn hợp khí gồm
CO2, NO2, O2, SO2. Hoà tan hết B với dung dịch HNO3 đặc nóng, dư (thấy có 0,67 mol HNO3 phản ứng), thu
được dung dịch C và 3,136 lít hỗn hợp X gồm NO =321 / 14 2 và CO2 ( dX/H2
). Đem C tác dụng hoàn toàn với
dung dịch BaCl2 dư, thu được 2,33 gam kết tủa. Biết các khí đo ở đktc. Giá trị của m gần nhất với giá trị nào sau đây là A. 48. B. 33. C. 40. D. 42.
Câu 118. Phương trình phản ứng hóa học nào sau đây không đúng?
A. Fe + CuSO4 → FeSO4 + Cu
B. Ba + 2H2O → Ba(OH)2 + H2
C. 2Cr + 6HCl → 2CrCl3 + 3H2
D. KOH + KHCO3 → K2CO3 + H2O
Câu 119. Ở nhiệt độ cao, khí hiđro khử được oxit nào sau đây? A. CaO. B. Na2O. C. CuO. D. MgO.
Câu 120. Kim loại Cu không tác dụng với
A. dung dịch HNO3 loãng. B. dung dịch AgNO3.
C. dung dịch H2SO4 đặc.
D. dung dịch HCl loãng.
Câu 121. Cho 5,4 gam bột Al vào dung dịch chứa 0,15 mol CuSO 4. Sau phản ứng hoàn toàn, thu được m
gam chất rắn. Giá trị của m là A. 12,3. B. 15,5. C. 9,6. D. 12,8.
Câu 122. Thực hiện các thí nghiệm sau:
(a) Nhúng thanh Fe vào dung dịch CuSO4.
(b) Cho miếng gang (hợp kim Fe-C) vào dung dịch HCl.
(c) Cho miếng Na vào dung dịch AgNO3.
(d) Quấn dây Cu quanh thanh Al và nhúng vào dung dịch HCl.
(e) Cho miếng Cu vào dung dịch FeCl3.
(f) Cho miếng sắt vào dung dịch HCl và ZnCl2.
Số thí nghiệm có xảy ra ăn mòn điện hóa học là A. 2. B. 4. C. 5. D. 3.
Câu 123. Điện phân dung dịch X chứa a mol CuSO4 và 0,2 mol KCl (điện cực trơ, màng ngăn xốp,
cường độ dòng điện không đổi) trong thời gian t giây, thu được 2,464 lít khí ở anot (đktc). Nếu thời gian
điện phân là 2t giây thì tổng thể tích khí thu được ở cả hai điện cực là 5,824 lít (đktc). Biết hiệu suất điện
phân 100%, các khí sinh ra không tan trong dung dịch. Giá trị của a là A. 0,26. B. 0,15. C. 0,24. D. 0,18.
Câu 124. Kim loại nào trong số các kim loại dưới đây không khử được ion Fe3+ trong dung dịch? A. Cu. B. Zn. C. Ag. D. Fe.
Câu 125. Kim loại nào sau đây thuộc nhóm B trong bảng tuần hoàn? A. K. B. Cr. C. Al. D. Mg.
Câu 126. Khi điện phân Al2O3 nóng chảy (điện cực trơ bằng than chì), khí nào sau đây không sinh ra ở điện cực anot? A. H2. B. O2. C. CO2. D. CO.
Câu 127. Cho m gam bột sắt vào 200 ml dung dịch HNO3 4M. Sau phản ứng hoàn toàn, thu được khí NO
(sản phẩm khử duy nhất) và còn lại 1 gam bột sắt chưa tan. Giá trị của m là A. 16,8. B. 17,8. C. 15,0. D. 12,2.
Câu 128. Cho 2 gam hỗn hợp X gồm Mg, Al, Fe và Zn tác dụng với dung dịch hỗn hợp chứa HCl và H2SO4
loãng dư, sau phản ứng thu 0,05 mol khí. Mặt khác, cho 2 gam hỗn hợp X tác dụng với Cl2 dư, sau phản ứng
thu được 5,763 gam hỗn hợp muối khan. Phần trăm khối lượng Fe trong X là A. 16,8%. B. 8,4%. C. 22,4%. D. 19,2%.
Câu 129. Hòa tan 31,76 gam hỗn hợp CuSO4 và NaCl vào nước thu được 300 gam dung dịch X. Điện phân
dung dịch X (điện cực trơ, màng ngăn xốp) thì thu được 283,32 gam dung dịch Y (không còn màu xanh) và
có V lít khí (đktc) thoát ra ở anot. Cho Y tác dụng với Mg dư thấy giải phóng 1,344 lít khí H2 (đktc). Biết các
phản ứng xảy ra hoàn toàn, hiệu suất phản ứng điện phân bằng 100% (bỏ qua sự hòa tan khí trong nước và sự
bay hơi của nước). Giá trị của V là A. 2,464. B. 2,520. C. 3,136. D. 2,688.
Câu 130. Kim loại nào sau đây thuộc nhóm VIIIB trong bảng tuần hoàn hoá học là A. Cu. B. Zn. C. Fe. D. Cr.
Câu 131. Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy oxit tương ứng? A. Na. B. Al. C. Cr. D. Fe.
Câu 132. Cho các phương pháp sau:
(a) Gắn kim loại kẽm vào kim loại sắt.
(b) Gắn kim loại đồng vào kim loại sắt.
(c) Phủ một lớp sơn lên bề mặt sắt.
(d) Tráng thiếc lên bề mặt sắt.
Số phương pháp điện hóa được sử dụng để bảo vệ kim loại sắt không bị ăn mòn là A. 3. B. 2. C. 1. D. 4.
Câu 133. Điện phân dung dịch chứa 14,28 gam hỗn hợp CuSO4 và NaCl bằng dòng điện một chiều có
cường độ 4A (điện cực trơ, có màng ngăn, hiệu suất 100%). Sau thời gian t giây thì ngừng điện phân, thu
được dung dịch X (có pH < 7) và 4,48 lít (đktc) hỗn hợp khí thoát ra ở cả hai điện cực, có tỉ khối so với He là
6,2. Bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Giá trị của t là A. 5790. B. 6755. C. 7720. D. 8685.
Câu 134. Hòa tan hết 30,56 gam hỗn hợp gồm Mg, Fe3O4 và FeCO3 trong dung dịch chứa HCl và 0,24 mol
HNO3, thấy thoát ra hỗn hợp khí X gồm CO2, NO và 0,08 mol N2O; đồng thời thu được dung dịch Y có khối
lượng tăng 22,60 gam so với dung dịch ban đầu. Tỉ khối hơi của X so với He bằng 9,95. Cho dung dịch
AgNO3 đến dư vào dung dịch Y, thu được 0,03 mol khí NO (sản phẩm khử duy nhất của N+5) và 239,66 gam
kết tủa. Phần trăm khối lượng của Fe3O4 có trong hỗn hợp ban đầu là A. 32,04%. B. 39,27%. C. 38,62%. D. 37,96%.
Câu 135: Phương pháp điều chế kim loại Mg là
A. điện phân nóng chảy MgCl2.
B. cho Na tác dụng với dung dịch MgCl2.
C. khử MgO bằng CO.
D. điện phân dung dịch MgCl2.
Câu 136: Tính chất nào sau đây không phải tính chất vật lí chung của kim loại? A. Tính dẻo. B. Tính cứng. C. Ánh kim.
D. Tính dẫn điện.
Câu 137: Trường hợp nào sau đây xảy ra hiện tượng ăn mòn điện hóa?
A. Đốt Fe trong bình chứa Cl2.
B. Cho thanh Cu vào dung dịch FeCl3.
C. Gang thép để trong không khí ẩm.
D. Cho thanh Fe vào dung dịch HNO3.
Câu 138: Khí nào sau đây có trong không khí đã làm cho các đồ dùng bằng bạc lâu ngày bị xám đen? A. CO2. B. SO2. C. O2. D. H2S.
Câu 139: Hòa tan hoàn toàn m gam hỗn hợp X chứa Mg, Mg(NO3)2, Fe, Fe2O3 và Fe(NO3)2 trong dung dịch
chứa 0,1 mol HNO3 và 0,75 mol H2SO4 thu được dung dịch Y chỉ chứa (m + 67,58) gam hỗn hợp muối và
5,824 lít (đktc) hỗn hợp khí Z gồm H2 và NO có tổng khối lượng là 3,04 gam. Cho Ba(OH)2 dư vào Y (không
có không khí) thu được 223,23 gam kết tủa. Phần trăm khối lượng của Fe2O3 trong X gần nhất với giá trị nào sau đây? A. 27%. B. 45%. C. 38%. D. 33%.
Câu 140: Hòa tan hoàn toàn m gam hỗn hợp gồm CuSO4 và FeCl3 vào nước thu được dung dịch X. Điện
phân dung dịch X (với các điện cực trở) đến khi ở anot thoát ra 0,2 mol hỗn hợp khí có tỉ khối so với H2 bằng
30,625 thì dừng lại. Dung dịch thu được sau điện phân có chứa 2 muối có nồng độ mol bằng nhau. Giả sử
hiệu suất điện phân là 100% khí sinh ra không tan trong nước. Giá trị của m là A. 48,25. B. 64,25. C. 62,25. D. 56,25.
Câu 141: Kim loại có khối lượng riêng nhỏ nhất, là vật liệu quan trọng trong việc sản xuất anot của pin điện là A. Cs. B. Hg. C. Al. D. Li.
Câu 142: Kim loại nào sau đây thuộc nhóm IIA trong bảng tuần hoàn? A. Na. B. Ca. C. Al. D. Fe.
Câu 143: Thực hiện các thí nghiệm sau:
(a) Đốt bột nhôm nguyên chất trong khí oxi.
(b) Để thanh thép lâu ngày trong không khí ẩm.
(c) Ngâm thanh đồng nguyên chất vào dung dịch NaNO3.
(d) Cho lá kẽm nguyên chất vào dung dịch chứa H2SO4 và CuSO4.
Số thí nghiệm xảy ra ăn mòn điện hóa là A. 2. B. 3. C. 4. D. 1.
Câu 144: Điện phân 600ml dung dịch X chứa NaCl 0,5M và CuSO4 a mol/l (điện cực trơ, màng ngăn xốp)
thu được dung dịch Y có khối lượng giảm 24,25 gam so với khối lượng dung dịch X thì ngừng điện phân.
Nhúng thanh sắt nặng 150 gam vào dung dịch Y đến khi các phản ứng xảy ra hoàn toàn, lấy thanh kim loại
ra, rửa sạch, làm khô cân được 150,4 gam (giả thiết toàn bộ kim loại tạo thành đều bám hết vào thanh sắt và
không có sản phẩm khử của S+6 sinh ra). Biết hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong
nước. Giá trị của a là A. 1,00. B. 1,50. C. 0,50. D. 0,75.
Câu 145: Hỗn hợp M gồm Al, Al2O3, Fe3O4, CuO, Fe và Cu, trong đó oxi chiếm 20,4255% khối lượng
hỗn hợp. Cho 6,72 lít khí CO (đktc) đi qua 35,25 gam M nung nóng, sau một thời gian thu được hỗn hợp
rắn G và hỗn hợp khí X có tỉ khối so với H 2 bằng 18. Hòa tan hết toàn bộ G trong lượng dư dung dịch
HNO3 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa m gam muối (không có muối NH +
4 ) và 4,48 lít (đktc) hỗn hợp khí Z gồm NO và N2O. Tỉ khối của Z so với H2 là 16,75. Giá trị của m là A. 96,25. B. 117,95. C. 139,50. D. 80,75.




