










Preview text:
ĐỀ CƯƠNG ÔN TẬP GIỮA HỌC KÌ I – HÓA HỌC 11
NĂM HỌC 2024 – 2025
I– TRẮC NGHIỆM (Chọn 1 phương án đúng)
Chương I: CÂN BẰNG HÓA HỌC
KHÁI NIỆM VỀ CÂN BẰNG HÓA HỌC
Câu 1: Mối quan hệ giữa tốc độ phản ứng thuận vt và tốc độ phản ứng nghịch vn ở trạng thái cân bằng được biểu diễn như thế nào?
A. vt = 2vn. B. vt = vn≠ 0. C. vt = 0,5vn. D. vt = vn = 0.
Câu 2: Phản ứng thuận nghịch là phản ứng
A. Trong cùng điều kiện, phản ứng xảy ra theo hai chiều trái ngược nhau.
B. Có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
C. Chỉ xảy ra theo một chiều nhất định.
D. Xảy ra giữa hai chất khí.
Câu 3: Tại nhiệt độ không đổi, ở trạng thái cân bằng,
A. Thành phần của các chất trong hỗn hợp phản ứng không thay đổi.
B. Thành phần của các chất trong hỗn hợp phản ứng vẫn liên tục thay đổi.
C. Phản ứng hoá học không xảy ra.
D. Tốc độ phản ứng hoá học xảy ra chậm dần.
Câu 4: Cho phản ứng thuận nghịch ở trạng thái cân bằng:
4 NH3 (g) + 3 O2 (g) 2 N2 (g) + 6 H2O(g) (
<0)
Cân bằng sẽ chuyển dịch theo chiều thuận khi:
A. Tăng nhiệt độ B. Thêm chất xúc tác C. Tăng áp suất D. Loại bỏ hơi nước
Câu 5: Phản ứng thuận nghịch là phản ứng
A. phản ứng xảy ra theo hai chiều ngược nhau trong cùng điều kiện.
B. có phương trình hoá học được biểu diễn bằng mũi tên một chiều.
C. chỉ xảy ra theo một chiều nhất định.
D. xảy ra giữa hai chất khí.
Câu 6: Phản ứng nào sau đây là phản ứng thuận nghịch?
A. Mg + 2HCl → MgCl2 + H2. B. 2SO2 + O2 2SO3.
C. C2H5OH + 3O2 2CO2 + 3H2O. D. 2KClO3
2KCl + 3O2
Câu 7: Khi một hệ ở trạng thái cân bằng thì trạng thái đó là
A. cân bằng tĩnh. B. cân bằng động.
C. cân bằng bền. D. cân bằng không bền.
Câu 8: Biểu thức tính hằng số cân bằng (KC) của phản ứng tổng quát: aA + bB cC + dD là
A. B.
C.
D.
Câu 9: Biểu thức tính hằng số cân bằng của phản ứng: H2(g) + I2(g) 2HI(g) là
A. B.
C.
D.
Câu 10: Biểu thức tính hằng số cân bằng của phản ứng: CaO(s) + CO2(g) CaCO3(s) là
A. B.
C.
D.
Câu 11: Hằng số cân bằng KC của một phản ứng thuận nghịch phụ thuộc vào yếu tố nào sau đây?
A. Nồng độ B. Nhiệt độ C. Áp suất D. Chất xúc tác
Câu 12: Sự phá vỡ cân bằng cũ để chuyển sang một cân bằng mới do các yếu tố bên ngoài tác động được gọi là
A. sự biến đổi chất. B. sự dịch chuyển cân bằng.
C. sự chuyển đổi vận tốc phản ứng. D. sự biến đổi hằng số cân bằng.
Câu 13: Các yếu tố có thể ảnh hưởng đến cân bằng hoá học là
A. nồng độ, nhiệt độ và chất xúc tác. B. nồng độ, áp suất và diện tích bề mặt.
C. nồng độ, nhiệt độ và áp suất. D. áp suất, nhiệt độ và chất xúc tác.
Câu 14: Phát biểu nào sau đây về một phản ứng thuận nghịch tại trạng thái cân bằng là sai?
A. Tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
B. Nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi.
C. Nồng độ mol của chất phản ứng luôn bằng nồng độ mol của chất sản phẩm phản ứng.
D. Phản ứng thuận và phản ứng nghịch vẫn diễn ra.
Câu 15: Xét cân bằng sau:
Nếu tăng nồng độ SO2(g) (các điều kiện khác giữ không đổi), cân bằng sẽ chuyển dịch theo chiều cao?
A. Chuyển dịch theo chiều nghịch.
B. Chuyển dịch theo chiều thuận.
C. Có thể chuyển dịch theo chiều thuận hoặc nghịch tùy thuốc vào lượng SO2 thêm vào.
D. Không thay đổi.
Câu 16: Cho hệ cân bằng trong một bình kín: N2(g) + O2(g) 2NO(g);
> 0
Cân bằng trên chuyển dịch theo chiều thuận khi
A. thêm chất xúc tác vào hệ. B. giảm áp suất của hệ.
C. thêm khí NO vào hệ. D. tăng nhiệt độ của hệ.
Câu 17: Hệ cân bằng sau được thực hiện trong bình kín:
CO (g) + H2O (g) CO2 (g) + H2 (g) ;
< 0
Cân bằng trên chuyển dịch theo chiều thuận khi
A. tăng áp suất chung của hệ. B. cho chất xúc tác vào hệ.
C. thêm khí H2 vào hệ. D. giảm nhiệt độ của hệ.
Câu 18: Cho cân bằng hoá học: N2 (g) + 3H2 (g) 2NH3 (g); phản ứng thuận là phản ứng toả nhiệt. Cân bằng hoá học không bị chuyển dịch khi
A. thay đổi áp suất của hệ. B. thay đổi nồng độ N2.
C. thay đổi nhiệt độ. D. thêm chất xúc tác Fe.
Câu 19: Cân bằng hoá học nào sau đây không bị chuyển dịch khi thay đổi áp suất?
A. B.
C. D.
Câu 20: Cho phản ứng: N2 (g) + 3H2 (g) 2NH3 (g);
= –92 kJ. Hai biện pháp đều làm cân bằng chuyển dịch theo chiều thuận là
A. giảm nhiệt độ và giảm áp suất. B. tăng nhiệt độ và tăng áp suất.
C. giảm nhiệt độ và tăng áp suất. D. tăng nhiệt độ và giảm áp suất.
Câu 21: Cho cân bằng sau trong bình kín: 2NO2 (g) N2O4 (g).
(màu nâu đỏ) (không màu)
Biết khi hạ nhiệt độ của bình thì màu nâu đỏ nhạt dần. Phản ứng thuận có
A. > 0, phản ứng tỏa nhiệt. B.
< 0, phản ứng tỏa nhiệt.
C. > 0, phản ứng thu nhiệt. D.
< 0, phản ứng thu nhiệt.
Câu 22: Cho các cân bằng sau:
(1) 2SO2(g) + O2(g) 2SO3(g) (3) CO2(g) + H2(g)
CO(g) + H2O(g)
(2) N2(g) + 3H2(g) 2NH3(g) (4) 2HI(g)
H2(g) + I2(g)
Khi thay đổi áp suất, nhóm gồm các cân bằng hoá học đều không bị chuyển dịch là
A. (1) và (2). B. (1) và (3). C. (3) và (4). D. (2) và (4).
Câu 23: Cho các cân bằng hoá học:
(1) N2(g) + 3H2(g) 2NH3(g) (3) 2SO2(g) + O2(g)
2SO3(g)
(2) H2(g) + I2(g) 2HI(g) (4) 2NO2(g)
N2O4(g)
Khi thay đổi áp suất những cân bằng hóa học bị chuyển dịch là:
A. (1), (2), (3). B. (2), (3), (4). C. (1), (3), (4). D. (1), (2), (4).
CÂN BẰNG TRONG DUNG DỊCH NƯỚC
Câu 24: Phát biểu nào sau đây đúng khi nói về sự điên li?
A. Sự điện li là quá trình phân li một chất trong nước thành ion.
B. Sự điện li quá trình hòa tan một chất vào nước tạo thành dung dịch.
C. Sự điện li quá trình phân li một chất dưới tác dụng của dòng điện.
D. Sự điện li thực chất là quá trình oxi hóa – khử.
Câu 25: Các dung dịch acid, base, muối dẫn điện được là do trong dung dịch của chúng có các
A. ion trái dấu. B. anion (ion âm). C. cation (ion dương). D. chất.
Câu 26: Chất nào sau đây là chất điện li?
A. Cl2. B. HNO3. C. MgO. D. CH4.
Câu 27: Chất nào sau đây không phải chất điện li?
A. KOH. B. H2S. C. HNO3. D. C2H5OH.
Câu 28: Chất nào dưới đây không phân li ra ion khi hòa tan trong nước?
A. MgCl2. B. HClO3.
C. Ba(OH)2. D. C6H12O6 (glucose).
Câu 29: Dung dịch nào sau đây có khả năng dẫn điện?
A. Dung dịch đường. C. Dung dịch rượu.
B. Dung dịch muối ăn. D. Dung dịch benzene trong ancol.
Câu 30: Dung dịch chất nào sau đây không dẫn điện được?
A. HCl trong C6H6 (benzene). C. Ca(OH)2 trong nước.
B. CH3COONa trong nước. D. NaHSO4 trong nước.
Câu 31: Trường hợp nào sau đây dẫn điện được?
A. KCl rắn, khan. C. CaCl2 rắn, khan.
B. Glucose tan trong nước. D. HBr hòa tan trong nước.
Câu 32: Chất nào sau đây thuộc loại chất điện li mạnh?
A. CH3COOH. B. C2H5OH. C. H2O. D. NaCl.
Câu 33: Chất nào sau đây thuộc loại chất điện li mạnh?
A. CO2. B. NaOH. C. H2O. D. H2S.
Câu 34: Chất nào sau đây thuộc loại chất điện li mạnh?
A. NaHCO3. B. C2H5OH. C. H2O. D. NH3.
Câu 35: Chất nào sau đây thuộc loại chất điện li yếu?
A. NaHCO3. B. C2H5OH. C. H2S. D. NH4Cl.
Câu 36: Chất nào sau đây thuộc loại chất điện li yếu?
A. KCl. B. HF. C. HNO3. D. NH4Cl.
Câu 37: Chất nào sau đây là chất điện li yếu?
A. CH3COOH. B. FeCl3. C. HNO3. D. NaCl.
Câu 38: Phương trình điện li viết đúng là
A. H2SO4 → 2H+ + SO4- B. NaOH Na+ + OH-
C. HF H+ + F- D. AlCl3 → Al3+ + Cl3-
Câu 39: Phương trình điện li viết đúng là
A. B. KOH → K+ + OH-.
C. D.
Câu 40: Phương trình điện li nào dưới đây viết không đúng?
A. B. CH3COOH
CH3COO- + H+
C. NaOH Na+ + OH- D.
Câu 41: Phương trình điện li nào sau đây không đúng?
A. B. K2SO4
2K+ + SO42-
C. HF H+ + F- D. BaCl2 → Ba2+ + 2Cl-
Câu 42: Phương trình mô tả sự điện li của NaCl trong nước là
A. B.
C. D.
Câu 43: Trong dung dịch nitric acid (bỏ qua sự phân li của H2O) có những phần tử nào?
A. H+, NO3-. B. H+, NO3-, H2O.
C. H+, NO3-, HNO3. D. H+, NO3-, HNO3, H2O.
Câu 44: Trong dung dịch acetic acid (bỏ qua sự phân li của H2O) có những phần tử nào?
A. H+, CH3COO-. B. H+, CH3COO-, H2O.
C. CH3COOH, H+, CH3COO-, H2O. D. CH3COOH, CH3COO-, H+.
Câu 45: Cho phương trình: NH3 + H2O NH4+ + OH-
Trong phản ứng thuận, theo thuyết Bronsted – Lowry chất nào là base?
A. NH3. B. H2O. C. NH4+. D. OH-.
Câu 46: Cho phương trình: NH3 + H2O NH4+ + OH-
Trong phản ứng thuận, theo thuyết Bronsted – Lowry chất nào là acid?
A. NH3. B. H2O. C. NH4+. D. OH-.
Câu 47: Cho phương trình: CH3COOH + H2O CH3COO- + H3O+
Trong phản ứng thuận, theo thuyết Bronsted – Lowry chất nào là acid?
A. CH3COOH. B. H2O. C. CH3COO-. D. H3O+.
Câu 48: Cho phương trình: CH3COOH + H2O CH3COO- + H3O+
Trong phản ứng nghịch, theo thuyết Bronsted – Lowry chất nào là acid?
A. CH3COOH. B. H2O. C. CH3COO-. D. H3O+.
Câu 49: Trong phản ứng sau đây, những chất nào đóng vai trò là acid theo thuyết Bronsted – lowry?
A. H2S và H2O B. H2S và H3O+ C. H2S và HS- D. H2O và H3O+
Câu 50: Trong phản ứng sau đây, những chất nào đóng vai trò là base theo thuyết Bronsted – lowry?
A. CO32- và OH- B. CO32- và HCO3+ C. H2O và OH- D. H2O và CO32-
Câu 51: Vì sao dung dịch của các muối, acid, base dẫn điện?
A. Do có sự di chuyển của electron tạo thành dòng elctron.
B. Do phân tử của chúng dẫn được điện.
C. Do các ion hợp phần có khả năng dẫn điện.
D. Do muối, acid, base có khả năng phân li ra ion trong dung dịch.
Câu 52: Dung dịch sodium chloride (NaCl) dẫn được điện là do
A. NaCl tan được trong nước. B. NaCl điện li trong nước thành ion.
C. NaCl có vị mặn. D. NaCl là phân tử phân cực.
Câu 53: Saccharose là chất không điện li vì
A. Phân tử saccharose không có khả năng hòa tan trong nước.
B. Phân tử saccharose không có khả năng phân li thành ion trong nước.
C. Phân tử saccharose không có tính dẫn điện.
D. Phân tử saccharose có khả năng hòa tan trong nước.
Câu 54: Dãy chất nào sau đây, trong nước đều là chất điện li mạnh?
A. H2SO4, Cu(NO3)2, CaCl2, H2S. B. HCl, H3PO4, Fe(NO3)3, NaOH.
C. HNO3, CH3COOH, BaCl2, KOH. D. H2SO4, MgCl2, Al2(SO4)3, Ba(OH)2.
Câu 55: Hãy cho biết tập hợp các chất nào sau đây đều là chất điện li yếu?
A. Cu(OH)2, NaCl, C2H5OH, HCl. B. C6H12O6, Na2SO4, NaNO3, H2SO4.
C. NaOH, NaCl, Na2SO4, HNO3. D. CH3COOH, HF, CH3COOH, H2S.
Câu 56: Đối với dung dịch acid yếu CH3COOH 0,10 M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion sau đây là đúng?
A. [H+] = 0,10 M. B. [H+] < [CH3COO-]. C. [H+] > [CH3COO-]. D. [H+] < 0,10 M.
Câu 57: Dung dịch chất nào sau đây (có cùng nồng độ) dẫn điện tốt nhất?
A. K2SO4. B. KOH. C. NaCl. D. KNO3.
Câu 58: Các dung dịch sau đây có cùng nồng độ 0,10 mol/L, dung dịch nào dẫn điện kém nhất?
A. HCl. B. HF. C. HI. D. HBr.
Câu 59: Nồng độ mol của ion NO3- trong dung dịch Al(NO3)3 0,05 M là
A. 0,02 M. B. 0,15 M. C. 0,1 M. D. 0,05 M.
Câu 60: Trộn 200 mL dung dịch HCl 0,2 M với 300 mL dung dịch H2SO4 0,1M thu được dung dịch X. Coi như thể tích dung dịch thay đổi không đáng kể, nồng độ mol của ion H+ trong X là
A. 0,3 M. B. 0,1 M. C. 0,2 M. D. 0,25 M.
Câu 61: Trộn 600 mL dung dịch HNO3 0,1 M với 400 mL dung dịch Ba(OH)2 0,05 M thu được dung dịch X. Coi như thể tích dung dịch thay đổi không đáng kể, tổng nồng độ mol của các cation trong X là
A. 0,04 M. B. 0,01 M. C. 0,02 M. D. 0,05 M.
Câu 62: Theo thuyết Bronsted – Lowry, acid có thể là
A. phân tử. B. ion
C. nguyên tử. D. phân tử hoặc ion.
Câu 63: Theo thuyết Bronsted – Lowry, dãy các chất nào sau đây là acid?
A. NH4+, HCl, PO43-. B. CO32-, SO32-, PO43-.
C. Na+, H+, NH4+. D. NH4+, HSO4-, H2CO3.
Câu 64: Theo thuyết Bronsted – Lowry, dãy các chất nào sau đây là base?
A. S2-, HCl, PO43-. B. CO32-, SO32-, PO43-.
C. HSO4-, H+, NH4+. D. HS-, Na+, H2CO3.
Câu 65: Theo thuyết Bronsted – Lowry, dãy các chất nào sau đây lưỡng tính?
A. H+, OH-, H2O. B. HCO3-, HSO3-, H2PO4-.
C. NH4+, Na+, H+. D. NaOH, HCl, NaHCO3.
Câu 66: Dung dịch chất nào sau đây làm xanh quỳ tím?
A. HCl. B. Na2SO4. C. NaOH. D. KCl.
Câu 67: Dung dịch chất nào sau đây làm quỳ tím hóa đỏ?
A. HCl. B. K2SO4. C. KOH. D. NaCl.
Câu 68: Dung dịch chất nào sau đây không làm đổi màu quỳ tím?
A. HCl. B. Na2SO4. C. Ba(OH)2. D. HClO4.
Câu 69: Dung dịch nào sau đây có pH > 7?
A. NaCl. B. NaOH. C. HNO3. D. H2SO4.
Câu 70: Dung dịch chất nào sau đây có pH > 7?
A. NaNO3. B. KCl. C. H2SO4. D. KOH.
Câu 71: Dung dịch nào sau đây có pH < 7?
A. BaCl2. B. KOH. C. HNO3. D. Na2SO4.
Câu 72: Dung dịch nào sau đây có pH = 7?
A. NaCl. B. NaOH. C. HNO3. D. H2SO4.
Câu 73: Dung dịch chất nào sau đây làm quỳ tím chuyển thành màu đỏ?
A. H2SO4. B. KOH. C. NaCl. D. C2H5OH.
Câu 74: Dung dịch chất nào sau đây làm quỳ tím chuyển thành màu xanh?
A. HCl. B. CH3COONa. C. KNO3. D. C2H5OH.
Câu 75: Khi chuẩn độ, người ta thêm từ từ dung dịch đựng trong (1) … vào dung dịch đựng trong bình tam gác. Dụng cụ cần điền vào (1) là
A. Bình định mức. B. Burette. C. Pipette. D. Ống đong.
Câu 76: Một dung dịch có pH = 11,7. Nồng độ ion hydrogen (H+) của dung dịch là
A. 2,3M B. 11,7M C. 5,0.10-3M D. 2,0.10-12M
Câu 77: Calcium hydroxide rắn được hòa tan trong nước cho tới khi pH của dung dịch đạt 10,94. Nồng độ của ion hydroxide (OH-) trong dung dịch là
A. 1,1.10-11 M B. 3,06 M C. 8,7.10-4 M D. 1,0.10-14 M
Câu 78: Giá trị pH của dung dịch HCl 0,001M là
A. 3. B. 11. C. 12. D. 2.
Câu 79: Giá trị pH của dung dịch H2SO4 0,005 M là
A. 2. B. 12. C. 10. D. 4.
Câu 80: Giá trị pH của dung dịch NaOH 0,1 M là
A. 1. B. 13. C. 11. D. 3.
Câu 81: Trộn lẫn V mL dung dịch NaOH 0,01 M với V mL dung dịch HCl 0,03 M được 2V mL dung dịch Y. Dung dịch Y có pH là
A. 4. B. 3. C. 2. D. 1.
Chương II: NITROGEN- SULFUR
NITROGEN
Câu 82: Trong tự nhiên, đơn chất nitrogen có nhiều trong
A. nước biển. B. không khí. C. cơ thể người. D. mỏ khoáng.
Câu 83: Trong không khí, chất nào sau đây chiếm phần trăm thể tích lớn nhất?
A. O2. B. NO. C. CO2. D. N2.
Câu 84: Khí nào phổ biến nhất trong khí quyển Trái Đất?
A. Oxygen. B. Nitrogen. C. Ozone. D. Argon.
Câu 85: Ở dạng hợp chất, nitrogen tồn tại nhiều trong các mỏ khoáng dưới dạng
A. NaNO3. B. KNO3. C. HNO3. D. Ba(NO3)2.
Câu 86: Trong tự nhiên, nguyên tố nitrogen tồn tại trong hợp chất hữu cơ nào sau đây?
A. Tinh bột. B. Cellulose. C. Protein. D. Glucose.
Câu 87: Diêu tiêu Chile (hay diêm tiêu natri) là tên gọi khác của hợp chất nào sau đây?
A. Sodium chloride. B. Potassium sulfate.
C. Sodium nitrate. D. Potassium nitrate.
Câu 88: Công thức hóa học của diêm tiêu Chile là
A. Ca(NO3)2. B. NH4NO3. C. NH4Cl. D. NaNO3.
Câu 89: Ở trạng thái tự nhiên, nitrogen:
A. tồn tại ở dạng đơn chất và hợp chất.
B. Chỉ tồn tại ở dạng đơn chất.
C. Chỉ tồn tại ở dạng hợp chất.
D. tự do chiếm khoảng 20% thể tích không khí.
Câu 90: Trong tự nhiên, nguyên tố nitrogen tồn tại chủ yếu ở dạng đồng vị nào sau đây?
A. 14N. B. 13N. C. 15N. D. 12N.
Câu 91: Cấu hình electron nguyên tử của nitrogen là:
A. 1s22s22p1 B. 1s22s22p5 C. 1s22s22p4 D. 1s22s22p3
Câu 92: Vị trí (chu kì, nhóm) của nguyên tố nitrogen trong bảng tuần hoàn là
A. Chu kì 2, nhóm VA. B. chu kì 3, nhóm VA.
C. chu kì 2, nhóm VIA. D. chu kì 3, nhóm IVA.
Câu 93: Đặc điểm cấu tạo của phân tử N2 là
A. có 1 liên kết ba. B. có 1 liên kết đôi. C. Có 2 liên kết đôi. D. có 2 liên kết ba.
Câu 94: Số liên kết sigma (σ) và số liên kết pi (π) trong phân tử nitrogen lần lượt là
A. 2 và 1. B. 0 và 3. C. 3 và 0. D. 1 và 2.
Câu 95: Số oxi hóa thấp nhất và cao nhất của nguyên tử nitrogen lần lượt là
A. 0 và +5. B. -3 và 0. C. -3 và +5. D. -2 và +4.
Câu 96: Trong hợp chất nitrogen có các mức oxi hóa nào sau đây?
A. -3, +3, +5. B. -3, 0, +3, +5.
C. -3, +1, +2, +3, +4, +5. D. -3, 0, +1, +2, +3, +4, +5.
Câu 97: Tính chất nào sau đây không phải tính chất vật lí của N2?
A. Chất khí. B. Không màu.
C. Nặng hơn không khí. D. Tan ít trong nước.
Câu 98: Trong phản ứng: N2(g) + 3H2(g) 2NH3(g). N2 thể hiện
A. tính khử. B. tính oxi hóa. C. tính base. D. tính acid.
Câu 99: Trong phản ứng tổng hợp ammonia từ nitrogen và hydrogen, nitrogen đóng vài trò là
A. chất khử. B. chất oxi hóa. C. acid. D. base.
Câu 100: Trong phản ứng: N2(g) + O2(g) 2NO(g). N2 thể hiện
A. tính khử. B. tính oxi hóa. C. tính base. D. tính acid.
Câu 101: Nitrogen thể hiện tính khử trong phản ứng nào sau đây?
A. . B.
.
C. . D.
.
Câu 102: Trong phản ứng hóa hợp với oxygen, nitrogen đóng vai trò là
A. chất oxi hóa. B. base. C. chất khử. D. acid.
Câu 103: Trong những cơn mưa dông kèm sấm sét, nitrogen kết hợp trực tiếp với oxygen tạo thành sản phẩm là
A. NO. B. N2O. C. NH3. D. NO2.
Câu 104: Ứng dụng nào sau đây không phải của N2?
A. Tổng hợp NH3. B. Bảo quản máu.
C. Diệt khuẩn, khử trùng. D. Bảo quản thực phẩm.
Câu 105: Ở nhiệt độ thường, nitrogen khá trơ về mặt hoạt động hóa học là do
A. nitrogen có bán kính nguyên tử nhỏ. B. nitrogen có độ âm điện lớn.
C. phân tử nitrogen có liên kết ba bền vững. D. phân tử nitrogen không phân cực.
Câu 106: Khí nitrogen ít tan trong nước là do
A. nitrogen có bán kính nguyên tử nhỏ. B. nitrogen có độ âm điện lớn.
C. phân tử nitrogen có liên kết ba bền vững. D. phân tử nitrogen không phân cực.
Câu 107: Trong phòng thí nghiệm, người ta thu khí nitrogen bằng phương pháp dời nước vì
A. N2 nhẹ hơn không khí. B. N2 ít tan trong nước.
C. N2 không duy trì sự sống, sự cháy. D. N2 hoá lỏng, hóa rắn ở nhiệt độ rất thấp.
Câu 108: Nhận định nào sau đây về phân tử nitrogen là đúng?
A. Có ba liên kết đơn bền vững.
B. Chứa nguyên tử nitrogen có số oxi hóa là -3.
C. Có liên kết cộng hóa trị có cực.
D. Thể hiện cả tính oxi hóa và tính khử.
Câu 109: Trong nghiên cứu, khí nitrogen thường được dùng để tạo bầu khí quyển trơ dựa trên cơ sở nào?
A. Nitrogen có tính oxi hóa mạnh. B. Nitrogen rất bền với nhiệt.
C. Nitrogen khó hóa lỏng. D. Nitrogen không có cực.
Câu 110: Trong tự nhiên, phản ứng giữa nitrogen và oxygen (trong cơn mưa dông kèm sấm sét) là khởi đầu cho quá trình tạo và cung cấp loại phân bón nào cho cây?
A. Phân kali. B. Phân đạm ammonium.
C. Phân lân. D. Phân đạm nitrate.
Câu 111: Cho cân bằng hoá học: N2(g) + 3H2(g) 2NH3(g). Phản ứng thuận là phản ứng toả nhiệt. Cân bằng hoá học không bị chuyển dịch khi
A. thay đổi áp suất của hệ. B. thay đổi nồng độ N2.
C. thay đổi nhiệt độ. D. thêm chất xúc tác Fe.
Câu 112: Quá trình tạo đạm nitrate từ nitrogen trong tự nhiên được mô tả theo sơ đồ sau:
Công thức của X là
A. Cl2. B. O2. C. H2. D. CO2.
AMMONIA VÀ MUỐI AMMONIUM
Câu 113: Trong ammonia, nitrogen có số oxi hóa là
A. +3. B. -3. C. +4. D. +5.
Câu 114: Liên kết hoá học trong phân tử NH3 là liên kết
A. cộng hoá trị có cực. B. ion.
C. cộng hoá trị không cực. D. kim loại.
Câu 115: Dạng hình học của phân tử ammonia là
A. hình tam giác đều. B. hình tứ diện.
C. đường thẳng. D. hình chóp tam giác.
Câu 116: Ở trạng thái lỏng nguyên chất, phân tử chất nào sau đây tạo được liên kết hydrogen với nhau?
A. Nitrogen. B. Ammonia. C. Oxygen. D. Hydrogen.
Câu 117: Khí nào sau đây dễ tan trong nước do tạo được liên kết hydrogen với nước?
A. Nitrogen. B. Hydrogen. C. Ammonia. D. Oxygen.
Câu 118: Khi tác dụng với nước và hydrochloric acid, ammonia đóng vai trò là
A. acid. B. base. C. chất oxi hóa. D. chất khử.
Câu 119: Cho vài giọt quỳ tím vào dung dịch NH3 thì dung dịch chuyển thành
A. màu hồng. B. màu vàng. C. màu đỏ. D. màu xanh.
Câu 120: Hiện tượng xảy ra khi cho giấy quỳ khô vào bình đựng khí ammonia là
A. giấy quỳ chuyển sang màu đỏ. B. giấy quỳ chuyển sang màu xanh.
C. giấy quỳ mất màu. D. giấy quỳ không chuyển màu.
Câu 121: Cho vài giọt dung dịch phenolphthalein vào dung dịch NH3, phenolphthalein chuyển sang màu nào sau đây?
A. Hồng. B. Xanh. C. Không màu. D. Vàng.
Câu 122: Nhúng 2 đũa thuỷ tinh vào 2 bình đựng dung dịch HCl đặc và NH3 đặc. Sau đó đưa 2 đũa lại gần nhau thì thấy xuất hiện
A. khói màu trắng. B. khói màu tím. C. khói màu nâu. D. khói màu vàng.
Câu 123: Tính chất hóa học của NH3 là
A. tính base, tính khử. B. tính base, tính oxi hóa.
C. tính acid, tính base. D. tính acid, tính khử.
Câu 124: Dung dịch NH3 phản ứng được với dung dịch nào sau đây?
A. NaOH. B. KCl. C. HCl. D. KOH
Câu 125: Cho dung dịch NH3 vào dung dịch chất nào sau đây thu được kết tủa trắng ?
A. HCl. B. H2SO4. C. H3PO4. D. AlCl3.
Câu 126: Dung dịch NH3 có thể tác dụng được với các dung dịch
A. HCl, CaCl2. B. KNO3, H2SO4.
C. Fe(NO3)3, AlCl3. D. Ba(NO3)2, HNO3.
Câu 127: Trong phương pháp Ostwald, ammoni bị oxi hóa bởi oxygen không khí (xúc tác Pt, to) tạo thành sản phẩm chính là
A. NO. B. N2. C. N2O. D. NO2.
Câu 128: Vai trò của NH3 trong phản ứng là
A. chất khử. B. acid. C. chất oxi hóa. D. base.
Câu 129: Trong nước, phân tử/ion nào sau đây thể hiện vai trò là acid Bronsted?
A. NH3. B. . C.
. D. N2.
Câu 130: Có thể nhận biết muối ammonium bằng cách cho muối tác dụng với dung dịch kiềm thấy thoát ra một chất khí. Chất khí đó là
A. NH3. B. H2. C. NO2 D. NO.
Câu 131: Phân biệt được dung dịch NH4Cl và NaCl bằng thuốc thử là dung dịch
A. KCl. B. KNO3. C. KOH. D. K2SO4.
Câu 132: Trong dung dịch, ammonia thể hiện tính base yếu do
A. phân tử ammonia chứa liên kết cộng hoá trị phân cực và liên kết hydrogen.
B. phân tử ammonia chứa liên kết cộng hoá trị phân cực và liên kết ion.
C. phần lớn các phân tử ammonia kết hợp với nước tạo ra các ion và
.
D. một phần nhỏ các phân tử NH3 kết hợp với ion H+ của nước tạo và
.
Câu 133: Nhận định nào sau đây về phân tử ammonia không đúng?
A. Phân cực mạnh. B. Có một cặp electron không liên kết.
C. Có độ bền nhiệt rất cao. D. Có khả năng nhận proton.
Câu 134: Cho thí nghiệm như hình vẽ, bên trong bình có chứa khí NH3, trong chậu thủy tinh chứa nước có nhỏ vài giọt phenolphthalein.
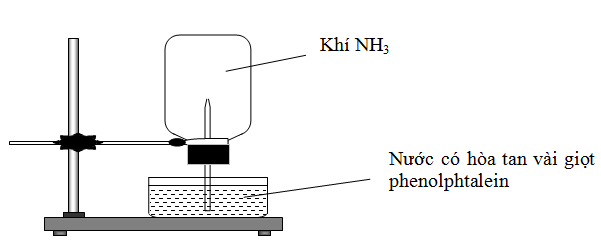
Hiện tượng xảy ra trong thí nghiệm là:
A. Nước phun vào bình và chuyển thành màu hồng.
B. Nước phun vào bình và chuyển thành màu tím.
C. Nước phun vào bình và không có màu.
D. Nước phun vào bình và chuyển thành màu xanh.
Câu 135: Xét cân bằng hóa học: NH3 + H2O NH4+ + OH-
Cân bằng sẽ chuyển dịch theo chiều thuận khi cho thêm vài giọt dung dịch nào sau đây?
A. NH4Cl. B. NaOH. C. HCl. D. NaCl.
Câu 136: Có thể dùng chất nào sau đây để làm khô khí ammonia?
A. Dung dịch H2SO4 đặc. B. P2O5 khan. C. MgO khan. D. CaO khan.
Câu 137: Để tách riêng NH3 ra khỏi hỗn hợp gồm N2, H2, NH3 trong công nghiệp, người ta đã
A. cho hỗn hợp qua nước vôi trong dư.
B. cho hỗn hợp qua bột CuO nung nóng.
C. nén và làm lạnh hỗn hợp để hóa lỏng NH3.
D. cho hỗn hợp qua dung dịch H2SO4 đặc.
Câu 138: Tã lót trẻ em sau khi được giặt sạch vẫn còn mùi khai do vẫn lưu lại một lượng ammonia. Để khử hoàn toàn mùi của ammonia thì người ta cho vào nước xả cuối cùng một ít hoá chất có sẵn trong nhà. Hãy chọn hoá chất thích hợp:
A. Phèn chua. B. Giấm ăn.
C. Muối ăn. D. Nước gừng tươi.
Câu 139: Khi cho dung dịch NaOH vào dung dịch NH4Cl, đun nóng thì thấy thoát ra
A. một chất khí màu lục nhạt.
B. một chất khí không màu, mùi khai, làm xanh giấy quỳ tím ẩm.
C. một chất khí màu nâu đỏ, làm xanh giấy quỳ tím ẩm.
D. chất khí không màu, không mùi.
Câu 140: Phát biểu nào sau đây không đúng?
A. Ammonia là base Bronsted khi tác dụng với nước.
B. Ammonia được sử dụng làm chất làm lạnh.
C. Muối ammonium là tinh thể ion, dễ tan trong nước.
D. Các muối ammonium đều rất bền với nhiệt.
Câu 141: Thuốc thử duy nhất để nhận biết 4 dung dịch đựng trong 4 lọ mất nhãn là KOH, NH4Cl K2SO4, (NH4)2SO4 là
A. dung dịch AgNO3 B. dung dịch BaCl2.
C. dung dịch NaOH. D. dung dịch Ba(OH)2.
MỘT SỐ HỢP CHẤT VỚI OXYGEN CỦA NITROGEN
Câu 142: Oxide phổ biến của nitrogen trong không khí là
A. NO, N2O. B. NO, NO2. C. N2O3, NO2. D. NO, N2O4.
Câu 143: Nitrogen dioxide là tên gọi của oxide nào sau đây?
A. NO. B. NO2. C. N2O. D. N2O4.
Câu 144: Nitrogen monoxide là tên gọi của oxide nào sau đây?
A. NO. B. NO2. C. N2O. D. N2O4.
Câu 145: Mưa acid là hiện tượng tượng nước mưa có pH như thế nào?
A. > 5,6. B. < 7. C. > 7. D. < 5,6.
Câu 146: Hiện tượng mưa acid
A. là hiện tượng sẵn có trong tự nhiên.
B. xảy ra do sự bốc hơi của nước rồi ngưng tụ.
C. xảy ra khi nước mưa có pH < 7.
D. xảy ra khi nước mưa có pH < 5,6.
Câu 147: Mưa acid là hiện tượng nước mưa có pH thấp hơn 5,6 (giá trị pH của khí carbon dioxide bão hòa trong nước). Hai tác nhân chính gây mưa acid là
A. Cl2, HCl. B. N2, NH3. C. SO2, NOx. D. S, H2S.
Câu 148: Hiện tượng mưa acid là do không khí bị ô nhiễm bởi các khí nào sau đây?
A. SO2, NO, NO2. B. NO, CO, CO2. C. CH4, HCl, CO. D. Cl2, CH4, SO2.
Câu 149: Số oxi hóa thấp nhất của nitrogen là
A. -3. B. 0. C. +1. D. +4.
Câu 150: Trong phân tử HNO3, nguyên tử N có số oxi hóa là
A. +5. B. +3. C. +4. D. -3.
Câu 151: Phân tử nào sau đây có liên kết cho – nhận?
A. NH3. B. N2. C. HNO3. D. H2.
Câu 152: Nitric acid dễ bị phân hủy bởi ánh sáng hoặc nhiệt độ tạo thành các sản phẩm là
A. NO2, H2O. B. NO2, O2, H2O. C. N2, O2, H2O. D. N2. H2O.
Câu 153: Acid nào sau đây thể hiện tính oxi hóa mạnh khi tác dụng với chất khử?
A. HCl. B. HNO3. C. HBr. D. H3PO4.
Câu 154: Trong công nghiệp, quá trình sản xuất Ca(NO3)2 cùng làm phân bón được thực hiện bằng phương phản ứng giữa dung dịch HNO3 với hợp chất phổ biến, giá rẻ nào sau đây?
A. CaO. B. Ca(OH)2. C. CaCO3. D. CaSO4.
Câu 155: Kim loại nào sau đây không tác dụng với nitric acid?
A. Zn. B. Cu. C. Ag. D. Au.
Câu 156: Nhóm các kim loại đều không phản ứng được với HNO3?
A. Al, Fe. B. Au, Pt. C. Al, Au. D. Fe, Pt.
Câu 157: Kim loại không tan trong dung dịch HNO3 đặc, nguội là
A. Mg. B. Al. C. Zn. D. Cu.
Câu 158: Kim loại iron không phản ứng được với dung dịch nào sau đây?
A. HNO3 đặc, nguội. B. H2SO4 đặc, nóng. C. HNO3 loãng. D. H2SO4 loãng.
Câu 159: Kim loại Fe bị thụ động bởi dung dịch
A. H2SO4 loãng B. HCl đặc, nguội C. HNO3 đặc, nguội D. HCl loãng
Câu 160: Kim loại bị thụ động trong HNO3 đặc, nguội là
A. Al, Fe. B. Ag, Fe. C. Pb, Ag. D. Pt, Au.
Câu 161: Hiện tượng phú dưỡng là một biểu hiện của môi trường ao, hồ bị ô nhiễm do dư thừa các chất dinh dưỡng, Sự dư thừa dinh dưỡng chủ yếu do hàm lượng các ion nào sau đây vượt quá mức cho phép?
A. Sodium, potassium. B. Calcium, magnesium.
C. Nitrate, phosphate. D. Chloride, sulfate.
Câu 162: Các oxide của nitrogen không được tạo thành trong trường hợp nào sau đây?
A. Núi lửa phun trào.
B. Đốt cháy các nhiên liệu hóa thạch.
C. Mưa dông, sấm sét.
D. Xả thải nước thải công nghiệp chưa qua xử lí.
Câu 163: Hoạt động nào sau đây góp phần gây nên hiện tượng phú dưỡng?
A. Sự quang hợp của cây xanh.
B. Nước thải sinh hoạt thải trực tiếp vào nguồn nước chưa qua xử lí.
C. Ao hồ thả quá nhiều tôm, cá.
D. Khử trùng ao hồ sau khi tát cạn bằng vôi sống (CaO).
Câu 164: HNO3 tinh khiết là chất lỏng không màu, nhưng dung dịch HNO3 để lâu thường chuyển sang màu vàng là do
A. HNO3 tan nhiều trong nước.
B. khi để lâu thì HNO3 bị khử bởi các chất của môi trường
C. dung dịch HNO3 có tính oxi hóa mạnh.
D. dung dịch HNO3 có hoà tan một lượng nhỏ NO2.
II- CÂU TRẮC NGHIỆM ĐÚNG SAI: Trong mỗi ý a), b), c), d) ở mỗi câu chọn đúng hoặc sai.
KHÁI NIỆM CÂN BẰNG HÓA HỌC
Câu 165: Xét phản ứng: Cl2(g) + H2O(l) HCl(aq) + HClO(aq)
a. Phản ứng trên là phản ứng thuận nghịch.
b. Cl2, H2O là chất tham gia của phản ứng thuận.
c. HCl, HClO là sản phẩm của phản ứng nghịch.
d. Phản ứng thuận nghịch là phản ứng xảy ra theo hai chiều ngược nhau trong điều kiện khác nhau.
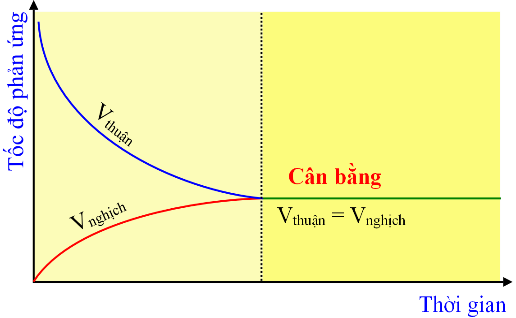
Câu 166: Cho đồ thị:
 a. Đồ thị trên biểu diễn tốc độ của phản ứng một chiều phụ thuộc vào thời gian.
a. Đồ thị trên biểu diễn tốc độ của phản ứng một chiều phụ thuộc vào thời gian.
b. Tại trạng thái cân bằng, tốc độ phản ứng thuận bằng tốc độ phản ứng nghịch.
c. Khi phản ứng thuận nghịch xảy ra thì tốc độ phản ứng thuận tăng dần còn tốc độ phản ứng nghịch giảm dần.
d. Khi phản ứng đạt trạng thái cân bằng thì phản ứng thuận và phản ứng nghịch dừng lại.
Câu 167: Cho phản ứng tổng hợp amonia:
N2(g) + 3H2(g) 2NH3(g)
a. Phản ứng trên là phản ứng tỏa nhiệt theo chiều thuận.
b. Khi tăng nhiệt độ của hệ thì cân bằng chuyển dịch theo chiều nghịch.
c. Khi giảm áp suất của hệ thì cân bằng chuyển dịch theo thuận.
d. Để phản ứng tổng hợp NH3 đạt hiệu suất cao thì người ta thực hiện ở nhiệt độ thấp và áp suất cao.
Câu 168: Cho cân bằng hoá học sau: 2NH3(g) N2(g) + 3H2(g). Khi tăng nhiệt độ của hệ thì tỉ khối của hỗn hợp so với hydrogen giảm.
a. Khi tăng nhiệt độ của hệ, cân bằng chuyển dịch theo chiều thuận.
b. Phản ứng thuận là phản ứng toả nhiệt.
c. Khi tăng áp suất của hệ, cân bằng chuyển dịch theo chiều nghịch.
d. Khi tăng nồng độ của NH3, cân bằng chuyển dịch theo chiều nghịch
Câu 169: Chất điện li là những chất khi tan trong nước phân li ra ion.
a. Chất điện li mạnh là chất khi tan trong nước, các phân tử hòa tan đều phân li.
b. Chất điện li mạnh gồm acid mạnh, base mạnh và hầu hết các muối.
c. Chất điện li yếu là chất khi tan trong nước, các phân tử hòa tan không phân li.
d. Trong dung dịch chất điện li yếu chứa cả phân tử và ion.
Câu 170: Phèn chua thường dùng để làm trong nước
a. Trong nước, phèn chua hòa tan nhưng không phân li, phân tử phèn chua có kích thước lớn nên hấp phụ các chất bẩn giúp làm trong nước.
b. Trong nước, phèn chua phân li tạo ion Al3+, ion này tác dụng với nước tạo môi trường acid làm phá hủy các chất bẩn trong nước.
c. Al(OH)3 tạo ra khi hòa tan phèn chua trong nước có khả năng hấp phụ các chất vì vậy có thể hấp phụ các chất bẩn sau đó lắng xuống đáy giúp làm trong nước.
d. Ngoài làm trong nước, phèn chua còn có được dùng làm bền màu trong công nghiệp nhuộm nhờ Al(OH)3 có khả năng hấp phụ các chất nhuộm sau đó bám vào sợi vải giúp cầm màu.
Câu 171: Cho hai phản ứng: (1) HCO3- + H2O CO32- + H3O+
(2) HCO3- + H2O H2CO3 + OH-
Xét theo thuyết acid – base của Bronsted – Lowry.
a. Trong phản ứng thuận của phản ứng (1) thì HCO3- là base, H2O là acid.
b. Trong phản ứng thuận của phản ứng (2) thì HCO3- là acid, H2O là base.
c. HCO3- vừa có tính acid, vừa có tính base nên là chất lưỡng tính.
d. H2O vừa có tính acid, vừa có tính base nên là chất lưỡng tính.
Câu 172: Chuẩn độ là phương pháp xác định nồng độ của một chất bằng một dung dịch chuẩn đã biết nồng độ.
a. Để chuẩn độ dung dịch NaOH có thể dùng dung dịch HCl đã biết trước nồng độ.
b. Thời điểm các chất phản ứng với nhau vừa đủ gọi là điểm cân bằng.
c. Chất chỉ thị để xác định thời điểm NaOH phản ứng với HCl vừa đủ là phenophthalein.
d. Để xác định chính xác nồng độ của dung dịch NaOH thì chỉ cần chuẩn độ một lần.
Câu 173: Xét cấu tạo và tính chất vật lí của nitrogen.
a. Trong bảng tuần hoàn, nitrogen thuộc ô số 7, chu kì 2, nhóm VA
b. Phân tử nitrogen chứa một liên kết ba năng lượng liên kết nhỏ và là phân tử không phân cực.
c. Ở điều kiện thường, nitrogen là chất khí không màu, không mùi, tan rất ít trong nước.
d. Khí nitrgen nặng hơn không khí, không duy trì sự cháy và sự hô hấp.
Câu 174: Nitrogen có nhiều ứng dụng trong đời sống và sản xuất.
a. Phần lớn nitrogen được dùng để tổng hợp NH3, từ đó sản xuất phân đạm, nitric acid, …
b. Ở điều kiện thường, nitrogen trơ về mặt hóa học nên thường dùng để bảo quản máu và các mẫu sinh vật học khác.
c. Nitrogen lỏng có nhiệt độ thấp nên thường dùng để dập tắt đám cháy do xăng dầu.
d. Trong các gói bim bim thường được bơm khí nitrogen để bảo quản tốt hơn không khí.
Câu 175: Xét các phát biểu về nitrogen.
a. Dù phân tử N2 có tính kém hoạt động hóa học, nhưng vẫn hoạt động hóa học mạnh hơn chlorine, Cl2.
b. Đơn chất nitrogen không phản ứng với hydrogen, oxygen ở điều kiện thường.
c. Do có nhiệt độ rất thấp nên nitrogen lỏng được sử dụng bảo quản một số loại mẫu vật.
d. Trong bầu khí quyển, khi có sấm chớp, khí nitrogen tạo các nitrogen oxide, là một nguyên nhân làm cho nước mưa có tính acid.
Câu 176: Xét tính chất hóa học của NH3.
a. Khí NH3 tác dụng với nước theo phản ứng: NH3 + H2O NH4+ + OH-
b. Trong phản ứng của NH3 tác dụng với dung dịch HCl thì NH3 đóng vai trò làm chất oxi hóa.
c. Trong phản ứng của NH3 tác dụng với O2 thì NH3 đóng vai trò làm chất khử.
d. Phản ứng: 4NH3 + 3O2 2N2 + 6H2O là giai đoạn trung gian trong quá trình điều chế nitric acid trong công nghiệp.
Câu 177: Trong công nghiệp, ammonia được tổng hợp theo quá trình Haber:
N2(g) + 3H2(g) 2NH3(g)
= - 92 kJ
a. Phản ứng trên là một phản ứng tỏa nhiệt theo chiều thuận.
b. Khi tăng áp suất cân bằng trên chuyển dịch theo chiều nghịch.
c. Khi giảm nhiệt độ cân bằng trên chuyển dịch theo chiều thuận.
d. Trong thực tế để phản ứng đạt hiệu suất cao người ta cần thực hiện phản ứng trên ở áp suất cao, nhiệt độ vừa phải.
Câu 178: Xét tính chất của muối ammonium.
a. Hầu hết các muối ammonium đều tan trong nước và phân li ra ion.
b. Khi đun nóng muối ammonium với dung dịch kiềm thấy xuất hiện khí mùi khai.
c. Nhiệt phân các muối ammonium đều thu được khí NH3.
d. Các muối ammonium khi nhiệt phân đều làm tăng áp suất nên có nguy cơ cháy nổ do đó cần bảo quản muối ammonium cẩn thận và tránh xa nguồn nhiệt.
Câu 179: Cho các NOx thường gặp trong không khí: NO, NO2, N2O, N2O4.
a. NO có tên gọi nitrogen monoxide, là một khí không màu hóa nâu trong không khí.
b. NO2 có tên gọi dinitrogen oxide, là một khí không màu còn gọi là khí cười.
c. N2O có tên gọi nitrogen dioxide, là một khí màu nâu đỏ.
d. N2O4 có tên gọi dinitrogen tetroxide, là một khí không màu.
Câu 180: Xét nguồn gốc các NOx trong không khí.
a. Do núi lửa phun trào, cháy rừng.
b. Do mưa dông kèm sấm sét và sự phân hủy các hợp chất vô cơ.
c. Do đốt cháy nhiên liệu trong các hoạt động giao thông, sản xuất.
d. Do trái đất nóng lên, băng tan ở hai cực.
Câu 181: Mưa acid là hiện tượng nước mưa có pH < 5,6.
a. Nguyên nhân gây mưa acid là do SO2, NOx trong không khí bị khử rồi hòa tan vào nước thành H2SO4, HNO3.
b. Nguồn gốc của SO2, NOx từ hoạt động của núi lửa, sấm sét, hoạt động công nghiệp, nhiệt điện, giao thông, …
c. Mưa acid tác động xấu đến môi trường, con người và sinh vật.
d. Mưa acid ăn mòn, phá hủy các công trình xây dựng bằng đá và kim loại.
Câu 182: Nitric acid là một chất có tính acid mạnh.
a. Dung dịch nitric acid làm quỳ tím chuyển màu đỏ.
b. Tất cả các basic oxide và oxide khi tác dụng với HNO3 đặc đều thu được muối nitrate và nước.
c. Một số muối có thể tác dụng với HNO3 tạo muối nitrate và acid yếu hơn.
d. Nitric acid khi tác dụng với muối có thể tạo ra muối nitrate như NH4NO3, Ca(NO3)2 là phân đạm cung cấp nguyên tố nitrogen cho cây trồng.
Câu 183: Phú dưỡng là hiện tượng dư thừa quá nhiều các nguyên tố dinh dưỡng (N, P) trong các nguồn nước làm cho các sinh vật trong nước như vi khuẩn, tảo, rong, rêu,… phát triển nhanh.
a. Nguyên nhân gây ra hiện tượng phú dưỡng do nguồn nước thải nông nghiệp, công nghiệp, sinh hoạt, ... chưa xử lí triệt để thải vào ao hồ.
b. Hiện tượng phú dưỡng làm giảm sự quang hợp của thực vật thủy sinh và làm tăng nguồn oxygen của tôm, cá, … gây mất cân bằng hệ sinh thái.
c. Các loại tôm, cá, … ở ao hồ có hiện tượng phú dưỡng thường khỏe mạnh và béo tốt vì có nguồn chất dinh dưỡng phong phú.
d. Để khắc phục hiện tượng phú dưỡng ta cần xử lí nước thải trước khi thải vào môi trường, sử dụng phân bón đúng liều lượng, khơi thông kênh rạch, ao hồ, lưu thông dòng nước.
III- CÂU TRẮC NGHIỆM YÊU CẦU TRẢ LỜI NGẮN
Câu 184: Cho phản ứng: N2(g) + 3H2(g) 2NH3(g). Ở một nhiệt độ xác định, khi phản ứng trên đạt trạng thái cân bằng thì nồng độ các chất là: [N2] = 0,01M; [H2] = 2 M; [NH3] = 0,4 M. Hằng số cân bằng KC của phản ứng ở nhiệt độ trên bằng bao nhiêu?
Câu 185: Ở 600 oC, khi phản ứng: H2(g) + CO2(g) H2O(g) + CO(g) đạt cân bằng thì nồng độ các chất lần lượt là:
H2 | CO2 | H2O | CO |
0,600 M | 0,459 M | 0,500 M | 0,420 M |
Hằng số cân bằng KC của phản ứng trên ở 600oC là bao nhiêu? Kết quả làm tròn đến phần trăm (sau dấu phẩy hai chữ số).
Câu 186: Ở 730 oC, hằng số cân bằng của phản ứng: H2(g) + Br2(g) 2HBr(g) là KC(1) = 2,86.106.
Cho 3,2 mol HBr vào bình phản ứng dung tích 10 lít ở 730 oC. Tính nồng độ HBr ở trạng thái cân bằng.
Câu 187: Khi tăng nhiệt độ, có bao nhiêu phản ứng chuyển dịch theo chiều thuận ?
Câu 188: Một dung dịch có chứa các ion: Na+ (0,2 mol), Mg2+ (0,1 mol), Ca2+ (0,05 mol), (0,15 mol) và Cl- (x mol). Giá trị của x là
Câu 189: Cho các dung dịch muối: KNO3, Na2CO3, NH4Cl, K2SO4, Cu(NO3)2. Số dung dịch có xảy ra phản ứng thủy phân của muối là bao nhiêu ?
Câu 190: Tính pH của dung dịch thu được sau khi trộn 50 mL dung dịch HCl 0,4 M với 50 mL dung dịch NaOH 0,5 M.



