
Preview text:
SỞ GIÁO DỤC VÀ ĐÀO TẠO
ĐỀ KIỂM TRA GIỮA HỌC KỲ II BẮC NINH
NĂM HỌC 2022 – 2023
Môn: HÓA HỌC – Lớp 11 (Đề có 02 trang)
Thời gian làm bài: 45 phút (không kể thời gian giao đề)
* Cho biết nguyên tử khối của các nguyên tố: H=1; C=12; N=14; O=16; Br=80; Ag=108.
* Các thể tích khí đo ở điều kiện tiêu chuẩn; giả thiết các khí sinh ra không tan trong nước.
I. PHẦN TRẮC NGHIỆM (3,0 điểm)
Câu 1: Chất nào sau đây là chất hữu cơ? A. C2H4. B. CO. C. CaCO3. D. CO2.
Câu 2: Cho thí nghiệm như hình vẽ:
Thí nghiệm trên dùng để định tính nguyên tố nào có trong glucozơ? A. Cacbon. B. Hiđro và oxi. C. Cacbon và hiđro. D. Cacbon và oxi.
Câu 3: Hợp chất Z có công thức đơn giản nhất là CH2O và có tỉ khối hơi so với hiđro bằng 30,0. Công thức phân tử của Z là A. CH2O. B. C2H4O2. C. C2H4O. D. C2H6O2.
Câu 4: Cặp chất nào sau đây là đồng phân của nhau?
A. CH3-OH và CH3-CH2-OH.
B. CH3-CH2-OH và CH3-COOH.
C. CH3CH2CH3 và CH3CH=CH2. D. HCOOCH3 và CH3COOH.
Câu 5: Ankan X có công thức CH3CH2CH3. Tên gọi của X là A. etan. B. pentan. C. butan. D. propan.
Câu 6: Cho butan tác dụng với Cl2 có ánh sáng khuếch tán, tỉ lệ số mol 1 : 1, số sản phẩm monoclo tối đa thu được là A. 4. B. 3. C. 1. D. 2.
Câu 7: Số liên kết π (pi) có trong phân tử vinyl axetilen (CH2=CH–C≡CH) là A. 1. B. 2. C. 3. D. 4.
Câu 8: Hấp thụ hoàn toàn 2,24 lít khí C2H2 vào lượng dư dung dịch AgNO3 trong NH3, sau phản ứng
thu được m gam kết tủa. Giá trị của m là A. 24,0. B. 21,6. C. 36,0. D. 12,0.
Câu 9: Số nguyên tử hiđro trong phân tử etilen là A. 2. B. 6. C. 4. D. 8.
Câu 10: Cho các chất sau: metan, etilen, buta-1,3-đien, isopren, anlen, axetilen, but-2-in. Số chất tác
dụng được với nước brom ở điều kiện thường là A. 4. B. 5. C. 6. D. 3.
Câu 11: Chất nào sau đây tác dụng với dung dịch KMnO4 ở điều kiện thường? A. Propen. B. Etan. C. Metan. D. Propan. Trang 1
SỞ GIÁO DỤC VÀ ĐÀO TẠO HƯỚNG DẪN CHẤM BẮC NINH
ĐỀ KIỂM TRA GIỮA HỌC KỲ II ¯¯¯¯¯¯¯¯¯¯
NĂM HỌC 2022 – 2023
Môn: Hóa Học – Lớp - 11
¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯¯
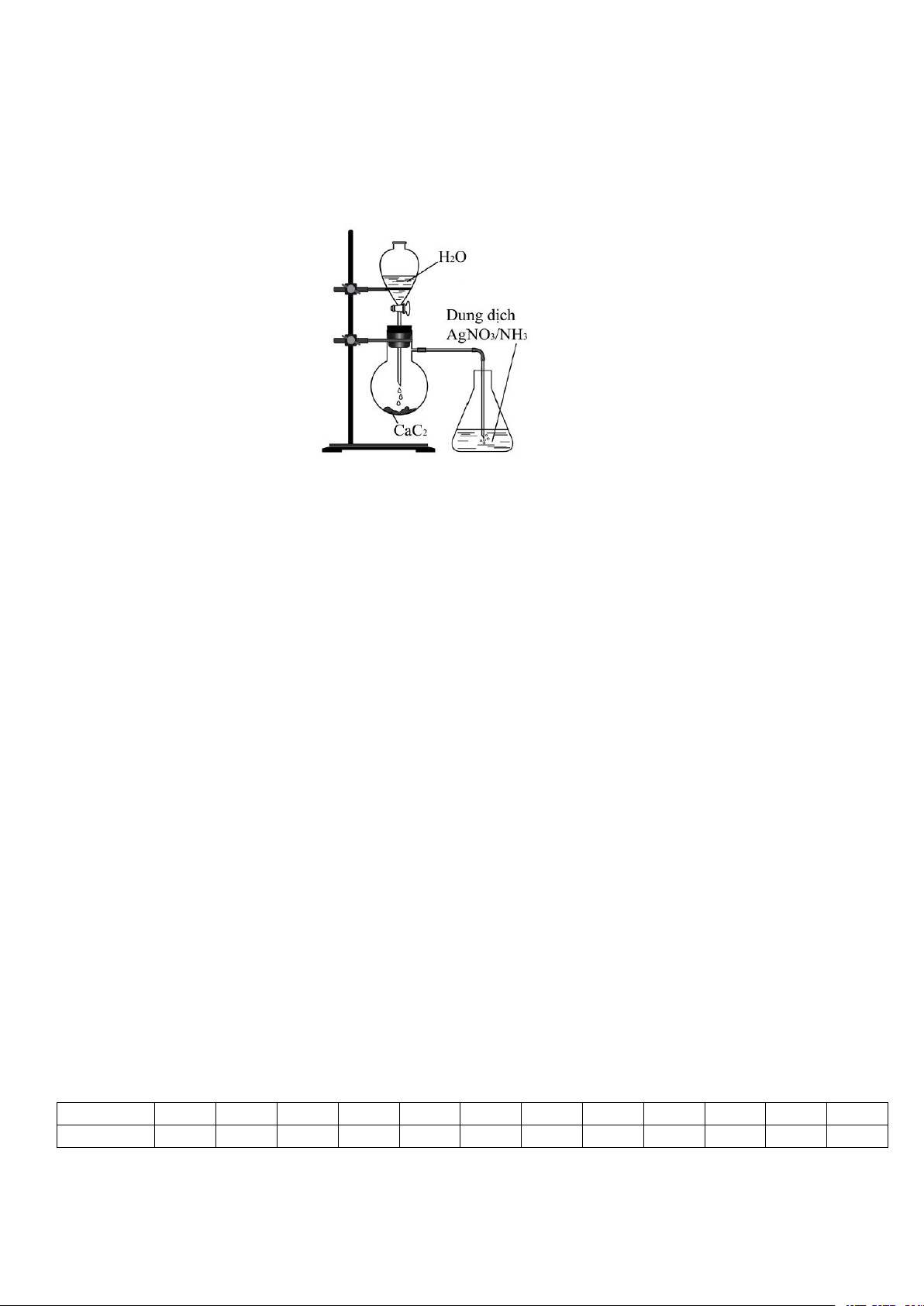
Câu 12: Thí nghiệm được tiến hành như hình vẽ bên. Hiện tượng xảy ra trong bình đựng dung dịch AgNO3 trong NH3 là
A. có kết tủa màu nâu đỏ.
B. có kết tủa màu vàng nhạt.
C. dung dịch chuyển sang màu da cam.
D. dung dịch chuyển sang màu xanh lam.
II. PHẦN TỰ LUẬN (7,0 điểm)
Câu 13. (2,0 điểm) Viết phương trình hóa học của các phản ứng xảy ra trong các trường hợp sau: a) CH3-CH2-CH=CH2 + Br2 b) CH3-CH=CH2 + H2O + 0 H , t
c) CH2=CH2 + KMnO4 + H2O d) C 0 t 2H2 + O2
Câu 14: (2,0 điểm) Trình bày phương pháp hóa học để nhận biết các khí riêng biệt sau: etan, propen,
propin, cacbonic. Viết phương trình hóa học của các phản ứng xảy ra.
Câu 15: (3,0 điểm) Dẫn 5,04 lít hỗn hợp khí X gồm {propan, etilen, axetilen} qua dung dịch brom dư,
thấy còn 1,26 lít khí không bị hấp thụ. Mặt khác, nếu dẫn 5,04 lít hỗn hợp khí X trên qua lượng dư
dung dịch AgNO3 trong NH3 thấy có 32,4 gam kết tủa vàng nhạt.
a. Viết phương trình hóa học để giải thích các hiện tượng ở thí nghiệm trên.
b. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp X.
c. Lấy lượng khí axetilen có trong 5,04 lít hỗn hợp khí X trên tác dụng vừa đủ với dung dịch chứa
0,18 mol Br2 trong CCl4. Tính khối lượng mỗi chất hữu cơ thu được.
–––––––– Hết –––––––
PHẦN I. TRẮC NGHIỆM (3,0 điểm)
Mỗi câu đúng được 0,25 điểm. Câu 1 2 3 4 5 6 7 8 9 10 11 12 Đáp án A C B D D D C A C C A B
PHẦN II. TỰ LUẬN (7,0 điểm) Trang 2 Câu Hướng dẫn Điểm
Câu 13. Mỗi công thức viết đúng, gọi tên đúng cho 0,5 đ 2,0đ a) CH3-CH2-CH=CH2 + Br2 CH3-CH2-CHBr-CH2Br 0,5đ b) CH 0,5đ 3-CH=CH2 + H2O + 0 H , t CH3CH(OH)CH3 CH3-CH=CH2 + H2O + 0 H , t CH3CH2CH2OH
c) 3CH2=CH2 + 2KMnO4 + 4H2O
3HOCH2CH2OH + 2KOH + 2MnO2↓ 0,5đ d) C 0 t 2H2 + 5/2O2 2CO2 + H2O 0,5đ
Câu 14. Để nhận biết các khí trên ta có thể tiến hành như sau: 2,0đ
- Dẫn lần lượt các khí qua dung dịch Ca(OH)2 dư
+ Có kết tủa trắng => CO2
CO2 + Ca(OH)2 CaCO3↓ + H2O 0,5đ
+ Không có hiện tượng => CH3-CH3, CH3-CH=CH2, CH3-C≡CH
- Dẫn lần lượt CH3-CH3, CH3-CH=CH2, CH3-C≡CH qua dung dịch AgNO3 trong dung dịch NH3
+ Có kết tủa vàng nhạt => CH3-C≡CH 0,5đ
CH3-C≡CH + AgNO3 + NH3 CH3-C≡CAg↓ + NH4NO3
+ Không thấy hiện tượng => CH3-CH3, CH3-CH=CH2
- Dẫn lần lượt CH3-CH3, CH3-CH=CH2 qua dung dịch nước Brom
+ Màu nâu đỏ của dung dịch nhạt dần => CH3-CH=CH2 0,5đ CH3-CH=CH2 + Br2 CH3-CHBr-CH2Br
+ Không thấy hiện tượng => CH3-CH3 0,5đ Câu 15. 3,0đ Câu 15. a) 0,75đ CH2=CH2 + Br2 CH2Br-CH2Br (1) 0,25đ CH≡CH + 2Br 0,25đ 2 (dư) CHBr2-CHBr2 (2) CH≡CH + 2AgNO 0,25đ
3 + 2NH3 AgC≡CAg↓ + 2NH4NO3 (3) Câu 15. b) 1,5đ nX = 5,04/22,4 = 0,225 mol;
- Khi cho X qua dung dịch brom dư => Khí không bị hấp thụ là CH3CH2CH3
=> nCH3CH2CH3= 1,26/22,4 = 0,05625 mol; 0,05625 %V =%n = .100%=25% 0,5đ CH3CH2CH3 CH3CH2CH3 0,225
- Khi cho X qua dung dịch AgNO3 trong NH3 chỉ có CH≡CH tác dụng
=> Theo phương trình (3) nAgC≡CAg↓= 32,4/240 = 0,135 mol => nCH≡CH =0,135 mol 0,135 %V =%n = .100%=60% CH CH CH CH 0,225 0,5đ %V =15% CH 0,5đ 2 =CH2 Câu 15. c) 0,75đ
nCH≡CH =0,135 mol; nBr2= 0,18 mol => xảy ra 2 phản ứng CH≡CH + Br2 CHBr=CHBr (4) CH≡CH + 2Br 0,25đ 2 CHBr2-CHBr2 (5)
Gọi số mol của CH≡CH phản ứng ở (4), (5) lần lượt là x, y mol => x + y = 0,135 x + 2y = 0,18 => x = 0,09; y = 0,045 0,25đ
=> mCHBr=CHBr = 0,09. 186 = 16,74 gam m 0,25đ
CHBr2-CHBr2= 0,045. 346 = 15,57 gam
Chú ý: Học sinh làm cách khác đúng vẫn cho điểm tối đa.
-------------Hết------------- Trang 3