






Preview text:
SỞ GIÁO DỤC VÀ ĐÀO TẠO
THI THỬ TỐT NGHIỆP THPT NĂM 2025 (LẦN 2) TỈNH THÁI NGUYÊN Môn thi: HÓA HỌC. ĐỀ THI CHÍNH THỨC
Thời gian làm bài: 50 phút, không kể thời gian phát đề.
(Đề thi có 6 trang) Mã đề thi 0301
Họ, tên thí sinh: .........................................................................................
Số báo danh: ..............................................................................................
Cho biết nguyên tử khối: H = 1; C = 12; Cl = 35,5; O = 16; S = 32; Al = 27; N = 14; P = 31; Na = 23; Mg = 24;
Ba = 137; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Cd = 112; Pb = 207.
Phần I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Polymer nào sau đây được điều chế bằng phản ứng trùng ngưng?
A. Poly(methyl methacrylate). B. Polyethylene.
C. Poly(hexamethylene adipamide).
D. Poly(vinyl chloride).
Câu 2: Phát biểu nào sau đây về carbohydrate là đúng?
A. Saccharose là chất lỏng, có vị ngọt và dễ tan trong nước.
B. Tinh bột và cellulose thuộc nhóm disaccharide.
C. Glucose và fructose có nhiều trong mật ong.
D. Maltose được cấu tạo từ một đơn vị α-glucose và một đơn vị β-fructose.
Câu 3: Nước cứng là loại nước có chứa hàm lượng các khoáng chất hòa tan dưới dạng các ion, chủ
yếu là cation Ca2+ và Mg2+ cao vượt quá mức cho phép (trên 300 mg/L). Nước cứng có nhiều tác hại
khi dùng lâu dài như: viêm da, khô tóc, quần áo bị xơ cứng, mau mục,…Có nhiều biện pháp để làm
mềm nước cứng, một trong những biện pháp đó là sử dụng các hóa chất. Chất nào sau đây có thể được
dùng để làm mềm nước cứng tạm thời? A. Ca(OH)2. B. Na2SO4. C. HCl. D. Na2S.
Câu 4: Không nên bón vôi sống (thành phần chính là CaO) cùng với phân superphosphate. Nguyên
nhân của khuyến cáo này là
A. làm giảm hàm lượng P2O5 trong phân bón do tạo ra Ca3(PO4)2 không tan.
B. tạo acid làm ảnh hưởng tới cây trồng.
C. làm đất bị chua.
D. xảy ra phản ứng trung hòa làm giảm pH của đất.
Câu 5: Cho dãy các kim loại: Na, Cu, Al, Cr. Kim loại mềm nhất trong dãy là A. Na. B. Cr. C. Cu. D. Al.
Câu 6: Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
A. Nhúng thanh Zn vào dung dịch hỗn hợp gồm H2SO4 và CuSO4.
B. Nhúng thanh Zn vào dung dịch H2SO4 loãng.
C. Để đinh sắt (làm bằng thép carbon) trong không khí ẩm.
D. Nhúng thanh sắt (làm bằng thép carbon) vào dung dịch H2SO4 loãng.
Câu 7: Chất nào sau đây được sử dụng làm thành phần chính của xà phòng? A. CH3COOK. B. C2H5ONa.
C. CH3[CH2]14COONa. D. CH3[CH2]16COOH.
Câu 8: Khi đun nóng hỗn hợp gồm nước và ethanol thu được từ quá trình lên men rượu, hơi bay ra
được dẫn qua ống làm lạnh để ngưng tụ thành chất lỏng, thu được dung dịch rượu có nồng độ cao hơn.
Phương pháp được sử dụng trong quá trình này là A. chiết. B. sắc kí. C. chưng cất. D. kết tinh.
Câu 9: Ở điều kiện thường, amine nào sau đây là chất khí, có mùi khai và tan nhiều trong nước? A. Diethylamine. B. Propylamine. C. Aniline. D. Methylamine.
Trang 1/6 - Mã đề thi 0301
Câu 10: Insulin là hocmon thuộc loại protein, được sinh ra bởi tuyến tụy, có chức năng điều hòa quá
trình chuyển hóa glucose trong cơ thể. Thủy phân một phần insulin thu được heptapeptide X. Khi thủy
phân không hoàn toàn X, thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu,
Val-Glu-Ala, His-Leu-Val, Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là 1, thì amino acid ở
vị trí số 3 trong X có kí hiệu là A. His. B. Leu. C. Val. D. Glu.
Câu 11: Cho các phát biểu sau về quá trình cháy của các hợp chất hữu cơ:
a) Khí CO là sản phẩm của quá trình cháy không hoàn toàn của các hợp chất hữu cơ.
b) Trong đám cháy không hoàn toàn, carbon chưa cháy hết dạng hạt có thể tạo ra khói đen.
c) HCl có thể sinh ra từ các đám cháy có chứa nhựa PVC.
d) Cách tốt nhất để xử lý rác thải nhựa, túi nylon là đốt cháy hoàn toàn. Các phát biểu đúng là A. b), d). B. a), c). C. a), b), c). D. a), c), d).
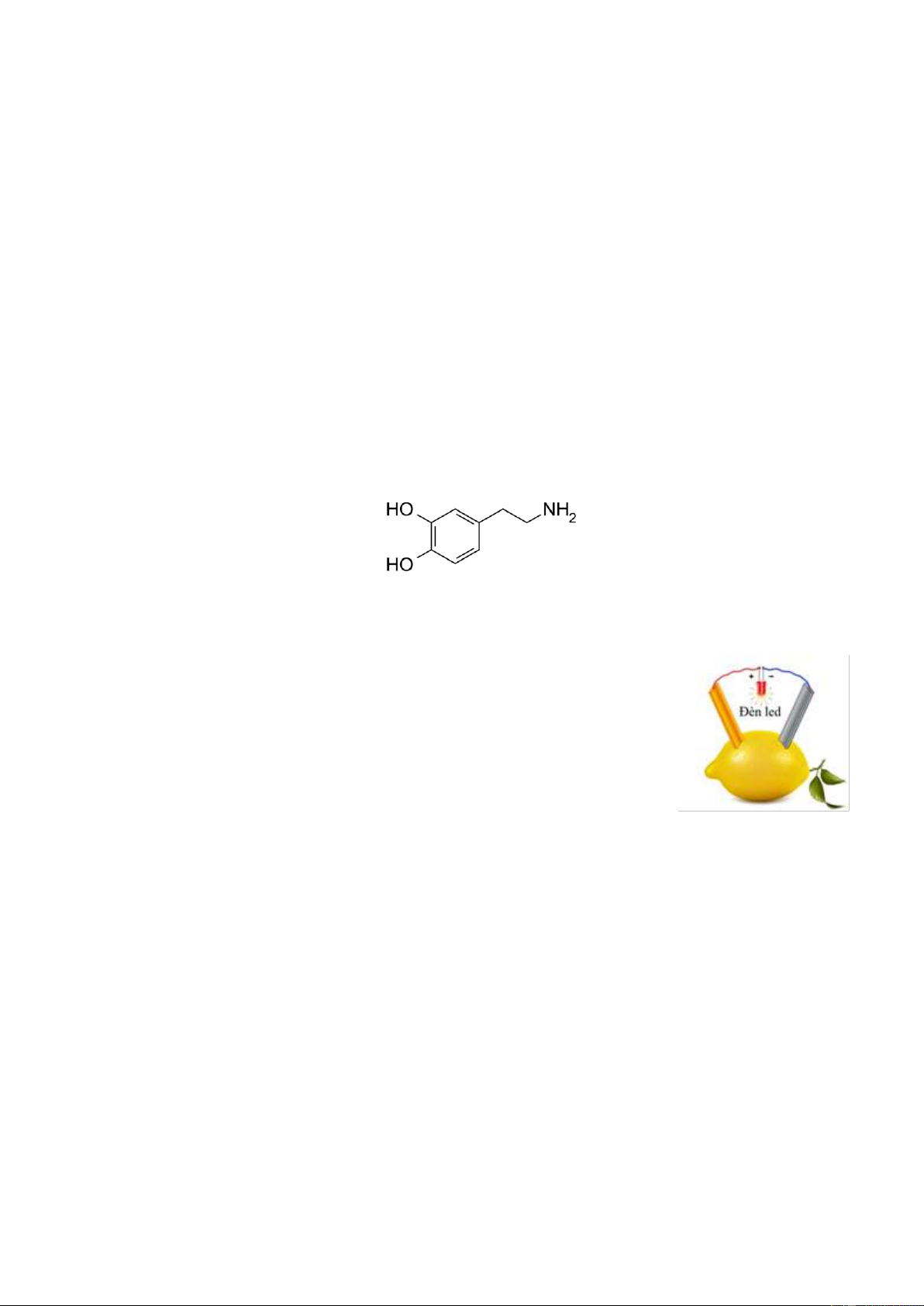
Câu 12: Dopamin là một hóa chất quan trọng có trong não, ảnh hưởng đến tâm trạng cũng như cảm
giác của bạn về sự hưng phấn, vui vẻ. Vì vậy, dopamine còn được gọi là hormone hạnh phúc. Dopamin
có công thức cấu tạo như sau:
Công thức phân tử của dopamine là A. C8H4O2N. B. C8H11O2N. C. C9H14O2N. D. C9H13O2N.
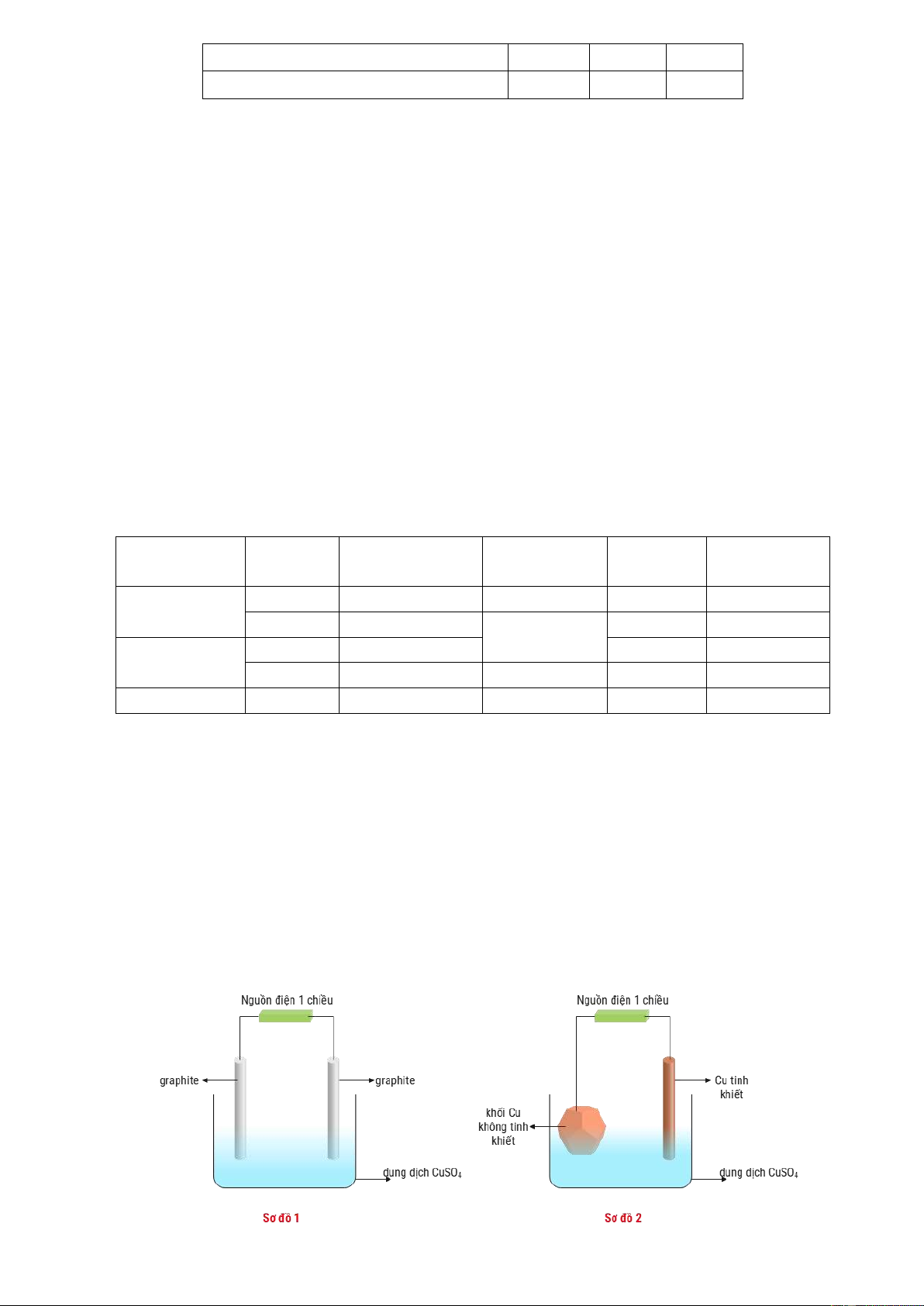
Câu 13: Một học sinh tiến hành thí nghiệm, sử dụng các thanh zinc (Zn),
thanh copper (Cu), dây dẫn, đèn LED và quả chanh để lắp ráp pin chanh như hình vẽ bên: Cho o E = -0,76 V. 2+ Zn /Zn o E = 0,34 V. 2+ Cu /Cu
Sau khi tiến hành thí nghiệm, học sinh đã viết báo cáo thực hành, nội dung
nào sau đây trong báo cáo không đúng? A. Do o E < o E
nên pin chanh tạo thành có Zn là cực âm, Cu là cực dương. 2+ Zn /Zn 2+ Cu /Cu
B. Ở điện cực dương xảy ra quá trình khử ion Cu2+: Cu2+ + 2e Cu.
C. Bóng đèn LED sáng yếu chứng tỏ có dòng điện chạy qua.
D. Sức điện động chuẩn của pin chanh trong thí nghiệm gần bằng 1,1 V.
Câu 14: Hợp chất hữu cơ nào sau đây thuộc loại ester? A. CH3OH. B. HCOOCH3. C. CH3COOH. D. CH3CHO.
Câu 15: Cho cấu hình electron nguyên tử của các nguyên tố sau: X: 1s22s22p6; Y: 1s22s22p63s2; Z: 1s22s22p3; T: 1s22s22p63s23p3.
Nhận xét nào sau đây đúng?
A. Z và T là phi kim.
B. Chỉ có T là phi kim.
C. X là khí hiếm, Z là kim loại.
D. Y và Z đều là kim loại.
Trang 2/6 - Mã đề thi 0301
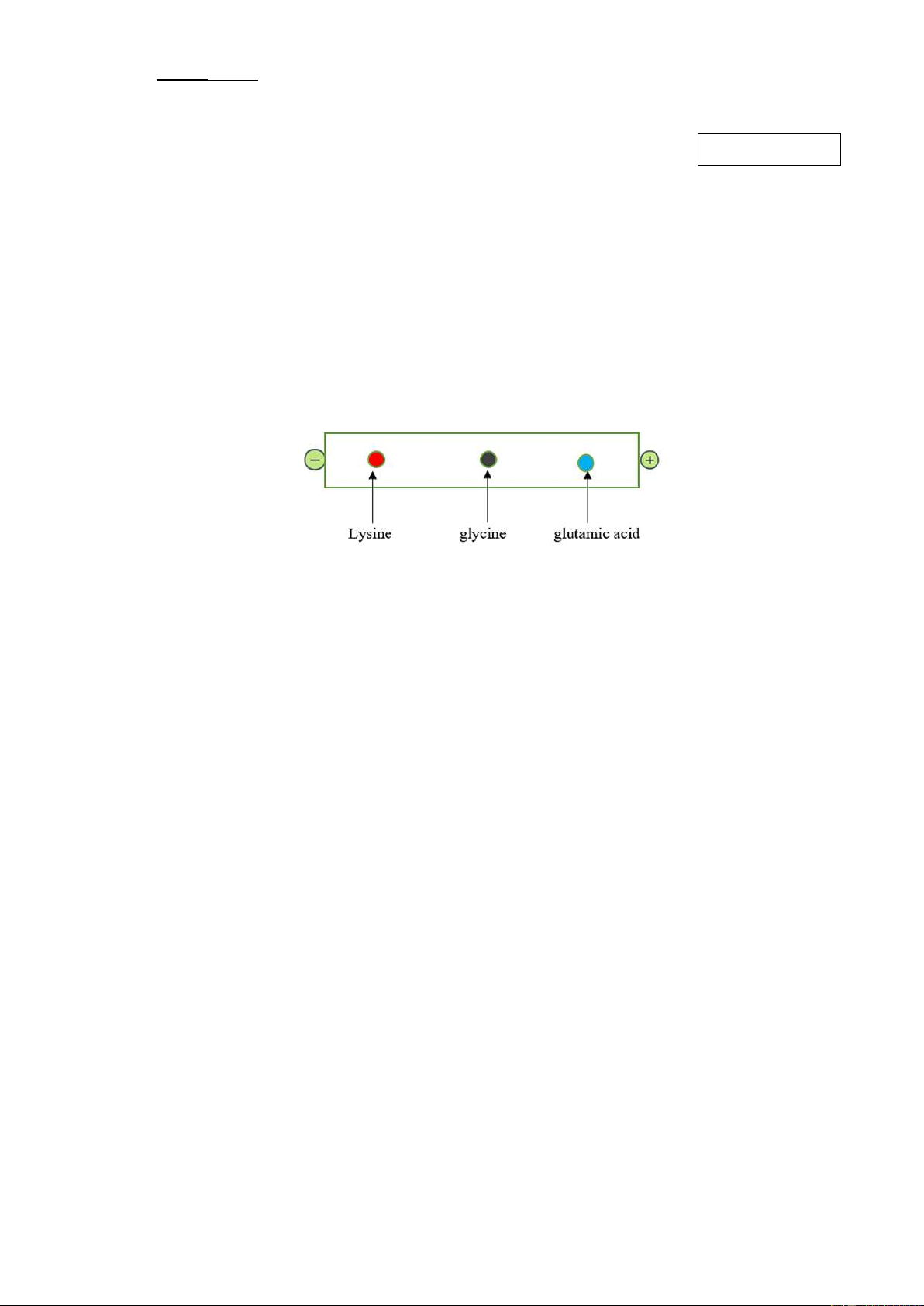
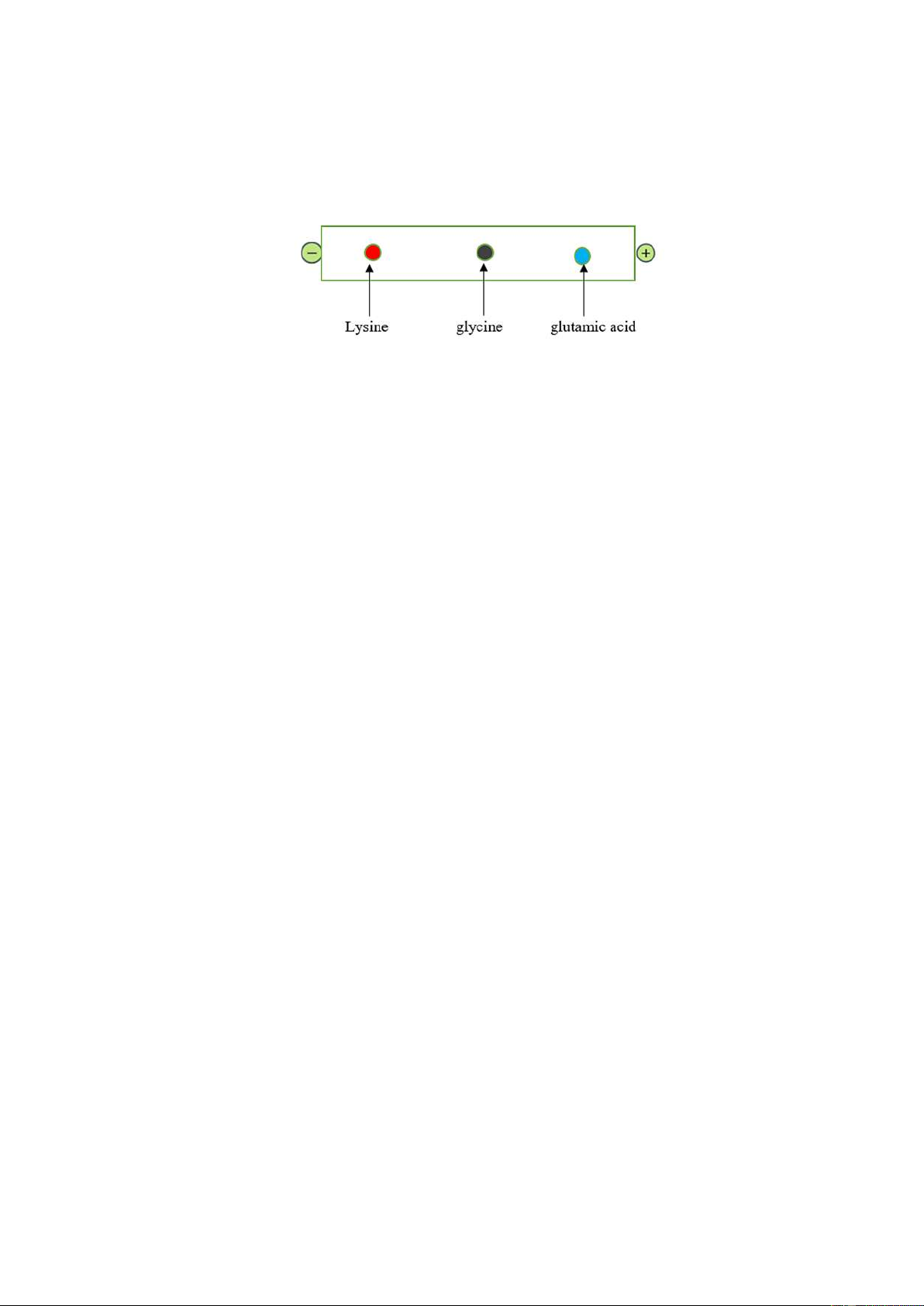
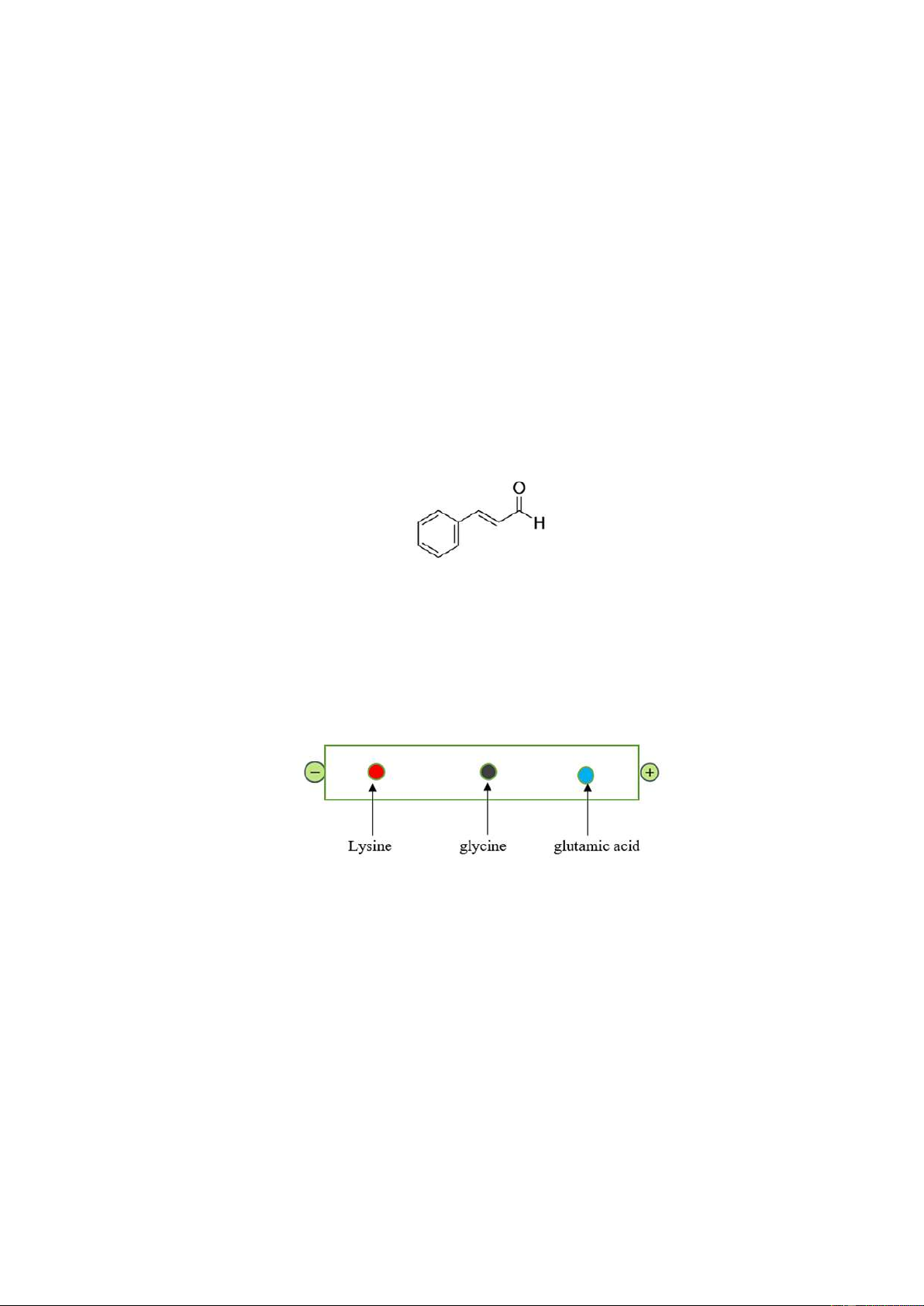
Câu 16: Quan sát hình ảnh sau đây:
Thực hiện thí nghiệm, đặt các amino acid trong điện trường, môi trường có pH bằng 6, phát biểu nào sau đây là đúng?
A. Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng anion.
B. Các amino acid tồn tại chủ yếu ở dạng ion lưỡng cực nên sẽ di chuyển về hai đầu điện cực.
C. Glutamic acid dịch chuyển về phía cực dương nên glutamic acid tồn tại chủ yếu ở dạng cation.
D. Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng ion lưỡng cực.
Câu 17: Cho thế điện cực chuẩn của các cặp oxi hóa – khử sau: o E o − E 2+ = +1,51 V và + = +0,77 V. MnO / Mn 3+ 2 4 Fe /Fe
Phát biểu nào sau đây sai? A. Ion MnO -
4 có tính oxi hóa mạnh hơn ion Fe3+.
B. Ion Fe2+ có tính khử mạnh hơn ion Mn2+. C. Ion MnO -
4 có thể oxi hóa ion Fe2+ trong dung dịch thành ion Fe3+. D. Ion MnO -
4 có thể khử ion Fe3+ trong dung dịch thành ion Fe2+.
Câu 18: Dãy gồm các kim loại được xếp theo thứ tự nhiệt độ nóng chảy tăng dần từ trái sang phải là A. Li, Na, K. B. Li, K, Na. C. K, Na, Li. D. K, Li, Na.
Phần II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Mẻ là một loại gia vị truyền thống tạo nên hương vị đặc trưng cho nhiều món ăn của ẩm thực
Việt Nam. Người ta thường làm mẻ bằng cách lên men bún hoặc cơm nát để nguội. Quá trình lên men
diễn ra nhờ vi khuẩn kỵ khí, biến tinh bột và đường thành lactic acid. Chính acid này đã tạo nên vị
chua của mẻ, sữa chua… Quá trình lên men thành lactic acid xảy ra các phản ứng hóa học sau: enzyme (C ⎯⎯⎯→ 6H10O5)n + nH2O nC6H12O6 enzyme C ⎯⎯⎯→ 6H12O6 2CH3CH(OH)COOH
Một học sinh tiến hành thử nghiệm làm ba lọ mẻ theo các cách sau:
- Lọ 1: Cho 150 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn 150 mL nước vo gạo, rồi đậy kín.
- Lọ 2: Cho 150 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn 50 mL nước đường saccharose 10%, rồi đậy kín.
- Lọ 3: Cho 150 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn khoảng 50 gam mẻ, rồi đậy kín.
Giả sử các điều kiện thực hiện phản ứng lên men đều giống nhau.
a) Thời gian thu được mẻ ngắn nhất là lọ 2 do saccharose dễ lên men hơn tinh bột.
b) Cơm nát chứa carbohydrate chủ yếu là tinh bột.
c) Có thể thay cơm nát bằng bánh mì vì đều chứa carbohydrate phức tạp.
d) Lactic acid tạo thành là một hợp chất hữu cơ tạp chức.
Câu 2: Hòa tan 0,350 gam mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả
lượng sắt có trong quặng đều chuyển thành Fe2+, thu được dung dịch X. Chuẩn độ Fe2+ trong dung dịch
X ba lần bằng chất chuẩn là dung dịch thuốc tím KMnO4 0,015M. Kết quả:
Trang 3/6 - Mã đề thi 0301 Lần chuẩn độ Lần 1 Lần 2 Lần 3
V dung dịch KMnO4 đã dùng (mL) 14,90 15,05 15,10
Mỗi phát biểu dưới đây là đúng hay sai?
a) Cần thêm chất chỉ thị phù hợp vào bình tam giác chứa dung dịch X để xác định được thời điểm
kết thúc quá trình chuẩn độ.
b) Cần tiến hành thí nghiệm chuẩn độ 3 lần để giảm sai số ngẫu nhiên, bảo đảm tính chính xác của kết quả.
c) Nếu chỉ có Fe2+ trong dung dịch X tác dụng được với thuốc tím thì việc chuẩn độ dung dịch X sẽ
giúp xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được % (theo khối lượng)
của nguyên tố sắt có trong mẫu khoáng vật là 18,02%.
d) Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch thuốc tím từ burette vào bình tam giác chứa dung dịch X.
Câu 3: Acetic acid là hợp chất hữu cơ phổ biến, tạo vị chua đặc trưng cho giấm ăn. Ngoài vai trò trong
ẩm thực, nó còn được dùng để:
- Bảo quản thực phẩm nhờ khả năng ức chế vi khuẩn.
- Tẩy cặn khoáng (CaCO3) trong ấm đun, vòi nước.
- Nguyên liệu tổng hợp dược phẩm (paracetamol), sợi tổng hợp (cellulose acetate).
Cho biết số sóng hấp thụ đặc trưng trên phổ hồng ngoại của một số nhóm chức cơ bản như sau: Liên kết Liên kết Loại hợp chất Số sóng (cm-1) Loại hợp chất Số sóng (cm-1) hấp thụ hấp thụ C=O 1740 – 1685 Alcohol O-H 3500 - 3200 Aldehyde C-H 2850 - 2695 C=O 1750 - 1715 Ester C=O 1760 - 1690 C-O 1300 - 1000 Carboxylic acid O-H 3300 - 2500 Ketone C=O 1715 – 1666 Amine N-H 3300 - 3000
Mỗi phát biểu dưới đây là đúng hay sai?
a) Phổ IR của acetic acid có peak ~1700 cm-1 và ~2900 cm-1.
b) Nhóm carboxyl (-COOH) phân ly thành H⁺ trong nước, tạo tính acid yếu.
c) Acetic acid có 2 liên kết π và 7 liên kết σ.
d) Giấm ăn pha loãng có thể làm mất mùi khai của ammonia (NH3) do phản ứng tạo ammonium acetate.
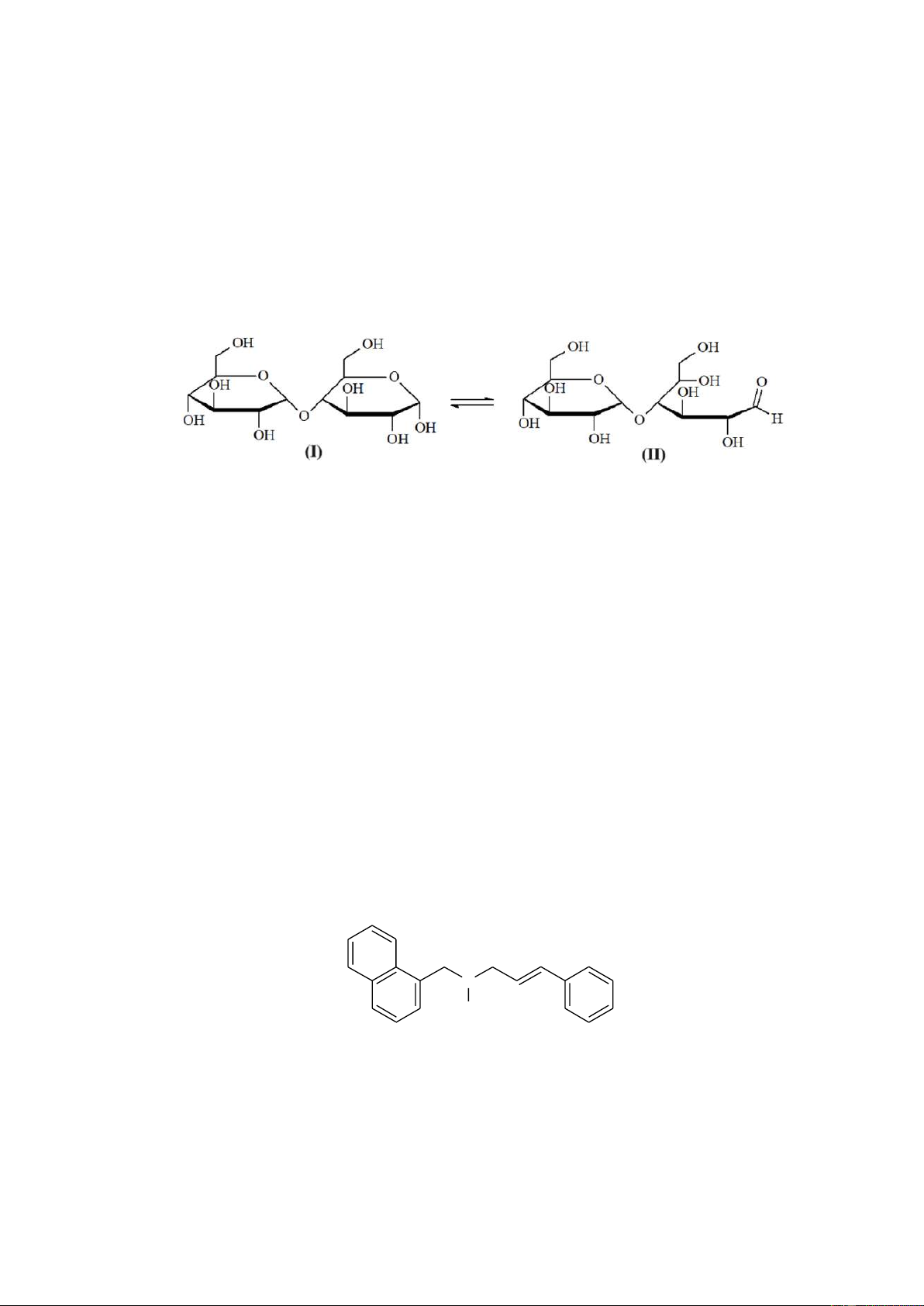
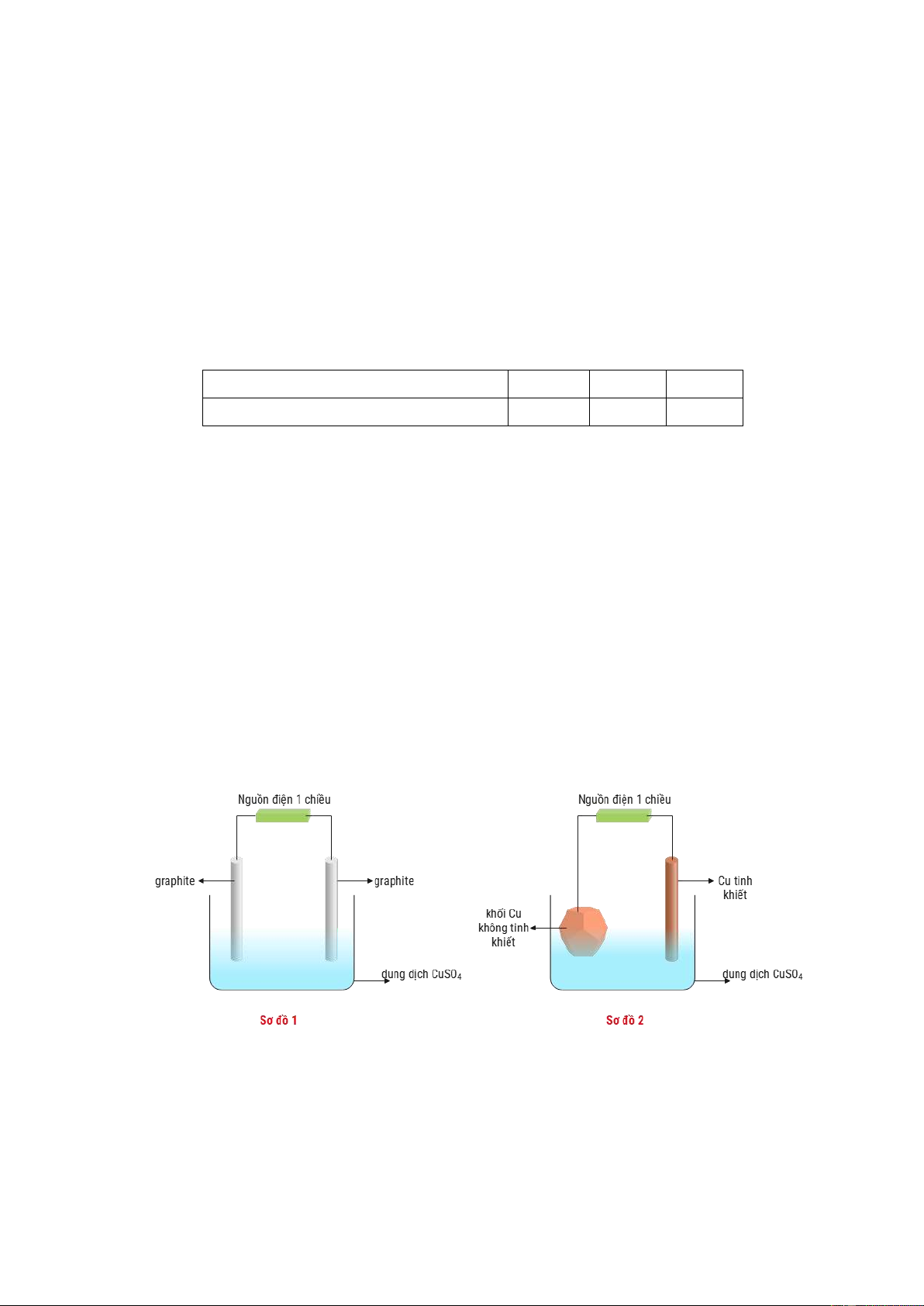
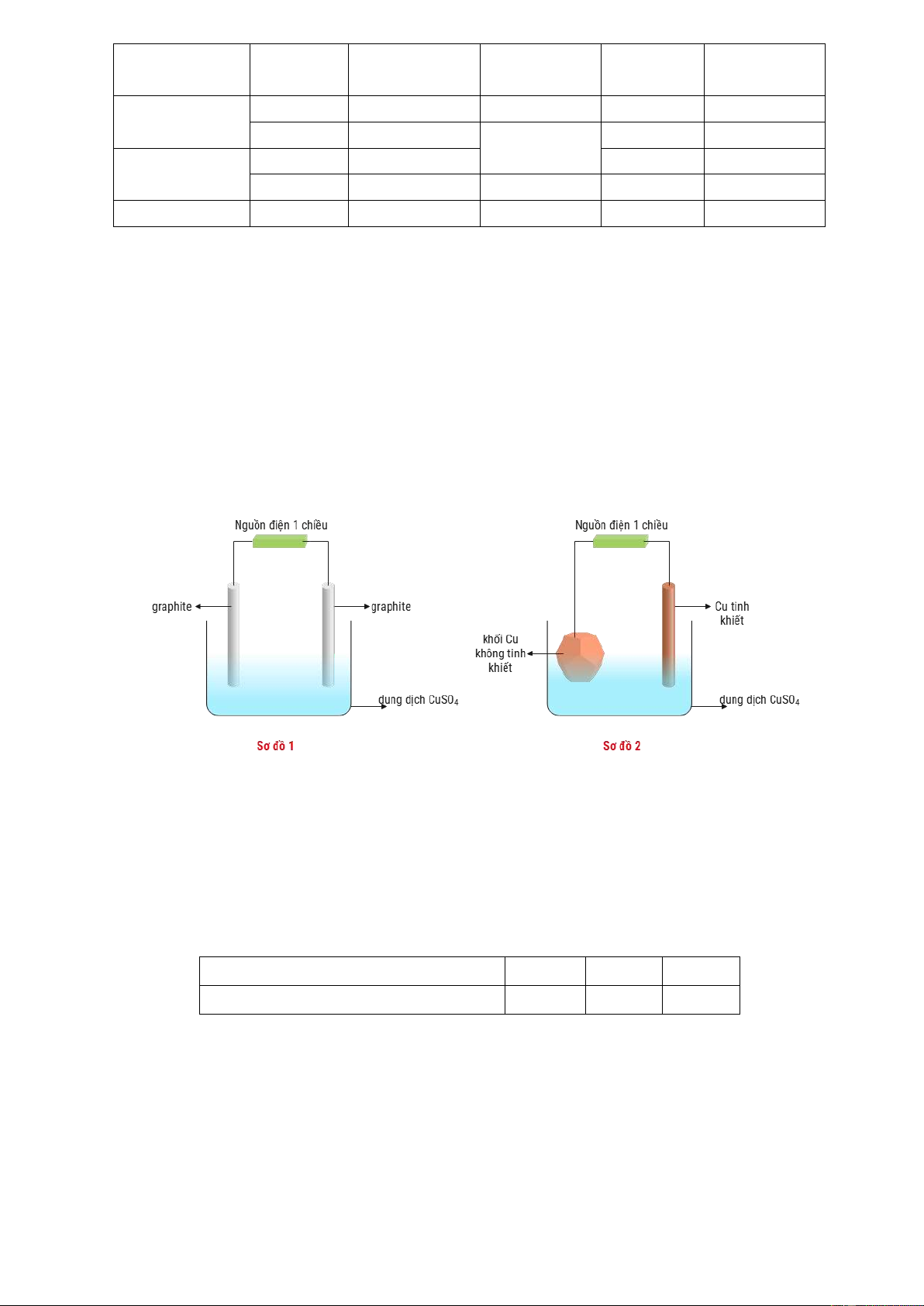
Câu 4: Cho sơ đồ 1 biểu diễn sự điện phân dung dịch CuSO4(aq) với điện cực trơ, sơ đồ 2 biểu diễn
quá trình tinh luyện đồng (Cu) bằng phương pháp điện phân. Trong sơ đồ 2, các khối đồng có độ tinh
khiết thấp được gắn với một điện cực của nguồn điện, các thanh đồng mỏng có độ tinh khiết cao được
gắn với một điện cực của nguồn điện. Dung dịch điện phân trong cả hai sơ đồ là dung dịch CuSO4.
Trang 4/6 - Mã đề thi 0301
a) Khi điện phân xảy ra ở sơ đồ 2, nồng độ ion Cu2+ trong dung dịch sẽ giảm dần theo thời gian.
b) Khi điện phân xảy ra ở sơ đồ 1, thì ban đầu ở cực âm xảy ra quá trình khử ion Cu2+ và ở cực
dương xảy ra quá trình oxi hóa H2O.
c) Trong cả hai sơ đồ, điện cực âm luôn xảy ra quá trình khử và điện cực dương luôn xảy ra quá trình oxi hóa.
d) Muốn tinh luyện Cu như sơ đồ 2 thì khối Cu không tinh khiết phải được nối vào anode, còn thanh Cu
tinh khiết được nối vào cathode, khi đó khối lượng Cu tan ra từ anode bằng khối lượng Cu tạo ra ở cathode.
Phần III. Thí sinh trả lời từ câu 1 đến câu 6.
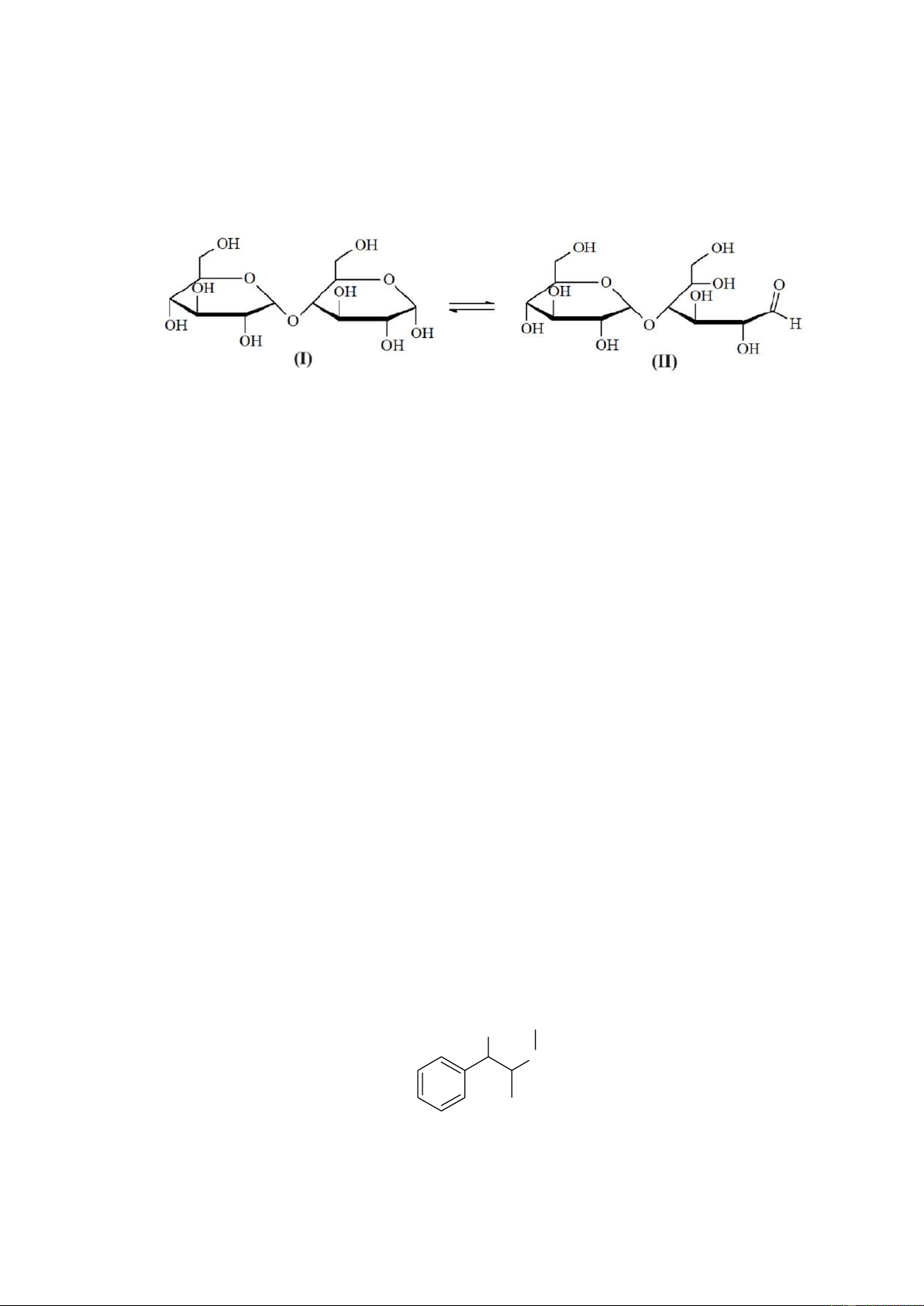
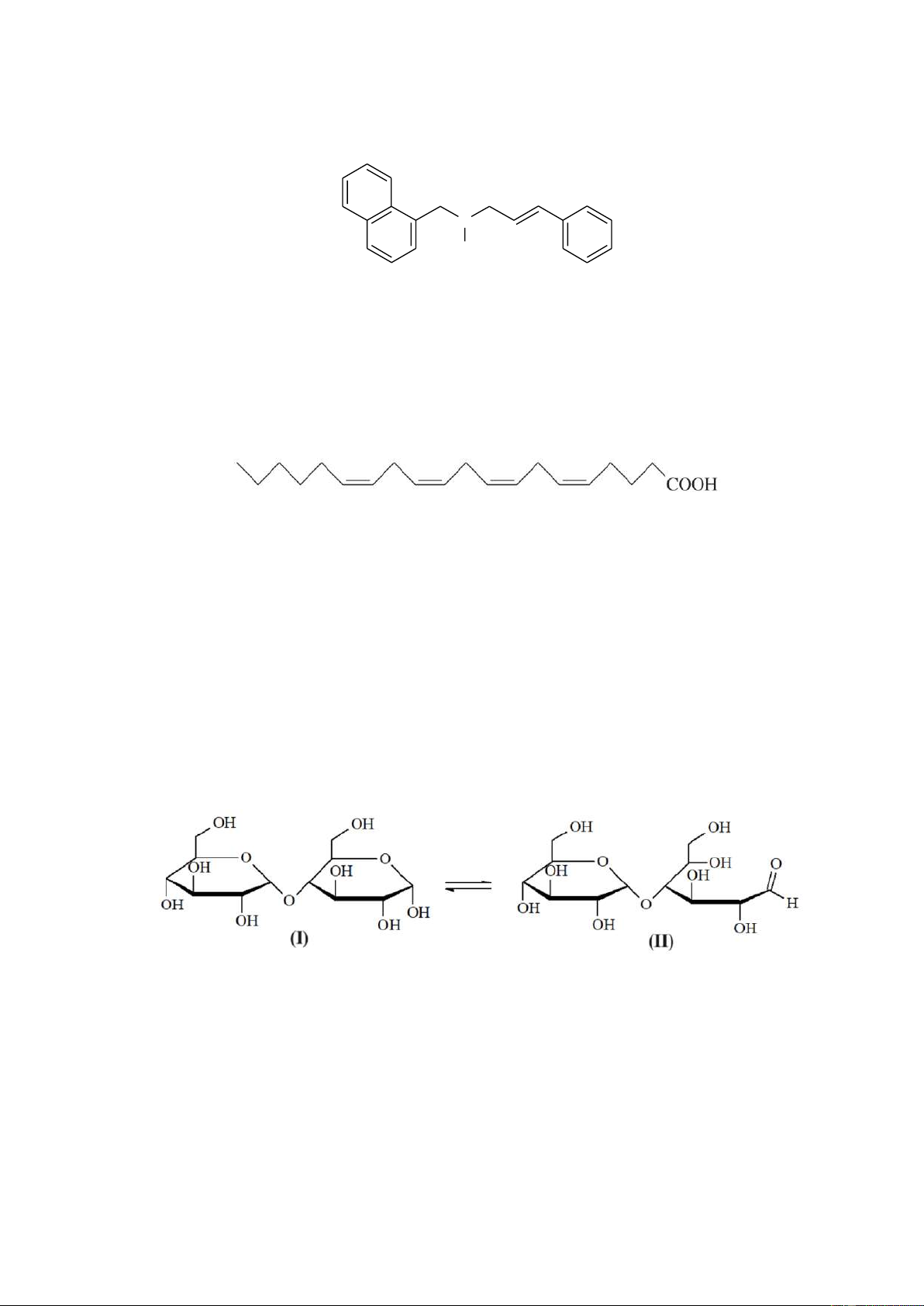
Câu 1: Maltose là thành phần chính của đường mạch nha. Trong dung dịch nước, maltose tồn tại chủ
yếu ở hai dạng cấu tạo (I) và (II). Các dạng này tồn tại trong cân bằng sau:
Maltose thủy phân trong môi trường acid hoặc enzyme tạo thành glucose. Cho các phát biểu sau:
1) Dạng (I) có nhiều liên kết sigma hơn dạng (II).
2) Liên kết giữa hai đơn vị monosaccharide trong phân tử maltose là liên kết β-1,4-glycoside.
3) Enzyme maltase xúc tác đặc hiệu cho phản ứng thủy phân maltose.
4) Phản ứng thủy phân maltose trong dung dịch H2SO4 98% xảy ra nhanh hơn trong dung dịch
H2SO4 50% vì nồng độ acid lớn hơn.
5) Dạng (I) có một nhóm –OH hemiacetal.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.
Câu 2: Biến thiên enthalpy chuẩn của quá trình “H2O(s) ⟶ H2O(l)” là 6,020 kJ.
Biết rằng để làm cho nhiệt độ của 1 mol nước lỏng thay đổi 1 °C cần một nhiệt lượng là 75,4 J. Giả
sử mỗi viên nước đá tương ứng với 1 mol nước, số viên đá tối thiểu cần tan chảy để có thể làm lạnh
500 gam nước lỏng ở 20 °C xuống 0 °C là x viên. Tính giá trị của x (làm tròn đến hàng đơn vị).
Câu 3: Naftifine là một loại thuốc kháng nấm hoạt động bằng cách ngăn chặn sự phát triển của các
loại nấm nhạy cảm. Naftifine được sử dụng để điều trị một số bệnh nhiễm trùng nấm da như hắc lào,
nấm kẽ chân và ngứa vùng bẹn và đùi trên. Naftifine có công thức cấu tạo như sau: N CH3 Naftifine
Naftifine thường được dùng ở dạng muối naftifine hydrochloride. Để phản ứng vừa đủ với 71,75
gam naftifine cần x mol HCl. Giá trị của x là?
Câu 4: Trong quá trình bảo quản, một mẫu muối FeSO4.7H2O (có khối lượng m gam) bị oxi hóa bởi
oxygen không khí tạo thành hỗn hợp X gồm các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X
trong dung dịch loãng chứa 0,035 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Trang 5/6 - Mã đề thi 0301
Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 20 mL dung dịch Y, thu được 2,33 gam kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 20 mL dung dịch Y, thu được dung dịch Z.
Nhỏ từ từ dung dịch KMnO4 0,03M vào Z đến khi phản ứng vừa đủ thì hết 18 mL.
Phần trăm số mol Fe(II) đã bị oxi hóa trong không khí là a%. Tính giá trị của a.
Câu 5: Ở điều kiện chuẩn, tiến hành các thí nghiệm điện phân (với điện cực trơ) các dung dịch sau:
(1) dung dịch NaCl; (2) dung dịch CuSO4; (3) dung dịch CuCl2; (4) dung dịch KBr; (5) dung dịch
AgNO3. Liệt kê theo số thứ tự tăng dần các thí nghiệm mà nước bị điện phân khi quá trình điện phân bắt đầu.
Câu 6: Acid béo omega-3 và omega-6 là các acid béo không no với liên kết đôi đầu tiên ở vị trí số 3 và
6 khi đánh số từ nhóm methyl. Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ thể,
giúp phòng ngừa nhiều loại bệnh. Linoleic acid có công thức cấu tạo như sau:
Linoleic acid thuộc loại acid béo omega-x và có phân tử khối là y. Bộ số xy có giá trị là? ----------- HẾT ----------
Trang 6/6 - Mã đề thi 0301
SỞ GIÁO DỤC VÀ ĐÀO TẠO
THI THỬ TỐT NGHIỆP THPT NĂM 2025 (LẦN 2) TỈNH THÁI NGUYÊN Môn thi: HÓA HỌC. ĐỀ THI CHÍNH THỨC
Thời gian làm bài: 50 phút, không kể thời gian phát đề.
(Đề thi có 6 trang) Mã đề thi 0302
Họ, tên thí sinh: .........................................................................................
Số báo danh: ..............................................................................................
Cho biết nguyên tử khối: H = 1; C = 12; Cl = 35,5; O = 16; S = 32; Al = 27; N = 14; P = 31; Na = 23; Mg = 24;
Ba = 137; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Cd = 112; Pb = 207.
Phần I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Phân lân có tác dụng làm cành lá khỏe, hạt chắc, củ quả to, cần thiết cho cây ở thời kì sinh
trưởng do thúc đẩy các quá trình sinh hóa, trao đổi chất của thực vật. Khi bón phân lân không nên bón cùng với A. phân đạm. B. phân kali. C. vôi bột. D. phân hữu cơ.
Câu 2: Quan sát hình ảnh sau đây:
Thực hiện thí nghiệm, đặt các amino acid trong điện trường, môi trường có pH bằng 6, phát biểu nào sau đây là đúng?
A. Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng cation.
B. Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng phân tử trung hòa.
C. Glutamic acid dịch chuyển về phía cực âm nên glutamic acid tồn tại chủ yếu ở dạng anion.
D. Các amino acid tồn tại chủ yếu ở dạng ion lưỡng cực nên sẽ di chuyển về hai đầu điện cực.
Câu 3: Khi cho thảo dược vào bình, đổ rượu phù hợp rồi đậy kín, đặt ở nơi tối, mát, sau một thời gian
phù hợp thu được rượu thuốc. Bằng cách làm này, dược chất đã hòa tan vào rượu, phương pháp được
sử dụng trong quá trình trên là A. chưng cất. B. kết tinh. C. chiết. D. sắc kí.
Câu 4: Polymer nào sau đây được điều chế bằng phản ứng trùng ngưng?
A. Poly(methyl methacrylate). B. Polyethylene.
C. Poly(phenol formaldehyde).
D. Poly(vinyl chloride).
Câu 5: Nước cứng là loại nước có chứa hàm lượng các khoáng chất hòa tan dưới dạng các ion, chủ
yếu là cation Ca2+ và Mg2+ cao vượt quá mức cho phép (trên 300 mg/L). Nước cứng có nhiều tác hại
khi dùng lâu dài như: viêm da, khô tóc, quần áo bị xơ cứng, mau mục,…Có nhiều biện pháp để làm
mềm nước cứng, một trong những biện pháp đó là sử dụng các hóa chất. Chất nào sau đây có thể được
dùng để làm mềm nước cứng vĩnh cửu? A. Ca(OH)2. B. Na2CO3. C. Na2SO4. D. HCl.
Câu 6: Ở điều kiện thường, amine nào sau đây là chất khí, có mùi khai và tan nhiều trong nước? A. Propylamine. B. Aniline. C. Ethylamine. D. Diethylamine.
Câu 7: Cho dãy các kim loại: Cu, Al, Ag, Fe. Kim loại dẫn điện tốt nhất trong dãy là A. Al. B. Cu. C. Fe. D. Ag.
Câu 8: Hợp chất hữu cơ nào sau đây thuộc loại ester? A. CH3CHO. B. CH3COOH. C. C2H5OH. D. CH3COOCH3.
Trang 1/6 - Mã đề thi 0302
Câu 9: Xét các phát biểu sau về những khí thải trong đám cháy nhựa và cao su:
a) Khí CO và HCl là những khí độc phổ biến trong đám cháy nhựa PVC.
b) Khí SO2 là sản phẩm chủ yếu của đám cháy nhựa polyethylene.
c) Khói từ đám cháy cao su thiên nhiên thường chứa nhiều chất độc hơn đám cháy nhựa PVC.
d) Việc cúi thấp người giúp tránh hít phải phần lớn khói độc trong đám cháy. Các phát biểu đúng là A. a), c), d). B. a), d). C. a), b). D. b), c), d).
Câu 10: Cho thế điện cực chuẩn của các cặp oxi hóa – khử sau: o E o − E 2+ = +1,51 V và + = +0,77 V. MnO / Mn 3+ 2 4 Fe /Fe
Phát biểu nào sau đây sai? A. Ion MnO -
4 có thể oxi hóa ion Fe2+ trong dung dịch thành ion Fe3+.
B. Ion Fe2+ có thể khử ion MnO -
4 trong dung dịch thành ion Mn2+.
C. Ion Fe2+ có tính khử yếu hơn ion Mn2+. D. Ion MnO -
4 có tính oxi hóa mạnh hơn ion Fe3+.
Câu 11: Dãy gồm các kim loại được xếp theo thứ tự nhiệt độ nóng chảy giảm dần từ trái sang phải là A. K, Na, Li. B. Li, K, Na. C. Li, Na, K. D. K, Li, Na.
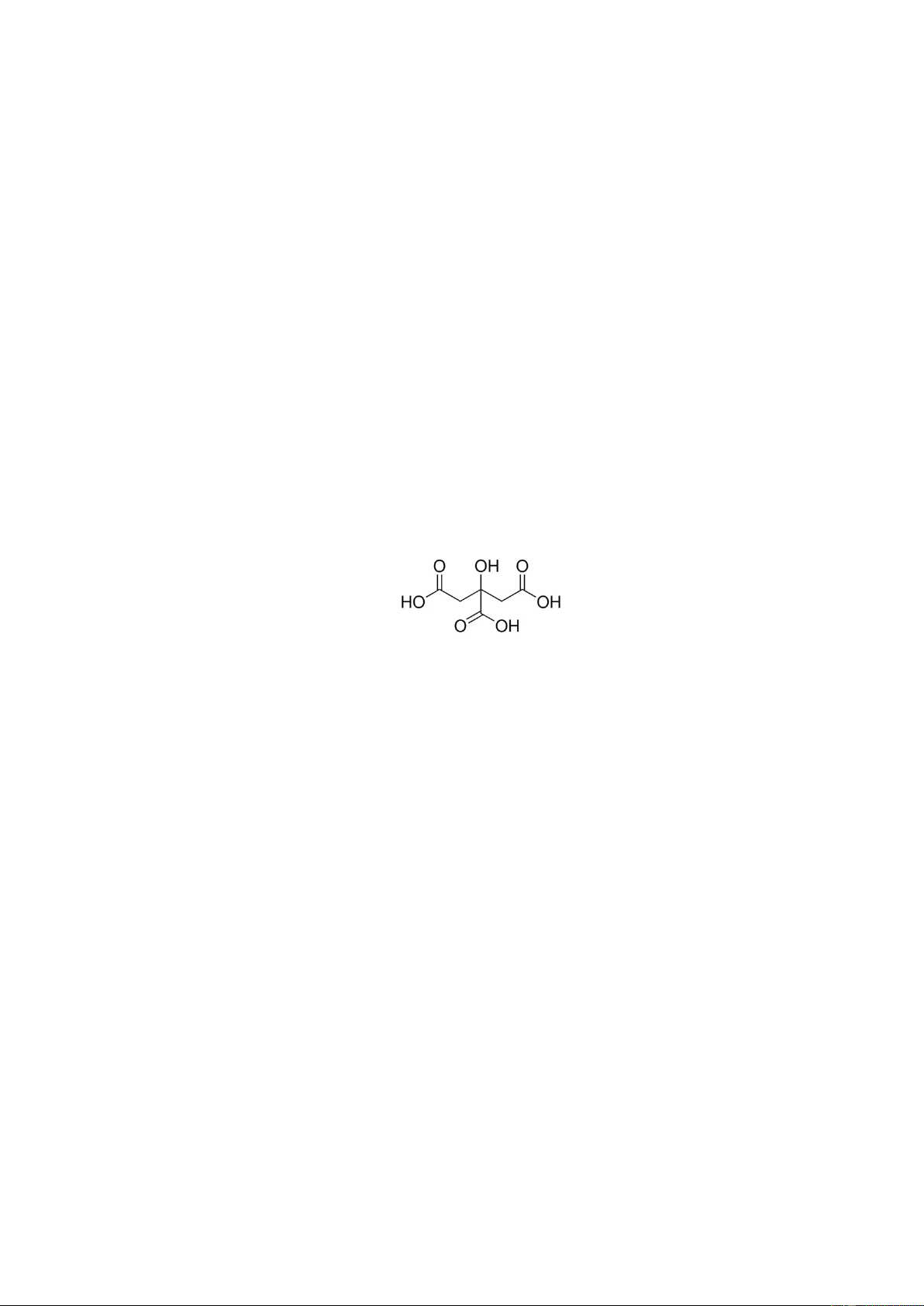
Câu 12: Citric acid là thành phần được tìm thấy trong quả chanh, có vị chua nhẹ và được sử dụng rộng
rãi trong thực phẩm, dược phẩm và công nghiệp. Citric acid có công thức cấu tạo như sau:
Công thức phân tử của citric acid là A. C6H8O7. B. C7H8O6. C. C7H10O7. D. C6H6O6.
Câu 13: Cho cấu hình electron nguyên tử của các nguyên tố sau: X: 1s22s22p6; Y: 1s22s22p63s2; Z: 1s22s22p3; T: 1s22s22p63s23p3.
Nhận xét nào sau đây đúng?
A. Y và Z đều là kim loại.
B. Chỉ có Z là phi kim.
C. X là khí hiếm, T là kim loại.
D. Chỉ có Y là kim loại.
Câu 14: Insulin là hocmon thuộc loại protein, được sinh ra bởi tuyến tụy, có chức năng điều hòa quá
trình chuyển hóa glucose trong cơ thể. Thủy phân một phần insulin thu được heptapeptide X. Khi thủy
phân không hoàn toàn X, thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu,
Val-Glu-Ala, His-Leu-Val, Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là 1, thì amino acid ở
vị trí số 4 trong X có kí hiệu là A. His. B. Leu. C. Val. D. Glu.
Câu 15: Chất nào sau đây được sử dụng làm thành phần chính của xà phòng? A. C2H5OK.
B. CH3[CH2]16COONa. C. CH3COONa. D. CH3[CH2]14COOH.
Câu 16: Phát biểu nào sau đây về carbohydrate là đúng?
A. Tinh bột và cellulose thuộc nhóm polysaccharide.
B. Saccharose được cấu tạo từ hai đơn vị α-glucose.
C. Glucose và fructose có công thức chung là C6H10O5.
D. Maltose là chất lỏng, có vị ngọt và dễ tan trong nước.
Trang 2/6 - Mã đề thi 0302
Câu 17: Một học sinh tiến hành thí nghiệm, sử dụng các thanh zinc (Zn),
thanh copper (Cu), dây dẫn, đèn LED và quả chanh để lắp ráp pin chanh như hình vẽ bên: Cho o E = -0,76 V. 2+ Zn /Zn o E = 0,34 V. 2+ Cu /Cu
Sau khi tiến hành thí nghiệm, học sinh đã viết báo cáo thực hành, nội
dung nào sau đây trong báo cáo không đúng? A. Do o E < o E
nên pin chanh tạo thành có Zn là cực dương, Cu là cực âm. 2+ Zn /Zn 2+ Cu /Cu
B. Ở điện cực dương xảy ra quá trình khử ion H+ (nước chanh): 2H+ + 2e H2.
C. Bóng đèn LED sáng yếu chứng tỏ có dòng điện chạy qua.
D. Sức điện động chuẩn của pin chanh trong thí nghiệm gần bằng 1,1 V.
Câu 18: Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
A. Nhúng thanh Zn vào dung dịch CuSO4.
B. Nhúng thanh Fe vào dung dịch CuSO4 và H2SO4 loãng.
C. Nhúng thanh Cu vào dung dịch Fe2(SO4)3.
D. Nhúng thanh Cu vào dung dịch AgNO3.
Phần II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Ethanol không chỉ dùng làm chất sát khuẩn trong y tế mà còn là thành phần của đồ uống có
cồn, nhiên liệu sinh học (xăng E5). Nó dễ bay hơi, có khả năng hòa tan nhiều hợp chất hữu cơ, được
ứng dụng trong công nghiệp mỹ phẩm và dược phẩm.
Cho biết số sóng hấp thụ đặc trưng trên phổ hồng ngoại của một số nhóm chức cơ bản như sau: Liên kết Loại hợp Liên kết Loại hợp chất Số sóng (cm-1) Số sóng (cm-1) hấp thụ chất hấp thụ C=O 1740 – 1685 Alcohol O-H 3500 - 3200 Aldehyde C-H 2850 - 2695 C=O 1750 - 1715 Ester C=O 1760 - 1690 C-O 1300 - 1000 Carboxylic acid O-H 3300 - 2500 Ketone C=O 1715 – 1666 Amine N-H 3300 - 3000
Mỗi phát biểu dưới đây là đúng hay sai?
a) Ethanol có 8 liên kết σ và không có liên kết π.
b) Phổ IR của ethanol có peak ~3300 cm-1 và ~1700 cm-1.
c) Cồn 700 sát khuẩn tốt hơn cồn 900 do khả năng thẩm thấu sâu vào tế bào vi khuẩn.
d) Ethanol nguyên chất được dùng sản xuất xăng E5 nhằm giảm phát thải CO2.
Câu 2: Mẻ là một loại gia vị truyền thống tạo nên hương vị đặc trưng cho nhiều món ăn của ẩm thực
Việt Nam. Người ta thường làm mẻ bằng cách lên men bún hoặc cơm nát để nguội. Quá trình lên men
diễn ra nhờ vi khuẩn kỵ khí, biến tinh bột và đường thành lactic acid. Chính acid này đã tạo nên vị
chua của mẻ, sữa chua… Quá trình lên men thành lactic acid xảy ra các phản ứng hóa học sau: enzyme (C ⎯⎯⎯→ 6H10O5)n + nH2O nC6H12O6 enzyme C ⎯⎯⎯→ 6H12O6 2CH3CH(OH)COOH
Một học sinh tiến hành thử nghiệm làm ba lọ mẻ theo các cách sau:
Trang 3/6 - Mã đề thi 0302
- Lọ 1: Cho 200 gam bún vào lọ thủy tinh sạch có sẵn 100 mL nước cơm (là phần nước được chắt ra
khi cơm đã sôi), rồi đậy kín.
- Lọ 2: Cho 200 gam bún vào lọ thủy tinh sạch có sẵn 80 mL nước đường maltose 10%, rồi đậy kín.
- Lọ 3: Cho 200 gam bún vào lọ thủy tinh sạch có sẵn khoảng 30 gam mẻ, rồi đậy kín.
Giả sử các điều kiện thực hiện phản ứng lên men đều giống nhau.
a) Thời gian thu được mẻ ngắn nhất là lọ 2.
b) Maltose (lọ 2) là disaccharide nên lên men chậm hơn glucose.
c) Bún và cơm đều cung cấp glycogen cho vi khuẩn lactic.
d) Lactic acid tạo thành là một hợp chất hữu cơ đa chức.
Câu 3: Hoà tan 0,250 gam mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả
lượng sắt có trong quặng đều chuyển thành Fe2+, thu được dung dịch X. Chuẩn độ Fe2+ trong dung dịch
X ba lần bằng chất chuẩn là dung dịch thuốc tím KMnO4 0,020M. Kết quả: Lần chuẩn độ Lần 1 Lần 2 Lần 3
V dung dịch KMnO4 đã dùng (mL) 12,50 12,45 12,55
Mỗi phát biểu dưới đây là đúng hay sai?
a) Nếu chỉ có Fe2+ trong dung dịch X tác dụng được với thuốc tím thì việc chuẩn độ dung dịch X sẽ
giúp xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được % (theo khối lượng)
của nguyên tố sắt có trong mẫu khoáng vật là 26,28%.
b) Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch thuốc tím từ burette vào bình tam giác chứa dung dịch X.
c) Cần thêm vài giọt HNO₃ vào dung dịch X để đảm bảo toàn bộ Fe chuyển thành Fe²⁺.
d) Trong nước thải công nghiệp chứa hỗn hợp nhiều ion như Fe2+, Cl-, Fe3+, NH + 4 , chất hữu
cơ,…Nên sử dụng phương pháp chuẩn độ KMnO4 để xác định hàm lượng Fe2+.
Câu 4: Cho sơ đồ 1 biểu diễn sự điện phân dung dịch CuSO4(aq) với điện cực trơ, sơ đồ 2 biểu diễn
quá trình tinh luyện đồng (Cu) bằng phương pháp điện phân. Trong sơ đồ 2, các khối đồng có độ tinh
khiết thấp được gắn với một điện cực của nguồn điện, các thanh đồng mỏng có độ tinh khiết cao được
gắn với một điện cực của nguồn điện. Dung dịch điện phân trong cả hai sơ đồ là dung dịch CuSO4.
a) Khi điện phân xảy ra ở sơ đồ 1, nồng độ ion Cu2+ trong dung dịch sẽ giảm dần theo thời gian.
b) Khi điện phân xảy ra ở sơ đồ 1, thì ban đầu ở cực âm xảy ra quá trình khử ion Cu2+ và ở cực
dương xảy ra quá trình oxi hóa SO 2- 4 .
c) Trong cả sơ đồ 1 và 2, đều xảy ra quá trình khử ion Cu2+ tại cathode.
d) Muốn tinh luyện Cu như sơ đồ 2 thì khối Cu không tinh khiết phải được nối vào cathode, còn
thanh Cu tinh khiết được nối vào anode, khi đó khối lượng Cu tan ra từ cathode bằng khối lượng Cu bám vào anode.
Trang 4/6 - Mã đề thi 0302
Phần III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1: Ở điều kiện chuẩn, tiến hành các thí nghiệm điện phân (với điện cực trơ) các dung dịch sau:
(1) dung dịch KCl; (2) dung dịch FeCl3; (3) dung dịch ZnSO4; (4) dung dịch NaF; (5) dung dịch
Cu(NO3)2. Liệt kê theo số thứ tự tăng dần các thí nghiệm mà nước bị điện phân khi quá trình điện phân bắt đầu.
Câu 2: Maltose là thành phần chính của đường mạch nha. Trong dung dịch nước, maltose tồn tại chủ
yếu ở hai dạng cấu tạo (I) và (II). Các dạng này tồn tại trong cân bằng sau:
Maltose thủy phân trong môi trường acid hoặc enzyme tạo thành glucose. Cho các phát biểu sau:
1) Dạng (I) và dạng (II) có số liên kết sigma bằng nhau.
2) Enzyme maltase xúc tác đặc hiệu cho phản ứng thủy phân maltose.
3) Liên kết giữa hai đơn vị monosaccharide trong phân tử maltose là liên kết α-1,4-glycoside.
4) Dạng (I) có một nhóm –OH hemiacetal.
5) Phản ứng thủy phân maltose trong dung dịch H2SO4 98% xảy ra nhanh hơn trong dung dịch
H2SO4 50% vì nồng độ acid lớn hơn.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.
Câu 3: Biến thiên enthalpy chuẩn của quá trình “H2O(s) ⟶ H2O(l)” là 6,020 kJ.
Biết rằng để làm cho nhiệt độ của 1 mol nước lỏng thay đổi 1 °C cần một nhiệt lượng là 75,4 J. Giả
sử mỗi viên nước đá tương ứng với 1 mol nước, số viên đá tối thiểu cần tan chảy để có thể làm lạnh
460 gam nước lỏng ở 25 °C xuống 0 °C là x viên. Tính giá trị của x (làm tròn đến hàng đơn vị).
Câu 4: Trong quá trình bảo quản, một mẫu muối FeSO4.7H2O (có khối lượng m gam) bị oxi hóa bởi
oxygen không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X
trong dung dịch loãng chứa 0,02 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 25 mL dung dịch Y, thu được 2,33 gam kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 25 mL dung dịch Y, thu được dung dịch Z.
Nhỏ từ từ dung dịch KMnO4 0,04 M vào Z đến khi phản ứng vừa đủ thì hết 22 mL.
Phần trăm số mol Fe(II) đã bị oxi hóa trong không khí là a%. Tính giá trị của a.
Câu 5: Ephedrine được sử dụng với hàm lượng nhất định trong các loại thuốc điều trị cảm và dị ứng.
Ephedrine có mùi tanh và dễ bị oxi hoá trong không khí, do đó người ta thường hạn chế sử dụng trực
tiếp. Ephedrine có công thức cấu tạo như sau: OH NH Ephedrine
Ephedrine hydrochloride khó bị oxi hoá, không mùi và vẫn giữ được hoạt tính của hợp chất.
Ephedrine hydrochloride được điều chế từ phản ứng của ephedrine với hydrochloric acid. Để phản ứng
vừa đủ với 19,8 gam ephedrine cần x mol HCl. Giá trị của x là?
Trang 5/6 - Mã đề thi 0302
Câu 6: Acid béo omega-3 và omega-6 là các acid béo không no với liên kết đôi đầu tiên ở vị trí số 3 và
6 khi đánh số từ nhóm methyl. Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ thể,
giúp phòng ngừa nhiều loại bệnh. Linolenic acid có công thức cấu tạo như sau:
Linolenic acid thuộc loại acid béo omega-x và có phân tử khối là y. Bộ số xy có giá trị là ----------- HẾT ----------
Trang 6/6 - Mã đề thi 0302
SỞ GIÁO DỤC VÀ ĐÀO TẠO
THI THỬ TỐT NGHIỆP THPT NĂM 2025 (LẦN 2) TỈNH THÁI NGUYÊN Môn thi: HÓA HỌC. ĐỀ THI CHÍNH THỨC
Thời gian làm bài: 50 phút, không kể thời gian phát đề.
(Đề thi có 6 trang) Mã đề thi 0303
Họ, tên thí sinh: .........................................................................................
Số báo danh: ..............................................................................................
Cho biết nguyên tử khối: H = 1; C = 12; Cl = 35,5; O = 16; S = 32; Al = 27; N = 14; P = 31; Na = 23; Mg = 24;
Ba = 137; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Cd = 112; Pb = 207.
Phần I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Ở điều kiện thường, amine nào sau đây là chất khí, có mùi khai và tan nhiều trong nước? A. Dimethylamine. B. Propylamine. C. Diethylamine. D. Aniline.
Câu 2: Cho thế điện cực chuẩn của các cặp oxi hóa – khử sau: o E o − E 2+ = +1,51 V và + = +0,77 V. MnO / Mn 3+ 2 4 Fe /Fe
Phát biểu nào sau đây sai? A. Ion MnO -
4 có tính oxi hóa yếu hơn ion Fe3+.
B. Ion Fe2+ có tính khử mạnh hơn ion Mn2+. C. Ion MnO -
4 có thể oxi hóa ion Fe2+ trong dung dịch thành ion Fe3+.
D. Ion Fe2+ có thể khử ion MnO -
4 trong dung dịch thành ion Mn2+.
Câu 3: Cho cấu hình electron nguyên tử của các nguyên tố sau: X: 1s22s22p6; Y: 1s22s22p63s1; Z: 1s22s22p4; T: 1s22s22p63s23p5.
Nhận xét nào sau đây đúng?
A. Y và Z đều là kim loại.
B. X là khí hiếm, Z là kim loại.
C. Z và T là phi kim.
D. Chỉ có T là phi kim.
Câu 4: Một học sinh tiến hành thí nghiệm, sử dụng các thanh zinc (Zn),
thanh copper (Cu), dây dẫn, đèn LED và quả chanh để lắp ráp pin chanh như hình vẽ bên: Cho o E = -0,76 V. 2+ Zn /Zn o E = 0,34 V. 2+ Cu /Cu
Sau khi tiến hành thí nghiệm, học sinh đã viết báo cáo thực hành, nội
dung nào sau đây trong báo cáo không đúng?
A. Ở điện cực dương xảy ra quá trình khử ion H+ (nước chanh): 2H+ + 2e H2.
B. Sức điện động chuẩn của pin chanh trong thí nghiệm gần bằng 1,1 V. C. Do o E < o E
nên pin chanh tạo thành có Zn là cực âm, Cu là cực dương. 2+ Zn /Zn 2+ Cu /Cu
D. Ở điện cực âm xảy ra quá trình oxi hóa: Cu Cu2+ + 2e.
Câu 5: Cho dãy các kim loại: Al, Li, Fe, Cr. Kim loại trong dãy có khối lượng riêng nhỏ nhất là A. Al. B. Cr. C. Fe. D. Li.
Câu 6: Insulin là hocmon thuộc loại protein, được sinh ra bởi tuyến tụy, có chức năng điều hòa quá
trình chuyển hóa glucose trong cơ thể. Thủy phân một phần insulin thu được heptapeptide X. Khi thủy
phân không hoàn toàn X, thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu,
Val-Glu-Ala, His-Leu-Val, Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là 1, thì amino acid ở
vị trí số 5 trong X có kí hiệu là A. His. B. Leu. C. Val. D. Glu.
Trang 1/6 - Mã đề thi 0303
Câu 7: Chất nào sau đây có tính năng giặt rửa? A. CH3[CH2]16COOH.
B. CH3[CH2]14COONa. C. CH3COOK. D. C2H5ONa.
Câu 8: Cho hỗn hợp các alkane có mạch carbon thẳng sau: pentane (sôi ở 36oC), heptane (sôi ở 98oC),
octane (sôi ở 126oC) và nonane (sôi ở 151oC). Có thể tách riêng các chất đó bằng cách nào sau đây? A. Chiết. B. Sắc kí. C. Chưng cất. D. Kết tinh.
Câu 9: Phân đạm có tác dụng kích thích sự sinh trưởng của cây, làm tăng tỉ lệ protein thực vật, giúp
cây phát triển nhanh và cho nhiều hạt, củ, quả. Phát biểu nào sau đây là đúng khi sử dụng phân đạm?
A. Tránh bón đạm urea cùng với vôi bột vì sẽ bị thất thoát đạm.
B. Nên bón đạm nitrate vào ngày trời mưa để cây dễ hấp thu đạm hơn.
C. Không được bón phân đạm cùng với phân kali vì sinh ra thành phần làm chai cứng đất.
D. Nên bón phân đạm ammonium sulfate cho đất có độ pH thấp.
Câu 10: Hợp chất hữu cơ nào sau đây thuộc loại ester? A. C6H5OH. B. HCOOCH3. C. HCHO. D. CH3NH2.
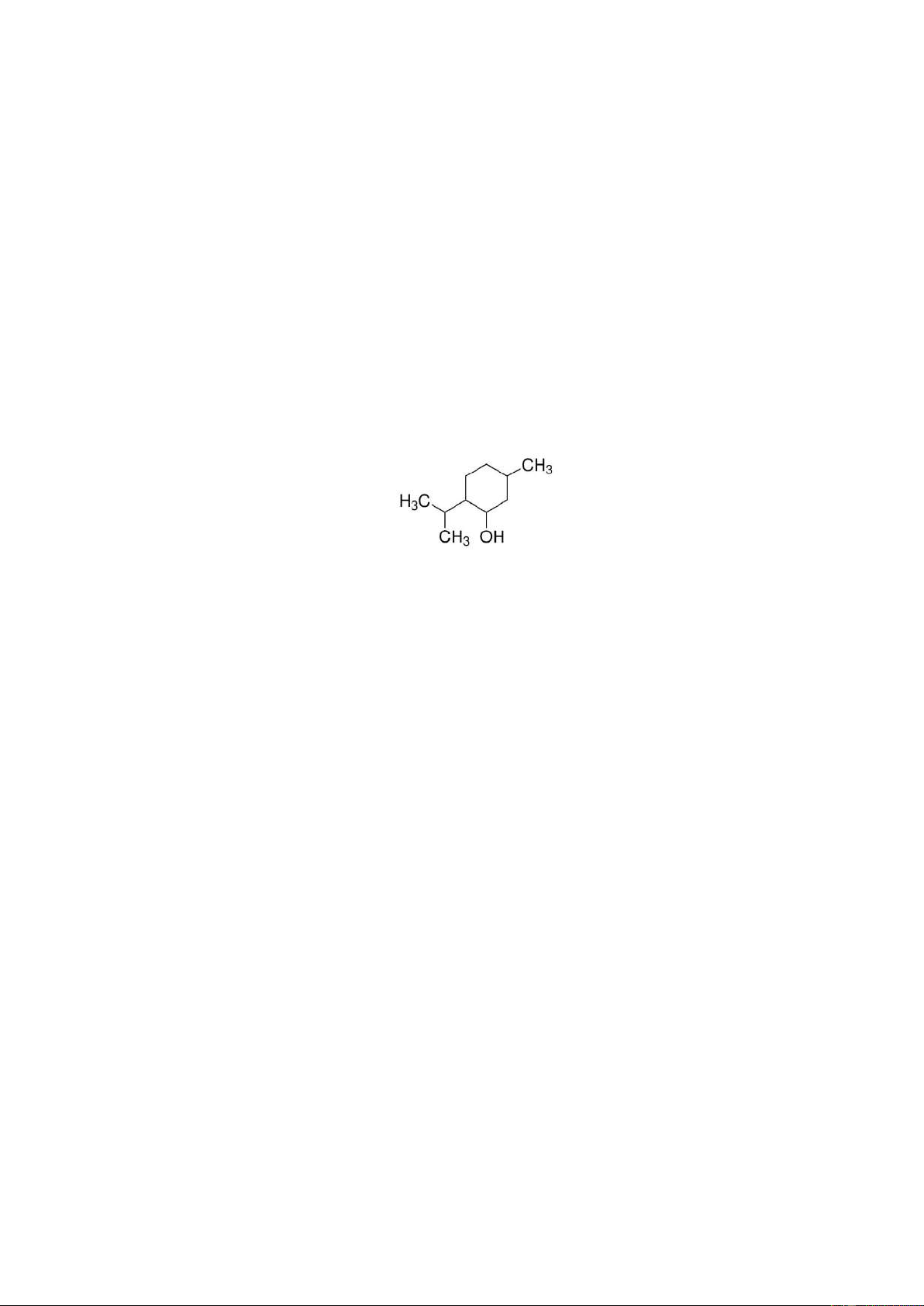
Câu 11: Menthol là một hợp chất hữu cơ có nguồn gốc tự nhiên từ bạc hà, nó có mùi thơm đặc trưng và
mang lại cảm giác mát lạnh khi tiếp xúc với da hoặc niêm mạc. Menthol có công thức cấu tạo như sau:
Công thức phân tử của menthol là A. C9H18O. B. C10H20O. C. C9H16O2. D. C10H18O.
Câu 12: Nước cứng là loại nước có chứa hàm lượng các khoáng chất hòa tan dưới dạng các ion, chủ
yếu là cation Ca2+ và Mg2+ cao vượt quá mức cho phép (trên 300 mg/L). Nước cứng có nhiều tác hại
khi dùng lâu dài như: viêm da, khô tóc, quần áo bị xơ cứng, mau mục,…Có nhiều biện pháp để làm
mềm nước cứng, một trong những biện pháp đó là sử dụng các hóa chất. Chất nào sau đây có thể được
dùng để làm mềm nước cứng tạm thời? A. H2SO4. B. NaCl. C. Ca(OH)2. D. KNO3.
Câu 13: Dãy gồm các kim loại được xếp theo thứ tự nhiệt độ sôi tăng dần từ trái sang phải là A. Li, Na, K. B. Li, K, Na. C. K, Na, Li. D. K, Li, Na.
Câu 14: Cho các phát biểu sau về quá trình cháy của các hợp chất hữu cơ:
a) Khi chất hữu cơ cháy không hoàn toàn, SO2 là sản phẩm chính.
b) CO2 là khí gây ra hiệu ứng nhà kính và là sản phẩm của quá trình cháy hoàn toàn.
c) Khi đốt cháy nhựa PVC, ngoài CO2 còn sinh ra khí độc HCl.
d) Khói từ đám cháy xăng, dầu chứa nhiều thành phần độc hại (CO, SO2, NOx,…). Các phát biểu đúng là A. a), b), d). B. a), b). C. b), c), d). D. a), d).
Câu 15: Thí nghiệm nào sau đây có xảy ra sự ăn mòn điện hóa học?
A. Nhúng thanh Zn vào dung dịch chứa hỗn hợp gồm CuSO4 và H2SO4.
B. Đốt dây Mg trong bình đựng khí O2.
C. Nhúng thanh Fe vào dung dịch HCl.
D. Nhúng thanh Cu vào dung dịch HNO3 loãng.
Câu 16: Polymer nào sau đây được điều chế bằng phản ứng trùng hợp? A. Polysaccharide. B. Cao su buna-S.
C. Poly(phenol formaldehyde). D. Nylon-6,6.
Trang 2/6 - Mã đề thi 0303
Câu 17: Phát biểu nào sau đây về carbohydrate là đúng?
A. Saccharose được cấu tạo từ một đơn vị α-glucose và một đơn vị β-fructose.
B. Maltose là chất lỏng, màu vàng, có nhiều trong cây mía.
C. Tinh bột và cellulose thuộc nhóm monosaccharide.
D. Glucose và fructose có công thức chung là C12H22O11.
Câu 18: Quan sát hình ảnh sau đây:
Thực hiện thí nghiệm, đặt các amino acid trong điện trường, môi trường có pH bằng 6, phát biểu nào sau đây là đúng?
A. Glutamic acid dịch chuyển về phía cực dương nên glutamic acid tồn tại chủ yếu ở dạng anion.
B. Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng phân tử trung hòa.
C. Các amino acid tồn tại chủ yếu ở dạng ion lưỡng cực nên sẽ di chuyển về hai đầu điện cực.
D. Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng anion.
Phần II. Thí sinh trả lời từ câu 1 đến câu 4. Trong mỗi ý a), b), c), d) ở mỗi câu, thí sinh chọn đúng hoặc sai.
Câu 1: Mẻ là một loại gia vị truyền thống tạo nên hương vị đặc trưng cho nhiều món ăn của ẩm thực
Việt Nam. Người ta thường làm mẻ bằng cách lên men bún hoặc cơm nát để nguội. Quá trình lên men
diễn ra nhờ vi khuẩn kỵ khí, biến tinh bột và đường thành lactic acid. Chính acid này đã tạo nên vị
chua của mẻ, sữa chua… Quá trình lên men thành lactic acid xảy ra các phản ứng hóa học sau: enzyme (C ⎯⎯⎯→ 6H10O5)n + nH2O nC6H12O6 enzyme C ⎯⎯⎯→ 6H12O6 2CH3CH(OH)COOH
Một học sinh tiến hành thử nghiệm làm ba lọ mẻ theo các cách sau:
- Lọ 1: Cho 150 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn 150 mL nước vo gạo, rồi đậy kín.
- Lọ 2: Cho 150 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn 50 mL nước đường glucose 10%, rồi đậy kín.
- Lọ 3: Cho 150 gam cơm nát để nguội vào lọ thủy tinh sạch có sẵn khoảng 50 gam mẻ, rồi đậy kín.
Giả sử các điều kiện thực hiện phản ứng lên men đều giống nhau.
a) Cơm nát chứa carbohydrate chủ yếu là cellulose.
b) Lactic acid tạo thành là một hợp chất hữu cơ tạp chức.
c) Glucose (lọ 2) là monosaccharide nên lên men nhanh hơn tinh bột.
d) Thời gian thu được mẻ ngắn nhất là lọ 3.
Câu 2: Acetic acid là hợp chất hữu cơ phổ biến, tạo vị chua đặc trưng cho giấm ăn. Ngoài vai trò
trong ẩm thực, nó còn được dùng để:
- Bảo quản thực phẩm nhờ khả năng ức chế vi khuẩn.
- Tẩy cặn khoáng (CaCO3) trong ấm đun, vòi nước.
- Nguyên liệu tổng hợp dược phẩm (paracetamol), sợi tổng hợp (cellulose acetate).
Cho biết số sóng hấp thụ đặc trưng trên phổ hồng ngoại của một số nhóm chức cơ bản như sau:
Trang 3/6 - Mã đề thi 0303 Liên kết Liên kết Loại hợp chất Số sóng (cm-1) Loại hợp chất Số sóng (cm-1) hấp thụ hấp thụ C=O 1740 – 1685 Alcohol O-H 3500 - 3200 Aldehyde C-H 2850 - 2695 C=O 1750 - 1715 Ester C=O 1760 - 1690 C-O 1300 - 1000 Carboxylic acid O-H 3300 - 2500 Ketone C=O 1715 – 1666 Amine N-H 3300 - 3000
Mỗi phát biểu dưới đây là đúng hay sai?
a) Acetic acid có 1 liên kết π và 6 liên kết σ.
b) Nhóm carboxyl (-COOH) phân ly thành H⁺ trong nước, tạo tính acid mạnh.
c) Giấm ăn pha loãng có thể làm mất mùi khai của ammonia (NH3) do phản ứng tạo ammonium acetate.
d) Phổ IR của acetic acid có peak ~1700 cm⁻¹ và ~3500 cm⁻¹.
Câu 3: Cho sơ đồ 1 biểu diễn sự điện phân dung dịch CuSO4(aq) với điện cực trơ, sơ đồ 2 biểu diễn
quá trình tinh luyện đồng (Cu) bằng phương pháp điện phân. Trong sơ đồ 2, các khối đồng có độ tinh
khiết thấp được gắn với một điện cực của nguồn điện, các thanh đồng mỏng có độ tinh khiết cao được
gắn với một điện cực của nguồn điện. Dung dịch điện phân trong cả hai sơ đồ là dung dịch CuSO4.
a) Quá trình điện phân trong cả hai sơ đồ đều làm pH của dung dịch giảm dần.
b) Trong sơ đồ 2, khối lượng đồng bám vào cathode bằng khối lượng đồng tan từ anode.
c) Trong cả sơ đồ 1 và 2, đều xảy ra quá trình oxi hoá ion Cu2+ tại cathode.
d) Ở sơ đồ 2, thanh đồng tinh khiết được nối với cực dương của nguồn điện.
Câu 4: Hoà tan 0,300 gam mẫu khoáng vật của sắt trong dung dịch sulfuric acid dư, sao cho tất cả
lượng sắt có trong quặng đều chuyển thành Fe2+, thu được dung dịch X. Chuẩn độ Fe2+ trong dung
dịch X ba lần bằng chất chuẩn là dung dịch thuốc tím KMnO4 0,015M. Kết quả: Lần chuẩn độ Lần 1 Lần 2 Lần 3
V dung dịch KMnO4 đã dùng (mL) 16,80 16,75 16,85
Mỗi phát biểu dưới đây là đúng hay sai?
a) Nếu chỉ có Fe2+ trong dung dịch X tác dụng được với thuốc tím thì việc chuẩn độ dung dịch X sẽ
giúp xác định được lượng nguyên tố sắt trong mẫu khoáng vật. Từ đó tính được % (theo khối lượng)
của nguyên tố sắt có trong mẫu khoáng vật là 23,52%.
b) Trong quá trình chuẩn độ trên, cần nhỏ từ từ dung dịch X từ burette vào bình tam giác chứa dung
dịch KMnO4 cho tới khi màu hồng bền trong khoảng 20 giây thì kết thúc chuẩn độ, ghi kết quả.
c) Sai số sẽ tăng nếu không loại bỏ hết O₂ hòa tan trong dung dịch trước khi chuẩn độ.
d) Thể tích KMnO4 dùng tỉ lệ nghịch với nồng độ Fe2+ trong dung dịch X.
Trang 4/6 - Mã đề thi 0303
Phần III. Thí sinh trả lời từ câu 1 đến câu 6.
Câu 1: Naftifine là một loại thuốc kháng nấm hoạt động bằng cách ngăn chặn sự phát triển của các
loại nấm nhạy cảm. Naftifine được sử dụng để điều trị một số bệnh nhiễm trùng nấm da như hắc lào,
nấm kẽ chân và ngứa vùng bẹn và đùi trên. Naftifine có công thức cấu tạo như sau: N CH3 Naftifine
Naftifine thường được dùng ở dạng muối naftifine hydrochloride. Để phản ứng vừa đủ với 45,92
gam naftifine cần x mol HCl. Giá trị của x là?
Câu 2: Acid béo omega-3 và omega-6 là các acid béo không no với liên kết đôi đầu tiên ở vị trí số 3
và 6 khi đánh số từ nhóm methyl. Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ
thể, giúp phòng ngừa nhiều loại bệnh. Arachidonic acid có công thức cấu tạo như sau:
Arachidonic acid thuộc loại acid béo omega-x và có phân tử khối là y. Bộ số xy có giá trị là?
Câu 3: Biến thiên enthalpy chuẩn của quá trình “H2O(s) ⟶ H2O(l)” là 6,020 kJ.
Biết rằng để làm cho nhiệt độ của 1 mol nước lỏng thay đổi 1 °C cần một nhiệt lượng là 75,4 J. Giả
sử mỗi viên nước đá tương ứng với 1 mol nước, số viên đá tối thiểu cần tan chảy để có thể làm lạnh
647 gam nước lỏng ở 20 °C xuống 0 °C là x viên. Tính giá trị của x (làm tròn đến hàng đơn vị).
Câu 4: Ở điều kiện chuẩn, tiến hành các thí nghiệm điện phân (với điện cực trơ) các dung dịch sau:
(1) dung dịch CuCl2; (2) dung dịch H2SO4; (3) dung dịch NaOH; (4) dung dịch AgNO3; (5) dung dịch
FeCl2. Liệt kê theo số thứ tự tăng dần các thí nghiệm mà nước bị điện phân khi quá trình điện phân bắt đầu.
Câu 5: Maltose là thành phần chính của đường mạch nha. Trong dung dịch nước, maltose tồn tại chủ
yếu ở hai dạng cấu tạo (I) và (II). Các dạng này tồn tại trong cân bằng sau:
Maltose thủy phân trong môi trường acid hoặc enzyme tạo thành glucose. Cho các phát biểu sau:
1) Dạng (I) có một nhóm –OH hemiacetal.
2) Dạng (I) có nhiều liên kết sigma hơn dạng (II).
3) Liên kết giữa hai đơn vị monosaccharide trong phân tử maltose là liên kết β-1,4-glycoside.
4) Enzyme maltase xúc tác đặc hiệu cho phản ứng thủy phân maltose.
5) Phản ứng thủy phân maltose trong dung dịch H2SO4 98% xảy ra nhanh hơn trong dung dịch
H2SO4 50% vì nồng độ acid lớn hơn.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.
Trang 5/6 - Mã đề thi 0303
Câu 6: Trong quá trình bảo quản, một mẫu muối FeSO4.7H2O (có khối lượng m gam) bị oxi hóa bởi
oxygen không khí tạo thành hỗn hợp X chứa các hợp chất của Fe(II) và Fe(III). Hòa tan toàn bộ X
trong dung dịch loãng chứa 0,025 mol H2SO4, thu được 100 mL dung dịch Y. Tiến hành hai thí nghiệm với Y:
Thí nghiệm 1: Cho lượng dư dung dịch BaCl2 vào 20 mL dung dịch Y, thu được 2,33 gam kết tủa.
Thí nghiệm 2: Thêm dung dịch H2SO4 (loãng, dư) vào 20 mL dung dịch Y, thu được dung dịch Z.
Nhỏ từ từ dung dịch KMnO4 0,1M vào Z đến khi phản ứng vừa đủ thì hết 8,6 mL.
Phần trăm số mol Fe(II) đã bị oxi hóa trong không khí là a%. Tính giá trị của a. ----------- HẾT ----------
Trang 6/6 - Mã đề thi 0303
SỞ GIÁO DỤC VÀ ĐÀO TẠO
THI THỬ TỐT NGHIỆP THPT NĂM 2025 (LẦN 2) TỈNH THÁI NGUYÊN Môn thi: HÓA HỌC. ĐỀ THI CHÍNH THỨC
Thời gian làm bài: 50 phút, không kể thời gian phát đề.
(Đề thi có 6 trang) Mã đề thi 0304
Họ, tên thí sinh: .........................................................................................
Số báo danh: ..............................................................................................
Cho biết nguyên tử khối: H = 1; C = 12; Cl = 35,5; O = 16; S = 32; Al = 27; N = 14; P = 31; Na = 23; Mg = 24;
Ba = 137; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Cd = 112; Pb = 207.
Phần I. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Câu 1: Cho dãy các kim loại: Na, Al, W, Fe. Kim loại trong dãy có nhiệt độ nóng chảy cao nhất là A. Fe. B. W. C. Al. D. Na.
Câu 2: Ở điều kiện thường, amine nào sau đây là chất khí, có mùi tanh và tan nhiều trong nước? A. Diethylamine. B. Trimethylamine. C. Propylamine. D. Aniline.
Câu 3: Insulin là hocmon thuộc loại protein, được sinh ra bởi tuyến tụy, có chức năng điều hòa quá
trình chuyển hóa glucose trong cơ thể. Thủy phân một phần insulin thu được heptapeptide X. Khi thủy
phân không hoàn toàn X, thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu,
Val-Glu-Ala, His-Leu-Val, Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là 1, thì amino acid ở
vị trí số 6 trong X có kí hiệu là A. His. B. Leu. C. Val. D. Glu.
Câu 4: Xét các phát biểu sau về những khí thải trong đám cháy xăng, dầu và nhựa:
a) Khí CO và HCl là những khí độc phổ biến trong đám cháy nhựa PE.
b) SO2 có thể sinh ra từ các đám cháy có chứa nhựa PS.
c) Khói từ đám cháy xăng, dầu chứa nhiều thành phần độc hại (CO, SO2, NOx,…).
d) Đốt cháy rác thải nhựa sẽ gây ảnh hưởng nghiêm trọng tới môi trường và sức khỏe con người. Các phát biểu đúng là A. b), c), d). B. a), b), d). C. a), b). D. c), d).
Câu 5: Nước cứng là loại nước có chứa hàm lượng các khoáng chất hòa tan dưới dạng các ion, chủ
yếu là cation Ca2+ và Mg2+ cao vượt quá mức cho phép (trên 300 mg/L). Nước cứng có nhiều tác hại
khi dùng lâu dài như: viêm da, khô tóc, quần áo bị xơ cứng, mau mục,…Có nhiều biện pháp để làm
mềm nước cứng, một trong những biện pháp đó là sử dụng các hóa chất. Chất nào sau đây có thể được
dùng để làm mềm nước cứng vĩnh cửu? A. H2SO4. B. NaCl. C. KNO3. D. Na2CO3.
Câu 6: Thí nghiệm nào sau đây có xảy ra ăn mòn điện hóa học?
A. Nhúng thanh Cu vào dung dịch Fe2(SO4)3.
B. Nhúng thanh Fe vào dung dịch CuCl2.
C. Nhúng dây Mg vào dung dịch HCl.
D. Đốt dây thép trong bình đựng khí Cl2.
Câu 7: Một học sinh tiến hành thí nghiệm, sử dụng các thanh zinc (Zn),
thanh copper (Cu), dây dẫn, đèn LED và quả chanh để lắp ráp pin chanh như hình vẽ bên: Cho o E = -0,76 V. 2+ Zn /Zn o E = 0,34 V. 2+ Cu /Cu
Sau khi tiến hành thí nghiệm, học sinh đã viết báo cáo thực hành, nội dung
nào sau đây trong báo cáo không đúng?
Trang 1/6 - Mã đề thi 0304 A. Do o E < o E
nên pin chanh tạo thành có Zn là cực âm, Cu là cực dương. 2+ Zn /Zn 2+ Cu /Cu
B. Ở điện cực dương xảy ra quá trình khử ion H+ (nước chanh): 2H+ + 2e H2.
C. Ở điện cực âm xảy ra quá trình oxi hóa: Zn Zn2+ + 2e.
D. Sức điện động chuẩn của pin chanh trong thí nghiệm bằng 1,2 V.
Câu 8: Chất nào sau đây có tính năng giặt rửa?
A. CH3[CH2]16COONa. B. CH3COONa. C. CH3[CH2]14COOH. D. C2H5OK.
Câu 9: Phát biểu nào sau đây về carbohydrate là đúng?
A. Glucose ở dạng mạch hở có năm nhóm hydroxy và một nhóm ketone.
B. Tinh bột và cellulose là đồng phân của nhau có công thức chung là Cn(H2O)m.
C. Saccharose là chất rắn, có nhiều trong cây mía và củ cải đường.
D. Maltose được cấu tạo từ một đơn vị α-glucose và một đơn vị β-fructose.
Câu 10: Polymer nào sau đây được điều chế bằng phản ứng trùng hợp?
A. Poly(phenol formaldehyde). B. Cao su buna-N. C. Polysaccharide. D. Nylon-6,6.
Câu 11: Cinnamaldehyde là hợp chất hữu cơ trong tinh dầu vỏ quế, có tác dụng chống oxy hóa, kháng
khuẩn, kháng viêm và giúp tăng cường miễn dịch. Cinnamaldehyde có công thức cấu tạo như sau:
Công thức phân tử của cinnamaldehyde là A. C8H10O. B. C9H12O. C. C10H10O. D. C9H8O.
Câu 12: Để tách riêng từng chất rắn từ hỗn hợp các chất rắn dựa vào độ tan khác nhau và sự thay đổi
độ tan của chúng theo nhiệt độ, phương pháp nào sau đây được dùng? A. Chiết. B. Kết tinh. C. Sắc kí cột. D. Chưng cất.
Câu 13: Quan sát hình ảnh sau đây:
Thực hiện thí nghiệm, đặt các amino acid trong điện trường, môi trường có pH bằng 6, phát biểu nào sau đây là đúng?
A. Lysine dịch chuyển về phía cực âm nên lysine tồn tại chủ yếu ở dạng anion.
B. Glutamic acid dịch chuyển về phía cực dương nên glutamic acid tồn tại chủ yếu ở dạng cation.
C. Theo pH của môi trường, các amino acid có khả năng di chuyển khác nhau trong điện trường.
D. Glycine hầu như không dịch chuyển nên glycine tồn tại chủ yếu ở dạng phân tử trung hòa.
Câu 14: Hợp chất hữu cơ nào sau đây thuộc loại ester? A. HCOOC2H5. B. CH3OCH3. C. CH3NHCH3. D. HCOOH.
Câu 15: Phân đạm có tác dụng kích thích sự sinh trưởng của cây, làm tăng tỉ lệ protein thực vật, giúp
cây phát triển nhanh và cho nhiều hạt, củ, quả. Lưu ý nào sau đây không đúng khi sử dụng phân đạm?
A. Không nên bón phân đạm ammonium sulfate cho đất cho độ pH thấp.
B. Không nên bón đạm nitrate vào ngày trời mưa để tránh bị rửa trôi.
C. Tránh bón đạm urea cùng với vôi bột vì sẽ bị thất thoát đạm.
D. Không được bón phân đạm cùng với phân kali vì sinh ra thành phần làm chai cứng đất.
Trang 2/6 - Mã đề thi 0304




