
Preview text:
BÀI 2: ĐỊNH TỈNH CÁC KHÁNG SINH PENICILLIN VÀ
KIỂM ĐỊNH KHÁNG SINH CLORAMPHENICOL
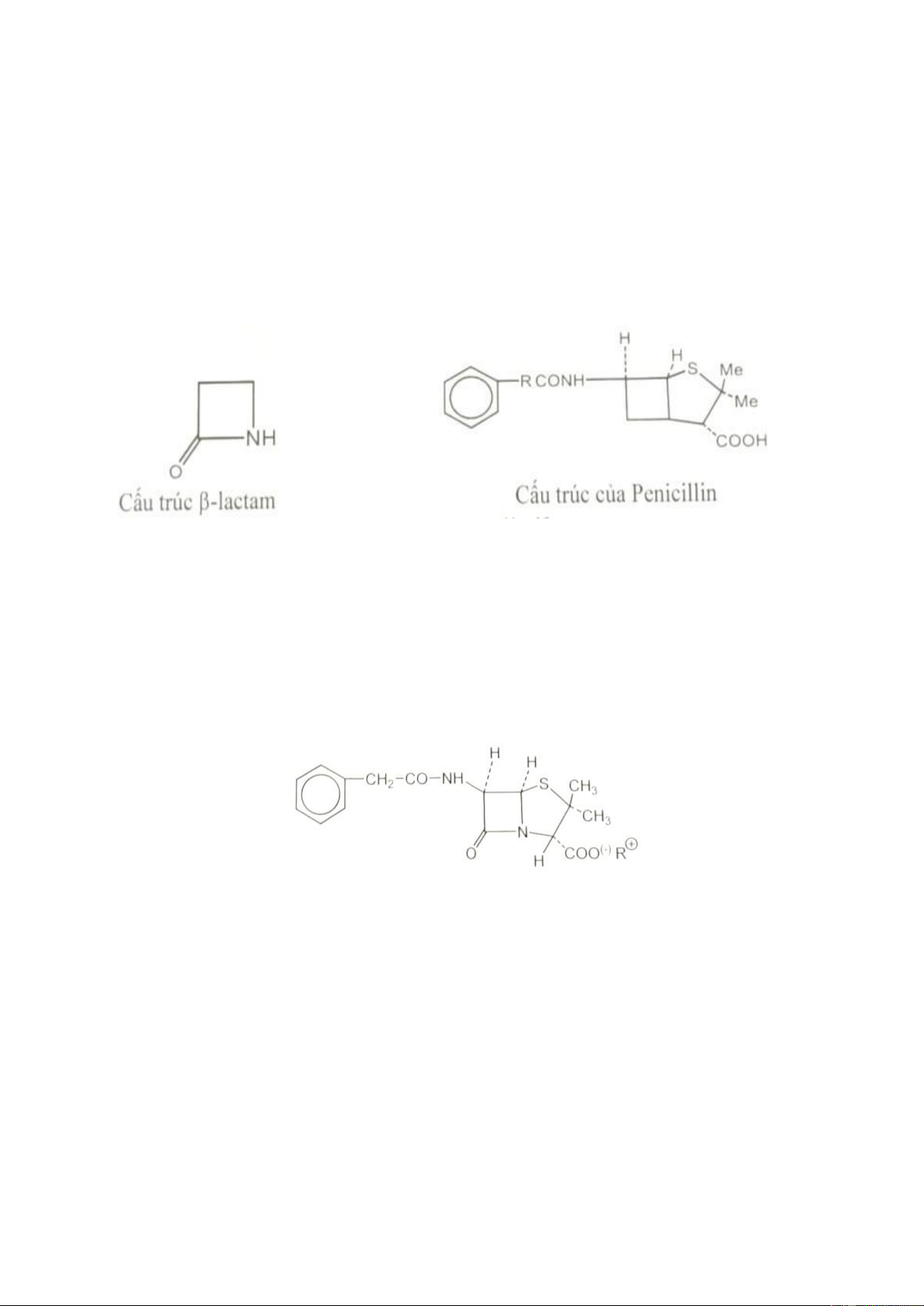
1. Tại sao penicillin là kháng sinh học β-lactam (giải thích rõ lactam là gì và
tại sao phải ở vị trí β) ?
- Lactam là amid nội vòng. Vòng -lactam = azetidin – 2 – on, vòng lactam đóng ở
vị trí ở phản ứng trùng ngưng.
- Penicillin là kháng sinh họ B-lactam vì trong cấu trúc có vòng β-lactam gắn vào vị trí β
2. Cơ chế tác động của kháng sinh họ β-lactam là gì?
- Ức chế hoạt động của các transpeptidase (PBP), enzyme tham gia vào quá trình
tăng hợp peptidoglycan (thành phần chính của vách tế bào vi khuẩn). Hoạt hóa hệ
thống thủy giải ở tế bào vi khuẩn, gây tổn thương và giết chết nó.
3. Tại sao penicillin V có thể sử dụng đường uống còn penicillin G thì không
(Giải thích bằng cấu trúc hóa học)?
- Penicillin G không uống được do điện tử tập trung nhiều ở amid nội vòng có xu
hưởng phá vô vòng để ghi phỏng điện tử, khi IV trong dịch vị đi qua điện tử sẽ
được cho H+ và vòng amid vỡ làm kháng sinh mất tác dụng.
4. Phân tích các hiện tượng trong thí nghiệm định tính penicillin?
- Phản ứng với thuốc thử Fehling : Fehling A: CuSO4
Fehling B: NaOOC-CHOH-CHOH-COOK Ta có:
• Amoxicillin tạo phức với Cư – phức màu tím (các nhóm chức tham gia tạo phic:
amin bậc 1 và 0 của khung B-lactam (tim đỏ -> đỏ tím -> xanh đen -> xanh lục ).
• Penicillin tạo phúc xanh với Cu2+ trong môi trường kiềm yếu.
5. Fehling A chứa chất gì? Fehling B chứa chất gì? Tại sao không trộn lại để
bảo quản mà khi sử dụng mới cần trộn lại? (Lưu ý: Khi trộn Fehling A và
Fehling B ta thu được thuốc thử Fehling).
- Thuốc thử Fehling có 2 loại là Fehling A có công thức CuSO, và Fehling B là
hỗn hợp của NaOH với muối tartrate của Na và K có công thức NaDOC CHOH-
CHOH-COOK (trong đó -DOC-CHOH-CHOH-COO- là gốc tartrate)
- Khi trộn Fehling A và Fehling B với nhau thì lúc đầu sẽ xảy ra phản ứng tạo kết
tủa Cu(OH), sau đó Cu(OH), phản ứng tiếp với muối tartrate tạo phức đồng tartrate màu xanh
2Na+ 2C4H4O6+2K++ Cu²+ + 20H -> Cu(C4H4O6)2+2Na+ + 2K+
- Hiện tượng hóa học : khi cho andehit vào dung dịch thuốc thử Fehling (A và B)
thấy xuất hiện kết tủa đỏ gạch. Dùng Fehling để cho phản ứng xảy ra dễ đẹp, hiện
tượng rõ ràng hơn là dùng Cu(OH)2 được điều chế từ NaOH và CuSO4 vì có thể nó
bị phân hủy tạo ra chất màu đen.
- Nguyên nhân là để lâu thì phức dồng tartarate không bền để lâu phân giải ra Cu2+
Cu +2 NaOH -> Cu(OH)2 + 2Na
- Khi đó Cu(OH)2 kết tủa làm Fehling không thể làm thuốc thử được nữa.
6. Cơ chế tác động của kháng sinh cloramphenicol?
- Cơ chế tác dụng và phổ kháng khuẩn Cloramphenicol có tác dụng kìm khuẩn,
gắn vào tiểu phần 50s của ribosom nên ngăn cản ARN m gắn vào ribosom, đồng
thời ức chế transferase nên acid amin được mã hóa không gắn được vào polypeptid
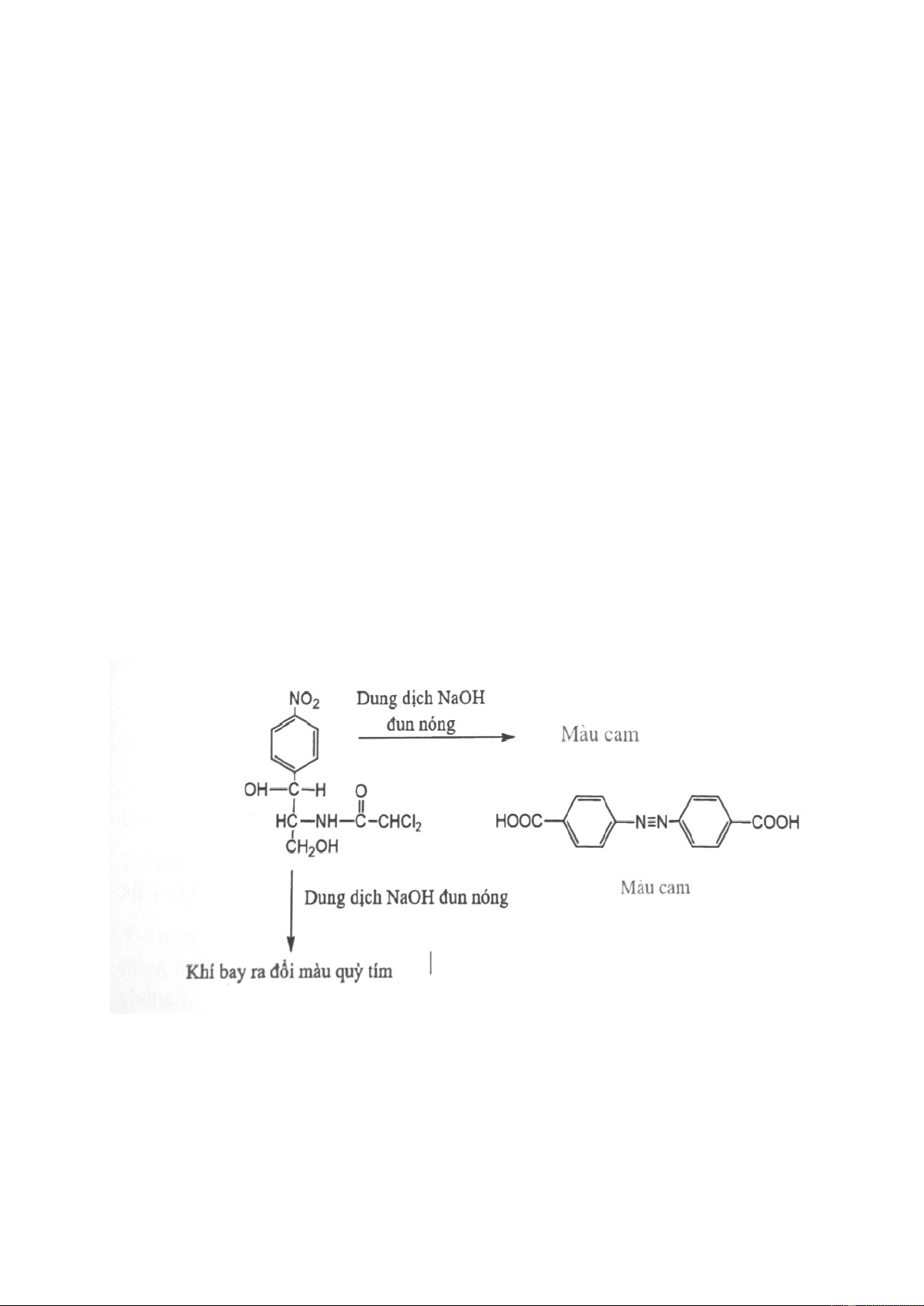
7. Phân tích các hiện tượng trong thí nghiệm định tính cloramphenicol?
BÀI 18: KIỂM ĐỊNH VIÊN NÉN METHIONIN
1. Công dụng của methionin là gì?
-Ngăn ngừa tổn thương gan khi ngộ độc Paracetamol
-Tăng độ acid của nước tiểu
-Điều trị rối loạn men gan
-Cải thiện,làm lành vết thương nhanh.
-Chữa trầm cảm,nghiện rượu,dị ứng,hen suyễn,ngộ độc đồng,tác
dụng về phóng xạ,tâm thần phân liệt,cai nghiện thuốc và bệnh
Pakinson-Dị tật ống thần kinh
-Ung thư ruột kết,ung thư vú.
2. Trình bày những nội dung cơ bản của phân tích thể tích:
-Chất cần phân tích: Methionin -Chất chuẩn:Mẫu trắng
-Môi trường phản ứng:Kiềm nhẹ
-Chất chỉ thị: Hồ tinh bột
-Hiện tượng kết thúc phản ứng: Dung dịch mất màu
-Phương pháp chuẩn độ:Phương pháp oxy hóa khử
-Kỹ thuật chuẩn độ: Chuẩn độ ngược
3. Vai trò K2HPO4 và KH2PO4 trong phương pháp định lượng là gì?
-Cung cấp hệ đệm(HCO32- ,H2CO3- ) giúp ổn định độ pH vì phản
ứng định lượng iod thừa trừ xảy ra trong môi trường kiềm nhẹ
-Trong quá trình phản ứng của iod và methionin sinh ra HI nên
ion K+ trong 2 chất trên sẽ trung hòa lượng HI đảm bảo ổn định
pH môi trường kiềm nhẹ.
4. Mẫu trắng là gì? Tại sao cần định lượng mẫu trắng?
-Mẫu trắng là dung dịch chứa hồ tinh bột + iod và không chứa
chất cần phân tích(Methionin)
- Cần định lượng mẫu trắng vì chúng ta cần xác định lại trong điều
kiện phản ứng lượng iod thay đổi như thế nào so với lượng
chúng ta cho vào, có thể lượng iod sẽ bị ảnh hưởng bởi 1 số yếu tố khách quan bên ngoài.
5. Lập công thức tính toán định lượng.Tính hàm lượng phần
trăm methionin trong mẫu ?
V Na2S2O3= mẫu trắng=24,4ml V1= 11,35 ml V2=11,13ml V3=11,15 ml Vtb=11,21ml
C Na2S2O3 . VNa2S2O3= CIod.VIod (CNa2S2O3=CIod)
V=Vtrắng-Vtb.(Vthử)= 24,4-11,21=12,19ml 1ml dd iod 0,1N -> 7,461 mg C5H11NO2S 12,19 ml -> 83,4886 mg C5H11NO2S
Trong 25ml dịch lọc có 83,4886 mg C5H11NO2S
Trong 100ml có 289,4868 mg C5H11NO2S
P= 289,4868/505,2 . 100% = 58,38%




