

Preview text:
Bài 22: Alkene 1. Khái niệm alkene
2. Tính chất hóa học của ethylene
3. Một số ứng dụng của Ethylene
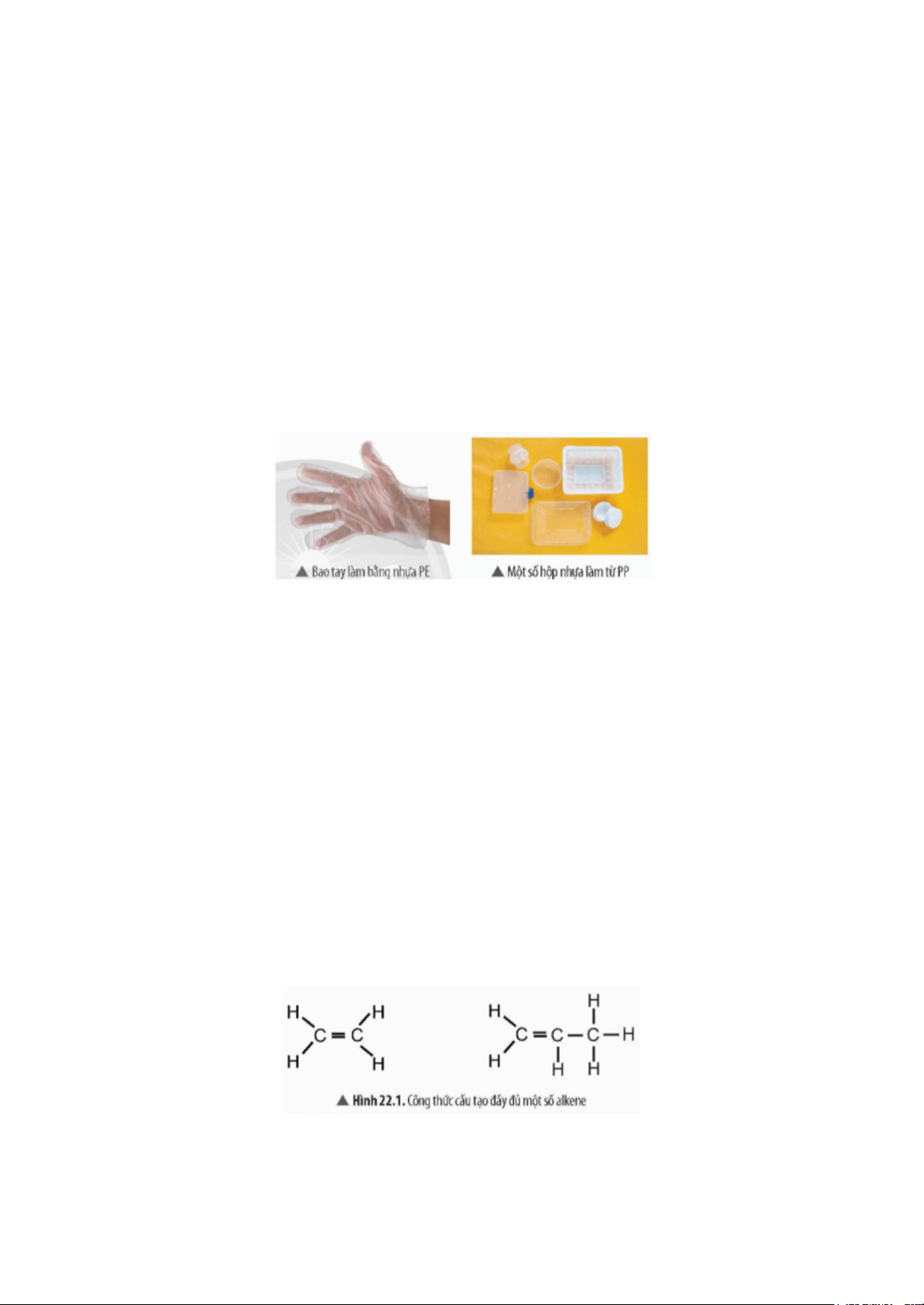
Mở đầu trang 97 Bài 22 KHTN 9: Nhiều vật dụng như: bao tay, hộp nhựa, … được
sản xuất từ hạt nhựa PE, PP. Các loại hạt nhựa này được tổng hợp từ các alkene
tương ứng là ethylene, propylene. Alkene là gì? Alkene đơn giản nhất (ethylene) có
tính chất và ứng dụng gì? Trả lời:
- Alkene là hydrocarbon mạch hở, chứa các liên kết đơn và có một liên kết đôi (C = C) trong phân tử.
- Alkene đơn giản nhất là ethylene, có công thức cấu tạo thu gọn là CH2 = CH2.
+ Tính chất vật lí của ethylene: là chất khí, không màu, không mùi, rất ít tan trong nước.
+ Tính chất hóa học của ethylene: có phản ứng cháy, tác dụng với nước bromine và
tham gia phản ứng trùng hợp tạo thành polymer. 1. Khái niệm alkene
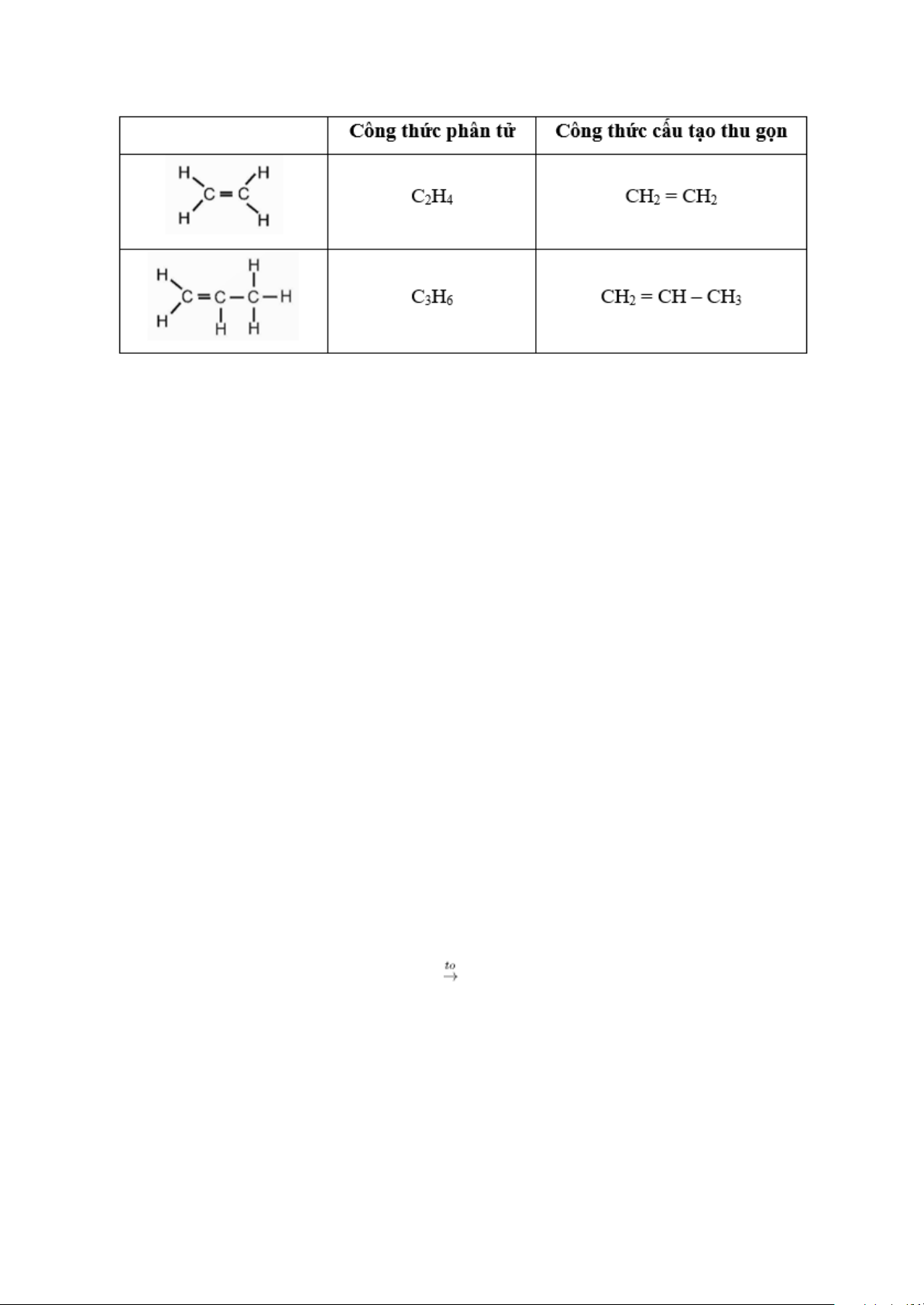
Câu hỏi thảo luận 1 trang 97 KHTN 9: Hãy viết công thức phân tử và công thức
cấu tạo thu gọn của các alkene ở Hình 22.1. Trả lời:
Câu hỏi thảo luận 2 trang 97 KHTN 9: Bằng cách nào để biết được ethylene nhẹ hơn không khí? Trả lời:
Công thức phân tử của ethylene là C2H4 có M = 28 g/mol < Mkk = 29g/mol
→ Ethylene nhẹ hơn không khí.
2. Tính chất hóa học của ethylene
Câu hỏi thảo luận 3 trang 98 KHTN 9: Nêu hiện tượng và viết phương trình hóa
học của phản ứng xảy ra ở thí nghiệm 1.
Thí nghiệm 1: Đốt cháy ethylene trong không khí
Dụng cụ và hoá chất: bật lửa, que đóm, ống thủy tinh vuốt nhọn, ống nghiệm, khí ethylene. Tiến hành:
Nối ống thuỷ tinh vuốt nhọn với ống dẫn khí ethylene (được điều chế từ ethylic
alcohol và dung dịch H2SO4 đặc), sau đó kẹp vào giá thí nghiệm rồi đốt. Trả lời:
Hiện tượng: Ethylene bùng cháy và tỏa nhiệt. Phương trình hóa học: C2H4 + 3O2 2CO2 + 2H2O
Câu hỏi thảo luận 4 trang 98 KHTN 9: Nêu hiện tượng của Thí nghiệm 2 ở Hình
22.2. Dùng công thức cấu tạo thu gọn, viết phương trình hóa học của phản ứng xảy ra. Trả lời:
Hiện tượng: Khi sục khí ethylene vào nước bromine, ta thấy nước bromine nhạt màu
dần và cuối cùng thì mất màu. Phương trình hóa học:
CH2 = CH2 + Br2 → BrCH2 – CH2Br
Câu hỏi củng cố trang 99 KHTN 9:Cho các hợp chất hữu cơ sau:
CH3-CH3,CH2=CH-CH3, CH2=CHCl, CH3-CH2-CH3. Trong các chất trên, chất nào có
phản ứng trùng hợp tạo polymer và chất nào có khả năng làm mất màu nước bromine? Giải thích. Trả lời:
Chất tham gia phản ứng trùng hợp là: CH2=CH-CH3, CH2=CHCl.
Chất có khả năng làm mất màu nước bromine là: CH2=CH-CH3, CH2=CHCl.
Giải thích: Các hợp chất hữu cơ có liên kết C=C sẽ có khả năng làm mất màu nước
bromine và tham gia phản ứng trùng hợp. Phương trình hóa học:
CH2 = CH – CH3 + Br2 → BrCH2 – CH(Br) – CH3
CH2 = CH – Cl + Br2 → BrCH2 – CH(Br) – Cl
Vận dụng trang 99 KHTN 9: PE được tạo ra từ ethylene, có nhiều ứng dụng trong
đời sống như làm màng bọc thực phẩm, các loại bao đựng, .... Hãy cho biết thêm
một số ứng dụng của polyethylene. Trả lời:
Một số ứng dụng của polyethylene như: làm vỏ bọc dây điện, chai lọ, ống dẫn nước,
sản xuất đồ chơi, đồ gia dụng, …
3. Một số ứng dụng của Ethylene
Vận dụng trang 99 KHTN 9: Tìm hiểu và trình bày một số ứng dụng của ethylene trong đời sống. Trả lời:
Một số ứng dụng của ethylene trong đời sống như:
- Trong công nghiệp, ethylene được ứng dụng rộng rãi trong việc sản xuất bao bì,
dệt may, điện tử; là nguyên liệu tổng hợp các chất hữu cơ; …
- Trong nông nghiệp, ethylene giúp cho trái cây chín nhanh và đều.



