










Preview text:
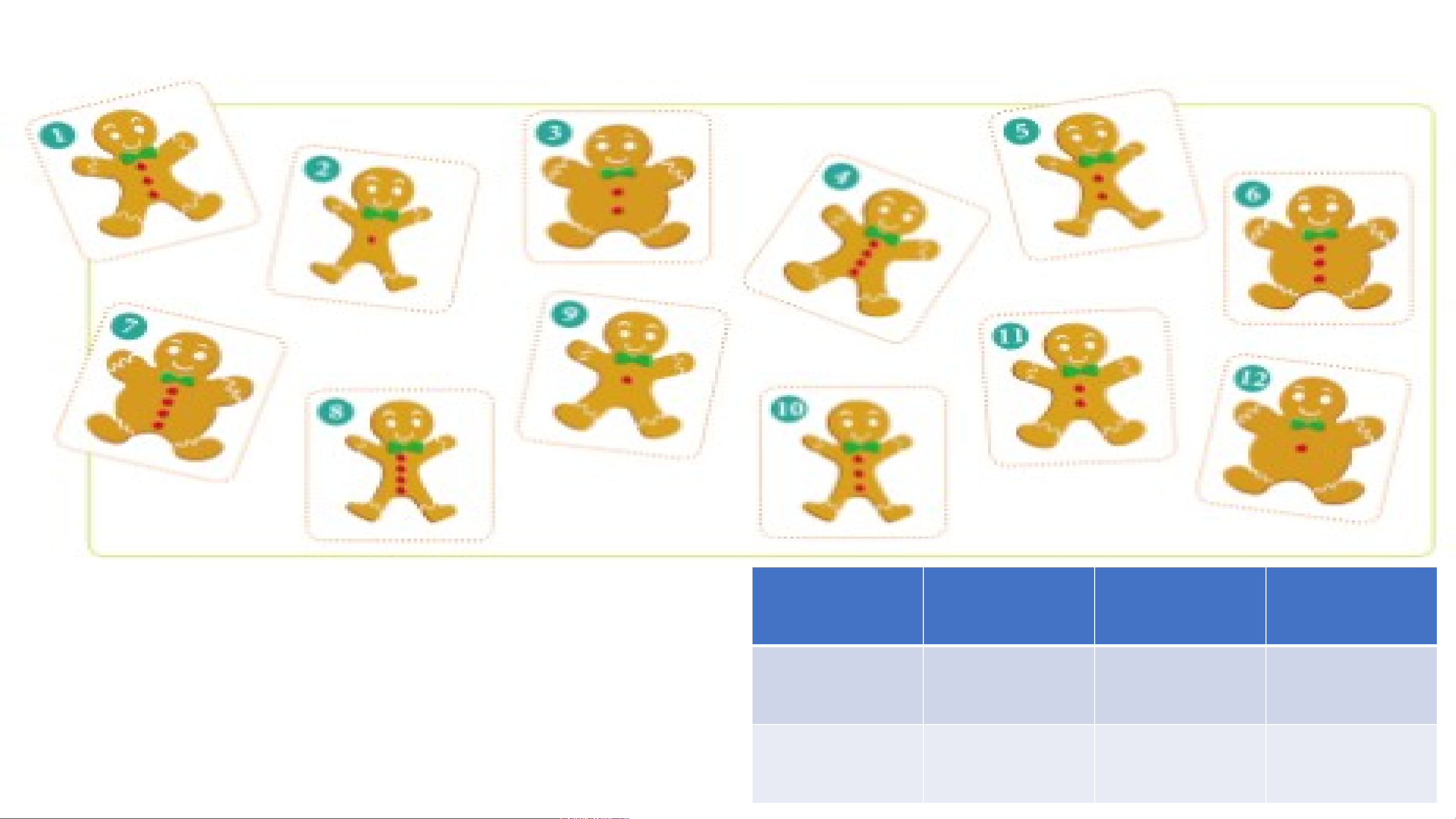
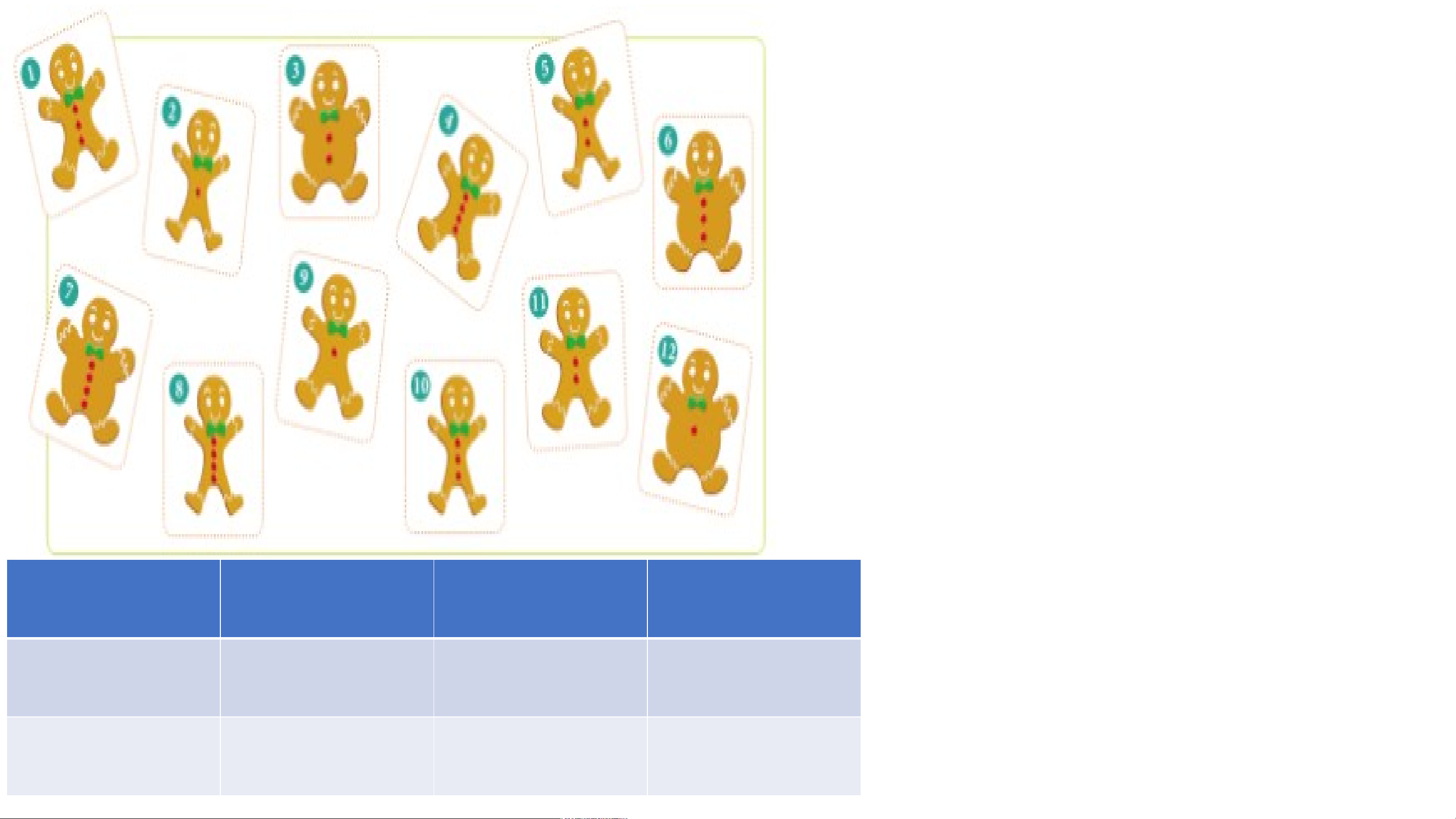
Hãy xếp những tấm thẻ vào các ô trong bảng dưới Trò chơi : Ai nhanh hơn ?
đây theo quy luật nhất định
- Hãy cho biết các tấm thẻ được xếp theo 2 ? 10 ?
quy luật nào theo hàng và theo cột. ? 11 ? ? 12 ? ? 7
Các tấm thẻ được xếp theo quy luật :
+ Theo hàng ngang từ trái sang phải : Các
chú gấu trong tấm thẻ có kích thước bằng
nhau, số khuy áo của các chú gấu tăng dần.
+ Theo cột từ trên xuống dưới : Các chú
gấu trong tấm thẻ có cùng số khuy áo, kích
thước các chú gấu tăng dần.
- Tương tự có thể sắp xếp các
nguyên tố hoá học theo quy luật vào 1 bảng đ 2 5 10 8 ược không ? 9 11 1 4 12 3 6 7
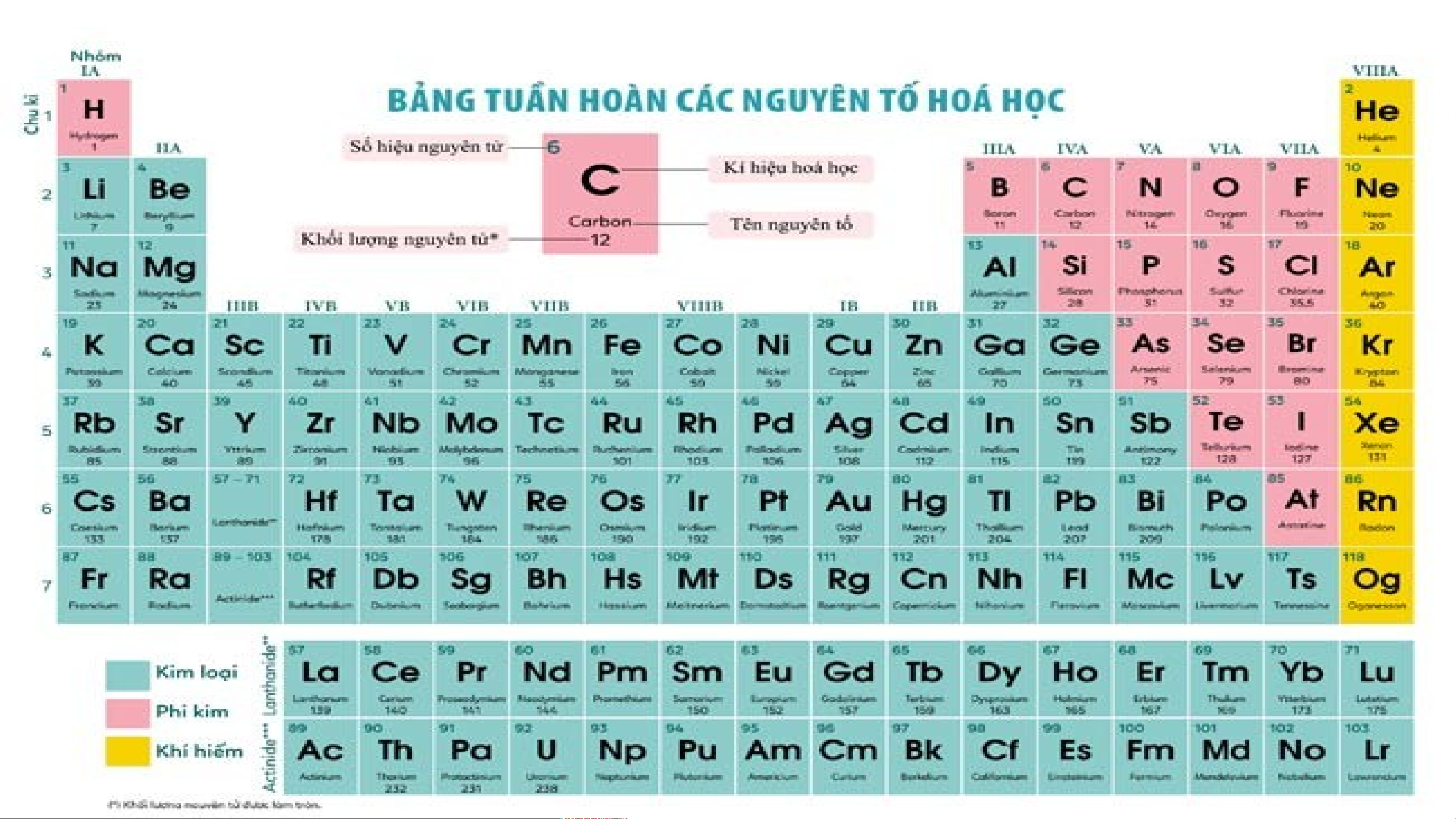
Khi nghiên cứu quy luật biến đổi tính chất
của các nguyên tố, các nhà khoa học đã tìm
cách sắp xếp các nguyên tố vào một bảng
theo nguyên tắc nhất định, gọi là bảng tuần
hoàn các nguyên tố hóa học. Các nguyên tố
hóa học được sắp xếp theo nguyên tắc
nào? Chúng ta biết được thông tin gì từ
bảng tuần hoàn các nguyên tố hóa học?
BÀI 3. SƠ LƯỢC BẢNG TUẦN HOÀN
CÁC NGUYÊN TỐ HÓA HỌC
BÀI 3. SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC NỘI DUNG BÀI HỌC 1
Nguyên tắc sắp xếp các nguyên tố
hoá học trong bảng tuần hoàn 2
Cấu tạo bảng tuần hoàn
Vị trí của các nguyên tố kim loại ,phi 3
kim và khí hiếm trong bảng tuần hoàn 4
Ý nghĩa của bảng tuần hoàn
BÀI 3. SƠ LƯỢC BẢNG TUẦN HOÀN
CÁC NGUYÊN TỐ HÓA HỌC ( tiết 1 )
I. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học Lịch sử phát minh ra bảng tuần hoàn các nguyên tố
BÀI 3. SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
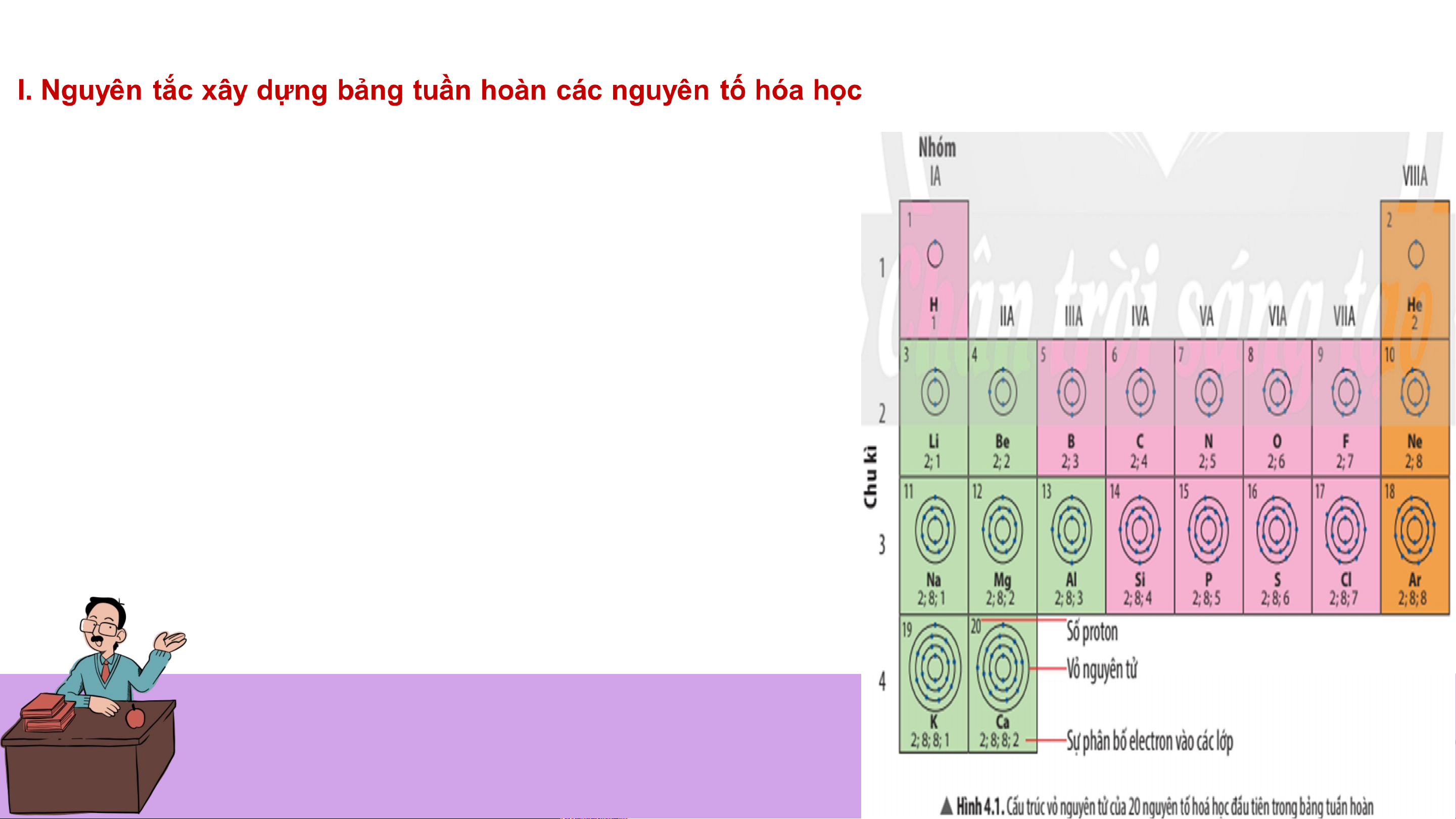
I. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
?. Cho biết điện tích hạt nhân của mỗi nguyên tử C (Carbon ), Si (Silicon ), O
( Oxygen), P (Phosphorus), N(Nitrogen ), S (Sulfur) lần lượt là 6, 14, 8, 15, 7, 16.
Hãy sắp xếp các nguyên tố trên theo chiều điện tích hạt nhân tăng dần từ trái
sang phải và từ trên xuống dưới C ? O Si ? ?
Sắp xếp các nguyên tố trên theo chiều điện tích hạt nhân tăng
dần từ trái sang phải và từ trên xuống dưới C (6) N(7) O(8) Các nguyên tố hoá học
được xếp theo chiều tăng Si(14) P(15) S(16)
dần của điện tích hạt nhân nguyên tử
BÀI 3. SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
I. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
Cơ sở chính để sắp xếp các nguyên tố hóa học vào bảng tuần hoàn các nguyên tố
hóa học là dựa vào điện tích hạt nhân nguyên tử.
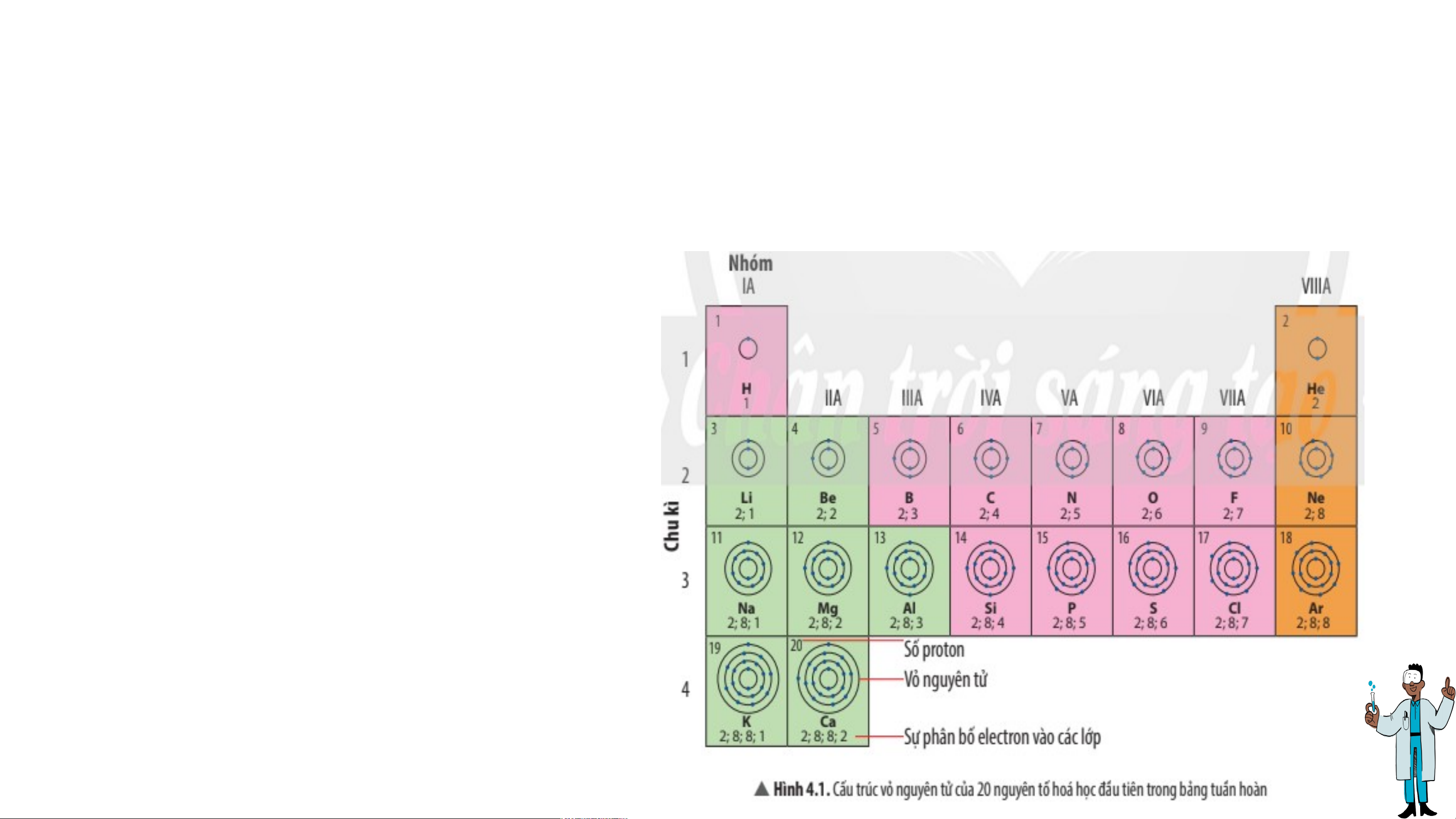
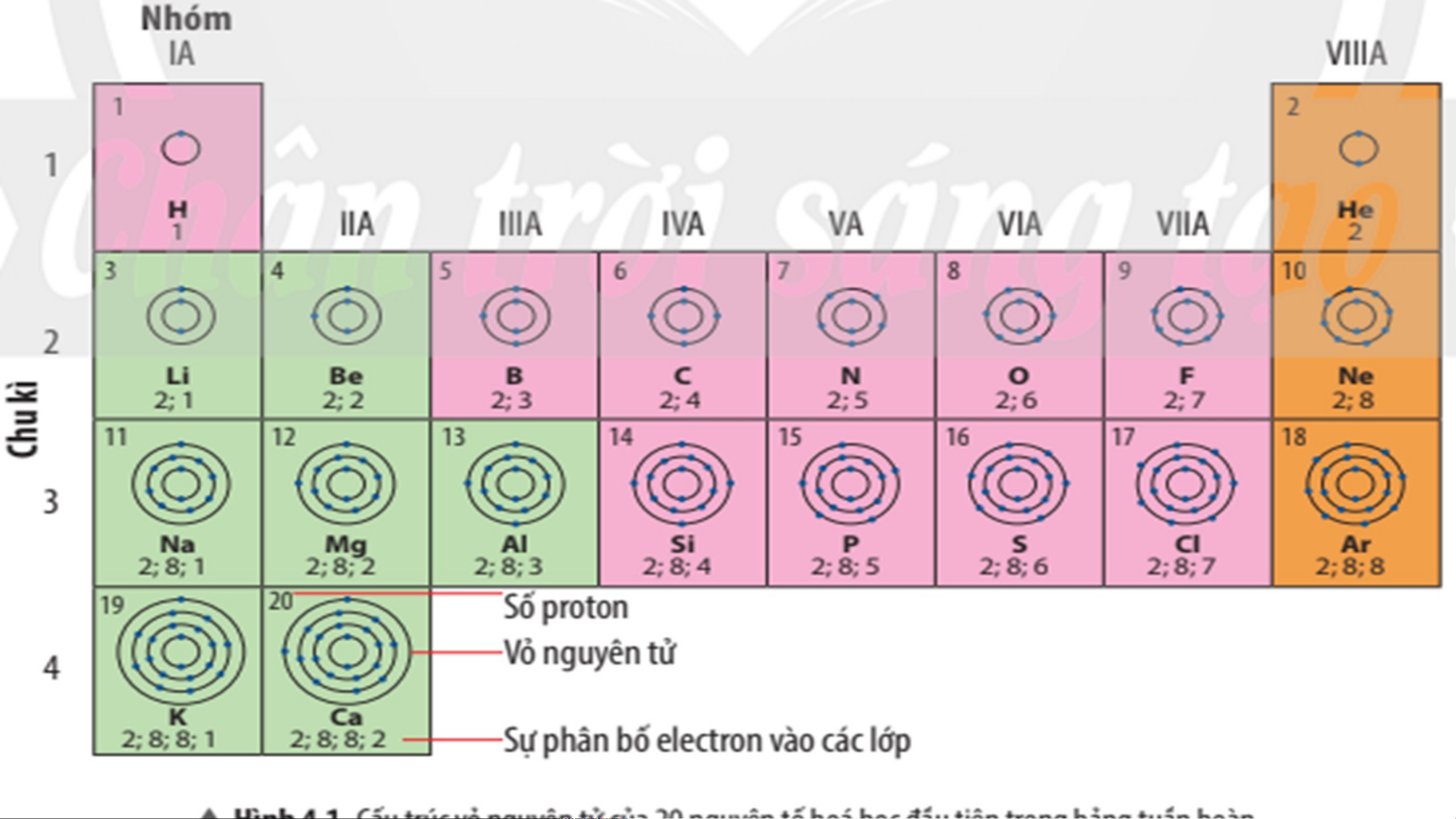
Câu 1: Quan sát hình ảnh và cho biết:
a) Nguyên tử của những nguyên tố nào có cùng số lớp electron.
b) Nguyên tử của những nguyên tố nào có
số electron ở lớp ngoài cùng bằng nhau? Câu trả lời:
a) Các nguyên tử của các nguyên tố
có cùng số lớp electron là: • 1 lớp: H, He
• 2 lớp: Li, Be, B, C, N, O, F, Ne
• 3 lớp: Na, Mg, Al, Si, P, S, Cl, Ar • 4 lớp: K, Ca
b) Nguyên tử các nguyên tố có số lớp electron lớp ngoài cùng bằng nhau: • 1 electron: H, Li, Na, K • 5 electron: N, P • 2 electron: Be, Mg, Ca, He • 6 electron: O, S • 3 electron: B, Al • 7 electron: F, Cl • 4 electron: C, Si • 8 lectron: Ne, Ar
Riêng He chỉ có 2 electron ở lớp ngoài cùng, lại được xếp vào nhóm VIIIA. Dựa v Dựa ào c vào ơ sở số l ớ nào đ p elecể sắp tron trong xếp các ngu
nguyên tử yên tố hóa học trong bảng tuần hoàn? KẾT LUẬN
Nguyên tắc sắp xếp các nguyên tố hoá học trong bảng tuần hoàn :
- Các nguyên tố hóa học trong bảng tuần hoàn được sắp xếp
theo chiều tăng dần điện tích hạt nhân của nguyên tử.
- Các nguyên tố hóa học có cùng số lớp electron trong
nguyên tử được xếp thành một hàng.
- Các nguyên tố có tính chất hóa học tương tự nhau được xếp thành một cột.
HƯỚNG DẪN VỀ NHÀ CẢM ƠN CÁC EM ĐÃ CHÝ Ý LẮNG NGHE!
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19




