









































Preview text:
Bài 4
SƠ LƯỢC BẢNG TUẦN HOÀN
CÁC NGUYÊN TỐ HOÁ HỌC : : :
THẦY CÔ SCAN ĐỂ NHẬN TOÀN BỘ BÀI GIẢNG MÔN KHTN 7
– Người dạy: Nguyễn Hoàng Sơn
Hoặc thầy cô copy đường dẫn này và dán vào youtube: https://www.youtube.com/watch?
v=XlJpP6O8T78&list=PL4t7JCy7eX7mKQgxAYc5BfQnmQzDwVR UV
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC NỘI DUNG BÀI HỌC • NGUYÊN TẮC XÂY DỰN
G BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
• CẤU TẠO BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
• CÁC NGUYÊN TỐ KIM LOẠI • CÁC NGUYÊN TỐ PHI KIM
• CÁC NGUYÊN TỐ KHÍ HIẾM
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
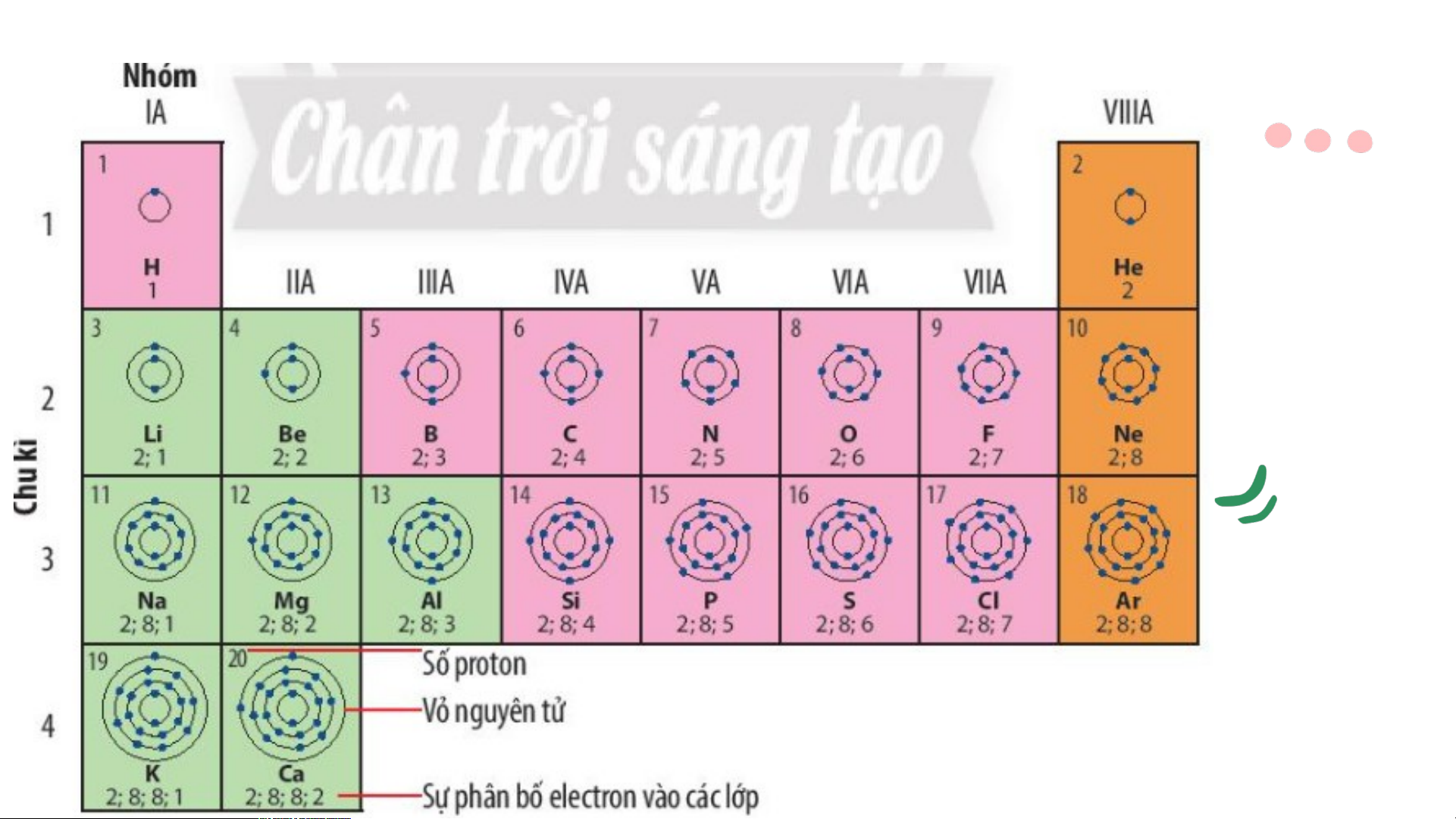
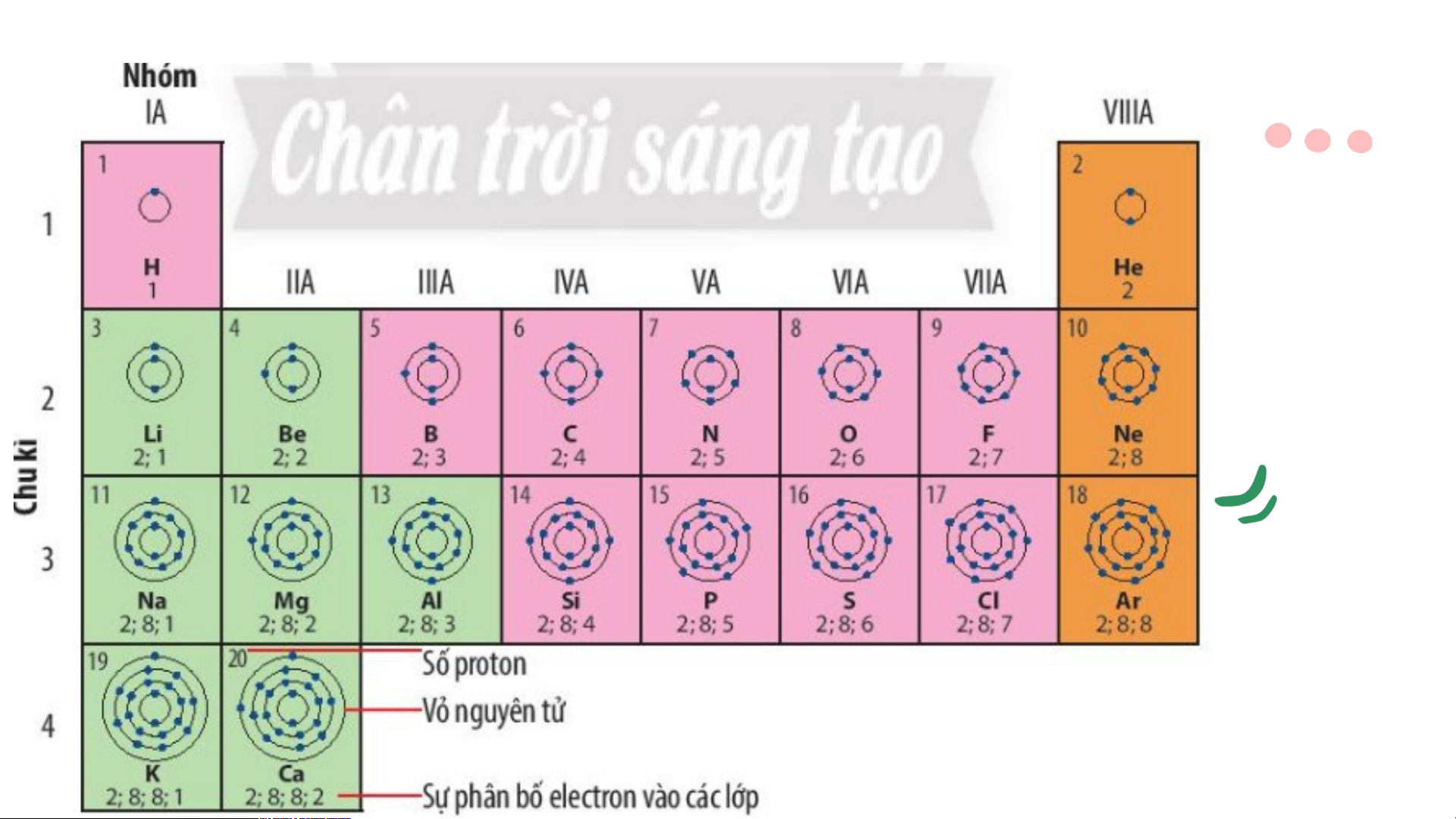
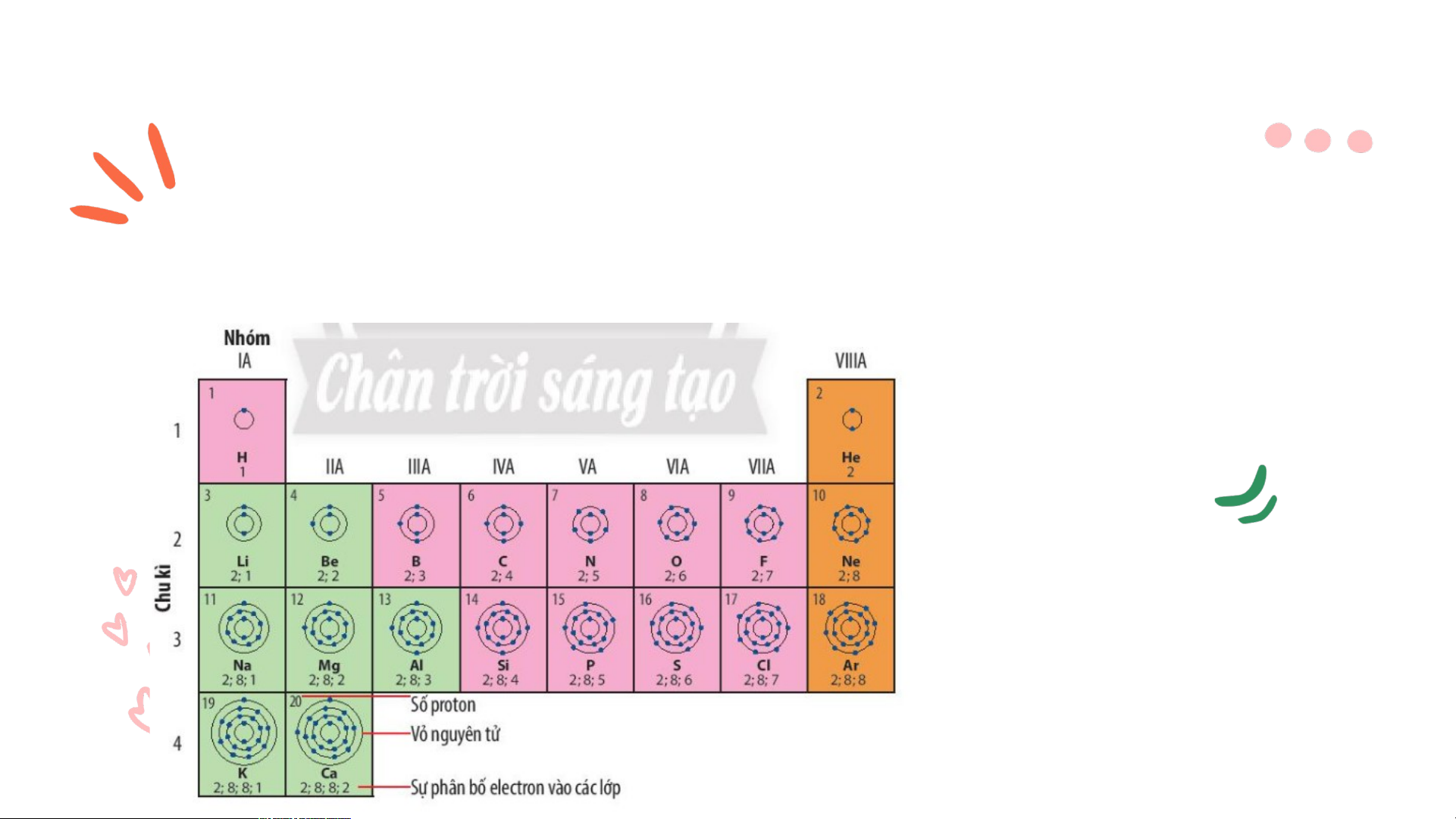
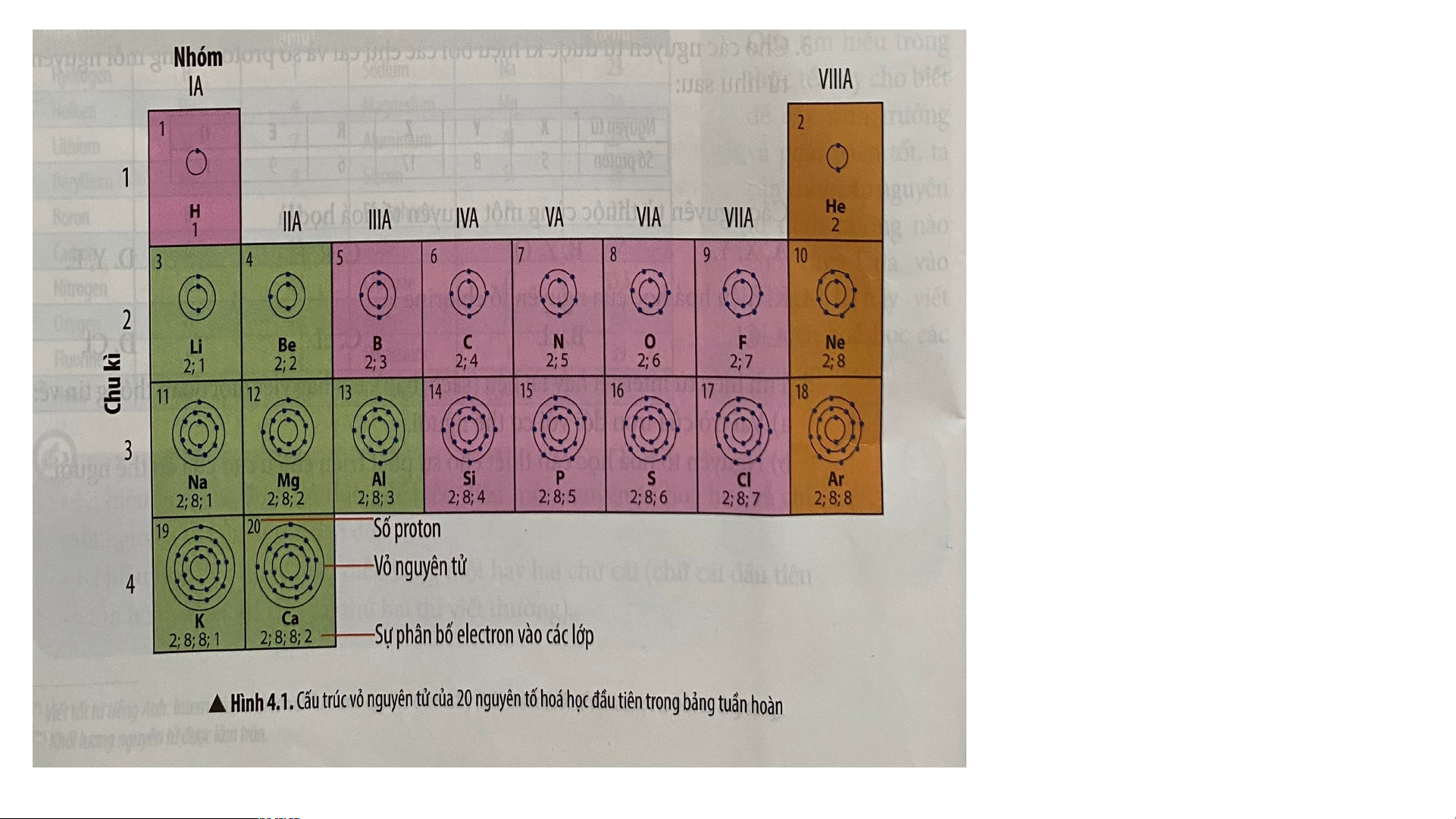
Quan sát hình 4.1 trang 22 SGK cho biết:
a) Nguyên tử của những nguyên tố nào có cùng số lớp electron? b) Nguyên tử của những nguyên tố nào có số electron ở lớp ngoài cùng bằng nhau?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
a) Nguyên tử của những nguyên tố có cùng số lớp electron • Các nguyên tử c
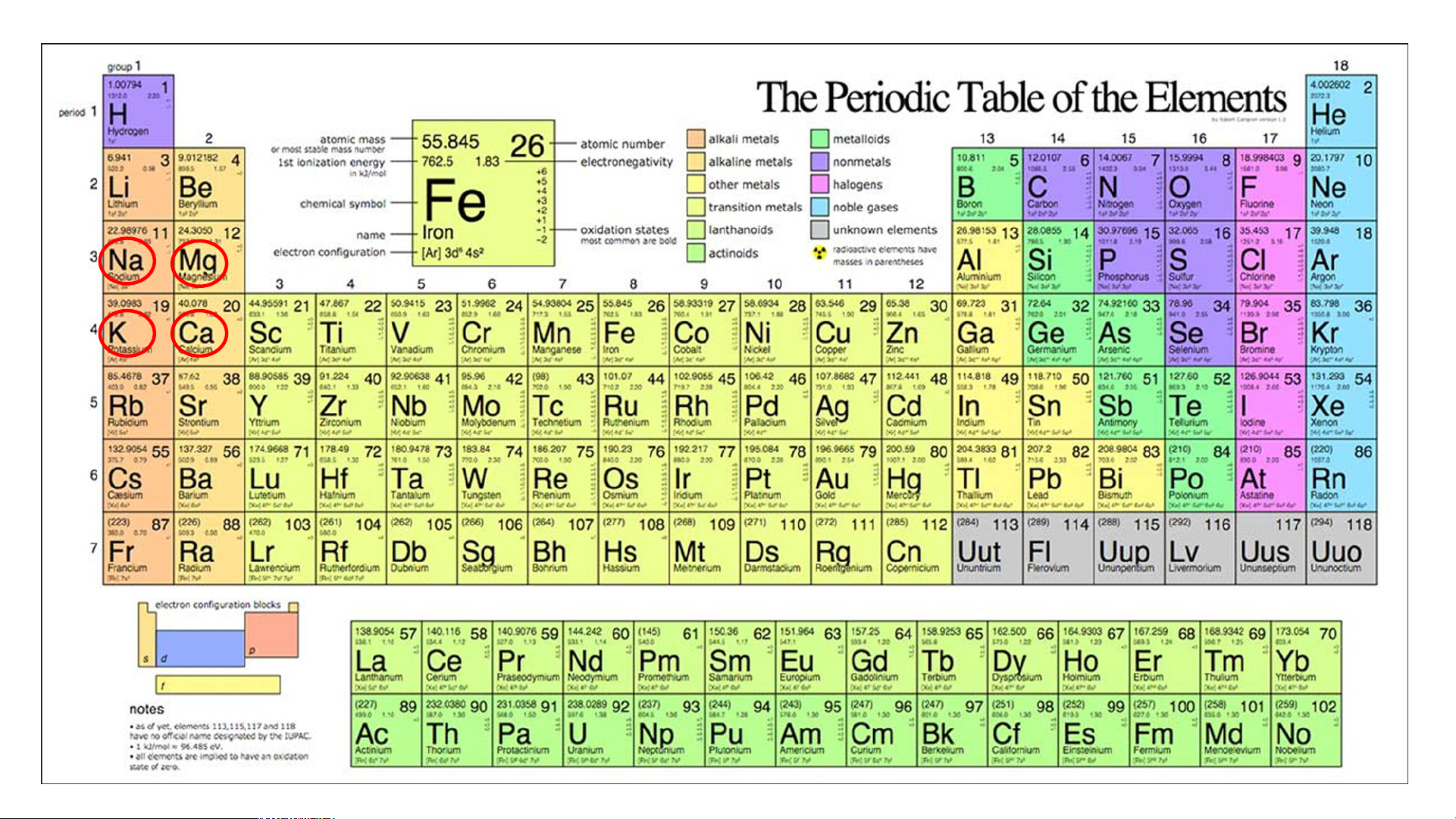
ủa các nguyên tố có cùng số lớp electron là: • 1 lớp: H, He
• 2 lớp: Li, Be, B, C, N, O, F, Ne
• 3 lớp: Na, Mg, Al, Si, P, S, Cl, Ar • 4 lớp: K,Ca
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
Quan sát hình 4.1 trang 22 SGK cho biết:
b) Nguyên tử của những nguyên tố nào
có số electron ở lớp ngoài cùng bằng nhau?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
a) Nguyên tử của những nguyên tố có cùng số lớp electron
b) Nguyên tử của những nguyên tố có số electron ở lớp ngoài cùng bằng nhau là
*Nguyên tử các nguyên tố có số lớp electron lớp ngoài cùng bằng nhau: • 1 electron: H, Li, Na, K • 2 electron: Be, Mg, Ca, He • 3 electron: B, Al • 4 electron: C, Si
*Riêng He chỉ có 2 electron ở lớp ngoài cùng, lại được xếp vào nhóm VIIIA.
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
Vậy em có nhận xét gì về nguyên tắc xây dựng bảng tuần hoàn?
*Nguyên tử các nguyên tố có số lớp electron lớp ngoài cùng bằng nhau: • 1 elec KẾ tr T oLn: U H Ậ , L N i, Na, K • • C 2 á el c ec n t guron yê : n B t e, ố M hó g a , C h a ọ , H c t e ron
g bảng tuần hoàn được sắp xếp theo chiều tăng
• 3 electron: B, Al dần điện tích hạt nhân của nguyên tử. • • Các4 el ng ec u t y r êo nn: t C ố , S
hóia học có cùng số lớp electron trong nguyên tử được xếp thành một hàng.
• Các nguyên tố có tính chất hóa học tương tự nhau được xếp thành một cột
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa họ
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
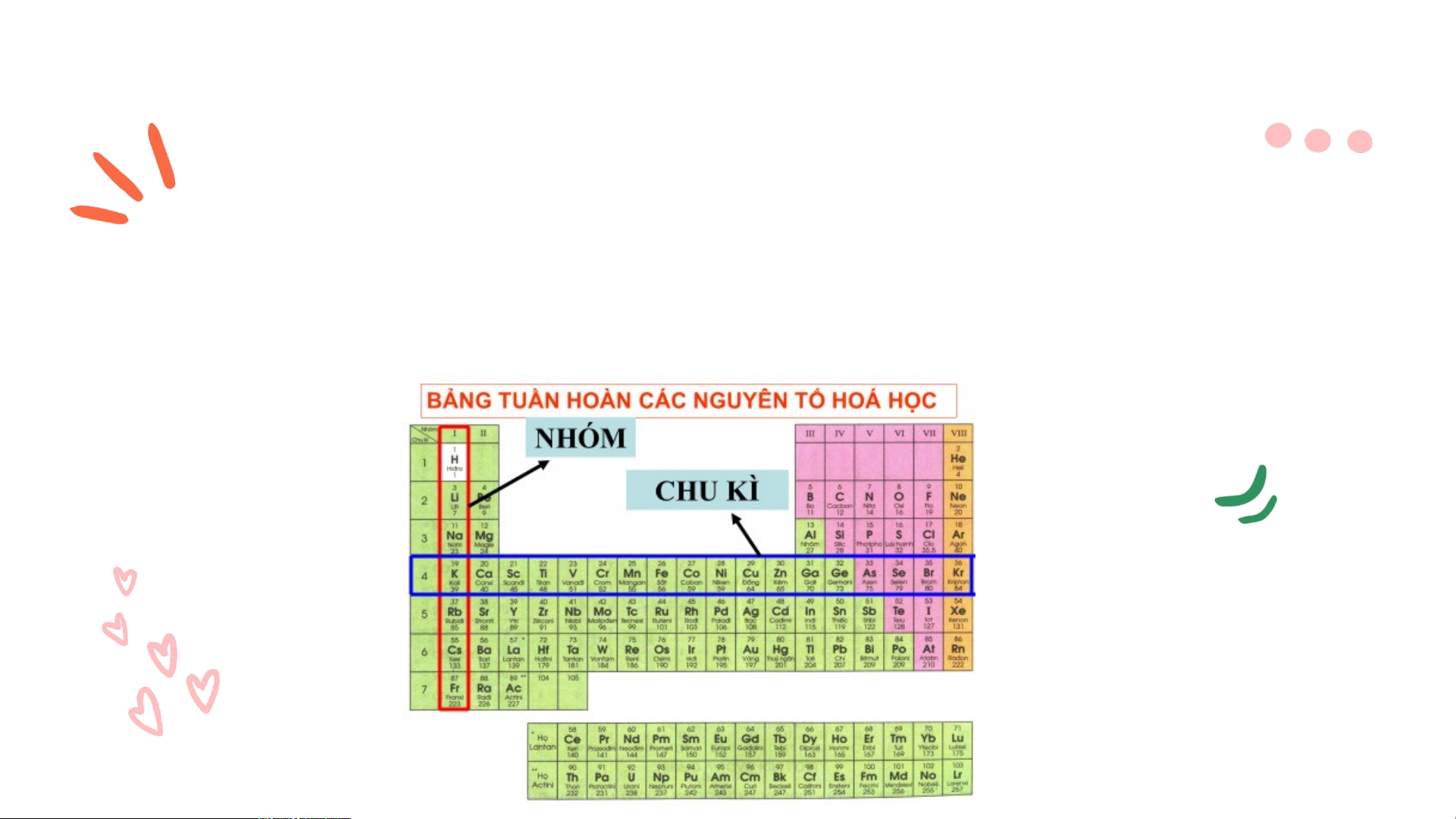
Quan sát bảng tuần hoàn các nguyên tố hóa học cho biết cấu tạo của bảng như thế nào?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
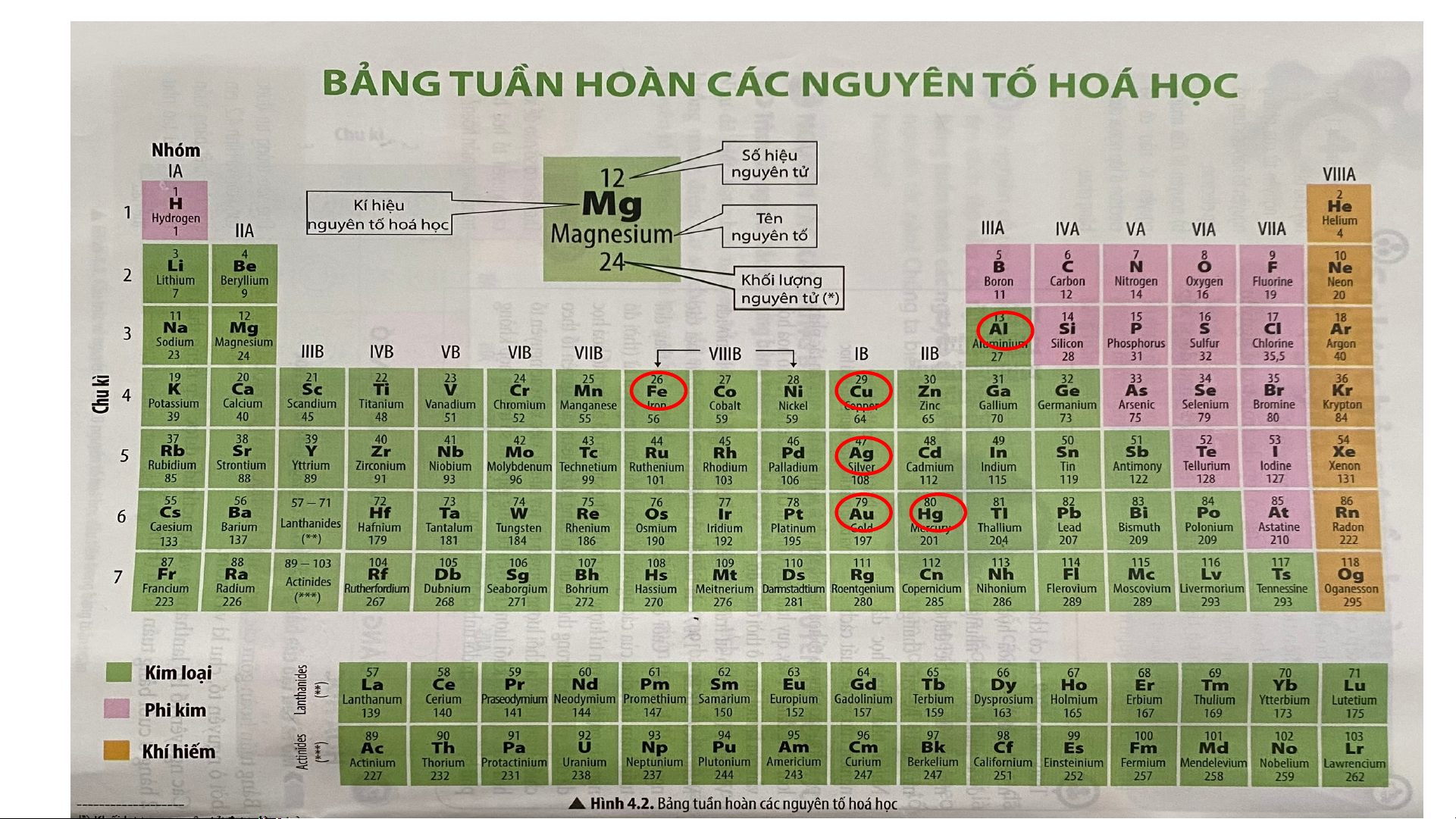
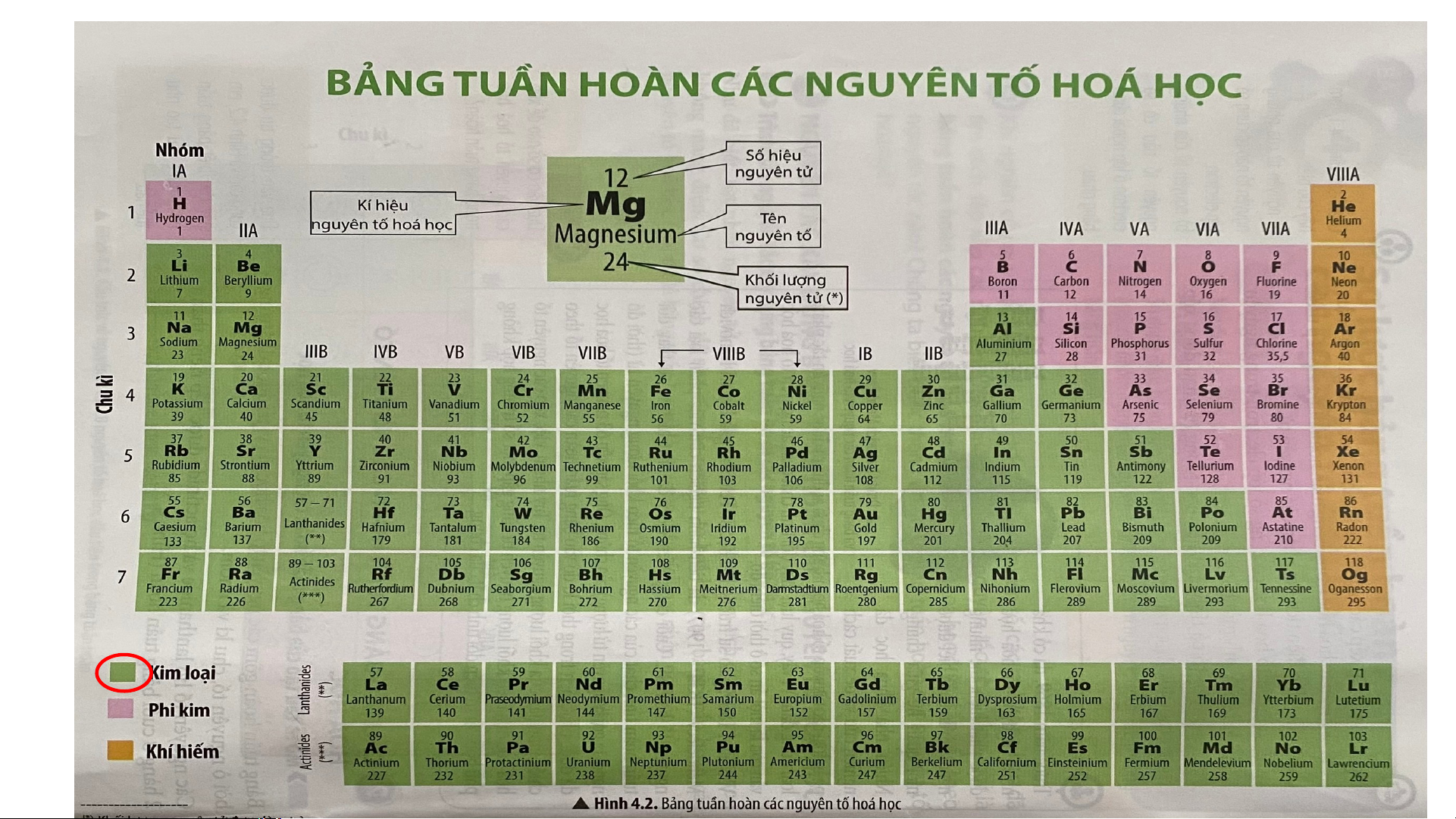
+ Bảng tuần hoàn gồm các nguyên tố hóa học
mà vị trí được đặc trưng bởi ô nguyên tố, chu kì và nhóm
+ Các nguyên tố họ lanthnide và họ actinide được
xếp riêng thành 2 hàng ở cuối bảng tuần hoàn
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong
bảng tuần hoàn các nguyên tố hóa học
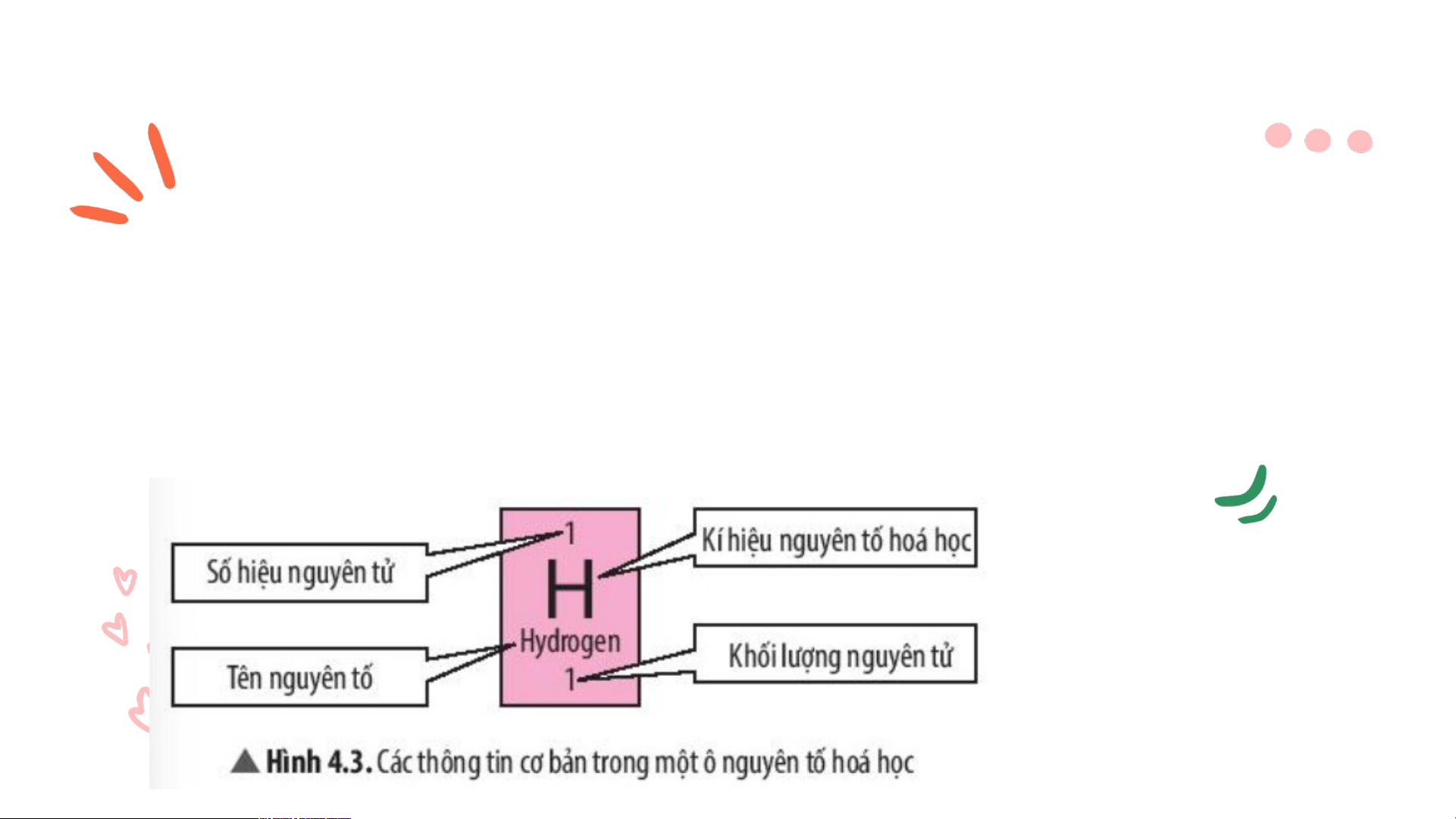
Quan sát hình 4.3 trả lời câu hỏi
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
*Có những thông tin cơ bản nào
trong một ô nguyên tố hóa học?
*Số hiệu nguyên tử của một nguyên tố hóa học cho biết những thông tin gì về nguyên tố đó?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố
2. Cấu tạo bảng tuần hoà h n óa h các ọ nc guyên tố hóa học
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm: + Số hiệu nguyên tử
+ Kí hiệu nguyên tố hóa học + Tên nguyên tố + Khối lượng nguyên tử
- Số hiệu nguyên tử cho biết số đơn vị điện tích hạt nhân và số electron trong nguyên tử *Bài tập luyên tập:
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa học
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học *Bài tập luyên tập:
Cho biết những thông tin cơ bản về nguyên tố hóa học đã cho dưới đây:
Giải: Những thông tin cơ bản về nguyên tố Oxygen: + Số hiệu nguyên tử: 8
+ Kí hiệu nguyên tố hóa học: O + Tên nguyên tố: oxygen
+ Khối lượng nguyên tử: 16
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các 2. Cấu tạo bảng tuần n h gu oànyên cá tố c n h guó ya ê h n ọ t c ố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
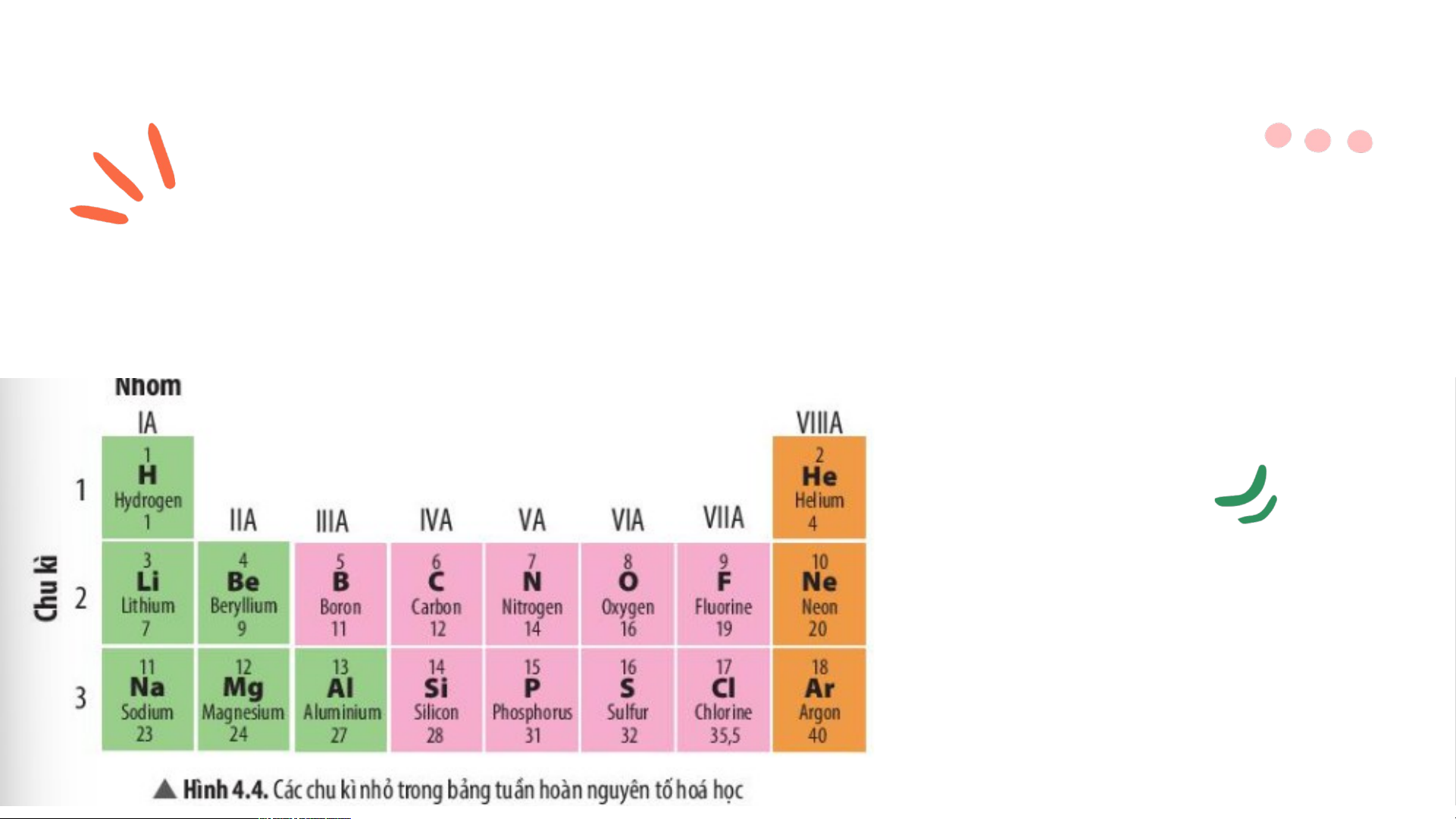
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố hóa học
Quan sát hình 4.4 trả lời chu kỳ là gì?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa
2. Cấu tạo bảng tuần hoàn cá h c n ọ g c uyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố hóa
Quan sát bảng tuần hoàn h tọ r c ả lời
Bảng tuần hoàn nguyên tố hóa học
có mấy chu kì? Bao nhiêu chu kì lớn, bao nhiêu chu kì nhỏ?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa
2. Cấu tạo bảng tuần ho h à ọ n c các nguyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố hóa
Quan sát bảng tuần hoàn th h ảo ọ l c uận nhóm Phiếu học tập
Câu 1.Mỗi chu kì bắt đầu từ
nhóm nào và kết thúc ở nhóm nào?
Câu 2. Em hãy chỉ sự tuần
hoàn ở mỗi chu kì trong bảng
tuần hoàn các nguyên tố hóa học?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hóa
2. Cấu tạo bảng tuần hoàn cá học c nguyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố
- Chu kì là tập hợp các hóa ng h u ọc
yên tố hóa học có cùng số lớp electron trong ngu
yên tử theo hàng ngang.
- Bảng tuần hoàn có 7 chu kì, gồm 3 chu kì nhỏ và 4 chu kì lớn + .
Mỗi chu kì bắt đầu từ nhóm IA và kết thúc ở nhóm VIIIA
+ Trong mỗi chu kì các nguyên tố được xếp thành hàng tăng dần điện tích hạt nhân.
Mỗi chu kì bắt đầu bằng nguyên tố có 1 electron lớp ngoài cùng, tiếp
theo là nguyên tố có 2 electron lớp ngoài cùng và cứ thế kết thúc
chu kì bằng 1 nguyên tố có 8 electron lớp ngoài cùng và tiếp tục một chu kì mới.
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố hóa
d. Tìm hiểu về nhóm trong bả h n ọ g c
tuần hoàn hoàn các nguyên tố hóa
- Các thông tin trong một ô nguyên tố hóa học gồm: học
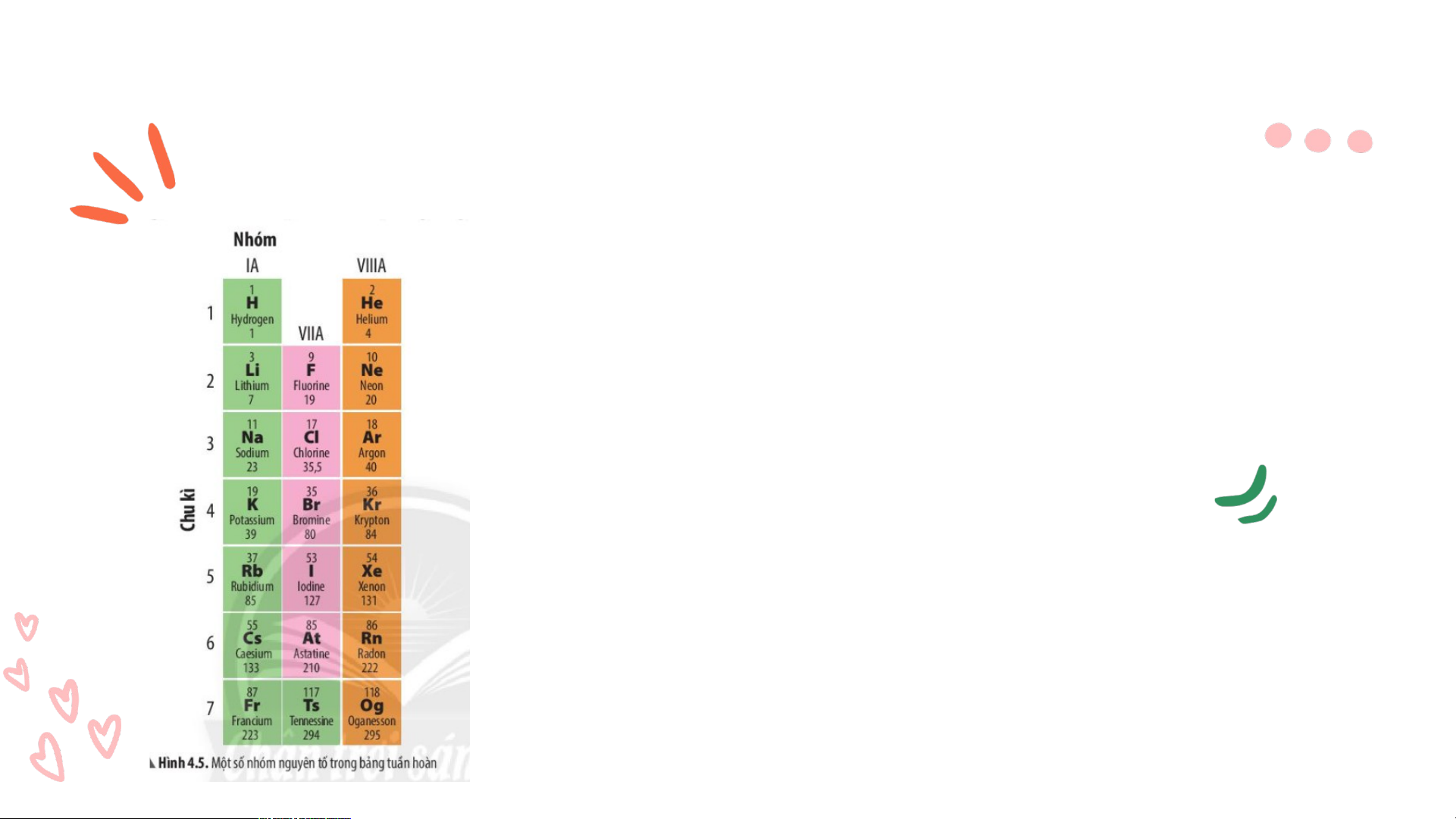
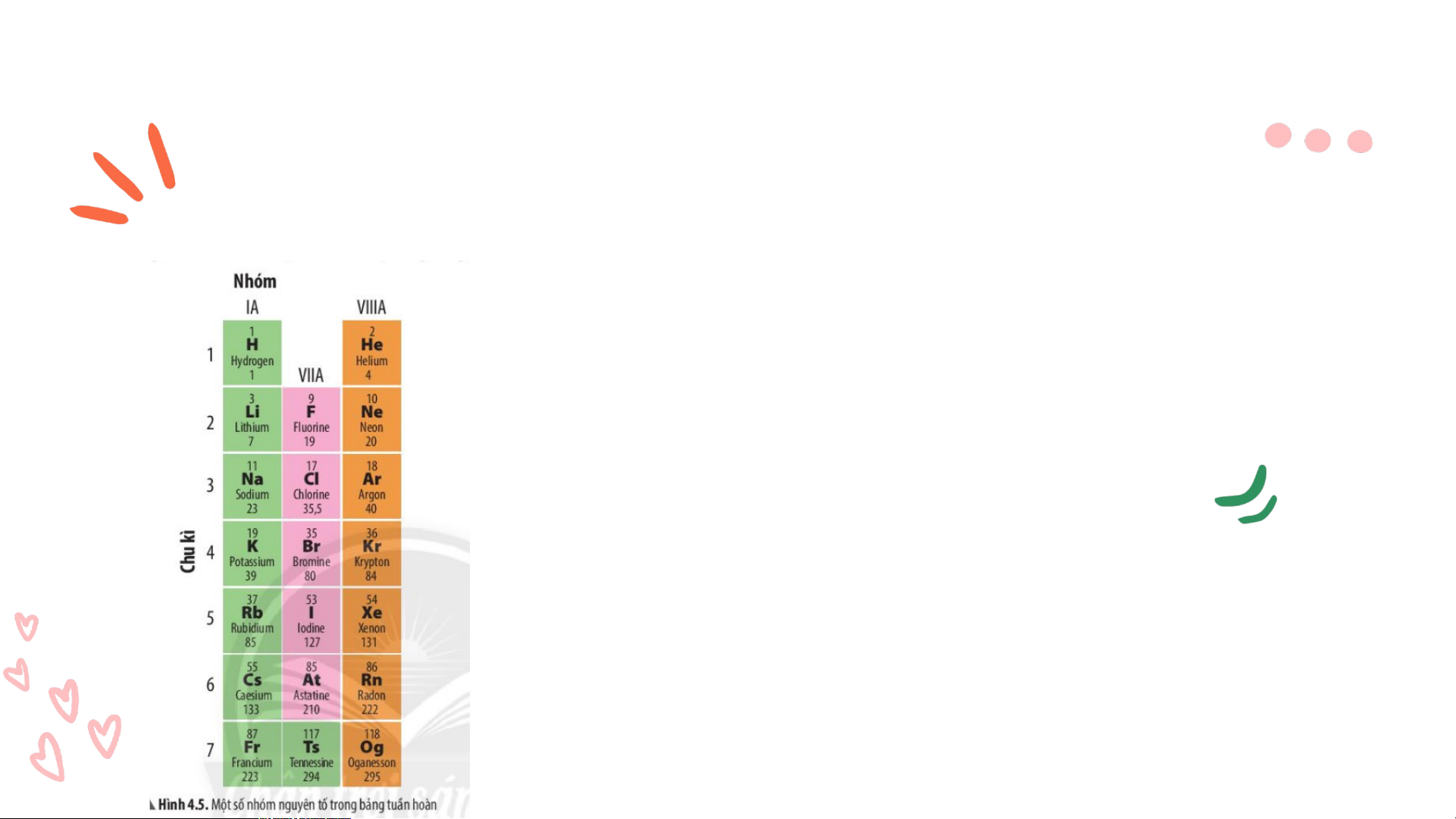
Quan sát hình 4.5 , cho biết những nguyên tố
nào có tính chất tương tự nhau? nhóm là gì?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA
2. Cấu tạo bảng tuần hoàn cH á Ọ c C nguyên tố hóa học
d. Tìm hiểu về nhóm trong bảng tuần hoàn hoàn các nguyên tố
Quan sát hình 4.5 , cho biết nhữn hóg n a hgu
ọc yên tố nào có tính chất tương tự
- Các thông tin trong một ô nguyên tố hóa học gồm: nh.au?
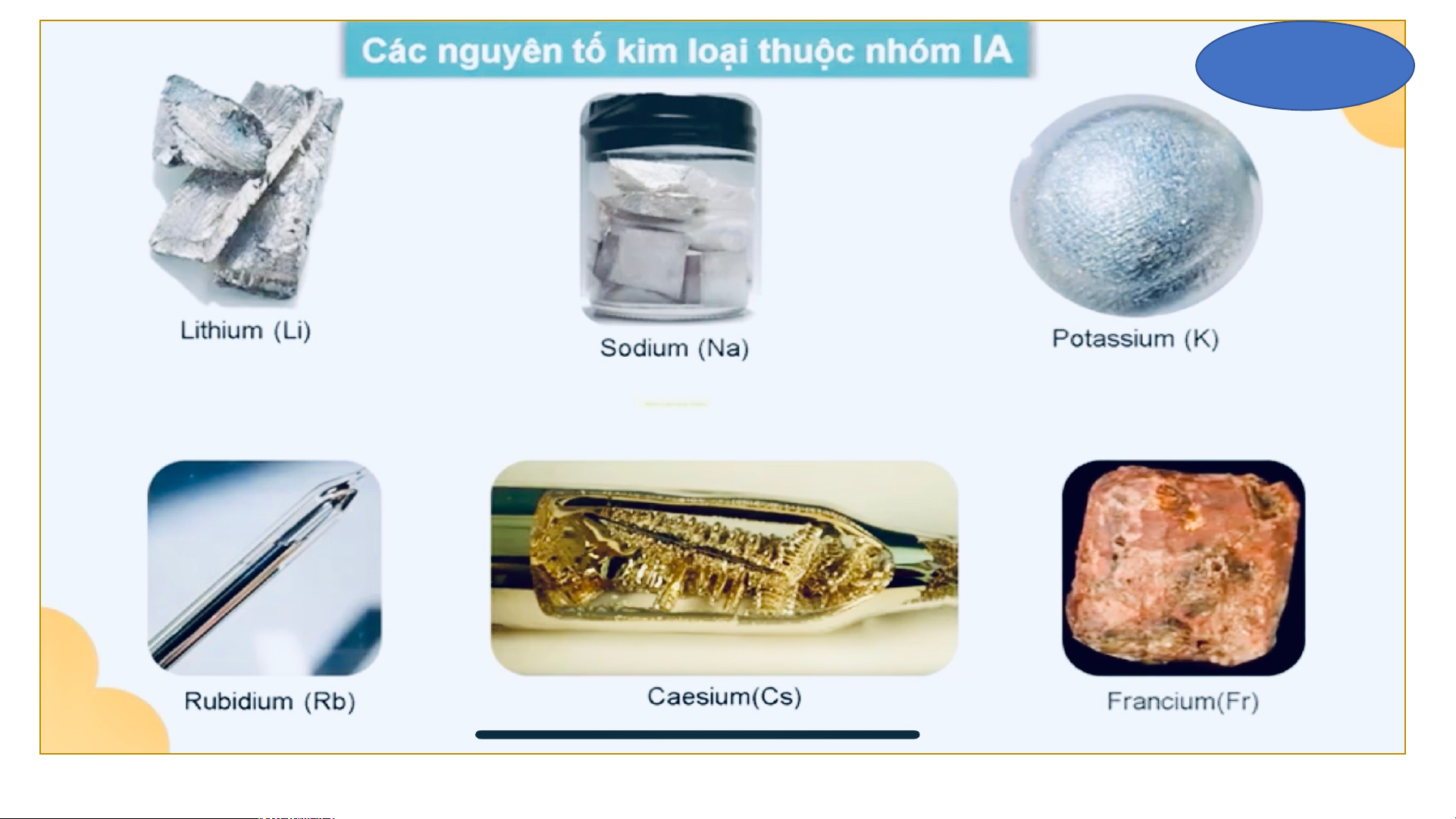
Những nguyên tố có tính chất tương tự nhau là: • H, Li, Na, K, Rb, Cs, Fr • F, Cl, Br, I, At, Ts • He, Ne, Ar, Kr, Xe, Rn, Og
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
d. Tìm hiểu về nhóm trong bảng tuần hoàn hoàn các nguyên tố
• Dựa vào hình 4.2, hãy h h o ó àn a t họh cành các
- Các thông tin trong một ô nguyên tố hóa học gồm:
thông tin còn thiếu trong b.ảng sau: Nguyên tố KHHH Nhóm Chu kỳ Calcium ? ? ? ? P ? ? Xenon ? ? ?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
2. Cấu tạo bảng tuần hoàn các nguyên tố hóa học
d. Tìm hiểu về nhóm trong bảng tuần hoàn hoàn các nguyên tố
• Dựa vào hình 4.2, hãy hoàn hó t a h h à ọ n c h các
- Các thông tin trong một ô nguyên tố hóa học gồm:
thông tin còn thiếu trong bản . g sau: Nguyên tố KHHH Nhóm Chu kỳ Calcium Ca II A 4 phosphorus P VA 2 Xenon Xe VIIA 5
Qua đây các con cho biết nhóm các nguyên tố hóa học là gì?
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố 2. Cấu tạo bảng tuần h h ó o a h àn ọc các nguyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố hóa
d. Tìm hiểu về nhóm trong bản h g tọc
uần hoàn hoàn các nguyên tố hóa học.
- Nhóm là tập hợp các nguyên tố có tính chất hóa học tương tự
nhau và được xếp thành cột, theo chiều tăng dần về điện tích hạt nhân.
BÀI 4: SƠ LƯỢC BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Nguyên tắc xây dựng bảng tuần hoàn các nguyên tố 2. Cấu tạo bảng tuần h h ó o a h àn ọc các nguyên tố hóa học
- Các thông tin trong một ô nguyên tố hóa học gồm:
a. Mô tả cấu tạo của bảng tuần hoàn các nguyên tố hóa học
b.Tìm hiểu ô nguyên tố trrong bảng tuần hoàn các nguyên tố hóa học
c. Tìm hiểu về chu kì trong bảng tuần hoàn các nguyên tố hóa
d. Tìm hiểu về nhóm trong bản h g t ọ u c
ần hoàn hoàn các nguyên tố hóa học.
Ôn tập lại nội dung 1 và nội dung 2
Câu 1. Hiện nay, có bao nhiêu chu kì trong bảng tuần hoàn các nguyên tố hoá học. A. 5. C.8 B. 7. D. 9.
Câu 2. Trong bảng tuần hoàn các nguyên tố hoá học, các
nguyên tố hoá học được sắp xếp theo thứ tự tăng dần của. A. Khối lượng. C. Số proton B. Tỉ trọng. D. Số neutron.
Câu 3. Tên gọi của các cột trong bảng tuần hoàn các
nguyên tố hoá học là gì?. A. Chu kì. C. Họ B. Loại. D. Nhóm.
Câu 4. Những nguyên tố nào sau đây thuộc nhóm VIIA (Halogen)?. A. Chlorine, bromine, Iorine.. C. Beryllium, carbon, oxygen B. Fluorine, carbon, bromine. D. Neon, helium, argon..
PHIẾU HỌC TẬP SỐ 1
BẢNG SO SÁNH CÁC LOẠI HỢP CHẤT VÔ CƠ
(Thời gian hoàn thành 5 phút)
Câu 1. Xác định vị trí ( ô nguyên tố, nhóm, chu kì) của các nguyên tố: OXIT V AX ị t IT rí BAZƠ MUỐI Tên nguyên tố Ô thứ nhóm Chu kì Potassium (K ) KHÁI SNIỆM odium (Na) Caesium (Ca) Magnesium -Công thức tổng quát:
- Công thức tổng quát: - Công thức tổng quát: - Công thức tổng quát: (Mg ) A O H A M(OH) M A x y n n x y Câu 2. Nêu cá- cA là kí h nguyêiệ n u t hóa ố kim l - oạ Ai tlà h g u ốc ộc axit. nhóm IA - M và c là áckim loại.
nguyê n tố - M là kim loại. C t Ô h N u G T ộc H Ứ n C hóm họ IIA. c. - n là chỉ số, là hóa - n là chỉ số, là hóa - A là gốc axit ; x,y là - x, y là chỉ số trị của A trị của M chỉ số.
Câu 3. Nêu một số ứng dụng của các nguên tố kim loại mà em biết. Nhóm kim loại kiềm Kim loại kiềm Nhóm kim loại kiềm thổ
Ứng dụng của một số nguyên tố kim loại nhóm A. potassium
PHIẾU HỌC TẬP SỐ 2
(Thời gian hoàn thành 5 phút)
Câu 1. Một kim loại ở thể lỏng trong điều kiện thường
được ứng dụng để chế tạo nhiệt kế. Đó là kim loại nào?
Cho biết vị trí ( ô, nhóm, chu kì) của nguyên tố đó.
Câu 2. Hãy cho biết những kim loại nào được sử dụng
làm đồ trang sức, làm dây dẫn điện, làm vật liệu trong xây
dựng, hãy cho biết vị trí (ô, nhóm, chu kì) của nguyên tố
đó trong bảng tuần hoàn.
Hg là chất độc hại gây nguy hiểm tới sức khỏe con người. Theo WHO (tổ chức y tế
thế giới) thì chất này là một trong mười nhóm hóa chất độc nhất. Ở dạng kim loại, các
hợp chất và muối của Hg rất độc. Khi cơ thể tiếp xúc, hít thở hay nuốt phải các chất
trên sẽ gây tổn thương não và gan.
Kim loại Hg: Tiếp xúc qua con đường không khí và được hít vào phổi. Thể hơi của Hg là
nguy hiểm nhất. Chất này được sinh ra từ hoạt động của các nhà máy nhiệt điện, lò đốt
rác hoặc cháy rừng, vỡ nhiệt kế.
ỨNG DỤNG CỦA MỘT SỐ KIM LOẠI NHÓM B 45
3. Các nguyên tố kim loại
a. Tìm hiểu các nguyên tố kim loại nhóm A
- Nguyên tố kim loại nhóm A gồm nhóm IA, IIA (trừ
nguyên tố hydrogen), IIIA (trừ nguyên tố boron) ...
+ Nguyên tố kim loại thuộc nhóm IA được gọi là nhóm kim loại kiềm.
+ Nguyên tố kim loại thuộc nhóm IIA gọi là nhóm kim loại kiềm thổ.
3. Các nguyên tố kim loại
a. Tìm hiểu các nguyên tố kim loại b. n T h ì óm h m i
Aểu các nguyên tố kim loại nhóm B
- Các nguyên tố nhóm B đều là kim loại.
- Một số kim loại nhóm B có ứng dụng rộng rãi: iron, copper, silver, ...
- Hơn 80% các nguyên tố hóa học trong bảng
tuần hoàn là kim loại, bao gồm một số nguyên
tố nhóm A và tất cả các nguyên tố nhóm B.
F- Fluorine dưới nhiều hình thức là thành phần hoạt chất phổ biến
nhất trong kem đánh răng để ngăn ngừa sâu răng. Fluoride có số
lượng nhỏ trong thực vật, động vật và một số nguồn nước tự nhiên.
Chất fluoride bổ sung trong kem đánh răng có tác dụng tốt đối với
quá trình hình thành men răng và xương.
PHIẾU HỌC TẬP SỐ 4
(Thời gian hoàn thành 6 phút)
Câu 1. Cho biết vị trí của các nguyên tố khí hiếm
Câu 2. Sử dụng hình 4.1 em hãy nhận xét về số electron lớp ngoài
cùng trong nguyên tử của các nguyên tố khí hiếm.
Câu 3. Vào những dịp tết hay lễ hội, ở một số thành phố hoặc khu
vui chơi giải trí công cộng chúng ta thường thấy những khinh khí
cầu đủ màu sắc bay trên bầu trời. Theo em người ta đã bơm khí
nào trong các khí: oxygen, helium, hydrogen vào khinh khí cầu?
Giải thích sự lựa chọn đó. 53 Các nguyên tố khí hiếm khi nghiên cứu các
nguyên tố khí hiếm, các
nhà hóa học phát hiện ra rằng các nguyên tố này
đều có số electron lớp ngoài cùng của nguyên tử bão hòa (2 hoặc 8 electron). Với cấu tạo
bền vững như vậy, chúng
hoạt động hóa học cực kì
yếu. Ở điều kiện thường, các nguyên tố này rất khó phản ứng hóa học
với các vật chất khác, để
hình thành các hợp chất.
ĐIỀU BẠN CẦN BIẾT
Khinh khí cầu, bóng bay có thể
bơm bằng khí helium hoặc hydrogen
vì chúng là các khí nhẹ nhất trong các chất khí.
Khi bạn ra đường mua bóng bay
được bơm hơi ở các điểm vui chơi
giải trí, hầu như tất cả những quả
bóng bay đó đều chỉ được bơm
bằng khí Hidro vì khí Heli rất đắt.
Nếu bán cho bạn 20.000 quả bóng
bay đó người ta cũng chỉ hòa hoặc
không đủ tiền mua khí Heli
Tuy nhiên, khi bơm bằng hydrogen
có thể nguy hiểm vì nó dễ phản ứng
với oxygen gây nổ, còn với helium là
khí ở điều kiện thường khó có thể
phản ứng với các vật chất khác nên an toàn hơn. Neon là loại đèn sử dụng ống thủy tinh với nhiều đường kính khác nhau. Chúng có thể phát sáng. Nhờ bên trong có chứa khí hiếm như Neon hoặc Argon, trong áp suất thấp. Neon sẽ cho ra ánh sáng màu đỏ. Còn Argon sẽ cho ra ánh sáng màu yếu hơn như vàng, xanh dương, xanh lá cây, trắng
3. Các nguyên tố kim loại
a. Tìm hiểu các nguyên tố kim loại nhóm A
b. Tìm hiểu các nguyên tố kim loại nhóm B
c. Tìm hiểu các nguyên tố phi kim
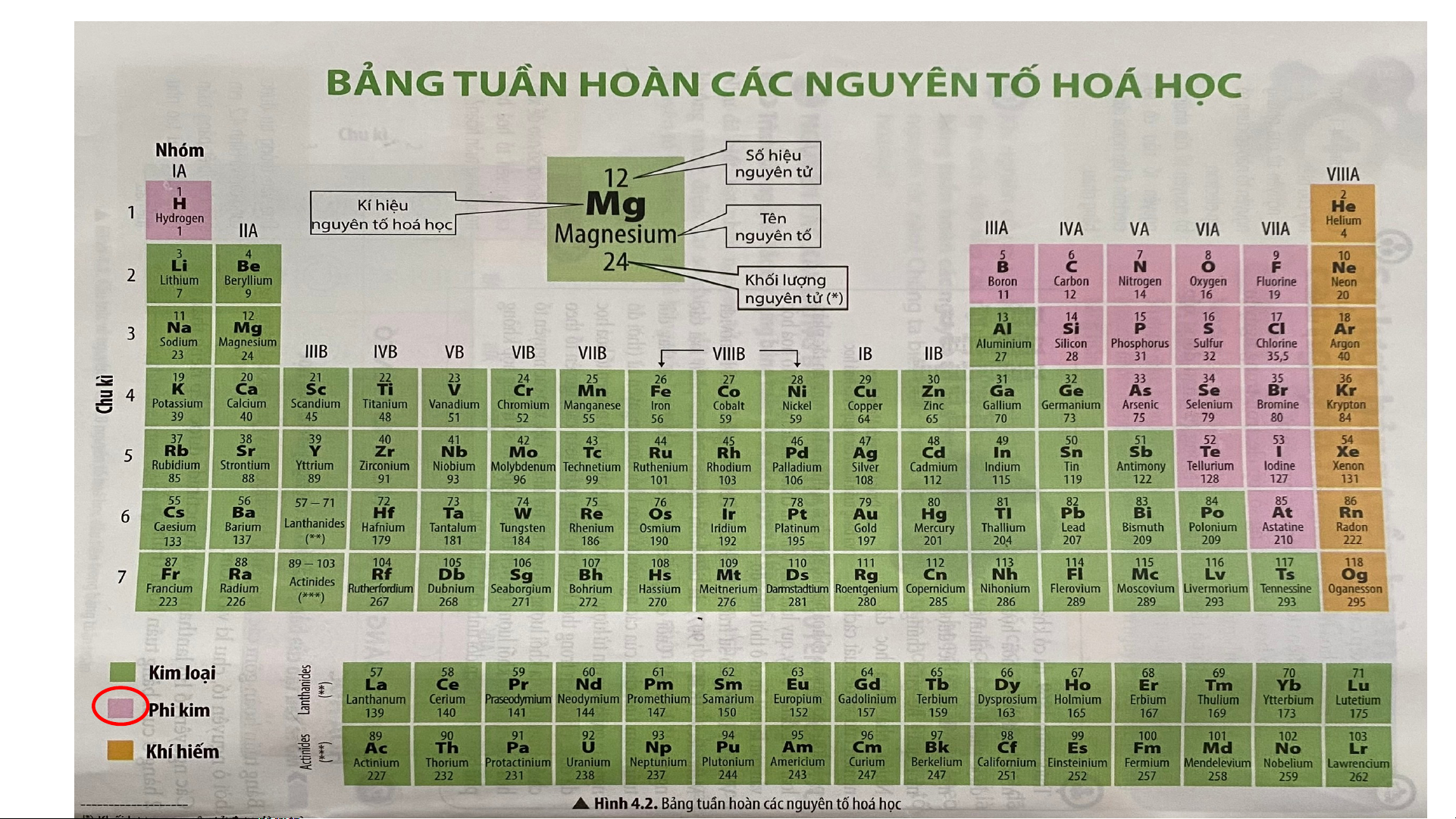
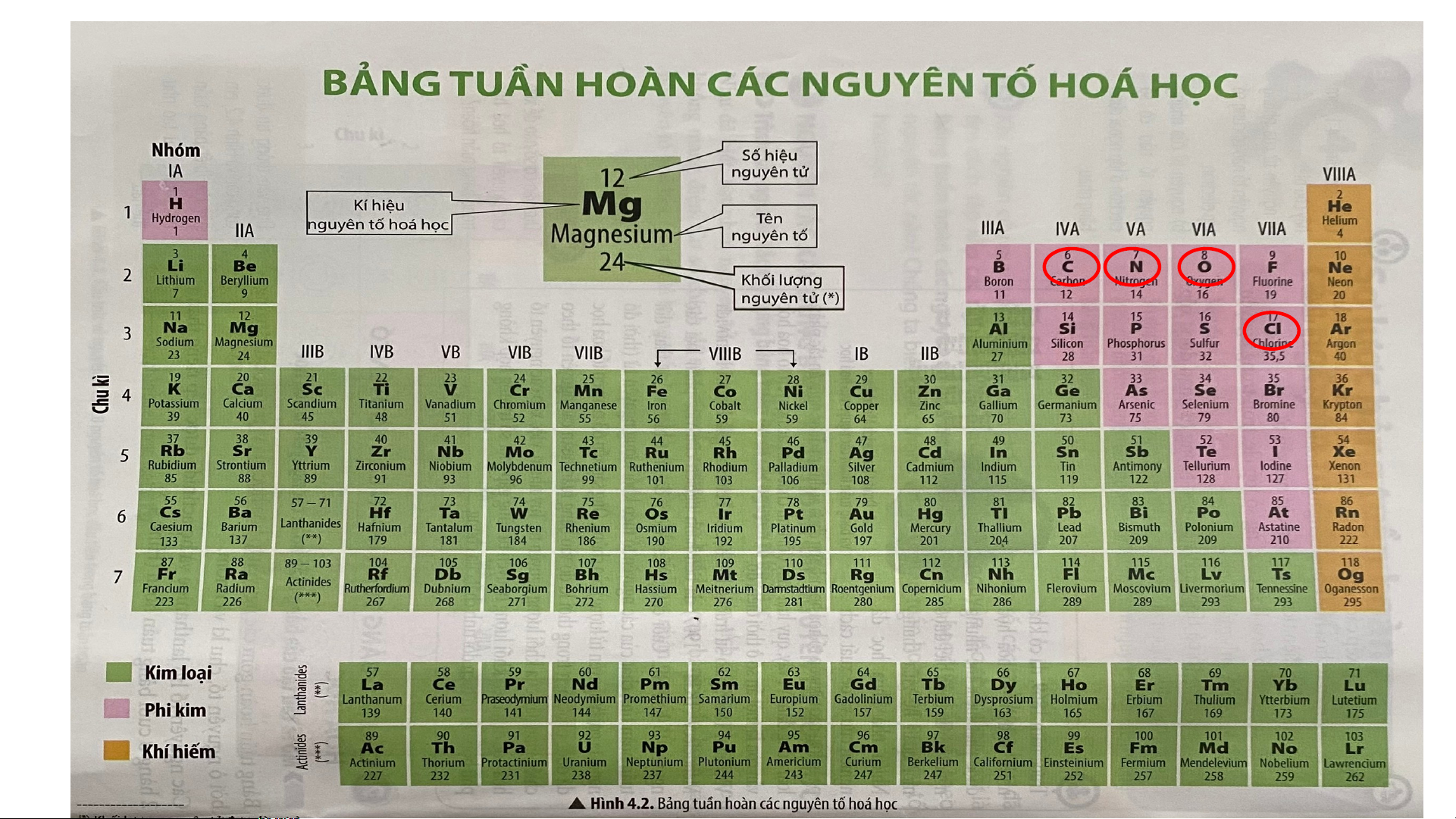
Các nguyên tố phi kim bao gồm:
+ Nguyên tố hydrogen ở nhóm IA
+ Một số nguyên tố nhóm IIIA và IVA
+ Hầu hết các nguyên tố thuộc nhóm VA, VIA và VIIA.
3. Các nguyên tố kim loại
a. Tìm hiểu các nguyên tố kim loại nhóm A
b. Tìm hiểu các nguyên tố kim loại nhóm B
c. Tìm hiểu các nguyên tố phi kim
d. Các nguyên tố khi hiếm:
Nhóm cuối cùng trong bảng tuần hoàn là
nhóm các nguyên tố khí hiếm (nhóm VIIIA). BÀI TẬP VỀ NHÀ
- Làm bài tập 4,5,6 sách giáo khoa, bài tập 2.10; 2.11; 2.12 sách bài tập.
- Đọc trước bài 5: Phân tử, đơn chất, hợp chất. 61
Cảm ơn quý thầy, cô cùng các em đã lắng nghe
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50
- Slide 51
- Slide 52
- Slide 53
- Slide 54
- Slide 55
- Slide 56
- Slide 57
- Slide 58
- Slide 59
- Slide 60
- Slide 61
- Slide 62




