


































Preview text:
Daï Hoï y c toá toá KHOA HỌC TỰ NHIÊN 7 t t
Hàng chục triệu chất trên Trái
Đất đều được tạo nên từ một
hoặc nhiều nguyên tố hóa học .
Các nhà khoa học đã phân loại chúng như thế nào?
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử:
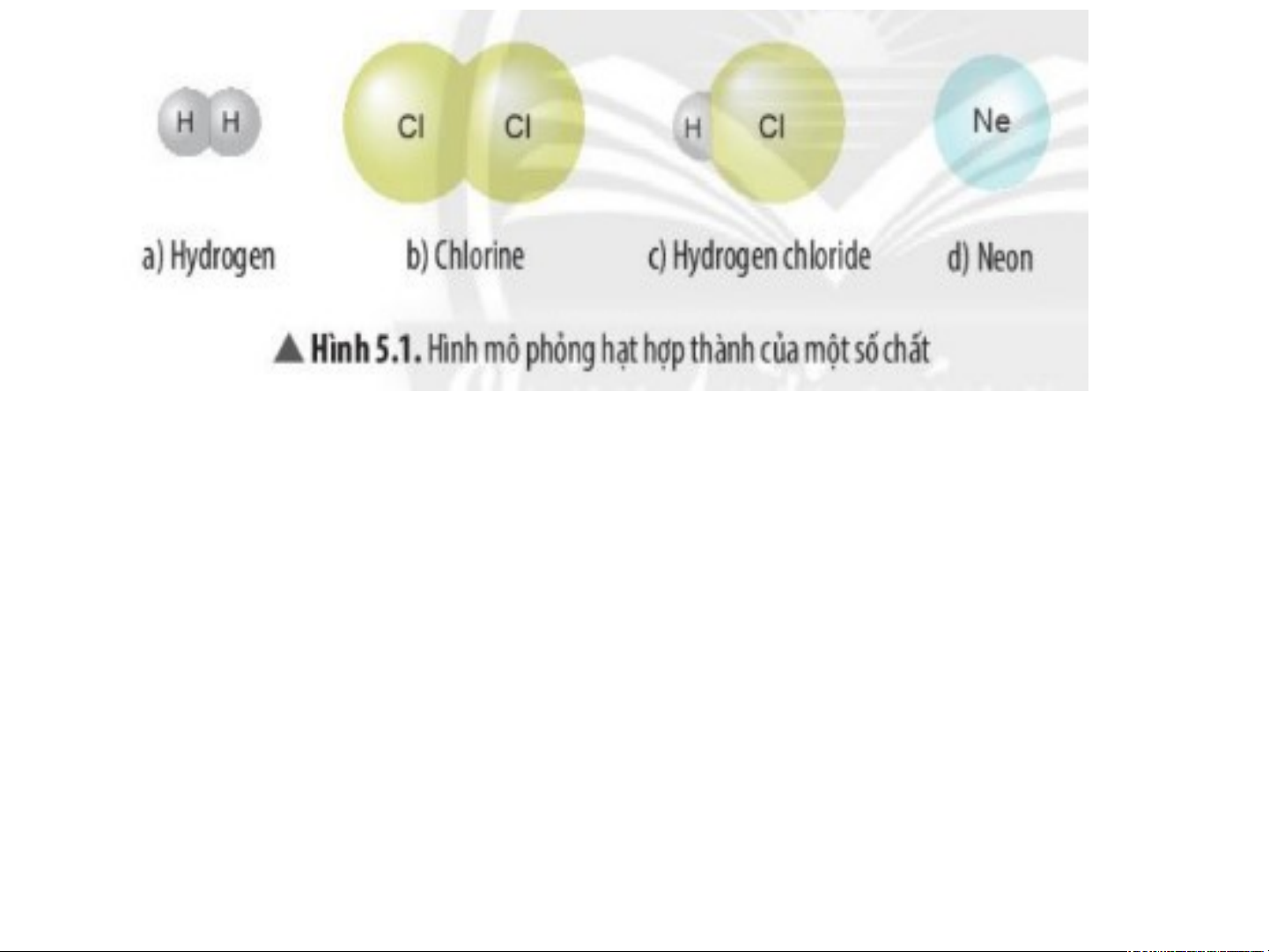
Quan sát Hình 5.1 và cho biết hạt hợp thành của chất nào
được tạo từ một nguyên tố hoá học. Hạt hợp thành của
chất nào được tạo từ nhiều nguyên tố hoá học?
+ Hạt hợp thành của chất được tạo từ một nguyên tố hoá
học là Hydrogen; Chlorine; Neon.
+ Hạt hợp thành của chất được tạo từ nhiều nguyên tố hoá học là Hydrogen chloride. Ví dụ: Các hạt hợp thành của
nước đều gồm 2 nguyên tử hydrogen và 1 nguyên O H tử oxygen. Nước O Khí Oxygen Muối ăn Thảo luận nhóm (5p)
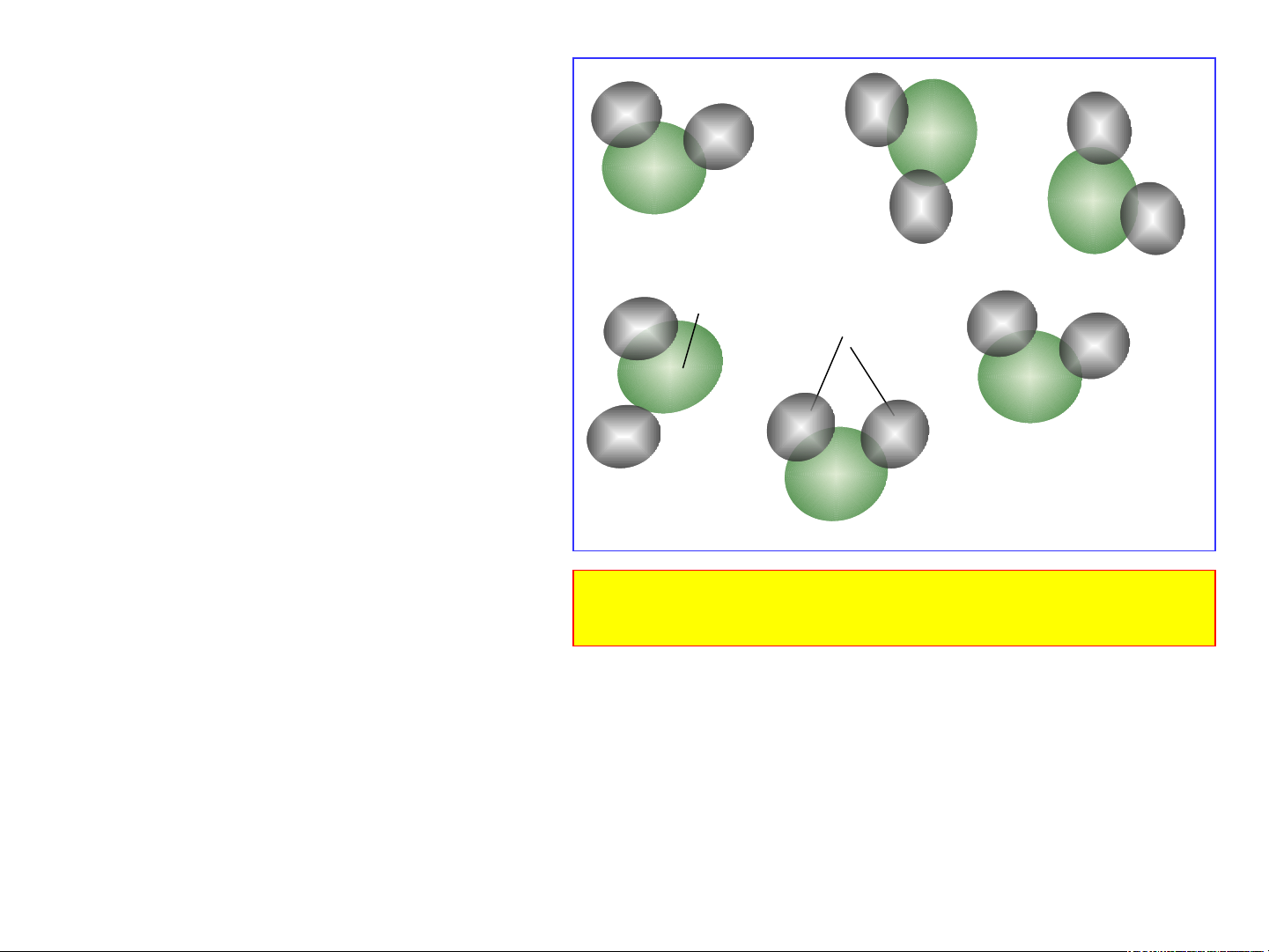
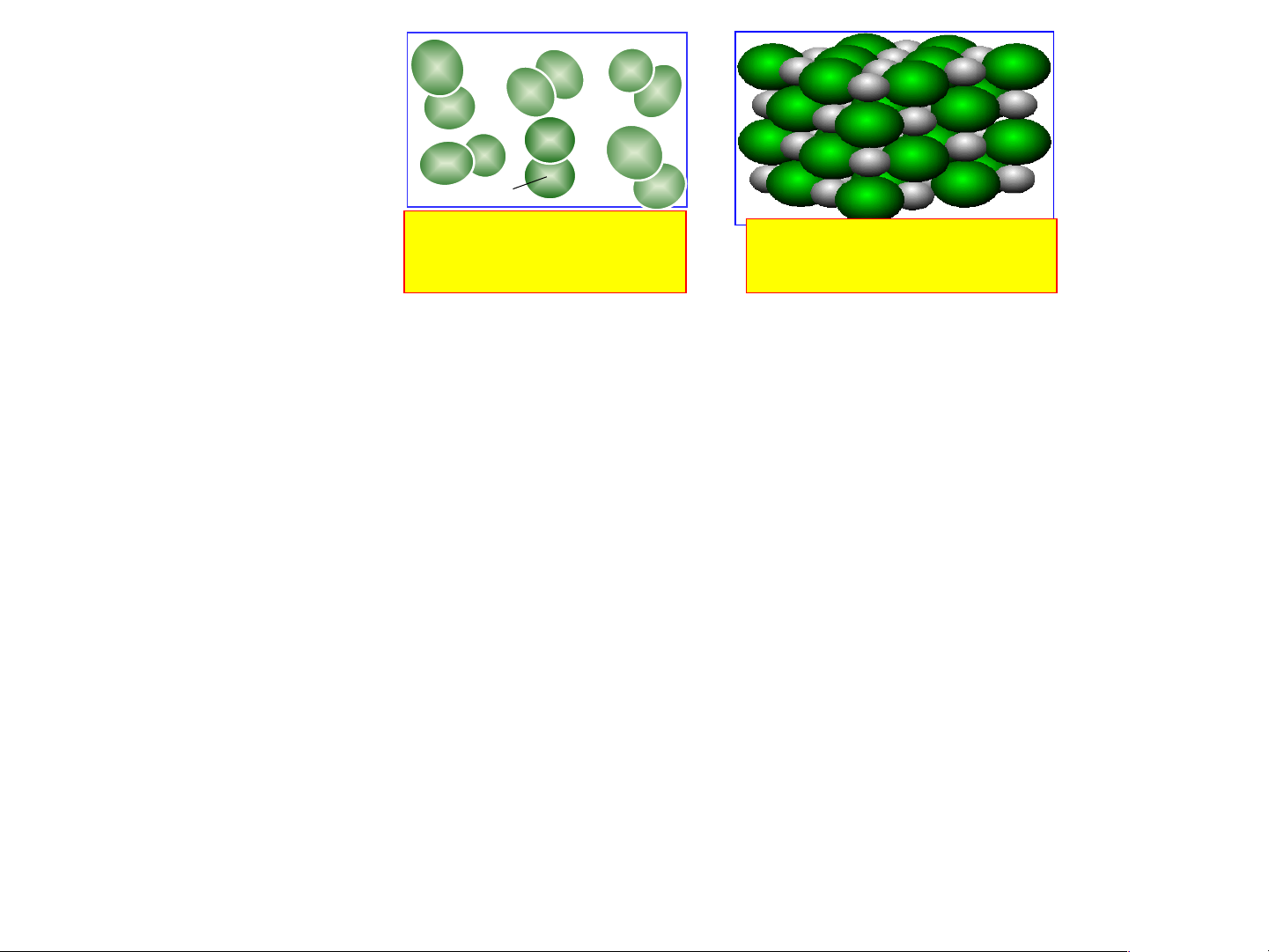
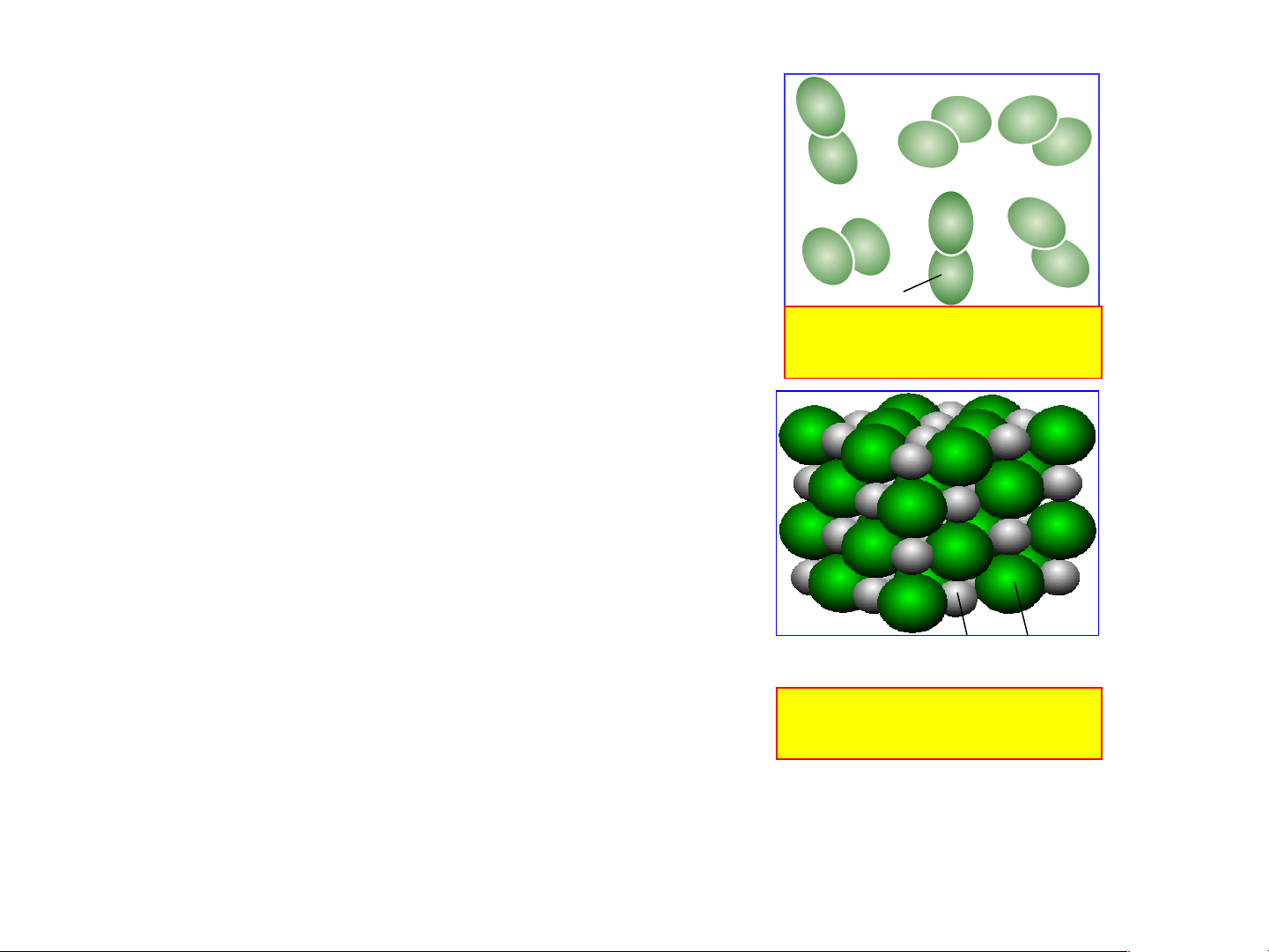
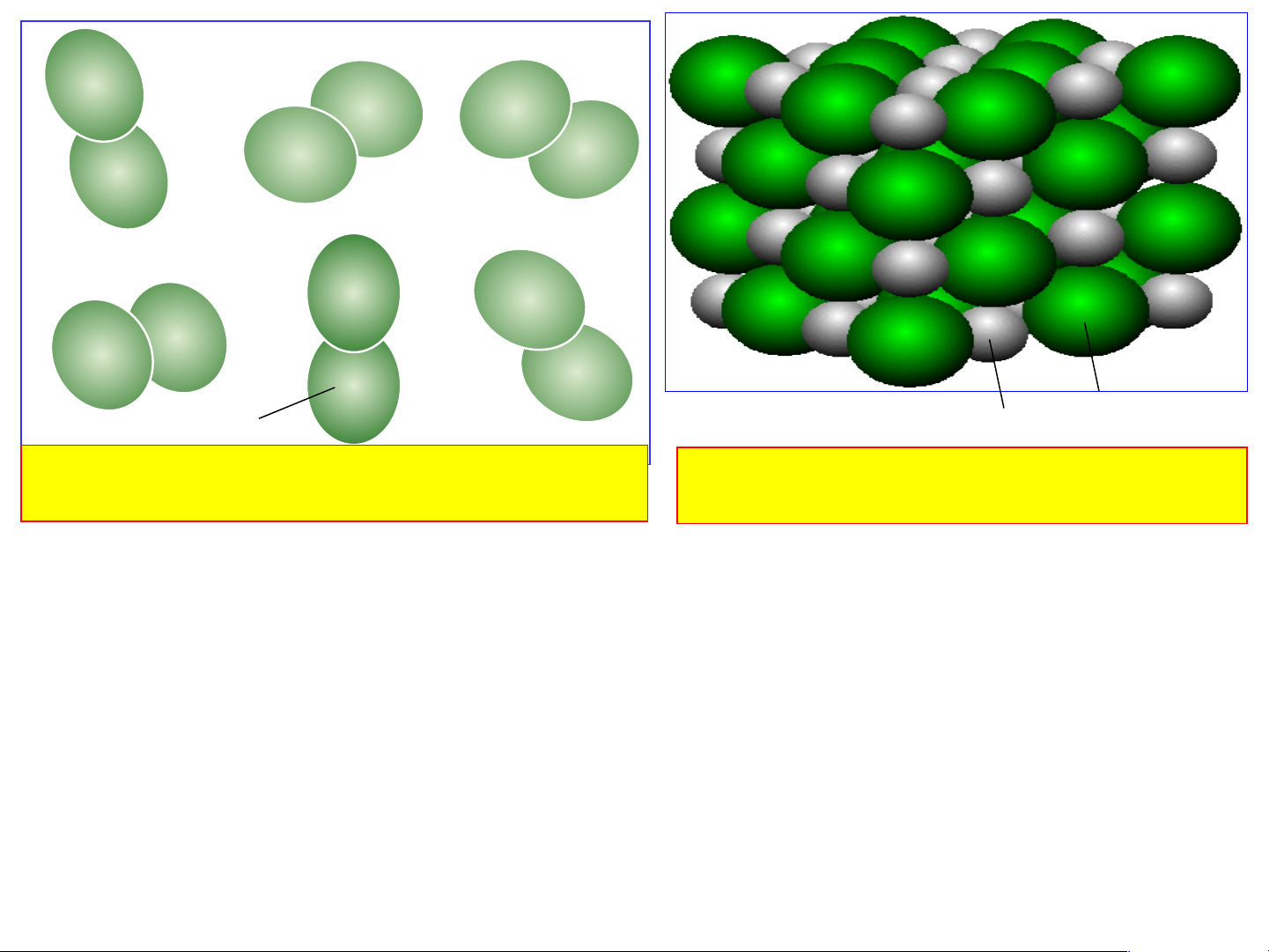
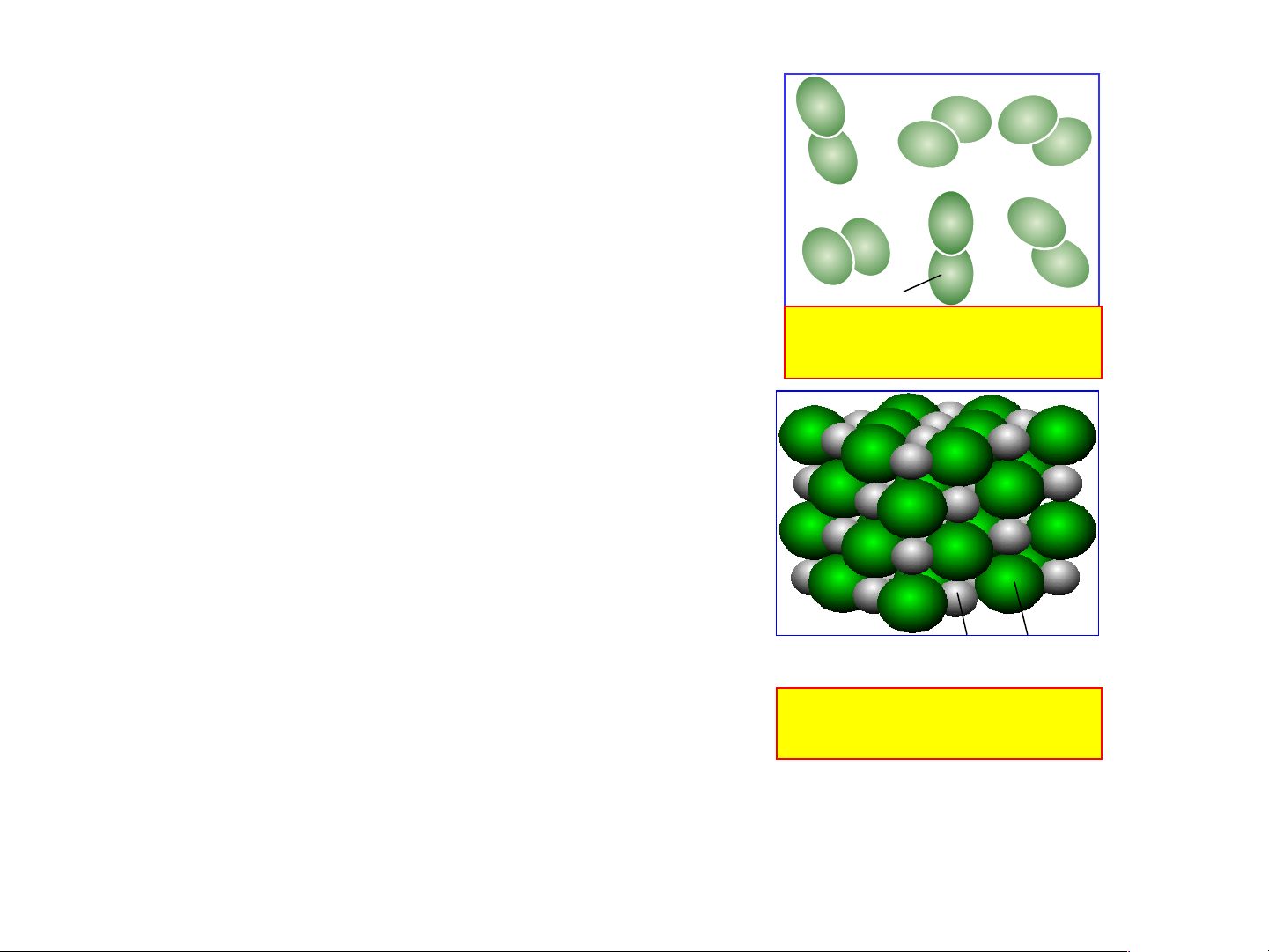
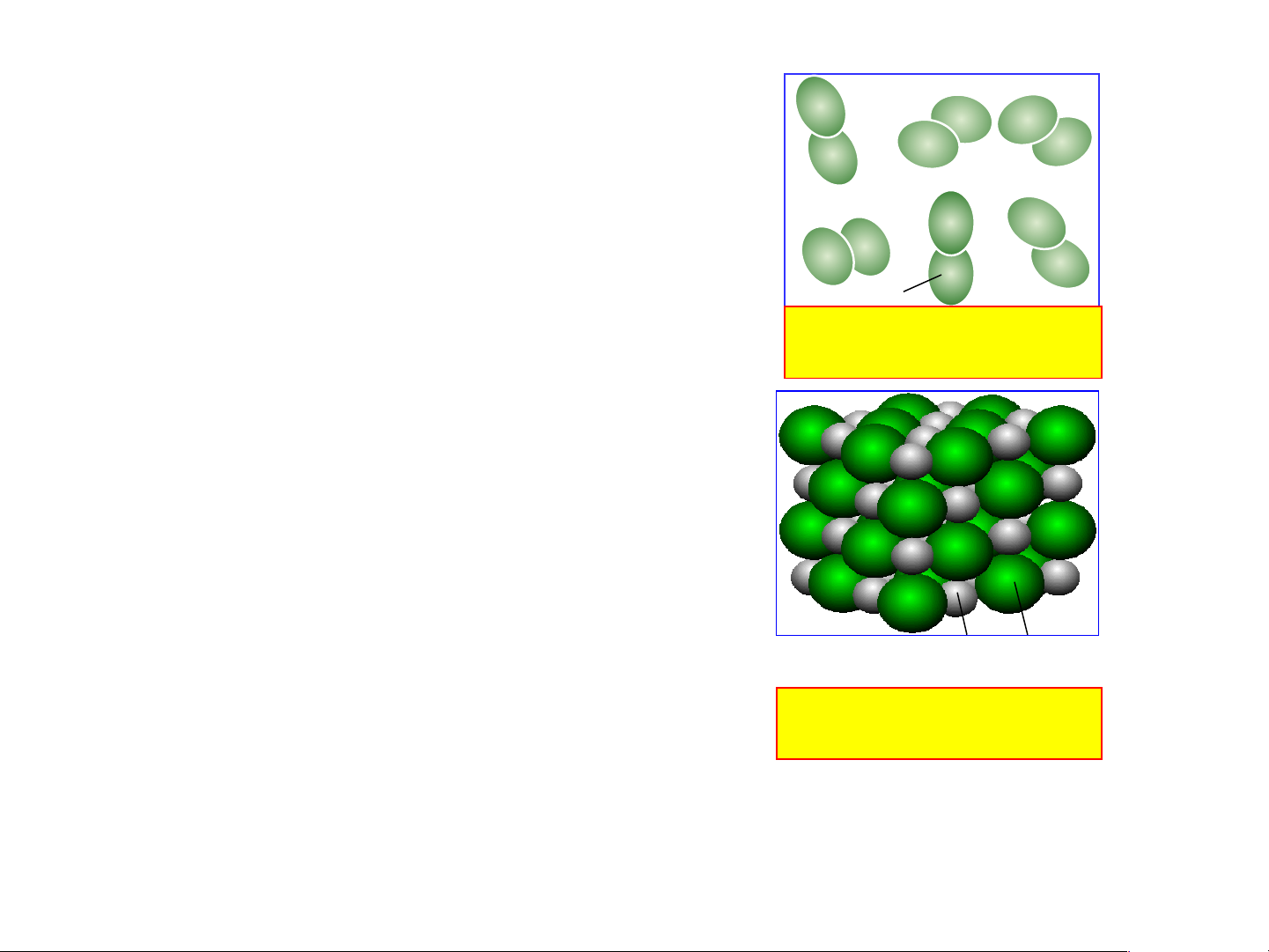
- Quan sát hình và cho biết: khí Oxygen, Muối ăn có
hạt hợp thành từ những nguyên tử nào?
- Từ hình em hãy nêu nhận xét về hình dạng, kích
thước, thành phần của các hạt hợp thành mẫu chất trên?
- Trong các mẫu chất trên, tính chất hóa học của các
hạt hợp thành chất có giống nhau không? Tại sao? - Quan sát hình và cho biết khí Oxygen, Muối
ăn có hạt hợp thành từ O
những nguyên tử nào? Khí Oxygen NaCl Muối ăn O Na Cl Khí Oxygen Muối ăn
Khí Oxygen có hạt hợp
Muối ăn có hạt hợp thành
thành gồm 2O liên kết với gồm 1 Na liên kết với 1 Cl nhau - Từ hình em hãy nêu
nhận xét về hình dạng,
kích thước, thành phần O
của các hạt hợp thành Khí Oxygen mẫu chất trên?
Các hạt hợp thành của mẫu
chất trên đều giống nhau về NaCl
hình dạng, kích thước, thành phần. Muối ăn
- Trong mẫu chất trên, tính
chất hóa học của các hạt
hợp thành chất có giống nhau không? Tại sao? O Khí Oxygen
Tính chất hóa học của các hạt
hợp thành chất giống nhau.
Vì chúng có hình dạng, kích
thước và thành phần cấu tạo NaCl giống nhau. Muối ăn
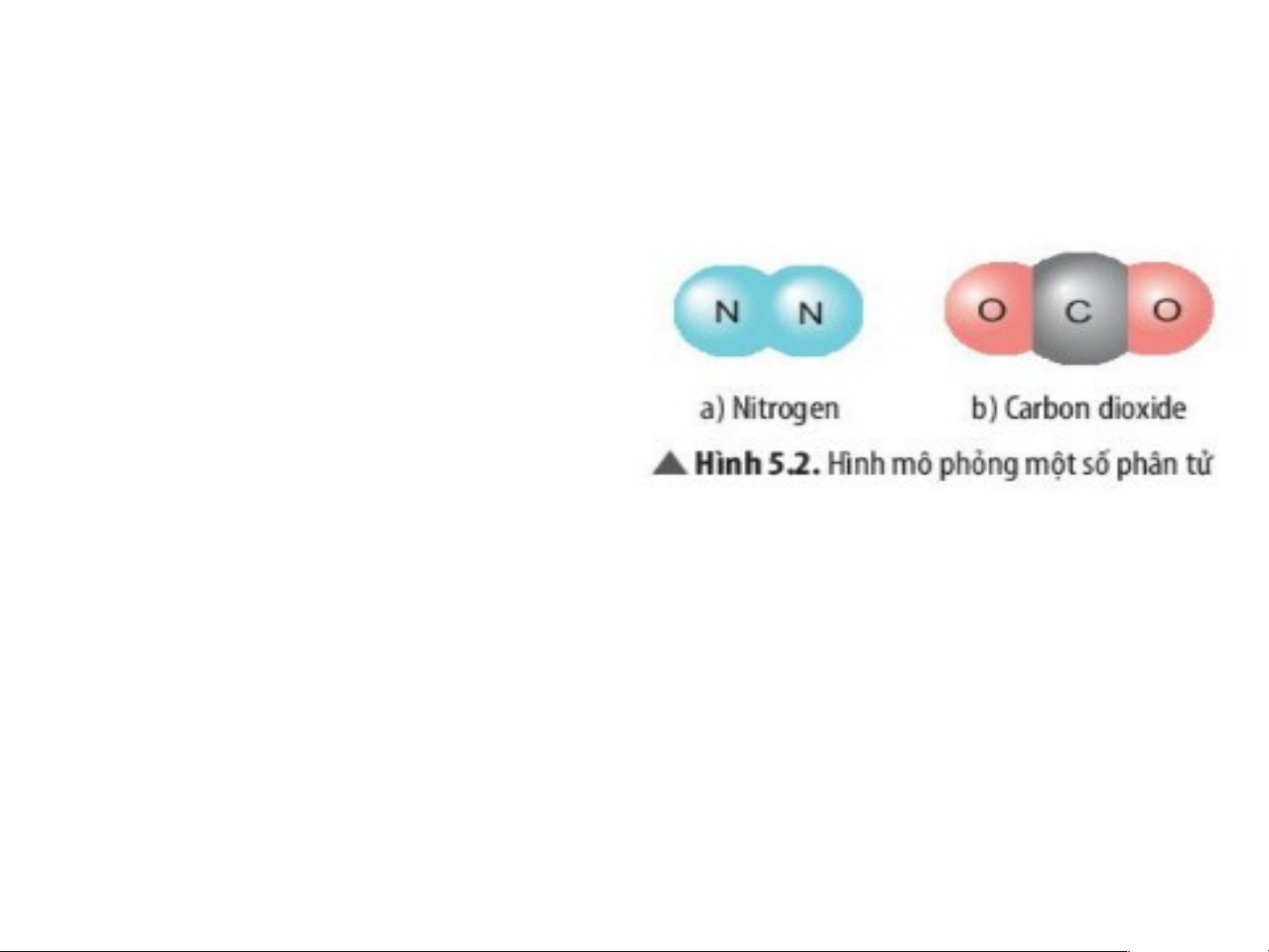
Tương tự kết quả ở các ví dụ trên, em hãy mô tả một
số phân tử được tạo thành từ một nguyên tố hóa học,
hai nguyên tố hóa học? Phân tử gồm có mấy dạng?
+ Phân tử được tạo thành từ một
nguyên tố hóa học: phân tử nitrogen, …
+ Phân tử được tạo thành từ 2
nguyên tố hóa học, phân tử cacbondioxide, …
+ Phân tử gồm 2 dạng là:
* phân tử tạo bởi một nguyên tố.
* phân tử tạo bởi hai nguyên tố.
- Thế nào là phân tử? Lấy ví dụ?
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử:
- Phân tử là hạt đại diện cho chất, gồm một số nguyên tử kết
hợp với nhau và thể hiện đầy đủ tích chất hóa học của chất.
- Phân tử được tạo thành từ một nguyên tố hóa học:
Ví dụ: phân tử chlorine (Cl ); phân tử nitrogen (N ); Phân tử 2 2 Oxygen (O ). 2
- Phân tử được tạo thành từ 2 nguyên tố hóa học:
Ví dụ: phân tử Hydrogen chlorine (HCl); phân tử cacbon dioxide (CO ). 2
- Vận dụng: Có nhiều loại bình chữa
cháy, hình bên là một loại bình chữa
cháy chứa chất khí đã được hóa lỏng.
Loại bình này dùng để dập tắt hiệu
quả các đám cháy nhỏ, nơi kín gió.
Ưu điểm của nó là không lưu lại chất
chữa cháy trên đồ vật.
Theo em, trong bình có chứa phân tử
chất khí gì? Phân tử đó gồm những
nguyên tố nào? Số lượng nguyên tử
của mỗi nguyên tố có trong phân tử
chất khí này là bao nhiêu?
- Khí trong bình chữa cháy là
carbon dioxide (CO ). Phân tử 2
CO gồm 2 nguyên tố: carbon và 2 oxygen.
- Phân tử carbon dioxide (CO ) 2
gồm 1 nguyên tử carbon và 2 nguyên tử oxygen.
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử:
- Phân tử là hạt đại diện cho chất, gồm một số nguyên tử kết
hợp với nhau và thể hiện đầy đủ tích chất hóa học của chất.
- Phân tử được tạo thành từ một nguyên tố hóa học:
Ví dụ: phân tử chlorine (Cl ); phân tử nitrogen (N ); Phân tử 2 2 Oxygen (O ). 2
- Phân tử được tạo thành từ 2 nguyên tố hóa học:
Ví dụ: phân tử Hydrogen chlorine (HCl); phân tử cacbon dioxide (CO ). 2. Khối lượng ph 2 ân tử:
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử:
2. Khối lượng phân tử:
Khối lượng phân tử bằng tổng khối lượng các nguyên tử có trong phân tử.
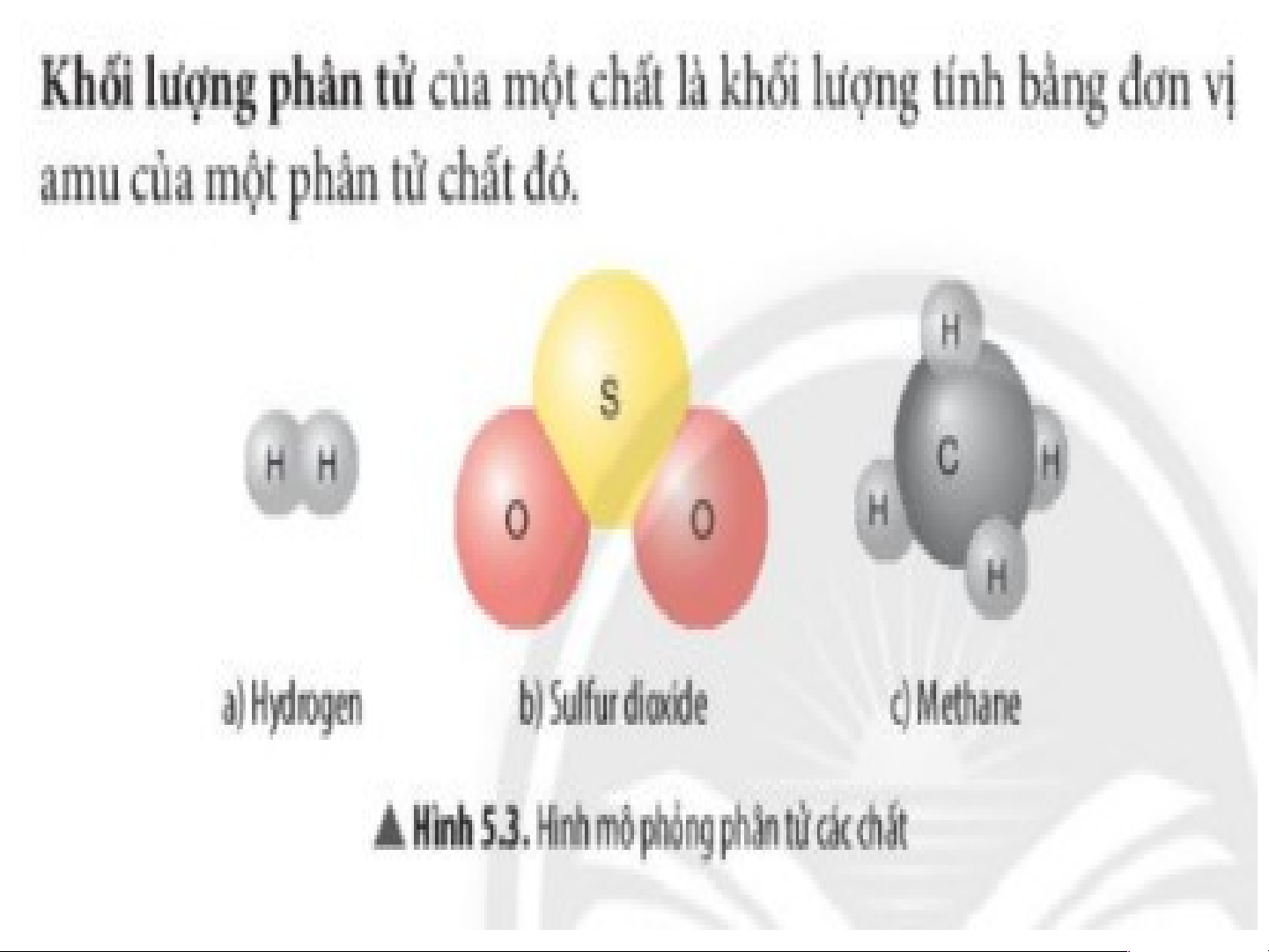
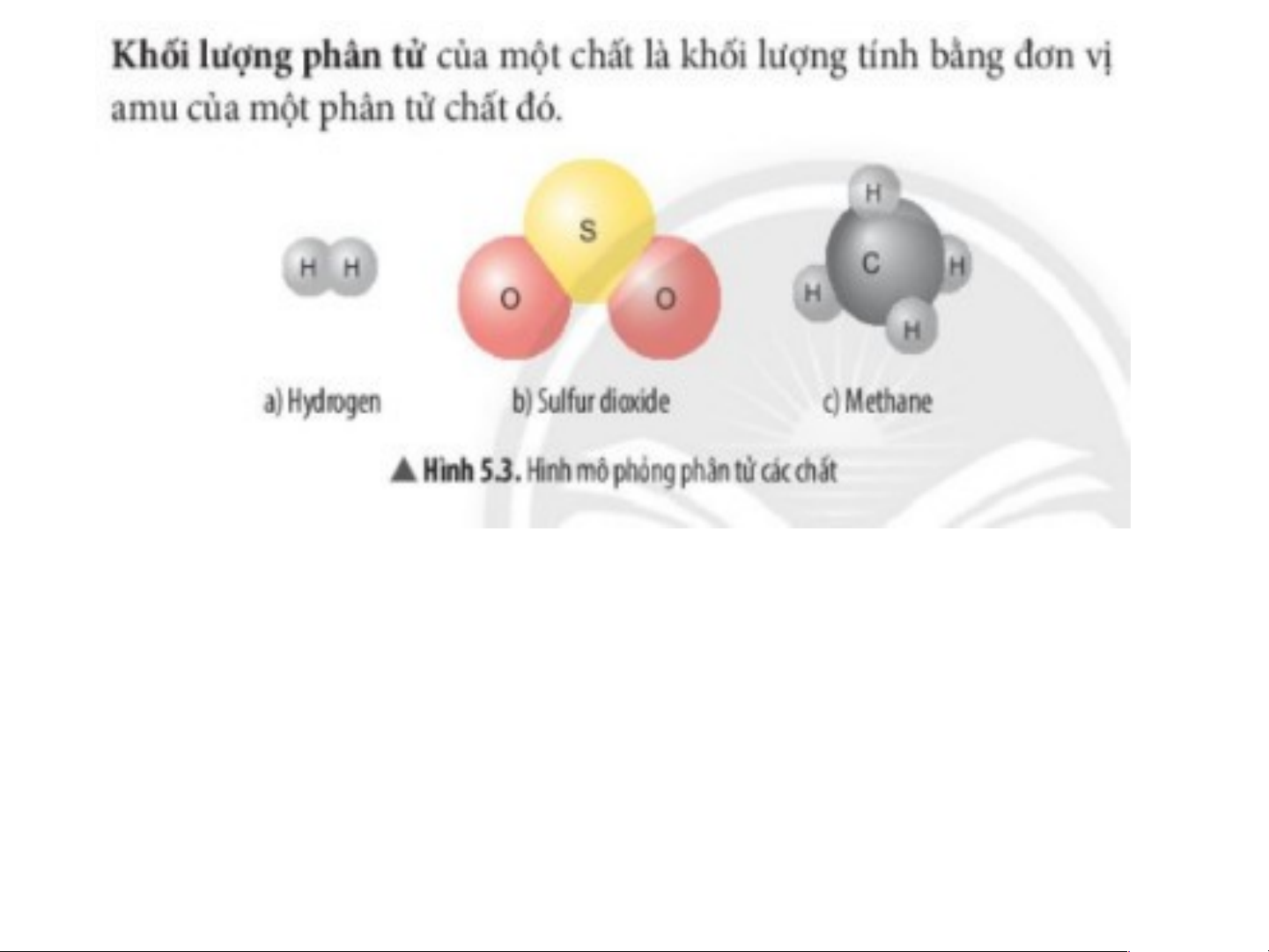
- Em hãy đề xuất cách tính khối lượng phân tử của mỗi chất ở H 5.3?
Khối lượng phân tử sẽ bằng tổng khối lượng các nguyên tử có trong phân tử. Theo đó:
Phân tử hydrogen: KLPT (H ) = 1 . 2 = 2 (amu). 2
Phân tử sulfur dioxide : KLPT (SO ) = 32 + 16 . 2 = 64 (amu). 2
Phân tử methane: KLPT (CH ) = 12 + 1 . 4 = 16 (amu). 4
- Khối lượng nguyên tử của oxygen bằng 16 amu.
Phân tử khí oxygen gồm 2 nguyên tử oxygen sẽ có
khối lượng bằng bao nhiêu?
Phân tử khí oxygen gồm 2 nguyên tử oxygen KLPT (O ) = 16 . 2 = 32 (amu). 2
- Khối lượng phân tử của một chất là khối lượng tính
bằng đơn vị amu của một phân tử chất đó.
- Cách tính khối lượng phân tử
Bước 1: Xác định số lượng nguyên tử của mỗi nguyên tố trong phân tử.
Bước 2: Tính khối lượng phân tử
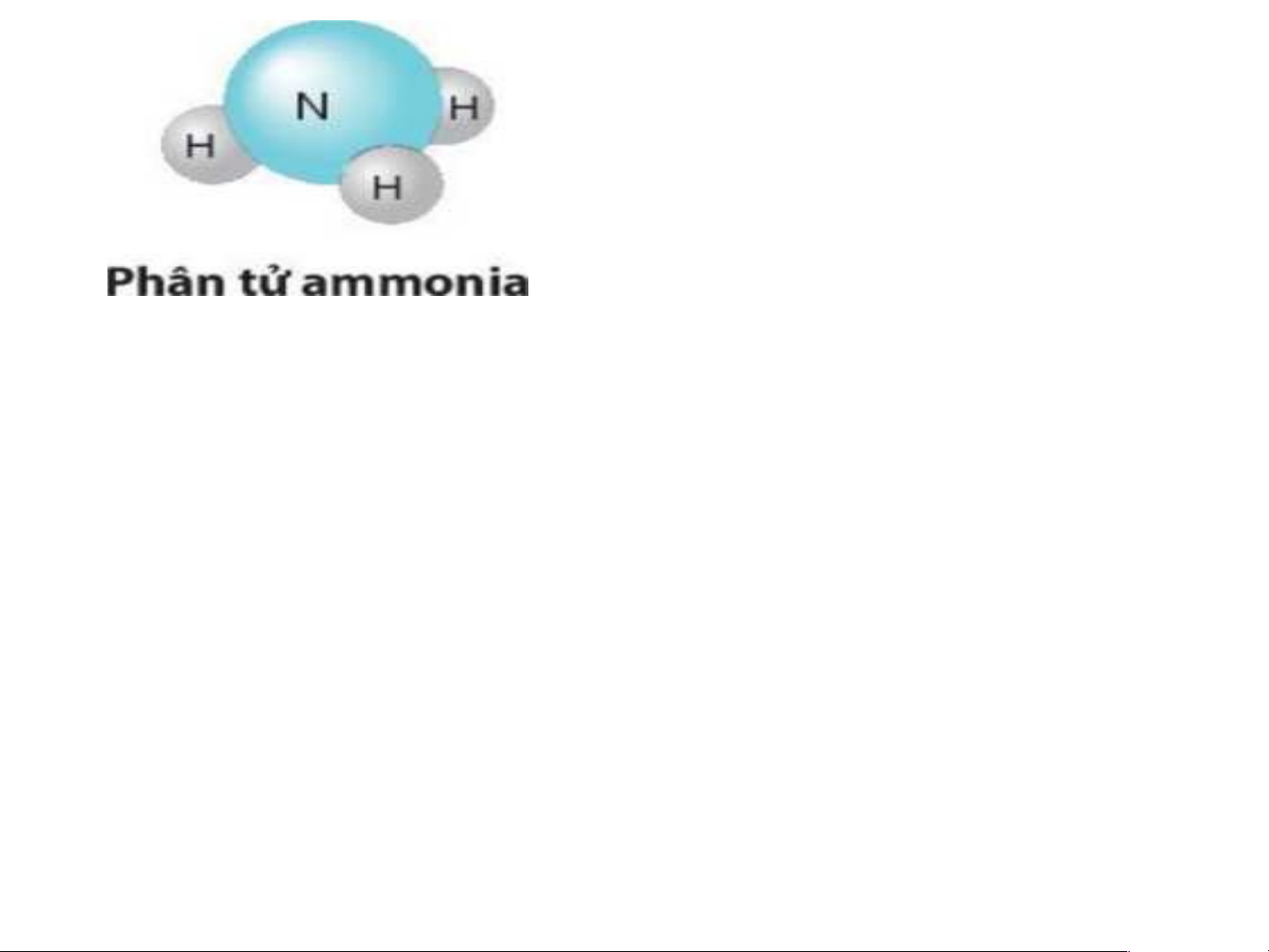
Ví dụ: tính khối lượng phân tử ammonia
Phân tử ammonia gồm 1 nguyên tử N và 3 nguyên tử H
KLPT (NH ) = 14.1 + 1.3 = 17 (amu) 3
Ví dụ: tính khối lượng phân tử ammonia
Phân tử ammonia gồm 1 nguyên tử N và 3 nguyên tử H
KLPT (NH ) = 14.1 + 1.3 = 17 (amu) 3
Vận dụng: Muối ăn có thành phần chính là sodium
chloride. Phân tử sodium chlorine gồm 1 nguyên tử
sodium và 1 nguyên tử chlorine. Em hãy tính khối
lượng phân tử của sodium chlorine.
KLPT (NaCl) = 23.1 + 35,5.1 = 58,5 (amu)
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử:
2. Khối lượng phân tử:
Khối lượng phân tử bằng tổng khối lượng các nguyên tử có trong phân tử.
Ví dụ: - KLPT ammonia (NH ) = 14.1 + 1.3 = 17 (amu) 3
- KLPT sodium chlorine (NaCl) = 23.1 + 35,5.1 = 58,5 (amu)
KLPT (CaCO ) = 40.1 + 12.1+ 16.3 = 100 (amu) 3
Vận dụng: Trong nước rửa tay khô có thành phần
chính là chất gì? Khối lượng phân tử của chất đó là bao nhiêu?
- Thành phần chính trong nước rửa tay khô là ethyl
alcohol (ancol etylic) (C H OH) 2 5
- KLPT ancol etylic (C H OH) = 2 5
12 . 2 + 1 . 5 + 16 + 1 = 46 (amu)
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử 2. Khối lượng phân tử II. Đơn chất:
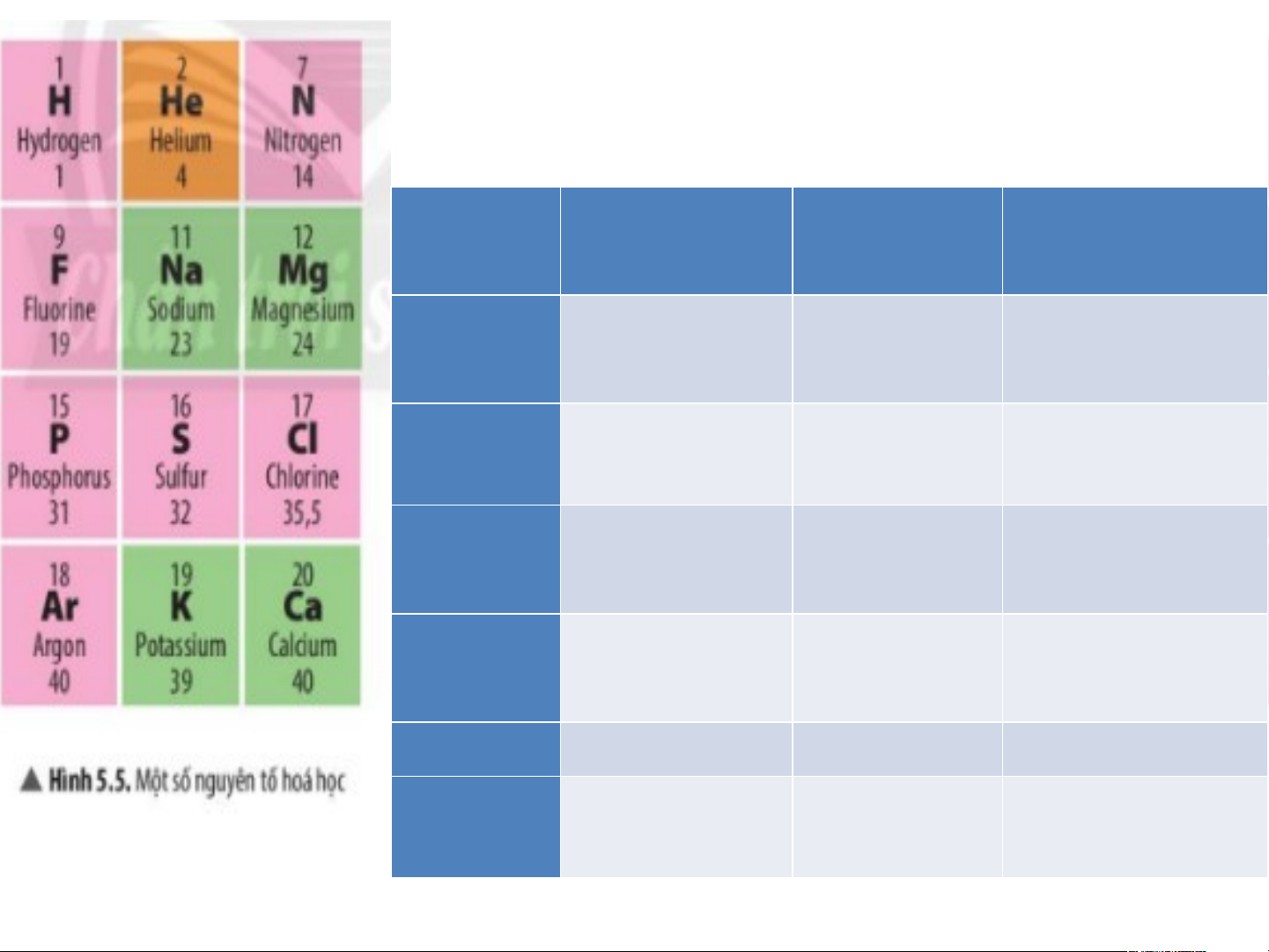
Dựa vào Hình 5.5, cho biết tên các
đơn chất được tạo nên từ nguyên tố hoá học tương ứng? Nguyên Đơn chất - Đơn chất - Tên tố Tên đơn chất Nguyên tố đơn chất H - Khí 2 H hydrogen P P - Phosphorus He - Khí He helium S S - Sulfur N - Khí Cl - Khí 2 2 N nitrogen Cl chlorine F - Khí 2 F fluorine Ar Ar - Khí argon Na Na - Sodium K K - Potassium Mg - Mg Magnesium Ca Ca - Calcium
- Ngoài các đơn chất tạo từ các nguyên tố ở Hình 5.5, em
hãy liệt kê thêm 2 đơn chất tạo thành từ nguyên tố kim
loại và 2 đơn chất tạo thành từ nguyên tố phi kim khác?
2 đơn chất tạo bởi nguyên tố kim loại: Al (aluminium), Fe (iron).
2 đơn chất tạo bởi nguyên tố phi kim: C (carbon), O (khí 2 oxygen).
- Quan sát Hình 5.6, em hãy cho biết số nguyên tử và thành
phần nguyên tố có trong mỗi phân tử đơn chất?
Số nguyên tử và thành phần nguyên tố có trong mỗi phân tử đơn chất ở H 5.6 là
(a) gồm 2 nguyên tử Br (b) gồm 3 nguyên tử O.
Các phân tử đơn chất này đều chỉ tạo từ một nguyên tố hoá học.
- Thế nào là đơn chất? Lấy ví dụ?
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử 2. Khối lượng phân tử II. Đơn chất :
Đơn chất là chất được tạo từ một nguyên tố hoá học.
Ví dụ: - Đơn chất một nguyên tử: Ca; Mg; Fe; …
- Đơn chất nhiều nguyên tử : O ; N ; H ; O ; … 2 2 2 3
- Các mẫu vật: cuộn dây nhôm, lưu huỳnh, than gỗ
được tạo ra từ phân tử đơn chất.
+ Đơn chất nhôm được tạo thành từ nguyên tố nhôm.
+ Đơn chất lưu huỳnh được tạo thành từ nguyên tố lưu huỳnh.
+ Than gỗ được tạo thành từ nguyên tố carbon.
+ Đá vôi không phải là đơn chất vì được tạo thành từ
3 nguyên tố là calcium, carbon, oxygen.
CHỦ ĐỀ 2: PHÂN TỬ
BÀI 5- PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT: I. Phân tử: 1. Khái niệm phân tử 2. Khối lượng phân tử II. Đơn chất: III. Hợp chất: - Quan sát Hình 5.7, em hãy cho biết phân
tử chất nào là phân tử
đơn chất, phân tử chất nào là phân tử hợp chất? Giải thích?
- Muối ăn (Hình 5.8) là đơn chất hay hợp chất? Vì sao?
- Phân tử đơn chất: Hydrogen; Oxygen Vì phân tử tạo nên
từ 1 nguyên tố hóa học.
- Phân tử hợp chất: Nước Vì phân tử tạo nên từ 2 (nhiều)
nguyên tố hóa học là Hydrogen và Oxygen.
- Muối ăn (H5.8) là hợp chất vì nó được tạo bởi từ nhiều
nguyên tố hoá học (gồm nguyên tố Na và nguyên tố Cl).
- Hãy nêu một số ví dụ về phân tử hợp chất mà em biết và cho biết
phân tử đó được tạo thành từ các nguyên tử của nguyên tố nào? Phân tử hợp chất Đặc điểm cấu tạo
1 nguyên tử carbon và 4 nguyên tử Khí methane hydrogen.
1 nguyên tử sulfur và 2 nguyên tử Sulfur dioxide oxygen.
- Thế nào là hợp chất? Lấy ví dụ?
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử 2. Khối lượng phân tử II. Đơn chất : III. Hợp chất :
Hợp chất là chất tạo nên từ 2 hay nhiều nguyên tố hóa học.
Ví dụ: Carbon dioxide (CO ); sulfur dioxide( SO ) ... 2 2
Vận dụng: Carbon dioxide là thành phần tạo ra
bọt khí trong nước giải khát có gas (hình
dưới). Theo em, carbon dioxide là đơn chất hay hợp chất?
Carbon dioxide (CO ) là hợp chất được tạo 2
thành từ 1 nguyên tử carbon và 2 nguyên tử oxygen.
CHỦ ĐỀ 2. PHÂN TỬ
BÀI 5. PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT I. Phân tử: 1. Khái niệm phân tử 2. Khối lượng phân tử II. Đơn chất : III. Hợp chất :
Hợp chất là chất tạo nên từ 2 hay nhiều nguyên tố hóa học.
Ví dụ: Carbon dioxide (CO ); sulfur dioxide( SO ) ... 2 2 Bài tập trang 36 Bài tập 1 trang 36
+ 5 đơn chất: Na, Ba; Al; K; Mg
+ 5 hợp chất chứa 2 nguyên tố: CO ; SO ; NaCl; CH ; H O 2 2 4 2 Bài tập 2 trang 36 Chất Phân tử
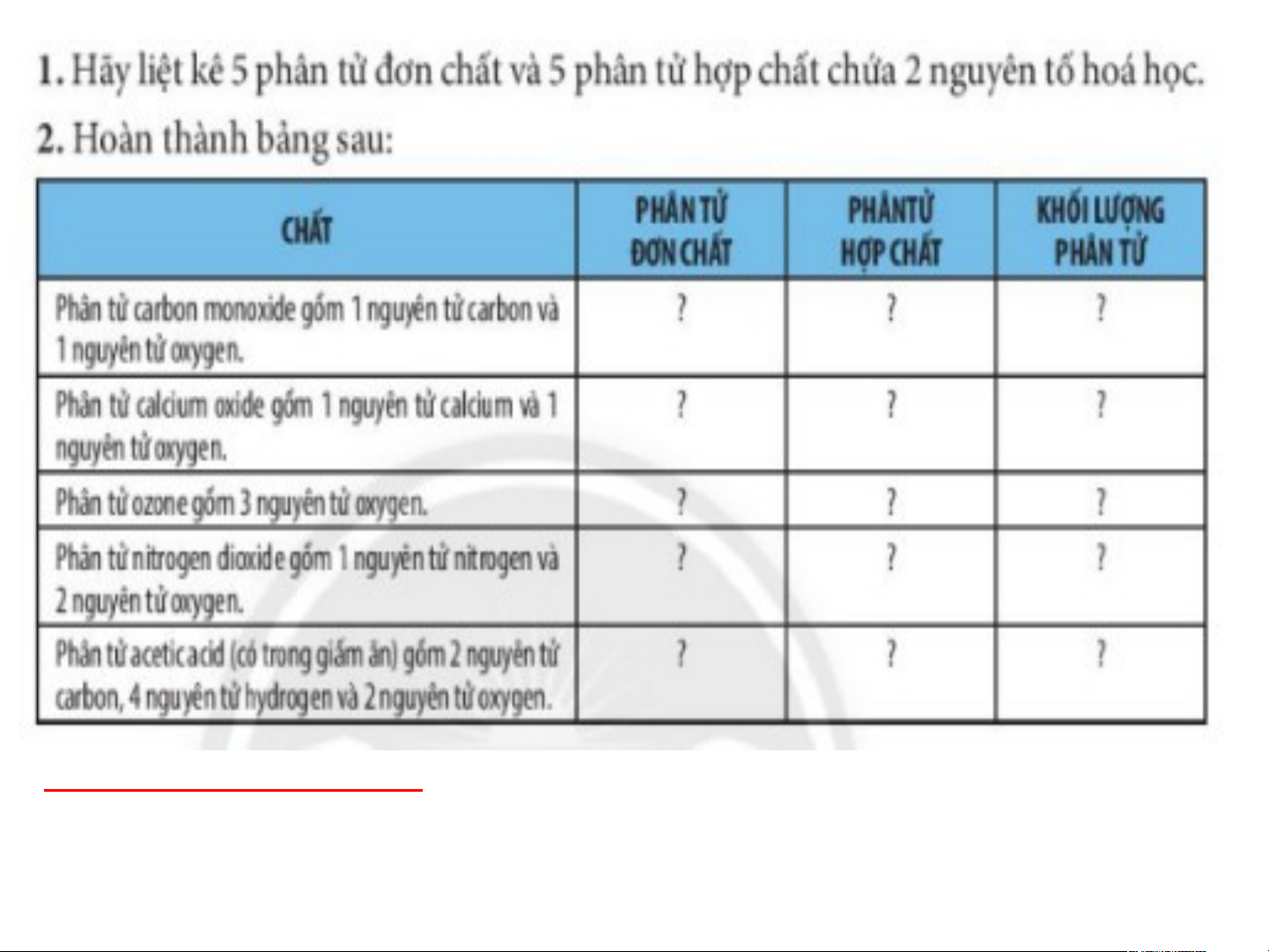
Phân tử hợp Khối lượng đơn chất chất phân tử
Phân tử cacbon monoxide gồm 1 nguyên tử x 28 amu
carbon và 1 nguyên tử oxygen.
Phân tử calcium oxide gồm 1 nguyên tử x 56 amu
calcium và 1 nguyên tử oxygen
Phân tử ozone gồm 3 nguyên tử oxygen x 48 amu
Phân tử nitrogen dioxide gồm 1 nguyên tử x 46 amu
nitrogen và 2 nguyên tử oxygen
Phân tử acetic acid (có trong giấm ăn) gồm x 60 amu
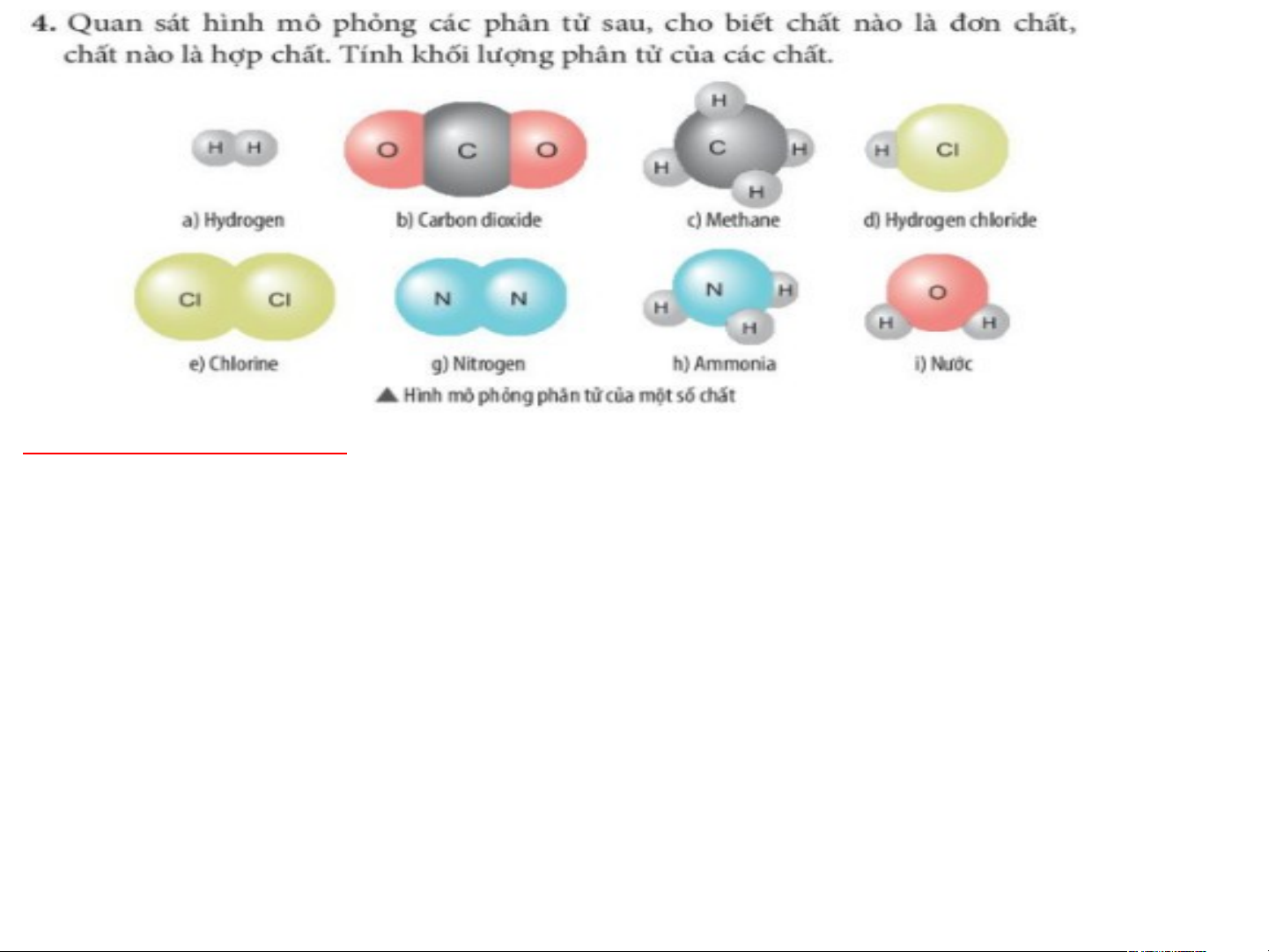
2 nguyên tử carbon, 4 nguyên tử hydrogen và 2 nguyên tử oxygen. Bài tập 4 trang 36
Đơn chất : + Hydrogen: KLPT(H )=1.2=2 amu 2
+ Chlorine: KLPT(Cl )=35,5.2=70 amu 2
+ Nitrogen: KLPT(N )=14.2=28 amu 2
Hợp chất : + Carbon dioxide: KLPT(CO )=12.1+16.2= 44 amu 2
+ Methane: KLPT(CH )= 12.1 + 1.4 =16 amu 4
+ Hydrogen chlorine: KLPT(HCl)=1.1+ 35,5.1= 36,5 amu
+ Amonia: KLPT(NH )= 14.1 + 1.3 =17 amu 3
+ Nước : KLPT(H O )=1.2+ 16.1= 18 amu 2 Bài tập 3 trang 36 Giải : a) Quan sát hình ta thấy: Baking soda được tạo bởi 4 nguyên tố: C, H, O, và X => Baking soda là phân tử hợp chất.
b) Quan sát hình ta thấy: phân tử baking soda có 1 nguyên tử X nên
KLPT (baking soda) = X.1 + 1.1 + 12.1 + 16.3 84 = X + 61 => X = 84 - 61 = 23 amu => X là Sodium (Na) HƯỚNG DẪN VỀ NHÀ
- Học bài 5: Phân tử - đơn chất – hợp chất
Đọc và nghiên cứu trước bài 6: Giới thiệu
về liên kết hóa học.
- Làm các bài tập trong Sách bài tập.
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- Slide 20
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32
- Slide 33
- Slide 34
- Slide 35
- Slide 36
- Slide 37
- Slide 38
- Slide 39
- Slide 40
- Slide 41
- Slide 42
- Slide 43
- Slide 44
- Slide 45
- Slide 46
- Slide 47
- Slide 48
- Slide 49
- Slide 50




