



















Preview text:
CHƯƠNG II
PHÂN TỬ - LIÊN KẾT HÓA HỌC BÀI 5
PHÂN TỬ - ĐƠN CHẤT – HỢP CHẤT
I. Đơn chất và hợp chất
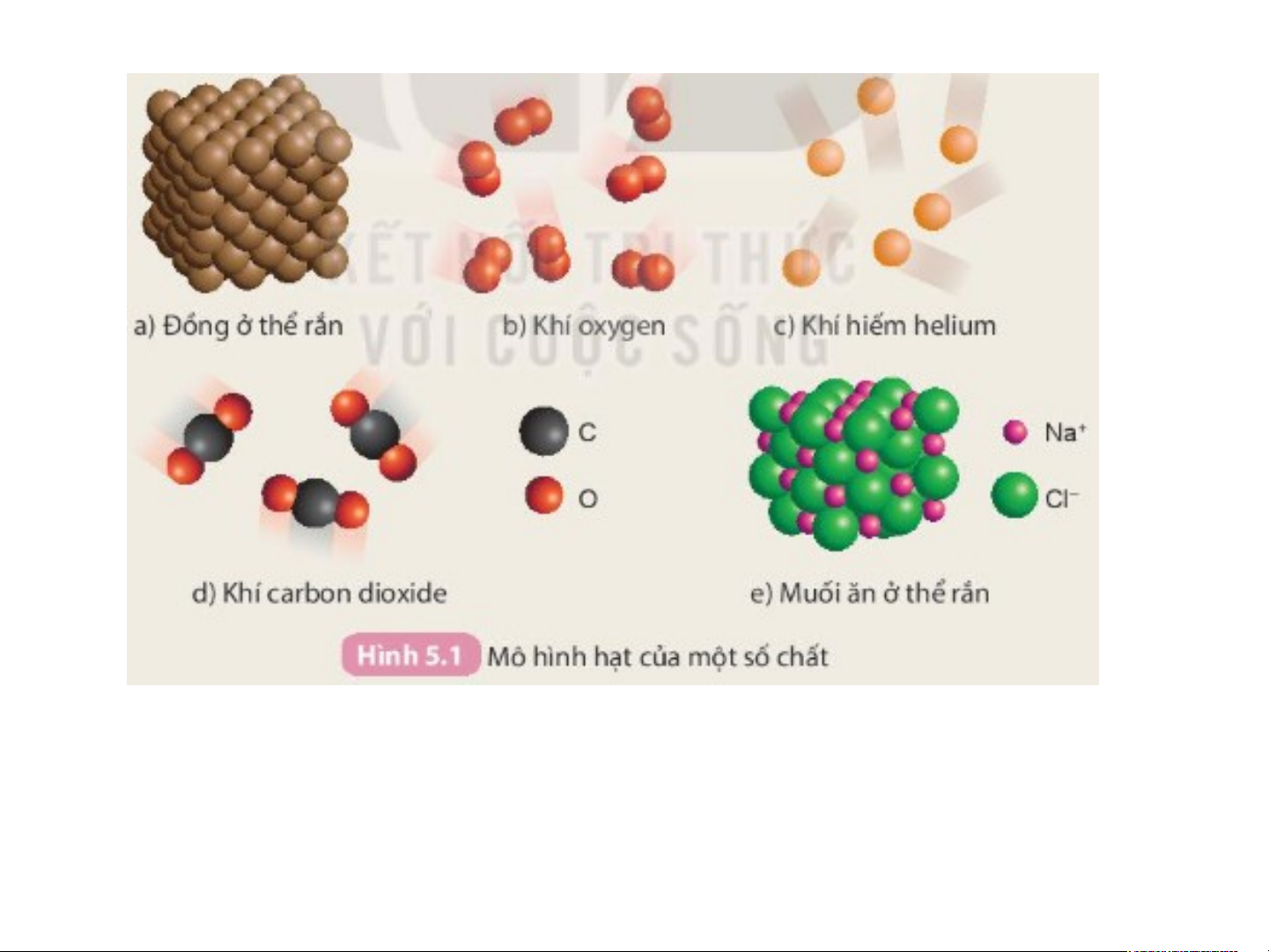
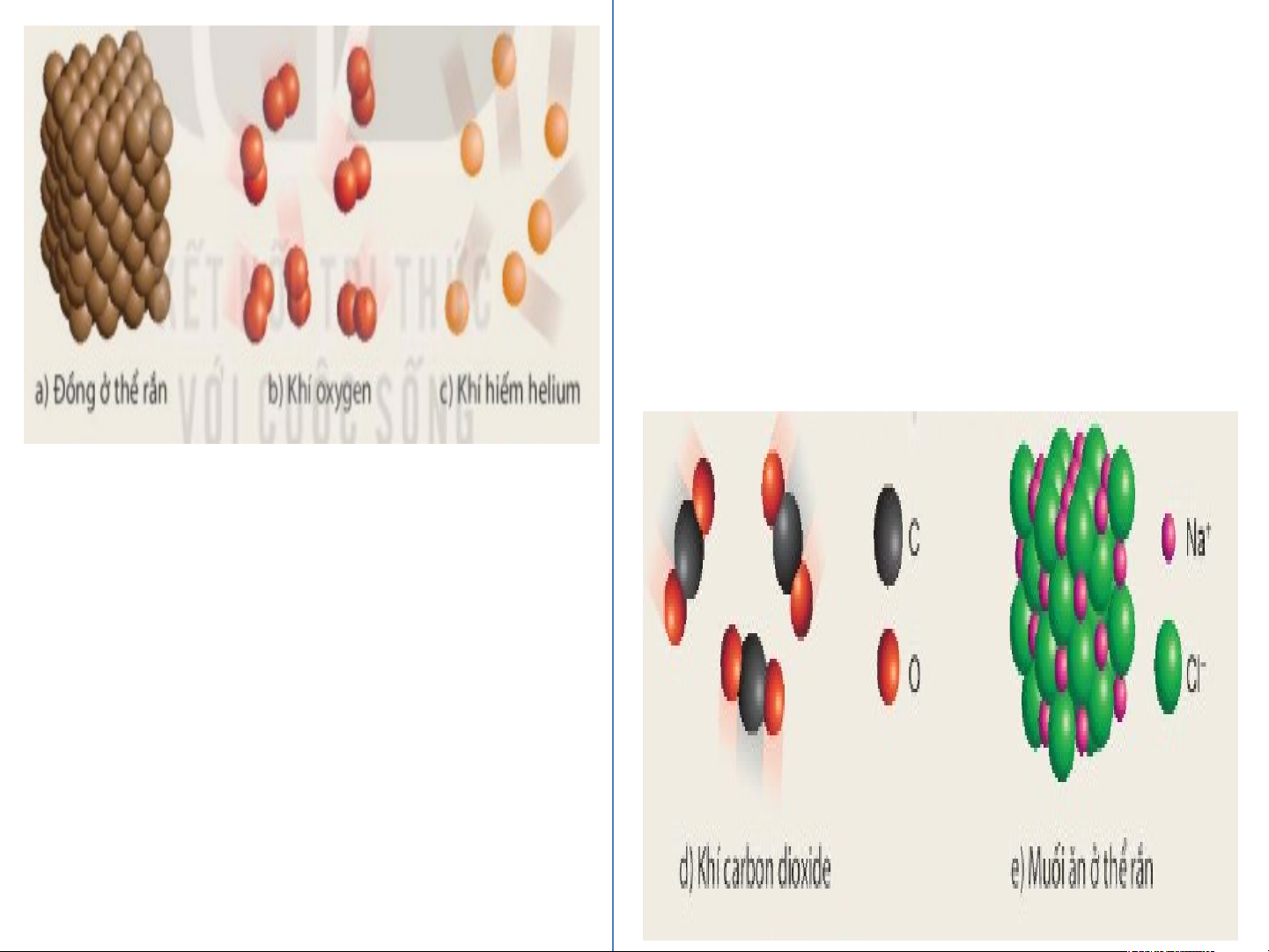
Quan sát các mô hình trong Hình 5.1, thào luận và thực hiện yêu cầu sau:
Dựa vào thành phần nguyên tố, em hãy phân loại các chất trên
thành hai loại: chất được tạo nên từ một nguyên tố hoá học và chất
được tạo nên từ hai nguyên tố hoá học
Chất được tạo nên từ hai nguyên tố hoá học: d) Khí carbon dioxide
e) Muối ăn ở thể rắn Chất được tạo nên từ một nguyên tố hoá học: a) Đồng ở thể rắn b) Khí oxygen c) Khí helium 1. Đơn chất
- Đơn chất là những chất được tạo
nên từ một nguyên tố hoá học.
Ví dụ: Đồng , khí oxygen, khí hydrogen, … Chú ý:
- Một nguyên tố thường chỉ tạo nên một dạng đơn chất
- Một số nguyên tố có thể tạo nên các dạng đơn chất khác nhau
Một số nguyên tố tạo nên các dạng đơn chất khác nhau Than chì và kim cương đều tạo nên từ nguyên tố carbon
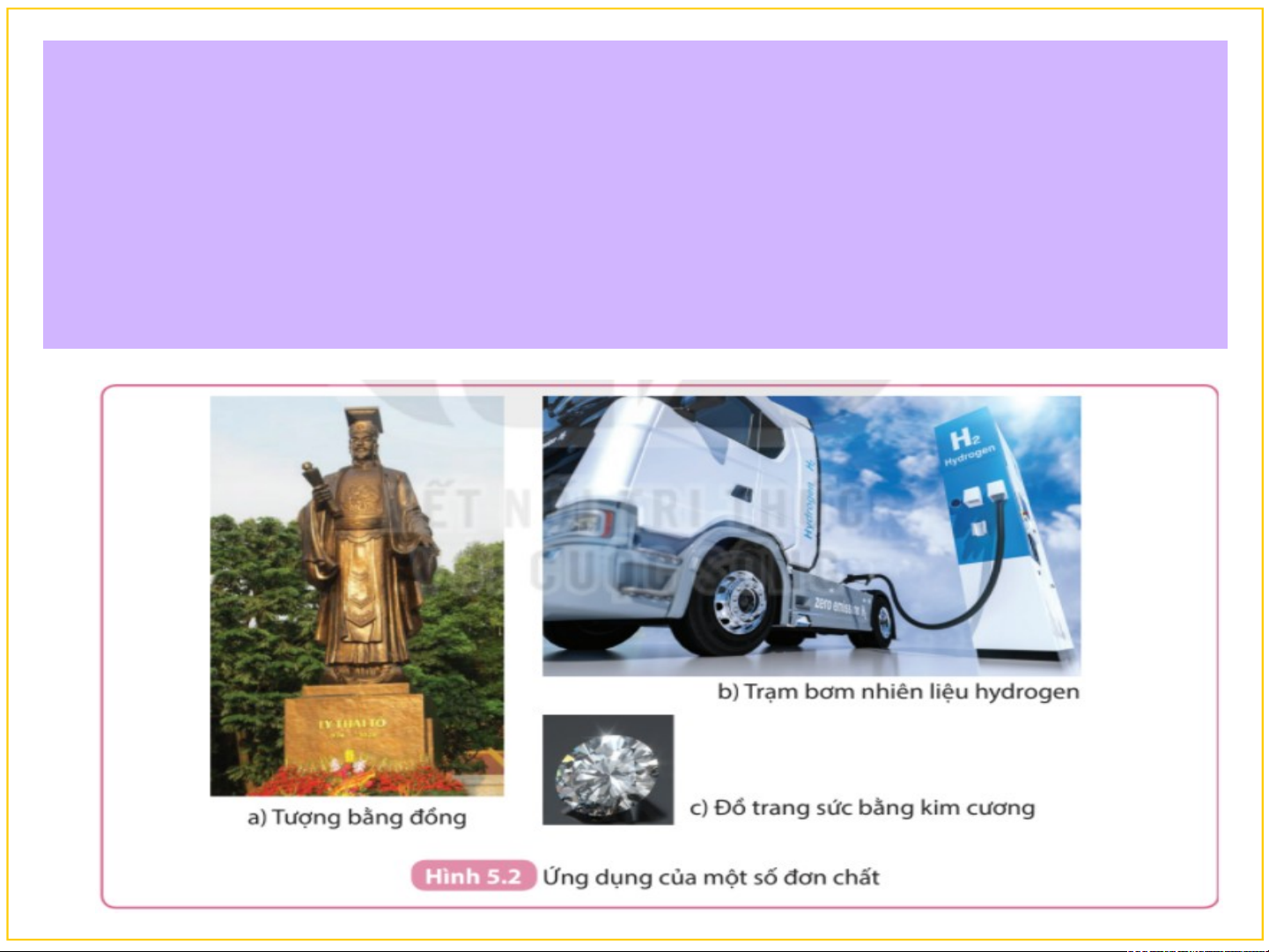
Tượng đồng, nhiên liệu hydrogen, đồ trang sức
bằng kim cương trong Hình 5.2 là ví dụ về ứng dụng
của đồng, hydrogen và carbon. Em hãy kể ra các
ứng dụng khác của đồng, hydrogen và carbon mà em biết. Đơn chất được phân loại thành mấy loại? 8
Đơn chất được phân loại thành 3 loại: Kim loại Phi kim Khí hiếm Thể rắn Thể rắn Thể ...... khí Thể Thể Thể lỏng lỏng khí Nhôm Sulfur Khí Hydrogen 2 Hợp chất 1. Hãy trìn h trìn Lời bày b sự khác h giải biệt b giữa đơn iệt giữa đơn O O - Đơn chất oxygen chất ox chất ygen g en Oxygen được tạo nên từ 1 và hợp c và hợ hất h nguyên tố là: oxygen carbon carb (O) dioxide d v ioxide ề C - Hợp chất carbon thàn t h p hàn hầ h p n hầ O O
dioxide được tạo nên từ nguyên n tố guyên v tố à 2 nguyên tố là: carbon Carbon vai trò c vai t ủa ủ dioxide (C) và oxygen (O) chúng đ chún ối với g đ
- Oxygen duy trì sự sống và sự sự sống ố v ng à
cháy. Carbon dioxide không duy trì sự cháy h ? sự sống và sự cháy
Hợp chất là chất được tạo nên
từ hai hay nhiều nguyên tố hoá học. 1 2
2. Hãy dự đoán số lượng của các đơn chất
nhiều hơn hay ít hơn số lượng của các hợp chất. Giải thích.
- Các nhà khoa học đã tìm ra 118 nguyên tố hóa học -
Hợp chất được tạo nên từ 2 hay nhiều nguyên tố,
hiện nay người ta đã biết hàng chục triệu hợp chất
khác nhau. Do hợp chất được tạo nên từ tổ hợp các
nguyên tố với các tỉ lệ nguyên tố trong hợp chất khác nhau
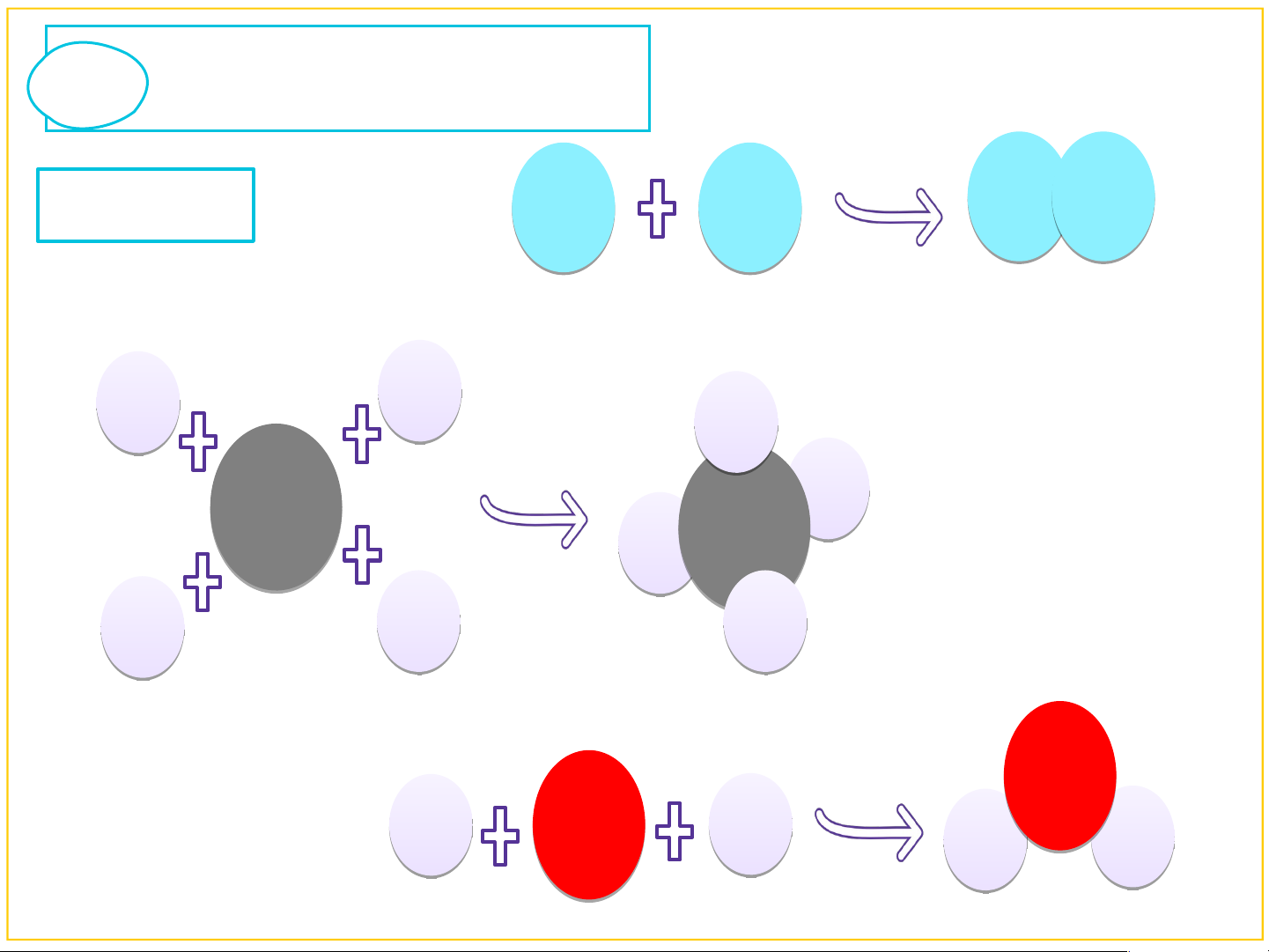
⇒ Số lượng của các hợp chất nhiều hơn số lượng của các đơn chất II. PHÂN TỬ 1 Khái niệm N N Ví dụ: N N H H H H C H C H H H O H O H H H
Phân tử là hạt đại diện cho chất, gồm 1 số
nguyên tử liên kết với nhau và thể hiện đầy đủ tính chất của chất. 1 7 2
Khối lượng phân tử
Ví dụ: Cách tính khối lượng phân tử nước
- Bước 1: Xác định số lượng nguyên
tử của mỗi nguyên tố O H H
Phân tử nước gồm 2 nguyên tử H và 1 nguyên tử O
- Bước 2: Tính khối lượng phân tử M = 2 x 1 + 1 x 16 = 18 amu nước
Khối lượng phân tử được tính
theo đơn vị amu, bằng tổng
khối lượng của các nguyên tử trong phân tử. III. LUYỆN TẬP
Câu 1: Đánh dấu X vào ô trống sao cho hợp lí: Chất Chất nguyên chất Hỗn hợp Đơn chất Hợp chất Nước cất X Nước đường X X Iron (Sắt) X Không khí X X Aluminium (Nhôm) X Nước cam X X Nước biển X X
Câu 2. Sử dụng giá trị khối lượng nguyên tử của
một số nguyên tố trong bảng tuần hoàn để tính
khối lượng phân tử của các chất được biểu diễn
trong Hình 5.3a và Hình 5.3b Lời giải
- Xét Hình 5.3a: phân tử nitrogen được tạo
bởi 2 nguyên tử N (có khối lượng nguyên tử = 14)
⇒ Khối lượng phân tử của nitrogen bằng: 14.2 = 28 (amu)
- Xét Hình 5.3b: phân tử methane được tạo bởi 1
nguyên tử C (có khối lượng nguyên tử = 12) và 4
nguyên tử H (có khối lượng nguyên tử = 1)
⇒ Khối lượng phân tử của methane bằng = 12.1 + 1.4 = 16 (amu) CỦNG CỐ Câu 1
Đơn chất là những chất được tạo nên
từ bao nhiêu nguyên tố hoá học?
A Từ 1 nguyên B Từ 2 nguyên tố tố C Từ 3 D Từ 4 nguyên tố nguyên tố trở lên Câu 2
Chọn câu phát biểu đúng:
Hợp chất là chất được cấu tạo bởi: 1 nguyên 2 chất tố hoá A trộn lẫn học B với nhau 2 nguyên 3 nguyên tố hoá học C tố hoá học trở lên D trở lên Câu 3
Cách viết sau có ý nghĩa gì 5 O, Na, Cl2
Phân tử Oxygen, hợp chất sodium, nguyên tố A chlorine
B 5 nguyên tử Oxygen,nguyên tử nguyên tố sodium, phân tử chlorine C
Phân tử khối Oxygen, nguyên tử sodium, phân tử chlorine
5 phân tử Oxygen, phân tử sodium, nguyên tố D chlorine Câu 4
Khối lượng phân tử của CH và H O 4 2 CH =15 4 amu, A B CH =16 4 amu, H O=17 2 H O=18 amu C D 2 CH =H O=18 amu 4 2 amu Không tính được Câu 5
Để chỉ hai phân tử hydrogen ta viết: A B C D 2H 2H 4H 4H 2 2 Câu 6
Hợp chất Al (NO ) có phân tử khối là x 3 3 213. Giá trị của x là: A 1 B 2 C 3 D 4
Câu 7:Cho biết đâu là đơn chất, đâu là hợp chất ?
Giải thích và Tính khối lượng phân tử của các chất sau
a/Copper sulfate biết mỗi phân tử gồm 1 nguyên tử
Cu, 1 nguyên tử S và 4 nguyên tử O
b/Oxygen biết mỗi phân tử gồm 2 nguyên tử O
c/Muối ăn biết mỗi phân tử gồm 1 nguyên tử Na và 1 nguyên tử Cl
d/Khí amoniac biết mỗi phân tử gồm 1 nguyên tử N và 3 nguyên tử H
e/Bromine: biết mỗi phân tử gồm 2 nguyên tử Br
a/ Copper sulfate biết mỗi phân tử gồm 1 nguyên tử Cu, 1
nguyên tử S và 4 nguyên tử O
b/ Oxygen biết mỗi phân tử gồm 2 nguyên tử O
c/Muối ăn biết mỗi phân tử gồm 1 nguyên tử Na và 1 nguyên tử Cl
a/ Copper sulfate :Hợp chất vì tạo 3 nguyên tố là Cu ( copper), S ( sulfur) và oxygen
PTK = Cu + S + 4 O = 64 + 32 + 4. 16 = 160 amu
b/ Oxygen: đơn chất tạo bởi 1 nguyên tố là O PTK = 2 . O = 16.2 =32 amu
c/Muối ăn : hợp chất vì tạo bởi 2 nguyên tố gồm Na( sodium) và Cl ( chlorine)
PTK = Na + Cl = 23 + 35,5 = 58,5 amu
d/ Khí amoniac biết mỗi phân tử gồm 1
nguyên tử N và 3 nguyên tử H
e/ Bromine: biết mỗi phân tử gồm 2 nguyên tử Br
d/ Khí amoniac: hợp chất vì tạo bởi 2 nguyên tố là N và H PTK = N + 3H = 14 + 3.1 =17amu
e/ Bromine: đơn chất vì tạo bởi 1 nguyên tố Br PTK = 2 Br = 2.80 = 160 amu
Document Outline
- Slide 1
- Slide 2
- Slide 3
- Slide 4
- Slide 5
- Slide 6
- Slide 7
- Slide 8
- Slide 9
- Slide 10
- Slide 11
- Slide 12
- Slide 13
- Slide 14
- Slide 15
- Slide 16
- Slide 17
- Slide 18
- Slide 19
- III. LUYỆN TẬP
- Slide 21
- Slide 22
- Slide 23
- Slide 24
- Slide 25
- Slide 26
- Slide 27
- Slide 28
- Slide 29
- Slide 30
- Slide 31
- Slide 32




