












Preview text:
MỤC LỤC
DANH MỤC CÁC CHỮ VIẾT TẮT........................................................................2
DANH MỤC CÁC HÌNH.........................................................................................3
1. TỔNG QUAN VỀ MONTELUKAST..................................................................4
2. LEUKOTRIENE VÀ RECEPTOR.......................................................................4
2.1. Sinh tổng hợp và chuyển hóa Leukotriene......................................................5
2.2. Các receptor của Leukotriene..........................................................................8
2.3. Receptor Cysteinyl Leukotriene......................................................................9
3. CƠ CHẾ TÁC DỤNG.........................................................................................11
3.1. Cơ chế tổng quát............................................................................................11
3.2. Mô tả cơ chế ở mức độ phân tử.....................................................................12
4. HIỆU ỨNG DƯỢC LÝ.......................................................................................14
4.1. Tác dụng chống viêm của MTK phụ thuộc vào CysLTR1 của CysLT với các
tế bào của hệ thống miễn dịch bẩm sinh..............................................................14
4.2. Cơ chế chống viêm độc lập với CysLTR1 của chất đối kháng CysLTR1......15
TÀI LIỆU THAM KHẢO.......................................................................................17 2
DANH MỤC CÁC CHỮ VIẾT TẮT Chữ viết tắt Diễn giải CysLT Cysteinyl leukotriene CysLTR Receptor cysteinyl leukotriene GPCRs G-protein-coupled receptors LT Leukotriene LTRA Antileukotriene MTK Montelukast 3 DANH MỤC CÁC HÌNH
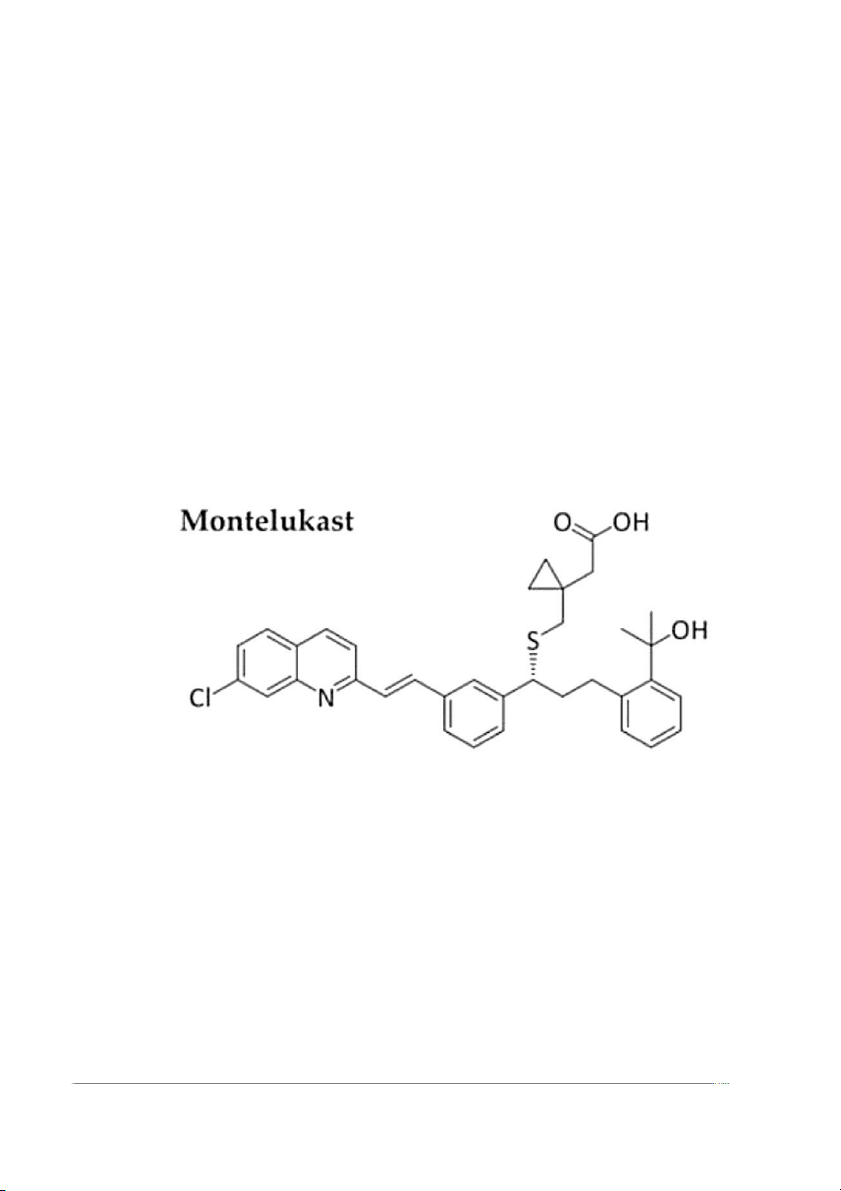
Hình 1. Cấu trúc hóa học của Montelukast.............................................................4
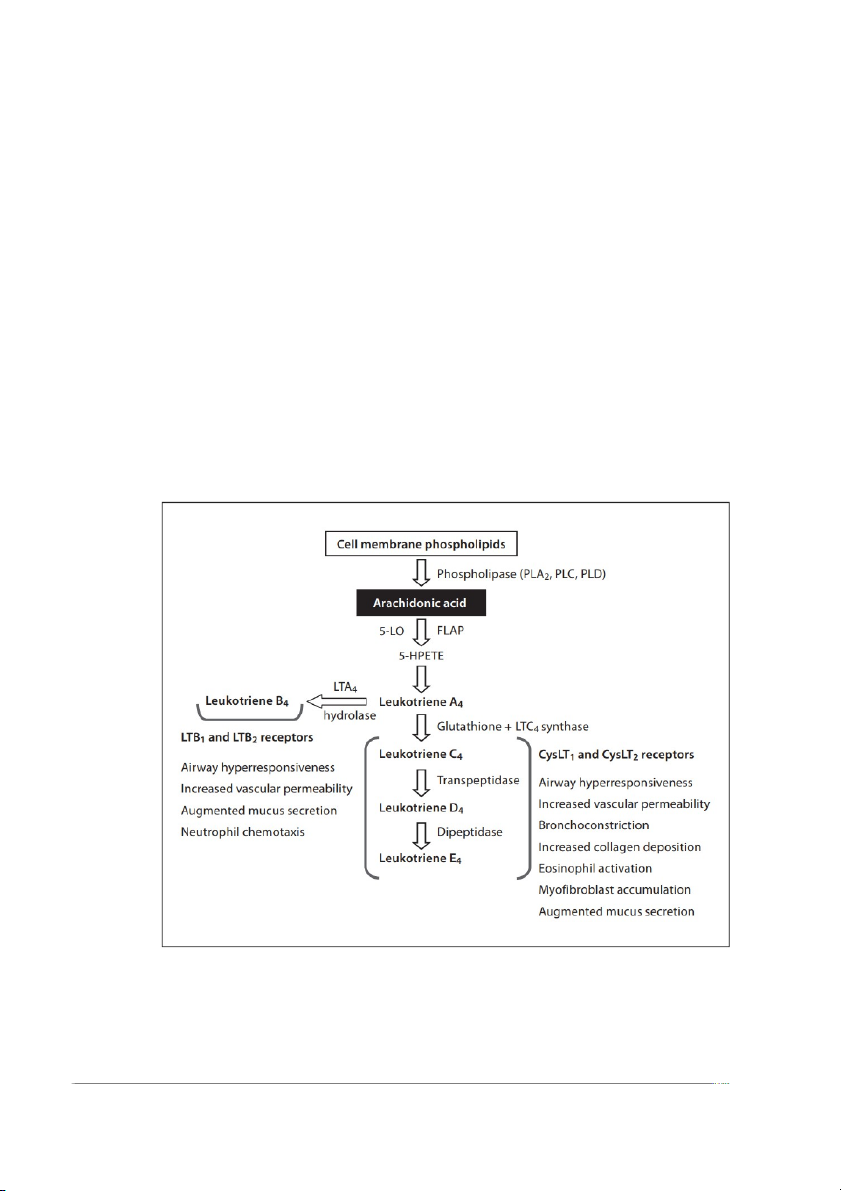
Hình 2. Sơ đồ tóm tắt quá trình sinh tổng hợp Leukotriene và các receptor .........5
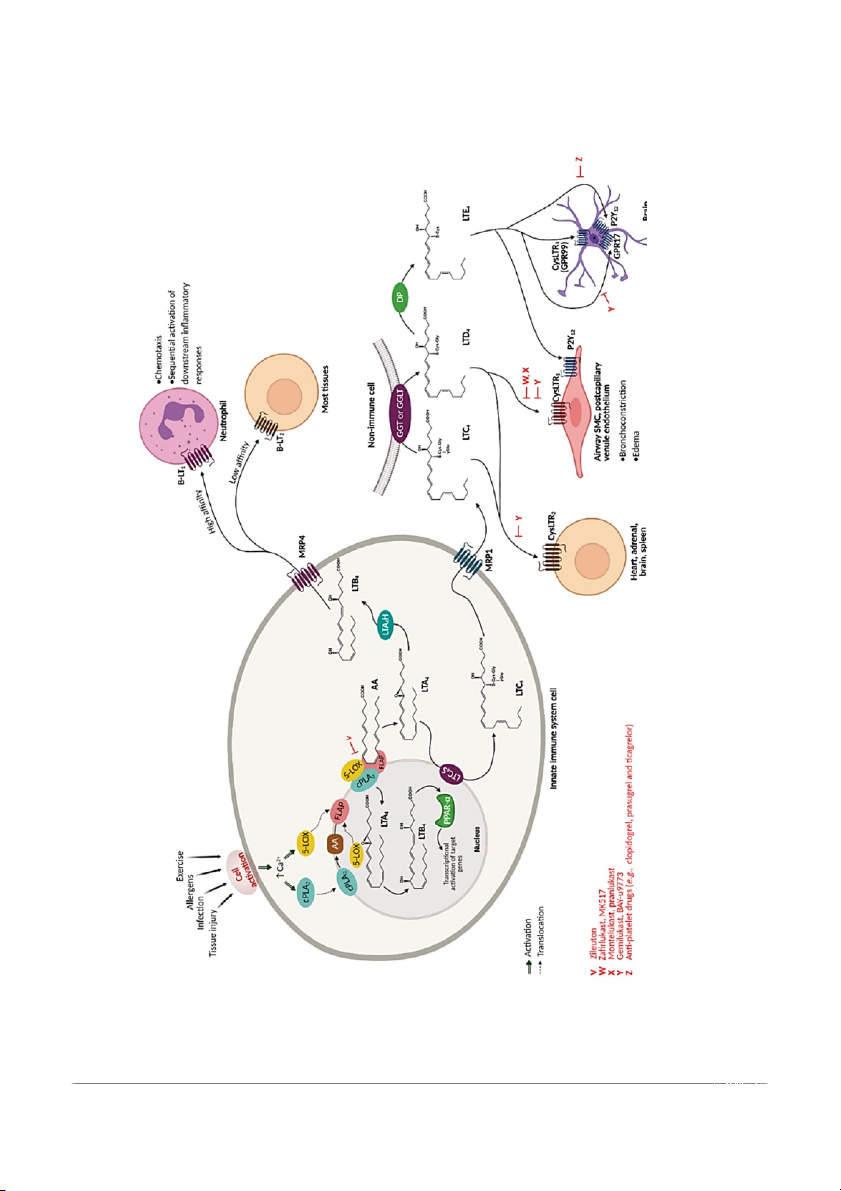
Hình 3. Con đường sinh tổng hợp leukotriene và nhận diện receptor ...................7
Hình 4. Con đường sinh tổng hợp và receptor cho Leukotrienes ..........................8
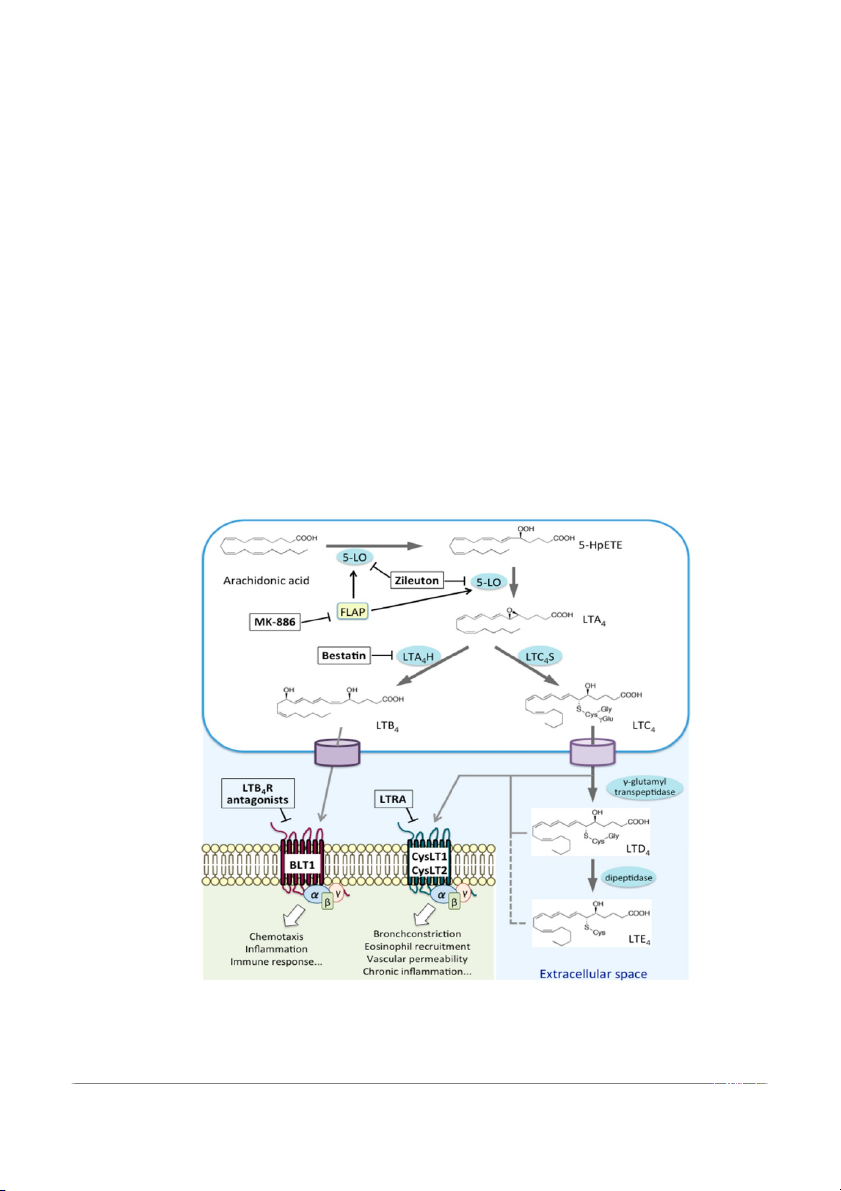
Hình 5. Cơ chế hoạt động của các antileukotriene...................................................
Hình 6. Cơ chế truyền tín hiệu và các tác động sinh học qua trung gian CysLTs
(LTC4, LTD4 và LTE4) và LTB4..............................................................................12
Hình 7. Tác dụng của cysteinyl leucotriene trên cấu trúc đường thở...................13 DANH MỤC CÁC BẢNG
Bảng 1. Tóm tắt về receptor cysteinyl leukotriene ở người và chuột ..................11
Bảng 2. Tương tác tiền viêm của cysteinyl leukotrienes với các tế bào của hệ thống
miễn dịch bẩm sinh ...............................................................................................15
Bảng 3. Các hoạt động kháng viêm không phụ thuộc receptor cysteinyl
leukotriene 1 của các antileukotriene ...................................................................16 4
1. TỔNG QUAN VỀ MONTELUKAST [3] [5]
- Hoạt chất: Montelukast (tên thương mại Singulair)
- Danh pháp IUPAC: [R-(E)]-1-[[[1-[3-[2-(7-chloro-2-quinolinyl)ethenyl]phenyl]-
3-[2-(7-chloro-2-quinolinyl)ethenyl]phenyl]-3-[2-(1-hydroxy-1-
methylethyl)phenyl]propyl]thio]methyl cyclopropane acetic acid sodium
- Công thức hóa học: C35H35ClNNaO3S
- Nhóm dược lý: Thuốc chữa hen và bệnh phổi tắc nghẽn mãn tính
- Phân nhóm điều trị: Chất đối kháng receptor Leukotriene LTD4
- Receptor cysteinyl leukotriene 1 (CysLTR1) thuộc loại receptor kết dính G-
protein (GPCRs) trên màng tế bào.
Hình 1. Cấu trúc hóa học của Montelukast [5]
2. LEUKOTRIENE VÀ RECEPTOR [4] [5] [7]
Leukotriene (LT) là chất trung gian lipid gây viêm có nguồn gốc từ acid
arachidonic, được tổng hợp chủ yếu trong các tế bào từ hệ thống miễn dịch bẩm
sinh (ví dụ: bạch cầu đa nhân, đại thực bào, tế bào mast và vi thần kinh đệm não). 5
LT đóng vai trò quan trọng trong các phản ứng viêm, chúng phát huy tác
dụng sinh học của mình bằng cách liên kết với các receptor trên màng tế bào, thuộc
siêu họ của receptor kết dính G-protein (GPCRs).
Các phân nhóm receptor LT khác nhau thể hiện các chức năng và kiểu biểu
hiện độc đáo. Các receptor leukotriene B-LT1 và B-LT2 được kích hoạt bởi
leukotriene B4 (LTB4), trong khi các receptor CysLT1 và CysLT2 được kích hoạt bởi cysteinyl LT (CysLTs).
LT có liên quan đến các bệnh viêm khác nhau, bao gồm hen suyễn, viêm
mũi dị ứng, viêm da dị ứng, viêm kết mạc dị ứng, viêm khớp dạng thấp, sốc phản
vệ, bệnh phổi tắc nghẽn mãn tính (COPD), viêm tiểu phế quản tắc nghẽn sau ghép phổi và bệnh phổi kẽ.
2.1. Sinh tổng hợp và chuyển hóa Leukotriene [5]
Hình 2. Sơ đồ tóm tắt quá trình sinh tổng hợp Leukotriene và các receptor [7] 6
Hệ thống miễn dịch bẩm sinh (ví dụ: bạch cầu đa nhân, đại thực bào, tế bào
mast và vi thần kinh đệm não) được kích hoạt bởi các kích thích miễn dịch và
không miễn dịch như nhiễm trùng, tổn thương mô, chất gây dị ứng và tập thể dục
(Hình 3). Sau khi tế bào bị kích thích, nồng độ canxi trong tế bào tăng lên, và các
enzym phospholipase A2 (cPLA2) và 5-lipoxygenase (5-LOX) trong tế bào được
kích hoạt và chuyển đến vỏ hạt nhân.
Ở đó, cPLA2 tách glycerophospholipid, giải phóng axit arachidonic (AA),
được chuyển đổi thành hydroperoxide mạch hở 5(S)-axit hydroperoxy-
eicosatetraenoic (5-HpETE) bởi quá trình oxy hóa qua trung gian 5-LOX khi kích
hoạt LOX bằng protein kích hoạt 5-LOX (FLAP); Ngược lại, 5-HpETE bị mất
nước thành trienepoxide leukotriene A4 (LTA4) liên hợp không ổn định, chất
chuyển hóa đầu tiên trong con đường leukotriene.
LTA4 là một chất trung gian tồn tại trong thời gian ngắn có thể trải qua quá
trình thủy phân để tạo thành leukotriene B4 (LTB4) hoặc liên hợp với glutathione
được xúc tác bởi LTC4 synthase để tạo thành leukotriene C4 (LTC4, một S-glutathionyl leukotriene).
LTB4 và LTC4 được chuyển đến không gian ngoại bào chủ yếu bằng các
protein kháng đa thuốc, cụ thể là thông qua MRP4 (LTB4) và MRP1 (LTC4), trong
đó sự phân tách LTC4 thành leukotriene D4 (LTD4) và sau đó thành leukotriene E4
(LTE4 ) diễn ra. LTD4, một S-cysteinyl LT, được tổng hợp từ LTC4 bởi sự phân cắt
qua trung gian γ-glutamyl transpeptidase (GGT), trong khi LTE4 là kết quả của sự
phân cắt LTD4 bởi một dipeptidase (DP) gắn màng. 7
các cơ quan khác nhau thông T, tác động lên diện receptor [5] sinh tổng hợp L
ức chế con đường leukotriene; tất cả đều được đánh dấu màu đỏ. và Z là chất
Con đường sinh tổng hợp leukotriene và nhận Y , X, W Hình 3. ong khi eceptor khác nhau. hất ức chế 5-LOX, tr là c
Leukotrienes được tổng hợp khi kích hoạt hệ thống miễn dịch thông qua một chuỗi qua các r V 8
2.2. Các receptor của Leukotriene [4] [5]
LTB4 là một leukotriene tiền viêm tác động lên các bạch cầu đa nhân trung
tính ở người chẳng hạn như bạch cầu hạt trung tính, thông qua các receptor kết
dính G-protein B-LT1 hoặc B-LT2, kích hoạt hóa hướng động và kích hoạt phản
ứng viêm sau đó. (Hình 3,4)
LTC4, LTD4 và LTE4 tạo thành một nhóm các leukotriene cysteinyl (CysLT)
hoạt động thông qua các receptor trên bề mặt tế bào loại kết dính với G-protein,
trong đó hai loại cổ điển là các receptor cysteinyl leukotriene 1 và 2 (CysLTR1, CysLTR2). (Hình 3)
LTC4 là chất chủ vận của CysLTR1 trong khi LTD4 gắn kết với CysLTR1 và
CysLTR2. LTE4 được mô tả là chất chủ vận của CysLTR3 (còn được gọi là receptor
GPR99) và của các receptor purin GPR17 và P2Y12. (Hình 3,4) 9
Hình 4. Con đường sinh tổng hợp và receptor cho Leukotrienes [4] 10
2.3. Receptor Cysteinyl Leukotriene [7] 2.3.1. Phân loại:
CysLT phát huy tác dụng của chúng thông qua các receptor trên bề mặt tế
bào. Theo International Union of Pharmacology, receptor CysLT ban đầu được
phân loại dựa trên độ nhạy cảm với các chất đối kháng “cổ iển”, đ bao gồm
montelukast, zafirlukast, pranlukast, pobilukast và MK571.
Theo đó, receptor cysteinyl leukotriene chủ yếu được chia thành hai loại:
- CysLT1 nhạy cảm với các chất đối kháng cổ điển;
- CysLT2 làm trung gian cho một số hiệu ứng không bị ức chế bởi các chất đối kháng cổ điển.
Theo một số nghiên cứu, “chất đối kháng kép” duy nhất - BAYu9773, thể hiện
hoạt tính ở cả hai receptor CysLT1 và CysLT2 , tuy nhiên hoạt tính không mạnh và
không chọn lọc đối với các receptor CysLT, đặc biệt là trong các mô người. Mặt
khác, BAYu9773 cũng đã được báo cáo là chất chủ vận từng phần cho receptor CysLT2.
2.3.2. Cấu trúc protein, vị trí và sự biểu hiện của receptor CysLT1:
Gen của receptor CysLT1 được định vị trên nhiễm sắc thể X, Xq13–Xq21, và đã
được chứng minh là bao gồm ít nhất 3 exon, với toàn bộ khung đọc mở ở exon cuối cùng.
Receptor CysLT1 của người mã hóa một protein gồm 337 axit amin với khối
lượng phân tử được tính toán là 38 kDa, được quan sát thấy di chuyển ở trọng
lượng phân tử khoảng 42 kDa dưới dạng đơn phân, nhưng chủ yếu hiện diện ở
dạng dime và oligome, thậm chí với sự có mặt của các tác nhân biến tính.
Receptor CysLT1 ở người có tính tương đồng cao nhất (32% nhận dạng axit
amin) với receptor purin P2Y1 và receptor cho yếu tố kích hoạt tiểu cầu, trong khi 11
đó có mức tương đồng thấp hơn (28% nhận dạng axit amin) với receptor
leukotriene đã biết khác, receptor B-LT.
Receptor CysLT1 ở người sở hữu 4 vị trí N-glycosyl hóa tiềm năng, 1 ở đuôi N
ngoại bào, 2 ở vòng thứ hai và 1 ở vòng ngoại bào thứ ba, ngoài ra còn có nhiều vị
trí phosphoryl hóa protein kinase A và C tiềm năng, chủ yếu nằm ở vòng nội bào
thứ ba và đầu cuối carboxyl.
mRNA của receptor CysLT1 lần đầu tiên được xác định trong các tế bào cơ trơn
phổi bình thường và các đại thực bào kẽ, với ít hoặc không có trong các tế bào biểu
mô đường dẫn khí bình thường. mRNA và protein của receptor CysLT1 cũng biểu
hiện trong bạch cầu ái toan máu ngoại vi bình thường, tập hợp con của bạch cầu
đơn nhân, đại thực bào và tế bào CD34+ tiền bạch cầu. Tế bào mast có nguồn gốc
từ máu cuống rốn của con người cũng biểu hiện receptor CysLT1, nhưng không biểu hiện receptor CysLT2.
Giả thuyết rằng receptor CysLT1 được biểu hiện bởi nhiều loại tế bào viêm
niêm mạc đường thở trong bệnh hen suyễn và số lượng tế bào biểu hiện receptor
CysLT1 tăng lên trong bệnh hen suyễn, ổn định hoặc liên quan đến đợt cấp, đã
được xác nhận bằng các kết quả thu được từ các đối tượng bình thường cho thấy
bạch cầu ái toan niêm mạc phế quản, bạch cầu trung tính, tế bào mast, đại thực
bào, tế bào lympho B và tế bào plasma, nhưng không phải tế bào lympho T, biểu hiện receptor CysLT1.
Nghiên cứu của Zhu et al. chứng minh thêm rằng số lượng mRNA của receptor
CysLT1 và tế bào viêm dương tính với protein cao hơn đáng kể ở những đối tượng
mắc bệnh hen ổn định và bệnh nhân nhập viện vì cơn hen nặng hơn so với nhóm
chứng, và tồn tại mối tương quan tích cực mạnh mẽ giữa quan sát này và số lượng CD45+ tiền thân tăng lên.
Ở niêm mạc mũi của người, receptor CysLT1 đã được xác định ở mức độ gen
cũng như protein trong mạch máu và trong các tế bào kẽ như tế bào nội mô mạch
máu, bạch cầu ái toan, tế bào mast, ại
đ thực bào và bạch cầu trung tính. Vì những 12
đối tượng mắc bệnh hen suyễn do aspirin gây ra có phản ứng quá mức ở đường hô
hấp đối với tác dụng của CysLT trong thuốc giảm đau so với bệnh nhân hen suyễn
dung nạp aspirin, Sousa và cộng sự đưa ra giả thuyết rằng điều này có thể là do
biểu hiện tăng cao của receptor CysLT1 trên các tế bào viêm.
Receptor CysLT1 ở người đã được chứng minh là được biểu hiện nhiều nhất ở lá
lách, tế bào bạch cầu trong máu ngoại vi và ít mạnh mẽ hơn ở phổi, ruột non, tuyến
tụy và nhau thai và ít hoặc không biểu hiện ở gan, ruột kết, thận, cơ xương, tuyến
ức, buồng trứng, tinh hoàn, tim và não.
Sự biểu hiện của receptor CysLT1 cũng đã được báo cáo trong các tĩnh mạch
hiển ở chân, nơi nó làm trung gian cho các tác động co bóp của CysLT. Trong hệ
tiêu hóa, biểu hiện của receptor CysLT1 đã được ghi nhận ở ruột non và ruột kết.
Bảng 1. Tóm tắt về receptor cysteinyl leukotriene ở người và chuột [7]
3. CƠ CHẾ TÁC DỤNG [1] [2] [7] [10]
3.1. Cơ chế tổng quát
CysLT gắn lên receptor ở mặt ngoài tế bào sẽ làm hoạt hóa chúng. CysLTR1
sau khi được hoạt hóa sẽ hoạt hóa protein G nằm trên màng tế bào làm thay đổi
hoạt tính enzym của effector (phospholipase C) dẫn đến thay đổi nồng độ chất
truyền tin thứ 2 nội bào (IP3). Những chất này sẽ gây ra một loạt phản ứng trong tế
bào dẫn đến tăng Ca2+ nội bào.
Montelukast (MTK) là chất đối kháng cạnh tranh, chọn lọc với cysteinyl
leukotriene LTD4 trên receptor CysLT1 dẫn đến giảm viêm và giảm phản ứng quá
mức của đường thở đối với hệ thống miễn dịch và không có hoạt tính chủ vận nào. 13
Hình 5. Cơ chế hoạt động của các antileukotriene [9]
3.2. Mô tả cơ chế ở mức độ phân tử
Các receptor CysLT thuộc loại receptor kết dính với G-protein (GPCR), là
sự gắn kết của ligand với receptor được tăng cường bởi các cation hóa trị hai,
nhưng bị ức chế bởi các ion natri và các chất tương tự GTP không thể thủy phân.
Phân tích tính kỵ nước của cấu trúc sơ cấp được suy luận cho thấy cả CysLT1 và
CysLT2 đều có 7 miền xuyên màng kỵ nước được liên kết bởi 6 vòng ưa nước, biểu
thị một đặc tính điển hình của GPCR.
Ở trạng thái không hoạt động, 3 tiểu đơn vị α, β, γ của protein G vẫn gắn vào
nhau và vào receptor, trong đó tiểu đơn vị α ở dạng không hoạt động. Khi ligand
(LTD4) gắn vào receptor màng (CysLTR1) làm thay đổi cấu tạo của receptor,
receptor được hoạt hóa dẫn đến một loạt sự kiện truyền tín hiệu nội bào (Hình 6): 14 - GDP chuyển thành GTP
- Tiểu đơn vị α được hoạt hóa, tách khỏi phức hợp β, γ
- Phức hợp α-GTP tác động lên Phospholipase C chuyển hóa PIP2 thành IP3.
IP3 đóng vai trò chất truyền tin thứ hai gây ra sự mở kênh ion Ca2+ làm tăng Ca2+ nội bào.
Montelukast (MTK) là antileukotriene (LTRA) được kê đơn rộng rãi nhất ở
Hoa Kỳ và Châu Âu. Các nghiên cứu in vitro chỉ ra rằng MTK có liên quan đến ái
lực phân tử nano thấp và nó là chất đối kháng cạnh tranh chọn lọc ngăn chặn sự
gắn kết của LTD4 với receptor CysLT1 làm đảo ngược tác động gây viêm của CysLT.
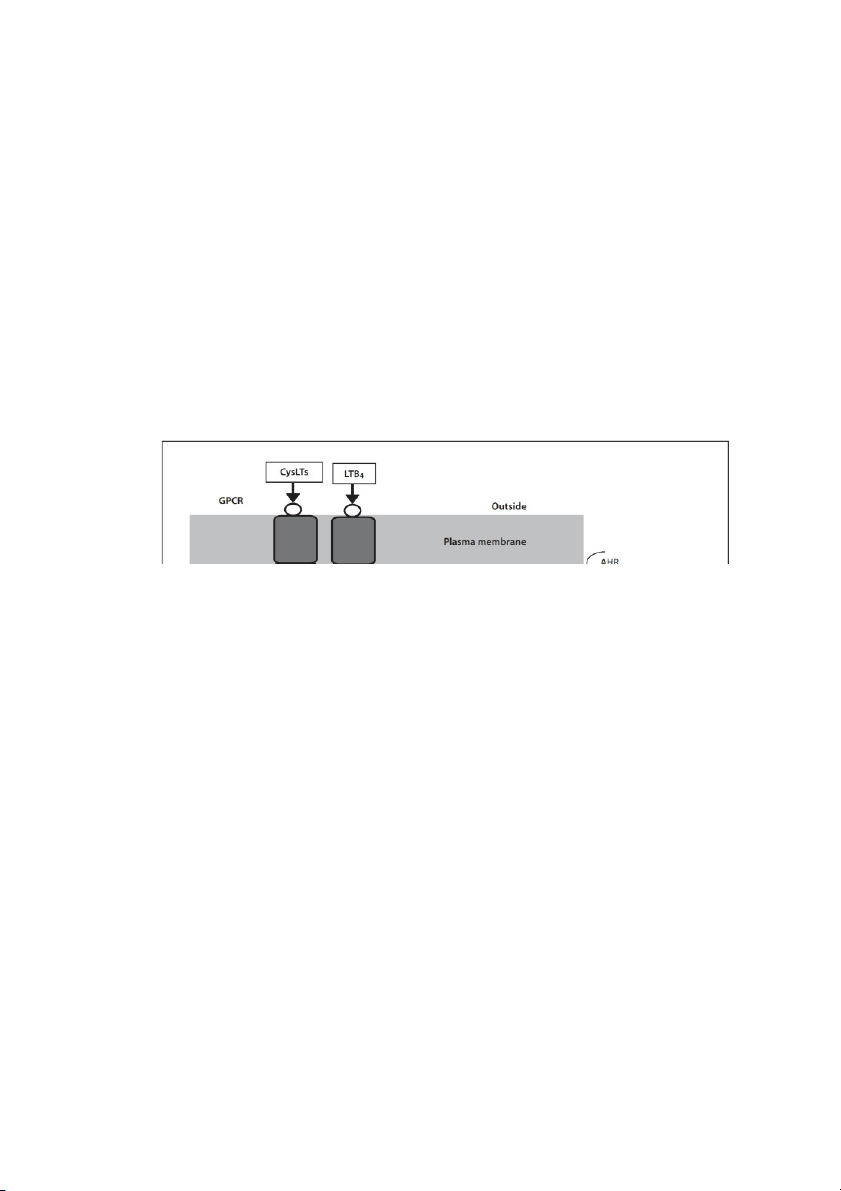
Hình 6. Cơ chế truyền tín hiệu và các tác động sinh học qua trung gian CysLTs
(LTC4, LTD4 và LTE4) và LTB4 [7]
Ghi chú: PIP2 = Phosphatidylinositol biphotphat; IP3 = inositol triphotphat; DAG
= diacylglycerol; ER = lưới nội chất; PKC = protein kinase C
Cả CysLTs và LTB4 đều hoạt động thông qua GPCR (kết hợp với tiểu đơn vị
α Gq) làm tăng canxi nội bào. LTB4 là một chất hóa học hấp dẫn mạnh đối với bạch 15
cầu trung tính và CysLT là chất gây co thắt phế quản mạnh. CysLTs và LTB4
thường gây tăng phản ứng quá mức đường thở (AHR), tăng tiết chất nhầy và tăng
tính thấm mao mạch. CysLT cũng kích hoạt bạch cầu ái toan đồng thời làm giảm
quá trình chết theo chương trình của bạch cầu ái toan. CysLT cũng tham gia vào
quá trình tái tạo đường thở bằng cách tích tụ nguyên bào sợi cơ và tăng sản cơ trơn đường thở.
Hình 7. Tác dụng của cysteinyl leucotriene trên cấu trúc đường thở [6]
4. HIỆU ỨNG DƯỢC LÝ [8] [10]
4.1. Tác dụng chống viêm của MTK phụ thuộc vào CysLTR1 của CysLT với
các tế bào của hệ thống miễn dịch bẩm sinh
Hiện tại, MTK và các LTRA khác được sử dụng trong điều trị hen suyễn và
các bệnh viêm nhiễm khác nhắm mục tiêu cụ thể vào receptor cysLTR1. Sự tương
tác của cysLTs với cysLTR1 thể hiện trên các tế bào của hệ thống miễn dịch bẩm
sinh, cơ trơn đường thở và các loại tế bào cấu trúc khác dẫn đến việc giải phóng 16
một loạt các chất trung gian gây viêm, ngoài việc làm trầm trọng thêm tình trạng
tăng phản ứng của phế quản, tăng tiết chất nhầy và tái tạo đường thở, còn gây ra
viêm đường thở do bạch cầu ái toan qua trung gian tế bào Th2.
Các tế bào của hệ thống miễn dịch bẩm sinh trải qua quá trình kích hoạt khi
tiếp xúc với cysLT bao gồm tế bào mast/basophils, tế bào đơn nhân/đại thực bào và
tế bào đuôi gai myeloid, tất cả đều tạo ra cysLT. Mặt khác, bạch cầu trung tính chỉ
phản ứng khiêm tốn với cysLTs nhưng lại cực kỳ nhạy cảm với tác dụng ức chế
của chất đối kháng cysLTR1 (xem phần 4.2).
Các tương tác tiền viêm của cysLT với tế bào mast, bạch cầu đơn nhân/đại
thực bào, bạch cầu ái toan, tế bào đuôi gai và bạch cầu trung tính , tất cả đều bị
montelukast đối kháng, được tóm tắt trong Bảng 2.
Bảng 2. Tương tác tiền viêm của cysteinyl leukotrienes với các tế bào của hệ thống miễn dịch bẩm sinh [8]
4.2. Cơ chế chống viêm độc lập với CysLTR1 của chất đối kháng CysLTR1
Ngoài hoạt động chống viêm đạt được thông qua đối kháng cysLTR1,
montelukast cũng đã được báo cáo là có các đặc tính chống viêm, chủ yếu nhắm
vào bạch cầu trung tính và bạch cầu đơn nhân/đại thực bào, không phụ thuộc vào sự ối kháng đ
của cysLTR1. Trong bối cảnh này, tác dụng chống viêm của MTK đạt
được ở nồng độ cao hơn một chút so với nồng độ cần thiết để đạt được sự đối 17
kháng cysLTR1 tối đa, nhưng dù sao cũng gần với nồng độ cao nhất trong huyết thanh đạt được.
Một số cơ chế củng cố các hoạt động chống viêm độc lập với cysLTR1 của
các chất đối kháng cysLTR1 đã cập nhật trong các nghiên cứu như sau:
(i) ức chế 5-LO, dẫn đến suy giảm sản xuất của cysLT và cả LTB4;
(ii) ức chế không đặc hiệu nucleotide phosphodiesterase tuần hoàn (PDEs),
dẫn đến tăng nồng độ 3,5-cyclic adenosine monophosphate (cAMP), chất điều hòa
chính các hoạt động tiền viêm của các tế bào của hệ thống miễn dịch bẩm sinh;
(iii) ức chế hoạt động của yếu tố phiên mã, NF𝜅B;
(iv) ức chế prostaglandin E synthase;
(v) ức chế sự kết dính và di cư của bạch cầu ái toan;
(vi) đối kháng receptor purinergic P2Y.
Bảng 3. Các hoạt động kháng viêm không phụ thuộc receptor cysteinyl
leukotriene 1 của các antileukotriene [8] 18 TÀI LIỆU THAM KHẢO 1.
PGS. TS. Dương Xuân Chữ (2022), Tài liệu Giảng dạy "Dược lý phân tử",
Trường Đại học Y Dược Cần Thơ, Cần Thơ. 2.
GS. TS. Nguyễn Xuân Thắng (2011), Dược lý phân tử: Từ phân tử đến lâm sàng, NXB Y học, Hà Nội. 3.
ASHP (2022), Montelukast (Monograph), Drugs.com, truy cập ngày 09/05/2023, tại trang web
https://www.drugs.com/monograph/montelukast.html?references=1. 4.
Airi Jo-Watanabe, Toshiaki Okuno và Takehiko Yokomizo (2019), "The
Role of Leukotrienes as Potential Therapeutic Targets in Allergic Disorders",
International Journal of Molecular Sciences. 20(14), pp. 3580. 5.
Cátia F. Marques, Maria Matilde Marques và Gonçalo C. Justino (2022),
"Leukotrienes vs. Montelukast - Activity, Metabolism, and Toxicity Hints
for Repurposing", Pharmaceuticals. 15(9), pp. 1039. 6.
José Dirceu Ribeiro, Adyléia A D C Toro và Emílio C E Baracat (2006),
"Antileukotrienes in the treatment of asthma and allergic rhinitis", Jornal de
pediatria. 82(5 Suppl), pp. S213-21. 7.
R.K. Singh và các cộng sự. (2010), "Cysteinyl Leukotrienes and Their
Receptors: Molecular and Functional Characteristics", Pharmacology. 85(6), pp. 336-349. 8.
A.J. Theron và các cộng sự. (2014), "Cysteinyl Leukotriene Receptor-1
Antagonists as Modulators of Innate Immune Cell Function", Journal of Immunology Research. 2014. 9.
Domenico Lorenzo Urso và các cộng sự. (2012), "Role of antileukotrienes in acute asthma exacerbations", . 3(2). 2012 10.
Stacy Gelhaus Wendell, Hao Fan và Cheng Zhang (2019), "G Protein-
Coupled Receptors in Asthma Therapy: Pharmacology and Drug Action",
Pharmacological Reviews. 72(1), pp. 1-49.




